Что такое органические кислоты кратко
Обновлено: 05.07.2024
Органические кислоты — органические вещества, проявляющие кислотные свойства. К ним относятся карбоновые кислоты, содержащие карбоксильную группу -COOH, сульфоновые кислоты, содержащие сульфогруппу -SO3H и некоторые другие.
Самыми известными органическими кислотами являются уксусная, муравьиная, лимонная, щавелевая и молочная.
- Дополнить статью (статья слишком короткая либо содержит лишь словарное определение).
- Найти и оформить в виде сносок ссылки на авторитетные источники, подтверждающие написанное.
Wikimedia Foundation . 2010 .
Смотреть что такое "Органические кислоты" в других словарях:
ОРГАНИЧЕСКИЕ КИСЛОТЫ — ОРГАНИЧЕСКИЕ КИСЛОТЫ … Большая политехническая энциклопедия
ОРГАНИЧЕСКИЕ КИСЛОТЫ — органические соединения, имеющие свойства кислот. Играют важную роль в обмене веществ, принимают участие в реакциях фотосинтетического цикла, обусловливают необходимое соотношение катионов и анионов при поступлении питательных веществ в корни… … Словарь ботанических терминов
органические кислоты — органические кислоты, карбоновые кислоты, органические соединения, содержащие одну или несколько карбоксильных групп (COOH). Присутствуют во всех живых клетках. Атом водорода карбоксильной группы легко может быть замещён металлом с… … Сельское хозяйство. Большой энциклопедический словарь
Органические кислоты — см. Кислоты органические … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
ОРГАНИЧЕСКИЕ КИСЛОТЫ — то же, что кар боновые кислоты … Большой энциклопедический политехнический словарь
ОРГАНИЧЕСКИЕ КИСЛОТЫ — карбоновые кислоты, органич. соединения, содержащие одну или неск. карбоксильных групп ( СООН). Присутствуют во всех живых клетках. Атом водорода карбоксильной группы легко может быть замещён металлом с образованием соли (при физиол. значениях рН … Сельско-хозяйственный энциклопедический словарь
Предельные органические кислоты* — (хим.) П. органические кислоты можно рассматривать как продукты замещения водородных атомов предельных углеводородов (см. Парафины) карбоксильными группами (см. Кислоты). Смотря по числу последних различают кислоты П. одноосновные, общей формулы… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Предельные органические кислоты — (хим.) П. органические кислоты можно рассматривать как продукты замещения водородных атомов предельных углеводородов (см. Парафины) карбоксильными группами (см. Кислоты). Смотря по числу последних различают кислоты П. одноосновные, общей формулы… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Четырехосновные органические кислоты — (хим.) представляют вещества общей формулы CxH2y(СО2Н)4 (см. Карбоксил, Углеводороды, Унитарная система), где x и y целые числа, причем y≤x 1; известны многочисленные представители как жирных, так и ароматических Ч. органических кислот; так как… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Кислоты Желчные (Bile Acids) — органические кислоты, присутствующие в желчи; чаще встречаются в виде солей желчных кислот (гликохолата натрия и таурохолата натрия). К ним относятся: холевая, деоксихолевая, гликохолевая и таурохолевая кислоты. Источник: Медицинский словарь … Медицинские термины
Кислота — это вещество, в молекуле которого находится атом водорода вместе с остатком. Её можно как синтезировать искусственно, так и выделить с живого организма. Пожалуй, каждый в быту сталкивается хотя бы с одним соединением, входящим в список органических кислот. Встречаются они чаще в растительных продуктах и их широко используют в пищевой промышленности. Именно эти вещества и позволяют создавать комбинированные вкусовые ощущения.

Понятие кислота
В 1877 году химик из Швеции Сванте Аррениус предложил разделять ряд веществ на основания и кислоты. Согласно его теории, если при растворении в воде элемент высвобождает протон водорода Н+, его нужно относить к кислоте, а если гидроксид-иона (ОН-), то к основанию. Это правило позволило объяснить нейтрализацию веществ при взаимодействии друг с другом. Позже учёный дал уточнение, что сталкивание гидроксид-иона с ионом водорода образовывает воду H2O.

В начале двадцатого века британец Томас Лаури и датчанин Йоханнсен Брёнстед расширили определение. Они предложили относить к кислотам любую молекулу (ион), способную отдавать протон. Это позволило описать реакции, проходящие c водой, например, хлорид аммония.
В 1923 году американец Льюис на основании двух определений сформулировал своё правило. Его формулировка и стала использоваться повсеместно. По нему, кислота — это химическое соединение, принимающее электронную пару и образовывающее ковалентную связь. Основание же, напротив — соединение, способное избавляться от электронной пары.
Все кислоты в химии принято разделять на 2 типа:
Кроме этого, соединения могут быть одноосновными, двухосновными или трёхосновными. Все кислоты, за исключением кремниевой, отлично растворяются в воде. При взаимодействии с основаниями образуют соль, воду и кислотный остаток. Протекание реакции при соприкосновении с металлами происходит не всегда. Взаимодействие возможно лишь элементов, которые располагаются левее водорода. При этом кислотное соединение должно быть не только сильным, но и способным отдавать частицы водорода, которые выделяются во время взаимодействия.
Кислотные растворы могут изменять цвет. Так, лакмус становится красным. Соединение при взаимодействии имеет кислый вкус, появляется электрическая проводимость.
Если же в кислотный раствор добавить спирт, образуется сложный эфир. Все приведенные свойства характерны как для органических соединений, так и неорганических.
Особенности органического класса
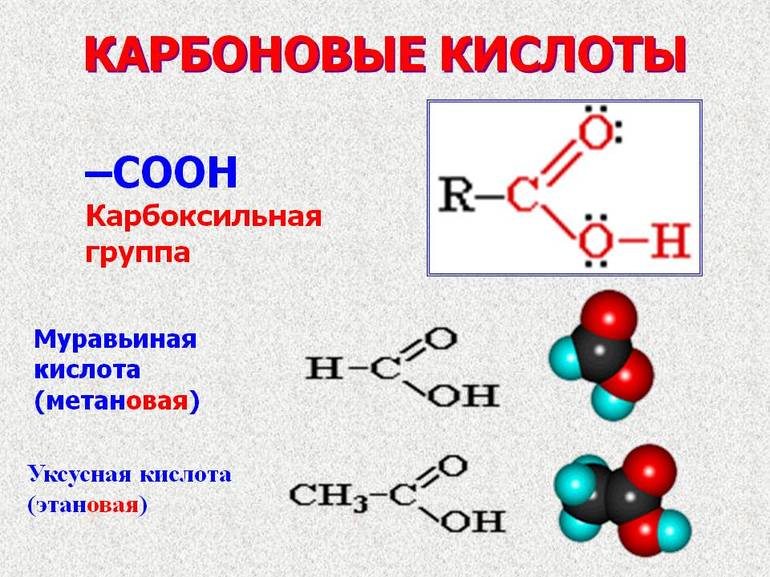
Органическая химия изучает синтезирование углеводородов и их производство. Производные соединения углерода и водорода в молекулах относятся к карбоксильной группе (- COOH). Название веществ состоит из двух элементов: карбонита и гидроксила. Свойства же группы определяется смещением электронной плотности к карбонильному кислороду и образованной поляризацией связи O-H.

Другое название карбонатных кислот — органические. Их свойства определяются строением. Особенности группы из-за диссоциации с образованием частиц водорода в том, что её свойства совпадают с минеральными кислотами. Некоторые соединения, например, уксусная кислота (СН3СОOН) в своей молекуле имеют углеводородный радикал, поэтому возможны реакции, сопровождающиеся выбиванием водорода галогеном. Этот процесс приводит к повышению степени диссоциации, и кислота становится сильнее.
Из свойств органических соединений можно выделить:
- При реагировании с металлами образуется соль и водород — CH3-CH2-COOH + K → CH3-CH2-COO-K + H2.
- Реакция с галогенами описывается формулой: CH3 — CH2 — C = O (-OH) + Cl2 → CH3 — CH (-Cl) — C = O (-OH) + HCl, то есть протекает с появлением галогеносодержащих кислот.
- Взаимодействие со спиртом приводит к возникновению эфира: CH3 — CH2 — COOH + CH3 — OH → CH3 — COOH — CH3.
- При реагировании с металлами образуется соль и вода: CH3-CH2-COOH + MgO →Mg (CH3-CH2-COO)2 + H2O.
- Соединение с солью приводит к слабой кислотности с образованием иной соли: CH3CH2-COO-Na + H2O + CO2.
Так как карбоновые кислоты распадаются на ионы, степень растворимости и достаточно большая температура кипения определяют межмолекулярные водородные связи. При этом с возрастанием молекулярной массы растворимость соединения уменьшается.
Карбоновые кислоты принято разделять и по природе углеводородного радикала: они бывают алифатическими, ароматическими и алициклическими. Если же в первом типе содержится более шести атомов углерода, соединение называют жирной кислотой. Это происходит из-за того, что в виде сложных эфиров они являются частью природных жиров и масел.
Ароматическая представляет собой бензойную и дикарбоновую кислоту, а алициклическая – циклопропан-карбоновую и циклогексанкарбоновую кислоты. Из структуры соединений выделяют радикалы (ацилы). Подписывают их используя суффикс – ил., например, бутрил, формил.
Таблица соединений
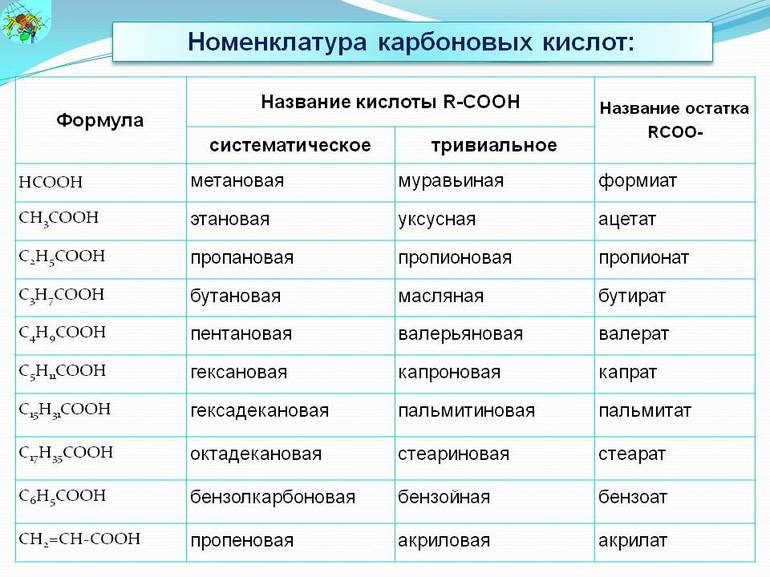
Существует две системы обозначений для карбоновых соединений. Их классификация допускает использование тривиального названия и по ИЮПАК. В то же время применение систематической номенклатуры считается более предпочтительной. Всё дело в том, что тривиальные имена не содержат сведений о составе и строении соединений, а некоторые сложные эфиры и соли вовсе не имеют сокращённых наименований.
В мире насчитывается более сотни различных видов органических кислот. Они входят в компоненты природных вод и связаны с жизнедеятельностью человека, животных и растений. Общую формулу для всей группы можно изобразить как R—COOH. Из наиболее популярных соединений можно выделить:
Отдельно нужно выделить муравьиную кислоту (HCOOH). Это одноосновное соединение. В природе она вырабатывается у пчёл, муравьёв, содержится в крапиве и хвое. Проявляет восстановительные свойства. Эта кислота очень востребована как антибактериальное средство.
Происхождение и получение
Получение HOOC-соединений связано с окислением спиртов. Протекающую реакцию окисления этилового спирта можно записать как CH3 – CH2 – OH → CH3 – C = O (-OH) + H2O. Окисление же уксусного альдегида выглядит следующим образом: CH3 – C = O (H) → CH3 – C =O (-OH). Образование возможно и гидролизом нитрилов. Побочным продуктом является аммиак: CH3 – C = N + H2O → CH3 – C = O (-OH) + NH3.

Карбоновую кислоту можно создать гидролизом сложного эфира. В результате реакции получается спирт. Что интересно, если в реакции использовать щёлочь, продуктом станет соль. Но если её поместить в минеральную кислоту, получится органическая. Реакция имеет вид: СH3 – C = O (-CH3) + H2O → CH3 – C = O (-OH) – CH3OH. Этот способ применяется для получения высших соединений: пальмитинового ( C 16 H 32 O 2), стеаринового ( c17h35cooh), олеинового ( c17h33cooh). При этом в воде они не растворяются.
Сульфокислоты, описываемые формулой RSO3H с органическим радикалом, по функциям сходны с сульфогруппой -SO3H. Получают их путём сульфирования ароматических углеводов. Например, нуклеофильным обменом иона галогена на сульфогруппу, сульфоокислением алканов, тиолов и органических дисульфидов.
Всего же можно выделить следующие способы:
- окисление;
- гидролиз;
- разложение цианидов;
- использование раствора Гриньяра.
В промышленности предельные монокарбоновые кислоты получают из жиров, восков, масел. Довольно распространённый способ образования соединений - путём окисления алканов и алкенов. Например, муравьиная кислота образовывается из метана 2CH4 + + 3O2 → 2HCOOH + 2H2O, а уксусная из н-бутана 2CH3-CH2-CH2-CH3 + 5O2 → 4CH3COOH + 2H2O. Кроме этого, выполняют окисление алканов, гомологов бензола. Производство возможно и в лабораторных условиях. Так в них выполняют гидролиз сложных эфиров и галогенпроизводных, растворяют ангидриды. Какой способ предпочтителен, зависит от имеющихся реактивов и необходимой концентрации полученного раствора.

Некоторые кислоты можно выделить из живых организмов. Например, муравьиную, уксусную. Если первую выделяют из красных муравьёв, вторая содержится в выделениях животных, образуется в результате брожения или скисания. Бензойная кислота находится в ладане, эфирных маслах, бальзамах. Нельзя не упомянуть и самую известную кислоту - лимонную. Способ её чистого получения был открыт в 1860 году и стал называться биосинтезом.

Органические кислоты, как не трудно догадаться, – это органические вещества, проявляющие кислотные свойства. В их состав включают карбоновые кислоты, сульфоновые кислоты, а также некоторые другие. Карбоновые кислоты содержат карбоксильную группу -COOH, а сульфоновые содержат сульфогруппу с общей формулой SO3H.
Карбоновые кислоты
Карбоновыми кислотами называют производные углеводородов, в молекулах которых один или несколько углеродных атомов образуют карбоксильную группу. Карбоновые кислоты классифицируются по основности (числу карбоксильных групп) и по виду радикала:
- Одноосновные предельные кислоты. Первый член гомологического ряда – муравьиная кислота HCOOH, далее уксусная (этановая) кислота CH3COOH. В природе в составе жиров встречаются высшие жирные кислоты. Из них наиболее важны стеариновая кислота C17H335COOH.
- Двухосновные предельные кислоты.
наличие водородных связей делает температуры кипения и плавления карбоновых кислот даже более высокими, чем в случае спиртов близкой молекулярной массы. Кислоты даже в парах существуют в виде димеров.
Низшие кислоты хорошо растворимы в воде. Чем больше длина цепи, тем растворимость меньше вследствие возрастания влияния неполярной части молекулы. Высшие кислоты в воде нерастворимы, ароматические растворимы очень мало, причем все являются кристаллическими.
Сульфоновые кислоты
Сульфоновые кислоты имеют общую формулу RSO3H или R-SO2-OH. Низшие сульфокислоты являются кристаллическими веществами, которые хорошо растворяются в воде.
Самой сильной сульфокислотой является трифторметансульфокислота CF3SO3H. Главными свойствами сульфокислот является способность реагировать с основаниями и со спиртами. получают эти кислоты путем сульфирования ароматических углеводородов и их производных.
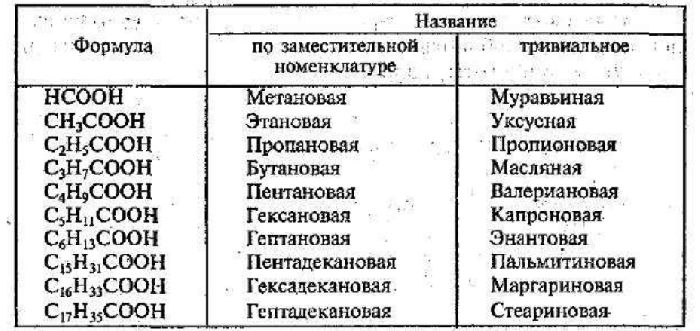
Рис. 3. Список органические кислоты.
Что мы узнали?
Органические кислоты состоят из сульфокислот и карбоновых кислот. формула сульфокислот – -SO3H, а формула карбоновых – COOH. К карбоновым кислотам относится щавелевая, муравьиная, бензойная кислота, а к сульфоновым кислотам – трифторметансульфокислота и др.

Кислоты, их свойства и роль мы изучали в школьном курсе химии. Основной акцент учитель ставил на органические кислоты (organicum acidum). И не только потому, что они обладают довольно сложным строением и не простой классификацией. Интересно их разнообразие в природе, яркие названия, возможность сложных превращений, роль в организме. Насколько важен этот класс соединений и стоит ли недооценивать их значение?
Классификация
Органические кислоты – это соединения, которые отличаются по числу карбоксильных групп. Они бывают одноосновными и многоосновными.

Исходя из строения углеродного радикала все organicum acidum подразделяют на:
- алифатические с нормальной или разветвленной радикальной цепочкой (уксусная);
- ароматические, где радикал замкнут в круг (фталевая, бензойная);
- ациклические с прямой цепью и двумя карбоксигруппами (щавелевая, янтарная).
За счет карбоксильной группы происходит химическое взаимодействие с другими веществами. Водородные связи между молекулами определяют их физические свойства: это кислые жидкости, хорошо растворимые в воде и спиртах. С ростом молекулярной массы их растворимость снижается. Среди organicum acidum встречаются летучие соединения с характерным, резким запахом. Например, уксусная, пропионовая, масляная легко испаряются при обычных условиях. Остальные кислоты не летучи.
Этот класс соединений богат и разнообразен. В группе organicum acidum есть представители с разветвленной и циклической цепью. Они различаются по количеству групп –СООН (ди-, три-, тетро- кислоты). В их состав могут входить разные функциональные группы –ОН, -СО, -NH2.
Эта группа веществ входит в состав живых организмов: они включены в обменные реакции и общий метаболизм. Представители класса встречаются в природных водах, а значит – задействованы в общем круговороте веществ. Органические кислоты, список которых значителен, оказывают существенное влияние и на здоровье человека.
Алифатические organicum acidum, содержащие более шести атомов углерода в углеводородном радикале, получили название жирных кислот. Такое наименование обосновано: они входят в состав природных жиров и масел в виде сложных эфиров.
Полезные свойства органических кислот и их влияние на организм
Благодаря щелочной среде, в организме лучше функционирует иммунная система, продуктивно работают штаммы бактерий в кишечнике, активнее протекают химические реакции. Закисление внутренней среды нарушает процессы жизнедеятельности организма и приводит к различным заболеваниям. Для сохранения кислотно-щелочного равновесия оrganicum acidum незаменимы. Благодаря этим соединениям:
- улучшается перистальтика кишечника;
- нормализуется стул;
- медленнее развиваются гнилостные бактерии;
- улучшается выделение желудочного сока.
Органические кислоты поддерживают уровень рН в пределах 7,4 (щелочная среда). Они создают оптимальные условия для работы пищеварительного тракта, способствуя нормальному перевариванию пищи.[
Продукты, богатые органическими кислотами
Овощи — не такой богатый источник organicum acidum: в среднем их содержание в 100 г съедобной части не больше 0,1 – 0,3 г. Этот показатель высокий у ревеня (1 г), значителен в грунтовых томатах (0,8 г) и щавеле (0,7 г). Больше всего этот класс соединений представлен в ягодах и фруктах.
| № | название кислоты | содержание на 100 г продукта |
|---|---|---|
| 1. | лимон | 5,7 г |
| 2. | клюква | 3,1 г |
| 3. | красная смородина | 2,5 г |
| 4. | черная смородина | 2,3 г |
| 5. | рябина садовая | 2,2 г |
| 6. | вишня, гранат, мандарины, грейпфрут, земляника, рябина черноплодная | 1,9 г |
| 7. | ананас, персики, виноград, алыча, айва | 1 г |
| 8. | молоко и кисломолочные продукты | 0,5 г |
Благодаря их большому количеству в ягодах и фруктах они получили название фруктовых кислот. Каждая из них отличается по вкусу, который может быть терпким, кислым или вяжущим. Например, винная обладает терпко-кислым, слегка резковатым вкусом, а лимонная дарит приятную кислинку.
В пищевой промышленности organicum acidum используют в качестве консервантов, влагоудерживающих компонентов, регуляторов кислотности, антиокислителей. Каждая их них имеет свой код. Такое кодирование позволяет определить, какое соединение введено в состав продукта. Например:
- Е236 – муравьиная;
- Е296 – яблочная;
- Е326-327 – молочная;
- Е331-333 – лимонная;
- Е363 – янтарная.
Не все органические кислоты должны поступать извне, часть из них организм способен вырабатывать самостоятельно.
Суточная норма
Признаки избытка органических кислот в организме
При состоянии хронической усталости, недостатке витаминов, пониженного выделения желудочного сока стоит ввести в рацион больше ягод и фруктов. Но необходимо соблюдать баланс: избыток organicum acidum не идет на пользу организму. При переизбытке наблюдаются следующие нежелательные процессы:
- сгущение крови;
- проблемы с работой ЖКТ;
- нарушение деятельности почек;
- болезни суставов.
И самое опасное — смещение кислотно-щелочного равновесия, которое так важно для нормальной жизнедеятельности в целом.
Недостаток органических кислот в организме
- развитие авитаминоза;
- плохое усвоение пищи;
- не полное усвоение минералов;
- слабая выносливость организма;
- снижение тонуса скелетной мускулатуры и спазмы в мышцах;
- хроническая усталость и недомогание;
- частые головные боли;
- плохое состояние кожи и волос.
Органические кислоты благотворно влияют на внешний облик. При их нормальном поступлении кожа, волосы и ногти выглядят ухоженными. Например, аскорбинка придает коже здоровый вид и сияние. А янтарная кислота улучшает состояние волос и тургор кожи. Но при этом не стоит забывать, что на внешность также влияют другие соединения и факторы среды.
Усвоение органических кислот зависит от продуктов питания, с которыми их потребляют. Они хорошо сочетаются с хлебобулочными изделиями из твердых сортов пшеницы, с растительными маслами первого отжима. При курении кислоты превращаются в никотиновые составляющие, что наносит существенный вред здоровью.

Образование: Высшее, Томский государственный научно- исследовательский университет им.Куйбышева, 1988г., биолог с правом преподавания биологии и химии. Специализация: ботаника, биохимия. Опыт работы: корреспондент, корректор; и.о. директора профессионального лицея №37; преподавателем химии, биологии в школе и лицее, высшая квалификационная категория. 20 лет педагогического стажа; научный сотрудник лаборатории физиологии растений и биотехнологии; старший научный сотрудник лаборатории биохимии ОПХ им. Сидоренко.
Читайте также:
- Психолого педагогическая характеристика одаренных детей младшего школьного возраста
- Анализ умк школа 21 века по решению задач уравнением
- Чем отличается пропуск от неявки в школе
- План наставника музыкального руководителя с молодым специалистом в доу
- Какое значение для народов россии имело вхождение в состав единого союзного государства кратко

