Врожденный токсоплазмоз и его профилактика реферат
Обновлено: 02.07.2024
Врожденный токсоплазмоз – это паразитарная патология, которая возникает при трансплацентарном инфицировании ребенка Toxoplasma gondii. У большинства детей протекает бессимптомно. Возможные проявления заболевания: интоксикационный синдром, пятнисто-папулезная сыпь, лимфаденопатия, желтуха, гепатоспленомегалия, отеки нижних конечностей. Часто провоцирует развитие патологий органа зрения, слуха, ЦНС; реже – миокарда, легких и печени. Антенатальная диагностика базируется на проведении биопсии, постнатальная – на совокупности анамнестических и клинико-лабораторных данных (ИФА, ПЦР). Этиотропное лечение врожденного токсоплазмоза проводится при помощи схем на основе препаратов пириметамина и сульфадимезина или спирамицина.
МКБ-10
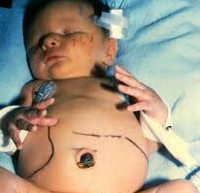
Общие сведения
Врожденный токсоплазмоз – заболевание в педиатрии и неонатологии, возникающее в результате трансплацентарного заражения плода на фоне острой формы токсоплазменной инфекции у матери. Впервые Toxoplasma gondii была описана французами К. Николь и Л. Монсо в 1908 году. В 1939 г. американцы Э. Вольф, Д. Кауэн и Б. Пэйдж подтвердили трансплацентарный механизм передачи возбудителя. Промежуточными хозяевами могут выступать более 400 видов животных. Согласно статистическим данным ВОЗ, число инфицированных токсоплазмой людей в мире составляет порядка 1,5 млрд. человек, в России – около 30% всего населения. Частота врожденной формы 1,5:1000 новорожденных. Даже на фоне лечения средний показатель смертности у детей до 5 лет составляет 12%, осложнения возникают почти у 90%.

Причины врожденного токсоплазмоза
Врожденный токсоплазмоз развивается только при инфицировании матери Toxoplasma gondii во время вынашивания ребенка. Механизм заражения беременной женщины – фекально-оральный. Наиболее распространенные причины: контакт с животными из семейства кошачьих и употребление термически необработанной пищи. Инвазивная форма возбудителя – ооциста – формируется в кишечнике животных и выделяется с калом, после чего может на протяжении 12 и больше месяцев сохранять контагиозность в условиях внешней среды. В крайне редких случаях этиологическим фактором может стать трансплантация контаминированных органов или переливание крови. Заражение плода T. gondii происходит трансплацентарным путем. После рождения ребенка развивается интенсивный гемолиз, возникают геморрагии на слизистых оболочках, расширение камер сердца, пневмония или интерстициальный отек легких, некроз печени и селезенки, увеличение лимфоузлов, воспаление и отек тканей головного мозга, некробиоз сетчатки. При гистологическом исследовании непосредственно пораженных тканей определяется некроз, гранулематозная или диффузная пролиферация ретикулоцитов, инфильтрация плазмоцитами и лимфоцитами, перифокально – множество токсоплазм. Впоследствии на месте некротизированных участков формируется фиброз, переходящий в кальциноз.
Классификация врожденного токсоплазмоза
В зависимости от периода инфицирования плода врожденный токсоплазмоз может протекать в трех формах:
- Хроническая форма. Заражение происходит в I-II триместрах беременности. Риск передачи возбудителя – 13-18%. При такой форме могут развиваться атрофия головного мозга, гидроцефалия, деформация желудочков мозга, анофтальмия, колобома, атрофия сетчатки, врожденные пороки сердца и других органов и систем.
- Подострая форма. Инфицирование – III триместр. Риск заражения ребенка – 75-85%. Проявления могут включать в себя энцефалит, менингоэнцефалит, очаговый некроз сетчатки, увеит.
- Острая форма. Токсоплазма попадает в организм ребенка непосредственно перед родами. Возможные симптомы: гипертермия, пятнисто-папулезная сыпь, интенсивная желтуха, гепатоспленомегалия, анемия, миокардит, пневмония.
Симптомы врожденного токсоплазмоза
Врожденный токсоплазмоз может проявляться в различные периоды жизни ребенка – от первых дней до нескольких месяцев. Специфических симптомов данное заболевание не имеет. Зачастую присутствующая клиника нечеткая и имитирует другие врожденные патологии. Наиболее вероятные проявления врожденного токсоплазмоза: ухудшение общего состояния, пятнисто-папулезная сыпь различной локализации, генерализованная лимфаденопатия, увеличение печени и селезенки, желтуха, отеки нижних конечностей, субфебрильное повышение температуры тела. Тяжесть симптомов зависит от степени инфицирования токсоплазмами, триместра беременности, в котором произошло инфицирование, и иммунных сил матери. Примерно 70-90% детей не имеют каких-либо проявлений в ранние периоды жизни, но почти у всех спустя некоторое время возникают осложнения. Классический врожденный токсоплазмоз проявляется триадой Сэбина – обструктивная гидроцефалия, хориоретинит и массивное внутричерепное обызвествление. Наблюдается данный комплекс не более чем у 3% детей. Помимо триады, часто возникают миокардит, миозит, гепатит и пневмония. Клинические проявления напрямую зависят от присутствующих патологических изменений. Вероятность развития поздних осложнений на фоне латентного врожденного токсоплазмоза составляет порядка 90%. Период возникновения может быть разным – от нескольких месяцев до нескольких лет. Наиболее часто наблюдается поражение глаз, органа слуха и ЦНС. Самое распространенное осложнение – ретинит (примерно 85% случаев). К другим последствиям перенесенного врожденного токсоплазмоза относят олигофрению, гидроцефалию, повышение внутричерепного давления, острый и хронический энцефалит, эпилепсию, полную глухоту и/или слепоту, микрофтальм, увеит, хроническую гипертермию, редко – шизофрению.
Диагностика врожденного токсоплазмоза
Диагностика врожденного токсоплазмоза может проводиться в антенатальном и постнатальном периоде. Антенатальное исследование подразумевает использование инвазивных методов с дальнейшими лабораторными анализами. Абсолютное показание к их проведению – острый токсоплазмоз матери в сумме с нарушениями развития плода по результатам акушерского УЗИ. Выбор методики исследования зависит от срока беременности. При гестации от 10 недель проводится биопсия хориона, от 16 недель – амниоцентез, от 18 – кордоцентез. Для верификации инфекции полученный материал исследуют при помощи ПЦР. Постнатальная диагностика включает в себя сбор анамнестических данных и проведение клинического и лабораторного исследования. Данная мера является обязательной для всех детей, входящих в группу риска внутриутробного инфицирования. Неспецифическая диагностика и ее результаты зависят от присутствующих симптомов и синдромов. Список исследований может включать в себя ОАК (анемия, тромбоцитопения, лейкоцитоз); рентгенографию ОГК (признаки инфильтрации легких); нейросонографию и КТ головного мозга; биохимическое исследование крови с измерением АЛТ и АСТ, определением СРБ, уровня билирубина и его фракций (все показатели выше нормы); офтальмоскопию (некроз сетчатки); спинномозговую пункцию (признаки воспаления). Специфические методы подразумевают серодиагностику биологических жидкостей методом ИФА, при котором наблюдается возрастание титра антител IgG в 4 и больше раз и высокий уровень IgM на протяжении 10-14 суток. При необходимости проводится ПЦР с целью идентификации ДНК токсоплазмы.
Лечение врожденного токсоплазмоза
Лечение новорожденного с выраженной клинической картиной врожденного токсоплазмоза проводится только в условиях стационара, в отделении патологии новорожденных. Соблюдение специфического режима и рациона не требуется, их коррекция проводится в соответствии с состоянием ребенка. При наличии отягощенного анамнеза матери этиотропную терапию начинают с момента постановки предварительного диагноза. В других случаях перед началом лечения требуется проведения лабораторных методов исследования. Используемые схемы: пириметамин и сульфадимезин на 1-1,5 месяца; спирамицин или другие макролиды на 4-6 недель. В некоторых случаях применяют системные глюкокортикостероиды – преднизолон. Симптоматическое лечение зависит от присутствующих симптомов и синдромов, выявленных педиатром или неонатологом. При стойком повышении внутричерепного давления или развитии гидроцефалии показано хирургическое лечение. При необходимости дальнейшее лечение может проводиться амбулаторно под контролем педиатра, инфекциониста и других специалистов. В таких же условиях проводится терапия субклинической и латентной формы врожденного токсоплазмоза. Решение об отказе от приема препаратов принимается на основе клинико-лабораторных показателей, находящихся в пределах возрастной нормы, и заключения всех лечащих врачей.
Прогноз и профилактика врожденного токсоплазмоза
Прогноз при врожденном токсоплазмозе зависит от триместра, в котором произошло инфицирование плода и тяжести клинических проявлений. При развитии патологии в I триместре может наблюдаться самопроизвольное прерывание беременности и выкидыш или дальнейшее развитие тяжелых форм заболевания, однако аномалии органов при этом не возникают. При адекватной и своевременной терапии прогноз для жизни благоприятный, для выздоровления – сомнительный. Неспецифическая профилактика врожденного токсоплазмоза включает в себя ограничение контакта домашних животных с беременной женщиной, соблюдение гигиенических норм, прием в пищу только термически обработанных продуктов, тщательное мытье овощей и фруктов. При наличии факторов, указывающих на возможное инфицирование матери, проводится специфическая диагностика, направленная на идентификацию T. gondii. При подтверждении диагноза показано немедленное проведение этиотропной терапии. Специфической профилактики врожденного токсоплазмоза не разработано.

Токсоплазмоз – протозойная инфекция, характеризующаяся поражением нервной, лимфоидной системы, печени, селезенки, скелетных мышц, миокарда, глаз.
Заболевание имеет достаточно широкую распространенность среди людей и животных.
В большинстве случаев наблюдается бессимптомное паразитоносительство или же заболевание протекает хронически без характерных симптомов.
По некоторым данным, среди населения встречается от 10 до 30% клинически здоровых носителей токсоплазм. В некоторых же случаях может наступить обострение хронического токсоплазмоза с воспалительными процессами и поражением нервной ткани, глаз, сердечной мышцы, сосудистой системы.
Опасно заражение токсоплазмозом женщин во время беременности. Из организма матери через плаценту токсоплазмы могут проникнуть в организм плода и вызвать его гибель. В других случаях могут рождаться мертвые или нежизнеспособные дети с различными уродствами. Иногда у детей наблюдается острый врожденный токсоплазмоз, характеризующийся высокой температурой, отеком, сыпью. Результатом врожденного токсоплазмоза может быть отставание в умственном развитии вплоть до идиотии.
I. Токсоплазма-возбудитель токсоплазмоза
Тип: Простейшие (Protozoa)
Класс: Споровики (Sporozoa)
Отряд: Кокцидий (Coccidia)
Представитель: Toxoplazma gondii
Токсоплазмы имеют сложный цикл развития, который происходит в организме окончательного и промежуточного хозяина.
По своей форме токсоплазмы напоминают дольку апельсина или полумесяц. Они изогнуты, один конец их заострен, другой более округлый, с размерами 4-7х2-5 мкм. В центре находится крупное рыхлое ядро.
На заостренном конце токсоплазмы при исследовании под электронным микроскопом обнаруживается коноид – образование, похожее на присоску. Коноид служит для фиксации паразита на поверхности клетки при проникновении в нее. Далее вращательным движением паразит внедряется в клетку хозяина. Для эндозоида характерно бесполое размножение путем деления. В результате многократных делений в цитоплазме клетки хозяина накапливается большое число токсоплазм, растягивающих наружную мембрану клетки. Формируется скопление токсоплазм под клеточной мембраной, называемое псевдоцистой. После разрушения пораженной клетки токсоплазмы внедряются в новую. При хроническом токсоплазмоме помимо псевдоцист формируются и настоящие цисты. Цисты в клетках хозяев могут сохранять жизнеспособность на протяжении нескольких лет.
Для поддержания вида токсоплазме необходимо осуществлять половое размножение. Оно происходит в организме окончательного хозяина – хищников семейства кошачьих. При этом в эпителии тонкой кишки из одних эндозоидов образуются макрогаметы, а из других – микрогаметы. После копуляции гамет возникает зигота, покрывающаяся плотной оболочкой. Такая форма называется ооцистой. Ооцисты выделяются во внешнюю среду с испражнениями кошки. Они очень стойки к неблагоприятным условиям и в почве могут сохраняться годами.
II. Пути заражения
Человек может заражаться токсоплазмозом от животных при снятии шкуры, разделке туши, алиментарным или воздушно-капельным путем.
Наиболее распространенный способ инфицирования – уход за больным животным и уборка его испражнений. Домашние животные способны переносить токсоплазмоз на шерсти. Заразиться токсоплазмозом так же можно при употреблении в пищу инфицированных продуктов, мяса. После попадания в кишечник цисты, происходит распространение паразита с током крови по всему организму.
Стоит отметить, что заразиться токсоплазмозом при контакте с человеком невозможно. Передача токсоплазмоза от человека к человеку осуществляется только трансплацентарно, при заражении плода от больной матери.
III.Профилактика токсоплазмоза
Для профилактики токсоплазмоза большое значение имеет оздоровление природных очагов, лечение домашних животных, ограничение контакта с кошками, соблюдение правил личной гигиены, термическая обработка пищевых продуктов, особенно мяса. Следует избегать загрязнения почвы испражнениями кошек в районе расположения детских игровых площадок, песочниц. Домашних кошек не рекомендуется кормить сырым мясом. Следует обследовать их на токсоплазмоз и, в случае обнаружения заболевания, лечить.
Для предупреждения врожденного токсоплазмоза необходимо всех беременных женщин, впервые обратившихся в женскую консультацию, обследовать с помощью внутрикожной пробы с токсоплазмином. Беременные с положительными иммунологическими реакциями, т.е. иммунные, в дальнейшем наблюдении и тем более в этиотропном лечении не нуждаются. Беременные с отрицательными иммунологическими реакциями (неиммунные) относятся к группе риска, так как могут заразиться токсоплазмозом в ходе настоящей беременности. Они подлежат повторному иммунологическому обследованию во втором и третьем триместрах беременности. Сохранение отрицательных иммунологических проб свидетельствует об отсутствии заражения.
Заключение
Токсоплазмоз – заболевание, вызываемое микроскопическим паразитом, называемым Toxoplasma gondii. Существует две группы риска по заражению токсоплазмозом: беременные женщины и лица с иммунодефицитами. По результатам статистического исследования (США), каждый год приблизительно 3000 детей рождаются инфицированными токсоплазмозом.
Токсоплазмоз является одним из самых распространенных паразитарных заболеваний у человека. В Южной Америке, в странах Африки болезнь поразила более 90 процентов жителей. В США и Западной Европе количество инфицированных варьируется в пределах от 25 до 50 процентов.
По статистике в России токсоплазмозом заражен каждый третий человек. Несмотря на тот факт, что болезнь поражает большое количество жителей, часто она никак не проявляет себя. Более того, многие люди даже не догадываются о том, что являются носителями токсоплазмоза: симптомы заболевания списываются на уже существующие болячки, и обращение к врачу происходит в редких случаях. При тяжелых формах инфекция поражает нервную систему, глаза, селезенку, мышцы сердца и даже печень.
Список источников информации:
Грачева, Л.И. Проблема токсоплазмоза / Л.И. Грачева // 1999
2. Биология: учебник в 2-х т. / под ред. В.Н. Ярыгин. – Москва: ГЭОТАР-Медиа, 2013.
3. Пехов А.П. Биология: медицинская биология, генетика и паразитология: учебник/ А.П. Пехов. – М.: ГЭОТАР-Медиа, 2010. – 656 с.
Читайте также:

