Острые нарушения мезентериального кровообращения реферат
Обновлено: 30.06.2024
Острая мезентериальная ишемия – внезапная острая артериальная или венозная окклюзия или снижение кровотока в пределах мезентериального кровообращения [2].
Соотношение кодов МКБ-10 и МКБ-9
| МКБ-10 | МКБ-9 | ||
| Код | Название | Код | Название |
| К 55.0 | Острая мезентериальная ишемия | 45.30 | Локальное иссечение тонкой кишки |
| 45.63 | Тотальное иссечение тонкой кишки | ||
| 45.40 | Локальное иссечение толстой кишки | ||
| 45.70 | Частичная резекция толстой кишки | ||
| 45.73 | Правая гемиколэктомия | ||
| 45.74 | Резекция поперечно-ободочной кишки | ||
| 45.75 | Левая гемиколэктомия | ||
| 45.76 | Удаление сигмовидной кишки (Гартмана) | ||
| 45.79 | Другая частичная резекция толстой кишки | ||
| 54.11 | Лапаротомия диагностическая | ||
| 54.12 | Релапаротомия на месте недавней лапаротомии | ||
| 54.21 | Лапароскопия | ||
Дата разработки/пересмотра протокола: 2016 год.
Пользователи протокола: врачи скорой помощи, хирурги, анестезиологи-реаниматологи, ВОП, терапевты.
Категория пациентов: взрослые.
Шкала уровня доказательности
Уровни доказательности и степени рекомендаций [1], используемые в данном клиническом протоколе.
| Уровень достоверности определения | |
| IA | Данные из мета-анализа рандомизированных контролируемых исследований |
| IB | Данные, полученные из по меньшей мере одного рандомизированного контролируемого исследования |
| IIA | Данные, полученные из по меньшей мере одного контролируемого исследования без рандомизации |
| IIB | Данные, полученные из по меньшей мере одного квази-экспериментального исследования |
| III | Данные из неэкспериментальных описательных исследований, таких как сравнительные исследования, тематические контролируемые исследования |
| IV | Данные из отчетов экспертного комитета, мнений или клинического опыта |

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Клиническая классификация:
По этиологии [2]:
Острая артериальная мезентериальная ишемия (АМI):
1. артериальная эмболия (ЕАМI);
2. артериальный тромбоз (ТАМI);
3. венозный тромбоз (ВАМI);
4. неокклюзионная брыжеечная ишемия (NOMI).
Стадии болезни [3]:
1. ишемии;
2. инфаркта;
3. перитонита.
Состояние мезентериального кровотока:
1. компенсация;
2. субкомпенсация;
3. декомпенсация (быстро или медленно прогрессирующая).
Клиническая классификация сепсиса [ACCP/SCCM CC, 1992, Чикаго, 4, 5, 6]
| Патологический процесс | Клинико-лабораторные признаки |
| ССВО (SIRS – System inflammatory response syndrome) - синдром системного воспалительного ответа макроорганизма на мощное повреждающее воздействие (инфекция, травма, операция) | · температура тела выше ≥ 38С или ≤ 36С · тахикардия (ЧСС ≥ 90/мин) · тахипное (ЧД> 20/мин) или гипервентиляция (PаСО2 ≤ 32 мм рт. ст.) · лейкоциты> 12 х10 9 /л или 9 /л или наличие >10% незрелых форм |
| Сепсис (абдоминальный): системный ответ организма на инфекцию (инфекция + ССВО) | · наличие инфекционного очага (перитонит) · наличие 2х и более критериев ССВО (SIRS) · установление бактериемии не обязательно |
| Тяжелый сепсис | · дисфункция органов · нарушение перфузии (лактат-ацидоз, олигоурия, нарушение сознания) или гипотония (САД |
| Септический шок | · гипотония, резистентная к возмещению ОЦК · тканевая и органная гипоперфузия |
| Дополнительные определения | |
| Синдром полиорганной недостаточности (СПОН) | · дисфункция 2 и более систем организма |
| Рефрактерный септический шок | · гипотония, резистентная к возмещению ОЦК, инотропной и вазопрессорной поддержке |
Диагностика (амбулатория)
ДИАГНОСТИКА НА АМБУЛАТОРНОМ УРОВНЕ
Диагностические критерии
Физикальное исследование (осмотр, пальпация, перкуссия, аускультация, определение показателей гемодинамики – ЧСС, АД):
· возможно повышение артериального давления на 60-80 мм рт. ст. - симптом Блинова [3] (при окклюзии верхней брыжеечной артерии), брадикардия;
· несоответствие интенсивности боли физикальным данным при осмотре живота (в стадии ишемии живот мягкий, безболезненный; в стадии инфаркта живот вздут, болезнен, при этом зона болезненности не соответствует локализации спонтанных болей в животе);
· в стадии перитонита живот напряжен, резко болезнен, определяется симптом Щеткина-Блюмберга.
Лабораторные исследования: при подозрении на острое нарушение мезентериального кровообращения не проводятся.
Инструментальные исследования: при подозрении на острое нарушение мезентериального кровообращения не проводятся.
Диагностический алгоритм при обращении пациента в поликлинику
· к терапевту, ВОП:

· к хирургу:

Диагностика (стационар)
ДИАГНОСТИКА НА СТАЦИОНАРНОМ УРОВНЕ
Физикальное иссследование: Состояние больного зависит от стадии развития острой мезентериальной ишемии.
· В стадии ишемии больные беспокойны из-за выраженного болевого синдрома. При окклюзии верхней брыжеечной артерии возможно повышение артериального давления на 60-80 мм рт. ст. (симптом Блинова), брадикардия. Язык влажный, живот участвует в акте дыхания, мягкий и совершенно безболезненный, симптомов раздражения брюшины нет, перистальтика ослаблена или отсутствует, стул жидкий.
· В стадии инфаркта поведение становится более спокойным вследствие уменьшения болевого синдрома, на фоне нарастающей интоксикации появляется эйфория. Тахикардия. Язык сухой, в рвотных массах появляется кровь, живот вздут, мягкий, определяется отчетливая болезненность при пальпации, при этом зона болезненности не соответствует локализации спонтанных болей в животе. При венозном тромбозе появляется симптом Мондора – пальпация инфарцированной кишки в виде инфильтрата мягкоэластической консистенции без четких границ. При аускультации - перистальтика ослаблена или отсутствует. Стул жидкий с примесью крови.
· В стадии перитонита больной в вынужденном положении – на боку с приведенными к животу ногами, при перемене положения тела отмечается усиление боли в животе. Состояние больных резко ухудшается вследствие эндотоксикоза, возможно нарушение сознания. Гемодинамика не стабильная. Язык сухой. Отмечаются признаки системной воспалительной реакции: лихорадка, тахипноэ, тахикардия. Живот вздут, при пальпации определяется болезненность. Особенностью клинического проявления перитонита при ОМИ является более позднее появление мышечного напряжения и симптома Щеткина-Блюмберга. При аускультации - перистальтика ослаблена или отсутствует.
Все больные с подозрением на ОМИ должны быть осмотрены per rectum: в стадии инфаркта отмечается выделение крови в виде малинового желе.
При развитии абдоминального сепсиса к местным проявлениям (боль в животе, мышечное напряжение, положительные симптомы раздражения брюшины) присоединяются 2 и более критерия ССВО [4,5,6]:
· определяется температура тела выше ≥ 38С или ≤ 36С;
· тахикардия ≥ 90/мин, тахипное> 20/мин;
· лейкоциты> 12 х10 9 /л или 9 /л, или наличие >10% незрелых форм).
При тяжелом абдоминальном сепсисе развивается дисфункция органов (смотреть Приложение 1, настоящего КП):
· гипотензия (САД
Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований*
Дифференциальная диагностика проводится с острым панкреатитом, перфоративной язвой, желудочно-кишечным кровотечением.
| Заболевание | Предрасположенность | Клинические проявления |
| Артериальная окклюзионная Внезапная окклюзия верхней брыжеечной артерии эмболом или тромбом у больных с предрасположенностью | · Сердечная аритмия, фибрилляция предсердий · Ишемическая болезнь сердца, состояние после инфаркта миокарда · Окклюзионные заболевания периферических артерий | · Внезапные боли в животе · Безболезненный интервал от 6 до 12 часов после появления боли · Последующая гангрена кишечника с перитонитом |
| Артериальная неокклюзионная Ишемия, вызванная уменьшением сердечного выброса с реактивным спазмом мезентериаль-ных артерий | · Состояние после операции на сердце с искусственным кровообращением, осложненное течение заболеваний сердца · Долгосрочный гемодиализ · Прием сердечных гликозидов | · Усиление боли в животе · У интубированных пациентов: вздутие живота, повышение воспалительных параметров, появление признаков сепсиса |
| Венозный тромбоз Тромбоз мезентериаль- ной вены | · Панкреатит, рак · Врожденные тромбофилии (АТ-III-дефицит, дефицит протеина С, дефицит протеина S) · Гепатоцеллюлярный рак | · В зависимости от степени выраженности тромбоза · Часто неспецифические абдоминальные жалобы длятся несколько дней · Венозный тромбоз с перитонитом - в меньшинстве случаев |
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Азитромицин (Azithromycin) |
| Азтреонам (Aztreonam) |
| Алпростадил (Alprostadil) |
| Амикацин (Amikacin) |
| Аминофиллин (Aminophylline) |
| Амоксициллин (Amoxicillin) |
| Ампициллин (Ampicillin) |
| Апротинин (Aprotinin) |
| Ванкомицин (Vancomycin) |
| Гентамицин (Gentamicin) |
| Гепарин натрия (Heparin sodium) |
| Добутамин (Dobutamine) |
| Допамин (Dopamine) |
| Дорипенем (Doripenem) |
| Имипенем (Imipenem) |
| Калия хлорид (Potassium chloride) |
| Кальция хлорид (Calcium chloride) |
| Кетопрофен (Ketoprofen) |
| Кеторолак (Ketorolac) |
| Кларитромицин (Clarithromycin) |
| Комплекс аминокислот для парентерального питания (Complex of amino acids for parenteral nutrition) |
| Левофлоксацин (Levofloxacin) |
| Магния хлорид (Magnesium chloride) |
| Меропенем (Meropenem) |
| Метоклопрамид (Metoclopramide) |
| Метронидазол (Metronidazole) |
| Микафунгин (Micafungin) |
| Моксифлоксацин (Moxifloxacin) |
| Морфин (Morphine) |
| Надропарин кальция (Nadroparin calcium) |
| Натрия лактат (Sodium lactate) |
| Натрия хлорид (Sodium chloride) |
| Натрия хлорид (Sodium chloride) |
| Неостигмин (Neostigmine) |
| Пантопразол (Pantoprazole) |
| Пентоксифиллин (Pentoxifylline) |
| Пиперациллин (Piperacillin) |
| Повидон - йод (Povidone - iodine) |
| Сорбитол (Sorbitol) |
| Тазобактам (Tazobactam) |
| Тигециклин (Tigecycline) |
| Трамадол (Tramadol) |
| Тримеперидин (Trimeperidine) |
| Фамотидин (Famotidine) |
| Флуконазол (Fluconazole) |
| Фуросемид (Furosemide) |
| Хлоргексидин (Chlorhexidine) |
| Цефепим (Cefepime) |
| Цефоперазон (Cefoperazone) |
| Цефотаксим (Cefotaxime) |
| Цефтазидим (Ceftazidime) |
| Цефтриаксон (Ceftriaxone) |
| Цефуроксим (Cefuroxime) |
| Циластатин (Cilastatin) |
| Ципрофлоксацин (Ciprofloxacin) |
| Эноксапарин натрия (Enoxaparin sodium) |
| Эпопростенол (Epoprostenol) |
| Эртапенем (Ertapenem) |
| Этанол (Ethanol) |
Лечение (амбулатория)
ЛЕЧЕНИЕ НА АМБУЛАТОРНОМ УРОВНЕ
Алгоритм действий при неотложных ситуациях:

Немедикаментозное лечение: нет.
Медикаментозное лечение: нет.
Перечень основных лекарственных средств: нет
Перечень дополнительных лекарственных средств: нет.
Показания для консультации специалистов:
· консультации узких специалистов – по показаниям.
Профилактические мероприятия:
Первичная профилактика:
· своевременная профилактика и лечение сердечно-сосудистых заболеваний;
· Д-наблюдение за больными, перенесшими интервенционные процедуры.
Профилактика вторичных осложнений:
· своевременное обращение больных за медицинской помощью при возникновении абдоминальной боли;
· своевременная диагностика: высокий индекс подозрений на ОМИ является показанием для экстренного направления больного в профильный стационар и проведения диагностических и мероприятий.
Мониторинг состояния пациента: наблюдение у врача по месту жительства.
Индикаторы эффективности лечения:
· своевременное направление на стационарное лечение.
Лечение (скорая помощь)
ДИАГНОСТИКА И ЛЕЧЕНИЕ НА ЭТАПЕ СКОРОЙ НЕОТЛОЖНОЙ ПОМОЩИ
Диагностические мероприятия
Физикальное исследование (осмотр, пальпация, перкуссия, аускультация, определение показателей гемодинамики – ЧСС, АД):
· возможно повышение артериального давления на 60-80 мм рт. ст. - симптом Блинова [3] (при окклюзии верхней брыжеечной артерии), брадикардия;
· несоответствие интенсивности боли физикальным данным при осмотре живота (в стадии ишемии живот мягкий, безболезненный; в стадии инфаркта живот вздут, болезнен, при этом зона болезненности не соответствует локализации спонтанных болей в животе);
· в стадии перитонита живот напряжен, резко болезнен, определяется симптом Щеткина-Блюмберга.
Медикаментозное лечение:
| №п/п | Название МНН | Доза | Кратность | Способ введения | Продолжи- тель-ность лечения | Примечание | УД |
| 1 | натрия хлорид | 0,9% раствор - 400мл. | 1-2 раза | в/в капельно | по пути следо-вания в стацио-нар | при нестабильной гемодинамике (септический шок) | IА |
Лечение (стационар)
ЛЕЧЕНИЕ НА СТАЦИОНАРНОМ УРОВНЕ
Тактика лечения: [2]
При острой мезентериальной ишемии в стадии ишемии (до 12 часов от начала заболевания) выполняются эндоваскулярные вмешательства (если позволяют ресурсы клиники) или открытая эмболтромбэктомия с целью восстановления мезентериального кровобращения.
При острой мезентериальной ишемии в стадии инфаркта кишки и перитонита выполняется резекция кишки, санация, дренирование брюшной полости, по показаниям – реваскуляризация.
При установленной неокклюзионной ишемии и венозном тробозе в стадии ишемии проводится консервативное лечение.
Дифференцированная лечебная тактика
(Рекомендации ESTES
European Society for Trauma and Emergency Surgery, 2016) [2]:
Тактика лечения ОМИ в стадии ишемии (без деструкции и перитонита):
· при ОМИ без деструкции и перитонита выполняется вмешательство по восстановлению мезентериального кровобращения не позднее 12 часов с момента появления симптомов УД III [2]. Выбор метода (эндоваскулярное вмешательство или открытая тромбоэмболэктомия) определяется ресурсами клиники, личным опытом и техническими возможностями хирурга УД IV [2];
· при обнаружении артериальной эмболии (ЕАМI) во время лапаротомии должна быть выполнена открытая эмболэктомия, если нет противопоказаний УД IV [2];
· при артериальном тромбозе (ТАМI) без деструкции и перитонита выполняется эндоваскулярное вмешательство, если позволяют ресурсы клиники, личный опыт и технические возможности хирурга УД III [2];
· при обнаружении артериального тромбоза (ТАМI) во время лапаротомии выбор сосудистого вмешательства определяется ресурсами клиники, личным опытом и техническими возможностями хирурга УД IV [2];
· венозный тромбоз (VАМI) без деструкции кишки и перитонита лечится консервативно антикоагулянтами под контролем коагулограммы (5000 МЕ гепарина с последующим непрерывным введением (перфузор) в дозе 20 000 МЕ гепарина / 24 часа); при отрицательной динамике консервативного лечения венозного мезентериального тромбоза выполняется эндоваскулярное вмешательство УД IV [2];
· неокклюзионная брыжеечная ишемия (NOMI) без деструкции кишки и перитонита лечится консервативно путем коррекции основной причины (улучшение брыжеечной перфузии путем прямого введения простагландинов в SMA (PGE 1 алпростадил 20 мкг болюсно, с последующим непрерывным введением (перфузор) в дозе от 60 до 80 мкг / 24 часа (альтернатива: PGI 2 эпопростенол до 6 нг / кг / мин, гепарин IV 20 000 МЕ / 24 часа). Для оценки эффективности вазодилатации проводится ангиография в динамике I В [ACC / AHA].
Хирургическое вмешательство.
Анестезиологическое обеспечение – общее обезболивание.
Доступ – широкая срединная лапаротомия.
Немедикаментозное лечение:
· Режим: в тяжелом состоянии – постельный, при отчетливой положительной динамике – ранняя активизация больного;
· Диета: после установления диагноза до операции и 1-2-е сутки после операции – стол 0, в послеоперационном периоде - раннее зондовое энтеральное питание с целью защиты слизистой ЖКТ и профилактики бактериальной транслокации.
Острое нарушение мезентериального кровотока — тяжелейшее заболевание как у молодых, так и у лиц пожилого и старческого возраста с громадной летальностью, которая, по данным академика B.C. Савельева и И.В. Спиридонова, достигает до 85—100% в зависимости от распространенности острой ишемии кишечника.
Причины столь высокой летальности: поздняя госпитализация, несвоевременная диагностика, отсутствие безопасных тромболитиков, соответственно — неадекватное лечение. В связи со сниженным барьером чувствительности позднее обращение к специалистам особенно актуально для стариков.
Кроме того, необходимо подчеркнуть и анатомо-физиологические особенности у них кишечного кровоснабжения:
1. крайняя недостаточность коллатерального кровоснабжения и возможности компенсации кровообращения через коллатерали;
2. быстрый некроз слизистой и стенок при острой ишемии и венозном тромбозе;
3. частые ангиоспазмы, наступающие во время пищеварения и перистальтики кишечника.
Помимо всего, острые нарушения мезентериального кровоснабжения у рассматриваемой категории больных чаще возникают на фоне гипертонической болезни, атеросклероза, инфаркта миокарда, нарушений ритма сердечных сокращений, эндокардита, тромбоза аорты, заболеваний, сопровождающихся гиперкоагуляцией (злокачественных новообразований), обезвоживанием, декомпенсацией сердечной деятельности и др.
Первыми клинико-морфологическую картину артериальной непроходимости описали немецкие патологи R. Tiedemann и R.K. Virchov. Модель инфаркта кишечника создал М. Litten путём перевязки ВБА. С помощью этой модели он обосновал, что основной причиной сосудистых расстройств кишечника служит закупорка крупных артериальных сосудов.
Правильный дооперационный диагноз при эмболии верхней брыжеечной артерии поставил Opolzer.
Основные вопросы кровоснабжения кишечника были описаны еще А. Везалием.
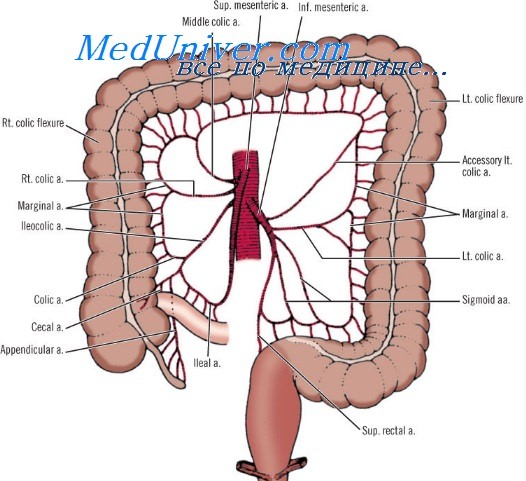
Кровоснабжение кишечника осуществляется двумя висцеральными ветвями брюшной аорты: верхней и нижней брыжеечными артериями.
Верхняя брыжеечная артерия, без сомнения, играет наиболее важную роль в кровоснабжении пищеварительного тракта. Верхняя брыжеечная артерия отходит от передней полуокружности аорты обычно чуть выше отхождения почечных артерий, на уровне диска I и II поясничных позвонков. В своем начале она имеет диаметр 0,5—1 см. Артерия проходит непосредственно сзади шейки поджелудочной железы, а затем пересекает спереди 12-перстную кишку.
Первая ветвь ВБА — нижняя панкреатодуоденальная артерия, которая идет вверх позади головки поджелудочной железы до соединения с верхней панкреатодуоденальной ветвью желудочно-дуоденальной артерии. Эти небольшие, диаметром 1—2 мм, сосуды имеют важное клиническое значение. Во-первых, они играют основную роль в кровоснабжении головки поджелудочной железы и нижней части общего желчного протока. Еще важнее то, что этот анастомоз представляет главный коллатеральный путь между зонами, кровоснабжаемыми чревным стволом и верхней брыжеечной артерией, и при окклюзии ВБА может дилатироваться в значительной степени.
При выходе из зоны двенадцатиперстной кишки ВБА проходит вниз в корне брыжейки тонкой кишки к правой подвздошной ямке, как правило, с изгибом в левую сторону.
Ее следующая ветвь после нижней панкреатодуоденальной артерии — средняя ободочная артерия, которая, отходя от правой стороны ВБА, достигает поперечноободочной кишки и разделяется на левую и правую ветви, составляющие часть важного маргинального (краевого) кровоснабжения толстой кишки.
Почти на 4 см ниже средней ободочной артерии от ВБА отходит обычно очень небольшая правая ободочная артерия.
Основной ствол ВБА идет вниз и входит в систему маргинального кишечного кровообращения в виде подвздошно-ободочной артерии (a. ileocolica). Из этих трех сосудов правой половины толстой кишки анатомически постоянна лишь подвздошно-ободочная артерия, которая снабжает начальную часть правой половины толстой кишки. От основного ствола правая и средняя ободочные артерии часто отходят вместе. В 10% случаев правая ободочная артерия отходит от подвздошно-ободочной артерии.
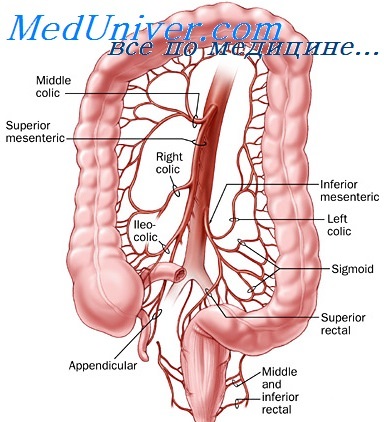
В тонкий кишечник кровь поступает из ветвей, отходящих от левой стороны ВБА, через так называемые кишечные артерии, число которых колеблется от 3 до 12, и из ряда артериальных дуг; их количество увеличивается сверху вниз, а строение усложняется.
Нижняя брыжеечная артерия намного меньше, чем ВБА. Она отходит от переднелевой поверхности аорты приблизительно на 3—4 см выше бифуркации. Левая ободочная артерия идет кверху и до соединения с маргинальной артерией ободочной кишки отдает до 3—4 ветвей vasa recta.
Далее она спускается позади ректосигмоидального соединения и прямой кишки, заканчиваясь a. haemorrodalis superior, которая делится на три крупные артериальные ветви (одна слева и две справа). Эта нижняя зона кровоснабжения нижней брыжеечной артерии широко анастомозирует с коллатералями ветвей внутренней подвздошной артерии (точнее, со средней прямокишечной артерией, отходящей от внутренней половой артерии).
Промежуточные артерии. Между тремя главными ветвями аорты и микроскопическими сплетениями, которые непосредственно кровоснабжают структуры внутренних органов, находится сеть достаточно крупных сосудов. Эти сосуды важны с клинической точки зрения, поскольку именно там может быть локализован патологический процесс или повреждение вследствие случайной или хирургической травмы.
Данная промежуточная часть системы кровообращения включает кишечные сосуды и аркады тонкого кишечника, маргинальное кровообращение и vasa recta толстой кишки. Окклюзия какого-то отделенного сосуда этой системы не приводит ни к расстройству кровообращения в слизистой оболочке, ни к нарушению функции кишечника. Однако поражение нескольких сосудов, как это может быть при эмболии или тромбозе на фоне атероматоза, а также вследствие ранения, образования гематомы в результате плохо выполненной хирургической резекции, может быть причиной значительных расстройств вплоть до полного некроза кишки.
Ввиду особенностей архитектоники этих сосудов, повреждения, локализованные в правом углу по отношению к длинной оси кишечника, менее опасны, чем расположенные параллельно ему.
Ветви ВБА, идущие к тонкой кишке, в самом начале имеют небольшой диаметр, расположены с интервалом 1—2 см и не формируют аркадной системы. Проходя вниз вдоль тонкого кишечника, сосудистая система становится более сложной, образует три-четыре яруса параллельных аркад.
Кровоснабжение терминального отдела подвздошной кишки имеет анатомические особенности, отражающие эмбриогенез. В период внутриутробного развития плода, когда его размер достигает 17 мм, основная правая дистальная ветвь ВБА (будущая подвздошно-ободочная артерия) кровоснабжает зачаток, из которого образуются слепая кишка, червеобразный отросток и терминальный отдел подвздошной кишки. Этот сосуд формирует лишь одну коллатераль к дистальной части пупочной петли.
Таким образом, в процессе эмбрионального развития возникают две различные сосудистые зоны, связанные с верхней брышеечной артерией:
1) проксимальный сегмент пупочной петли, из которого образуются третья и четвертая части двенадцатиперстной кишки, вся тощая и большой отдел подвздошной кишки, кровоснабжается через сеть коллатералей, отходящих от левой стороны артерии;
2) дистальный сегмент пупочной петли, образующий терминальный отдел подвздошной кишки, слепую и восходящую кишку, а также большую часть поперечной ободочной кишки, сегмент снабжается кровью через 2—3 ветви, отходящие от правой стороны верхней брыжеечной артерии.
Это объясняет, почему область между двумя указанными сегментами подвздошной кишки, один из которых относится к зоне со многими сосудами, а другой — к зоне с малым числом сосудов, получила репутацию имеющей скудное кровоснабжение.
На самом деле исследования последних лет показали, что такая точка зрения на анатомию взрослого организма неправильна. Vasa recta равномерно распределяются на всем протяжении подвздошной кишки, за исключением ее последних 5 см, где промежутки между сосудами больше. Однако терминальный отдел подвздошной кишки отчасти снабжается по коллатералям от сосудов слепой кишки.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Острая окклюзия мезентериальных сосудов – острое нарушение кровообращения в брыжеечных сосудах, приводящее к ишемии кишечника. Заболевание проявляется резкой, нестерпимой болью в животе, рвотой и поносом с примесью крови, шоковым состоянием. Диагноз острой окклюзии мезентериальных сосудов определяют на основании клинической картины, данных селективной ангиографии, рентгенографии брюшной полости, лапароскопии. Острая окклюзия мезентериальных сосудов требует экстренного оперативного вмешательства (эмбол- или тромбэндартериоэктомии, резекции пораженных отделов кишечника), профилактики перитонита и повторных окклюзий.
Общие сведения
Острая окклюзия мезентериальных сосудов - неотложная патология в гастроэнтерологии, возникающая вследствие тромбоза или эмболии сосудов брыжейки. Острая окклюзия мезентериальных сосудов проявляется резким нарушением кровообращения в сосудистых участках проксимальнее и дистальнее места обструкции, сопровождается выраженным ангиоспазмом и дополнительным тромбообразованием, в результате чего возникает острое нарушение питания и ишемическое поражение стенки кишечника. В дальнейшем начинают развиваться необратимые деструктивные изменения, формируется анемический и геморрагический инфаркт (некроз) кишечника. Острая окклюзия мезентериальных сосудов характеризуется крайне тяжелым течением и высокой летальностью.
Локализация и протяженность ишемического поражения кишечника при острой окклюзии мезентериальных сосудов зависит от вида и уровня обструкции, наличия коллатеральных путей компенсации кровотока. В 90% случаев наблюдается окклюзия основного ствола или одной из ветвей верхней брыжеечной артерии, в большей степени обеспечивающей кровоснабжение пищеварительного тракта. Нижняя брыжеечная артерия имеет хорошие коллатеральные связи, поэтому при ее окклюзии редко возникают серьезные нарушения мезентериального кровообращения. Окклюзия брыжеечных вен встречается реже; возможно также смешанное поражение брыжеечных артерий и вен, при котором острой окклюзии одного из сосудов предшествует хроническая обструкция другого.
Острая окклюзия мезентериальных сосудов встречается преимущественно у лиц мужского пола в возрасте старше 50-60 лет.

Причины острой окклюзии мезентериальных сосудов
Острая окклюзия мезентериальных сосудов развивается как осложнение различных сердечно-сосудистых заболеваний (атеросклероза, пороков сердца, системных аллергических васкулитов, ревматизма, гипертонической болезни, аневризмы брюшной аорты, аритмии), предшествующих операций на сердце и аорте, злокачественных опухолей, травм.
Непосредственной причиной острой окклюзии мезентериальных сосудов являются тромбоз и эмболия. При тромбозе просвет сосудов брыжейки перекрывается тромбом, образовавшимся вследствие изменения сосудистых стенок на фоне повышенной свертываемости крови и замедленного кровотока (патогенетическая триада Вихрова). При эмболии наблюдается обструкция брыжеечных сосудов частицей тканью опухоли, инородным телом или пузырьком воздуха, мигрировавшими от первичного источника поражения с током крови.
Острая окклюзия мезентериальных сосудов может протекать с компенсацией, субкомпенсацией и декомпенсацией мезентериального кровотока. При компенсации мезентериального кровотока (спонтанно или под воздействием консервативной терапии) все функции кишечника восстанавливаются полностью. Субкомпенсация мезентериального кровотока ввиду недостаточного кровоснабжения может приводить к ряду заболеваний кишечника: брюшной жабе, язвенным энтеритам и колитам и др. Декомпенсация мезентериального кровообращения вызывает распространенный гнойный перитонит и развитие тяжелого абдоминального сепсиса.
Симптомы острой окклюзии мезентериальных сосудов
Наблюдается резкая бледность кожных покровов, цианоз, шоковое состояние, повышение артериального давления на 60-80 единиц (симптом Блинова), брадикардия. Для острой окклюзии мезентериальных сосудов характерно несоответствие между тяжестью состояния больного и данными его осмотра: в первые часы живот остается мягким, брюшная стенка участвует в дыхании, отмечается незначительная болезненность без симптомов раздражения брюшины.
В стадии инфаркта (через 6-12 часов от начала острой окклюзии мезентериальных сосудов) болевые ощущения немного уменьшаются, но нарастает локальная (в зоне поражения кишки) болезненность при пальпации, между пупком и лобком может прощупываться тестовидная припухлость (симптом Мондора), ухудшается состояние больного. Эвакуаторная функция кишечника сохраняется, артериальное давление нормализуется, пульс учащается.
Диагностика
Распознавание острой окклюзии мезентериальных сосудов опирается на анализ клинической картины заболевания: острый болевой абдоминальный синдром, поражение сердца и сосудов в анамнезе. Важное диагностическое значение имеет исследование коагулограммы, определение количества тромбоцитов, холестерина крови.
При обзорной рентгенографии брюшной полости определяется пневматизация кишечника, наличие горизонтальных уровней жидкости в брюшной полости. Специфическим методом диагностики острой окклюзии мезентериальных сосудов является селективная мезентерикография, которая уже на ранней стадии заболевания может выявить отсутствие кровотока в стволе и ветвях брыжеечной артерии. При наличии технической возможности выполняется магнитно-резонансная ангиография мезентериальных сосудов.
Диагностическая лапароскопия позволяет обнаружить изменения кишечника и брюшной полости, наличие признаков анемического и геморрагического инфаркта кишки. Острую окклюзию мезентериальных сосудов дифференцируют от прободной язвы желудка и двенадцатиперстной кишки, острого аппендицита, кишечной непроходимости, острого панкреатита и острого холецистита.
Лечение острой окклюзии мезентериальных сосудов
При острой окклюзии мезентериальных сосудов показано экстренное хирургическое вмешательство, целью которого служит ревизия кишечника с оценкой его жизнеспособности, ревизия основных брыжеечных сосудов, устранение причины сосудистой непроходимости и восстановление мезентериального кровотока, резекция некротизированных отделов кишечника, профилактика перитонита.
Реваскуляризация кишечника выполняется путем непрямой эмбол- или тромбэндартериоэктомии, в трудных случаях проводится реконструктивное обходное шунтирование с использованием сосудистых протезов (протезирование верхней брыжеечной артерии).
При некрозе кишечника реваскуляризация дополняется частичной или обширной резекцией пораженных участков кишечника и активным назоинтестинальным дренированием для лечения послеоперационного пареза кишечника. Через 24-48 часов возможно выполнение релапаротомии с целью контроля состояния брюшной полости или наложения отсроченного анастомоза.
Пред- и послеоперационное ведение больного с острой окклюзией мезентериальных сосудов включает назначение антитромботических препаратов для профилактики повторной эмболии и ретромбоза; мероприятия интенсивной терапии с целью восстановления ОЦК, устранения интоксикации, улучшения кровотока и тканевого метаболизма, стабилизации сердечной деятельности. Проводится антибактериальная терапия, дренирование и санация брюшной полости для предупреждения гангрены и перитонита.
Прогноз и профилактика
Профилактика острой окклюзии мезентериальных сосудов заключается в своевременном устранении потенциального источника тромбоэмболии, т. е. первичного заболевания (атеросклероза, мерцательной аритмии, ревматического порока сердца, аневризм и др.).
Острое нарушение мезентериального кровообращения (ОНМК) относится к числу наиболее тяжелых, недостаточно изученных заболеваний в хирургии [1—4], высокие показатели послеоперационной летальности обусловлены запоздалой диагностикой, обширным ишемическим повреждением и некрозом кишечника. Отсутствие патогномоничных симптомов, невысокие показатели чувствительности и специфичности лучевых, лабораторных методов на ранних стадиях ОНМК приводят к промедлению с эффективными методами лечения [5].
Несмотря на происшедшие за последние десятилетия достижения в диагностике и лечении, отмечается высокий уровень смертности при ишемии в бассейне верхней брыжеечной артерии — от 40 до 70% [7].
Ранняя диагностика предполагает соответственно раннее начало лечения, а опоздание с диагностикой влечет плохие исходы, 24-часовое опоздание снижает выживаемость на 20% [7]. ОНМК наступает в результате гипоксии, что приводит к инфаркту кишечника. Больные с ОНМК не имеют обычной истории (анамнеза) атеросклеротического поражения сосудов, как, например, при инфаркте миокарда, стенокардии, хронической сердечной недостаточности, инсульте или заболеваниях периферических сосудов [8].
ОНМК может быть вызвано эмболией или тромбозом (в 70—80% в бассейне брыжеечной артерии) [3], или окклюзионными заболеваниями сосудов, а также может быть обусловлено ятрогенией [9—11]. ОНМК в 50% случаев наступает из-за тромбоэмболии, в 12% — артериального тромбоза, в 8% — венозного тромбоза, в 20% причинами служат неокклюзионные нарушения, в 10% заболевание вызвано другими причинами [4, 5]. В случае тромбоэмболической окклюзии ввиду отсутствия выраженного коллатерального кровообращения наступает ранняя ишемия и последующий трансмуральный некроз. Более редкими причинами ОНКМ являются венозный тромбоз, нетромботические механические причины, например ущемленные грыжи [12]. Повышенному риску ОНМК подвержены больные с историей артериальной эмболии, васкулита, тромбозом глубоких вен конечностей, гиперкоагуляцией, а также с хронической постпрандиальной болью [13]. Васкулит выступает общей причиной ишемии верхней брыжеечной артерии у молодых лиц с аутоиммунными заболеваниями [14]. Описаны случаи причастности к ОНМК сосудистых аномалий [15]. Сердце является наиболее частым источником эмболизации (≈80% случаев): самая частая причина — мерцательная аритмия (≈75%), затем следует тромбоз левого желудочка после недавнего инфаркта миокарда (≈25%) [16].
Состояние гиперкоагуляции, приводящее к артериальному или венозному тромбозу брыжеечных сосудов, может быть спровоцировано недостатком белков С и S, дефицитом антитромбина III, антител к фосфолипидам, гепарин-индуцированной тромбоцитопенией, мутацией V фактора Лейдена, использованием эстрогенов, в частности в виде противозачаточных средств [9—11, 17].
Неокклюзионное ОНМК относится к кишечной ишемии без артериальной или венозной обструкции и встречается приблизительно у 20% больных [11]. Это состояние, являясь обычно результатом низкого сердечного выброса, приводит к снижению брыжеечной перфузии. Неокклюзионные формы ОНМК были описаны у больных с застойной сердечной недостаточностью, сепсисом, глубокой гипотензией и гиповолемией. Эти условия индуцируют спланхническую вазоконстрикцию [18], которая может привести к инфаркту кишечника. Кроме того, такие препараты, как алкалоид спорыньи, кокаин, наперстянка, могут вызвать также развитие спланхнической вазоконстрикции [17, 18]. ОНМК главным образом встречается у лиц пожилого возраста, имеющих часто другие коморбидные заболевания, из-за возраста и наличия нескольких заболеваний у этих пациенов снижен физиологический резерв, что делает их уязвимыми. Следовательно, необходимо иметь в виду высокую степень риска ОНМК у данного контингента и предпринимать меры по ранней его диагностике, что приведет к снижению осложнений и смертности.
Клинические проявления ОНМК разнообразны, для классического начала заболевания характерна острая сильная абдоминальная боль. Перитонит и сепсис способствуют прогрессированию ишемии в трансмуральный некроз [19]. Постпрандиальные боли, тошнота, потеря веса часто отмечаются у пациентов с хронической мезентериальной ишемией и тромбозом верхней брыжеечной артерии [19]. Хроническая мезентериальная ишемия ассоциируется с болями после еды, страхом еды, последующим похуданием [13]. Ранняя диагностика ОНМК представляет сложную задачу из-за широкой изменчивости клинической картины. Боль в животе — доминирующий симптом — выявляется почти у 85% больных [8, 16], изменения психического статуса — у 30% пожилых пациентов [20]. Часто боли, локализованные в околопупочной области, связаны с малыми проявлениями кишечной ишемии. У больных с хронической мезентериальной ишемией развитие острой абдоминальной боли обусловливается острым артериальным тромбозом верхней брыжеечной артерии, пораженной тяжелым атеросклерозом [21, 22]. Неокклюзионную кишечную ишемию можно заподозрить у больных с болью или без боли в животе, у которых отмечаются понос и бактериемия после сердечно-легочной реанимации [23]. Другие симптомы ОНМК — понос, тошнота, рвота, которые наблюдаются у 50% больных [12], диарея часто кровавая, особенно при инфаркте кишечника. Рвота и тошнота возникают в результате интенсивного мышечного спазма и гиперперистальтики в раннем периоде ишемии кишечника [24].
Мезентериальный венозный тромбоз имеет вариабельную симптоматику и зачастую менее тяжелую клиническую картину, прогрессирование симптомов происходит медленнее, чем при артериальном тромбозе. Абдоминальная боль (около 85% случаев), анорексия (около 50%), тошнота и рвота (около 45%), кровотечение из верхних и нижних отделов ЖКТ (около 35 и 20% соответственно) и запор (около 10%) являются типичными симптомами патологии. По наблюдениям, пациенты страдают от боли до 5 дней, прежде чем обратиться за медицинской помощью [10].
Живот может быть мягким при глубокой пальпации, кишечные шумы — нормальными. С нарастанием ишемии кишечника у больных развивается вздутие и ослабление кишечных шумов в результате гипоперистальтики. Почти в 75% случаев выявляется скрытая кровь в кале [12]; если ишемия прогрессирует к инфаркту кишечника, возникают перитонеальные знаки, лихорадка, тахикардия [18]. При невыполнении хирургического вмешательства в ранние сроки у больных возникают сепсис, гипотензия, почечная недостаточность с летальным исходом.
Для диагностики ОНМК исследуют ряд лабораторных показателей, которые не относятся к специфическим. Лейкоцитоз со сдвигом влево является общим показателем [22, 23, 25], может быть повышенной амилаза сыворотки крови [4], метаболический ацидоз развивается у большинства больных в результате накопления молочной кислоты [22, 25, 26]. Кроме того, при некрозе кишечника повышается уровень лактата сыворотки, фосфатов, щелочной фосфатазы, отмечаются преренальная азотемия, гипоксемия, бактериемия, сепсис [27]. При ОНМК, кроме лейкоцитоза, метаболического ацидоза, лактата крови, отмечают повышение показателей D-димеров, [19]. Считается, что высокий лейкоцитоз (более 20×10 9 /л) не позволяет отличить ОНМК от других заболеваний [28, 29]. В проспективных клинических исследованиях классически описывается метаболический ацидоз [30], а первоначальный анализ газов крови показал, что метаболический алкалоз наблюдается чаще, чем ацидоз, и это происходит при тяжелой рвоте во время раннего периода ишемии кишечника. Предполагалось, что D-димеры — важный показатель ОНМК, однако D-димеры как продукты деградации фибрина освобождаются во время внутрисосудистого свертывания и осаждения фибрина и могут присутствовать при наличии нескольких условий [31]. В недавнем исследовании было продемонстрировано, что определение D-димеров не дифференцирует пациентов с ОНМК и пациентов без острой ишемии, нет какой-либо разницы в уровнях D-димеров при некрозе кишечника и при резектабельных и нерезектабельных поражениях [32]. L-лактат ассоциируется с поздней стадией брыжеечной ишемии с обширным трансмуральным некрозом, гипоперфузией, превалированием анаэробного метаболизма и смертью [33]. В некоторых исследованиях сообщается об отсутствии высокого уровня L-лактата в случаях обширной ишемии кишечника, данный факт объясняют способностью печени очищать большое количество L-лактата из мезентериально-портального кровотока [34]. Далее было показано, что уровень L-лактата, повышение и количество лейкоцитов не могут использоваться как маркеры брыжеечной ишемии [35], вышеуказанные показатели были недискриминационными в определении ишемии кишечника или других заболеваний, таких как перфорация желудка, панкреатит, перфоративный аппендицит. Количество лейкоцитов существенно не отличалось у разных групп пациентов (13,9×10 9 /л): с ишемией кишечника и с другими заболеваниями (перфорацией желудка, панкреатитом, перфоративным аппендицитом). Количество лейкоцитов у пациентов с ишемией кишечника (13,9×10 9 /л) существенно не отличается от такового у пациентов контрольной группы (12,7×10 9 /л). Эти лабораторные показатели не являются чувствительными или достаточно конкретными, чтобы установить или исключить ОНМК, они возникают только после трансмурального инфаркта кишечника и поэтому не могут использоваться для ранней диагностики [13].
В последнее время предлагаются биохимические маркеры для раннего обнаружения ишемии кишечника, которая начинается в слизистой оболочке и распространяется в сторону серозной оболочки [33]. Идеальным может быть биомаркер, исходящий из слизистой оболочки кишечника на ранних стадиях ишемии. Согласно опубликованному обзору [36] таковыми могут быть белок, связывающий жирные кислоты кишечника (I-FABP), альфа глутатион S-трансфераза (GST) и D-лактат. Белки, связывающие жирные кислоты, представляют собой цитозолевые белки с низкой молекулярной массой (14—15кДа) I-FABP и участвуют в поглощении и потреблении жирных кислот. Эти белки в венозную систему поступают при нарушении целостности мембраны энтероцитов. При развитии мезентериальной ишемии и повреждении энтероцитов I-FABP являются ее маркерами, в анализах мочи и крови уровень белка значительно выше по сравнению с таковым у здоровых лиц [37]. Показатель I-FABPбыл повышен и при ограниченных некрозах кишечника, в отличие от случаев кишечной непроходимости с подозрением на ишемию [38]. Другие исследования показали высокую чувствительность и специфичность (0,90 и 0,89 соответственно) показателей FABP в моче [35].
Другой потенциальный маркер — альфа-GSTиз цитозольных ферментов, участвующих в детоксикации и освобождающихся из различных клеток при повреждении мембраны клеток [39]. GST участвует в детоксикации ряда токсических соединений путем конъюгации глутатиона, отличается высокой активностью, особенно в печени и слизистой оболочке кишечника [33]. Чувствительность и специфичность GST в диагностике ОНМК — 0,68 и 0,85 соответственно.
Предполагают, что увеличение уровня D-лактата, производного бактерий (кишечной палочки) [34], при ОНМК связано с транслокацией бактерий и дисбактериозом после повреждения слизистой оболочки. Следует отметить, что чувствительность и специфичность определения D-лактата составляют лишь 0,82 и 0,48 соответственно, что делает непригодным его использование в качестве маркера ишемии кишечника, учитывая превосходство альтернативных методов — FABP и GST.
Описано обследование 291 больного с острым животом, которым вычисляли мультидетекторные ряды при КТ-сканировании [42], все оригинальные КТ-заключения (диагнозы) были установлены несколькими радиологами. Чувствительность и специфичность КТА мультидетекторных рядов для диагностики ОНМК равнялись 0,79 и 0,98 соответственно. На основании вышеуказанных данных считается, что КТА — наиболее приемлемый и точный метод диагностики. Однако раннее выявление больных с ишемией кишечника остается проблемным. В начале идентификации радиолог может провести структурную оценку данных КТ-сканирования ОНМК, что может повысить чувствительность КТА [41].
Анализ эффективности КТА позволил выделить две группы признаков — неспецифические и косвенные [2]: свободный газ в просвете венозных сосудов брыжейки тонкой и толстой кишки, в стенке кишечника, указывающий на наличие некроза стенки. К неспецифическим признакам авторы отнесли пневматоз кишечника, отек брыжейки, усиление сосудистого рисунка брыжейки, к косвенным — асцит, атеросклеротическое поражение брюшной аорты, ее висцеральных ветвей.
При поступлении и динамическом наблюдении больных с подозрением на ОНМК лапароскопия выполнялась у 56,1% больных, ввиду ложноотрицательных результатов в стадии ишемии кишечника, чувствительность ее составила 83% [2].
Обзорная рентгенография брюшной полости может не выявлять каких-либо отклонений при наличии клинической картины ОНМК. Однако она является полезной в выявлении других серьезных заболеваний: кишечной непроходимости, динамической кишечной непроходимости, толстокишечной псевдонепроходимости.
Конкретные рентгенологические признаки ОНМК включают отек кишечной стенки, кровоизлияния, некрозмышечного слоя, что приводит к выраженному угнетению (до аперистальтики) перистальтики кишечника примерно у 25% больных [43]. Серьезные рентгенологические выводы включают пневмоперитонеум как результат перфорации кишечника, пневматоз тонкой кишки, пневматоз воротной вены, газ в стенке кишки [44]. Дуплексное УЗИ верхней брыжеечной артерии может быть полезным для диагностики острой мезентериальной непроходимости, но это зависит от надлежащей подготовки, а также от технологии и опыта исследователя.
КТ-ангиографическая 3D-реконструкция позволяет визуализировать случаи сложной анатомии [44].
Новые диагностические стратегии для раннего выявления ишемии кишечника (кроме биохимических маркеров) включают МРТ-ангиографию (МРТА) — метод является привлекательным, неинвазивным, позволяет избежать аллергических рисков и нефротоксичности, связанных с применением йодконтрастного препарата [4]. Диагностическая МРТА обладает чувствительностью и специфичностью 0,95 и 1,00 соответственно, позволяет диагностировать стеноз или окклюзии чревного ствола, верхней брыжеечной артерии [45]. Однако данный метод подходит для идентификации более дистально расположенных окклюзий и не имеет пространственного разрешения, как КТА [31]. В случае получения в будущем пространственного разрешения МРТА может стать методом выбора в диагностике ОНМК.
Больные с ОНМК требуют агрессивной реанимации и гидратации, кроме того, коррекции метаболического ацидоза и электролитного дисбаланса, назначения антибиотиков от грамотрицательных и анаэробных бактерий [5]. Декомпрессия через назогастральный зонд имеет важное значение, необходимо прекращать прием препаратов, вызывающих чревную вазоконстрикцию (вазопрессин, дигоксин).
Традиционным лечением ОНМК служила хирургическая реваскуляризация после лапаротомии для оценки жизнеспособности кишечника и резекции некротических участков. Первые задачи после лапаротомии — определение или подтверждение причины и степени окклюзии верхней брыжеечной артерии, оценка жизнеспособности кишечника [21, 22, 46]. Хирургическое лечение ОНМК включает эмболэктомию из брыжеечных артерий, шунтирование верхней брыжеечной артерии, помимо резекции некротизированных сегментов кишечника. Первая в мире открытая эмболэктомия из верхней брыжеечной артерии была выполнена в 1950 г. А. Klass [47], тромбэктомия — в 1958 г. R. Shaw и E. Maynard [48], в нашей стране тромбэктомия впервые выполнена в 1961 г. А.С. Любским [49].
Чрескожные катетерные эндоваскулярные вмешательства могут использоваться при инвазивной ангиографии [1, 2, 50, 51]. Успех стратегии эндоваскулярных вмешательств при лечении ОНМК в конечном счете зависит от своевременности диагностики и раннего начала терапии. В небольшой серии исследований показано успешное применение селективной фибринолитической терапии при тромботической окклюзии [52]. Недостатком селективного катетерного фибринолизиса является то, что реперфузия может занять несколько часов, причинив потенциальный ущерб жизнеспособности кишечника или привести к усилению ишемии или инфаркту. Таким образом, эти пациенты требуют пристального наблюдения.
Должен ли каждый больной с ОНМК пройти лапароскопическое исследование или выполнять экслоративную лапаротомию для исключения инфаркта кишечника, остается спорным вопросом. Многие исследователи выступают за использование обычных хирургических методов исследования для оценки жизнеспособности кишечника и резекцию его некротических участков. Другие полагают, что пациенты, которые подвергались успешным эндоваскулярным вмешательствам, могут контролироваться путем лапароскопической оценки жизнеспособности кишечника или другими нехирургическими методами исследования [52]. Условиями для проведения эндоваскулярного вмешательства в бассейне верхней брыжеечной артерии при ОНМК являются: отсутствие перитонеальной симптоматики; отсутствие выраженного пневматоза кишечника на обзорной рентгенограмме; отсутствие свободного газа в венозной системе брыжейки кишечника и стенке кишки по данным нативной КТ как признака некротического поражения тонкой и/или толстой кишки [50]. Применение эндоваскулярных вмешательств позволяет уменьшить объем резекции (52 см против 160 см) при традиционном лечении, снижает частоту осложнений, улучшает результаты лечения [53]. Современные методы эндоваскулярной хирургии включают механическую реканализацию, селективный тромболизис, баллонную ангиопластику, аспирационную и реолитическую тромбэктомию, антеградное стентирование [1].
Гибридные вмешательства (комбинация открытой и эндоваскулярной операций) более предпочтительны ввиду меньшей травматичности по сравнению с открытыми реконструкциями артерий, а также возможности визуализировать просвет брыжеечных артерий и проводить дополнительные эндоваскулярные вмешательства. Тактическими приемами гибридной техники являются антеградная и ретроградная реканализация и стентирование пораженных сегментов верхней брыжеечной артерии после лапаротомии [54].
В заключение следует отметить, что ОНМК остается тяжелой, поздно диагностируемой абдоминальной патологией, вследствие чего результаты лечения оказываются неудовлетворительными. Прогресс в лечении ОНМК можно связать с разработкой более эффективных методов раннего его выявления, применения эндоваскулярных и гибридных оперативных вмешательств.

Острая брыжеечная ишемия обычно определяется как группа заболеваний, характеризующихся нарушением кровоснабжения в различных участках тонкой кишки, что приводит к ишемии и вторичным некротическим изменениям в ее стенке. Вопреки низкой заболеваемости — 0,09–0,2% общего числа острых хирургических заболеваний брюшной полости, представленная патология сопровождается чрезвычайно высокой летальностью (55–80%). Полиморфная боль в животе, характерная для заболевания, имеет разнообразную причину и не всегда наталкивает на мысль о катастрофе в брюшной полости специфического происхождения. Тогда как своевременная диагностика и неотложное хирургическое вмешательство являются краеугольными камнями эффективного лечения и снижения высокой летальности. К сожалению, до настоящего времени не было выработано каких-либо рекомендаций по лечению при данной патологии, основанных на достоверной доказательной базе. Все они грешили субъективизмом и индивидуальным взглядом в пользу той или иной методики и не могли быть унифицированы. Появление новых эндоваскулярных методов лечения и диагностики параллельно с развитием новых методик визуализации значительно расширило лечебные возможности врачей. Таким образом, подготовленные согласительной комиссией рекомендации Всемирного общества неотложной хирургии по диагностике и лечению мезентериальной ишемии под руководством профессора Бала Миклоша, Иерусалим, Израиль (Acute Care Surgery and Trauma Unit, General Surgery Department, Hadassah — Hebrew University Medical Center, Jerusalem, Israel) стали первым унифицированным документом, регламентирующим оказание помощи при данном заболевании. Рекомендации опубликованы в Международном журнале по неотложной хирургии (World Journal of Emergency Surgery) в августе 2017 г. Как считают авторы, данные рекомендации должны способствовать не только унификации и стандартизации помощи больным при острой мезентериальной ишемии, но значительно снизить летальность при терапии за счет применения научно обоснованных и эффективных методов диагностики и лечения.
Особенности мезентериального кровоснабжения
Кровоснабжение кишечника осуществляется из трех источников — чревный ствол, верхняя (ВБА) и нижняя брыжеечная артерии. Развитая сеть межсосудистых анастомозов между ветвями этих артерий обеспечивает возможность коллатерального кровообращения. Чревный ствол и ВБА являются основным источником кровоснабжения тонкого кишечника и проксимального участка толстого кишечника. Две трети толстого кишечника и прямая кишка кровоснабжаются из системы нижней брыжеечной артерии. В нормальных физиологических условиях кровоток по мезентериальным сосудам составляет 15–35% сердечного выброса и зависит от стадии пищеварения. Но при этом степень экстракции кислорода кишечной стенкой невысока и зависит от степени кислородной емкости и скорости кровотока в портальной вене, что способствует устойчивости кишечника к гипоксии. Стойкая гипоксия кишечника, таким образом, наступает при снижении его кровоснабжения на более чем 50%. Кроме того, наличие системы ауторегуляции кровоснабжения за счет вазодилатации позволяет увеличить скорость кровотока в кишечной стенке и повысить экстракцию кислорода, что способствует улучшению оксигенации кишечной стенки в неблагоприятных условиях. Экспериментально было показано, что мезентериальная ишемия развивается при снижении среднего артериального давления ≤45 мм рт. ст. и обеспечивает условия компенсаторного кровотока при его 75% снижении в течении 12 ч без риска развития необратимых изменений в стенке кишечника. Рекомендации Всемирного общества неотложной хирургии (2017) по неотложной хирургии при острой мезентериальной ишемии представлены в табл. 1.
Таблица 1. Острая мезентериальная ишемия: рекомендации по неотложной хирургии Всемирного общества неотложной хирургии, 2017 г.
| Уровень и степень доказательности | Рекомендация |
|---|---|
| Ключом ранней диагностики является высокий уровень клинически подозреваемого острого нарушения мезентериального кровообращения | |
| 1B | Выраженную боль в животе, подтвержденную при физикальном обследовании, необходимо рассматривать как подозрение на острую мезентериальную ишемию до тех пор, пока сомнения не будут окончательно опровергнуты. Наиболее частыми клиническими симптомами являются резкая боль в животе — 95%, тошнота — 45%, рвота — 35%, диарея и примесь крови в стуле — 16%. При запоздалом (более 12 ч) обращении и признаках перитонита у половины пациентов развивается тяжелое состояние с явлениями септического шока |
| Клиническая картина острой мезентериальной ишемии включает несколько этиологических факторов, которые необходимо учитывать: артериальную брыжеечную эмболию, артериальный брыжеечный тромбоз, вазоспастическую форму артериальной брыжеечной ишемии и острый венозный мезентериальный тромбоз | |
| 1B | Необходим тщательный анализ анамнестических данных для определения формы острой мезентериальной ишемии, что может повлиять на последующую лечебную тактику. Пациенты с брыжеечным артериальным тромбозом часто имею в анамнезе указание на постпрандиальную боль в животе, прогрессирующее уменьшение массы тела, реваскуляризацию мезентериального кровотока в анамнезе. Для неокклюзивной мезентериальной ишемии характерна диффузная разлитая боль в области живота, чаще связанная с нарушением сердечной деятельности. Острый мезентериальный венозный тромбоз сопровождается тошнотой, рвотой, диареей и спазматическими проявлениями в животе. Желудочно-кишечные кровотечения отмечают у 10%. |
Повышенный уровень лактата может быть обусловлен обезвоживанием или нарушением питьевого режима и не может служить абсолютным подтверждением развития ишемии кишечника без соответствующего клинического проявления. Но повышенная концентрация лактата в сыворотке крови >2 ммоль/л подтверждает развитие необратимой ишемии кишечника при подтвержденном диагнозе острой мезентериальной ишемии. Следует подчеркнуть, что наличие лактоацидоза в сочетании с болью в животе при отсутствии клиники перитонита должно быть поводом для выполнения раннего КT-обследования.
Мультидетекторная спиральная КТ является золотым стандартом ранней диагностики мезентериальной ишемии, имея чувствительность 93%, специфичность 97,9%, положительные и отрицательные прогностические значения 100 и 94% соответственно.
Она незаменима для подтверждения необратимых изменений в кишечнике при состоявшейся ишемии (дилатация и утолщение кишечной стенки, уменьшение или отсутствие висцерального усиления, пневматоз кишечника и наличие газа в воротной вене, наличие свободного газа в брюшной полости при перфорации кишечной стенки). 3D-реконструкция дает необходимую анатомическую детализированную информацию.
Комплексная двухфазная КT включает следующие важные шаги:
— выявление кальциноза сосудистой стенки, мелкодисперсных внутрисосудистых тромботических масс и интрамуральных кровоизлияний в стенку тонкой кишки;
— в артериальную и венозную фазы определяются тромботические массы в брыжеечных артериях и венах, аномальное усиление стенки кишечника и наличие эмболии или инфаркта других органов брюшной полости;
— многоплановая реконструкция используется для оценки анатомии отхождения брыжеечных артерий.
У пациентов, перенесших сердечно-легочную реанимацию, у которых развивается бактериемия и диарея, следует заподозрить наличие мезентериальной ишемии неокклюзивного генеза, особенно при наличии в стуле кала с малиновым окрашиванием.
Гипоперфузия желудочно-кишечного тракта часто развивается у пациентов, находящихся в критическом состоянии на ранних стадиях, а также после больших операций и обширных травм. Эта относительная брыжеечная гипоперфузия часто усугубляется малой объемной скоростью перфузии и гиповолемией.
Необходимо проводить гемодинамический мониторинг и электролитный контроль для предупреждения развития гиперкалиемии.
Вазопрессоры использовать с осторожностью и только для предупреждения перегрузки жидкостью и развития компартмент-синдрома.
Цель хирургического вмешательства при острой мезентериальной ишемии:
— восстановление кровоснабжения ишемизированного участка кишки;
— удаление всех нежизнеспособных сегментов кишечника;
— сохранение жизнеспособности оставшейся кишки.
Для определения состояния кровотока по мезентериальным артериям и в стенке кишечника необходимо проведение допплеровской флоуметрии или интраоперационной артериографии при наличии гибридной операционной.
Восстановление кровотока по ВБА при тромбоэмболической окклюзии предполагает проведение тромбэктомии с восстановлением стенки заплатой либо прямого обходного аутовенозного шунтирования.
Вазоспастическая форма ишемии брыжейки и венозный тромбоз не требуют проведения сосудистого вмешательства.
В случае развития перитонита показано экстренное оперативное вмешательство.
Во время оперативного вмешательства необходимо радикально устранить только явно некротизированные и нежизнеспособные участки кишечника и участки с перфорацией.
Патофизиология и эпидемиология
Острая мезентериальная артериальная эмболия
Примерно 50% всех случаев острой мезентериальной ишемии обусловлены эмболией брыжеечных артерий. Ее источником могут быть левые отделы сердца, особенно при нарушениях сердечного ритма, резко сниженной насосной функции левого желудочка и глобальном снижении сократимости, наличии искусственных клапанов сердца и клапанном эндокардите. В редких случаях эмболы могут формироваться на изъязвленных бляшках аорты при ее атеросклеротическом поражении. Фиксация эмболов происходит, как правило, в местах физиологических сужений. Наиболее уязвимой для эмболических отсевов является ВБА из-за ее относительно большого диаметра и малого угла отхождения от аорты. В большинстве случаев эмболы в ВБА располагаются на расстоянии 3–10 см от ее устья. Более чем в 20% случаев эмболия ВБА сопровождается одновременной эмболией других артерий — почечной или селезеночной. Изменения в этих органах при компьютерной томографии (КT) косвенно могут указывать на наличие проксимальной эмболии.
Острый мезентериальный артериальный тромбоз
Тромбоз ВБА в приблизительно 25% случаев обусловлен атеросклерозом артерий и наличием хронических атеросклеротических отложений в ее стенке, способствующих ее сужению. У многих из этих пациентов имеются расстройства, подтверждающие наличие хронической мезентериальной ишемии, включая боль, возникающую после приема пищи — постпрандиальную боль, потерю массы тела, страх приема пищи, что важно учитывать при установлении диагноза или подозрении на развитие острой ишемии кишечника. Тромбоз, как правило, развивается на фоне атеросклеротического поражения мезентериальных артерий и имеет непрерывное развитие с постепенным сужением ВБА. Хроническая ишемия кишечника способствует развитию компенсаторного коллатерального кровотока. Поэтому клиника симптоматического тромбоза ВБА, как правило, развивается при нарушении кровотока в чревном стволе. Кроме атеросклероза тромбоз ВБА может возникать в результате системного васкулита, при остром расслоении стенки брыжеечной артерии или аневризме брюшной аорты грибковой этиологии. Вовлечение в процесс а. ileocolicа способствует развитию некроза проксимальной части ободочной кишки.
Острая мезентериальная ишемия на фоне вазоспазма
Нетромботическая мезентериальная ишемия встречается примерно в 20% случаев и, как правило, является следствием вазоконстрикции ВБА с явлениями резкого снижения объемного кровотока по мезентериальным артериям. Как правило, в процесс вовлекается не только ВБА, но и ветвь а. ileocolicа, приводя к ишемии проксимального участка ободочной кишки. Мезентериальная ишемия на фоне вазоконстрикции, как правило, развивается у пациентов с тяжелыми соматическими заболеваниями, при сердечной недостаточности на фоне сепсиса. Часто ее развитие провоцирует гиповолемия и использование сосудосуживающих лекарственных препаратов.
Мезентериальный венозный тромбоз
Мезентериальный венозный тромбоз развивается менее чем в 10% случаев. В большинстве случаев этиология венозного тромбоза объясняется триадой Вирхова — снижение скорости кровотока, гиперкоагуляция и воспаление сосудистой стенки. Но примерно у 20% он является идиопатическим. Гиперкоагуляция может быть обусловлена наследственными заболеваниями, таким как мутация фактора V, мутация гена протромбина, дефицит белка C и S, дефицит антитромбина III, и антифосфолипидным синдромом. Кроме того, доказана связь повышенного риска развития мезентериального венозного тромбоза при выявлении повышенной устойчивости к тканевому активатору плазминогена при проведении фибринолиз-теста. Повышенный риск развития тромбоза возможен при злокачественных новообразованиях, заболеваниях крови и приеме оральных контрацептивов. Состояния, которые могут существенно опосредованно повысить риск мезентериального венозного тромбоза путем изменения кровотока, включают портальную гипертензию, острый панкреатит, воспалительные заболевания кишечника, сепсис и травму. Развивающийся в этих ситуациях отек кишечной стенки и повышение сосудистого сопротивления как вторичная причина по отношению к тромбозу усугубляют ишемию кишечной стенки.
Факторы риска, обусловливающие вероятность развития нарушения мезентериального кровообращения по этиологическому принципу, приведены в табл. 2.
Таблица 2. Состояния, повышающие риск развития нарушения мезентериального кровообращения
Читайте также:

