Анемический синдром реферат кратко и понятно
Обновлено: 04.07.2024
Информация, представленная на странице, не должна быть использована для самолечения или самодиагностики. При подозрении на наличие заболевания, необходимо обратиться за помощью к квалифицированному специалисту. Провести диагностику и назначить лечение может только ваш лечащий врач.
Содержание статьи:
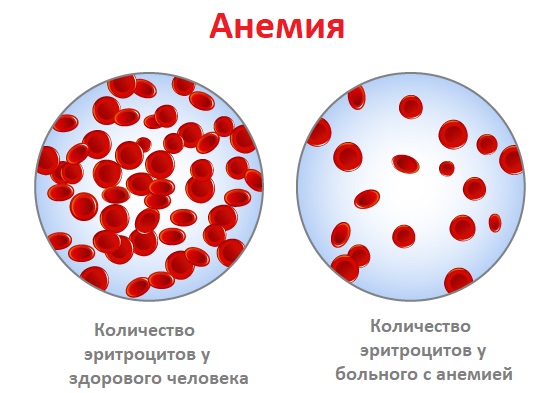
Анемия (малокровие) – патология, для которой свойственно снижение уровня гемоглобина в крови, количества эритроцитов (красных кровяных телец), изменение их формы. Пониженный гемоглобин – обязательный признак анемии, изменение числа эритроцитов и их деформация присутствуют не всегда.
Анемия – распространенное заболевание. Ему подвержены более четверти всего населения мира – 27,9 % или 1,9 млрд человек. Ежегодный темп прироста анемий составляет 6,6 %. Чаще всего патология встречается у детей дошкольного возраста (47,4 % от всех случаев), женщин, особенно во время беременности, реже – у мужчин (12,7 %). В России анемия ежегодно диагностируется у более чем 1,5 млн пациентов.
Причины возникновения патологии
Железодефицитная анемия (ЖДА), самая частая форма малокровия, обусловлена тремя факторами: недостаток поступления железа, его усиленная потеря, высокая потребность в этом микроэлементе, не восполняемая в достаточной мере.
Одна из причин недостатка поступления железа – неполноценное питание (недоедание, однообразное меню с малым количеством белка и красного мяса, вегетарианство, искусственное вскармливание). Кроме того, поступлению необходимого объема микроэлемента препятствует нарушение его усвояемости. Это происходит из-за различных патологий, мешающих ионизации железа в желудке (гастрит с атрофией слизистой, резекция желудка, гипо- и авитаминоз витамина C), и затрудняющих его всасывание в кишечнике (дуоденит, энтерит, колит).
Потерю железа сверх нормы провоцируют кровотечения – из носа, десен, желудочно-кишечные, геморроидальные, маточные, почечные, геморрагические диатезы, частое донорство.
Гиперпотребность в железе вызывают физиологические и патологические состояния. К физиологическим относятся интенсивный рост и половое созревание, беременность и кормление грудью, профессиональные тренировки, тяжелые физические нагрузки. К патологическим – глистные инвазии.
Дефицит железа бывает связан с некоторыми инфекционными болезнями, также нехватка этого элемента фиксируется у детей, рожденных матерями с анемией.
Группы риска
Исходя из причин, можно выделить категории людей, подверженных развитию малокровия:
- пациенты с пищевыми расстройствами, вегетарианцы, соблюдающие строгую диету;
- беременные и кормящие матери, женщины с обильными менструациями;
- дети и подростки, особенно не получающие полноценного питания;
- люди пожилого возраста;
- профессиональные спортсмены;
- доноры крови;
- люди с различными хроническими патологиями.
Патогенез болезни
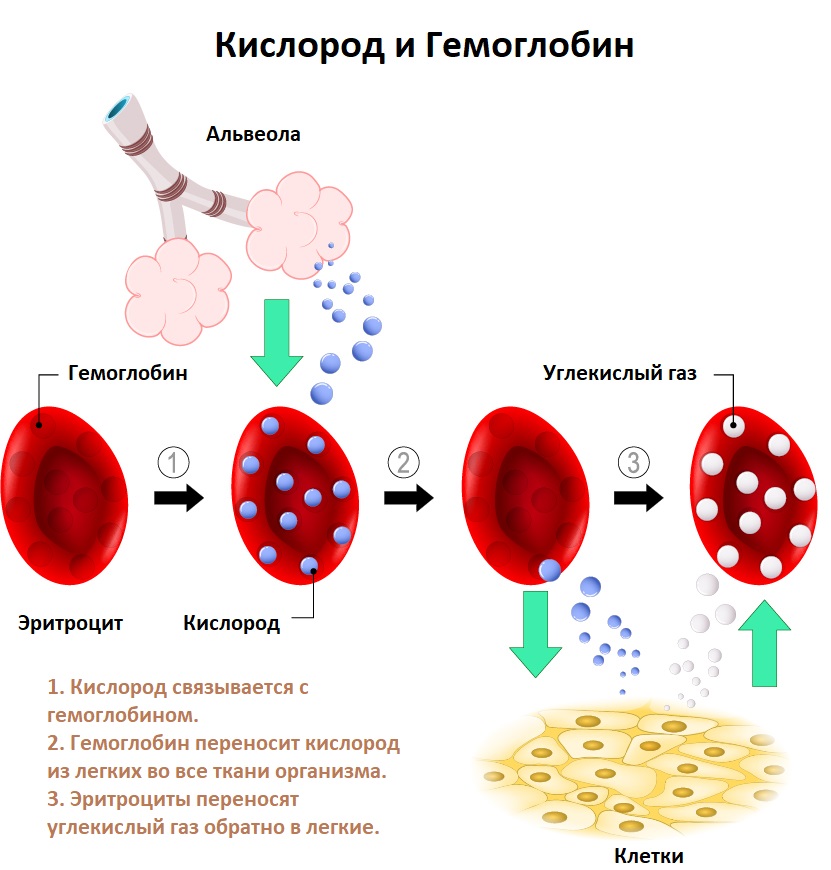
Ведущее звено патогенеза ЖДА – нарушение синтеза гемоглобина вследствие снижения запасов железа, которое крайне необходимо для нормальной жизнедеятельности организма. Железо присутствует в составе гемоглобина и миоглобина, отвечает за транспортировку кислорода, различные биохимические процессы.
Железо всасывается в кровь из желудочно-кишечного тракта (ЖКТ), соединяется с трансферрином и либо накапливается в печени в составе белка ферритина, либо направляется в красный костный мозг, где с его участием идет синтез гемоглобина. Некоторая часть микроэлемента в составе трансферрина принимает участие в окислительно-восстановительных реакциях в тканях.
Нарушения на любом из описанных этапов затрудняют или делают невозможным процессы всасывания железа, его соединения с трансферрином, способствуют возникновению анемии. Всасыванию микроэлемента препятствуют заболевания ЖКТ, отсутствие части желудка или кишечника, гиповитаминоз витамина C, целиакия. При затруднении связывания железа с трансферрином оно не попадает в органы-депо (печень, селезенка) и красный костный мозг, как результат – нарушается синтез гемоглобина. Нехватка железа, требующегося для биохимических реакций, приводит к дестабилизации выработки некоторых гормонов, уменьшению адаптационных возможностей организма, снижению иммунитета Источник:
Седунова Е.Г. Структура заболеваемости анемиями различного генеза / Е.Г. Седунова, И.Р. Балданова // Вестник Бурятского университета. - 2010. - № 12. - С. 151-153 .
Симптомы анемии
Симптоматика любых анемий в первую очередь обусловлена кислородным голоданием тканей. Поэтому независимо от причин малокровия, признаки разных видов анемии будут схожими, а их интенсивность – варьироваться в зависимости от степени тяжести болезни.
Общие признаки:
- слабость, сонливость;
- головокружение, шум в ушах, мушки перед глазами;
- увеличение частоты сердечных сокращений, одышка;
- сухая и бледная кожа, иногда с желтоватым оттенком;
- голубоватый цвет склер;
- ломкие и слоящиеся ногти, их деформация – ногти становятся плоскими или вогнутыми, на них появляются поперечные борозды;
- тусклые, секущиеся, выпадающие больше нормы волосы;
- жжение языка, заеды – мелкие трещины в углах рта, небольшие изъязвления в ротовой полости, затруднения глотания;
- извращенные вкусовые и обонятельные пристрастия;
- потеря аппетита.
Зачастую начальные симптомы заболевания при легкой стадии анемии пациенты списывают на усталость, недосып, тяжелый рабочий график. Человека должны насторожить такие признаки как слабость при незначительной нагрузке, чувство разбитости, сонливость даже после полноценного ночного сна. В этом случае следует сдать общий анализ крови, чтобы не пропустить начало заболевания.
При острых и тяжелых анемиях возможно резкое ухудшение самочувствия – тошнота, рвота, обмороки, вплоть до гипоксической комы.
Классификация
Разновидности анемии в зависимости от причины:
- Железодефицитная – диагностируется в 90 % всех случаев. В анализе крови наблюдается снижение числа эритроцитов. Транспортировка кислорода из легких затрудняется, развивается кислородное голодание органов и тканей.
- Пернициозная анемия – возникает в результате нехватки витамина B12, обычно в результате наличия воспалительного очага или хронического заболевания кишечника.
- Фолиеводефицитная – следствие нехватки в организме фолиевой кислоты. Часто наблюдается у беременных женщин, недоношенных детей, при алкоголизме, длительном приеме противосудорожных средств.
- Гемолитическая анемия характеризуется разрушением эритроцитов и снижением срока их жизни. В анализе крови число эритроцитов может превышать норму – так организм компенсирует невозможность красных кровяных телец выполнять возложенную на них функцию.
- Постгеморрагическая – результат острой или хронической кровопотери.
- Апластическая анемия – недостаток выработки эритроцитов костным мозгом. Может быть результатом длительного приема цитостатиков, радиоактивного облучения при терапии онкологических заболеваний.
- Серповидноклеточная – изменение нормальной формы эритроцитов, которые принимают очертания полумесяца. Эритроциты перестают выполнять свои функции и могут закупоривать мелкие кровеносные сосуды, что чревато дополнительными осложнениями. Заболевание имеет генетическую предрасположенность, распространено на африканском континенте.
- Сидеробластная анемия – приобретенная или наследственная патология, характеризующаяся гипохромией эритроцитов при высоком содержании железа в сыворотке крови и его отложении в тканях Источник:
Полуэктова О.Ю. Важнейшие анемии в общей врачебной практике. Гипорегенеративные анемии / О.Ю. Полуэктова [и др.] // Земский врач. - 2011. - № 4 (8). - С. 9-13. .
По качественным и количественным показателям:
- микроцитарная гипохромная – размер эритроцитов меньше нормы, они не могут транспортировать нужное количество гемоглобина;
- макроцитарная гиперхромная – крупные эритроциты транспортируют достаточное количество гемоглобина, но цикл их жизни короче обычного;
- нормоцитарная нормохромная – эритроциты обычной формы и размера, но их количество в крови снижено.
В этой классификации применяется величина цветового показателя крови (ЦП), норма которого равна 0,86-1,1. При нормохромной анемии ЦП остается в допустимых пределах, при гипохромной – опускается ниже 0,86, при гиперхромной – поднимается выше 1,1.
По течению (для геморрагических анемий):
- Острая – результат массивной кровопотери при травмах кровотечениях. Требует экстренной медицинской помощи, иногда – переливания донорской крови.
- Хроническая – возникает вследствие незначительных повторяющихся кровопотерь (при патологиях ЖКТ, доброкачественных и злокачественных опухолях, циррозе печени, геморрое).
Стадии анемии
ЖДА развивается, последовательно проходя три этапа:
- Прелатентный дефицит железа. Симптоматика отсутствует, показатели общего анализа крови в норме. Снижаются запасы железа в печени и костном мозге, уровень ферритина.
- Латентный (скрытый) дефицит железа. Запасы железа истощаются, уровень гемоглобина пока еще в норме. Возникают первые, слабо выраженные симптомы заболевания, – слабость, утомляемость, бледность и сухость кожи, одышка при физической нагрузке. В анализах крови количество гемоглобина и эритроцитов в норме, снижается ферритин, сывороточное железо, повышается общая железосвязывающая способность сыворотки крови.
- Непосредственно железодефицитная анемия. Присутствуют характерные симптомы и изменения в анализах крови. Уровень гемоглобина и эритроцитов, ферритина, сывороточного железа снижается, изменяется размер и форма эритроцитов.
Для ЖДА выделяют три степени тяжести, каждой из которых соответствует определенный уровень гемоглобина. В норме показатель составляет от 110 до 130 г/л, нижняя граница допустима для детей и беременных женщин, верхняя – для мужчин.
Диагностические мероприятия
Основа диагностики анемии – общий (ОАК) и биохимический анализ крови.
ОАК позволяет оценить уровень гемоглобина и эритроцитов, средний объем эритроцитов, среднее содержание и концентрацию гемоглобина в эритроцитах, ЦП, скорость оседания эритроцитов, лейкоцитарную формулу Источник:
Байрамалибейли И.Э. Алгоритм диагностики анемий / И.Э. Байрамалибейли [и др.] // Вестник Российского университета дружбы народов. Серия: Медицина. - 2006. - № 1 (33). - С. 12-20. .
По биохимическому анализу оцениваются уровень сывороточного железа и ферритина, увеличение общей железосвязывающей способности сыворотки, коэффициент насыщения трансферрина железом.
Дополнительно к анализам показаны фиброгастроскопия, колоноскопия, ЭКГ, УЗИ сердца для выявления причины, вызвавшей ЖДА, и контроля за состоянием пациента в целом. Больному также могут потребоваться консультации врачей различной специализации либо гематолога, если не удастся выявить причину анемии Источник:
Мещерякова Л.М., Левина А.А., Цыбульская М.М., Соколова Т.В. Лабораторные возможности дифференциальной диагностики анемий. Онкогематология, 2015. с. 46-50 .
Лечение анемии
Важный этап в лечении – устранение факторов, вызывающих недостаток железа. Одновременно больному назначается терапия для нормализации уровня этого микроэлемента. Диета – важная составляющая процесса лечения, но она является вспомогательным элементом, вылечить анемию без применения лекарств невозможно.
В основе лечения – препараты железа. Предпочтение отдается пероральному приему лекарств, инъекционно они вводятся только при тяжелом течении анемии, необходимости быстрого восстановления уровня железа, непереносимости или неэффективности пероральных препаратов, заболеваниях органов пищеварения, препятствующих всасыванию лекарственных средств.
Помимо препаратов железа рекомендованы витамины (B12, C), фолиевая кислота.
Для лечения отдельных видов анемий применяются специальные методы. При постгеморрагической анемии требуется восполнение объема циркулирующей крови, в том числе с помощью гемотрансфузий. При апластической анемии показаны гемотрансфузии, гормональная терапия и другие мероприятия, вплоть до трансплантации костного мозга.
Лечение железодефицитной анемии продолжается от 3 до 6 месяцев. Его нельзя прекращать сразу после восстановления уровня гемоглобина, в организме должен сформироваться запас железа.
Осложнения болезни
Последствия анемии возникают при ее долгом течении и отсутствии терапии. Дефицит железа в организме вызывает ослабление иммунитета, уменьшается сопротивляемость простудным, вирусным, бактериальным заболеваниям. Возможны осложнения со стороны нервной системы, нарушения функций печени, сбои менструального цикла. Из-за постоянной гипоксии возникают нарушения функций сердечно-сосудистой системы – дистрофия миокарда, застойные явления, развивается сердечно-сосудистая недостаточность. Наиболее тяжелым осложнением анемии является гипоксическая кома.
Прогноз и профилактика анемии
При своевременной диагностике и адекватной терапии прогноз благоприятный. Как правило заболевание лечится амбулаторно, госпитализация пациента не требуется.
Для профилактики ЖДА необходимо полноценное питание с достаточным поступлением белка, ежегодная сдача общего анализа крови, контроль за состоянием здоровья в целом и устранение заболеваний, которые могут стать источником пусть даже небольшой хронической кровопотери. Люди из групп риска по назначению врача могут ежегодно принимать курс препаратов железа, однако делать это самостоятельно недопустимо, так как бесконтрольный прием этих лекарств может вызвать тяжелые побочные эффекты.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Анемии: причины появления, симптомы, диагностика и способы лечения.
Определение
Анемия – это уменьшение содержания гемоглобина и/или снижение количества эритроцитов в единице объема крови, приводящее к снижению снабжения тканей кислородом.
Анемия встречается при ряде заболеваний (язвы и полипы желудочно-кишечного тракта, хроническая болезнь почек, онкологические, инфекционные заболевания, глистные инвазии и др). Чем ниже уровень гемоглобина, тем тяжелее протекает анемия.
Причины появления анемии
Анемия может возникнуть в результате нарушения образования эритроцитов, повышенного их разрушения или потери эритроцитов с кровью.
Статистика утверждает, что самой распространенной является анемия, возникшая после кровопотери (острой или хронической). Острой считается кровопотеря с объемом крови более 500-700 мл (у взрослых), которая происходит в течение короткого промежутка времени. Потеря крови может быть видимой (кровотечение из ран, кровавая рвота, маточное, носовое кровотечения) и первоначально скрытой (кровотечения в кишечник, в полость живота и/или плевры, большие гематомы).
Хронические кровопотери развиваются в результате незначительных, но длительных потерь крови (обильные и длительные менструации, язва желудка, рак, геморрой, проведение процедур гемодиализа и др.). С течением времени незначительные кровопотери приводят к истощению запасов железа в организме, когда количество теряемого организмом железа превышает его поступление с пищей. В результате дефицита железа нарушается синтез гемоглобина.
Дефицит железа может возникнуть из-за снижения всасывания железа в результате различных заболеваний двенадцатиперстной кишки и начальных отделов тонкой кишки (энтеритов, опухолей, состояний после оперативных вмешательств на данном участке кишечника). Состояния, приводящие к снижению уровня белков крови, являющихся переносчиками железа (нефротический синдром, нарушение белково-синтетической функции печени, синдром нарушенного всасывания, алиментарная недостаточность), также могут привести к его снижению и, как следствие, к анемии.
Железодефицитные анемии, связанные с исходно недостаточным уровнем железа (недостаток железа у матери в период беременности), наблюдаются у новорожденных и детей младшего возраста.
Анемии вследствие нарушенного кроветворения возникают:
- при недостаточном поступлении в организм или нарушении всасывания в желудочно-кишечном тракте компонентов, необходимых для образования эритроцитов (витамина В6, витамина В12, фолиевой кислоты и др.);
- поражении клеток костного мозга - предшественников эритроцитов токсическими веществами, ионизирующей радиацией;
- образовании вторичных очагов опухолевых клеток в костном мозге (метастазировании);
- нарушении синтеза небелковой части гемоглобина (гема) и накоплении его токсичных продуктов;
- нарушении регуляции образования эритроцитов (уменьшении продукции гормона, стимулирующего рост и размножение эритроцитов (эритропоэтин) или воздействии ингибиторов).
Развитие наследственных гемолитических анемий связано с генетическими дефектами (нарушением активности ферментов эритроцитов, нарушением структуры или синтеза гемоглобина, дефектами мембран эритроцитов).
Приобретенные гемолитические анемии могут быть обусловлены разрушением эритроцитов в результате воздействия на них антител, механических повреждений оболочки эритроцитов, химических повреждений эритроцитов, недостатка витаминов, разрушения эритроцитов паразитами.
Классификация анемий
1. Анемии, связанные с кровопотерей:
- анемии, связанные с нарушением образования гемоглобина;
- анемии, связанные с нарушением синтеза ДНК и РНК;
- анемии, связанные с нарушением процессов деления эритроцитов;
- анемии, связанные с угнетением пролиферации (размножения) клеток костного мозга.
- наследственные гемолитические анемии;
- приобретенные гемолитические анемии.
Существуют общие (неспецифические) проявления анемии и признаки, которые специфичны для определенного вида анемий.
Отсутствие этих признаков не исключает наличие анемии, поскольку при легкой и среднетяжелой форме заболевания, а также его медленном развитии клиническая картина может быть смазанной.
Клинические проявления недостатка железа в организме: сухость кожи, нарушение целостности эпидермиса, ломкость ногтей, волос, изъязвления и трещины в углах рта, мышечная слабость. Может наблюдаться чувство жжения языка, извращение вкуса в виде неукротимого желания есть мел, зубную пасту, землю, сырую крупу, сырое мясо, а также пристрастие к некоторым запахам (ацетона, бензина).
Дефицит витамина В12 также может проявляться поражением желудочно-кишечного тракта (атрофическим гастритом) и неврологической симптоматикой (парестезиями, нарушением чувствительности, онемением конечностей). При крайне тяжелом течении заболевания наблюдаются психические нарушения, бред, галлюцинации, приобретенное слабоумие и др.
Клиническая картина дефицита фолиевой кислоты очень похожа на дефицит витамина В12, но при фолиеводефицитных состояниях отсутствует неврологическая симптоматика и редко возникает воспаление языка. Дефицит фолиевой кислоты приводит к обострению шизофрении, учащению и утяжелению приступов эпилепсии.
Для гемолитических анемий характерны желтушность кожных покровов и слизистых, увеличение размера селезенки, склонность к образованию камней в желчных путях.
При массивном гемолизе эритроцитов (гемолитическом кризе) кроме анемии, желтухи и ухудшения общего состояния могут наблюдаться тошнота, рвота, расстройство сознания, судороги, развитие острой почечной и/или сердечно-сосудистой недостаточности.
При апластической анемии, которая возникает на фоне угнетения пролиферации клеток костного мозга, происходят кровоизлияния (преимущественно в области бедер, голеней, живота, в местах инъекций образуются гематомы). Часто диагностируются бронхиты, пневмонии.
Диагностика анемии
Анемия может возникать под влиянием самых разнообразных факторов. Чаще всего встречаются дефицитные анемии (железодефицитные, B12-дефицитные, фолиеводефицитные и др.).
Большую роль в выявлении причины анемии играют сведения, полученные при опросе пациента: возраст, наличие профессиональных вредностей, характер диеты, наличие сопутствующих заболеваний, прием лекарственных препаратов, информация о наследственности и др. Не менее важны данные осмотра: изменение цвета и состояния кожи; увеличение лимфатических узлов, печени, селезенки; наличие поражения нервной системы.
Первый этап диагностики анемии обычно включает следующие исследования:
-
клинический анализ крови: определение концентрации гемоглобина, количества эритроцитов, лейкоцитов, величины гематокрита и эритроцитарных индексов (MCV, RDW, MCH, MCHC), лейкоцитарной формулы и СОЭ (с микроскопией мазка крови при наличии патологических сдвигов);
Одно из основных лабораторных исследований для количественной и качественной оценки всех классов форменных элементов крови. Включает цитологическое исследование мазка крови для подсчета процентного содержания разновидностей лейкоцитов и определение скорости оседания эритроцитов.
Определение понятия и классификации анемии. Распространенность в мире, основные симптомы и причины возникновения заболевания. Общие принципы лечения и профилактики анемии. Особенности течения, терапии и профилактики заболевания у беременных и детей.
| Рубрика | Медицина |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 07.11.2016 |
| Размер файла | 27,1 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Государственное образовательное учреждение среднего профессионального образования
на тему: " Анемия, причины возникновения, лечение и профилактика"
Выполнила: Лоскутникова Ирина Сергеевна
Проверила: Котельникова Анастасия Анатольевна
1. ПОНЯТИЕ АНЕМИИ
2. КЛАССИФИКАЦИЯ АНЕМИИ
3. СИМТОМЫ АНЕМИИ
4. ЛЕЧЕНИЕ И ПРОФИЛАКТИКА АНЕМИИ
5. АНЕМИЯ У БЕРЕМЕННЫХ И ДЕТЕЙ
Во всем мире анемии подвержено 1,62 миллиарда человек, что соответствует 24,8% населения . Наибольшая распространенность отмечается у детей дошкольного возраста (47.4%), и наименьшая распространенность анемии отмечается у лиц мужского пола (12.7%). Однако, группой населения с наибольшим количеством лиц, подверженных анемии, является группа не беременных 468,4 миллиона( 41,8%)
Целью настоящего исследования является изучение анемии и причины её возникновения.
В соответствии с целью были поставлены следующие задачи:
· изучить симптомы анемии;
· изучить принципы лечения и профилактики анемии;
· изучить особенности анемии у разных групп населения;
Для достижения поставленной цели и решения поставленных задач в данной работе была использована научная и учебная литература, а так же информационные ресурсы сети Интернет.
1. ПОНЯТИЕ АНЕМИИ
Анемия (малокровие) - состояние, характеризующееся снижением содержания гемоглобина в единице объема крови, чаще при одновременном уменьшении количества эритроцитов.
Нормальные показатели эритропоэза: число эритроцитов у женщин 4,0-5,0•10^12/л, у мужчин 4,5-5,5•10^12/л, гемоглобин у женщин - 120-140 г/л, у мужчин - 130-160 г/л. Все анемии имеют вторичное происхождение, чаще наблюдаются у женщин и нередко связаны с мено- и метроррагией[2]
Основной задачей эритроцитов является перенос кислорода и углекислого газа. Эта функция становится недостаточной вследствие:
· уменьшения количества эритроцитов в крови;
· падения содержания гемоглобина;
· появление в крови незрелых или патологически измененных эритроцитов;
· наличие эритроцитов с наследственным дефектом;
· потери способности гемоглобина связывать кислород и другие.
Анемия возникает на почве:
· различных заболеваний и интоксикаций;
· недостатка факторов, участвующих в кроветворении;
· гипоплазии костного мозга;
· кровопотерь и т.д.
Истинную анемию следует отличать от гемодилюции при уменьшении отеков, введении большого количества растворов. В то же время анемия может маскироваться сгущением крови при обезвоживании организма. При анемии, как правило, наблюдаются не только количественные, но и качественные изменения эритроцитов, их величины (анизоцитоз), формы (пойкилоцитоз).
Анемия может быть как самостоятельным заболеванием, так и проявлением или осложнением других заболеваний (синдромом). Причины возникновения и механизм развития анемии различны, выявление их имеет решающее значение для выбора рационального лечения.
При анемии нарушается дыхательная функция крови - доставка кислорода к тканям. Потребность организма кислороде в какой-то степени компенсируется мобилизацией защитно-приспособителных реакций, которые обычно возникают при гипоксических состояниях. В случае прогрессирующей анемии наступает тяжелая кислородная недостаточность, которая может стать причиной смерти.
Для различных видов анемии характерно не только уменьшение количества эритроцитов, но и качественные изменения эритроцитов крови, степени их зрелости, размеров, формы, окраски, структуры и биохимических свойств.
2. КЛАССИФИКАЦИЯ АНЕМИИ
анемия терапия симптом профилактика
Существует несколько классификаций анемий, основанных на этиологических, патогенетических, гематологических признаках. Не все они имеют практическое значение в связи с тем, что анемия преимущественно может быть симптомом какого-то заболевания, а пато-генетические механизмы развития ее при различных заболеваниях разнообразны и часто сложны.
Для практических целей наиболее удобной является классификация анемий, построенная по патогенетическому принципу. Согласно этой классификации выделяют 3 основные группы анемий.
Патогенетическая классификация анемий
Анемии вследствие кровопотери:
· Острая постгеморрагическая анемия
· Хроническая постгеморрагическая анемия
Анемии, обусловленные недостаточностью эритропоэза:
1. Гипохромные анемии:
· Анемии, связанные с нарушением синтеза порфиринов
2. Нормохромные анемии:
· Анемии хронических заболеваний
· Анемия при хронической почечной недостаточности
· Анемии при опухолевых и метастатических поражениях костного мозга
3. Мегалобластные анемии:
· Анемии, обусловленные дефицитом витамина В12
Анемии вследствие усиленного разрушения эритроцитов (гемолитические анемии):
1. Анемии, обусловленные внеэритроцитарными факторами:
· Иммунные гемолитические анемии:
§ изоиммунные гемолитические анемии;
§ аутоиммунные гемолитические анемии
· Гемолитические анемии, обусловленные механическим повреждением эритроцитов
2. Анемии, обусловленные эритроцитарными факторами:
· Гемолитические анемии, связанные с нарушением структуры мембраны эритроцитов (эритроцитопатии - наследственные и приобретенные):
§ микросфероцитарная гемолитическая анемия;
§ овалоцитарная гемолитическая анемия;
§ стоматоцитарная гемолитическая анемия;
§ гемолитические анемии, обусловленные нарушением структуры липидов мембраны эритроцитов (акантоцитоз)
· Гемолитические анемии, обусловленные дефицитом ферментов эритроцитов (эритроцитарные энзимопатии):
§ гемолитические анемии, связанные с недостаточностью активности ферментов гликолиза;
§ гемолитические анемии, связанные с недостаточностью активности ферментов пентозофосфатного шунта;
§ гемолитические анемии, связанные с недостаточностью активности ферментов глютатионовой системы.
· Гемолитические анемии, связанные с нарушенным синтезом глобина (гемоглобинопатии):
§ гемолитические анемии, обусловленные носительством аномальных гемоглобинов (НbS, НbС, НbD, НbЕ и др.);
§ гемолитические анемии, обусловленные носительством аномальных нестабильных гемоглобинов
3. Гемолитическая анемия, обусловленная соматической мутацией клеток-предшественников миелопоэза:
· пароксизмальная ночная гемоглобинурия[3].
Классификация анемий по степени тяжести
Легкая - уровень гемоглобина выше 90 г/л;
Средней тяжести - гемоглобин в пределах 90 - 70 г/л;
Тяжелая - уровень гемоглобина менее 70 г/л.
3. СИМТОМЫ АНЕМИИ
Симптомы анемии формируются на фоне снижения гемоглобина. Норма этого вещества дискутабельна. Признаки малокровия прослеживаются у некоторых людей при показателе гемоглобина - 110 г/л.
У других пациентов клинических проявлений заболевания не прослеживаются при концентрации ниже 90 г/л. По классическим меркам анемическое состояние тяжелой степени наблюдается при уровне гемоглобина ниже 70 г/л.
Некоторые терапевты наблюдали идеальное состояние здоровья у пожилых пациентов при более низких цифрах данного показателя. Конечно, патологические симптомы заболевания на этом фоне проявляются, но они совместимы с жизнью.
Дискуссии на тему лабораторной нормы при малокровии продолжаются, но это не отменяет клинические проявления заболевания, требующие незамедлительного лечения.
Симптомы анемии отличаются на начальных и поздних стадиях. Прелатентная форма заболевания характеризуется следующими проявлениями:
· Ускорение частоты сокращений сердца;
Жалоб у людей на ранней (латентной) стадии недуга немного. Чаще всего преобладает 2-3 из вышеописанных маркеров анемического состояния.
Признаки анемии зависят от биохимических изменений организма. При патологии страдают не только эритроциты. Наблюдается разрушение депо железа - ферритина, повышается уровень транспортного белка - трансферрина, происходит деструкция миоглобина. Эти процессы влияют на проявления недуга.
Какие признаки железодефицитной анемии при тяжелом течении:
· Тахикардия - учащение сердцебиения;
· Головокружение и головная боль;
· Сухость языка и отечность;
· Извращение вкуса (употребление мела и извести).
Симптомы анемии различаются в зависимости от вида болезни. Существует несколько его вариантов:
4. ЛЕЧЕНИЕ И ПРОФИЛАКТИКА АНЕМИИ
Большинство больных с анемическим синдромом обследуются и лечатся в амбулаторно-поликлинических условиях участковыми врачами, в ряде случаев после консультации гематолога. Это больные с ЖДА и В12 - фолиеводефицитными анемиями. Больные с гемолитическими, апластическими и другими анемиями постоянно наблюдаются гематологами. Показания к госпитализации больных с анемиями - острая постгеморрагическая анемия; гемолитические и апластические анемии; прекоматозное и коматозное состояния при любом типе анемий; тяжелые степени анемий; уточнение причины анемии, если возможности поликлиники в этом отношении исчерпаны; безуспешная амбулаторная терапия, необходимость хирургического или интенсивного лечения заболеваний, являющихся причиной анемического синдрома (фибромиома матки, кровоточашая гастродуоденальная язва, геморрой, опухоль и др. )[5].
Железодефицитная анемия. Её лечение состоит из трех компонентов. Первый компонент - это выявление и, по возможности, устранение причины, которая вызвала анемию. Второй этап лечебного процесса - это организация адекватного питания. В рационе больного железодефицитной анемии должно быть повышено содержание белка до 140 - 150 грамм в сутки, в основном за счет животных продуктов, а содержание жира снижено до 70 - 80 грамм. Особое внимание нужно уделить на насыщенность пищи витаминами. Здесь целесообразно использовать народные средства, приведенные выше. Однако следует обратить внимание на то, что рациональная диета, способствуя выздоровлению и профилактике рецидивов заболевания, сама по себе не может компенсировать уже развившийся дефицит железа с клиническим проявлениями. Третий этап - терапия препаратами железа, которые применяют перорально (ировит, ферронат, ферретаб, ферроплекс и другие) и парентерально (феррум лек, венофер и другие).
Лекарственные средства, используемые при лечении анемии по назначению врача: препараты железа - Железа сульфат (Гемофер, Ферроградумент), Комбинированные препараты (Актиферрин, Гемоферпролонгатум, Ирадиан, Иррвит, Тардиферон, Феррол, Ферромед, Ферроплекс, Ферроцин, Феррум Лек, Хеферол)
Лечение В-12 дефицитной анемии. Здесь основной принцип - это заместительная терапия витамином В-12. Используют цианкобаламин (100, 200 и 500 мкг/мл), который вводят ежедневно. После курса лечения проводят курс закрепляющей терапии (в течение двух месяцев цианкобаламин вводят еженедельно, а затем в течение полугода 2 раза в месяц по 400-500 мкг. После этого рекомендованы ежегодные профилактические курсы по 400 микрограмм через день в течение 3 недель.
Лекарственные средства, используемые при лечении анемии по назначению врача: витаминные препараты - Витамин В12 (Гидроксикобаламин, Цианокобаламин)
Лечение фолиеводефицитной анемии. Используют фолиевую кислоту от 5 до 15 мг в сутки, вводят обычно перорально. Если она выявлена во время беременности, то назначают в такой же дозировке, а потом оставляют по 1 мг в сутки до конца беременности или грудного вскармливания ребенка.
Лекарственные средства, используемые при лечении анемии по назначению врача: Фолиевая кислота, Комбинированные средства с добавками железа и витамина В (Гино-Тардиферон, Мальтофер Фол, Ферретаб комп, Ферро-Фольгамма)
Геморрагическая анемия, при хронических кровотечениях, после ликвидации его, лечение такое же, как и у железодефицитной анемии. При острой кровопотере используют препараты крови или кровезамещающие растворы[6].
Первичная профилактика (то есть до возникновения заболевания).
· Прием препаратов железа особым группам людей с наиболее высоким риском развития железодефицитной анемии -- донорам.
· Сбалансированное и рациональное питание (употребление в пищу продуктов с высоким содержанием клетчатки (овощи, фрукты, зелень), отказ от консервированной, жареной, острой, горячей пищи), употребление в пищу продуктов животного происхождения (яиц, икры, мяса, рыбы), а при вегетарианстве (отказе от использования в пищу продуктов животного происхождения) - применение поливитаминных комплексов. Частое дробное питание (5-6 раз в день небольшими порциями).
· Профилактика хронических заболеваний, вызывающих дефицит железа (например, профилактика заболеваний желудка и кишечника - регулярное питание, отказ от острой и жирной пищи, употребление тщательно вымытых овощей и фруктов и др.).
Вторичная профилактика (то есть после развития заболевания) заключается в регулярных профилактических осмотрах населения с целью наиболее раннего выявления у них анемии[7].
5. АНЕМИЯ У БЕРЕМЕННЫХ И ДЕТЕЙ
Анемия у детей может развиваться по разным причинам. Она может возникать из-за разных заболеваний пищеварительной системы, при заболеваниях почек, печени, при нарушенном всасывании, а так же является сопутствующим или самостоятельным признаком онкологических и инфекционных болезней. Так же анемия может возникать при таких физиологических состояниях как беременность, в период лактации, в период усиленного роста, в период полового созревания, после оперативного вмешательства или при гормональных изменениях.
Но в основном патологические состояния встречаются у детей. Детские органы кроветворения еще не полностью анатомо-физиологически зрелые, поэтому они легко поддаются действию всех негативных факторов окружающей среды. У деток раннего возраста анемия требует особого внимания, так как может привести к нарушению обмена веществ и к нарушению физического развития в целом. Часто малокровие у детей развивается в результате глистной инвазии, особенно при аскаридозе. Ребенок чаще всего подвергается данному заболеванию по причине нарушенного питания и развития инфекционных заболеваний.
Грудные дети, которые вскармливаются молоком матери, болеют анемией намного реже, чем дети, которые питаются коровьим молоком или смесями. Это объясняется химическим составом молока женщины: белки молока в организме младенца очень хорошо усваиваются и они при образовании гемоглобина более полноценны. В молоке матери содержится намного больше меди и железа, в коровьей молоке этих элементов незначительное количество, так как после пастеризации, которая обязательна, большая часть витаминов теряет свои свойства.
Если в пище недостаточное количество белка и других микроэлементов, таких как кобальт, никель, железо, медь, марганец, то процесс кроветворения затрудняется, а в редких случаях почти останавливается. Это ведет к появлению анемии. Так же развитию анемии способствует недостаток витаминов, в особенности группы В, фолиевой и аскорбиновой кислоты. У детей подросткового возраста причинами заболевания могут быть алкоголь, курение, употребление наркотиков.
Анемия беременных 90 % случаев является железодефицитной. В развитых странах Европы около 10 % женщин детородного возраста страдают железодефицитной анемией, у 30 % из них наблюдается скрытый дефицит железа, в некоторых регионах нашей страны данный показатель достигает 50-60 %.
В конце беременности практически у всех женщин имеется скрытый дефицит железа, причем у 1/3 из них развивается железодефицитная анемия.
Наличие железодефицитной анемии нарушает качество жизни пациенток, снижает их работоспособность, вызывает функциональные расстройства со стороны многих органов и систем. У беременных дефицит железа увеличивает риск развития осложнений в родах, а при отсутствии своевременной и адекватной терапии ведет к возникновению дефицита железа у плода.
Врачу необходимо знать формы анемии, при которых беременность противопоказана.
· Хроническая железодефицитная анемия III-IV степени.
· Анемия при гипо- и аплазии костного мозга.
· Болезнь Верльгофа с частыми обострениями.
Прерывание беременности следует проводить до срока 12 нед[8].
анемия терапия профилактика
В результате исследования данной работы были изучены вопросы, касающиеся анемии - причины, симптомы, лечение, профилактика и сделаны следующие выводы.
3. В.В. Долгов, С.А. Луговская, В.Т. Морозова, М.Е. Почтарь. Лабораторная диагностика анемий: Пособие для врачей. - Тверь: "Губернская медицина", 2001

2. Воробьев А.И. Городецкий В.М., Шулутко Е.М., Васильев С.А. Острая массивная кровопотеря. – М.: ГЭОТАР-МЕД, 2001. – 175 с.
6. Наглядная гематология / Перевод с англ. Под редакцией проф. В.И. Ершова. – 2-е изд. – М.: ГЭОТАР-Медиа, 2008. – 116 с.: ил.
8. Папаян А.В., Жукова Л.Ю. Анемии у детей: руководство для врачей. – СПб.: ПИТЕР. – 2001 год – 384 с.
9. Патофизиология: учебник: в 2 т./под ред. В.В. Новицкого, Е.Д. Гольдберга, О.И. Уразовой. – 4-е изд. – ГЭОТАР-Медиа, 2010. – Т.2. – 848 с.: ил.
11. Патофизиология: курс лекций/ [Порядин Г. В. и др.]; под ред. Г. В. Порядина. – М. : ГЭОТАР-Медиа, 2012. – 592 с.
14. Садчиков Д.В., Хоженко А.О., Черная А.В. Количественные и качественные изменения клеточных элементов системы крови при тяжелой постгеморрагической анемии (обзор). – Саратовский научнор-медицинский журнал, 2011. – Т.4. – №4. – С.809-813.
15. Третьякова О.С. Постгеморрагические анемии в педиатрической практике. – Здоровье Украины. – 2012. – №8. – С.37-44.
Анемии – состояния, характеризующиеся уменьшением содержания гемоглобина в общем объеме крови, а также как правило, и в единице объема крови.
Анемии следует отличать от гидремии, при которой абсолютное содержание гемоглобина в общем объеме крови не изменяется.
В большинстве случаев патологии анемии характеризуются и эритропенией, в связи с чем анемия может проявляться одновременным уменьшением содержания в единице объема крови и гемоглобина, и эритр оцитов.
Анемии в ряде случаев могут быть отнесены к самостоятельным нозологическим формам патологии, в других – являются лишь симптомом какого-то заболевания.
Касаясь механизмов развития и происхождения анемий, следует отметить, что они могут носить наследственный, врожденный характер, однако в большинстве случаев анемии являются вторичными, или приобретенными.
В зависимости от патогенеза выделяют три основные группы анемий:
1. Постгеморрагические (острые и хронические).
2. Гемолитические (врожденные и приобретенные).
3. Дизэритропоэтические, обусловленные нарушением костномозгового кроветворения.
В процессе установления патогенеза и проведения дифференциальной диагностики анемий используют нередко следующие показатели состояния периферической крови:
– размер и форму эритроцитов;
– наличие регенераторных форм.
В связи с этим принято различать следующие виды анемий:
1. Нормохромные (цветовой показатель 0,85-1,05).
2. Гиперхромные (цветовой показатель больше 1,05).
3. Гипохромные (цветовой показатель меньше 0,85).
Следует отметить, что в ряде случаев цветовой показатель дает возможность дать ориентировочную оценку происхождения анемии. Так, к числу гиперхромных анемий относятся В12-дефицитные, фолиеводефицитные анемии. Ж елезодефицитные анемии, в частности постгеморрагические,- гипохромные. В то же время метапластические, гемолитические анемии могут носить нормохромный характер.
В зависимости от регенераторной активности костного мозга выделяют следующие виды анемий:
4. Арегенераторные (гипо-, апластические анемии).
Для гиперрегенераторных анемий характерно наличие ретакулоцитарных кризов, когда содержание ретикулоцитов в периферической крови может достигать нескольких процентов. При этом отмечается поя вление в периферической крови эритрокариоцитов. К категории гиперрегенераторных анемий относят некоторые формы гемолитических анемий, к числу гипорегенераторных – В12-дефицитные, фолиеводефицитные, железодефицитные анемии.
При гипо- и арегенераторных фор мах анемий количество ретикулоцитов может быть сниженным или вообще не определяться в крови, одновременно возра стает уровень дегенеративных форм эритроцитов.
В зависимости от размеров эритроцитов выделяют следующие формы анемий:
1. Нормоцитарные (7,2-8,3мкм).
2. Микроцитарные (меньше 7,2 мкм).
3. Макроцитарные (9-12 мкм).
4. Мегалоцитарные (12-15 мкм).
Макроцитоз, мегалоцитоз отмечаются при В 12-, фолиеводефицитных анемиях; микроцитоз – при врожденных гемолитических анемиях; нормоцитарные анемии могут быть различного происхождения.
В зависимости от характера кроветворения анемии делят на две группы:
1. С нормобластическим типом кроветворения, для которого характерна последовательность дифференцировки элементов эритроцитарного ряда, включающая следующие этапы: эритробласт – пронормоцит – базофильный нормоцит – полихроматофильный нормоцит – оксифильный нормоцит, ретикулоцит – эритроцит;
2. С мегалобластическим типом кроветворения, включающ им следующие этапы дифференцировки: промегалобласт – базофильный мегалобласт – полихроматофильный мегалобласт – оксифильный мегалобласт – мегалоцит.
Использование приведенных выше классификаций анемий в клинической практике, безусловно, облегчит правильную постановку диагноза, а также даст возможность объективной оценки тяжести течения заболевания и его прогноза.
Постгеморрагические анемии. Различают острую и хроническую постгеморрагическую анемию.
Причины кровопотерь весьма разнообразны: травмы, оперативные вмешательства, поражение сосудистой стенки при язвенной болезни, опухолевом и туберкулезном процессе, мет ро- и меноррагии, спонтанные кровотече ния или слегка индуцированные при врожденно й или приобретенной недостаточности коагуляционного, тромбоцитарного звеньев системы гемостаза и т.д.
У но ворожденных причинами кровопотерь могут быть родовая травма ., трансплацентарная кровопотеря, кровотечение из сосудов пуповины , наследственные геморрагическ ие диатезы, коагулопатии, тромбоцитопении. У девочек возможны ювенильные кровотечения. Чем младше ребенок, тем чувствительнее он к кровопотере.
Реакция взрослого человека на кровопотерю определяется двумя основными факторами: объемом и скоростью кровопотери.
Одномоментная кровопотеря у взрослого человека в объеме 10-15 % всей массы крови не вызывает обычно развит ия шокового синдрома и соответственно тяжелых нарушен ий гемодинамикн. Меж ду тем быстрая пот еря крови новорожденным в таком же объеме может привести к развитию шока.
Для оценки степени кровопотери рекомендуют использовать следующую формулу:
где П – кровопотеря, в %; К – ко эффициент, равный 27 при желудочно-кишечной кровопотере; 33 – при полостных кровотечениях; 24 – при ранениях конечностей; 22 – при пораже нии грудной кл етк и; ШИ – шоковый индекс, равный отношению частоты пульса к систолическому давлению.
Касаясь значимости объема кровопотери, необходимо отметить, что выход из сос у дис то го русла до 20-25 % объема ц иркулирующей крови мало опасен и хорошо компенсируется за сч ет включен ия экстр енных механ измов адаптации, при чем в случае потери до 500 мл крови, что составляет в среднем 10 % ОЦК, клиническ ие проявления могут отсутствовать, иногда возникает умерен ная тахикардия.
При кровопотере объемом от 500 до 1200 мл (10-20 % ОЦК) возникает прогрессирующая тах икардия, снижа ется артериальное давление, появляются пр изнаки вазоконстрикции.
Потеря 25-35 % ц иркулирующей кров и (1200-1800 мл) сопровождается выраженными расстро йствами центральной, органно-тканевой и микрогемоциркуляцин. При этом отмечаются выраженная тахикардия (пульс с выше 120/мин), нарастающая гипотензия, потливость, бледность кожных покровов, беспокойство, слабость, олигурия.
При потере более 40 % объема циркулирующей крови возникает выраженная гипотензия, артериальное давление падает ниже 70 мм рт. ст., прогрессирующая тахикардия (пульс свыше 150/мин), бледность кожных покровов, холодный пот, беспокойство, слабость, олигурия.
Быстрая потеря 50 % крови от общего объема является, как правило, летальной. Потеря такого же объема крови в течение нескольких дней при маточном, желудочном, кишечном кровотечении, как правило, компенсируется при хорошей корригирующей терапии.
Следует отметить высокую чувствительность детского организма к потере крови. Уменьшение объема циркулирующей крови у ребенка на 15-20 % может привести к развитию шока с потерей сознания. У взрослого же человека уменьшение объема циркулирующей крови на 25 % может протека ть в ряде случаев без выраженной гипотензии.
В развитии постгеморрагической анемии следует выделить три стадии: начальную, компенсаторную и терминальную. Причем, характер изменений со стороны периферической крови при постгеморрагической анемии определяется не только тяжестью кровопотери, но и стадией развития постгеморрагической анемии.
Начальная стадия характеризуется уменьшением объема цир кулирующей крови – гиповолемией, при этом в единице объема крови не возникает существенных изменений содержания гемоглобина, количества эри троцитов. Однако снижение объема циркулирующей крови сопровождается уменьшением венозного возврата в сердце, снижением ударного и минутного объема крови, что приводит к развитию циркуляторной гипоксии. Таким образом, гемическая гипоксия при кровопотере всегда сочетается и с циркуляторной.
Возникновение гипоксии, гиповолемии, метаболического ацидоза инициирует ра звитие механизмов срочной адаптации. Одним из мобильных звеньев адаптации является активация симпатоадреналовой системы, что приводит к развитию комплекса защитно-приспособительных реакций. Во-первых, возникает рефлекторный спазм периферических сосудов, или рефлекторно-сосудистая компенсация постгеморрагической анемии, направленная на адаптацию емкости сосудистого русла к объему циркулирующей крови и предотвращение развития шокового синдрома. Однако даже при максимальном спазме сосудов емкость сосудистого русла может уменьшиться лишь на 15-20 % . Активация симпатоадреналовой системы в этот период анемии приводит к рефлекторному учащению сердечных сокращений.
Изучение гематологических показателей в период рефлекторно-сосудистой компенсации может выявить лишь незначительное снижение уровня гемоглобина и эритроцитов, отсутствие выраженных изменений гематокрита.
В условиях гипоксии, гиповолемии активируется ренин-ангиотензиновая система, усиливается освобождение минералокортикоидов, что приводит к усилению реабсорбции натрия в почечных канальцах, повышению осмотического давления в плазме крови, стимуляции выброса антидиуретического гормона и усилению факультативной реабсорбции воды в дистальных почечных канальцах. Жидкость поступает в кровеносные капилляры по градиенту осмотического давления. Развив ается так называемая гидремическая компенсация спустя 1-3 суток после кровопотери. для этого периода характерно уменьшение количества эритроцитов и гемоглобина в единице объема крови и во всем объеме крови. Анемия носит нормохромный характер.
Возникновение гипоксии при постгеморрагической анемии стимулирует продукцию эритропоэтина. по физико-химическим свойствам эритропоэтин представляет собой кислый термостабильный гликопротеин. Мономерная форма белка эритропоэтина имеет ММ от 23000 Д до 32000 Д. Однако в натуральном виде гормон представляет собой димер с ММ от 46000 Д до 60000 Д; содержание белка в нем составляет около 65,5 °/о ; углеводов – около 30 %. Считают, что эритропоэтин образуется в различных клетках нефрона, а также в печени и селезенке.
Существует точка зрения, что эритропоэтин почечного происхождения неактивен, его именуют эритрогенином. В процессе взаимодействия почечного эритрогенина со специализированными белками плазмы крови α2-глобулиновой фракции, вырабатываемыми в печени, образуется активная форма эритропоэтина.
Под влиянием эритропоэтина эритропоэтинчувствительные клетки дифференцируются в эритробласты и далее – до зрелых эритроцитов, которые выходят в сосудистое русло и компенсируют утраченные при кровопотере клетки. Возникает период костномозговой компенсации, выраженный обычно уже спустя 45 дней после кровопотери. При этом в периферической крови появляются молодые, не донас ыщенн ые гемоглоб ином формы эритроцитов – ретикулоциты, оксифильные, полихроматофильные, базофильные нормоциты, т. е. клетки, характеризующие регенераторную активность костного мозга. Анемия приобретает гипохромный характер. Одновременно в периферическую кровь из костного мозга поступают и другие клеточные элементы. Признаком достаточно выраженной регенераторной способности костного мозга является возникновение нейтрофильного лейкоцитоза со сдвигом влево.
Стимуляторами костномозговой компенсации после кровопотери являются и такие гормоны адаптации, как катехоламины, глюкокортикоиды. Однако их стимулирующий эффект на кроветворение опосредуется, по-видимому, за счет первичной активации синтеза под влиянием этих гормонов эритропоэтина.
Параллельно с костномозговой компенсацией развертывается белковая компенсация за счет активации синтеза в печени различных плазменных белков, в частности, плазменных белковых факторов свертывания крови. Следует отметить, что активация протеосинтеза наблюдается уже через несколько часов после кровотечения и регистрируется в течение последующих 1,5-3 недель и более в зависимости от объема кровопотери и состояния реактивности организма.
Вышеописанная стадийность развития свойственна острым постгеморрагическим анемиям. Все постгеморрагические анемии – острые и хронические – являются железодефицитными, поэтому характеризуются комплексом метаболических и функциональных расстройств, обусловленных недостаточностью железа.
Читайте также:

