Жизненный цикл малярийного плазмодия кратко
Обновлено: 03.07.2024
Малярийный плазмодий (Plasmodium vivax) (рис. 1) относится к подотряду Кровяные споровики (Haemosporidina). Вызывает у человека тяжелое широко распространенное заболевание малярию. Заражение человека происходит при укусе малярийного комара (род Anopheles), слюна которого содержит возбудителя на стадии спорозоитов.
Веретенообразные тонкие спорозоиты током крови доносятся до печени, внедряются в ее клетки, где развиваются и делятся путем шизогонии. Образовавшиеся в результате деления в клетках печени молодые плазмодии (мерозоиты) поступают в кровь и проникают в эритроциты. В эритроцитах они превращаются сначала в трофозоиты (питание гемоглобином и рост), затем – в шизонты (бесполое размножение). Таким образом, различают две формы шизогонии: тканевая и эритроцитарная. В результате эритроцитарной шизогонии образуются 10–20 мерозоитов, которые разрушают эритроцит, выходят в кровь и заражают следующие эритроциты. При разрушении эритроцитов в кровь попадают и токсичные продукты жизнедеятельности плазмодия. Эритроцитарная шизогония длится у данного вида плазмодия 48 часов. Цикличность приступов малярии обусловлена цикличностью выходов мерозоитов и продуктов их метаболизма из эритроцитов в плазму крови.
После нескольких циклов шизогонии в эритроцитах образуются гамонты, которые в организме комара превратятся в макрогаметы и микрогаметы.
При сосании комаром крови больного человека, гамонты попадают в кишечник комара, где превращаются в гаметы. Из микрогамонта образуется 4–8 микрогамет, из макрогамонта – яйцеклетка, происходит копуляция гамет. Образовавшаяся в результате оплодотворения зигота обладает подвижностью и называется оокинетой. Оокинета мигрирует через стенку кишечника комара и на внешней поверхности кишечника превращается в ооцисту. Ядро ооцисты многократно делится и ооциста распадается на огромное количество спорозоитов – до 10000, этот процесс называется спорогонией. Спорозоиты перемещаются в слюнные железы комара.

рис. 1. Жизненный цикл малярийного плазмодия:
1 - спорозоиты, 2-4 - шизогония в печени (2 - спороит,
внедрившийся в печеночную клетку, 3 - растущий шизонт
с многочисленными ядрами, 4 - шизонт, распадающийся на
мерозоиты), 5-9 - эритроцитарная шизогония, 10 - мерозоиты,
11-12 - гаметогония и образование гамонтов, 13 - макрогамета,
14 - микрогамонт, 15 - образование микрогамет (фрагелляция),
16 - копуляция, 17 - зигота, 18 - подвижная зигота (оокинета),
19 - проникновение оокинеты сквозь стенку кишечника комара,
20 - превращение оокинеты в ооцисту на наружной стенке
кишечника комара, развитие ооцисты, 21-23 - развитие ооцисты,
24 - спорозоиты, покидающие ооцисту, 25 - спорозоиты
в слюнных железах комара.
В жизненном цикле малярийного плазмодия человек является промежуточным хозяином (тканевая шизогония, эритроцитарная шизогония, начало гаметогонии), а малярийный комар – окончательным (завершение гаметогонии, оплодотворение и спорогония).
Малярия характеризуется периодическими приступами лихорадки, каждый приступ включает стадии озноба, повышения температуры до 41° и длится до 6–12 часов. Интервалы между приступами зависят от вида плазмодия. Кроме лихорадочного состояния развивается анемия (малокровие).
Лабораторная диагностика – обнаружение плазмодиев в мазке или толстой капле крови.
Токсоплазма (Toxoplasma gondii) относится к подотряду Эймериевые (Eimeriina). Является внутриклеточным паразитом человека и животных, вызывает повсеместно распространенное заболевание токсоплазмоз.
Жизненный цикл (рис. 2) происходит со сменой хозяев. Окончательным хозяином является кошка, в ее кишечнике происходит половое размножение, промежуточными хозяевами являются человек, грызуны, крупный имелкий рогатый скот и другие виды теплокровных животных. Клинические симптомы токсоплазмоза разнообразны и зависят от того, какие именно органы поражены паразитом. Токсоплазма может паразитировать в нервной, половой, лимфатической и других системах. У взрослых токсоплазмоз может быть бессимптомным. Заражение человека происходит различными способами: а) перорально при употреблении сырого или полусырого мяса больного животного; б) перорально с овощами, фруктами, загрязненными ооцистами; в) через загрязненные ооцистами руки и предметы; г) трансплацентарно от матери-носительницы к плоду. В последнем случае плод погибает (выкидыш, мертворождение) или рождается с симптомами острого врожденного токсоплазмоза поражения (печени, селезенки, нервной системы, интоксикация, повышенная температура и др.).

рис. 2. Жизненный цикл токсоплазмы:
А - окончательный хозяин (кошка), Б - промежуточный
хозяин (грызуны): 1-3 - стадии развития ооцисты
во внешней среде, 4 - внутриутробное заражение.
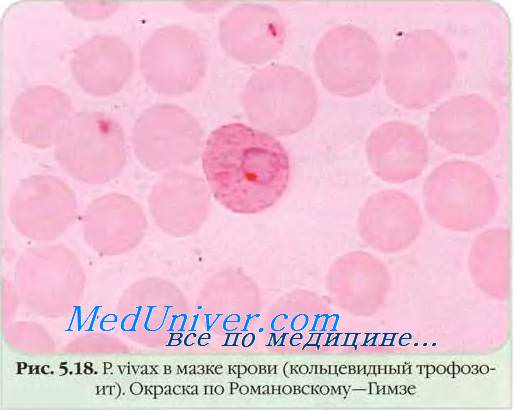
Малярию выявляют в регионах от 45° северной до 40° южной широты, чаще в тропиках и субтропиках. В странах с умеренным климатом основной возбудитель малярии — P. vivax, в тропиках — P. falciparum.
Резервуар возбудителя малярии — больной человек; основной механизм заражения — трансмиссивный. Переносчики малярии — самки комаров рода Anopheles; этиологическую роль комаров доказал Р. Росс (1897). Человек— промежуточный, а комар — окончательный хозяин паразита. Также возможно вертикальное заражение от матери к плоду.
В 104 эндемичных малярии странах регистрируют около 250 млн новых случаев заболевания; смертность от малярии достигает 1-2 млн ежегодно. Заболеваемость напрямую зависит от размеров популяции комаров и количества больных, служащих резервуаром инфекции. В связи с развитием индустрии туризма заболевание стали выявлять в странах, лежащих за пределами естественного ареала.
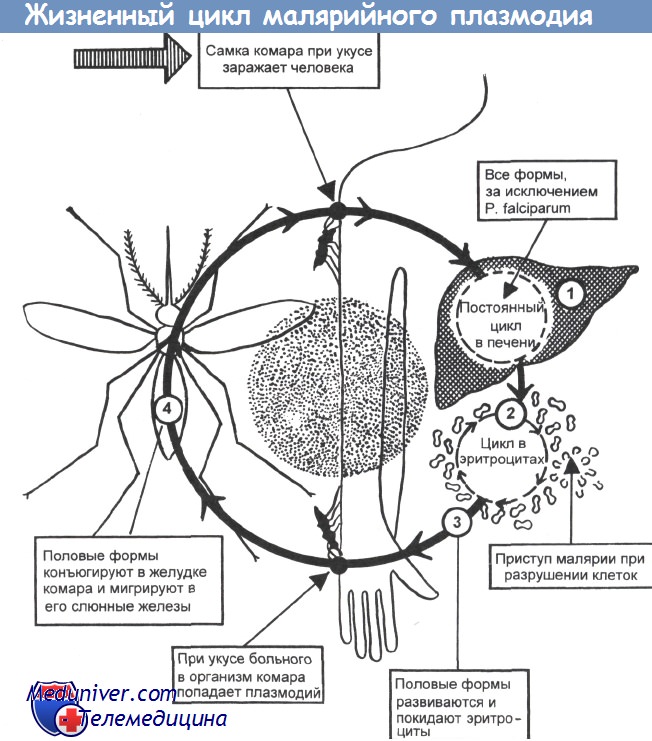
Жизненный цикл малярийных плазмодиев
У различных видов малярийных плазмодиев жизненный цикл практически одинаков, а основные различия связаны с характером поражений эритроцитов. В организме человека происходит бесполая стадия (шизогония), в организме комаров — половая стадия (спорогония).
• Спорогония малярийных плазмодиев происходит в клетках эпителия ЖКТ комара; её продолжительность 1 -3 нед. С кровью больного в организм комара проникают мужские и женские гаметы (гамонты), попарно сливающиеся в зиготы, проникающие в стенку кишки и образующие там ооцисты. Содержимое ооцист претерпевает процесс спорогонии, то есть многократного деления с образованием веретенообразных спорозоитов. Спорозоиты — подвижные клетки длиной 11-15мкм, диссеминирующие по всему организму насекомого. Часть из них проникает в слюнные железы комара, в результате чего он становится переносчиком болезни.
• Тканевая (экзоэритроцитарная) шизогония малярийных плазмодиев происходит в гепатоцитах и продолжается 1-2,5 нед. Уже через час после укуса комара спорозоиты проникают с кровотоком в клетки печени, где происходит их размножение и деление. В результате деления образуются мерозоиты (каждый спорозоит может образовать от 2000 до 40 000 мерозоитов), разрушающие гепатоциты и проникающие в кровоток.
• Эритроцитарная шизогония малярийных плазмодиев происходит после проникновения мерозоитов в эритроциты путём эндоцитоза, где образуется паразитоформная псевдовакуоль. Затем мерозоиты превращаются в трофозбиты (бесполые формы), утилизирующие гемоглобин. В ходе развития паразитов в эритроцитах происходит накопление пигмента. Юные трофозои-ты содержат ядро с одним хроматиновым зерном и внешне напоминают перстень или кольцо. Незрелые трофозоиты имеют амёбовидную форму, а трофозоиты P. vivax способны передвигаться внутри эритроцитов [от лат. vivax, живой]. У зрелых трофозоитов ядра делятся; образуются многоядерные шизонты (делящиеся формы), дающие новое поколение мерозоитов. Выход мерозоитов из эритроцита сопровождается его разрушением. Цикл развития для P. malariae составляет 72 ч, для других видов — 48 ч. В некоторых эритроцитах развиваются мужские (микрогаметоциты) и женские (макрогаметоциты) гамонты, завершающие своё развитие только в организме комара в течение 7-45 сут.
• С наступлением эритроцитарной шизогонии малярийных плазмодиев размножение P. malariae и Pj. falciparum в печени прекращается, однако у P. vivax и P. ovale часть спорозоитов (гипнозоиты) остаётся в гепатоцитах, образуя дремлющие очаги, дающие отдалённые рецидивы.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Малярийный плазмодий вызывает у человека такое опасное протозойное заболевание, притом хроническое и протекающее с рецидивами, как малярия, от которого, по данным Всемирной организации здравоохранения, во всем мире каждый год уходит из жизни почти 2 млн. человек.
И сегодня в списке инфекционных заболеваний со смертельным исходом на первом месте стоит не СПИД, а малярия.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12]
Строение малярийного плазмодия
Единственный путь, которым малярийный плазмодий проникает в организм человека, это укус комара. И из более трех тысяч существующих в природе видов этих двукрылых насекомых данный паразит переносится только малярийным комаром рода анофелес (Anopheles superpictus). Причем, этот комар обязательно должен быть самкой, так как именно ей нужна кровь как источник белков для выведения яиц.
В момент укуса комар впрыскивает в кожу человека слюну (чтобы кровь не свертывалась), и вместе со слюной в кожу попадают спорозоиты малярийного плазмодия. Спорозоит - репродуктивная форма только одной стадии жизненного цикла этого протиста. Строение малярийного плазмодия на стадии спорозоитов имеет вид продолговатых и слегка изогнутых клеток размером не более 15 мкм.
Основной хозяин малярийного плазмодия - комар анофелес, поскольку в его организме плазмодий занимается спорогонией (половым размножением). А человек - промежуточный хозяин малярийного плазмодия, так как организм Homo sapiens он использует для агамогенеза, то есть бесполого размножения. Биологи выяснили, что у одноклеточных рода Plasmodium бесполое размножение имеет особую форму шизогонии, когда первоначальная клетка делится не на две дочерние, а сразу на множество. Таким образом размножение малярийного плазмодия адаптировано к способу его распространения – от одного хозяина к другому.
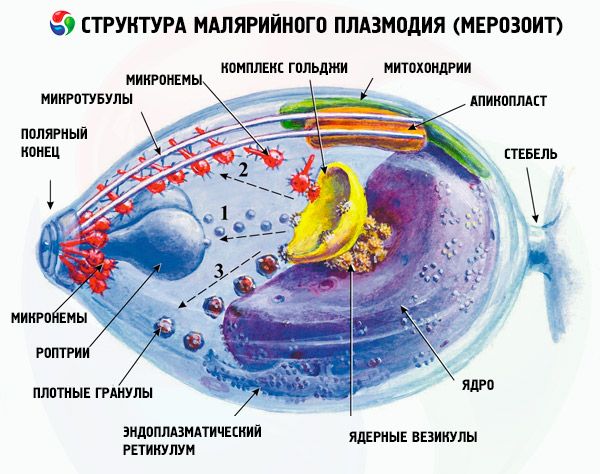
Цикл развития малярийного плазмодия
Малярийный плазмодий относится к простейшим микроорганизмам царства Протиста (Protista), класса Споровиков (Sporozoa), отряда гемоспоридий (Haemosporidia), рода Plasmodium.
Виды малярийных плазмодиев Plasmodium vivax, Plasmodium malariae, Plasmodium falciparum и Plasmodium ovale опасны для человека, так как являются причиной возникновения малярии. Вид малярийных плазмодиев Plasmodium ovale – более редкий, и подхватить его можно только в африканских или азиатских тропиках.
Цикл развития малярийного плазмодия: от комара - к человеку
Цикл развития малярийного плазмодия разбит на две практические равные части, каждая из которых проходит в организме либо комара, либо человека. Начнем с того момента, когда спорозоиты малярийного плазмодия проникают в организм человека.
Попадая в кровь, спорозоит очень быстро оказываются в ткани печени и уже здесь начинают бесполое размножение (шизогонию), превращаясь в мерозоиты. Эти голодные молодые плазмодии проникают в красные кровяные тельца (эритроциты) и, поглощая гемоглобин, продолжают так же бесполым способом усиленно размножаться. На этой стадии строение малярийного плазмодия представляет собой клетки размером не более 2 мкм с протоплазмой и ядром, их форма – округлая или овальная (похожая на амебу).
Затем мерозоиты, разрушая эритроциты, выходят из них и принимают форму колец, а в их протоплазме образуются полости – пищеварительные вакуоли, которые накапливают питательные вещества и выводят продукты жизнедеятельности: так токсины плазмодия попадают в кровоток человека.
Эритроцитарная шизогония циклично повторяется и продолжается до тех пор, пока количество мерозоитов не достигнет нужного уровня. И тогда цикл развития малярийного плазмодия вступает в следующую стадию, и образуются половые клетки гаметоциты.
Цикл развития малярийного плазмодия: от человека - к комару
Чтобы началось половое размножение малярийного плазмодия (спорогония), ему необходимо сменить хозяина и попасть в желудок комара анофелеса. К этому времени гаметоциты готовы к разделению на микрогаметоциты и макрогаметоциты.
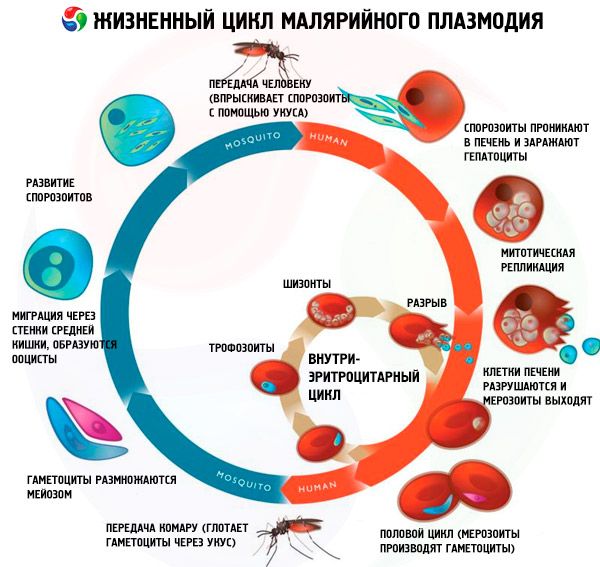
Зиготы малярийного плазмодия весьма подвижные и, не мешкая, встревают между клетками мышечной стенки желудка насекомого, закрепляются там и образуют спороцисты – круглые клетки-инкубаторы, покрытые оболочкой (созданной, между прочим, из тканей комара). Этот цикл развития малярийного плазмодия в организме комара – один из последних. В ходе роста спороцист, под их оболочкой продолжается клеточный митоз, и в каждой образуются сотни спорозоитов (строение которых было описано выше).
Кровь на малярийный плазмодий
Кровь на малярийный плазмодий берут из пальца на руке обычным способом, а затем делают на стерильном предметном стекле мазок крови, который изучают под микроскопом.
Поскольку виды малярийных плазмодиев несколько различаются друг от друга по своему строению, то каждый вид имеет четкие диагностические признаки.
К таким признакам специалисты относят и строение малярийного плазмодия, и характер изменения пораженных эритроцитов. Как правило, такие красные кровяные тельца увеличены, некоторые меняют свою форму и цвет и т.д.

[13], [14], [15], [16], [17], [18], [19], [20]
Профилактика малярийных плазмодиев
До сегодняшнего дня никому не удалось создать вакцину против малярии, поэтому так важна профилактика малярийных плазмодиев.
В эндемичных для малярии районах земного шара профилактика малярийных плазмодиев, в первую очередь, она направлена на уничтожение комаров Anopheles с помощью инсектицидов.
Для индивидуальной защиты от укусов малярийных комаров применяют различные репелленты (жидкие, в виде кремов и аэрозолей), надевают закрытую одежду и противокомариные сетки, которые также опрыскивают репеллентами.
Есть специальные фармацевтические препараты для профилактики малярийных плазмодиев. Отправляясь в места, где распространена малярия и существует вероятность ее подцепить, эти средства необходимо принимать заранее.
Например, противомалярийное средство Делагил (Хлорохин, Резохин) в таблетках принимают по 0,5 г дважды в течение неделю, а потом - по 0,5 г один раз в неделю. Действие препарата базируется на способности его активного вещества - производного 4-аминохинолина – тормозит синтез нуклеиновых кислот и тем самым уничтожать клетки малярийного плазмодия. Данное средство противопоказано при нарушениях работы почек и печени, тяжелой сердечной недостаточности, снижении кроветворной функции костного мозга. Его также нельзя принимать беременным и детям дошкольного возраста. Медики отмечают, что, покинув малярийно опасную местность, препарат нужно продолжать принимать еще как минимум месяц.
Как знать, что бы еще завоевал Александр Македонский и что бы сделал для Англии Оливер Кромвель, если бы их не укусил малярийный комар, и малярийный плазмодий не вызвал бы смертельную болезнь.

Род включен в состав типа apicomplexa класса sporozoea отряда eucoccidiida подотряда haemosporma. Род включает более 100 видов, паразитирующих в организмах рептилий птиц и животных. Четыре вида патогеннs для человека и вызывает малярию — трансмиссивное заболевание человека, характеризующееся преимущественным поражением ретикулогистиоцитарной системы и эритроцитов, приступами лихорадки, анемией и гепатоспленомегалией. Plasmodium vivax - возбудитель трехдневной малярии, Р. malariae - возбудитель четырехдневной малярии, Р. falciparum - возбудитель тропической малярии, Р. ovale - возбудитель малярии овале (типа трехдневной).
Возбудителя малярии (микрогаметы Р. falciparum) в крови человека впервые обнаружил Лаверан (6 ноября 1880 г). Принадлежность возбудителя к споровикам установил И. И. Мечников (1886). Цикл развития паразита в организме, стадии и закономерности появления приступов были установлены Гольджи (1889). Следует отметить, что известны случаи заболевания человека малярией обезьян в эндемичных очагах.
Жизненный цикл (Рис. 1) различных видов плазмодиев практически одинаковый (основные различия связаны с образованием поколений поражающих эритроциты) включает бесполую стадию (шизогония), проходящую в организме человека, и половую стадию (спорогония), проходящую в организме переносчика — самок комаров рода anopheles (цикл Росса).
Рисунок 1. Жизненный цикл различных плазмодиев
Спорогония малярийного плазмодия происходит в клетках эпителия ЖКТ комара и продолжается 1-3 нед.
Процесс начинается с проникновения мужских и женских гамет (гамонтов) в организм комара с кровью больного.
Гамонты сливаются попарно в зиготы, проникающие в стенку кишки и образующие там ооцисты.
Содержимое ооцист претерпевает процесс спорогонии — многократно делится и образует спорозоиты (веретенообразные клетки длиной 11-15 мкм), диссеминирующие по всему организму насекомого. Часть из них проникает в слюнные железы, делая комара переносчиком болезни.
Тканевая или экзоэритроцитарная шизогония плазмодия происходит в гепатоцитах человека и продолжается 1-2 нед (цикл размножения Р. falciparum и Р. malarie в печени варьирует в пределах 10-18 сут).
Через час после кровососания спорозоиты проникают с кровотоком в клетки печени где размножаются и делятся.
В результате деления образуются мерозоиты (каждый спорозоит может образовать от 2000 до 40 000 мерозоитов), разрушающие гепатоциты и проникающие в кровоток.
Эритроцитариая шизогония происходит после проникновении мерозоитов в эритроциты.

Проникшие в клетки мерозоиты превращаются в трофозоиты (растущие формы) размером 2 мкм, микроскопия пораженных эритроцитов выявляет покоящиеся формы, содержащие ядро с одним хроматиновым зерном (Рис. 2), и формы с псевдовакуолью, внешне напоминающие перстень или кольцо (Рис. 3).
Рисунок 2. Покоящиеся формы, содержащие ядро с одним хроматиновым зерном

Рисунок 3. Формы с псевдовакуолью, внешне напоминающие перстень или кольцо
Размеры трофозоитов Р. falciparum меньше половины эритроцита и не вызывают его деформации.

Трофозоиты Р. vivax больше по размерам, имеют псевдоподии и способны передвигаться внутри эритроцита (отсюда vivax — живой), вызывая увеличение и деформацию клеток (Рис. 4).
Рисунок 4. Трофозоиты Р. vivax

Несмотря на наличие нескольких псевдоподий, трофозоиты Р. malariae практически неподвижны в мазках часто выглядят как тельца включений или ленты. Пораженные эритроциты не деформированы (Рис. 5).
Рисунок 5. Трофозоиты Р. malariae

Поскольку Р. ovale занимает промежуточное положение между Р. vivax и Р. malariae, то он деформирует около 60% инфицированных эритроцитов делая их овальными (Рис. 6).
Рисунок 6. Трофозоиты Р. ovale
Трофозоиты позднее увеличиваются и образуют многоядерные шизонты (делящиеся формы).

Шизонты образуют новое поколение мерозоитов. Каждая клетка может образовывать 6-24 дочерних мерозоита инфицирующих другие эритроциты (Рис. 7, 8).
Рисунок 7. Многоядерный шизонт

Рисунок 8. Многоядерный шизонт

Выход мерозоитов из эритроцита сопровождается его разрушением (Рис. 9).
Рисунок 9. Выход мерозоитов из эритроцита
Указанный цикл развития для Р. malariae составляет 72 ч, для других видов — 48 ч.
В некоторых эритроцитах из макрогаметоцитов (Рис. 10) развиваются женские, из микрогаметоцитов (Рис. 11) мужские гамонты, завершающие своё развитие только в организме комара в течение 7-45 сут (в зависимости от температуры воздуха).

Рисунок 10. Макрогаметоцит

Рисунок 11. Микрогаметоцит
Распространение. Малярию выявляют повсеместно (Рис 12) от 45° северной до 40° южной широты (но чаще в тропиках и субтропиках) на высоте от 0 до 1 800 м над уровнем моря. В странах с умеренным климатом более часто выделяют Р. vivax, реже — Р. malariae. В тропиках основной возбудитель — Р. falciparum, и лишь спорадически в африканских странах выделяют Р. ovale. В 40-50-х гг. значительная часть очагов малярии в Европе и США была уничтожена применением инсектицидов, в частности ДДТ. теории развития заболеваний. В опубликованном в 1717 г. сочинении (mal'aria) в организм, что дало начало известной

Распространение. Малярию выявляют повсеместно (Рис 12) от 45°
Рисунок 12. Распространение малярии
Заболеваемость. Ежегодно в 104 эндемичных странах заболевают около 250 млн человек. Смертельные исходы чаще всего наблюдают среди детей, но также регистрируют среди неиммунизированных взрослых (1-2 млн ежегодно). Заболеваемость напрямую зависит от размеров популяции комаров и количества больных, служащих резервуаром инфекции. В связи с развитием индустрии туризма заболевание выявляют в странах, лежащих за пределами естественного ареала.
Анализ эпидемиологических факторов показывает, что передача инфекционного агента в большинстве случаев носит горизонтальный характер (распространение в течение эпидемического сезона возможно только через комара); что касается вертикальной передачи (наличие преемственной связи между сезонами), то она встречается редко. Подобные ситуации опосредуют лица-гамонтоносители, количество которых часто недооценивают. Следует учитывать, что в селезёнке количество гамонтов превышает таковое в периферической крови. Фактическое количество гамонтоносителей составляет 20-80% всех паразитоносителей.
Лихорадка наблюдается в момент выхода мерозоитов из разрушенных эритроцитов; интервалы между проявлениями приступов зависят от биологического цикла паразита. Начало острое, температура тела может достигать 40-41,7 °С (обычно подъём наблюдают в дневное время). Через несколько часов она литически снижается до 35-36 °С. При разрушении эритроцитов в кровь выделяется эндопироген, структура которого остаётся неидентифицированной (определённая роль может принадлежать гематину). Определённую роль в развитии лихорадочной реакции могут играть ИЛ-1 и фактор некроза опухолей, выделяемые макрофагами, активируемыми во время утилизации остатков эритроцитов.
Анемия — следствие массивного лизиса эритроцитов и фагоцитоза поражённых клеток фагоцитами. При тропической малярии, вызванной Р. falciparum черно-водная лихорадка (гемоглобинурийная лихорадка). Характерны острый массивный гемолиз, гемолитическая желтуха, боли в пояснице, гемоглобинурия. Может развиться как осложнение малярии, возникающее после приёма хинина и примахина; чаще возникает у лиц с повышенной ломкостью эритроцитов. Вследствие наследственного дефекта глюкозо-6-фосфатдегидрогеназы по типу анемии Маркиафавы-Микели, а также как реакция ГЗТ на хинин; комплексы хинин-АТ сорбируются на мембранах эритроцитов, активируют комплемент, что приводит к их генерализованному разрушению. Значительно реже и лишь при тропической малярии наблюдают внутрисосудистый гемолиз.
Нарушения кровообращения в первую очередь опосредованы подъёмами температуры тела. Дилатация сосудов приводит к снижению ОЦК и АД. Последующий спазм сосудов, повышенная вязкость крови, закупорка капилляров остатками эритроцитов приводят к ишемии органов и тканей.
Иногда тропическую (falciparum) малярию сопровождает острый гломерулонефрит.
Р. malariae может развиться прогрессирующая почечная недостаточность. Механизмы нефропатологии при малярии по большей части опосредованы аутоиммунными механизмами.
Заболевание часто сопровождают спленомегалия (увеличение не всегда соответствует тяжести заболевания) и тромбоцитопения.
Поражения органов ЖКТ достаточно многообразны — от гангренозно-язвенных до холероподобных. Печень обычно увеличена, гиперемирована и окрашена в тёмно-коричневый цвет. При хронических поражениях её масса достигает 3-5 кг. Нередки поражения поджелудочной железы вплоть до фиброзного панкреатита.
Иммунные реакции
Проникновение плазмодиев в кровоток индуцирует развитие иммунного ответа, направленного на подавление активности возбудителя и значительно смягчающего тяжесть клинических проявлений. Отмечены случаи абсолютной резистентности к инфекции, опосредованные иммунными и генетическими механизмами, передающимися по наследству.
Поскольку заболевание носит длительный циклический характер, уровень иммунного ответа постоянно нарастает. Под воздействием иммунных механизмов цикл шизогоний постепенно замещается спорогониями со смягчением симптоматики. В редких случаях возможно спонтанное выздоровление.
В подавлении размножения плазмодиев задействованы гуморальное и клеточное звенья иммунного ответа. Однако, степень их участия неопределенна.
Факторы организма, влияющие на заболеваемость
Лица, эритроциты которых не несут Аг группы duffy обладают естественной резистентностью к возбудителям малярии (отсутствуют у многих представителей негроидной расы).
Естественной резистентностью обладают лица с врождённым дефицитом глюкозо-6-дегидрогеназы, т.к. паразиты не способны использовать глюкозо-монофосфатный шунт в качестве источника энергии и в подобных условиях не могут развиваться в эритроцитах.
Лица с гемоглобинопатиями также резистентны к заражению, т.к. паразиты не способны размножаться в эритроцитах с изменённой морфологией, например при серпо-видноклеточной анемии.
Лабораторная диагностика малярии основана на выявлении паразитов в крови и соответствующей симптоматике. Некоторые отличительные признаки малярийных плазмодиев в мазке периферической крови представлены в табл. 1.
Для приготовления мазков пригодна капиллярная и венозная кровь. Мазки окрашивают по Райту или Романовскому Гимзе. Различные виды дифференцируют по морфологическим признакам.
При эпидемических обследованиях регионов более пригодна серологическая идентификация, например методом непрямой иммунофлюоресценции, выявляющим Аг в мазках. Также можно воспользоваться новокаин-формалиновой пробой Касты.
При невозможности обнаружения паразитов косвенные данные могут дать изменения лейкоцитарной формулы даже при однократном исследовании (моноцитоз, анэозинофилия, ядерный сдвиг влево в лейкоцитарной формуле).
Для экспресс-диагностики возможна микроскопия крови в толстой капле (препараты окрашиваются без фиксации). Следует помнить, что в препаратах эритроциты разрушаются, лейкоциты деформируются, а возбудитель может частично сморщиваться. Отличительные признаки приведены в табл. 2.
Отличительные признаки малярийных плазмодиев в мазке периферической крови (окраска по Романовскому-Гимза)
| Паразиты | Р. vivax | Р. ovale | Р. malariae | Р. falciparum |
| Эритроциты | ||||
| Увеличенные, бледно-розовые | + | + | - | - |
| Овоидные, края часто бахромчатые | - | + | - | - |
| Зернистость в пораженном эритроците | ||||
| Мелкая, обильная, красная (зерна Шюффнера) | + | - | - | - |
| Крупная, менее обильная (зерна Джеймса) | - | + | - | - |
| Единичные крупные розовые или фиолетовые пятна (пятна Маурера) | - | - | - | + |
| Паразит | ||||
| Наличие всех стадии шизогонии | + | + | + | + |
| Стадия кольца (количество паразитов в эритроците) | 2-3 | 2-3 | 1 | 2-3 |
| Лентовидные формы | - | - | + | - |
| Двойные пятна хроматина | - | - | - | + |
| Округлые гамонты | + | + | + | - |
| Полулунные гамонты | - | - | - | + |
| Пигмент во взрослом трофозоите | Обильный рассеянный | Более грубый, рассеянный | Более грубый, рассеянный | Компактный, в виде кучки |
Отличительные признаки малярийных плазмодиев в толстой капле крови (окраска по Романовскому-Гимзе)
| Признак | Р. vivax | Р. ovale | Р. malariae | Р. falciparum |
| Кольца | Часто разорваны, напоминают восклицательный знак или летящую птицу | Сходны с Р. vivax | Сохраняют форму, часто в виде ядра с небольшим ободком цитоплазмы | Сходны с другими видами, ядра крупные, неправильные |
| Эритроциты | Часто сохраняются в виде розоватых дисков с шизонтами и зернами Шюффнера | Не сохраняются | Не сохраняются | Сохраняются остатки эритроцитов даже на стадии кольца |
| Трофозоиты | Амебовидные содержат комочки цитоплазмы вокруг ядра, зрелые — компактные, круглые | Круглые, хорошо окрашенные | Обычно не обнаруживают | Компактные |
| Пигмент | Мелкий, палочковидны | Круглые, крупные зерна | В виде черной глыбки | Буровато-коричневый |
Лечение. История терапии малярии насчитывает более 350 лет (в 1640 г. испанцы завезли в Европу кору хинного дерева, употреблявшуюся индейцами в Эквадоре в качестве противо-лихорадочного средства). Длительное время хинин — алкалоид коры хинного дерева (cinchona) — оставался единственным средством химиотерапии. Современный арсенал препаратов позволяет ингибировать эритроцитарную шизогонию (препятствуя развитию приступов лихорадки), внеэритроцитарную шизогонию (препятствуя развитию рецидивов) и элиминировать циркулирующие гамонты (препятствуя переносу возбудителя от человека к человеку). Препараты, действующие одновременно по трем указанным направлениям, отсутствуют. Приступы лихорадки купируют многие препараты
Среди них наиболее известно производное 4-аминохинолина — хлорохин (в отечественной фармакопее — хингамин). Препарат активен против всех видов плазмодиев, однако существуют формы, резистентные к его действию.
Профилактика. Смысл профилактики сводится к разрыву биоценоза плазмодий-комар-человек, что может быть достигнуто терапевтическим уничтожением возбудителя в организме человека (метод Коха) либо бонификацией (метод Росса). Несмотря на ликвидацию малярии на территории бывшего СССР, вероятность ее возобновления в РФ постоянно возрастает. Это связано с нарушением системы контроля за местами выплода комаров рода anopheles и постоянным завозом малярии из стран юго-восточной Азии, Африки и Латинской Америки. В связи с этим необходимо проводить исследование на малярию независимо от сезона (приказ МЗ СССР № 930 от 23. 09. 76) осуществлять санацию и контроль за носителями. Несмотря на многочисленные попытки, эффективные средства вакцинопрофилактики отсутствуют.
СХЕМЫ МИКРОСКОПИЧЕСКОГО СТРОЕНИЯ РАЗЛИЧНЫХ ФОРМ ВОЗБУДИТЕЛЕЙ МАЛЯРИИ, ИДЕНТИФИЦИРУЕМЫХ В ЭРИТРОЦИТАХ
Читайте также:

