Пути обезвреживания аммиака в организме кратко
Обновлено: 05.07.2024
Е.В. Голованова
Кафедра поликлинической терапии ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России, Москва
Аммиак является одним из важнейших нейротоксических метаболитов в организме человека. В клинической практике наиболее частым проявлением гипераммониемии является печеночная энцефалопатия (ПЭ) при патологии печени, представляющая собой спектр нервно-психических расстройств на фоне острой или хронической печеночно-клеточной недостаточности и/или порто-системном шунтировании крови. Снижение уровня аммиака является патогенетическим подходом к лечению хронических заболеваний печени, позволяющим не только снизить проявления ПЭ, но и уменьшить активацию звездчатых клеток печени, улучшить печеночный кровоток, препятствовать развитию и прогрессированию фиброза печени.
Основным источником образования аммиака в организме человека является азот пищевого белка, образующийся в ходе реакций дезаминирования аминокислот в печени. Дополнительными источниками образования аммиака являются:
- Разложение мочевины и белка уреазаположительной микрофлорой желудочно-кишечного тракта (ЖКТ).
- Образование аммиака в мышечной ткани при физической нагрузке.
- Распад глутамина в тонкой кишке.
- Абсорбция аммиака в почках при гипокалиемии и/или алкалозе.
Выделение мочевины осуществляется преимущественно через почки (около 80%), примерно 20% мочевины повторно поступают в ЖКТ, где вновь разлагается уреазаположительными бактериями до аммиака.
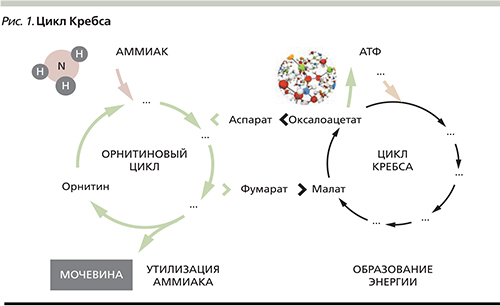
Детоксикация аммиака в организме осуществляется преимущественно в митохондриях перипортальных гепатоцитов за счет связывания в орнитиновом цикле с аминокислотами и образованием нетоксичной мочевины (рис. 1). Частично детоксикация аммиака происходит в мышечной ткани в процессе синтеза глутамина при участии фермента глутаминсинтетазы. Эта реакция с меньшей интенсивностью протекает также в астроцитах головного мозга и перивенозных гепатоцитах печени. Образующийся в результате этих превращений глутамин нетоксичен и выделяется с мочой.
Таким образом, являясь основным источником аммиака, печень в то же время служит главным местом его обезвреживания. Именно поэтому гипераммониемия развивается в организме человека, прежде всего при хронических заболеваниях печени (ХЗП). К причинам этого относятся снижение активности орнитинового цикла и глутаминсинтетазной реакции при печеночно-клеточной недостаточности и порто-системное шунтирование при развитии и прогрессировании портальной гипертензии.
Значительно реже в рутинной клинической практике встречаются генетически детерминированные ферментопатии, которые сопровождаются повышением концентрации аммиака в сыворотке крови. В зависимости от дефицита или дефекта того или иного фермента выделяют несколько видов генетических заболеваний: гипераммониемию типа I (в основе – дефект карбамоилфосфатсинтетазы I), гипераммониемию типа II (в основе – дефект орнитинкарбамоилтрансферазы), цитруллинемию (в основе – дефект аргининосукцинатсинтетазы), аргининосукцинатурию (в основе – дефект аргининосукцинатлиазы), гипераргининемию (в основе – дефицит аргиназы).
Известно, что аммиак является одним из важнейших нейротоксических метаболитов в организме человека. В клинической практике наиболее частым проявлением гипераммониемии является печеночная энцефалопатия (ПЭ) при патологии печени, представляющая собой спектр нервно-психических расстройств на фоне острой или хронической печеночно-клеточной недостаточности и/или портосистемном шунтировании крови. В основе патогенеза ПЭ лежит дисбаланс аминокислот в головном мозге, приводящий к отеку астроглии и нарушениям ее функций, таких как изменения постсинаптических рецепторов и процессов нейротрансмиссии, нарушение проницаемости гематоэнцефалического барьера, снижение энергетического обеспечения нейронов. Степень клинических проявлений напрямую коррелирует с уровнем аммиака в сыворотке крови. В зависимости от выраженности нарушений деятельности головного мозга выделяют четыре степени тяжести печеночной энцефалопатии (от минимальной до комы).
В последние годы в связи с совершенствованием диагностических методик актуально отделение клинически выраженных стадий ПЭ (дезориентация, атаксия, кома) от стадии с минимально выраженными проявлениями (латентная ПЭ). Такую ПЭ можно выявить, используя специальные опросники или метод вызванных потенциалов головного мозга. При этом выявляются когнитивные и психомоторные расстройства, такие как трудности с принятием решений, снижение скорости психомоторных реакций и др. К клиническим симптомам латентной ПЭ относятся повышенная утомляемость, слабость, раздражительность, инверсия сна (сонливость днем и бессонница ночью), нарушения речи, изменения почерка, рассеянность за рулем и при выполнении работы, требующей повышенной концентрации внимания, тремор, снижение мышечных рефлексов.
К сожалению, результатом таких нарушений могут стать серьезные дорожно-транспортные происшествия с тяжелыми последствиями [1, 2]. В связи с этим выявление минимальной ПЭ имеет большое значение для работников многих профессий: водителей автотранспорта, операторов на автоматизированном оборудовании и др.
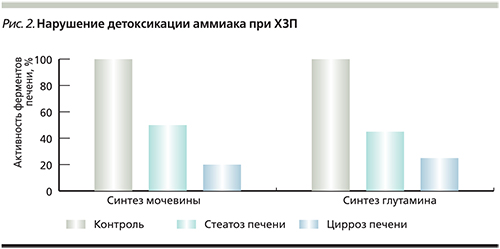
В исследованиях показано, что у больных стеатозом печени при отсутствии клинических признаков воспаления и печеночно-клеточной недостаточности уже имеется выраженное снижение детоксикации аммиака по обоим путям (уменьшается синтез и мочевины, и глутамина) за счет выраженного снижения активности соответствующих ферментов в печени (рис. 2).
В 2016 г. ученые из Великобритании получили новые научные данные, свидетельствующие о том, что гипераммониемия активирует звездчатые клетки печени (ЗКП) и как следствие – может приводить к усиленному коллагенообразованию и прогрессирующему фиброзированию [3].
Известно, что ЗКП являются основными профиброгенными клетками органа. Хроническое повреждение печени под влиянием различных этиологических факторов (алкоголь, вирусная инфекция, лекарства, холестаз и др.) способствует их активации и дифференцировке в миофибробластоподобные клетки, которые приобретают сократительные, провоспалительные и фиброгенетические свойства. При этом ЗКП пролиферируют, из них исчезают капли жира, увеличивается шероховатая эндоплазматическая сеть, в них появляется специфический белок гладких мышц (α-актин), увеличивается количество рецепторов к цитокинам, стимулирующим пролиферацию и фиброгенез.
К факторам, активирующим ЗКП, относятся трансформирующий фактор роста (TGF-β1 – Transforming growth factor beta), тромбоцитарный фактор роста (PDGF – Platelet-derived growth factor), фактор роста фибробластов, интерлейкин-1 (ИЛ-1), эпидермальный фактор роста, фактор некроза опухоли α. Среди всех факторов роста TGF-β1 позиционируется как ключевой медиатор в фиброгенезе у человека. Различные способы, воздействующие на синтез этого фактора или на сигнальные пути, которые реализуются с участием этого фактора, значимо снижают фиброз в экспериментальных моделях [4].
Активированные ЗКП мигрируют и аккумулируются в месте поражения ткани печени, при этом секретируя большое количество внеклеточного матрикса и одновременно регулируя деградацию этих молекул на уровнях транскрипции и посттранскрипции. Повышение содержания информационной коллагеновой РНК является опосредующим фактором, повышающим синтез коллагена активированными ЗКП. В этих клетках посттранскрипционная регуляция коллагена осуществляется путем последовательности 3-го нетранслируемого региона РНК-связующего протеина aСР2, равно как и посредством структуры в 5-м окончании коллагена информационной РНК. Кроме этого ЗКП экспрессируют большое количество нейроэндокринных маркеров (реелин, нестин, нейротрофины, синаптофизин и глиально-фибриллярные кислотные протеины), а также несут рецепторы нейротрансмиттеров, выделяют провоспалительные цитокины, нейрофильный и моноцитарный хемоаттрактаны, которые усиливают воспалительную реакцию в пораженной печени [5].
Фиброз печени является основным, этиологически независимым путем прогрессирования хронических диффузных заболеваний печени вплоть до цирроза. Печеночный фиброз ассоциируется с изменением количества и качественного состава экстрацеллюлярного коллагенового матрикса (ЭКМ). При выраженных стадиях фиброза печень содержит приблизительно в 6 раз больше ЭКМ, чем в норме, а в его составе определяются коллагены (1-го, 3 и 4-го типов), фибронектин, ундулин, эластин, ламинин, гиалуронан и протеогликаны. Снижение скорости резорбции ЭКМ и выведение молекул металлопротеиназ являются в основном следствием перевысвобождения их специфических ингибиторов (TIMPs – tissue inhibitors of metalloproteinases). Результатом превалирования процессов образования внеклеточного матрикса над его разрушением является формирование фиброзного рубца, при этом фиброз на ранних стадиях развития – процесс обратимый, а цирроз с характерными сшивками между коллагеновыми волокнами и узлами регенерации необратим. Прогрессирующее накопление и отложение внеклеточного матрикса в пространстве Диссе приводят к исчезновению фенестров эндотелия, капилляризации и стенозированию синусоидов с постепенным развитием портальной гипертензии [6–8].
In vitro показано, что аммиак дозозависимо снижает клеточную пролиферацию и метаболизм в первичных человеческих ЗКП, но не вызывает гибели клеток.
Длительная обработка клеток аммиаком (до 72 часов) индуцирует развитие и прогрессирование эндоретикулярного стресса в hHSCs, что проявлялось выраженным перинуклеарным накоплением красителя (ER-Tracker™ Red) и появлением цитоплазматических вакуолей по мере роста концентрации аммиака. Использование Image IT™-набора для определения зеленых активных форм кислорода позволило исследователям выявить аммиак-дозозависимое образование активных радикалов кислорода (ROS – Reactive oxygen species) в hHSCs. Таким образом, установлено, что увеличение концентрации аммиака и время его воздействия напрямую влияют на уровни мРНК экспрессии маркеров стресса [3].
Исследование также показало, что при повышенных концентрациях аммиака hHSCs приобретают выраженный профиброгенный и провоспалительный потенциал, что подтверждается результатами исследования in vitro:
- аммиак значительно увеличивает экспрессию белка α-SMA, являющегося активатором ЗКП, а при уровне аммиака 300 мкМ увеличивается синтез виментина – важного промежуточного филамента;
- возрастание концентраций аммиака сопровождается увеличением уровней миозина IIa (играющего ключевую роль в сокращении HSC), миозина IIb (важный фактор активации HSC); экспрессией p38 MAPK, ростом уровней PDGF-Rβ и коллагена I типа;
- повышение уровней аммиака индуцирует сильный и значимый рост мРНК экспрессии металлопротеиназ-2, в то время как мРНК-экспрессия TIMP1 снижается;
- при обработке hHSC аммиаком в концентрации 300 мкМ на протяжении 72 часов мРНК значительно возрастает экспрессия провоспалительного ИЛ-1β;
- аммиак в дозах 50 и 100 мкМ значительно увеличивает в hHSC мРНК- экспрессию ИЛ-6, но не изменяет мРНК-экспрессию ИЛ-8.
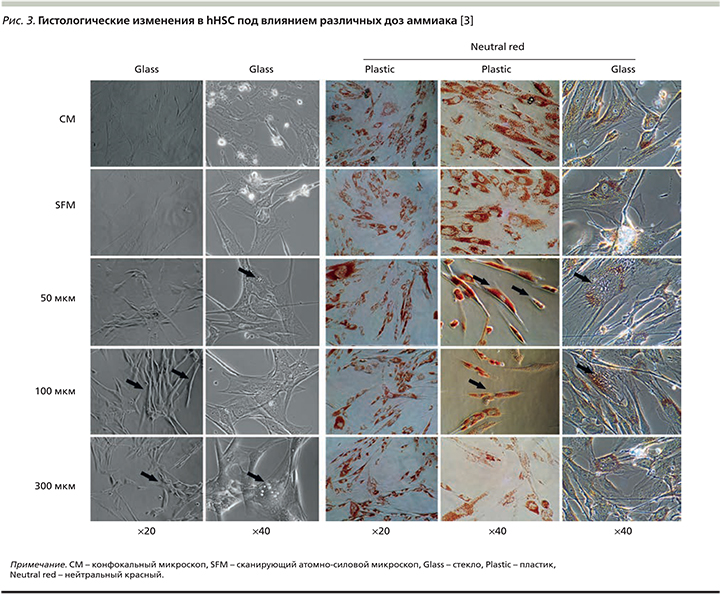
При гистологическом изучении клеток установлено, что аммиак дозозависимо вызывает серьезные морфологические изменения. Так, при световой микроскопии и в тесте жизнеспособности с нейтральным красным (20х, 40х) наблюдали превращение миофибробластоподобных клеток в веретеноподобные фибробласты под действием повышенных концентраций аммиака (рис. 3). Электронная микроскопия показала изменения структуры цитоскелета клеток с образованием цитоплазматических вакуолей при гипераммониемии, однако эти изменения быстро регрессировали после помещения клеток в безаммиачную среду [3].
Вторая часть исследования была проведена на самцах крыс, которые были разделены на три группы: в двух группах проведено перевязывание общего желчного протока (BDL – экспериментальная модель холестаза) с целью формирования экспериментального повреждения печени, при этом крысам одной из групп вводился орнитин (ОР), второй – физиологический раствор. Третья группа животных была контрольной, без повреждения печени.
Анализ результатов опыта показал, что концентрации аммиака были значительно увеличены в плазме крыс с BDL по сравнению с контролем (182±12,8 против 62,51±6,2 мкМ; p
1. Bajaj J.S., Pinkerton S.D., Sanyal A.J., Heuman D.M. Diagnosis and treatment of minimal hepatic encephalopathy to prevent motor vehicle accidents: a cost-effectiveness analysis. Hepatology. 2012;55(4):1164–71.
2. Богомолов П.О., Буеверов А.О., Уварова О.В., Мациевич М.В. Гипераммониемия у пациентов с заболеваниями печени на доцирротической стадии: возможно ли это? Клин. перспективы гастроэнтерол., гепатол. 2013;5:3–8.
3. Джалан Р., Де Чиара Ф., Баласубраманиян В., Андреола Ф., Кхетан В., Малаго М., Пинзани М., Мукерджи Р.П., Ромбоутс К. Аммиак приводит к патологическим изменениям в звездчатых клетках печени, и является целью при лечении портальной гипертензии. Журн. гепатологии. 2016;64:823–33.
4. Gressner A.M., Weiskirchen R., Breitkopf K., Dooley S. Roles of TGF-beta in hepatic fibrosis. Front. Biosci. 2002;7:d793–d807.
5. Lindquist J.N., Parsons C.J., Stefanovic B., Brenner D.A. Regulation of alpha1(I) collagen messenger RNA decay by interactions with alphaCP at the 3?-untranslated region. J. Biol. Chem. 2004;279:23822–29.
6. Benyon R.C., Iredale J.P. Is liver fibrosis reversible? Gut. 2000;46:443–46.
7. Arthur M.J. Fibrogenesis II. Metalloproteinases and their inhibitors in liver fibrosis. Am. J. Physiol. Gastrointest. Liver Physiol. 2000;279:G245–G249.
8. Arthur M.J. Reversibility of liver fibrosis and cirrhosis following treatment for hepatitis C. Gastroenterology. 2002;122:1525–28.
10. Бурков С.Г., Арутюнов А.Г., Годунова С.А., Гурова Н.Ю., Егорова Н.В., Должикова Т.А., Шиковная Ю.Н. Эффективность гранул L-орнитин-L-аспартата в лечении неалкогольной жировой болезни печени. Consilium Medicum. 2010;12(8):43–7.
11. Осипенко М.Ф., Редькина А.В., Бикбулатова Е.А., Моисеенко Е.Е., Скалинская М.А., Казакова Е.А. Оценка L-орнитин-Lаспартата (Гепа-Мерц) в комплексном лечении неалкогольного стеатогепатита. Consilium Medicum. Прил. Гастроэнтерология. 2010;1:35–8.
12. Грюнграйфф К., Ламберт-Бауманн Й. Эффективность гранул L-орнитин-L-аспартата при лечении хронических заболеваний печени. Сучасна гастро-ентерологія. 2008;2:59–67.
13. Ермолов С.Ю., Шабров А.В., Ермолова Т.В. и др. Новые подходы к диагностике и коррекции портопеченочной гемодинамики. Эксперим. и клин. гастроэнтерология. 2007;4:13–6.
14. Ермолова Т.В., Яковлева Д.М. Эффективность применения L-орнитина-L-аспартата у больных стеатогепатитом. Соврем. гастроэнтерология и гепатология. 2012;1:22–6.
В организме человека подвергается распаду около 70 г аминокислот в сутки, при этом в результате реакций дезаминирования и окисления биогенных аминов освобождается большое количество аммиака, являющегося высокотоксичным соединением. Поэтому концентрация аммиака в организме должна сохраняться на низком уровне. Действительно, уровень аммиака в крови в норме не превышает 60 мкмоль/л (это почти в 100 раз меньше концентрации глюкозы в крови). В опытах на кроликах показано, что концентрация аммиака 3 ммоль/л является летальной. Таким образом, аммиак должен подвергаться связыванию в тканях с образованием нетоксичных соединений, легко выделяющихся с мочой.
Один из путей связывания и обезвреживания аммиака в организме, в частности в мозге, сетчатке, почках, печени и мышцах,– это биосинтез глутамина (и, возможно, аспарагина). Глутамин и аспарагин выделяются с мочой в небольшом количестве. Было высказано предположение, что они выполняют скорее транспортную функцию переноса аммиака в нетоксичной форме. Ниже приводится химическая реакция синтеза глутамина, катализируемого глутаминсинтетазой.
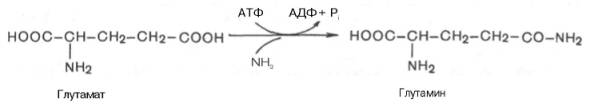
Механизм этой синтетазной реакции, подробно изученный А. Майсте-ром, включает ряд стадий. Синтез глутамина в присутствии глутамин-синтетазы может быть представлен в следующем виде:
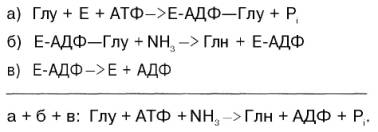
Биосинтез аспарагина протекает несколько отлично и зависит от природы ферментов и донора аммиака. Так, у микроорганизмов и в животных тканях открыта специфическая аммиакзависимая аспарагинсинтетаза, которая катализирует синтез аспарагина в две стадии:
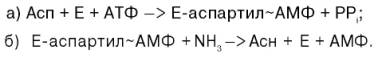
В животных тканях содержится, кроме того, глутаминзависимая аспа-рагинсинтетаза, которая для синтеза во второй стадии использует амидную группу глутамина:
б) Е-аспартил~АМФ + Глн -> Асн + Е + АМФ + Глу.
Суммарная ферментативная реакция синтеза аспарагина может быть представлена в следующем виде:
Асп + АТФ + NН3 (или Глн) –> Асн + АМФ + РРi + (Глу).
Видно, что энергетически синтез аспарагина обходится организму дороже, поскольку образовавшийся РРi далее распадается на ортофосфат.
Часть аммиака легко связывается с α-кетоглутаровой кислотой благодаря обратимости глутаматдегидрогеназной реакции. Если учесть связывание одной молекулы аммиака при синтезе глутамина, то нетрудно видеть, что в организме имеется хорошо функционирующая система, связывающая две молекулы аммиака:
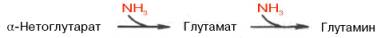
Глутамин, кроме того, используется почками в качестве резервного источника аммиака (образуется из глутамина под действием глутаминазы), необходимого для нейтрализации кислых продуктов обмена при ацидозе и защищающего тем самым организм от потери с мочой используемых для этих целей ионов Na + .
Реферат выполнила студентка 12 группы II курса пед/ф-та Пасько С.П..
Саратовский Государственный Медицинский Университет
Промежуточный обмен аминокислот в тканях.
Промежуточный метаболизм аминокислот белковых молекул, как и других питательных веществ в организме, включает катаболические (распад до конечных продуктов) и анаболические (биосинтез аминокислот) процессы, а также ряд других специфических превращений, сопровождающихся образованием биологически активных веществ. Условно промежуточный метаболизм аминокислот можно разделить на общие пути обмена и индивидуальные превращения отдельных аминокислот.
Общие пути обмена аминокислот.
Общие пути превращения аминокислот включают реакции дезаминирования, трансаминирования, декарбоксилирования, биосинтеза и рацемизации. Реакции рацемизации характерны только для микроорганизмов, физиологическая роль которой заключается в синтезе D-изомеров аминокислот для построения клеточной оболочки.
Дезаминирование ( отщепление аминогруппы) – существует четыре типа реакций, катализируемых своими ферментами:
Восстановительное дезаминорование ( +2H + )
Гидролитическое дезаминированиие (+H 2 О)
Окислительное дезаминирование (+1/2 О 2 )
Во всех случаях NH 2 - группа аминокислоты высвобождается в виде аммиака. Помимо аммиака продуктами дезаминирования являются жирные кислоты, окикислоты и кетокислоты. Для животных тканей, растений и большинства микроорганизмов преобладающим типом реакций является окислительное дезаминирование аминокислот, за исключением гистидина, который подвергается внутримолекулярному дезаминированию.
Кроме перечисленных четырех типов реакций и катализирующих их ферментов в животных тканях и печени человека открыты также три специфических фермента (серин- и треониндегидратазы и цистатионин-γ- лиаза), катализирующих неокислительное дезаминирование серина, треонина и цистеина. Они требуют присутствия пиридоксаль-фосфата в качестве кофермента. Конечными продуктами реакции являются пируват и α- кетобутират, аммиак и сероводород.
Трансаминирование – реакции межмолекулярного переноса аминогруппы (NH 2 ) от аминокислоты на α-кетокислоту без промежуточного образования аммиака (глутамат+ пируват =
α-кетоглутарат + аланин). Впервые эти реакции были открыты в 1937г. А.Е. Браунштейном и М.Г. Крицман. Реакции трансаминирования являются обратимыми и универсальными для всех живых организмов, они протекают при участии специфических ферментов – аминотрансфераз (трансамниназ). Теоретически реакции возможны между любой амино- и кетокислотой, но наиболее интенсивно они протекают, если один из партнеров представлен дикарбоновой амино- или кетокислотой. В переносе амниогруппы активное участие принимает кофермет трансминаз – пиридоксальфосфат (производное витамина В 6 ). Для реакций трансаминирования характерен общий механизм. Ферменты реакции катализируют перенос аминогруппы не на α -кетокислоту, а на кофермент; образовавшееся промежуточное соединение (шиффово основание) подвергается внутримолекулярным превращениям, приводящим к освобождению α-кетокислоты и пиридоксамнофосфата. Последний на втолрой стадии реагирует с любой другой α-кетокислотой, что через те же стадии приводит к синтезу новой аминокислоты и пиридоксальфосфата.
Декарбоксилирование - отщепление карбоксильной группы в виде СО 2 , образующиеся продукты реакции называются биогенными аминами, они оказывают сильное фармакологическое действие на множество функций. Эти реакции являются необратимыми, они катализируютя специфическими ферментами – декарбоксилазами аминокмлот- которые в качестве кофермента содержат пиридоксальфосфат ( кроме гистидиндекарбоксилазы и аденозилдекарбоксилазы – содержат остаток пировиноградной кислоты в качестве кофермента). В живых организмах открыты четыре типа декарбоксилирования аминокислот.
α-декарбоксилирование – характерно для тканей животных: от аминокислот отщепляется соседняя от α-углеродного атома карбоксильная группа.
ω-декарбоксилирование- свойственно микроорганизмам
декарбоксилирование, связанное с реакцией трансаминирования. Образуется альдегид и новая аминокислота, соответствующая исходной кетокислоте.
Декарбоксилирование, связанное с реакцией конденсацией двух молекул:
Обезвреживание аммиака в организме.
В организме человека подвергается распаду около 70г аминокислот в сутки: при этом освобождается большое количество аммиака, являющегося высокотоксичным соединением. Поэтому крнцентрация аммиака должна сохраняться на низком уровне (в норме уровень его не превышает 60 мкмоль/л). Концентрация аммиака 3 ммоль/л является летальной.
Одним из путей связывания и обезвреживания аммиака в мозге, сетчатке, почках и мышцах, является биосинтез глутамина( и, возможно, аспарагина). Поскольку глутамин и аспарагин с мочой выделяются в небольших количествах, было высказано предположение, что они выполняют скорее транспортную функцию переноса аммиака в нетоксичной форме.
Часть аммиака легко связывается с α-кетоглутаровой кислотой благодаря обратимости глутаматдегидрогеназной реакции; при синтезе глутамина связывается ещё 1 молекула, т.о. нейтрализуются две молекулы аммиака:
Орнитиновый цикл мочевинообразования.
Основным механизмом обезвреживания аммиака в организме является биосинтез мочевины (в основном,в печени).Она выводится с мочой в качестве главного конечного продукта белкового, соответственно аминокислотного, обмена. На долю мочевины приходится до 80-85% всего азота мочи. Реакции синтеза мочевины, представлены в виде цикла, получившего название орнитинового цикла мочевинообразования Кребса.
На первом этапе синтезируется макроэргическое соединение карбамоилфосфат – это метаболически активная форма аммиака, используемая в качестве исходного продукта для синтеза ряда других азотистых соединений.
На втором этапе цикла мочевинообразования происходит конденсация карбамоилфосфата и орнитина с образованием
цитруллина; реакцию катализирует орнитинкарбамоилтрансфераза:
На следующей стадии цитруллин превращается в аргинин в результате двух последовательно протекающих реакций. Первая из них, энергозависимая, сводится к конденсации цитруллина и аспаргиновой кислоты с образованием аргининосукцината ( эту реакцию катализирует аргининосукцинат-синтетаза). Аргининсукцинат распадается во второй реакции на аргинин и фумарат поддействием аргининосукцинат-лиазы.
На последнем этапе аргинин расщепляется на мочевину и орнитин под действием аргиназы. Суммарная реакция синтеза мочевины без учёта промежуточных продуктов:
Это энергетически выгодная реакция, поэтому процесс всегда протекает в направлении синтеза мочевины.
В состоянии азотистого равновесия организм человека потребляет и соответственно выделяет примерно 15 г азота в сутки; из экскретируемого с мочой количества азота на долю мочевины приходится около 85% , креатинина-около 5%, аммонийных солей – 3%, мочевой кислоты-1% и на другие формы-около 6%.
Типы азотистого обмена. А м м о н и о т е л и ч е с к и й т и п , при котором главным конечным продуктом азотистого обмена является аммиак, свойствен рыбам. У р е о т е л и ч е с к и й т и п обмена - основным конечным продуктом обмена белков является мочевина, характерен для человека и животных. У р и к о т е л и ч е с к и й т и п - главным конечным продуктом обмена является мочевая кислота, характерен для птиц и рептилий.
Катаболизм аминокислот в тканях происходит постоянно со скоростью -100 г/сут. При этом в результате дезаминирования аминокислот освобождается большое количество аммиака. Значительно меньшие количества его образуются при дезаминировании биогенных аминов и нуклеотидов. Основные источники аммиака в клетках представлены в табл. 9-3.
Таблица 9-3.
Основные источники аммиака

Часть аммиака образуется в кишечнике в результате действия бактерий на пищевые белки (пше-ние белков в кишечнике) и поступает в кровь воротной вены. Концентрация аммиака в крови воротной вены существенно больше, чем в общем кровотоке. В печени задерживается большое количество аммиака, что поддерживает низкое содержание его в крови. Концентрация аммиака в крови в норме редко превышает 0,4—0,7 мг/л (или 25—40 мкмоль/л). В крови и цитозоле клеток при физиологических значениях pH аммиак переходит в ион аммония — NH4 + , количество неионизированного NH3 невелико (~ 1%).

Аммиак — токсичное соединение. Даже небольшое повышение его концентрации оказывает неблагоприятное действие на организм, и прежде всего на ЦНС. Так, повышение концентрации аммиака в мозге до 0,6 ммоль вызывает судороги. К симптомам гипераммониемии относят тремор, нечленораздельную речь, тошноту, рвоту, головокружение, судорожные припадки, потерю сознания. В тяжёлых случаях развивается кома с летальным исходом.
- Аммиак легко проникает через мембраны в клетки и в митохондриях сдвигает реакцию, катализируемую глутаматдегидрогеназой, в сторону образования глутамата:
α -Кетоглутарат + NADH + Н + + NH3 ⇒ Глутамат + NAD + .
- угнетение обмена аминокислот (реакции трансаминирования) и, следовательно, синтеза из них нейромедиаторов (ацетилхолина, дофамина и др.);
- гипоэнергетическое состояние в результате снижения скорости ЦТК.
- Повышение концентрации аммиака в крови сдвигает pH в щелочную сторону (вызывает алкалоз). Это, в свою очередь, увеличивает сродство гемоглобина к кислороду, что приводит к гипоксии тканей, накоплению СO2 и гипоэнергетическому состоянию, от которого главным образом страдает головной мозг.
- Высокие концентрации аммиака стимулируют синтез глутамина из глутамата в нервной ткани (при участии глутаминсинтетазы):
- Ион NH4 + практически не проникает через цитоплазматические и митохондриальные мембраны. Избыток иона аммония в крови способен нарушать трансмембранный перенос одновалентных катионов Na + и К + , конкурируя с ними за ионные каналы, что также влияет на проведение нервных импульсов.
Б. Связывание (обезвреживание) аммиака
Высокая интенсивность процессов дезаминирования аминокислот в тканях и очень низкий уровень аммиака в крови свидетельствуют о том, что в клетках активно происходит связывание аммиака с образованием нетоксичных соединений, которые выводятся из организма с мочой. Эти реакции можно считать реакциями обезвреживания аммиака. В разных тканях и органах обнаружено несколько типов таких реакций.
Основной реакцией связывания аммиака, протекающей во всех тканях организма, является синтез глутамина под действием глутаминсинтетазы:

Глутаминсинтетаза локализована в митохондриях клеток, для работы фермента необходим кофактор — ионы Mg 2+ Глутаминсинтетаза — один из основных регуляторных ферментов обмена аминокислот и аллостерически ингибируется АМФ, глюкозо-6-фосфатом, а также Гли, Ала и Гис.
Глутамин легко транспортируется через клеточные мембраны путём облегчённой диффузии (для глутамата возможен только активный транспорт) и поступает из тканей в кровь. Основными тканями-поставщиками глутамина служат мышцы, мозг и печень. С током крови глутамин транспортируется в кишечник и почки.
В клетках кишечника под действием фермента глутаминазы происходит гидролитическое освобождение амидного азота в виде аммиака:

Образовавшийся в реакции глутамат подвергается трансаминированию с пируватом. а-Аминогруппа глутаминовой кислоты переносится в состав аланина (рис. 9-10). Большие количества аланина поступают из кишечника в кровь воротной вены и поглощаются печенью. Около 5% образовавшегося аммиака удаляется в составе фекалий, небольшая часть через воротную вену попадает в печень, остальные ~90% выводятся почками.

Рис. 9-10. Метаболизм азота глутамина в кишечнике
В почках также происходит гидролиз глутамина под действием глутаминазы с образованием аммиака. Этот процесс является одним из механизмов регуляции кислотно-щелочного равновесия в организме и сохранения важнейших катионов для поддержания осмотического давления. Глутаминаза почек значительно индуцируется при ацидозе, образующийся аммиак нейтрализует кислые продукты обмена и в виде аммонийных солей экскретируется с мочой (рис. 9-11). Эта реакция защищает организм от излишней потери ионов Na+ и К+, которые также могут использоваться для выведения анионов и утрачиваться. При алкалозе количество глутаминазы в почках снижается.

Рис. 9-11. Метаболизм амидного азота глутамина в почках
В почках образуется и выводится около 0,5 г солей аммония в сутки.
Высокий уровень глутамина в крови и лёгкость его поступления в клетки обусловливают использование глутамина во многих анаболических процессах. Глутамин — основной донор азота в организме. Амидный азот глутамина используется гпя синтеза пуриновых и пиримидиновых нуклеотидов, аспарагина, аминосаха-ров и других соединений (рис. 9-12).

Рис. 9-12. Пути использования глутамина в организме
Ещё одной реакцией обезвреживания аммиака в тканях можно считать синтез аспарагина под действием аспарагинсинтетазы.
В мозге и некоторых других органах может протекать восстановительное аминирование α -кетоглутарата под действием глутаматдегидрогеназы, катализирующей обратимую реакцию. Однако этот путь обезвреживания аммиака в тканях используется слабо, так как глутаматдегидрогеназа катализирует преимущественно реакцию дезаминирования глутамата. Хотя, если учитывать последующее образование глутамина, реакция выгодна для клеток, так как способствует связыванию сразу 2 молекул NH3.
Существуют 2 изоформы этого фермента — глутаминзависимая и аммиакзависимая, которые используют разные доноры амидных групп. Первая функционирует в животных клетках, вторая преобладает в бактериальных клетках, но присутствует и у животных. Однако такой путь обезвреживания аммиака в клетках человека используется редко и к тому же требует больших энергетических затрат (энергию двух макроэргических связей), чем синтез глутамина.
Наиболее значительные количества аммиака обезвреживаются в печени путём синтеза мочевины. В первой реакции процесса аммиак связывается с диоксидом углерода с образованием карба-моилфосфата, при этом затрачиваются 2 молекулы АТФ. Реакция происходит в митохондриях гепатоцитов под действием фермента карбамоилфос-фатсинтетазы I. Карбамоилфосфатсинтетаза II локализована в цитозоле клеток всех тканей и участвует в синтезе пиримидиновых нуклеотидов (см. раздел 10). Карбамоилфосфат затем включается в орнитиновый цикл и используется для синтеза мочевины.
Из мышц и кишечника избыток аммиака выводится преимущественно в виде аланина. Этот механизм необходим, так как активность глутаматдегидрогеназы в мышцах невелика и непрямое дезаминирование аминокислот малоэффективно. Поэтому в мышцах существует ещё один путь выведения азота. Образование аланина в этих органах можно представить следующей схемой (см. схему).
Схема

Аминогруппы разных аминокислот посредством реакций трансаминирования переносятся на пируват, основным источником которого служит процесс окисления глюкозы.
Мышцы выделяют особенно много аланина в силу их большой массы, активного потребления глюкозы при физической работе, а также потому, что часть энергии они получают за счёт распада аминокислот. Образовавшийся аланин поступает в печень, где подвергается непрямому дезаминированию. Выделившийся аммиак обезвреживается, а пируват включается в глюконеогенез. Глюкоза из печени поступает в ткани и там, в процессе гликолиза, опять окисляется до пирувата (рис. 9-13).
Рис. 9-13. Глюкозо-аланиновый цикл
Образование аланина в мышцах, его перенос в печень и перенос глюкозы, синтезированной в печени, обратно в мышцы составляют глюкозо-аланиновый цикл, работа которого сопряжена с работой глюкозо-лакгатного цикла (см. раздел 7).
Совокупность основных процессов обмена аммиака в организме представлена на рис. 9-14. Доминирующими ферментами в обмене аммиака служат глутаматдегидрогеназа и глутаминсинтетаза.

Рис. 9-14. Обмен аммиака. Основной источник аммиака — аминокислоты. Большая часть образовавшегося аммиака обезвреживается в орнитиновом цикле в печени и выделяется в виде мочевины. Основной реакцией обезвреживания аммиака в тканях является синтез глутамина, который затем используется в анаболических процессах и для обезвреживания веществ в печени. Ферменты глутаматдегидрогеназа и глутаминсинтетаза являются регуляторными и обусловливают скорость процессов образования и обезвреживания аммиака
Читайте также:

