Применение кальция кратко биология
Обновлено: 02.07.2024
Природный кальций состоит из смеси нуклидов с массовыми числами 40 (в смеси по массе 96, 94 %), 44 (2, 09%), 42 (0, 667%), 48 (0, 187%), 43 (0, 135%) и 46 (0, 003%). Конфигурация внешнего электронного слоя 4s 2 . Практически во всех соединениях степень окисления кальция +2 (валентность II).
Радиус нейтрального атома кальция 0, 1974 нм, радиус иона Cа 2+ от 0, 114 нм (для координационного числа 6) до 0, 148 нм (для координационного числа 12). Энергии последовательной ионизации нейтрального атома кальция равны, соответственно, 6, 133, 11, 872, 50, 91, 67, 27 и 84, 5 эВ. По шкале Полинга электроотрицательность кальция около 1, 0. В свободном виде кальций — серебристо-белый металл.
История открытия
Нахождение в природе
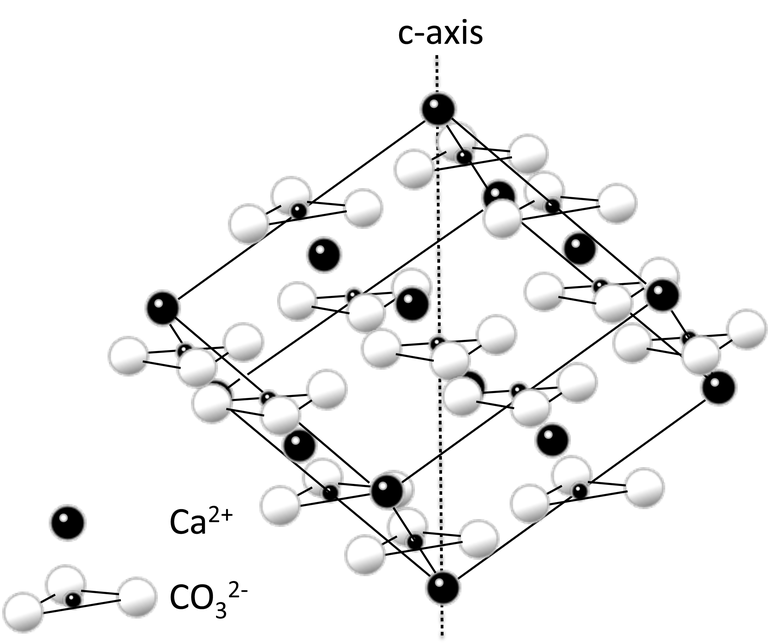
Кальций — один из наиболее распространенных на Земле элементов. На его долю приходится 3, 38% массы земной коры (5-е место по распространенности после кислорода, кремния, алюминия и железа). Из-за высокой химической активности кальций в свободном виде в природе не встречается. Большая часть кальция содержится в составе силикатов и алюмосиликатов различных горных пород (граниты, гнейсы и т. п.). В виде осадочных пород соединения кальция представлены мелом и известняками, состоящими в основном из минерала кальцита (CaCO3). Кристаллическая форма кальцита — мрамор — встречается в природе гораздо реже.
Довольно широко распространены такие минералы кальция, как известняк СaCO3, ангидрит CaSO4 и гипс CaSO4·2H2O, флюорит CaF2, апатиты Ca5(PO4)3(F, Cl, OH), доломит MgCO3·СaCO3. Присутствием солей кальция и магния в природной воде определяется ее жесткость. Значительное количество кальция входит в состав живых организмов. Так, гидроксилапатит Ca5(PO4)3(OH), или, в другой записи, 3Ca3(PO4)2 ·Са(OH)2 — основа костной ткани позвоночных, в том числе и человека; из карбоната кальция CaCO3 состоят раковины и панцири многих беспозвоночных, яичная скорлупа и др.
Получение
Металлический кальций получают электролизом расплава, состоящего из CaCl2 (75-80%) и KCl или из CaCl2 и CaF2, а также алюминотермическим восстановлением CaO при 1170-1200 °C:
Физические и химические свойства
Металл кальций существует в двух аллотропных модификациях (см. Аллотропия). До 443 °C устойчив α-Ca с кубической гранецентрированной решеткой (параметр а = 0, 558 нм), выше устойчив β-Ca с кубической объемно центрированной решеткой типа α-Fe (параметр a = 0, 448 нм). Температура плавления кальция 839 °C, температура кипения 1484 °C, плотность 1, 55 г/см 3 .
Химическая активность кальция высока, но ниже, чем всех других щелочноземельных металлов. Он легко взаимодействует с кислородом, углекислым газом и влагой воздуха, из-за чего поверхность металлического кальция обычно тускло серая, поэтому в лаборатории кальций обычно хранят, как и другие щелочноземельные металлы, в плотно закрытой банке под слоем керосина.
В ряду стандартных потенциалов кальций расположен слева от водорода. Стандартный электродный потенциал пары Ca 2+ /Ca 0 –2, 84 В, так что кальций активно реагирует с водой:
При нагревании на воздухе или в кислороде кальций воспламеняется. С менее активными неметаллами (водородом, бором, углеродом, кремнием, азотом, фосфором и другими) кальций вступает во взаимодействие при нагревании, например:
Протекание указанных выше реакций, как правило, сопровождается выделением большого количества теплоты (т. е. эти реакции — экзотермические). Во всех соединениях с неметаллами степень окисления кальция +2. Большинство из соединений кальция с неметаллами легко разлагается водой, например:
Оксид кальция — типично основной. В лаборатории и технике его получают термическим разложением карбонатов:
Полученный таким способом Ca(ОН)2 обычно называют гашеной известью или известковым молоком из-за того, что растворимость гидроксида кальция в воде невелика (0, 02 моль/л при 20°C), и при внесении его в воду образуется белая суспензия.
Такие соли кальция, как хлорид CaCl2, бромид CaBr2, иодид CaI2 и нитрат Ca(NO3)2, хорошо растворимы в воде. Нерастворимы в воде фторид CaF2, карбонат CaCO3, сульфат CaSO4, средний ортофосфат Ca3(PO4)2, оксалат СаС2О4 и некоторые другие.
Важное значение имеет то обстоятельство, что в отличие от среднего карбоната кальция СаСО3 кислый карбонат кальция (гидрокарбонат) Са(НСО3)2 в воде растворим. В природе это приводит к следующим процессам. Когда холодная дождевая или речная вода, насыщенная углекислым газом, проникает под землю и попадает на известняки, то наблюдается их растворение:
В тех же местах, где вода, насыщенная гидрокарбонатом кальция, выходит на поверхность земли и нагревается солнечными лучами, протекает обратная реакция:
Наличие в воде растворенного гидрокарбоната кальция во многом определяет временную жесткость воды. Временной ее называют потому, что при кипячении воды гидрокарбонат разлагается, и в осадок выпадает СаСО3. Это явление приводит, например, к тому, что в чайнике со временем образуется накипь.
Применение кальция и его соединений
Металлический кальций применяют для металлотермического получения урана, тория, титана, циркония, цезия и рубидия.
Природные соединения кальция широко используют в производстве вяжущих материалов (цемент, гипс, известь и др.). Связывающее действие гашеной извести основано на том, что с течением времени гидроксид кальция реагирует с углекислым газом воздуха. В результате протекающей реакции образуются игольчатые кристаллы кальцита СаСОз, которые прорастают в расположенные рядом камни, кирпичи, другие строительные материалы и как бы сваривают их в единое целое. Кристаллический карбонат кальция — мрамор — прекрасный отделочный материал. Мел используют для побелки. Большие количества известняка расходуются при производстве чугуна, так как позволяют перевести тугоплавкие примеси железной руды (например, кварц SiO2) в сравнительно легкоплавкие шлаки.
Хлорид кальция CaCl2 используют наряду с поваренной солью для борьбы с оледенением дорожных покрытий. Фторид кальция СаF2 — прекрасный оптический материал.
Кальций в живых организмах
Кальций — биогенный элемент, постоянно присутствующий в тканях растений и животных. Важный компонент минерального обмена животных и человека и минерального питания растений, кальций выполняет в организме разнообразные функции. В составе апатита, а также сульфата и карбоната кальций образует минеральный компонент костной ткани. В организме человека массой 70 кг содержится около 1 кг кальция. Кальций участвует в работе ионных каналов, осуществляющих транспорт веществ через биологические мембраны, в передаче нервного импульса, в процессах свертывания крови и оплодотворения. Регулируют обмен кальция в организме кальциферолы (витамин D).
Недостаток кальция в организме в младенчестве может привести к заболеванию рахитом, а в зрелом возрасте — к остеопорозу. Избыток кальция может вызвать гиперкальцемию и привести к заболеванию кальцинозом. Поэтому пища человека должна в нужных количествах содержать соединения кальция (600-1500 мг кальция в сутки в зависимости от возраста). Содержание кальция высоко, в некоторых семенах и плодах растений и других продуктах питания, и относительно высоко в молочных продуктах (таких, как творог, сыр, молоко). Препараты кальция широко используются в медицине.
Продукты, содержащие кальций и нормы его потребления
Мак
Семена кунжута
Твердые сыры
Крапива
Сардины в масле
Подорожник
Семена подсолнечника
Базилик
Плоды шиповника
Миндаль
Петрушка
Лесной орех
Семя амаранта
Листья кресс-салата
Фасоль
Молоко коровье
Творог обезжиренный
1460
670 – 1000
800 – 1200
713
400 – 450
412
250 – 300
370
257
250 – 270
245
225
214
180 – 200
180 – 200
120
100– 120
Потребность в кальции зависит от возраста. Рекомендуемые Всемирной организацией здравоохранения (ВОЗ) суточные нормы потребления кальция составляют:

Кальций (Ca от лат. Calcium ) — элемент второй группы (по старой классификации — главной подгруппы второй группы), четвёртого периода, с атомным номером 20. Простое вещество кальций — мягкий, химически активный щёлочноземельный металл серебристо-белого цвета. Впервые получен в чистом виде Г. Дэви в 1808 году.
Содержание
- 1 История и происхождение названия
- 2 Нахождение в природе
- 2.1 Изотопы
- 2.2 В горных породах и минералах
- 2.3 Миграция в земной коре
- 2.4 В биосфере
![Кальций]()
История и происхождение названия
Соединения кальция — известняк, мрамор, гипс (а также известь — продукт обжига известняка) применялись в строительном деле уже несколько тысячелетий назад. Вплоть до конца XVIII века химики считали известь простым телом. В 1789 году А. Лавуазье предположил, что известь, магнезия, барит, глинозём и кремнезём — вещества сложные.
Нахождение в природе
Из-за высокой химической активности кальций в свободном виде в природе не встречается.
На долю кальция приходится 3,38 % массы земной коры (5-е место по распространенности (3-е среди металлов) после кислорода, кремния, алюминия и железа). Содержание элемента в морской воде — 400 мг/л .
Изотопы
Кальций встречается в природе в виде смеси шести изотопов: 40 Ca, 42 Ca, 43 Ca, 44 Ca, 46 Ca и 48 Ca, среди которых наиболее распространённый — 40 Ca — составляет 96,97 %. Ядра кальция содержат магическое число протонов: Z = 20 . Изотопы 40
20 Ca 20
и 48
20 Ca 28
являются двумя из пяти существующих в природе дважды магических ядер.Из шести природных изотопов кальция пять стабильны. Шестой изотоп 48 Ca, самый тяжёлый из шести и весьма редкий (его изотопная распространённость равна всего 0,187 %), испытывает двойной бета-распад с периодом полураспада (4,39 ± 0,58)⋅10 19 лет .
В горных породах и минералах
Кальций, энергично мигрирующий в земной коре и накапливающийся в различных геохимических системах, образует 385 минералов (четвёртое место по числу минералов).
Большая часть кальция содержится в составе силикатов и алюмосиликатов различных горных пород (граниты, гнейсы и т. п.), особенно в полевом шпате — анортите Ca[Al2Si2O8].
![Кальций]()
Довольно широко распространены такие минералы кальция, как кальцит CaCO3, ангидрит CaSO4, алебастр CaSO4·0.5H2O и гипс CaSO4·2H2O, флюорит CaF2, апатиты Ca5(PO4)3(F,Cl,OH), доломит MgCO3·CaCO3. Присутствием солей кальция и магния в природной воде определяется её жёсткость.
Осадочная порода, состоящая в основном из скрытокристаллического кальцита — известняк (одна из его разновидностей — мел). Под действием регионального метаморфизма известняк преобразуется в мрамор.
Миграция в земной коре
(равновесие смещается влево или вправо в зависимости от концентрации углекислого газа).
Огромную роль играет биогенная миграция.
В биосфере
Соединения кальция находятся практически во всех животных и растительных тканях (см. ниже). Значительное количество кальция входит в состав живых организмов. Так, гидроксиапатит Ca5(PO4)3OH, или, в другой записи, 3Ca3(PO4)2·Ca(OH)2 — основа костной ткани позвоночных, в том числе и человека; из карбоната кальция CaCO3 состоят раковины и панцири многих беспозвоночных, яичная скорлупа и др. В живых тканях человека и животных 1,4—2 % Ca (по массовой доле); в теле человека массой 70 кг содержание кальция — около 1,7 кг (в основном в составе межклеточного вещества костной ткани).
Получение
Свободный металлический кальций получают электролизом расплава, состоящего из CaCl2 (75—80 %) и KCl или из CaCl2 и CaF2, а также алюминотермическим восстановлением CaO при 1170—1200 °C 4CaO + 2Al → CaAl2O4 + 3Ca
Физические свойства
Металл кальций существует в двух аллотропных модификациях. До 443 °C устойчив α -Ca с кубической гранецентрированной решеткой (параметр а = 0,558 нм ), выше устойчив β -Ca с кубической объемно-центрированной решеткой типа α -Fe (параметр a = 0,448 нм ). Стандартная энтальпия ΔH 0 перехода α → β составляет 0,93 кДж/моль .
При постепенном повышении давления начинает проявлять свойства полупроводника, но не становится полупроводником в полном смысле этого слова (металлом уже тоже не является). При дальнейшем повышении давления возвращается в металлическое состояние и начинает проявлять сверхпроводящие свойства (температура сверхпроводимости в шесть раз выше, чем у ртути, и намного превосходит по проводимости все остальные элементы). Уникальное поведение кальция похоже во многом на стронций (то есть параллели в периодической системе сохраняются).
![Кальций]()
Химические свойства
Кальций — типичный щёлочноземельный металл. Химическая активность кальция высока, но ниже, чем более тяжёлых щёлочноземельных металлов. Он легко взаимодействует с кислородом, углекислым газом и влагой воздуха, из-за чего поверхность металлического кальция обычно тускло-серая, поэтому в лаборатории кальций обычно хранят, как и другие щёлочноземельные металлы, в плотно закрытой банке под слоем керосина или жидкого парафина.
В ряду стандартных потенциалов кальций расположен слева от водорода. Стандартный электродный потенциал пары Ca 2+ /Ca 0 −2,84 В , так что кальций активно реагирует с водой, но без воспламенения:
С активными неметаллами (кислородом, хлором, бромом, йодом) кальций реагирует при обычных условиях:
Кроме получающихся в этих реакциях фосфида кальция Ca3P2 и силицида кальция Ca2Si, известны также фосфиды кальция составов CaP и CaP5 и силициды кальция составов CaSi, Ca3Si4 и CaSi2.
Протекание указанных выше реакций, как правило, сопровождается выделением большого количества теплоты. Во всех соединениях с неметаллами степень окисления кальция +2. Большинство из соединений кальция с неметаллами легко разлагается водой, например:
Ион Ca 2+ бесцветен. При внесении в пламя растворимых солей кальция пламя окрашивается в кирпично-красный цвет.
Такие соли кальция, как хлорид CaCl2, бромид CaBr2, йодид CaI2 и нитрат Ca(NO3)2, хорошо растворимы в воде. Нерастворимы в воде фторид CaF2, карбонат CaCO3, сульфат CaSO4, ортофосфат Ca3(PO4)2, оксалат CaC2O4 и некоторые другие.
Важное значение имеет то обстоятельство, что, в отличие от карбоната кальция CaCO3, кислый карбонат кальция (гидрокарбонат) Ca(HCO3)2 в воде растворим. В природе это приводит к следующим процессам. Когда холодная дождевая или речная вода, насыщенная углекислым газом, проникает под землю и попадает на известняки, то наблюдается их растворение, а в тех местах, где вода, насыщенная гидрокарбонатом кальция, выходит на поверхность земли и нагревается солнечными лучами, протекает обратная реакция
Наличие в воде растворенного гидрокарбоната кальция во многом определяет вре́менную жёсткость воды. Вре́менной её называют потому, что при кипячении воды гидрокарбонат разлагается, и в осадок выпадает CaCO3. Это явление приводит, например, к тому, что в чайнике со временем образуется накипь.
Применение
Главное применение металлического кальция — это использование его как восстановителя при получении металлов, особенно никеля, меди и нержавеющей стали. Кальций и его гидрид используются также для получения трудно восстанавливаемых металлов, таких, как хром, торий и уран. Сплавы кальция со свинцом применяются в некоторых видах аккумуляторных батарей и при производстве подшипников. Кальциевые гранулы используются также для удаления следов воздуха из электровакуумных приборов. Чистый металлический кальций широко применяется в металлотермии при получении редкоземельных элементов.
Кальций широко применяется в металлургии для раскисления стали наряду с алюминием или в сочетании с ним. Внепечная обработка кальцийсодержащими проволоками занимает ведущее положение в связи с многофакторностью влияния кальция на физико-химическое состояние расплава, макро- и микроструктуры металла, качество и свойства металлопродукции и является неотъемлемой частью технологии производства стали. В современной металлургии для ввода в расплав кальция используется инжекционная проволока, представляющая из себя кальций (иногда силикокальций или алюмокальций) в виде порошка или прессованного металла в стальной оболочке. Наряду с раскислением (удалением растворенного в стали кислорода) использование кальция позволяет получить благоприятные по природе, составу и форме неметаллические включения, не разрушающиеся в ходе дальнейших технологических операций.
Изотоп 48 Ca — один из эффективных и употребительных материалов для производства сверхтяжёлых элементов и открытия новых элементов таблицы Менделеева. Это связано с тем, что кальций-48 является дважды магическим ядром, поэтому его устойчивость позволяет ему быть достаточно нейтроноизбыточным для лёгкого ядра; при синтезе сверхтяжёлых ядер необходим избыток нейтронов.
Биологическая роль
Потребность в кальции зависит от возраста. Для взрослых в возрасте 19—50 лет и детей 4—8 лет включительно дневная потребность (RDA) составляет 1000 мг , а для детей в возрасте от 9 до 18 лет включительно — 1300 мг в сутки . В подростковом возрасте потребление достаточного количества кальция очень важно из-за интенсивного роста скелета. Однако по данным исследований в США всего 11 % девочек и 31 % мальчиков в возрасте 12—19 лет достигают своих потребностей. В сбалансированной диете большая часть кальция (около 80 %) поступает в организм ребёнка с молочными продуктами. Оставшийся кальций приходится на зерновые (в том числе цельнозерновой хлеб и гречку), бобовые, апельсины, зелень, орехи. Всасывание кальция в кишечнике происходит двумя способами: через клетки кишечника (трансцеллюлярно) и межклеточно (парацелюллярно). Первый механизм опосредован действием активной формы витамина D (кальцитриола) и её кишечными рецепторами. Он играет большую роль при малом и умеренном потреблении кальция. При большем содержании кальция в диете основную роль начинает играть межклеточная абсорбция, которая связана с большим градиентом концентрации кальция. За счёт чрезклеточного механизма кальций всасывается в большей степени в двенадцатиперстной кишке (из-за наибольшей концентрации там рецепторов в кальцитриолу). За счёт межклеточного пассивного переноса абсорбция кальция наиболее активна во всех трёх отделах тонкого кишечника. Всасыванию кальция парацеллюлярно способствует лактоза (молочный сахар).
Усвоению кальция препятствуют некоторые животные жиры (включая жир коровьего молока и говяжий жир, но не сало) и пальмовое масло. Содержащиеся в таких жирах пальмитиновая и стеариновая жирные кислоты отщепляются при переваривании в кишечнике и в свободном виде прочно связывают кальций, образуя пальмитат кальция и стеарат кальция (нерастворимые мыла). В виде этого мыла со стулом теряется как кальций, так и жир. Этот механизм ответственен за снижение всасывания кальция, снижение минерализации костей и снижение косвенных показателей их прочности у младенцев при использовании детских смесей на основе пальмового масла (пальмового олеина). У таких детей образование кальциевых мыл в кишечнике ассоциируется с уплотнением стула, уменьшением его частоты, а также более частым срыгиванием и коликами.
Концентрация кальция в крови из-за её важности для большого числа жизненно важных процессов точно регулируется, и при правильном питании и достаточном потреблении обезжиренных молочных продуктов и витамина D дефицита не возникает. Длительный дефицит кальция и/или витамина D в диете приводит к увеличению риска остеопороза, а в младенчестве вызывает рахит.
Избыточные дозы кальция и витамина D могут вызвать гиперкальцемию. Максимальная безопасная доза для взрослых в возрасте от 19 до 50 лет включительно составляет 2500 мг в сутки (около 340 г сыра Эдам).
Кальций является структурным макроэлементом, содержание которого превышает по своему содержанию все остальные элементы в организме (кроме элементов-органогенов).
Общее количество кальция у взрослого человека может составлять более одного килограмма.
Практически весь (99%) кальций в организме находится в зубах и костях скелета, и только около 1% - во всех остальных органах, тканях и биологических жидкостях.Биологическая роль кальция
Прежде всего, кальций является важнейшим структурным компонентом костей и зубов.
Также кальций регулирует проницаемость клеточных мембран, а также инициирует ответы клеток на различные внешние стимулы. Присутствие кальция в клетки или во внеклеточной среде обуславливает дифференцировку клетки, а также сокращение мышц, секрецию и перистальтику. Кальций регулирует активность многих ферментов (включая ферменты систем свертывания крови). Кальций регулирует работу некоторых эндокринных желез, обладает десенсибилизирующим и противовоспалительным эффектом.Основные функции кальция в организме:
- структурный компонент костей и зубов
- участвует в мышечных сокращениях
- регулирует проницаемость клеточных мембран
- участвует проводимости сигнала по нервным клеткам
- регулирует сердечную деятельность
- участвует в свертывании крови
Пищевые источники кальция
Во многих продуктах питания растительного происхождения кальций содержится в виде труднорастворимых соединений (фосфатов, карбонатов, оксалатов), что обуславливает его плохое усвоение из них. Наиболее важным источником кальция является молоко (120мг/100г) и молочные продукты (особенно следует выделить сыр – содержит около 1000мг/100г). За счет молочных продуктов удовлетворяется до 80% от физиологической потребности человека в кальции.
Среди растительных продуктов кальцием наиболее богаты ламинария, орехи и семена, как миндаль, лесной орех, кунжут, фисташки, фасоль, инжир, брюква, капуста брокколи, капуста, хрен, петрушка, лук, курага, яблоки и др.
Дополнительным существенным источником кальция являются специально обогащенные пищевые продукты (соки и мука).
Кальций — один из важнейших для человеческого организма микроэлементов, который необходим для построения костной ткани и регулирования процессов клеточного обмена. Находится это соединение во второй группе периодической таблицы Менделеева, а открыто оно в 1808 году химиком Гемфри Дэви. Химический элемент кальций в природе находится в горных породах и в земле, встречается в овощах и фруктах, содержится в продуктах питания животного происхождения.
![Физические свойства кальция]()
История открытия
Считается, что кальций был известен человеку еще с древних времён. В Древнем Риме, в Месопотамии и других цивилизациях Востока с использованием гашеной и негашеной извести возводили массивные и долговечные здания и сооружения. Но в чистом виде этот микроэлемент удалось получить лишь в XIX веке. Английский химик Гемфри Дэви в 1808 году проводил опыты и путём электролизации гашеной извести получил оксиды ртути, из которой выплавил новый металл, названный кальцием.
![Кальций химический элемент]()
Ученый смог определить молярную формулу, вычислить уравнение и степень валентности этого микроэлемента.
В последующем человек научился получать чистый кальций путем использования различных технологий. Проведенные в последующем исследования показали, что этот микроэлемент содержится в большом количестве в земле, причём по мере приближения к ядру его массовая доля увеличивается. Он находится в различных горных породах, но в чистом виде в природе не встречается.
Нахождение в природе
Считается, что кальций — это один из самых распространённых элементов на Земле. Его общая доля составляет 3,38% всей массы коры. Однако из-за высокой активности его большая часть содержится в составе различных оксидов. Также он встречается в горных породах, в том числе в граните, различных силикатах и алюмосиликатах. В осадочных породах это соединение представлено в виде известняка, мела и различных минералов.
Природными источниками являются:
![Химические свойства кальция]()
- доломит;
- флюорит;
- кальцит;
- гипс;
- алебастр;
- апатиты.
Также широко распространены в природе минералы кальция, в том числе ангидрид, известняк, доломит, апатиты и флюорит. Соли этого элемента содержатся в пресной или морской воде, определяя её показатели жесткости.
Экспериментальным путем установлено, что кальций входит в состав различных живых организмов, в том числе в костную ткань позвоночных видов, к которым относится человек. Из карбоната состоят жёсткие панцири и раковины различных беспозвоночных, скорлупа яиц птиц с пресмыкающимися.
Характеристики вещества
В естественных условиях кальций представляет собой металл с характерным серебристо-белым цветом. Он имеет высокую химическую активность, поэтому часто образует множество различных классов и всевозможных соединений с оксидами. Этот элемент представляет большую ценность для промышленного и технического химического синтеза, он необходим для правильной жизнедеятельности большинства живых видов на планете Земля. По своим физическим свойствам кальций относится к категории щелочноземельных, он отлично растворяется в воде, в особенности много этого соединения содержится в морской воде.
Его химические и физические характеристики зависят от особенностей схемы кристаллической решетки этого элемента. Строение атома кальция стандартно и отличается простотой. В зависимости от содержащихся в нем примесей, строение решетки этого микроэлемента может быть объемно-центрическим или кубическо-гранецентрическим. За счёт наличия металлического типа связи в молекуле обеспечивается максимально возможная прочность такого соединения.
![Кальций кристаллическая решетка]()
Основные свойства:
- способность быстро окисляться на воздухе;
- образует многочисленные оксиды;
- применяется в восстановительных реакциях редкоземельных металлов.
Характеристики и химические свойства кальция могут изменяться в зависимости от наличия примесей и температуры окружающей среды. В обычных условиях этот металл имеет агрегатное твердое состояние. Его температура плавления составляет 842 градусов по Цельсию. Он является отличным тепло и электропроводником. Он реагирует на изменения показателей давления, которое модифицирует конфигурацию и положение его атомной решетки. При нагревании выше температуры плавления металл становится жидким, в последующем теряет свои свойства и переходит в парообразное состояние. Температура кипения составляет 1448 градусов.
Опытным путем установлена крайне интересная способность этого элемента. Под воздействием высокого давления это соединение теряет свою способность электропроводимости и другие характеристики кальция.
Однако в последующем после остывания все параметры восстанавливаются при этом отмечаются признаки сверхпроводника, которые в несколько раз превышают аналогичные показатели других элементов. Подобное делает кальций перспективным материалом при изготовлении микрочипов и изделий точной электроники.
Основные способы получения
Кальций обладает повышенной активностью, поэтому часто входит в различные соединения с другими элементами. Именно по этой причине длительное время не удавалось получить чистый материал без содержания различных примесей. Только лишь в начале XIX века англичанину Гемфри Дэви удалось путем электролиза синтезировать металл без содержания примесей. Ученый смог обнаружить взаимодействие электрического тока и расплавов солей с твердыми минералами.
Даже сегодня по прошествии стольких лет технология электролиза солей является наиболее востребованной, что объясняется её простотой и эффективностью. В металлургии применяется способ алюминотермии, который позволяет получить металл с чистотой порядка 98%. Развитие технологий и методов получения этого металла ограничено тем фактом, что такой процесс является ресурсоемким, требуя большого количества тепловой энергии и электрического тока огромной мощности.
![Гемфри Дэви]()
Чистый металл хранят в герметичных емкостях с ограниченным доступом кислорода. Для предупреждения реакции с кислородом и водой кальций заливают слоем специальной жидкости (керосином или жидким парафином), что позволяет осуществлять транспортировку и длительное хранение этого металла, предупреждая его окисление и потерю химической чистоты.
На открытом воздухе кальций быстро начинает взаимодействовать с углекислым газом и кислородом, покрываясь характерным темным налетом.
Применение кальция
В чистом виде металл кальций применяют в качестве восстановителя при химических реакциях изготовления редкоземельных сплавов. Также этот элемент незаменим как раскислитель для бронзы, стали и других различных соединений. В химической промышленности он применяется при производстве бензина, позволяя удалять из топлива лишнюю серу. Из оксидов этого элемента изготавливают оболочки электрических кабелей, также из него выполняют антифрикционные материалы, которые незаменимы в радиоэлектронике и электронной промышленности.
Кальций — это биогенный элемент, необходимый для правильного протекания всех жизненных процессов в организме человека. Он присутствует в жидкостях и тканях растений и животных, поэтому играет важнейшую роль в правильной регенерации клеток. Польза и значение этого элемента для организма была установлена в начале прошлого века, а сегодня выводы ученых подтверждены многочисленными исследованиями. У человека содержание кальция достигает 2%, а у некоторых микроорганизмов — до 38%. Ученым известно лишь несколько видов простейших животных, жизнедеятельность которых может происходить без этого микроэлемента.
![Кальций в организме человека]()
Большинство растений насыщаются кальцием из почвы, потребляя чистые микроэлементы с помощью специальных окислителей, выделяемых их клетками. Животные, в том числе человек, получают этот минерал с водой и пищей. Кальций необходим для образования клеточных мембран, также этот микроэлемент требуется для правильного обмена веществ. Его нехватка в организме приводит к развитию различных опасных заболеваний, вплоть до смерти человека.
Отдельные виды беспозвоночных научились запасаться кальцием, который необходим им для построения нового скелета и защитного панциря. К сожалению, у высших животных такой способности нет, поэтому им требуется постоянно получать этот микроэлемент извне, в том числе употребляя в пищу различные овощи и фрукты. Последние исследования показали, что обеспечить правильное всасывание кальция в организме человека можно лишь при наличии большого количества витамина D и других различных ферментов.
Кальций (Calcium, Са) – один из самых распространенных макроэлементов в организме человека, являющийся строительным материалом для костей человека или животных.
Кроме того, кальций в сочетании с натрием поддерживает здоровье клеточных мембран, участвует в передаче нервных импульсов, а также обладает противоаллергическим, противовоспалительным и детоксикационным действием.
![Кальций (Са) – роль в организме, применение, суточная потребность, источники кальция]()
История
Общие данные
Расположение в периодической таблице Д.И. Менделеева: в старой версии — IV период, IV ряд, II группа, в новой версии таблицы – 2 группа, 4 период.
- Атомный номер – 20
- Атомная масса – 40,078
- Электронная конфигурация – [Ar] 4s2
- Температура плавления (°С) – 839
- Температура кипения (°С) – 1487
- CAS: 7440-70-2
![Кальций в природе]()
Физико-химические свойства. Кальций представляет собой мягкий химически-активный металл серебристо-белого цвета. При контакте с кислородом (О) и углекислым газом (СО2) поверхность металла начинает тускнеть.
Биологическая роль кальция в организме
Кальций выполняет ряд полезных функций практически во всех живых организмах – человеческом, животных и даже растениях.
Согласно данным, только в костях среднестатистического человека находится от 1 до 1,7 кг кальция! В клеточной жидкости концентрация Ca ≈ 10−4 ммоль/л, межклеточной жидкости ≈ 2,5 ммоль/л.
В человеческом организме, в частности – костях, кальций содержится в форме гидроксиапатита, а выполняю большую часть различных биологических процессов – ионы кальция.
Кости большинства беспозвоночных, например – кораллов, моллюсков и др. состоят из карбоната кальция (известь). Также это вещество является одним из основных составляющих яичной скорлупы и раковин.
Среди основных функций кальция в организме человека и животных можно выделить:
- Является строительным материалом для костной ткани, в т.ч. зубов, благодаря чему кости максимально устойчивы к воздействию на них различных неблагоприятных факторов – травмированию, переломам, кариесу, увеличение пористости (остепороз) и другие. Также входит в состав клеточных ядра, мембраны, внутриклеточной и межклеточной жидкости.
- Участвует в передаче нервных импульсов, за счет чего нервная система управляет другими органами и системами, в т.ч. мышечными тканями. Напрямую поддерживает возможность мышцам сокращаться, что особенно важно в случае с сердечной мышцей (миокардом). Поддерживает работоспособность нервной системы.
- Участвует в регулировании процессов свертываемости крови, менструального цикла, уровня инсулина и глюкозы.
- Вместе с натрием, только противоположно, кальций участвует в регулировании проницаемости мембраны клеток — экзоцитозе.
- Обладает антиоксидантной, противоаллергичесской, противовоспалительной, противострессовой активностью.
- Помогает организму в очищении от тяжелых металлов, радионуклидов и других отравляющих его веществ.
- Выполняет функцию активатора некоторых ферментов, гормонов и нейромедиаторов.
- Участвует в поддержании организмом кислотно-щелочного баланса (рН), препятствуя появлению ацидоза (повышение кислотности).
- Необходим для нормального формирования ногтей и волос.
Применение кальция в других сферах человеческой жизни
Суточная потребность
Рекомендуемые суточные дозы кальция в зависимости от пола и возраста, рекомендуемые ВОЗ:
Дети от 1 до 3 лет 600 мг от 4 до 10 лет 800-1000 мг от 10 до 13 лет 1000—1300 мг Молодежь от 13 до 16 лет 1200 мг от 16 до 25 лет 1000 мг Взрослые от 25 до 50 лет 800-1200 мг Беременные и кормящие грудью 1500—2000 мг Важно! Поступление в организм кальция должно сочетаться с поступлением фосфора, в пропорции 1 (Са) к 1,5 (Р).
При сбалансированном питании, большая часть суточной нормы кальция поступает в организм с пищей, в частности – молочной продукцией, зерновыми культурами, зеленью, орехами и другими продуктами, о которых пойдет речь далее в статье.
Нехватка кальция
Нехватка кальция в организме может вызвать ряд осложнений со здоровьем, среди которых можно выделить:
Причины нехватки кальция
Основная причина нехватки кальция – несбалансированное питание (жесткие диеты, голодание, нерегулярный прием пищи и др.).
Также существуют продукты, которые препятствуют нормальному усвоению Са – говяжий жир, жир коровьего молока, пальмовое масло. Содержащиеся в этих продуктах пальмитиновая и стеариновая жирная кислота обладают связывающей Са активность, превращая его в свои производные — пальмитат и стеарат кальция. Далее, необходимый для здоровья кальций просто выводится из организма в процессе дефекации. Если питаться этими продуктами на постоянной основе, особенно с детства, у человека из-за нехватки кальция появится ряд проблем со здоровьем.
Среди других причин, которые могут вызвать дефицит кальция можно выделить – курение, алкоголь, недостаток витамина Д, повышенное употребление кофе и других кофеинсодержащих продуктов, дисбактериозы, беременность, период кормления грудью и менопауза, различные заболевания щитовидной и мочевыделительной системы.
Применение кальция
Применение кальция с лечебной целью целесообразно в следующих случаях:
![Применение кальция]()
- Беременность, лактация, менопауза, месячные, диарея, длительный прием мочегонных или противоэпилиптических препаратов, глюкокортикостероидов и другие состояния, при которых Са усиленно выводится из организма;
- Заболевания, которые характеризуются нарушением транспорта нервных импульсов – при онемениях, судорогах, а также повышенной проницаемости клеточных мембран;
- Уменьшение плотности костей (остеопороз), нарушение роста и формирования скелета (рахит);
- Обильные кровотечения; и связанные с ними состояния;
- Отравление организма – продуктами питания, алкоголем, тяжелыми металлами, солями магния (Mg 2+ );
- Заболевания печени (паренхиматозный гепатит), почек (нефриты), кожи (дерматозы);
- Нарушения метаболизма витамина Д, гипокальциемия.
Избыток кальция
Избыток кальция в организме также, как и нехватка может вызвать ряд осложнений со здоровьем, среди которых можно выделить:
- Гиперкальциемия;
- Отсутствие аппетита, ощущение сильной жажды и тошноты, приступы рвоты;
- Увеличение мочеотделения; ;
- Повышенная свертываемость крови (вязкость);
- Расстройства функционирования мышечной ткани;
- Нарушение усвояемости клетками костной ткани цинка (Zn).
Источник кальция
В каких продуктах содержится кальций больше всего?
![Источник кальция]()
Природные источники (мг на 100 г): мак (1450), молоко сухое обезжиренное (1155), сыры твердые (700-1000), кунжут (840), сухие сливки (740), семена крапивы (713), брынза (530), плавленый сырок (520), чай (495), сардины в масле (420), молоко сгущенное (310), шиповник (260), петрушка (245), укроп (223), кресс-салат (190), фундук (170), жирный творог (150), грецкие орехи (122) молоко коровье (120), кефир (120), шпинат (106), лук зеленый (100), горох (90), изюм (80), ячневая крупа (80), овсяная крупа (64), чеснок (60), яйцо куриное (55), морковь (51), репа (49), капуста (48), брокколи (47), хлеб пшеничный зерновой (43).
Если говорить о Са, как полезном ископаемом, то за счет его высокой химической активности в чистом виде он практически не встречается. Наибольшая вместимость кальция в природе наблюдается в таких образованиях, как – мел и другие разновидности известняка, полевой шпат, гранит.
Синтез в организме: — .
Взаимодействие кальция с другими веществами
Лучшая усвояемость Са кишечником происходит при одновременном его приеме с витамином D.
Для того, чтобы кальций максимально смог выполнять свои функции в организме, его прием необходимо сочетать с магнием (Mg) — в пропорции 1 (Са) к 0,7 (Mg) 1 , а также фосфором (Р) — 1 (Са) к 1,5 (Р).
Видео
Источники:
Читайте также: