Кривая диссоциации оксигемоглобина физиология кратко
Обновлено: 06.07.2024
4.1. Транспорт кислорода
В сложных механизмах транспорта газов кровью и газообмена в тканях важная роль отводится эритроцитам, ответственным за доставку О2 к различным органам и удаление образующегося в процессе метаболизма СО2.
Эритроцит – безъядерная клетка, лишенная митохондрий, основным источником энергии для эритроцита служит глюкоза, метаболизируемая в гексозомонофосфатном шунте или цикле Эмбдена-Мейергофа. Транспорт О2 обеспечивается в значительной мере гемоглобином, состоящим из белка глобина и гема. Последний представляет собой комплексное соединение железа и порфирина. Глобин представляет собой тетрамер полипептидной цепи. Hb A (HbA) – основной гемоглобин взрослых содержит 2 – альфа и 2 – бета – цепи, Hb A2 – содержит две альфа и две дельта цепи.
Гем состоит из иона железа, встроенного в порфириновое кольцо. Ион железа гема обратимо связывает одну молекулу О2. С одной молекулой Hb максимально связываются 4 молекулы О2 с образованием оксигемоглобина.
Гем может подвергаться не только оксигенации, но и истинному окислению, когда железо становится из двухвалентного трехвалентным. Окисленный гем носит название гематина, а молекула гемоглобина становится метгемоглобином. В крови человека метгемоглобин находится в незначительных количествах, его уровень резко возрастает при отравлениях. Метгемоглобин не способен отдавать кислород тканям.
В норме метгемоглобин составляет менее 3% общего Hb крови. Основная форма транспорта О2 – в виде оксигемоглобина. Кислород транспортируется артериальной кровью не только в связи с гемоглобином, но и в растворенном виде. Принимая во внимание тот факт, что 1 г Hb может связать 1,34 мл О2, кислородная емкость крови в среднем у взрослого человека составляет около 200 мл/л крови. Одним из показателей кислородного транспорта является насыщение артериальной крови О2(Sa O2), равного отношению О2, связанного с Hb, к кислородной емкости крови:
SaO2=O2, связанного с Hb/O2 емкость крови* 100%.
В соответствии с кривой диссоциации оксигемоглобина насыщение артериальной крови кислородом в среднем составляет 97%, в венозной крови – 75%.
PaO2 в артериальной крови около 100 мм. рт. ст., а в венозной – около 40 мм. рт. ст.
Количество растворенного кислорода в крови пропорционально парциальному давлению О2 и коэффициэнту его растворимости.
Последний для О2 составляет 0,0031/100 мл крови/ 1 мм. рт. ст.. Таким образом, 100 мл крови при PaO2, равном 100 мм. рт. ст., содержит менее 0,31 мл O2.
Диссоциация оксигемоглобина в тканях обусловлена главным образом химическими свойствами гемоглобина, а также рядом других факторов – температурой тела, рН среды, р СО2.
При понижении температуры тела наклон кривой диссоциации оксигемоглобина возрастает, а при ее повышении – снижается, и соответственно снижается сродство Hb к О2.
При снижении рН, т.е. при закислении среды, сродство гемоглобина к О2 уменьшается. Увеличение напряжения в крови СО2 также сопровождается снижением сродства Hb к О2 и уплощением кривой диссоциации оксигемоглобина.
Известно, что степень диссоциации оксигемоглобина определяется содержанием в эритроцитах некоторых фосфорорганических соединений, главным из которых является 2,3 – ДФГ (2,3 дифосфоглицерат), а также содержанием в эритроцитах катионов. В случаях развития алкалозов, поглощение О2 в легких увеличивается, но в то же время затрудняется отдача кислорода тканями. При ацидозах наблюдается обратная картина.
4.2.Утилизация кислорода тканями
Касаясь патогенеза метаболических сдвигов, свойственных гипоксическим состояниям, следует отметить, что в организме человека более 90% всего потребляемого кислорода восстанавливается с участием цитохромоксидазы митохондрий, и лишь около 10% кислорода метаболизируется в тканях с участием оксигеназ: диоксигеназы и монооксигеназы.
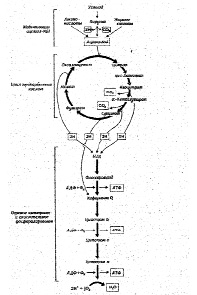
Рис.6. Схема тканевого дыхания. Конечные продукты каждой стадии даны в рамке (Ленинджер А., 1999)
Наиболее многочисленны и сложны монооксигеназные реакции, протекающие в эндоплазматическом ретикулуме клеток при участии цитохрома Р-450 и обеспечивающие гидроксилирование субстрата (стероидных гормонов, лекарственных препаратов и различных др. соединений) и, как правило, его инактивацию.
Диоксигеназы катализируют реакции, в которых в молекулу органического субстрата включаются оба атома молекулы кислорода (например, реакция окисления катехола молекулярным кислородом с раскрытием кольца).
В реакциях, связанных с переносом электронов, т.е. в реакциях окисления-восстановления, где, как указывалось выше, используется более 90% потребляемого кислорода, атомы водорода, отщепленные дегидрогеназами от субстратов в цикле лимонной кислоты, передают свои электроны в цепь переноса электронов и превращаются также в Н +. Как известно, помимо 4 пар атомов водорода, поставляемых каждым оборотом цикла лимонной кислоты, образуются и другие атомы водорода, отщепленные дегидрогеназами от пирувата, жирных кислот и аминокислот в процессе их расщепления до Ацетил-СоА и других продуктов.
Таким образом, все атомы водорода, отщепляемые дегидрогеназами от субстратов, передают свои электроны в дыхательную цепь к конечному акцептору электронов – кислороду.
Касаясь последовательности транспорта электронов в окислительно-восстановительных реакциях, протекающих на внутренней мембране митохондрий, прежде всего, следует отметить, что от всех НАД – зависимых реакций дегидрирования восстановленные эквиваленты переходят к митохондриальной НАДН – дегидрогеназе, затем через ряд железосерных ферментов передаются на убихинон М цитохрому b. Далее электроны переходят последовательно на цитохромы С1 и С, затем на цитохромы аа 3 (цитохромоксидазу – медьсодержащий фермент). В свою очередь цитохромоксидаза передает электроны на кислород. Для того, чтобы полностью восстановить кислород с образованием 2-х молекул воды требуется 4 электрона и четыре Н+ .
Скорость утилизации О2 в различных тканях различна. В среднем взрослый человек потребляет 250 мл О2 в 1 мин. Максимальное извлечение О2 из притекающей артериальной крови свойственно миокарду.
Кислород используется в клетках, в основном в метаболизме белков, жиров, углеводов, ксенобиотиков, в окислительно-восстановительных реакциях в различных субклеточных фракциях: в митохондриях, в эндоплазматическом ретикулуме, в реакциях липопероксидации, а также в межклеточном матриксе и в биологических жидкостях.
Коэффициент утилизации О2 в тканях равен отношению потребления О2 к интенсивности его доставки, широко варьирует в различных органах и тканях.
В условиях нормы минимальную потребность в О2 проявляют почки и селезенка, а максимальную потребность – кора головного мозга, миокард и скелетные мышцы, где коэффициент утилизации О2 колеблется от 0,4 до 0,6, а в миокарде до 0,7. При крайне интенсивной физической работе коэффициент утилизации О2 мышцами и миокардом может возрастать до 0,9.
Обмен дыхательных газов в тканях происходит в процессе свободной и облегченной диффузии. При этом О2 переносится по градиенту напряжения газа из эритроцитов и плазмы крови в окружающие ткани.
Одновременно происходит диффузия СО2 из тканей в кровь. На выход О2 из крови в ткани влияет диссоциация оксигемоглобина в эритроцитах, что обеспечивает так называемую облегченную диффузию О2. Интенсивность диффузионного потока О2 и СО2 определяется градиентом их напряжения между кровью и тканями, а также площадью газообмена, плотностью капилляров, распределением кровотока в микроциркуляторном русле. Интенсивность окислительных процессов в тканях определяется величиной критического напряжения О2 в митохондриях, которое в условиях нормы должно превосходить 0,1-1 мм рт. ст.
Соответствие доставки О2 к органам и тканям, возросшим потребностям в оксигенации обеспечивается на клеточном, органном уровнях за счет образования метаболитов изнашивания, а также при участии нервных, гормональных и гуморальных влияний.
Основная масса углекислого газа (СО2) образуется в организме как конечный продукт различных метаболических реакций и транспортируется к легким с кровью. Вдыхаемый воздух содержит лишь незначительное количество СО2.
Транспорт СО2 кровью осуществляется в 3-х состояниях: в виде аниона бикарбоната, в растворенной форме и в виде карбаминовых соединений.
СО2 хорошо растворяется в плазме крови и в артериальной крови, около 5% от общей двуокиси углерода содержится в крови в растворенной форме.
Анион бикарбоната составляет около 90% от общего содержания СО2 в артериальной крови: СО2+Н2О - Н++НСО-3.
Эта реакция медленно протекает в плазме крови, но чрезвычайно интенсивно происходит в эритроцитах при участии фермента карбоангидразы. Мембрана эритроцита относительно непроницаема для Н+, как и вообще для катионов, но в тоже время, проницаема для ионов НСО-3, выход которых из эритроцитов в плазму обеспечивается притоком Cl- из плазмы в эритроциты. Часть Н+ забуферивается гемоглобином с образованием восстановленного гемоглобина.
Третьей формой транспорта СО2 кровью являются карбаминовые соединения, образованные взаимодействием СО2 с концевыми группами белков крови преимущественно с гемоглобином:
Hb NH2 + CO2 - Hb NH COOH > Hb NH COO + Н+
Карбаминовые соединения составляют около 5% от общего количества СО2, транспортируемого кровью.
В оксигенированной артериальной крови напряжение СО2 составляет 40 мм. рт. ст., а в венозной крови Рv СО2 равно 46 мм. рт. ст.
4.4.Связывание гемоглобина с окисью углерода
Угарный газ (СО) – окись углерода обладает значительно большим сродством к гемоглобину, чем О2, с последующим образованием карбоксигемоглобина. СО входит в состав бытового газа, а также выделяется при работе двигателей внутреннего сгорания. При концентрации СО во вдыхаемом воздухе всего в количестве 7*10- 4 около 50% гемоглобина превращается в карбоксигемоглобин. В норме в крови содержится около 1% HbCO, у курильщиков – 3% . В крови водителей такси концентрация карбоксигемоглобина достигает 20%. Карбоксигемоглобин диссоциирует с отдачей О2 в 200 раз медленней оксигемоглобина и в то же время препятствует его диссоциации в тканях.
Медицинское компьютерное оборудование для диагностики функционального состояния организма у больных, здоровых и спортсменов.
Кривая диссоциации оксигемоглобина
Нормальная кривая диссоциации оксигемоглобина представлена на рис. 1.7; В исходной ее точке, когда РаО2 гемоглобин не содержит кислорода и Sa О2 также равняется нулю. По мере повышения Ра02 гемоглобин начинает быстро насыщаться кислородом, превращаясь в оксигемоглобин: небольшого увеличения напряжения кислорода оказывается достаточно для существенного прироста содержания НЬО2. При 40 мм рт. ст. содержание НЬО2 достигает уже 75 %. Затем наклон кривой становится все более и более пологим. На этом участке кривой гемоглобин уже менее охотно присоединяет к себе кислород, и для насыщения оставшихся 25 % НЬ требуется поднять Ра02 с 40 до 150 мм рт. ст. Впрочем, в естественных условиях гемоглобин артериальной Крови никогда не насыщается кислородом полностью, потому НТО при дыхании атмосферным воздухом Ра02 не превышает 100 мм рт. ст. (см. ранее).

Рис. 1.7. Кривая диссоциации оксигемоглобина.
Зависимость SaO 2 от РaО2 для каждого больного можно описать эмпирическими формулами (уравнение Хилла, алгоритмы Кел-мана, Северингхауза и др.), в которых учитываются температура, рН и прочие факторы. Данные формулы в разных модификациях обычно вводят в современные автоматические приборы контроля КЩС и газового состава крови ( Radiometer , AVL , Instrumentation Laboratories и пр.), которые вычисляют сатурацию гемоглобина по напряжению кислорода в крови. Собственно, сама кривая диссоциации оксигемоглобина и является графическим выражением этих уравнений. Более простой показатель положения кривой диссоциации — индекс Рм; он равен напряжению кислорода в крови, при котором сатурация гемоглобина составляет 50 % (рис. 1.7).
Нормальная величина P 50 равна 27 мм рт. ст. Ее уменьшение соответствует сдвигу кривой влево, а увеличение — сдвигу вправо.
После полного насыщения гемоглобина кислородом дальнейшее повышение Ра02 сопровождается лишь незначительным приростом СаО2 за счет физически растворенного кислорода. Поэтому увеличение концентрации кислорода во вдыхаемом или вдуваемом газе ( F 1 O 2) сверх уровня, достаточного для полного насыщения гемоглобиновой емкости ( Sa 02 = 99-100 %), редко бывает оправданным.
Проходя через капилляры, артериальная кровь отдает тканям часть содержащегося в ней кислорода и превращается в венозную ( PvO 2 = 40 мм рт. ст., SvO 2 = 75 %). Таким образом, в газообмене участвует лишь около 25 % запаса кислорода артериальной крови, а сатурация и десатурация гемоглобина происходят, на пологом участке кривой диссоциации.
Гемоглобин как транспортный белок призван решать две задачи: присоединять кислород в легких и отдавать его тканям. Эти задачи противоположны по своей сути, но выполняются одним и тем же веществом, поэтому стремление гемоглобина связываться с кислородом (сродство гемоглобина к кислороду) должно быть достаточным — чтобы обеспечить оксигенацию крови в легких, но не избыточным — чтобы не нарушить процесс отдачи кислорода на периферии. Нормальное положение кривой диссоциации оксигемоглобина как раз и соответствует оптимальной готовности гемоглобина к реализации обеих задач. Но при определенных условиях баланс между стремлением гемоглобина присоединить кислород и готовностью его отдать нарушается. Графически это выражается сдвигом кривой диссоциации вправо или влево (рис. 1.8).

Рис. 1.8. Сдвиг кривой диссоциации оксигемоглобина.
При ацидозе (респираторном или метаболическом), гипертермии и увеличении концентрации 2,3-дифосфоглицерата (2,3-ДФГ) в эритроцитах сродство гемоглобина к кислороду снижается и кривая диссоциации НЬО2 сдвигается вправо. При этом насыщение гемоглобина кислородом в легких ухудшается (уменьшение Sp02 при прежнем РаО2), но отделение кислорода от оксигемоглобина в капиллярах облегчается.
Если газообмен в легких не нарушен, то даже существенный сдвиг кривой диссоциации вправо сопровождается весьма незначительным снижением Sp02, поскольку события в легких происходят на пологом участке кривой. В тканях же напряжение кислорода повышается. В отношении кислородного гомеостаза это в целом безопасная ситуация. Некоторые специалисты даже счи-
тают, что при нормальной работе легких ацидоз способствует снабжению тканей кислородом.
Иная картина наблюдается при грубой патологии дыхания, когда от легких оттекает кровь с низким напряжением кислорода, соответствующим крутому участку кривой диссоциации НЬО2. Если при этом кривая сдвинута вправо, SpO 2 может оказаться намного ниже, чем при нормальном положении кривой. Данное обстоятельство — дополнительный удар по снабжению тканей кислородом и важный вклад в дело развития гипоксии. Таким образом, при исходной артериальной гипоксемии (низком уровне РаС>2) метаболический ацидоз, гиперкапния и гипер-термия способны заметно снизить сатурацию гемоглобина (Sp02) и, следовательно, содержание кислорода в артериальной крови.
Алкалоз (респираторный или метаболический), гипотермия и уменьшение концентрации 2,3-ДФГ повышают сродство гемоглобина к кислороду, и кривая диссоциации НЬ02 сдвигается влево. В этих условиях гемоглобин жадно присоединяет к себе кислород в легких ( SpO 2 возрастает при прежнем РаО2) и неохотно отдает его тканям. Считается, что сдвиг кривой диссоциации влево всегда неблагоприятно сказывается на оксигенации тканей, ибо небольшой прирост содержания (но не напряжения) кислорода в артериальной крови не окупает последующего нежелания оксигемоглобина делиться кислородом с тканями на периферии. Пожалуй, от левого положения кривой диссоциации НЬО2 не страдают только новорожденные. Но это отдельная тема.
Непостоянство отношений между РаО2 и SpO 2 может затруднить осмысление данных пульсоксиметрии: далеко не всегда известно, по какой кривой диссоциации работает гемоглобин в данный момент.
Красный пигмент крови человека, сложный железосодержащий белок (хромопротеин, состоящий из глобина и четырех гемов с двухвалентным железом в центре каждого) – гемоглобин (Hb), соединяясь с молекулярным кислородом (O2) в легких, образует оксигенированную форму – оксигемоглобин (HHbO2). Оксигемоглобин, приобретая уникальные свойства и обеспечивая дыхание, как одно из элементарных проявлений жизни, продолжает саму жизнь организма. Например, достаточно ввести окись углерода вместо кислорода или нарушить потребление О2 клетками при попадании цианидов (солей синильной кислоты), которые ингибируют ферментные системы тканевого дыхания, как тут же наступает гибель организма.

Дыхание, на первый взгляд, кажется совсем простым процессом. Между тем, оно основано на взаимодействии многих компонентов, составляющих гигантскую молекулу красного пигмента крови – хромопротеина гемоглобина, который, в свою очередь, отличается многообразием производных, где из их числа несомненный интерес вызывает оксигемоглобин. Итак, оксигемоглобин образуется в легких путем соединения сложного железосодержащего белка гемоглобина с кислородом, поступающим с вдыхаемым воздухом.
Образование и распад оксигемоглобина
В спокойном состоянии тканям человеческого тела достаточно около 0,2 л кислорода в одну минуту, но все меняется при физической нагрузке и чем она интенсивнее, тем больше необходимого для дыхания газа запрашивают ткани. Для удовлетворения их нужд потребность в кислороде может увеличиваться в 10 – 15 раз и составлять до 2, а то и 3 литров О2 в одну минуту. Однако газообразный кислород в данном количестве никак не сможет пробраться в ткани, поскольку он почти не растворим и в воде, и в плазме, то есть, этот элемент в ткани должен доставить какой-то белок, способный соединиться с ним и решить задачу транспорта.

Кровь, как биологическая среда, реализует свои функциональные обязанности по обеспечению дыхания за счет присутствия в ней сложного содержащего железо протеина – гемоглобина, физиологическая роль которого, как транспортного средства кислорода, базируется на способности Hb связывать и отдавать О2 в корреляции с концентрацией (парциальным давлением – P) данного газа в крови. Образование оксигемоглобина осуществляется в паренхиме легких, куда кислород прибывает при дыхании из воздуха окружающей среды.
Процесс образования HHbO2 происходит в доли секунды (0,01 с), поскольку кровь в легких задерживается всего-то на полсекунды. Схематично и коротко образование оксигемоглобина можно представить в следующем виде:
- Попадая в капиллярные сосуды легких, кровь обогащается кислородом, то есть, красный кровяной пигмент к своим 4 гемам присоединяет кислород – идет реакция окисления (оксигенации);
- Кислород связывается с гемами хромопротеина при помощи координационных связей феррума (железо – Fe) и, не изменяя в данном случае валентности последнего (в геме валентность железа всегда – II), переводит его (Hb) в несколько иное состояние;
- Гем железосодержащего протеина представляет собой активный центр, с его помощью хромопротеин в результате вышеуказанной реакции переходит в непрочный комплекс – оксигенированный гемоглобин (HHbO2), который, находясь в красных кровяных тельцах – эритроцитах, с током крови доставляется к клеткам тканей, чтобы через распад оксигемоглобина и выделения в процессе диссоциации кислорода, обеспечить их дыхание.
Таким образом, результатом реакции оксигенации становится образование оксигемоглобина, подкисление биологической жидкости, снижение ее щелочного резерва, то есть, ее умения связывать углекислоту (СО2), которое, разумеется, на тот момент снижается.
Железосодержащий протеин, насытившись в легочной паренхиме кислородом и приобретя оксигенированную форму, уносит О2 к тканям, в капиллярных сосудах которых его концентрация в крови резко понижена. Там происходит распад оксигемоглобина (диссоциация), кислород уходит на тканевое дыхание, гемоглобин забирает отработанный углекислый газ, превращаясь в другую физиологическую модель – карбогемоглобин (HHbCO2), и в этом качестве отправляется в главный орган дыхания, чтобы обменять CO2 на очередную порцию необходимого организму газа.

Кривая образования и распада (диссоциации) оксигемоглобина
Агентом, гарантирующим быстрое насыщение железосодержащего белка кислородом (образование оксигемоглобина), выступает высокое напряжение (парциальное давление) О2 в легочных альвеолах (порядка 100 мм рт. ст.).
Корреляцию между степенью насыщения красного кровяного пигмента кислородом и парциальным давлением O2 (PO 2) выражают в виде S-образной кривой (сигмоиды), которую называют кривой диссоциации оксигемоглобина.

Свойственная красному кровяному пигменту S-образная (сигмоида) кривая диссоциации оксигемоглобина свидетельствует о том, что контактирование первой молекулы О2 с одним из гемов Hb открывает путь присоединению других молекул элемента остальными тремя гемами. Кривой насыщения железосодержащего белка кислородом принадлежит немалая физиологическая значимость – S-образная конфигурация позволяет крови обогатиться данным газом при изменениях концентрации кислорода в биологической жидкости в довольно обширных интервалах. К примеру, не следует ожидать таких особенных расстройств дыхательной функции крови, как выраженное кислородное голодание (гипоксия), при подъеме на высоту до 3,5 км над уровнем моря или во время перелета на самолете. Хотя PO 2 во вдыхаемом воздухе сильно понизится, концентрация кислорода в крови будет находиться на достаточно высоком уровне, чтобы обеспечить насыщение Hb данным газом. На это указывает и отлогий график формирования и распада оксигемоглобина на верхнем его отрезке (верхний отрезок кривой свидетельствует о течении процесса насыщения О2 красного пигмента крови в легочной паренхиме и находится в пределах 75 – 98%).
Кривая диссоциации оксигемоглобина может быть разделена на 4 отрезка, каждому их которых соответствует определенный период образования оксигемоглобина (зависимость скорости насыщения хромопротеина кислородом от парциального давления газа в крови):
- 0 – 10 мм рт. ст. – гемоглобин не спешит насыщаться;
- 10 – 40 мм рт. ст. – оксигенация резко ускоряется (стремительный подъем кривой), доходя до 75%;
- 40 – 60 мм рт. ст. – оксигенация заметно замедляется, потихоньку добираясь до 90%;
- Значения PO2 пересекают отметку 60 мм рт. ст. – насыщение идет слабо (линия лениво ползет вверх). Однако кривая медленно продолжает стремиться к отметке 100%, но, так и не достигнув ее, останавливается на уровне 96 – 98%. Кстати, и такие показатели насыщения Hb кислородом отмечаются только у молодых и здоровых людей (PO2 артериальной крови ≈ 95 мм рт. ст., легочных капилляров – ≈ 100 мм рт. ст.). С возрастом дыхательные способности крови снижаются.
Несовпадение парциального давления кислорода артериальной крови и смеси газов в альвеолах легких трактуется:
- Некоторыми разногласиями между интенсивностью тока крови и вентилированием разных отделов главного органа дыхания – легких;
- Притоком незначительного объема крови из бронхиальных вен в венозные сосуды легких (шунтирование), где, как известно, течет артериальная кровь;
- Прибытием доли крови из коронарных вен в левый желудочек сердца посредством тебезиевых вен (вены Тебезия-Вьессена), в которых проходимость возможна в обоих направлениях.
Между тем, причины, вследствие которых кривая образования и диссоциации оксигемоглобина приобрела сигмоидную форму, пока остаются не до конца выясненными.
Смещение кривой диссоциации оксигемоглобина
Но кривая диссоциации оксигемоглобина, о которой идет речь выше, справедлива, если в организме все нормально. В других ситуациях график может сдвигаться в ту или иную сторону.
В числовом выражении сродство гемоглобина к кислороду обозначается величиной P50 – напряжение полунасыщения красного пигмента крови кислородом или иными словами: парциальное напряжение О2, при котором 50% Hb пребывает в форме оксигемоглобина (оптимальные условия: рН – 7,4, tº – 37ºC). Нормальные значения этого показателя в артериальной крови приближаются к величине 34,67 гПа (26 мм рт. ст.). Смещение графика вправо указывает на то, что способность красного кровяного пигмента соединяться с кислородом снижается, что, естественно, увеличивает значения P50. И, наоборот – смещение кривой влево говорит об увеличении сродства этого хромопротеина к кислороду (↓P50.).

Ходу сигмоиды помогают некоторые факторы, повышающие обогащение крови кислородом и таким образом участвующие в тканевом дыхании, поэтому названные вспомогательными:
- Повышение водородного показателя (pH) крови (эффект Бора), поскольку способность гемоглобина присоединять кислород связана с водородным показателем (pH) данной биологической среды (гемоглобин представляет одну из четырех буферных систем и влияет на регуляцию кислотно-основного баланса, поддерживая pH на нужном уровне: 7,36 – 7,4). Следовательно, чем выше водородный показатель, тем активнее ведет себя гемоглобин в отношении кислорода и наоборот – снижение pH отнимает возможности хромопротеина присоединять кислород, например: ↓pH до 7,2 заставит график отклоняться вправо (≈ на 15%), ↑pH до 7,6 передвинет кривую диссоциации оксигемоглобина влево (≈ на 15%);
- Отделение углекислого газа от карбогемоглобина в легких и выход СО2 с выдыхаемым воздухом (эффект Бора-Вериго) на фоне повышения водородного показателя создает условия для жадного насыщения гемоглобина кислородом (образование оксигемоглобина в легких);
- Возрастание уровня значимого для обмена фосфата – 2,3-дифосфоглицерата (2,3-ДФГ), содержание которого в крови меняется в зависимости от условий протекания обменных процессов;
- Снижение температуры в легких (в тканях она выше, нежели в легких) и чем ниже упадет tº, тем больше способностей присоединять кислород появляется у железосодержащего белка (при повышении температуры идет обратный эффект).
Уровень красного пигмента в крови, а также его способность присоединять кислород (кривая диссоциации оксигемоглобина) в некоторой степени подвержены возрастным колебаниям. Так, у младенцев, только-только известившим мир о своем появлении первым криком, количество гемоглобина заметно выше, что объясняется присутствием фетального гемоглобина, который, как известно, обладает повышенным сродством к кислороду. Красный пигмент крови стариков, напротив, постепенно снижает способности связывать кислород.
В заключение хочется заметить, что гемоглобин не только имеет сродство к кислороду и довольно легко соединяется с углекислым газом. Кроме физиологических соединений красного кровяного пигмента при определенных условиях возникают связи с другими газами, в частности – с угарным газом (CO) и оксидом азота (NO), причем соединение происходит также непринужденно
Высокое сродство Hb к угарному газу влечет образование карбоксигемоглобина (HHbCO), который препятствует соединению хромопротеина с кислородом, а в результате этого ткани остаются без O2. К чему это может привести – всем известно: при отравлении угарным газом высок риск смертельного исхода, если вовремя не помочь человеку.
При отравлении оксидом азота или парами нитробензола гемоглобин переходит в метгемоглобин (HHbOH) с изменением валентности железа (II → III). Метгемоглобин также не позволяет кислороду соединиться с гемоглобином, в итоге – наступает кислородное голодание тканей, создается угроза жизни организма.
Диффузионная способность легких по монооксиду углерода
Диффузионная способность легких по монооксиду углерода (DLCO) – мера способности газа переходить из альвеол через альвеолярный эпителий и капиллярный эндотелий в эритроциты. DLCO зависит не только от области и толщины альвеолярно-капиллярной мембраны, но также от объема крови в легочных капиллярах. Распределение альвеолярного объема и вентиляции также вызывает изменение показателя.

DLCO определяется с помощью анализа воздуха на содержание монооксида кислорода (СО) в конце выдоха, после того как пациент вдыхает незначительное количество СО, задерживает дыхание и выдыхает. Определяемые показатели DLCO должны быть соотнесены с альвеолярным объемом (который оценивается разведением гелия Легочные объемы Определение скорости потока и легочных объемов используют для дифференцировки обструктивных и рестриктивных пульмональных нарушений, определения тяжести заболевания и оценки эффективности лечения. Прочитайте дополнительные сведения ) и уровнем гематокрита пациента. DLCO измеряется в мл/минуту/мм.рт.ст. и в процентах от должного.
Причины снижения DLCO
Заболевания, которые прежде всего повреждают легочную сосудистую сеть, такие как первичная легочная гипертензия Легочная гипертензия Легочная гипертензия – это повышение давления в малом круге кровообращения. В большинстве случаев она является вторичной, в некоторых случаях – идиопатической. При легочной гипертензии происходит. Прочитайте дополнительные сведения и тромбоэмболия легочной артерии Тромбоэмболия Легочной Артерии (ТЭЛА) Тромбоэмболия легочной артерии – это окклюзия легочных артерий тромбами любого происхождения, чаще всего образующихся в крупных венах ног или малого таза. Факторами риска тромбоэмболии легочной. Прочитайте дополнительные сведения , уменьшают DLCO. Диффузные заболевания легких, такие как эмфизема Хроническая обструктивная болезнь легких (ХОБЛ) Хроническая обструктивная болезнь легких (ХОБЛ) – ограничение воздушного потока, вызванное воспалительным ответом на вдыхаемые токсины, чаще всего сигаретный дым. Менее распространенными причинами. Прочитайте дополнительные сведения и легочный фиброз Идиопатический легочный фиброз Идиопатический легочный фиброз (ИЛФ), наиболее распространенная форма идиопатической интерстициальной пневмонии, вызывает прогрессирующий фиброз легких. Жалобы и симптомы появляются постепенно. Прочитайте дополнительные сведения , уменьшают и DLCO и альвеолярную вентиляцию (VA). Снижение DLCO также наблюдается у больных после резекции легкого, поскольку объем легких уменьшается, но DLCO соответствует или даже превышает норму при коррекции на VA, поскольку в оставшемся легком увеличивается площадь поверхности сосудов. Пациенты с анемией часто имеют более низкую DLCO, которую необходимо корректировать в зависимости от цветного показателя крови
Причины повышения DLCO
Условия, при которых значения DLCO будут выше, чем прогнозировалось, включают
Во время сердечной недостаточности DLCO увеличивается предположительно вследствие повышения объема крови в легочных капиллярах из-за повышенных легочных венозного и артериального давлений. При эритроцитемии увеличение DLCO обусловлено увеличением количества эритроцитов, а также из-за сосудистого наполнения вследствие возрастания легочного давления, обусловленного повышенной вязкостью крови. При альвеолярном кровотечении эритроциты также могут связывать монооксид углерода в альвеолярном пространстве, увеличивая DLCO. При астме увеличение DLCO связывают с увеличением перфузируемых сосудов, однако согласно некоторым данным, не исключено влияние различных факторов роста, индуцирующих неоангиогенез.
Пульсоксиметрия
Чрескожная пульсоксиметрия оценивает сатурацию кислорода (SpО2) капиллярной крови по поглощению света от светоиспускающих диодов, помещенных в клипсу для пальца или датчик на пластыре. В целом результаты чрезвычайно точные и коррелируют с сатурацией кислорода с погрешностью в пределах 5% (SaО2). Результаты могут быть менее точными у пациентов с
Очень пигментированная кожа
Выраженной системной вазоконстрикцией
Результаты пульсоксиметрии также менее точны при наличии накрашенных ногтей у пациентов.
Пульсоксиметрия способна определять содержание только оксигемоглобина или дезоксигемоглобина, но не другие формы гемоглобина (например, карбоксигемоглобин, метгемоглобин); данные фракции завышают показатели SpO2, когда их ошибочно принимают за оксигемоглобин.
Исследование газового состава артериальной крови (ГСАК)
Исследование газового состава артериальной крови проводится для получения точных значений парциального давления кислорода в артериальной крови (PaO2), парциального давления углекислого газа в артериальной крови (PaCO2) и pH артериальной крови; эти показатели, откорректированные с учетом температуры пациента, позволяют рассчитать уровень бикарбоната (который может также быть измерен непосредственно в венозной крови) и SaO2. С помощью исследования газового состава также можно точно измерить уровень карбоксигемоглобина и метгемоглобина.
Обычно для взятия образцов артериальной крови используется лучевая артерия. Поскольку артериальная пункция может в редких случаях приводить к тромбозу и ухудшению перфузии дистальных отделов, вначале выполняется тест Аллена. Он позволяет оценить адекватность коллатерального кровообращения. При выполнении этой пробы одновременно пережимаются лучевая и локтевая артерии до тех пор, пока рука пациента не станет бледной. После этого локтевую артерию отпускают, в то время как давление на лучевую артерию продолжается. Появление розовой окраски во всей руке в течение 7 секунд после ослабления давления указывает на адекватный кровоток через локтевую артерию.
В стерильных условиях игла калибром 22–25G, присоединенная к гепаринизированному шприцу, вводится проксимальнее места максимальной пульсации лучевой артерии и продвигается немного дистальнее в артерию, пока не восстановится пульсация. Систолическое артериальное давление обычно является достаточным, чтобы выдвинуть поршень шприца обратно. После забора 3–5 мл крови игла быстро извлекается, и место пункции сильно прижимается для осуществления гемостаза. Одновременно образец артериальной крови помещается в лед (для уменьшения потребления кислорода и продукции углекислого газа лейкоцитами) и посылается в лабораторию.
Оксигенация
Гипоксемия – это снижение парциального давления кислорода (PO2) в артериальной крови; гипоксия – это снижение РO2 в тканях. Исследование газового состава точно определяет наличие гипоксемии, которая обычно определяется как достаточно низкое значение РаO2, способное уменьшить SaO2 ниже 90% (т.е. РаO2 60 мм.рт.ст.). Патологические формы гемоглобина (например, метгемоглобин), более высокая температура, низкий pH и высокий уровень 2,3-дифосфоглицерата уменьшают гемоглобин SaO2, несмотря на адекватный РаO2, как показано на кривой диссоциации оксигемоглобина ( Кривая диссоциация оксигемоглобина Кривая диссоциация оксигемоглобина Газообмен измеряется несколькими способами, включая Диффузионная способность легких для монооксида углерода Пульсоксиметрия Исследование газового состава артериальной крови Диффузионная способность. Прочитайте дополнительные сведения ).
Кривая диссоциация оксигемоглобина
Насыщение артериальной крови оксигемоглобином соответствует P o 2. P o 2 при сатурации 50% (P50) обычно соответствует 27 мм.рт.ст.
Кривая диссоциации смещается вправо при увеличении концентрации ионов водорода (Н + ), увеличении в эритроцитах 2,3-дифосфоглицерата, повышении температуры (Т) и увеличении P co 2.
Снижение уровня Н + , ДФГ, температуры и P co 2 вызывает смещение кривой влево.
Гемоглобин, характеризующийся смещением кривой вправо, имеет пониженное сродство к кислороду, а гемоглобин, характеризующийся смещением кривой влево, имеет повышенное сродство к кислороду.
Причины гипоксемии классифицируют в зависимости от значения (повышение или норма) альвеолярно-артериального градиента PО2 по кислороду ([A-а]DО2), который определяется как разница между альвеолярным напряжением кислорода (PAО2) и PaО2. РAO2 рассчитывается следующим образом:
где FIO2 – содержание кислорода во вдыхаемом воздухе (например, в комнатном воздухе – 0,21), Patm – барометрическое атмосферное давление (например, 760 мм.рт.ст. на уровне моря), PH2O – парциальное давление водяного пара (обычно 47 мм.рт.ст.), PaСО2 – измеренное парциальное давление углекислого газа в артериальной крови, R – дыхательный коэффициент, который принимают за 0,8 у пациента в состоянии покоя при обычном питании.
Для пациентов, находящихся на уровне моря при дыхания комнатным воздухом, FIO2 = 0,21 и (A-а) DO2 можно упростить следующим образом:
где (A-a)DО2 обычно 20, но увеличивается с возрастом (из-за снижения функции легких с возрастом) и с увеличением FIO2 (несмотря на то, что насыщение гемоглобина достигает 100% при PaО2 около 150 мм.рт.ст., кислород растворим в крови и кислород плазмы продолжает увеличиваться при повышении FIO2 ). Оценки нормального (А-а) DO2 значения как (2,5 + [FIO2 × возраст в годах]) или как менее абсолютного значения Fio2 (например, 21 при комнатной температуре; 30 на 30% FIO2) корректируют эти эффекты.
Гипоксемия с повышенным (А-а) DO2
Гипоксемия с повышенным (Aa)DO2 вызвана
Низкое вентиляционно-перфузионное (V/Q) соотношение (разновидность вентиляционно-перфузионного несоответствия)
Шунтирование крови справа налево
Серьезное нарушение диффузионной способности

Низкое отношение V/Q (вентиляционно-перфузный индекс) является наиболее распространенной причиной гипоксемии. Она вносит свой вклад в усиление гипоксемии при ХОБЛ Хроническая обструктивная болезнь легких (ХОБЛ) Хроническая обструктивная болезнь легких (ХОБЛ) – ограничение воздушного потока, вызванное воспалительным ответом на вдыхаемые токсины, чаще всего сигаретный дым. Менее распространенными причинами. Прочитайте дополнительные сведения и бронхиальной астме Астма Бронхиальная астма – заболевание, характеризующееся диффузным воспалением дыхательных путей с разнообразными пусковыми механизмами, которое приводит к частично или полностью обратимому бронхоспазму. Прочитайте дополнительные сведения . В норме региональная перфузия соответствует региональной вентиляции благодаря вазоконстрикции артериол, которая развивается в ответ на альвеолярную гипоксию. При патологии нарушение регуляции приводит к перфузии альвеолярных участков, которые недостаточно вентилируются (вентиляционно-перфузионное несоответствие). В результате венозная кровь проходит через легочные капилляры, не достигая нормальных уровней PaO2. Несоответствие V/Q также может возникать при увеличении кровотока даже при нормальной вентиляции, как при болезнях печени. Дополнительный кислород позволяет скорректировать гипоксемию, вызванную низким вентиляционно-перфузионным соотношением, за счет увеличения PAО2, хотя (A-a)DО2 сохраняется повышенным.
Шунтирование крови справа налево является ярким примером низкого вентиляционно-перфузионного соотношения. При шунтировании дезоксигенированная легочная артериальная кровь поступает в левую половину сердца, не пройдя через вентилируемые сегменты легкого. Шунтирование может проходить через паренхиму легкого, через патологические связи между легочными артериальными и венозными сосудами или через патологические анатомические структуры в сердце (например, открытое овальное отверстие). При наличии подобного шунтирования справа налево устранить гипоксемию с помощью кислородотерапии не представляется возможным.
Сниженная диффузионная способность редко встречается изолированно; обычно она сопровождается низким вентиляционно-перфузионным соотношениями. Поскольку кислород полностью насыщает гемоглобин только после контакта крови с воздухом, гипоксемия из-за сниженной диффузионной способности встречается только при увеличенном сердечном выбросе (например, во время физической нагрузки), при низком атмосферном давлении (например, на высоте в горах) или при разрушении > 50% легочной паренхимы. Как при низким вентиляционно-перфузионном соотношении, (A-a)DO2 увеличен, но PaO2 может быть быстро увеличен благодаря увеличению FIO2. Гипоксемия, развивающаяся вследствие нарушения диффузионной способности, корректируется с помощью кислородотерапии.
Читайте также:

