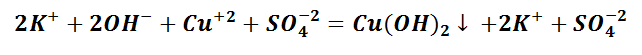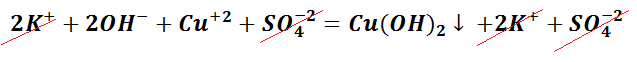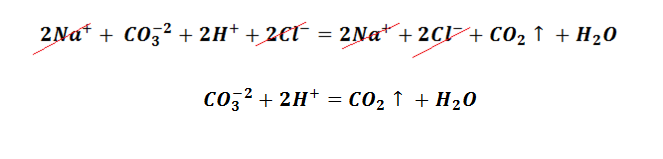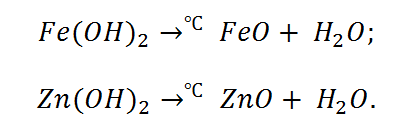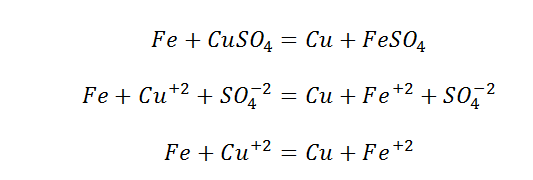Химические реакции в растворах кратко
Обновлено: 02.07.2024
Химия настолько уникальная и удивительная наука, что во время проведения опытов, иногда, кажется, что происходят чудеса. Сливая два раствора, можем наблюдать, как бурно выделяется газ, или меняется цвет, или выпадает яркий осадок. Однако бывают и такие случаи, что реакция не происходит. А выяснить причину этому поможет наш урок, в котором рассмотрим реакции ионного обмена.
План урока:
Особенности протекания реакций в растворе
Химические реакции, в отличие от физических, характеризуются образованием новых веществ. Судить об их получении, мы можем, наблюдая изменение окраски, либо выделение газа или осадка.
Вспомним, что происходит с веществом, когда оно попадает в воду. Оно распадается на ионы. Тем не менее, этот процесс характерен не для всех веществ, а только для сильных электролитов, к которым относятся растворимые соли и кислоты, а также щёлочи.
Также необходимо вспомнить, какие реакции относятся к типу обмена.
Судить произошла реакция или нет, мы можем, если будет выполняться хотя бы одно из условий.
Условия протекания реакций между ионами сложных веществ.
Рассмотрим подробно каждое условие и составим алгоритм написания уравнений.
Выпадение осадка является подтверждением того, мы визуально видим, что реакция произошла. Составим уравнение между щёлочью – гидроксидом калия и солью – сульфатом меди (II). Запишем молекулярное уравнение.
Выполняя данный опыт, Вы могли бы наблюдать образование осадка голубого цвета.
Чтобы понять, какое вещество выпало в осадок, воспользуемся таблицей растворимости, а также составим полное ионно-молекулярное уравнение, которое отображает все частицы, находящиеся в растворе, с учётом коэффициентов.
Таким образом, KOH, K2SO4 и CuSO4 – это сильные электролиты, которые запишем в ионном виде. Cu(OH)2 – нерастворимое вещество, будет в молекулярном виде со стрелкой ↓. Также обращаем внимание, что перед щёлочью КОН находится коэффициент 2. Значит, образуется по два моля ионов К + и ОН − .
При написании уравнений реакций, не забываем о законе сохранения вещества. Поэтому количество атомов, а также ионов, до реакции и после должны быть равны.
Следует отметить, что в полном ионно-молекулярном уравнении, слева и справа, имеются одинаковые частицы, их можно сократить.
Эти ионы при взаимодействии не образуют вещества, поэтому находятся в растворе в свободном виде как K + и SO4 −2 .
Сокращённая реакция ионного обмена отображает суть химического процесса, а именно, между какими частицами происходит реакция.
Следственно, Cu(OH)2 будет осадком в растворе состоящем из ионов SO4 2− и К + .
Вторым из условий является выделение газа. Эту реакцию Вы наблюдаете, когда гасите соду кислотой, не важно, какой уксусной, лимонной, яблочной, или же при добавлении к ней кефира, результат будет один и тот же, образование пузырьков углекислого газа. Для примера возьмём взаимодействие соды и соляной кислоты. Составим молекулярное уравнение.
После сокращение одинаковых частиц левой и правой части, получаем сокращённое ионное уравнение.
И к третьему условию относится образование слабого электролита, зачастую это молекула воды, однако могут получаться и другие вещества. Ярким примером является реакция нейтрализации.
Почему этот тип реакции носит такое название? Рассмотрим на примере взаимодействия оснований КОН и Cu(OH)2 с раствором соляной кислоты.
В каждом случае происходит образование воды. В случае нерастворимых оснований, реакция идёт с образованием растворимой соли.
Уравнение реакции нейтрализации показывает, как два противоположных по свойствам класса неорганических соединений, отдавая по своей частице (Н + и ОН - ), образуют нейтральное вещество Н2О.
Кислоты и их свойства
Если посмотреть на состав этого класса соединений, то абсолютно во всех содержаться ионы водорода.
Следует заметить, что уравнение диссоциации кислот похожи, но отличие будет по кислотному остатку.Рассмотрим на примерах следующих многоосновных кислот –сернойН2SО4 и фосфорной Н3РО4.Характерной особенностью диссоциации многоосновных кислот – это ступенчатая диссоциация. Это означает, что ионы водорода будут отрываться не сразу все (2 или 3), а по одному.
Следствием этого является способность многоосновных кислот образовывать кислые соли.
Рассмотрим химические свойства кислот, за которые отвечают ионы Н + .
Каким образом можно доказать, что неизвестное вещество относится к кислотам. Для этих целей создали индикаторы, которые как настоящие сыщики, ищут ионы Н + или ОН - (в основаниях). Найдя их, они моментально меняют свою окраску. Кислая среда обусловлена наличием Н + .
В реакциях обмена на их место могут стать только ионы металла, поэтому кислоты реагируют со следующими веществами.
Следственно, при реакции кислот с основными оксидами образуется соль и вода.
Атомы металла входят в состав оснований, в результате реакции нейтрализации, аналогично, как и основными оксидами, продуктом реакции является соль (может быть и кислая, и средняя) и вода.
Взаимодействие кислот с солями возможно только в случае, когда соль образована слабой или летучей кислотой, а также в продукте будет газ или осадок.
Особенно хочется отметить взаимодействие металлов с кислотами, поскольку это будет реакция замещения со сменой степени окисления. Не все металлы способны реагировать с кислотами, а только те, что стоят в ряду напряжения до водорода и способны его вытеснить.
Действие концентрированных серной и азотной кислот на металлы отличается от их растворов, при этом происходит образование не водорода, а воды и других продуктов. Детально со свойствами азотной кислоты Вы познакомитесь чуть позже, однако сейчас необходимо запомнить, что при реакции с раствором этой кислоты водород не выделяется.
Основания и их свойства
Данный класс веществ характеризуется наличием функциональной группы, которая отвечает за химические свойства, а именно группы ОН - . По растворимости основания делятся на щёлочи (растворимые) и нерастворимые основания. Соответственно они будут отличаться по химическим свойствам. Щелочная среда образуется, если есть свободные ОН - , которые образуются при диссоциации щелочей.
Для щелочей, подобно многоосновным кислотам, характерна ступенчатая диссоциация.
Тем не менее, будет происходить не только взаимодействие щелочей с кислотами, но и нерастворимых оснований. Объяснением этому служит, то, что кислоты практически все растворимы, за исключением силикатной H2SiO3, которая реагирует только со щелочами. Продуктом будет соль (в зависимости от соотношения реагентов средняя, основная или кислая) и вода.
Кислотные оксиды со щелочами образуют соль и воду.
Для нерастворимых оснований эта реакция не характерна, поскольку именно гидроксильная группа реагирует с оксидами.
Амфотерные основания реагируют также с щелочами. Результатом данного взаимодействия будет соль, зачастую комплексная, и вода.
Взаимодействие солей с щелочами приводит к образованию соли либо основания. Также не забываем об условии, что в продукте должен быть либо газ, либо осадок.
Отличительной способностью обладают нерастворимые, а также амфотерные основания. Они при нагревании распадаются на оксиды.
Соли и их свойства
Этот класс веществ состоит из частичек кислоты – кислотного остатка и основания – катионов металла (либо иона аммония NH4 + ). Диссоциация солей всегда идёт в одну стадию.
Если посмотреть на состав соли, то смело можно предположить, что их растворы будут нейтральными. Поскольку нет ионов, которые отвечают за реакцию среды. Однако на деле совсем не так. Лакмус в водном растворе солей может иметь как красную, так и синюю окраску, а также не изменять её. Объяснением этого явления служит их взаимодействие с водой, которое имеет название гидролиз солей. Возьмём, к примеру, три пробирки, в которых содержатся растворы NaCl, ZnCl2 и Na2CO3. И в каждую добавим лакмус. Результаты эксперимента отображены на рисунке.
Запишем суть реакции соли с водой (молекулу Н2О распишем как НОН), с помощью ионно-молекулярных уравнений.
Сокращённое уравнение хорошо иллюстрирует, почему происходит изменение окраски индикатора. Теперь давайте разберёмся, какие соли подвергаются гидролизу.
Именно наличием ионов Н + в растворе соли ZnCl2, а также группы ОН - в солевом растворе карбоната натрия, объясняется изменение окраски индикатора.
Рассмотрим взаимодействие металлов с солями. Чтобы понять принцип их взаимодействия, вспомним ряд активностей металлов.
Данный вид взаимодействия Вы можете наблюдать, выполнив дома опыт (не забываем о разрешении родителей). Вам понадобится раствор медного купороса и скрепка, либо гвоздь.
На поверхности гвоздя выделилась медь в чистом виде. Это окислительно-восстановительная реакция.
Взаимодействие солей между собой возможно только, если реагенты растворимы, а в продукте будет осадок.
Свойства солей, кислот и оснований, рассмотренных выше, можно объединить в схематическом виде.
Большинство химических реакций, протекающих в природе, на заводах и в лабораториях, протекают в растворах.
Как и в других условиях, в растворах могут протекать реакции, сопровождающиеся передачей электронов (ОВР), реакции, сопровождающиеся передачей протонов (кислотно-основные реакции, КОР), и реакции, при которых не происходит ни того, ни другого. К последней группе относится большинство реакций, сопровождающихся образованием осадка.
Возьмем два вещества, сульфат натрия и хлорид бария, и растворим каждое из них в воде. Мы получим два раствора. Один из них, раствор сульфата натрия, состоит из молекул воды, гидратированных ионов натрия и гидратированных сульфат-ионов:
Другой раствор, раствор хлорида бария, состоит из молекул воды, гидратированных ионов бария и гидратированных хлорид-ионов:
Смешаем эти растворы. В получившемся растворе помимо молекул воды, казалось бы, должны присутствовать ионы:
Но практически мы обнаружим, что из раствора в виде осадка выделилось какое-то твердое вещество. Откуда же оно появилось? Очевидно, оно образовалось из присутствовавших в растворе ионов.
Соединяться, образуя ионные кристаллы, могут только разноименно заряженные ионы. Следовательно, выпавшим в осадок веществом может быть BaCl2, BaSO4, NaCl или Na2SO4. Но хлорид бария и сульфат натрия содержались в исходных растворах, а при смешивании этих растворов концентрация каждого из них уменьшилась, и потому никак не могла превысить растворимость. Следовательно, BaCl2 и Na2SO4 выпасть в осадок не могли. Остаются сульфат бария и хлорид натрия. Чтобы выяснить, какое из этих веществ выпало в осадок (а может быть, оба?), найдем эти вещества в таблице растворимости (приложение 11). NaCl растворим в воде, а BaSO4 в ней нерастворим, то есть в случае сульфата бария энергетически более выгодно существование кристаллов этого вещества, чем соответствующих гидратированных ионов. Следовательно, в осадок выпал сульфат бария. Уравнение этой реакции
означает, что вещество выделилось из раствора в виде осадка.
Что же осталось в растворе?
Если мы взяли порции хлорида бария и сульфата натрия, равные по количеству вещества, то в растворе остались только гидратированные ионы натрия и гидратированные хлорид-ионы. Если же какое-то из исходных веществ было взято в избытке, то избыток перешедших из него в раствор ионов тоже, естественно, останется в растворе. Так, если в избытке был взят сульфат натрия, то в растворе, кроме ионов натрия и хлорид-ионов, будут еще и сульфат-ионы (естественно, гидратированные).
Допустим, что были взяты порции, равные по количеству вещества. Тогда в получившемся растворе, как мы уже выяснили, будут присутствовать только гидратированные ионы натрия и хлорид-ионы. Если отделить раствор от осадка (например, фильтрованием) и выпарить воду, то образуется кристаллический хлорид натрия
Таким образом, проводя последовательно несколько химических процессов, мы из исходных веществ (Na2SO4 и BaCl2) получили новые вещества (BaSO4 и NaCl). Все это можно выразить одним (суммарным) химическим уравнением:
Очень похоже на это уравнение и " молекулярное " уравнение той реакции, которая непосредственно протекает в водном растворе. Так для нашей реакции (реакции образования осадка сульфата бария из ионов бария и сульфат-ионов)
" молекулярное " уравнение реакции выглядит так:
Оно означает, что при взаимодействии раствора хлорида бария с раствором сульфата натрия образуется осадок сульфата бария и раствор хлорида натрия. Индекс " р " в таких уравнениях показывает, что данное вещество находится в растворе. Иногда этот индекс " для краткости " не пишут, и тогда " молекулярное " уравнение перестает отличаться от суммарного уравнения нескольких химических процессов. Этого следует избегать.
Формально описанная реакция образования сульфата бария является реакцией обмена (судя по " молекулярному" уравнению), но по существу это скорее реакция соединения. Ведь во время этой реакции ионы бария и сульфат-ионы, теряя гидратные оболочки, соединяются в кристаллы сульфата бария (смотри ионное уравнение).

С помощью таких реакций можно получить самые разнообразные нерастворимые или малорастворимые вещества, и не только соли, но и, например, гидроксиды:(На самом деле, реакция образования малорастворимых гидроксидов - более сложные процессы. Они относятся к кислотно-основным реакциям (см.§8). Здесь дается их сильно упрощенное описание)
На первых порах составлять уравнения реакций нам поможет логический шаблон, который представлен в виде таблицы (табл. 32).
Таблица 32 . Логический шаблон для составления уравнений реакций, протекающих в растворах
в растворе после
завершения реакции
Пусть нам надо составить уравнение реакции, протекающей при сливании растворов хлорида кальция и карбоната натрия.Исходными веществами I и II здесь являются CaCl2 и Na2CO3.
Взаимодействие их с водой (химическое растворение) может быть описано следующими уравнениями:
Таким образом до начала реакции в растворе оказываются следующие частицы:
Используя таблицу растворимости, находим, что из ионов Ca 2
aq может образоваться осадок нерастворимого в воде вещества CaCO3. Отметив это в таблице, составляем ионное уравнение:
Остающиеся после завершения реакции частицы ( Cl
aq , H2O) между собой не реагируют и представляют собой раствор NaCl. Убедившись в этом, составляем " молекулярное " уравнение реакции:
Заполненная для этой реакции таблица выглядит следующим образом:
12.1. Образование осадка
Большинство химических реакций, протекающих в природе, на заводах и в лабораториях, протекают в растворах.
Как и в других условиях, в растворах могут протекать реакции, сопровождающиеся передачей электронов (ОВР), реакции, сопровождающиеся передачей протонов (кислотно-основные реакции, КОР), и реакции, при которых не происходит ни того, ни другого. К последней группе относится большинство реакций, сопровождающихся образованием осадка.
Возьмем два вещества, сульфат натрия и хлорид бария, и растворим каждое из них в воде. Мы получим два раствора. Один из них, раствор сульфата натрия, состоит из молекул воды, гидратированных ионов натрия и гидратированных сульфат-ионов:
Другой раствор, раствор хлорида бария, состоит из молекул воды, гидратированных ионов бария и гидратированных хлорид-ионов:
Смешаем эти растворы. В получившемся растворе помимо молекул воды, казалось бы, должны присутствовать ионы:
Но практически мы обнаружим, что из раствора в виде осадка выделилось какое-то твердое вещество. Откуда же оно появилось? Очевидно, оно образовалось из присутствовавших в растворе ионов.
Соединяться, образуя ионные кристаллы, могут только разноименно заряженные ионы. Следовательно, выпавшим в осадок веществом может быть BaCl2, BaSO4, NaCl или Na2SO4. Но хлорид бария и сульфат натрия содержались в исходных растворах, а при смешивании этих растворов концентрация каждого из них уменьшилась, и потому никак не могла превысить растворимость. Следовательно, BaCl2 и Na2SO4 выпасть в осадок не могли. Остаются сульфат бария и хлорид натрия. Чтобы выяснить, какое из этих веществ выпало в осадок (а может быть, оба?), найдем эти вещества в таблице растворимости (приложение 11). NaCl растворим в воде, а BaSO4 в ней нерастворим, то есть в случае сульфата бария энергетически более выгодно существование кристаллов этого вещества, чем соответствующих гидратированных ионов. Следовательно, в осадок выпал сульфат бария. Уравнение этой реакции
означает, что вещество выделилось из раствора в виде осадка.
Что же осталось в растворе?
Если мы взяли порции хлорида бария и сульфата натрия, равные по количеству вещества, то в растворе остались только гидратированные ионы натрия и гидратированные хлорид-ионы. Если же какое-то из исходных веществ было взято в избытке, то избыток перешедших из него в раствор ионов тоже, естественно, останется в растворе. Так, если в избытке был взят сульфат натрия, то в растворе, кроме ионов натрия и хлорид-ионов, будут еще и сульфат-ионы (естественно, гидратированные).
Допустим, что были взяты порции, равные по количеству вещества. Тогда в получившемся растворе, как мы уже выяснили, будут присутствовать только гидратированные ионы натрия и хлорид-ионы. Если отделить раствор от осадка (например, фильтрованием) и выпарить воду, то образуется кристаллический хлорид натрия
Таким образом, проводя последовательно несколько химических процессов, мы из исходных веществ (Na2SO4 и BaCl2) получили новые вещества (BaSO4 и NaCl). Все это можно выразить одним (суммарным) химическим уравнением:
Очень похоже на это уравнение и " молекулярное " уравнение той реакции, которая непосредственно протекает в водном растворе. Так для нашей реакции (реакции образования осадка сульфата бария из ионов бария и сульфат-ионов)
" молекулярное " уравнение реакции выглядит так:
Оно означает, что при взаимодействии раствора хлорида бария с раствором сульфата натрия образуется осадок сульфата бария и раствор хлорида натрия. Индекс " р " в таких уравнениях показывает, что данное вещество находится в растворе. Иногда этот индекс " для краткости " не пишут, и тогда " молекулярное " уравнение перестает отличаться от суммарного уравнения нескольких химических процессов. Этого следует избегать.
Формально описанная реакция образования сульфата бария является реакцией обмена (судя по " молекулярному" уравнению), но по существу это скорее реакция соединения. Ведь во время этой реакции ионы бария и сульфат-ионы, теряя гидратные оболочки, соединяются в кристаллы сульфата бария (смотри ионное уравнение).
С помощью таких реакций можно получить самые разнообразные нерастворимые или малорастворимые вещества, и не только соли, но и, например, гидроксиды:(На самом деле, реакция образования малорастворимых гидроксидов - более сложные процессы. Они относятся к кислотно-основным реакциям (см.§8). Здесь дается их сильно упрощенное описание)
На первых порах составлять уравнения реакций нам поможет логический шаблон, который представлен в виде таблицы (табл. 32).
Таблица 32 . Логический шаблон для составления уравнений реакций, протекающих в растворах
в растворе после
завершения реакции
Пусть нам надо составить уравнение реакции, протекающей при сливании растворов хлорида кальция и карбоната натрия.Исходными веществами I и II здесь являются CaCl2 и Na2CO3.
Взаимодействие их с водой (химическое растворение) может быть описано следующими уравнениями:
Таким образом до начала реакции в растворе оказываются следующие частицы:
Используя таблицу растворимости, находим, что из ионов Ca 2
aq может образоваться осадок нерастворимого в воде вещества CaCO3. Отметив это в таблице, составляем ионное уравнение:
Остающиеся после завершения реакции частицы ( Cl
aq , H2O) между собой не реагируют и представляют собой раствор NaCl. Убедившись в этом, составляем " молекулярное " уравнение реакции:

Химические реакции, их свойства, типы, условия протекания и прочая, являются одним из краеугольных столпов интересной науки под названием химия. Попробуем же разобрать что такое химическая реакция, и какова ее роль. Итак, химической реакцией в химии принято считать превращение одного либо нескольких веществ, в другие вещества. При этом ядра атомов у них не меняются (в отличие от реакций ядерных), зато происходит перераспределение электронов и ядер, и, разумеется, появляются новые химические элементы.
Реакции в природе и быту
Мы с вами окружены химическими реакциями, более того мы сами их регулярно осуществляем различными бытовыми действиями, когда например, зажигаем спичку. Особенно много химических реакций сами того не подозревая (а может и подозревая) делают повара, когда готовят еду.
Разумеется, и в природных условиях проходит множество химических реакций: извержение вулкана, фотосинтез листвы и деревьев, да что там говорить, практически любой биологический процесс можно отнести к примерам химических реакций.

Типы реакций
Все химические реакции можно условно разделить на простые и сложные. Простые химические реакции, в свою очередь, разделяются на:
- реакции соединения,
- реакции разложения,
- реакции замещения,
- реакции обмена.
Далее мы подробно остановимся на каждом из этих видов химических реакций, известных химии.
Реакция соединения
Реакция разложения
Тут все просто, реакция разложения является противоположностью реакции соединения. При ней из одного вещества получается два или более веществ. Простым примером химической реакции разложения может быть реакция разложение мела, в ходе которой из собственно мела образуется негашеная известь и углекислый газ.
Реакция замещения
Реакция замещения осуществляется при взаимодействии простого вещества со сложным. Приведем пример химической реакции замещения: если опустить стальной гвоздь в раствор с медным купоросом, то в ходе этого простого химического опыта мы получим железный купорос (железо вытеснит медь из соли). Уравнение такой химической реакции будет выглядеть так:
Реакция обмена
Реакции обмена проходят исключительно между сложными химическими веществами, в ходе которых они меняются своими частями. Очень много таких реакций имеют место быть в различных растворах. Нейтрализация кислоты желчью – вот хороший пример химической реакции обмена.
Так выглядит химическое уравнение этой реакции, при ней ион водорода из соединения HCl обменивается ионом натрия из соединения NaOH. Следствием этой химической реакции является образование раствора поваренной соли.
Признаки реакций
По признакам протекания химических реакций можно судить прошла ли химическая реакция между реагентами или нет. Приведем примеры признаков химических реакций:
- Изменение цвета (светлое железо, к примеру, во влажном воздухе покрывается бурым налетом, как результат химической реакции взаимодействия железа и кислорода).
- Выпадение осадка (если вдруг через известковый раствор пропустить углекислый газ, то получим выпадение белого нерастворимого осадка карбоната кальция).
- Выделение газа (если Вы капнете на пищевую соду лимонной кислотой, то получите выделение углекислого газа).
- Образование слабодиссоциированных веществ (все реакции, в результате которых образуется вода).
- Свечение раствора (примером тут могут служить реакции, происходящие с раствором люминола, излучающего при химических реакциях свет).
В целом, трудно выделить какие признаки химических реакций являются основными, для разных веществ и разных реакций характерны свои признаки.
Как определить признак реакции
Определить признак химической реакции можно визуально (при изменении цвета, свечении), или по результатам этой самой реакции.
Скорость реакции
К факторам скорости химической реакции можно отнести:
- природу реагирующих веществ,
- наличие катализатора,
- температуру,
- давление,
- площадь поверхности реагирующих веществ.
Все они имеют самое прямое влияние на скорость протекания химической реакции.
Равновесие реакции
Химическим равновесием называют такое состояние химической системы, при котором протекает несколько химических реакций и скорости в каждой паре прямой и обратной реакции равны между собой. Таким образом, выделяется константа равновесия химической реакции – это та величина, которая определяет для данной химической реакции соотношение между термодинамическими активностями исходных веществ и продуктов в состоянии химического равновесия. Зная константу равновесия можно определить направление протекания химической реакции.
Условия возникновения реакций
Чтобы положить начало химических реакций, необходимо для этого создать соответствующие условия:
- приведение веществ в тесное соприкосновение.
- нагревание веществ до определенной температуры (температура химической реакции должна быть подходящей).
Тепловой эффект химической реакции
Так называют изменение внутренней энергии системы как результат протекания химической реакции и превращения исходных веществ (реактантов) в продукты реакции в количествах, соответствующих уравнению химической реакции при следующих условиях:
- единственно возможной работой при этом есть только лишь работа против внешнего давления.
- исходные вещества и продукты, полученные в результате химической реакции, имеют одинаковую температуру.
Видео
И в завершение интересно видео про самые удивительные химические реакции.
Автор: Павел Чайка, главный редактор журнала Познавайка
Эта статья доступна на английском языке – Chemical Reactions.
Похожие посты:
4 комментария
Спасибо за статью, хотелось бы также больше узнать про химические реакции ферментов и необратимые химические реакции.
Пожалуй эти темы заслуживают отдельной статьи.
1. Вы пишете: “Зная константу равновесия можно определить направление протекания химической реакции.” Одного знания константы равновесия бывает недостаточно. В общем случае, необходимо знать еще концентрации веществ.
2. Про тепловой эффект реакции сразу видно, что переписан без пояснений соответствующий абзац из учебника. Может даже не школьного. Но народу будет не до конца понятно.
3. В начале статьи вы заикаетесь о биохимических реациях и далее даже говорите о том, что есть сложные реакции. И далее не слова про них. Интуитивно понятно, что сложные реакции это совокупность нескольких. Но по хорошему надо бы хотя бы обозначить определение. И пару предложений сказать про биохимические реакции
4. Вы пишете: “К факторам скорости химической реакции можно отнести:
природу реагирующих веществ,
наличие катализатора,
температуру,
давление,
площадь поверхности реагирующих веществ.
Все они имеют самое прямое влияние на скорость протекания химической реакции.” Перфекционисту, такое утверждение будет резать слух. Например, вы ничего не говорите о концентрациях, а также не разделяете гомогенные и гетерогенные реакции-для них немного разный набор влияющих факторов. Некоторые из указанных вами факторов не так сильно влияют на скорость (если влияют вообще).
4. Указывая признаки протекания химической реакции вы выделяете яркие, заметные но не всегда проявляемые факторы, а также не эти признаки являются фундаментальным признаком протекания химической реакции. Таковым является изменение количества(концентрации) реагирующих веществ. И именно эти изменения фиксируют, т.н. кинетические кривые, снимаемые по ходу реакции графики зависимости какого-либо параметра от количества вещества.
5. Если уж вас спросили в комментариях, и вы сами вкратце касаетесь понятия химического равновесия и т.н. константы равновесия можете в дальнейшем указать, что необратимые это те реакции, у которых очень большое значение константы равновесия.
И еще предложение “При этом ядра атомов у них не меняются (в отличие от реакций ядерных), зато происходит перераспределение электронов и ядер, и, разумеется, появляются новые химические элементы.” Перечитайте! Кто отличает ядерные реакции от химических (условно говоря, 90% школьников) им это предложение ни к чему. А кто захочет разобраться (те самые 10% кто не различает ядерные и химические реакции) они ничего не поймут!
Часто мы даже не подозреваем, что на наших глазах идет химическая реакция, а нередко и сами являемся ее участниками. Разбираемся, что же такое химические реакции, каковы их типы, классификация, скорость и признаки



Без химических реакций была бы невозможна эволюция в природе. В открытом космосе встречаются в основном только атомы водорода (H) и гелия (He). Это объясняется отсутствием необходимых условий для прохождения химических реакций.
Химическая реакция – это процесс превращения одного или нескольких веществ в другие вещества, в результате чего происходит перераспределение электронов и ядер. Сами ядра атомов при этом не меняются:
Химические реакции нельзя путать с физическими процессами. В физических процессах вещества сохраняют свой состав, хотя могут образовывать смеси, изменять внешнюю форму либо агрегатное состояние. Так, превращение воды в пар или лед является физическим процессом, а не химической реакцией. Химическое взаимодействие, в результате которого образуется вода, описывается формулой:
Отличаются химические реакции и от ядерных реакций, в которых происходят изменения в ядрах атомов и образуются атомы новых элементов. В ходе химических процессов новые вещества получаются в результате изменений, происходящих в электронной оболочке атомов.
Выделяют следующие типы химических реакций: реакции соединения, разложения, замещения и обмена.
Реакция соединения представляет собой образование одного сложного вещества в результате соединения двух или более веществ. Например:
В результате реакции разложения происходит распад одного сложного вещества на несколько простых.
Реакция замещения протекает между простыми и сложными веществами, при этом атомы простого вещества замещают атомы одного из элементов в сложном веществе.
Zn + 2HCL = ZnCl₂ + H₂
Реакция обмена возможна между двумя сложными веществами, в результате чего они обмениваются своими составными частями и образуются два новых сложных вещества.
MgO + H2SO₄ = MgSO₄ + H₂O

Существует целый ряд признаков, по которым можно классифицировать химические реакции: по агрегатному состоянию, по изменению степеней окисления реагентов, по тепловому эффекту реакции, по направлению протекания, по наличию катализаторов.
По агрегатному состоянию (газообразному, жидкому, твердому) реагирующих веществ химические реакции подразделяются на гомогенные и гетерогенные. Гомогенные реакции протекают в одной фазе, например, в виде раствора:
HCl + NaOH = NaCl + H₂O
Гетерогенные реакции осуществляются на границе раздела двух фаз. Например, твердое вещество и газ:
По изменению степеней окисления реагентов выделяют окислительно- восстановительные реакции. Окисление – это процесс отдачи электронов, что приводит к увеличению степени окисления. Восстановление – это присоединение электронов и уменьшение степени окисления. Элемент, отдающий электроны, называется восстановителем, а элемент, принимающий электроны, – окислителем. Например, в реакции Fe + CuSO₄ = FeSO₄ + Cu железо отдает два электрона и является восстановителем, а медь принимает два электрона и выступает в качестве окислителя.
По тепловому эффекту химические реакции делятся на экзотермические (сопровождающиеся выделением тепла +Q) и эндотермические (идущие с поглощением тепла -Q).
Яркий пример экзотермических реакций – процесс горения:
CH₄ + 2O₂ = CO₂ + 2H₂O +Q
К эндотермическим реакциям относятся реакции разложения:
CaCO₃ = CaO + CO₂ –Q
По направлению протекания химические реакции бывают обратимыми и необратимыми. Обратимые реакции одновременно протекают в двух противоположных направлениях: H₂ + I₂ = 2HI
Необратимые реакции идут только в одном направлении: 2Mg + O₂ = 2MgO
По наличию катализаторов (веществ, участвующих в реакции, изменяющих ее скорость, но остающихся неизменными после завершения реакции) химические реакции подразделяются на каталитические (протекающие в присутствии катализаторов) и некаталитические (идущие без катализаторов). В уравнениях каталитических реакций химическая формула катализатора записывается над знаком равенства или обратимости.
Скорость химической реакции показывает, как изменяется концентрация реагирующих веществ в единицу времени. Скорость реакции тем выше, чем больше количество реагирующих веществ и чем меньше время самой реакции. Данные процессы изучаются специальным разделом химии – химической кинетикой.
Скорость химических реакций зависит от следующих условий: наличие катализатора, степень измельченности реагирующих веществ, давление и температура, природа веществ, вступающих в реакцию, концентрация реагентов.
В соответствие с правилом Вант-Гофа в случае возрастания температуры на каждые 10 градусов по Цельсию скорость химической реакции увеличивается в 2-4 раза.
В результате химических реакций происходит превращение одних веществ в другие. При этом изменяются не только сами вещества, но и их свойства. Такие изменения и являются признаками химических реакций. К ним относятся:
- Яркое свечение и выделение или поглощение тепла

Скорость химической реакции зависит от целого ряда факторов.
1. Природа веществ, вступающих в химическую реакцию. Так, чем активнее металл, тем он быстрее окисляется и более бурно взаимодействует с водой. Знание природы реагирующих веществ позволяет предсказать скорость протекания химической реакции.
2. Концентрация реагентов. Чем выше их концентрация, тем больше скорость реакции, поскольку с увеличением концентрации возрастает количество столкновений молекул реагирующих веществ. Например, горение в чистом кислороде идет гораздо активнее, чем на воздухе, так как концентрация кислорода в воздушной среде в пять раз ниже.
3. Площадь поверхности реагирующих веществ. Чем эта площадь больше, тем выше скорость реакции. Твердые вещества поэтому измельчают, а жидкости – распыляют. К примеру, если кусок мрамора превратить в порошок, то его реакция с соляной кислотой намного ускорится.
4. Температура. Повышение температуры на каждый градус ведет к возрастанию скорости реакции. Это связано с увеличение числа активных молекул, имеющих повышенную энергию, способствующую вступлению веществ в химическую реакцию.
5. Давление. Оно оказывает существенное воздействие на скорость реакции в газообразном состоянии. При увеличении давления скорость реакции возрастает, что объясняется повышением концентрации молекул реагирующих веществ.
6. Катализатор. Скорость реакции увеличивается в присутствии специальных веществ – катализаторов. Они образуют промежуточные вещества, которые более активно реагируют между собой. При этом сам катализатор в процессе реакции не расходуется. Существуют также вещества, замедляющие процесс реакции (ингибиторы).
Читайте также: