Химические источники тока кратко
Обновлено: 08.07.2024
Химические источники тока (ХИТ) — эта тема имеет высокое практическое значение. Это кардиостимуляторы, электромобили, которые пытаются сохранить экологию, портативные устройства, включая фото и видеотехнику, компьютерную технику, навигаторы. За последние годы прогресс химических источников тока произошел большой, от известных свинцовых аккумуляторов, которые постепенно вытесняются литий-ионными, литий-полимерными и другими аккумуляторами.
В этой области борьба идет за мощность, емкость, которая позволяет максимально долго использовать источники тока. Дополнительным стимулом к их развитию является создание гибких источников тока. Научная составляющая в этой области лежит в плане разработки материалов для таких химических элементов.
Устройство и работа
Химические источники тока состоят из электродов и электролита, который находится в емкости. Электрод, на котором окисляется восстановитель, называется анодом. Электрод, на котором восстанавливается окислитель, называется катодом. В общем получается электрохимическая система.
Попутным результатом такой реакции стало возникновение тока. Восстановитель передает электроны на окислитель, который восстанавливается. Электролит, который находится между электродами, нужен для прохождения реакции. Если перемешать порошки различных двух металлов, то электричество не возникнет, энергия появится в виде теплоты. Электролит необходим для упорядочения процесса движения электронов. Электролит состоит обычно из раствора соли или расплавленного вещества.
Электроды имеют вид решеток или пластин из металла. При помещении их в раствор электролита получается разность потенциалов пластин. Анод отдает электроны, а катод их принимает. На поверхности возникают химические реакции. Когда цепь размыкается, то реакции прекращаются. Если реагенты закончились, то реакция также больше не идет. Если удалить один из электродов, то цепь размыкается.
Из чего состоят химические источники тока
В качестве окислителей применяются соли и кислородосодержащие кислоты, а также нитроорганические вещества, кислород. В качестве восстановителей применяются металлы, оксиды, углеводороды.
Электролит может состоять из:
- Соли, щелочи и кислоты, растворенные в воде.
- Соли в растворе, с возможностью электронной проводимости.
- Расплавленные соли.
- Твердые вещества с подвижным ионом.
- Электролиты в виде матрицы. Это растворы жидкости, расплавы, которые находятся в порах электроносителя.
- Электролиты с ионным обменом. Твердые вещества с закрепленными ионогенными группами, с одним знаком. С другим знаком ионы подвижны. Эта характеристика позволяет создать однополярную проводимость.
Гальванические элементы
Напряжение на ячейке составляет 0,5-4 вольта. В химических образцах источника применяют гальваническую батарею, которая состоит из элементов. Может использоваться параллельная схема нескольких элементов. При последовательной схеме в цепь включены одинаковые батареи. Они должны обладать одинаковыми свойствами, с одной конструкцией, технологией, типоразмером. Для схемы параллельного соединения подойдут элементы с различными свойствами.
Классы
Химические источники тока делятся по следующим свойствам:
- Размерности.
- Конструктивным особенностям.
- Применяемым химическим веществам.
- Источнику реакции.
Эти свойства создают эксплуатационные параметры источников, которые подходят для определенной области использования.
Деление на классы электрохимических источников основывается на отличии в способе действия устройства. По этим свойствам их различают:
- Первичные источники – для однократного применения. В них заключен определенный запас веществ, который будет израсходован при реакции. Когда произойдет разряд, ячейка исчерпывает свою способность к работе. Первичные источники, основанные на химических реакциях, называются элементами. Наиболее простой элемент – это батарейка типа АА.
- Химические источники тока , которые имеют возможность перезаряжаться, называются аккумуляторами, это вторичные многоразовые элементы. Израсходованные химические элементы могут регенерироваться и снова накопить энергию, путем подключения к ним тока. Это называется зарядкой элементов. Такие элементы применяют длительное время, так как их легко зарядить. В процессе разряда вырабатывается электрический ток. К таким источникам можно причислить элементы питания различных видов приборов и устройств, таких как смартфоны, ноутбуки и т.д.
- Тепловые химические источники тока – это приборы постоянного действия. В результате их работы постоянно поступает новая порция веществ и удаляется использованный продукт реакции.
- В смешанных элементах находится запас реагента. Другой реагент поступает в устройство снаружи. Время действия устройства имеет зависимость от резерва первого вещества. Комбинированные элементы применяются в качестве аккумуляторов, когда имеется возможность регенерации их заряда через прохождение тока от внешнего питания.
- Химические источники тока, которые могут возобновлять заряд , заряжаются разными способами. В них можно заменять израсходованные реагенты. Такие источники действуют не постоянно.
Свойства
Основные характеристики ХИТ можно перечислить в таком виде:
- Разрядное напряжение. Это свойство имеет зависимость от определенной электрохимической системы. А также оказывает влияние процент концентрации электролита, температура, ток.
- Мощность.
- Разрядный ток, зависящий от сопротивления цепи.
- Емкость, наибольшее количество энергии, которое источник выдает при общем разряде.
- Запас энергии – наибольшая энергия, которая получена при полном разряде устройства.
- Энергетические свойства и характеристики. Для батарей аккумуляторов это число циклов заряда и разряда, без уменьшения емкости и напряжения (ресурс).
- Температурный интервал работы.
- Сохраняемый срок – наибольший допускаемый период времени от изготовления до первого разряда элемента.
- Время службы – наибольший допускаемый срок работы и хранения. Для элементов на топливе имеют значение сроки работы при постоянной и периодической работе.
- Полная энергия, отданная за все время работы.
- Механическая, вибрационная прочность.
- Возможность функционирования в любом положении.
- Надежная работа.
- Простота в уходе.
Сахарная батарея
Чтобы произвести литий-ионные аккумуляторы в Японии закупают материалы в других странах. Это негативно сказывается на экономическом положении страны. Поэтому ученые ищут способы изготовления аккумуляторов из того сырья, которое имеется в наличии. Таким сырьем в Японии стал сахар. Аккумулятор на сахаре в Японии по свойствам имеет надежность и энергоемкость выше обычных аналогов, и стоимость его ниже.
Большой спрос на литий, который вызван резким распространением переносных аккумуляторов, озаботил производителей аккумуляторов, так как этот элемент добывается только в странах с политической нестабильностью. Это явилось вторым фактором поиска альтернативных материалов для недорогих аккумуляторов с высокой надежностью. Сахароза легко преобразуется в дешевый материал для анодного сырья в литий-ионных батареях.
Сахар нагревают в условиях вакуума под давлением до 1500 градусов. Он превращается в порошок, состоящий из углерода, который может повысить заряд на 20% больше аналогичных изделий. Это явилось первым шагом в разработке дешевых батарей. Пока такие виды батарей не составляют конкуренции современным аккумуляторам. Но ученые предполагают, что в будущем подобные разработки вытеснят дорогие изделия.
Требования
Конструктивные особенности химических источников тока должны создавать условия, которые способствовали бы максимальной эффективности химических реакций.
К таким условиям можно отнести:
- Недопущение утечек тока.
- Постоянная работа.
- Герметичность.
- Раздельное помещение реагентов.
- Качественное контактирование электролита с электродами.
- Хороший отвод тока из объекта химической реакции до наружного вывода с наименьшими потерями.
К химическим элементам предъявляются требования:
- Повышенные значения свойств.
- Максимальный диапазон температуры работы.
- Наибольшее напряжение.
- Минимальная себестоимость электричества.
- Постоянное значение напряжения.
- Хорошее сохранение заряда.
- Безопасное функционирование.
- Простое обслуживание, или ее отсутствие.
- Долговременная работа.
Эксплуатация источников тока
Основное достоинство первичных элементов состоит в отсутствии надобности обслуживания. Перед работой нужно просто осмотреть их, определить срок годности. При включении в цепь нельзя путать полярность и допускать повреждения контактов. Сложные конструкции источников требуют особого ухода. Цель его заключается в удлинении срока службы до максимума.
Уход за аккумуляторами требует выполнения следующих мероприятий:
- Обеспечение чистоты.
- Контроль параметра напряжения отключенной цепи.
- Обеспечение необходимого уровня электролита, доливки дистиллированной воды.
- Проверка концентрации электролита ареометром.
При использовании батареек (гальванических элементов) нужно выполнять требования, которые относятся к применению электрических приборов.
Сфера использования
В современное время химические источники тока используются в:
- Транспорте.
- Переносных устройствах.
- Космической технике.
- Оборудовании научных исследований.
- Медицинских приборах.
Применяются в бытовой сфере:
- Батарейки (сухие).
- Батареи аккумуляторов электроники.
- Аккумуляторы на автомобилях.
Большое распространение нашли литиевые химические источники тока. Это обусловлено наличием у лития максимальной удельной энергии. Он отличается наиболее отрицательным потенциалом электрода из металлов. Батареи литий ионного типа опередили все другие источники по размеру значений удельной энергии. В настоящее время ученые разрабатывают различные усовершенствования литиевых аккумуляторов. Разработки ведутся в направлении получения конструкций корпуса сверхмалой толщины, которые будут использоваться для питания смартфонов и подобных им гаджетов, а также создание сверхмощных батарей аккумуляторов.
В последнее время серьезные работы ученых ведутся по изобретению и модернизации топливных батарей – устройств, которые создают электрическую энергию, за счет проведения химических реакций веществ, постоянно подающихся к электродам снаружи. Для окисления берут кислород, а в качестве топлива пытаются использовать водород. На основе таких батарей уже действуют некоторые опытные образцы на электростанциях.
Химические источники тока: основные характеристики

Уже более двух столетий человечество использует энергию химических реакций между различными веществами для получения постоянного тока.
Принцип работы
Окислительно-восстановительная реакция, протекающая между веществами, обладающими свойствами окислителя и восстановителя, сопровождаются выделением электронов, движение которых образует электрический ток. Однако, чтобы использовать его энергию, необходимо создать условия для прохождения электронов через внешнюю цепь, в противном случае она при простом смешивании окислителя и восстановителя выделяется во внешнюю среду теплом.
Поэтому все химические источники тока имеют два электрода:
анод, на котором происходит окисление;
катод, осуществляющий восстановление вещества.
Электроды на расстоянии помещены в сосуд с электролитом — веществом, проводящим электрический ток за счет процессов диссоциации среды на ионы.
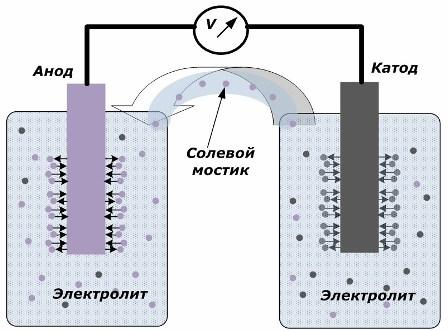
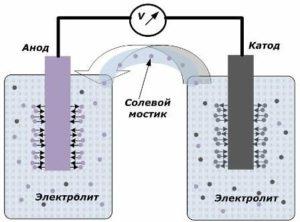
Принцип преобразования химической энергии в электрическую
На рисунке показано, что электроды размещены в отдельных сосудах, соединенных солевым мостиком, через который создается движение ионов по внутренней цепи. Когда внешняя и внутренняя цепь разомкнуты, то на электродах протекают два процесса: переход ионов из металла электрода в электролит и переход ионов из электролита в кристаллическую решетку электродов.
Скорости протекания этих процессов одинаковы и на каждом электроде накапливаются потенциалы напряжения противоположных знаков. Если их соединить через солевой мостик и приложить нагрузку, то возникнет электрическая цепь. По внутреннему контуру электрический ток создается движением ионов между электродами через электролит и солевой мостик. По внешней цепи возникает движение электронов по направлению от анода на катод.
Практически все окислительно-восстановительные реакции сопровождаются выработкой электроэнергии. Но ее величина зависит от многих факторов, включающих объемы и массы используемых химических веществ, примененных материалов для изготовления электродов, типа электролита, концентрации ионов, конструкции.
Наибольшее применение в современных химических источниках тока нашли:
для материала анода (восстановителя) — цинк (Zn), свинец (Pb), кадмий (Cd) и некоторые другие металлы;
для материала катода (окислителя) — оксид свинца PbO2, оксид марганца MnO2, гидроксооксид никеля NiOOH и другие;
электролиты на основе растворов кислот, щелочей или соли.
Способы классификации
Одна часть химических источников тока может повторно использоваться, а другая нет. Этот принцип взят за основу их классификации.
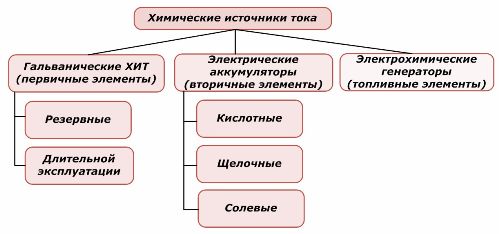
Классификация химических элементов
Электродвижущая сила гальванических элементов, в зависимости от конструкции, достигает 1,2÷1,5 вольта. Для получения больших значений их объединяют в батареи, соединяя последовательно. При параллельном подключении батарей увеличивается ток и мощность.
Принято считать, что первичные химические источники тока не поддерживают повторную зарядку, хотя более точно это положение можно сформулировать по-другому: ее проведение экономически не целесообразно.
Резервные первичные химические источники тока хранятся в состоянии, когда электролит изолирован от электродов. Это исключает протекание окислительно-восстановительной реакции и обеспечивает готовность к вводу в работу. Они не используются повторно. Срок хранения резервных химических источников тока ограничен в 10÷15 лет.
Аккумуляторы успешно перезаряжаются приложением внешней электрической энергии. Благодаря этой возможности их называют вторичными источниками тока. Они способны выдерживать сотни и тысячи циклов заряда-разряда. ЭДС аккумулятора может быть в пределах 1,0÷1,5 вольта. Их тоже объединяют в батареи.
Электрохимические генераторы работают по принципу гальванических элементов, но у них для проведения электрохимической реакции вещества поступают извне, а все выделяющиеся продукты удаляются из электролита. Это позволяет организовать непрерывный процесс.
Основные рабочие характеристики химических источников тока
1. Величина напряжения на разомкнутых клеммах
В зависимости от конструкции единичный источник может создавать только определенную разность потенциалов. Для использования в электрических устройствах их объединяют в батареи.
2. Удельная емкость
За определенное время (в часах) один химический источник тока может выработать ограниченное количество тока (в амперах), которые относят к единице веса либо объема.
3. Удельная мощность
Характеризует способность единицы веса или объема химического источника тока вырабатывать мощность, образованную произведением напряжения на силу тока.
4. Продолжительность эксплуатации
Еще этот параметр называют сроком годности.
5. Значение токов саморазряда
Эти побочные процессы электрохимических реакций приводят к расходу активной массы элементов, вызывают коррозию, снижают удельную емкость.
6. Цена на изделие
Зависит от конструкции, применяемых материалов и ряда других факторов.
Лучшими химическими источниками тока считаются те, у которых высокие значения первых четырех параметров, а саморазряд и стоимость низкие.
Принципы заряда аккумуляторов
Среди вторичных химических источников тока большую популярность набирают литий ионные модели, которые стали массово применяться для питания электронных устройств. У них материалом положительного электрода используется LiMO2 (M Co, Ni, Mn), а отрицательного — графит.
При заряде ионы лития от приложенной внешней энергии выделяются из металла катода, проходят через электролит и проникают в пространство между слоями графита, накапливаясь там.
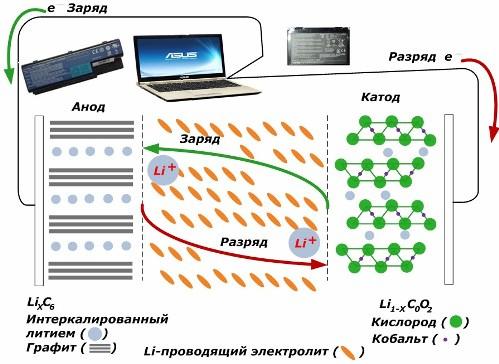
Когда энергия зарядного устройства отсутствует, а к электродам подключена нагрузка, то ионы лития в электролите двигаются в противоположную сторону.
Если заряд и разряд не проводятся, то энергия в аккумуляторе не расходуется, а сохраняется. Но ее количество ограничивается свойствами применяемых материалов. К примеру, у литий-ионных аккумуляторов значение удельной электроемкости составляет 130÷150 мАч/г. Оно лимитировано свойствами материала анода. Для графита емкость выше примерно в два раза.
Ученые сейчас ищут способы повышения емкости аккумулятора, изучают возможности использования химической реакции, проходящей между литием и кислородом воздуха. Для этого разрабатываются конструкции с воздушным, не расходуемым катодом, используемые в отдельных аккумуляторах. Этот метод может до 10 раз увеличить плотность энергии.
Эксплуатация химических источников тока требует знания основ электротехники, электрохимии, материаловедения и физики твердых тел.
Химические источники тока — это устройства и приборы которые в процессе химической окислительно-восстановительной реакции выделяют напряжение. Также они называются электрохимическими, гальваническими элементами. Основной принцип действия их основан на взаимодействии химических реагентов которые вступая, в реакцию друг с другом вырабатывают электроэнергию, в виде постоянного тока. Этот процесс происходит без механического или теплового воздействия, что является основными факторами играющими превосходящую роль среди других генераторов постоянного напряжения. Химические источники тока, сокращённо ХИТ, уже давно нашли применение не только в быту, но и на производстве.
Немного истории создания ХИТ
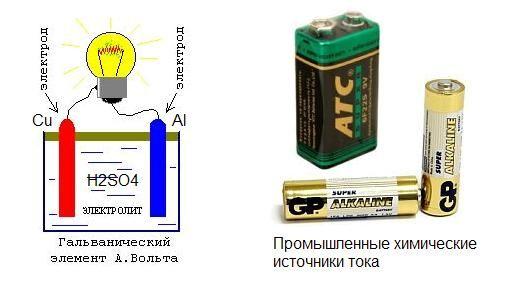
Ещё в восемнадцатом веке итальянский учёный Луиджи Гальвани придумал простейший элемент который химическим способом выделял электрический ток. Однако он был не только учёным, но и физиком, врачом, физиологом. Он интересовался и проводил опыты которые были направлены на изучение реакции животных на внешние раздражители. Как и всё гениальное первый химический источник энергии был получен Луиджи абсолютно случайно, во время многочисленных экспериментов над лягушками. После присоединения двух пластин из металла к лягушачьей мышце на лапке, было замечено мускульное сокращение. Гальвани посчитал это нервной реакцией на внешний раздражитель и изложил это в результатах своих исследований, попавших в руки другого великого учёного Алессандро Вольта. Он и выложил свою теорию о возникновении напряжения в результате химической реакции, возникшей между двумя металлическими пластинами в среде мускульной ткани лягушки.
Первый химический источник электрического тока представлял собой емкость с соляным составом, в который было погружено две пластины из разных материалов. Одна из меди, другая из цинка. Именно это устройство в будущем, а конкретнее во второй половине девятнадцатого века, было применено при изобретении и создании марганцево-цинкового элемента внутри которого был тот же солевой электролит.
Принцип действия
Устройства вырабатывающее электрический ток содержит два электрода, которые помещаются между электролитом. Именно на их границе соприкосновения и появляется небольшой потенциал. Один из них называют катодом, а другой анодом. Все эти элементы вместе образуют электрохимическую систему.
Во время возникновения окислительно-восстановительной реакции между электродами один элемент отдаёт мельчайшие частицы электроны другому. Поэтому она и не может происходить вечно, а со временем просто теряются свойства каждого элемента этой цепи.
Электроды могут быть представлены в виде пластин или решёток из металла. После погружения их в среду с электролитом меду их выводами возникает разность потенциалов, которая именуется напряжением разомкнутой цепи. Даже при удалении хотя бы одного из электродов с электролита процесс генерации напряжения прекращается.
Состав электрохимических систем
В качестве электролита используются следующие химические вещества:
- Водные растворы на основе щелочей, кислот, солей и т. д.;
- Растворы с ионной проводимостью на неводной основе, которые получены при растворении солей в неорганических или органических растворителях;
- Твердые соединения, содержащие ионную решетку, где один из ионов является подвижным;
- Матричные электролиты. Это особый вид жидких растворов и расплавов, которые находятся в порах твёрдого непроводящего элемента — электроносителя;
- Расплавы солей;
- Ионообменные электролиты с униполярной системой проводимости. Твёрдые тела с фиксированной ионогенной группой одного знака.
Классификация гальванических элементов и их подбор
Генераторы электрического тока получающегося во время химической реакции разделяются по:
- Размерам;
- Конструктивным особенностям;
- Способу и реагенту, за счёт которого, и получается электроэнергия.
Все элементы вырабатывающее ток во время химической реакции делятся на:
- Заряжаемые, которые в процессе эксплуатации могут неоднократно заряжаться от источника постоянного тока, они называются аккумуляторами;
- Не заряжаемые, то есть источники одноразового использования которые после завершения химической реакции просто приходят в негодность и должны быть утилизированы. Попросту это гальванический элемент или батарейка.
Для того чтобы подобрать источник электроэнергии, основанный на химической реакции, нужно понимать его характеристики, к которым относятся:
- Напряжение между анодом и катодом при разомкнутой цепи. Этот показатель чаще всего зависит от выбранной электрохимической системы, а также концентрации и вылечены всех составляющих;
- Мощность источника;
- Показатель силы тока;
- Емкость;
- Электротехнические показатели, то есть количество циклов заряда и разряда;
- Диапазон рабочих температур;
- Срок хранения между тем временем как элемент был создан и до начала его эксплуатации;
- Полный срок службы;
- Прочность, то есть защита корпуса от различных механических повреждений и влияний, а также вибраций;
- Положение работы, некоторые из них работают только в горизонтальных положениях;
- Надёжность;
- Простота в эксплуатации и обслуживании. В идеале отсутствие необходимости малейшего вмешательства в работу в течение всего срока эксплуатации.
При выборе нужной батареи или аккумулятора обязательно нужно учесть его электрические номиналы такие как напряжение и ток, а также ёмкость. Именно она является ключевой для сохранения работоспособности, подключаемого к источнику прибора.
Современные химические источники тока и их применение

Современный быт человека тяжело приставить без этих мобильных генераторов энергии, с которыми он сталкивается в течение всей жизни, начиная с детских игрушек и заканчивая, допустим, автомобилем.
Сферы применения различных батареек и аккумуляторов настолько разнообразны что перечислить их очень сложно. Работа любого мобильного телефона, компьютера, ноутбука, часов, пульта дистанционного управления была бы невозможна без этого переносного и очень компактного устройства для создания стабильного электрического заряда.
В медицине широко используются источники химической энергии при создании любого аппарата, помогающего человеку полноценно жить. Например, для слуховых аппаратов и электрокардиостимуляторов которые могут работать только от переносных источников напряжения, чтобы не сковывать человека проводами.
В производстве применяются целые системы аккумуляторных батарей для обеспечения напряжением цепей отключения и защит в случае пропадания входящего высокого напряжения на подстанциях. И также широко применяется это питание во всех транспортных средствах, военной и космической технике.
Одним из видов распространённых батарей являются литиевые источники электрического тока, так как именно этот элемент обладает высоким показателем удельной энергии. Дело в том что только этот химический элемент, оказывается, обладает сильным отрицательным потенциалом среди всех известных и изученных человеком веществ. Литий-ионные батареи выделяются среди всех остальных элементов питания по величине вырабатываемой энергии и низким габаритам, что позволяет применять их в самых компактных и мелких электронных устройствах.
Способы утилизации химических источников энергии

Проблема утилизации разных по габаритах химических источников напряжения является экологической проблемой всей планеты. Современные источники содержат в себе до тридцати химических элементов которые могут нанесите ощутимый вред природным ресурсам, поэтому для их утилизации разработаны целые программы и построены специализированные цеха по переработке. Некоторые методы позволяют не только качественно перерабатывать эти вредные вещества, но и возвращать в производство, тем самым защитив окружающую среду. В целях извлечения цветных металлов из батарей и аккумуляторов в настоящий момент разработаны и применены в цивилизованных странах, следящих и заботящихся об окружающей среде, целые пирометаллургические и гидрометаллургические комплексы. Самый же распространённый способ утилизации отработанных химических источников тока является метод, работающий на соединении этих процессов. Главным его достоинством считается высокая степень извлечения с минимальным количеством отходов.
Этот метод пирометаллургической, гидрометаллургической и механической переработки включает в себя восемь основных стадий:
- Измельчение;
- Магнитная сепарация;
- Обжиг;
- Дополнительное измельчение;
- Выделение крупных и мелких элементов с помощью грохочения;
- Водное очищение и выщелачивание;
- Сернокислотное выщелачивание;
- Электролиз.
Организация правильного сбора и утилизации ХИТ позволяет максимально уменьшить негативное влияние как на окружающую природу, так и на здоровье самого человека.
Химические источники тока сегодня актуальны, хотя и были изобретены более 2 веков назад. В настоящее время более современные варианты устройств практически вытеснили свинцовые аккумуляторы. Наука пытается создать менее опасные типы химических источников тока для окружающей среды, но с большей эффективностью работы, которая будет еще и долгосрочной. Ведется поиск путей достижения данной цели, которые еще и будут менее затратными, чтобы сделать устройство максимально доступным.
Что такое химические источники тока
Химический источник электрического тока — это устройство, благодаря конструкции которого в результате протекания окислительно-восстановительной реакции происходят выработка и подача постоянного электрического тока.

Литий-ионные источники тока — прогресс современности среди химических источников тока
К сведению! Чисто внешне устройства могут быть разными. Первые представляли собой две емкости, между которыми формировали металлический мостик. Теперь это достаточно портативные конструкции, которые могут иметь самые маленькие размеры и формы.
Зачем нужны
Химические источники электрической энергии нужны, чтобы приводить в действие портативные приборы, которые могут работать не от сети. Некоторые типы источников могут длительное время подпитывать весь механизм, приводя его в действие.
Благодаря открытию данных элементов стало возможным развитие таких отраслей, как автомобилестроение, космонавтика, а также сферы приборов бытового использования. Возможности человечества значительно расширились. Теперь не обязательно подключаться к электросети при необходимости использования некоторого устройства, которое требует наличия электрического тока.
Любой ученый знает, что химические источники тока очень важны для человечества. Но и простой пользователь сразу же оценит важность таких приспособлений, если лишится возможности пользоваться, например, телефоном, плеером. Кроме этого, такие варианты относительно портативные и могут обеспечить небольшой объект электрическим током.
Классификация
Самые распространенные виды — гальванические элементы и аккумуляторы. С ними знаком практически каждый. Но классификация таких приспособлений более широкая и предполагает еще и существование топливных элементов.
Гальванические элементы
Гальванический элемент получил свое название в честь ученого Гальвано, который и открыл чудесную возможность получения электрического тока посредством создания простой конструкции из электролита и электродов. Они считаются первыми прототипами современных устройств для получения электроэнергии благодаря химическим реакциям.
Обратите внимание! В настоящее время это приспособление имеет более компактный и безопасный для использования вид, это обычная батарейка. Особенность работы такого устройства заключается в том, что использование его одноразовое. После окончательного разложения электролита на вещества, повторно зарядить их для следующих реакций невозможно.
Электрические аккумуляторы
Электрический аккумулятор — это более универсальный вариант устройства, который можно заряжать несколько раз после потери заряда электролита. Такая особенность объясняется регенерацией веществ, которые образуют электролит.

Устройство аккумулятора
В данном случае зарядка производится от постороннего (внешнего) источника тока. Часто с такой потребностью в восстановлении реагента в аккумуляторах сталкиваются автомобилисты, производя зарядку аккумулятора.
Топливные элементы
Электрохимический топливный элемент является перспективным источником, который достаточно важен для создания комфортных и в некоторых ситуациях жизненно необходимых условий существования.

Тепловой химический источник
Особенность работы такого элемента заключается в следующем. К электродам каждый раз поступает определенная порция электролита, которая после разрядки выводится из конструкции. Например, резервный генератор тока благодаря такому принципу работы может производить электроэнергию в течение 10-15 лет.
Обратите внимание! После истечения срока эксплуатацию можно продлить, если восстановить питание.
Принцип работы
Химический источник, который вырабатывает постоянный ток, имеет определенный принцип работы. Алгоритм выработки электроэнергии посредством протекания химических реакций между некоторыми веществами достаточно прост для понимания, разобраться с этим сможет человек, далекий от химии или физики.
Важно! Из-за использования достаточно агрессивных типов веществ, которые входят в состав таких источников, самостоятельно вскрывать конструкции запрещено. Это может нанести вред здоровью и жизни. Дополнительно требуется определенная утилизация.
Между окислителем и восстановителем (электролитом) протекает окислительно-восстановительная реакция. В результате выделяются электроны, которые начинают последовательно двигаться в определенном направлении. Именно благодаря выделенной в результате химреакции энергии и происходит движение элементарных заряженных частиц.
Так и получается электрический ток, который нужно уметь еще и добыть. Если не создать нужные условия для выхода электронов на внешнюю цепь, то вещество будет выделять только тепло. Чтобы это сделать, нужно подготовить два электрода: анод (где происходит окисление) и катод (восстанавливает вещество).
Величина электроэнергии, которая получается в результате протекания окислительно-восстановительной реакции, зависит от таких факторов:
- объем и концентрация электролита;
- материал, из которого изготовлены электроды;
- конструкция внешней электрической цепи.
Есть несколько вариантов наиболее эффективных и применяемых электролитов с определенной концентрацией и массой.
Где применяются
Кажется, что вырабатываемый ток в результате химической энергии имеет минимальные показатели и может применяться только для изготовления обычных батареек в плеер или часы. Но это не так. Электроэнергия, полученная таким образом, используется в таких сферах:
Благодаря своей конструкции и принципу работы подобные устройства являются универсальными и могут применяться во многих сферах и отраслях.
Обратите внимание! Самой популярной в настоящее время является химическая батарея, которая используется в быту и производствах, подпитывая разнообразные приборы и устройства. Также в повседневной жизни используются аккумуляторы для электроники и автомобилей.
Электроэнергия — это жизненно необходимый ресурс для современного человечества. Получить электричество можно благодаря определенным источникам тока, но самыми популярными и удобными являются именно химические. Дополнительно они считаются весьма безопасными в экологическом плане для использования, если правильно их утилизировать.
Читайте также:

