Устройство калориметра принцип действия кратко
Обновлено: 04.07.2024
Калориметр
Современные калориметры работают в диапазоне температур от 0,1 до 3500 К и позволяют измерять количество теплоты с точностью до 10 -2 %. Устройство калориметров весьма разнообразно и определяется характером и продолжительностью изучаемого процесса, областью температур, при которых производятся измерения, количеством измеряемой теплоты и требуемой точностью.
Калориметр, предназначенный для измерения суммарного количества теплоты Q, выделяющейся в процессе от его начала до завершения, называют калориметром-интегратором; калориметр для измерения тепловой мощности L и её изменения на разных стадиях процесса — измерителем мощности или калориметром-осциллографом. По конструкции калориметрической системы и методу измерения различают жидкостные и массивные калориметры, одинарные и двойные (дифференциальные).
Калориметрические измерения позволяют непосредственно определить лишь сумму теплот исследуемого процесса и различных побочных процессов, таких как перемешивание, испарение воды, разбивание ампулы с веществом и т.п. Теплота побочных процессов должна быть определена опытным путём или расчётом и исключена из окончательного результата. Одним из неизбежных побочных процессов является теплообмен калориметра с окружающей средой посредством излучения и теплопроводности. В целях учёта побочных процессов и прежде всего теплообмена калориметрическую систему окружают оболочкой, температуру которой регулируют.
У жидкостных калориметров температуру оболочки поддерживают постоянной. При определении теплоты химической реакции наибольшие затруднения часто связаны не с учётом побочных процессов, а с определением полноты протекания реакции и с необходимостью учитывать несколько реакций.
В калориметре-интеграторе другого вида — изотермическом (постоянной температуры) введённая теплота не изменяет температуры калориметрической системы, а вызывает изменение агрегатного состояния тела, составляющего часть этой системы (например, таяние льда в ледяном калориметре Бунзена). Количество введённой теплоты рассчитывается в этом случае по массе вещества, изменившего агрегатное состояние (например, массе растаявшего льда, которую можно измерить по изменению объёма смеси льда и воды), и теплоте фазового перехода.
Массивный калориметр-интегратор чаще всего применяют для определения энтальпии веществ при высоких температурах (до 2500 °С). Калориметрическая система у калориметров этого типа представляет собой блок из металла (обычно из меди или алюминия) с выемками для сосуда, в котором происходит реакция, для термометра и нагревателя. Энтальпию вещества рассчитывают как произведение теплового значения калориметра на разность подъёмов температуры блока, измеряемых после сбрасывания в его гнездо ампулы с определённым количеством вещества, а затем пустой ампулы, нагретой до той же температуры.
Теплоёмкость газов, а иногда и жидкостей, определяют в т. н. проточных лабиринтных калориметрах — по разности температур на входе и выходе стационарного потока жидкости или газа, мощности этого потока и джоулевой теплоте, выделенной электрическим нагревателем калориметра.
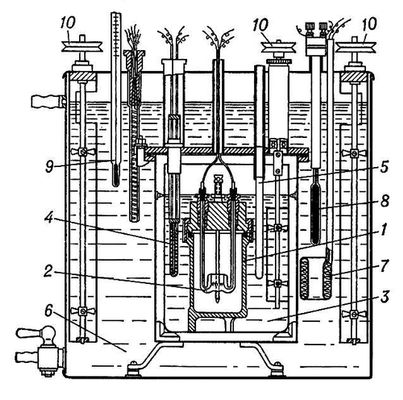
Калориметр, работающий как измеритель мощности, в противоположность калориметру-интегратору должен обладать значительным теплообменом, чтобы вводимые в него количества теплоты быстро удалялись и состояние калориметра определялось мгновенным значением мощности теплового процесса. Тепловая мощность процесса находится из теплообмена калориметра с оболочкой. Такие калориметры (рис. 2), разработанные французским физиком Э. Кальве (Е. Calvet, 1895—1966), представляют собой металлический блок с каналами, в которые помещают цилиндрические ячейки. В ячейке проводится исследуемый процесс; металлический блок играет роль оболочки (температура его поддерживается постоянной с точностью до 10 -5 —10 -6 К). Разность температур ячейки и блока измеряется термобатареей, имеющей до 1000 спаев. Теплообмен ячейки и эдс термобатареи пропорциональны малой разности температур, возникающей между блоком и ячейкой, когда в ней выделяется или поглощается теплота. В блок помещают чаще всего две ячейки, работающие как дифференциальный калориметр: термобатареи каждой ячейки имеют одинаковое число спаев и поэтому разность их эдс позволяет непосредственно определить разность мощности потоков теплоты, поступающей в ячейки. Этот метод измерений позволяет исключить искажения измеряемой величины случайными колебаниями температуры блока. На каждой ячейке монтируют обычно две термобатареи: одна позволяет скомпенсировать тепловую мощность исследуемого процесса на основе Пельтье эффекта, а другая (индикаторная) служит для измерения нескомпенсированной части теплового потока. В этом случае прибор работает как дифференциальный компенсационный калориметр. При комнатной температуре такими калориметрами измеряют тепловую мощность процессов с точностью до 1 мквт.
Общую классификацию калориметров можно построить на основе рассмотрения трёх главных переменных, определяющих методику измерений: температуры калориметрической системы Tc; температуры оболочки To, окружающей калориметрическую систему количества теплоты L, выделяемой в калориметре в единицу времени (тепловой мощности).
Калориметр с постоянными Tc и To называют изотермическим; с Tc = To — адиабатическим; калориметр, работающий при постоянной разности температур Tc — To, называют калориметром с постоянным теплообменом; у изопериболического калориметра (его ещё называют калориметром с изотермической оболочкой) постоянна To, а Tc является функцией тепловой мощности L.
Важным фактором, влияющим на окончательный результат измерений, является надёжная работа автоматических регуляторов температуры изотермических или адиабатических оболочек. В адиабатическом калориметре температура оболочки регулируется так, чтобы она была всегда близка к меняющейся температуре калориметрической системы. Адиабатическая оболочка — лёгкая металлическая ширма, снабженная нагревателем, — уменьшает теплообмен настолько, что температура калориметра меняется лишь на несколько десятитысячных град/мин. Часто это позволяет снизить теплообмен за время калориметрического опыта до незначительной величины, которой можно пренебречь. В случае необходимости в результаты непосредственных измерений вводится поправка на теплообмен, метод расчёта которой основан на законе теплообмена Ньютона — пропорциональности теплового потока между калориметром и оболочкой разности их температур, если эта разность невелика (до 3—4 ° С).
Для калориметра с изотермической оболочкой теплоты химической реакции могут быть определены с погрешностью до 0,01%. Если размеры калориметра малы, температура его изменяется более чем на 2—3 °С и исследуемый процесс продолжителен, то при изотермической оболочке поправка на теплообмен может составить 15—20% от измеряемой величины и существенно ограничить точность измерений. В этих случаях целесообразнее применять адиабатическую оболочку.
При помощи адиабатического калориметра определяют теплоёмкость твёрдых и жидких веществ в области от 0,1 до 1000 К. При комнатных и более низких температурах адиабатический калориметр, защищенный вакуумной рубашкой, погружают в Дьюара сосуд, заполненный жидким гелием, водородом или азотом (рис. 3). При повышенных температурах (выше 100 °С) калориметр помещают в термостатированную электрическую печь.
Лит.: Попов М. М., Термометрия и калориметрия, 2 изд., М., 1954; Скуратов С. М., Колосов В. П., Воробьев А. Ф., Термохимия, ч. 1—2, М., 1964—66; Кальве Э., Прат А., Микро-калориметрия, пер. с франц., М., 1963; Experimental thermochemistry, v. 1—2 N. Y. — L., 1956-62.
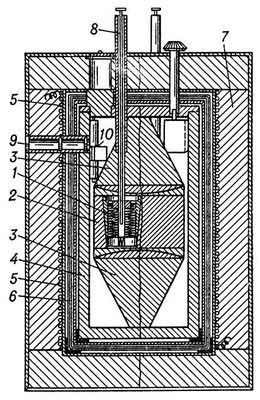
Рис. 2. Калориметр Э. Кальве для измерения тепловой мощности процессов (схема): 1 — калориметрическая ячейка с термопарами; 2 — блок калориметра; 3 — металлические конусы для создания однородного поля температур в блоке; 4 — оболочка; 5 — нагреватель для термостатирования прибора; 6 — тепловые экраны; 7 — тепловая изоляция; 8 — трубка для введения вещества в калориметр; 9 — окно для отсчётов показаний гальванометра 10.
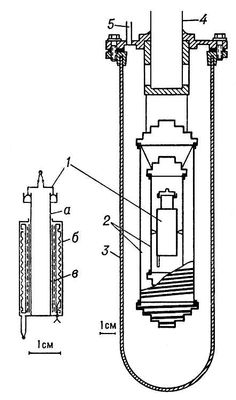
Рис. 3. Адиабатический калориметр для определения теплоёмкости при низких температурах (схема): 1 — калориметр (а — сосуд для вещества, б — термометр сопротивления, в — нагреватель); 2 — адиабатические оболочки (ширмы); 3 — вакуумная рубашка; 4 — труба для откачки; 5 — трубка для электрических проводов.
В камеру сгорания калориметра (см. рис.1) непрерывно подается жидкое топливо из баллона лампы газификации под действием сжатого воздуха. Теплота, выделяющаяся при сгорании топлива, передается воде, циркулирующей внутри калориметра. Количество сжигаемого топлива определяется с помощью прецизионных весов. Количество воды – с помощью счетчика.
Калориметр устанавливается в помещении без сквозняков. Его вертикальное положение обеспечивается установочными винтами 35.
Вода из водопроводной сети подается в напорный сосуд 2. Часть воды через регулировочный кран 5 поступает во внутрь калориметра, другая часть – через край переливной чаши и штуцер 4 вытекает в сливную воронку 33. Нагретая в калориметре вода выходит в сосуд с переливной воронкой 9 и оттуда в сливную воронку 33. Количество прошедшей через калориметр воды учитывается счетчиком СВК-15, позволяющем производить отсчет показаний с точностью ±0,0001 м 3 /ч.
Для переключения водяного потока служит кран 10, а для отвода воды – штуцеры 11 и 12. Температура воды до и после калориметра измеряется платиновыми термосопротивлениями 15 и 16 в комплекте со вторичным прибором 2ТРМ0.
Топливо под давлением воздуха подается из баллона 24 лампы газификации к горелке 25, испаряется; пары через сопло выходят в камеру сгорания 17 калориметра и сгорают. Продукты сгорания топлива первоначально поднимаются вверх по камере сгорания, затем опускаются вниз по трубкам 18 и выходят наружу через выхлопной штуцер 19. Термометр 21 служит для измерения температуры уходящих газов, заслонка 20 – для регулирования режимов горения.
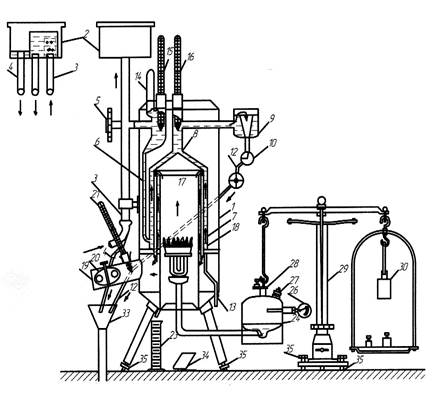
Рис. 1. Схема установки для определения теплоты сгорания жидкого топлива:
Водяные пары, образующиеся при горении топлива, конденсируются по мере охлаждения продуктов сгорания. Конденсат стекает вниз и вытекает через штуцер 22 в измерительную мензурку 23. Выступающая из верхней крышки трубка 14 служит для удаления воздуха при заполнении калориметра водой. Спускной кран 13 на днище калориметра во время работы должен быть закрытым.
Подготовка калориметра к работе
Перед началом работы лампу газификации заправляют жидким топливом (керосином). Для этого необходимо отвернуть пробку штуцера 27, влить в баллон 24 около 200 см 3 предварительно отфильтрованного топлива и плотно завернуть пробку. Затем лампу подвешивают к левому плечу коромысла прецизионных весов 29 и уравновешивают ее противовесами и мелкими гирями до тех пор, пока стрелка весов не установится на нуле. Прецизионные весы должны стоять справа от калориметра и на таком расстоянии от него, чтобы горелка 25 лампы находилась в центре камеры горения калориметра. Контроль положения горелки производят при помощи зеркала 34.
В ходе опытов должен быть обеспечен постоянный расход воды через калориметр. Для этого необходимо, чтобы вода через край переливной чашки напорного сосуда 2 переливалась по всему краю чашки.
Для зажигания и регулирования пламени лампу газификации снимают с прецизионных весов, заливают в чашку горелки спирт и поджигают его. При горении спирта нагреваются трубки горелки. К концу горения насосом накачивают воздух в баллон 24 лампы. Под напором воздуха керосин будет подниматься к горелке и, проходя через горячие трубки, испаряться. На выходе из сопла пары керосина воспламеняются от пламени спирта. Давление воздуха определяют по манометру 26. В баллоне необходимо создать такое давление воздуха, чтобы пламя было равномерным, а часовой тепловой эффект составил бы 4000 кДж тепла, для чего требуется сжечь в час около 0,1 кг керосина или бензина. После того, как пламя отрегулировано, лампу подвешивают к коромыслу весов, а горелку вводят в камеру горения калориметра. С помощью зеркала 34 проверяют правильность установки горелки. Горелка должна быть в центре горения, нельзя допускать удара пламени в стенку, что вызвало бы неполное сгорание топлива. В момент окончательной установки лампы вода из сосуда 9 должна вытекать полной струей.

Затем выполняется окончательная наладка калориметра. После установки лампы создают перевес на весах в сторону лампы с топливом на 15–20 г с тем, чтобы за время горения этого количества топлива окончательно наладить калориметр. Прежде всего, надо отрегулировать скорость движения воды через калориметр так, чтобы разность температур теплой и холодной воды была равна 10–12 °С. Регулировку производят регулировочным краном 5, одновременно наблюдая за показаниями термометров 15 и 16. Для получения наиболее точных результатов температура холодной воды должна быть на 4°С ниже температуры помещения, а относительная влажность воздуха соответствовать 60%.
С появлением капелек конденсата из штуцера 22 начинается основной опыт. Признакомустановившегося режимаработы калориметра является постоянство температур холодной и теплой воды.
Перед началом основного опыта необходимо определить расход воды через калориметр. Для этого нужно измерить время, за которое вода, прошедшая через калориметр, заполнит измерительную емкость, после чего с помощью весов определить массу воды.
Основной опыт
Основной опыт начинается, когда стрелка прецизионных весов указывает на нуль. В этот моментвключают секундомер и подставляют под штуцер 22 измерительную мензурку. Одновременно на чашку 28 необходимо положить гирю массой 10 г, в результате чего левое коромысло весов и лампа снижаются. Когда стрелка весов вновь укажет на нуль, секундомер следует выключить.
Измерения температуры должны производиться с точностью
±0,1 °С, количества охлаждающей воды ±0,0001 м 3 , количества конденсата ±1 мг. Период дискретизации – 1 мин.
Опыты производят дважды. Результаты измерений и расчетов записывают в протокол, форма которого приведена в табл. 2. После окончания экспериментов колпачок ниппеля снимают со штуцера 27, при этом пламя горелки должно потухнуть.
Обработка результатов
Высшая теплота сгорания жидкого топлива
где G – количество охлаждающей воды, кг; h1 и h2 – энтальпии теплой и холодной воды, соответственно, °С; B – количество сожженного в опыте топлива, г.

Калориметр (от латинского calor - тепло и. метр) - прибор для измерения количества теплоты, выделяющейся или поглощающейся при различных физических, химических, биологических или промышленных процессах. Используется, например, для определения теплоты сгорания топлива. Количество теплоты чаще всего определяется по изменению температуры какой-либо жидкости известной массы, в которую опускают образец.




Типы калориметров
Калориметр, предназначенный для измерения суммарного количества теплоты Q, выделяющейся в процессе от его начала до завершения, называют калориметр-интегратором; Калориметр для измерения тепловой мощности (скорости тепловыделения) L и её изменения на разных стадиях процесса — измерителем мощности или калориметр-осциллографом. По конструкции калориметрической системы и методу измерения различают жидкостные и массивные калориметры, одинарные и двойные (дифференциальные).
Принцип действия
Этот прибор состоит из двух сосудов, как показано на рисунке; принцип его действия следующий:
Калориметрические измерения
калориметр представляет собой устройство, которое используется для измерения изменения температуры определенного количества вещества (обычно воды) с известной удельной теплоемкостью. Это изменение температуры связано с поглощением или выделением тепла в исследуемом процессе; химический, если это реакция, или физический, если он состоит из изменения фазы или состояния.
В лаборатории самый простой калориметр, который можно найти, это калориметр. Он используется для измерения тепла, поглощенного или выделенного в реакции при постоянном давлении, в водном растворе. Реакции выбираются так, чтобы избежать вмешательства реагентов или газообразных продуктов..

В экзотермической реакции количество выделяемого тепла может быть рассчитано по увеличению температуры калориметра и водного раствора:
Количество тепла, которое выделяется в реакции = количество тепла, поглощенного калориметром + количество тепла, поглощенного раствором
Количество тепла, поглощаемое калориметром, называется калориметрической емкостью калориметра. Это определяется подачей известного количества тепла в калориметр с заданной массой воды. Затем измеряют повышение температуры калориметра и содержащегося в нем раствора..
С этими данными и использованием удельной теплоемкости воды (4,18 Дж / г ºC) можно рассчитать калорийность калориметра. Эта емкость также называется постоянной калориметра.
С другой стороны, тепло, получаемое водным раствором, равно m · ce · Δt. В формуле m = масса воды, ce = удельная теплоемкость воды и Δt = изменение температуры. Зная все это, можно рассчитать количество тепла, выделяемое экзотермической реакцией..
- 1 История калориметра
- 2 части
- 3 Типы и их характеристики
- 3.1 Кофейная чашка
- 3.2 Калориметрический насос
- 3.3 Адиабатический калориметр
- 3.4 Изопериболический калориметр
- 3.5 Проточный калориметр
- 3.6 Калориметр для дифференциальной сканирующей калориметрии
- 4.1 В физикохимии
- 4.2 В биологических системах
- 4.3 Калориметр кислородного насоса и калорийность
История калориметра
В 1780 году французский ученый А. Л. Лавуазье, считающийся одним из отцов химии, использовал морскую свинку, чтобы измерить выработку тепла при дыхании..
Как? Использование устройства, похожего на калориметр. О тепле, производимом морской свинкой, свидетельствует таяние снега, окружавшего аппарат.
Исследователи А. Л. Лавуазье (1743-1794) и П. С. Лаплас (1749-1827) разработали калориметр, который использовался для измерения удельной теплоты тела методом таяния льда.
Калориметр состоял из луженого цилиндрического стакана, покрытого лаком, удерживаемого штативом и внутренне ограниченного воронкой. Внутри было помещено еще одно стекло, похожее на предыдущее, с трубкой, проходящей через внешнюю камеру и снабженной ключом. Внутри второго стекла была сетка.
В эту сетку помещалось существо или объект, удельное тепло которого было желательно определить. Лед был помещен внутри концентрических сосудов, как в корзине.
Тепло, выделяемое телом, поглощалось льдом, вызывая его слияние. И жидкий водный продукт таяния льда собирали, открывая ключ внутреннего стекла.
И, наконец, при взвешивании воды масса расплавленного льда была известна.
части
Наиболее часто используемый калориметр в учебных лабораториях по химии - это так называемый калориметр для кофейных чашек. Этот калориметр состоит из стакана, или вместо этого, контейнера из аниме материала, который имеет определенные изолирующие свойства. Внутри этого контейнера находится водный раствор с телом, которое будет производить или поглощать тепло.
В верхней части контейнера размещена крышка из изоляционного материала с двумя отверстиями. В одном термометр вводится для измерения изменений температуры, а в другом - мешалка, предпочтительно из стеклянного материала, которая выполняет функцию перемещения содержимого водного раствора..
Изображение показывает части калориметрического насоса; Тем не менее, можно заметить, что он имеет термометр и мешалку, общие элементы в нескольких калориметрах.
Типы и их характеристики
Кофейная чашка
Это тот, который используется для определения тепла, выделяемого экзотермической реакцией, и тепла, поглощаемого в эндотермической реакции..
Кроме того, его можно использовать при определении удельной теплоты тела; то есть количество тепла, которое должен поглотить грамм вещества, чтобы повысить его температуру на один градус Цельсия. .
Калориметрический насос
Это устройство, в котором измеряется количество тепла, которое выделяется или поглощается в реакции, которая происходит при постоянном объеме..
Реакция протекает в прочном стальном сосуде (насосе), который погружается в большой объем воды. Это делает изменения температуры воды небольшими. Следовательно, предполагается, что изменения, связанные с реакцией, измеряются при постоянной температуре и объеме..
Вышесказанное указывает на то, что при проведении реакции в калориметрическом насосе работа не выполняется..
Реакция начинается с подачи электричества через кабели, подключенные к насосу.
Адиабатический калориметр
Он характеризуется наличием изолирующей структуры, называемой экраном. Экран расположен вокруг ячейки, где происходят изменения температуры и тепла. Он также подключен к электронной системе, которая поддерживает свою температуру очень близко к температуре элемента, чтобы избежать передачи тепла.
В адиабатическом калориметре разница температур между калориметром и его окружением сводится к минимуму; а также минимизировать коэффициент теплопередачи и время теплообмена.
Его части состоят из следующего:
-Ячейка (или контейнер), интегрированная в систему изоляции, с помощью которой пытаются избежать потери тепла.
-Термометр, для измерения изменений температуры.
-Нагреватель, подключенный к контролируемому источнику электрического напряжения.
-И щит, уже упоминавшийся.
В калориметре этого типа могут быть определены такие свойства, как энтропия, температура Дебая и плотность электронного состояния..
Изопериболический калориметр
Это устройство, в котором реакционная ячейка и насос погружены в конструкцию, называемую рубашкой. В этом случае так называемая рубашка состоит из воды, поддерживаемой при постоянной температуре.
Температура ячейки и насоса повышается при выделении тепла во время процесса сгорания; но температура водяной рубашки поддерживается на фиксированной температуре.
Микропроцессор контролирует температуру ячейки и кожуха, внося необходимые поправки в тепло утечки, возникающее в результате различий между двумя температурами..
Эти поправки применяются непрерывно и с окончательной поправкой, основанной на измерениях до и после испытания..
Проточный калориметр
Разработанный Caliendar, он имеет устройство для перемещения газа в контейнере с постоянной скоростью. При добавлении тепла измеряется увеличение температуры в жидкости..
Проточный калориметр характеризуется:
- Точное измерение постоянного расхода.
- Точное измерение количества тепла, вводимого в жидкость через нагреватель.
- Точное измерение повышения температуры в газе, вызванное подводом энергии
- Конструкция для измерения емкости газа под давлением.
Калориметр для дифференциальной сканирующей калориметрии
Он характеризуется наличием двух контейнеров: в одном помещается исследуемый образец, в то время как другой остается пустым или используется контрольный материал.
Два сосуда нагреваются с постоянной скоростью энергии с помощью двух независимых нагревателей. Когда начинается нагрев двух емкостей, компьютер будет отображать разницу тепловых потоков нагревателей в зависимости от температуры, что позволяет определить поток тепла..
Кроме того, можно определить изменение температуры как функции времени; и, наконец, калорийность.
приложений
По физикохимии
-Основные калориметры, типа кофейной чашки, позволяют измерять количество тепла, которое организм выделяет или поглощает. Они могут определить, является ли реакция экзотермической или эндотермической. Кроме того, удельная теплоемкость тела может быть определена.
-С помощью адиабатического калориметра удалось определить энтропию химического процесса и электронную плотность состояния.
В биологических системах
-Микрокалориметры используются для изучения биологических систем, которые включают взаимодействия между молекулами, а также происходящие конформационные изменения молекул; например, при развертывании молекулы. Линия включает в себя как дифференциальное сканирование, так и изотермическое титрование.
-Микрокалориметр используется при разработке лекарственных препаратов малых молекул, биотерапевтических средств и вакцин..
Кислородный насос калориметр и калорийность
Сжигание многочисленных веществ происходит в калориметре кислородного насоса, и его калорийность может быть определена. В число веществ, изученных с помощью этого калориметра, входят: уголь и кокс; пищевые масла, как тяжелые, так и легкие; бензин и все моторные топлива.
А также виды топлива для авиационных реакторов; топливные отходы и размещение отходов; пищевые продукты и добавки для питания человека; кормовые культуры и добавки для кормления животных; строительные материалы; ракетное и ракетное топливо.
Аналогично, калорийность была определена с помощью калориметрии в термодинамических исследованиях горючих материалов; в изучении энергетического баланса в экологии; во взрывчатых веществах и термопорошках и в обучении основным термодинамическим методам.
Читайте также:

