Область применения аргона кратко
Обновлено: 30.06.2024
Аргон – это простой одноатомный бесцветный, безвкусный газ, не имеющий запаха. Аргон тяжелее воздуха (плотность 1,78 кг/м 3 ), обладает низким потенциалом ионизации (15,7 В), не вступает в химические взаимодействия с другими элементами.
По объему и массе, после азота и кислорода, аргон самый распространенный газ в атмосфере: аргон в достаточных количествах содержится в свободном виде (0,9325% об., или 0,00007% вес.), что позволяет получать его из воздуха ректификационными методами.
Криогенный способ
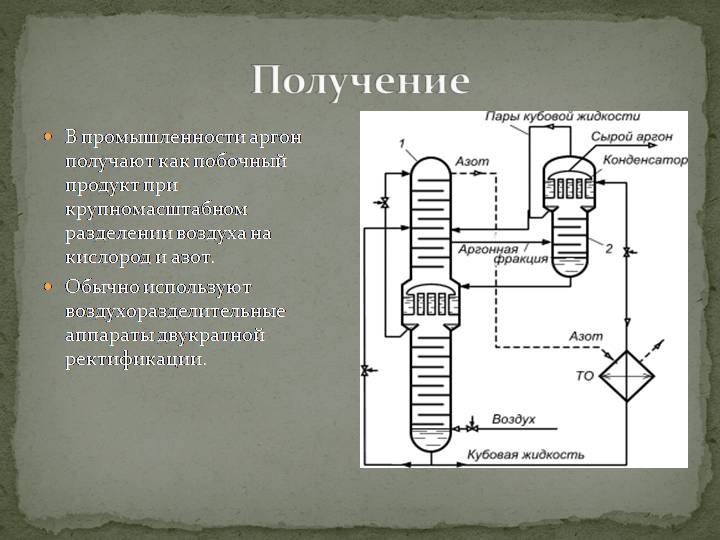
Побочный продукт при производстве аммиака
Еще один источник получения аргона – это аммиачное производство. В данном случае газообразный аргон является отходом – примесью, извлекаемой из азота, который необходим для синтеза аммиака. После взаимодействия азота и водорода с образованием аммиака, аргон просто остается как не прореагировавший остаток.
Применение аргона
Аргон широко используют для создания инертной и защитной атмосферы, прежде всего при термической обработке легко окисляющихся металлов (аргоновая плавка, аргоновая сварка и другие). В атмосфере аргона получают кристаллы полупроводников и многие другие сверхчистые материалы. Аргоном часто заполняют электрические лампочки (для замедления испарения вольфрама (W) со спирали). При пропускании электрического разряда через стеклянную трубку, заполненную аргоном, наблюдается сине-голубое свечение, что широко используется, например, в светящейся рекламе. В геохронологии по определению соотношения изотопов 40Ar/40К устанавливают возраст минералов.
Аргон успешно применяется в пищевой промышленности как упаковочный газ, в качестве вещества для тушения пожаров, в медицине для очистки воздуха и в качестве наркоза и в аргоновых лазерах. Однако наибольшее и наилучшее применение этот газ получил в сварочных работах. Сварка в защитных газах (аргон или многокомпонентные газовые смеси на основе аргона) применяется практически для всех металлов, включая углеродистую сталь, алюминий, медь, нержавейку и титан.
Электровакуумная техника
- Подавляющее большинство ламп накаливания заполняют смесью аргона (86%) и азота (14%).
- Используется аргон и в современных люминесцентных лампах для облегчения зажигания, лучшей передачи тока и предохранения катодов от разрушения.
Пищевая промышленность
Производство стекла, цемента и извести
Металлургия
В последние десятилетия наибольшая часть получаемого аргона идет в металлургию, металлообработку. В среде аргона ведут процессы, при которых нужно исключить контакт расплавленного металла с кислородом, азотом, углекислотой и влагой воздуха. Аргонная среда используется при горячей обработке титана, тантала, ниобия, бериллия, циркония, гафния, вольфрама, урана, тория, а также щелочных металлов. В атмосфере аргона обрабатывают плутоний, получают некоторые соединения хрома, титана, ванадия и других элементов (сильные восстановители).
Аргон используется для предупреждения контакта и последующего взаимодействия между расплавленным металлом и окружающей атмосферой.
Использование аргона позволяет оптимизировать такие производственные процессы, как перемешивание расплавленных веществ, продувка поддонов реакторов для предупреждения повторного окисления стали и обработка стали узкого применения в вакуумных дегазаторах, включая вакуумно-кислородное обезуглероживание, окислительно-восстановительных процессы и процессы открытого сжигания. Однако наибольшую популярность аргон приобрел в процессах аргоно-кислородного обезуглероживания нерафинированной высокохромистой стали, позволяя минимизировать окисление хрома.
Лабораторные исследования и анализы
- В чистом виде и в соединениях с другими газами аргон используется для проведения промышленных и медицинских анализов и испытаний в рамках контроля качества.
- В частности, аргон выполняет функцию газовой плазмы в эмиссионной спектрометрии индуктивно-связанной плазмой (ICP), газовой подушки в атомно-абсорбционной спектроскопии в графитной печи (GFAAS) и газа-носителя в газовой хроматографии с использованием различных газоанализаторов.
- В соединении с метаном аргон используется в счетчиках Гейгера и детекторах рентгеновского флуоресцентного анализа (XRF), где он выполняет функцию гасящего газа.
- В аргоновых лазерах.
Сварка, резка и нанесение покрытия
Все шире применяется дуговая электросварка в среде аргона. Продуваемый вдоль столба дуги аргон (в смеси с водородом) предохраняет кромки разреза и вольфрамовый электрод от образования окисных, нитридных и иных пленок. Одновременно он сжимает и концентрирует дугу на малой поверхности, отчего температура в зоне резки достигает 4000-6000°С. К тому же эта газовая струя выдувает продукты резки. При сварке в аргонной струе нет надобности во флюсах и электродных покрытиях, а стало быть, и в зачистке шва от шлака и остатков флюса.
Аргон используется в качестве защитной среды в процессах дуговой сварки, при поддуве защитного газа и при плазменной резке.
Электроника
Сверхчистый аргон служит в качестве газа-носителя для химически активных молекул, а также в качестве инертного газа для защиты полупроводников от посторонних примесей (например, аргон обеспечивает необходимую среду для выращивания кристаллов силикона и германия).
В ионном состоянии аргон используется в процессах металлизации напылением, ионной имплантации, нормализации и травления при производстве полупроводников и высокоэффективном производстве материалов.
Автомобильная и транспортная отрасль
Медицина
Противопожарная безопасность

История открытия Аргона
Впервые неизвестный до этого газ, при химических и физических экспериментах, обнаружил в 1785 году Генри Кавендиш — английский физик и химик. Но он не смог разгадать загадку и прекратил исследования. Позднее на записи Кавендиша обратил внимание Джеймс Максвелл.
И лишь спустя более ста лет, в 1894 году, химик Уильям Рамзай и физик Джон Уильям Стретт (Лорд Рэлей) сделали доклад об открытии нового элемента, который, за свою химическую неактивность, назвали аргоном. Это случилось в Оксфорде на собрании Британской ассоциации естествоиспытателей, физиков и химиков. Название нового газа произошло от греческого слова ἀργός, что в переводе означает — неактивный, медленный.
Спустя еще 10 лет, эти ученые получили Нобелевские премии за исследования газов, открытие аргона и других инертных газов в атмосфере.
Получение Аргона
Аргон — наиболее распространенный в воздухе инертный газ. В 1 м 3 содержится примерно 0,09 см 3 ксенона, 1,1 см 3 криптона, 5,2 см 3 гелия, 18,2 см 3 неона, 9000 см 3 аргона.
В атмосфере Земли аргон занимает третье место. На первом – азот, на втором - кислород. В процентном отношении это примерно 0,93% по объёму или 1.3% по массе. По этой причине он является самым легкодоступным и недорогим инертным газом.
Получение и промышленное производство этого газа происходит как выделение сопутствующего газа при добыче азота и кислорода из атмосферного воздуха. Наиболее простой метод — это глубокое охлаждение и ректификация с последующей доочисткой от примесей.
Кроме того, аргон получают при производстве аммиака. Доочистку аргона осуществляют по технологии гидрирования с платиновым катализатором или адсорбционным методом с использованием молекулярных сит или активного угля.
Применение Аргона
Основными потребителями аргона являются:
Металлургия. Применение аргона в современных технологических процессах выплавки стали — продувка расплава в ковше. Эта операция выполняет несколько функций: охлаждение металла, ускорение плавления вводимых в ковш лигатур и раскислителей, гомогенизация металла по химическому составу и температуре, очищение от неметаллических включений, образующихся от раскисляющих и легирующих добавок, углеродное раскисление металла и его обезуглероживание, удаление водорода и азота, ускорение десульфурации (удаление серы из расплава), вдувание раскисляющих и легирующих порошкообразных добавок.
В металлургии высококачественных сплавов аргон используется для защиты расплава от контакта с воздухом во время выплавки и разливки. Высокотемпературная обработка титана и его сплавов требует защитной аргоновой атмосферы. Незаменим аргон и в технологиях обработки таких редких металлов как цирконий, вольфрам, тантал, ниобий, бериллий, гафний и др.
Металлообрабатывающая промышленность. Основное использование аргона — создание защитной завесы при электродуговой (АРДЭС), контактной и лазерной сварке, термообработке. Аргон — плазмообразующий газ в установках сварки и резки активных, редких металлов, сплавов на их основе, например, алюминиевых и магниевых, нержавеющих, хромоникелевых, жаропрочных сплавов и легированных сталей.
Радиоэлектронная промышленность. Здесь аргон незаменим для создания инертной среды в установках плазменного напыления, заполнение колб электрических и люминесцентных ламп, электровакуумных приборов, газосветной рекламы. Например, сине-голубое свечение получается при заполнении трубок аргоном с парами ртути.
Спектральный анализ и метрология. В данной сфере аргон наиболее часто используется как газ-носитель, инертная среда и плазмообразующий газ в контрольно-измерительных приборах, а также при производстве поверочных газовых смесей (ПГС) для различных газоанализаторов.
В данной сфере применения чистота аргона имеет ключевое значение. Даже при минимальных отклонениях качества аргона от соответствующих ГОСТов и ТУ, регламентированных для использования в конкретных приборах, изменяются условия работы и анализа, что приводит к серьезным искажениям результатов измерений, нарушению работоспособности оборудования, снижению качества продукции, снижению ресурса фильтров и, как следствие, серьезным экономическим убыткам.
Для предотвращения вышеописанного, могут использоваться специализированные фильтры, а также установки доочистки аргона (инертных газов) лабораторного или промышленного назначения.
Так как наша компания занимается разработкой и производством спектрометров, применение аргона в этих приборах мы решили рассмотреть более подробно. Ниже в статье этому будет посвящена отдельная глава.
Прочие сферы применения. Огнетушительные установки, заполнение стеклопакетов и поддув сухих гидрокостюмов водолазов для лучшей теплоизоляции, в медицине — очистка разрезов при хирургическом вмешательстве, в химической промышленности — инертная среда для нестабильных на воздухе соединений, а так же в прочих областях промышленности.
Аргон — наиболее дешевый и доступный инертный газ, который в последние десятилетия массово применяется во многих сферах. Особенно он востребован в металлообработке, металлургии и ряде смежных отраслей промышленности.
Потребителю аргон может поставляться в двух состояниях: жидком или газообразном. В обоих случаях его перевозят железнодорожным или автомобильным транспортом в специальных цистернах и баллонах, способных выдерживать высокое давление.
Сжижать аргон требуется, как правило, для перевозок больших объемов. Жидкий аргон в баллонах или цистернах занимает намного меньше места, чем газообразный, а значит доставить его за один раз можно намного больше, что целесообразно с экономической точки зрения.
Где используют аргон?
Область его применения очень обширна. Помимо знакомой всем уличной рекламы, которая сияет красивыми цветами благодаря аргоновым лампам, этот газ используется во многих сферах.
- В металлургии и горнодобывающей промышленности.
- Плотность: 1,784 кг/м3.
- Температура кипения: -185,8 ˚С.
- Тройная точка: -189,8˚С.
- Содержание в воздухе: 0,9% объёма.
- Воздух очищается от пыли и подвергается сжатию до жидкого состояния.
- Жидкий воздух, состоящий преимущественно из кислорода, азота и аргона подвергается ректификации.
- После отделения азота, из получившейся при сжатии жидкости, осуществляется доочистка кислородно-аргоновой смеси.
- Малого объёма: 0,4 – 12 л.
- Среднего объёма: 20 – 50 л.
- Большого объёма: более 50 л.
- Надёжно закрепить баллоны.
- Размещение ёмкостей осуществляется в горизонтальной плоскости.
- Возможно вертикальное размещение только при наличии специальных приспособлений, повышающих устойчивость баллонов.
- Заправленные аргоном баллоны разрешается перевозить только при отсутствии утечек из ёмкости.
- Воздух очищается от пыли и подвергается сжатию до жидкого состояния.
- Жидкий воздух, состоящий преимущественно из кислорода, азота и аргона подвергается ректификации.
- После отделения азота, из получившейся при сжатии жидкости, осуществляется доочистка кислородно-аргоновой смеси.
Он применяется для выплавки металлов, обладающих особыми свойствами, а также в процессах, где требуется исключить контакт азота, кислорода, влаги или углекислоты с расплавленным металлом. Также аргон необходим при горячей обработке тантала, титана, циркония, ниобия, гафния, бериллия, урана, вольфрама, тория, плутония и др.
В лазерных и спектроскопических установках аргон используется для анализа чистоты материалов.
В этой области аргон применяют для защиты сварочной дуги в процессе электросварки алюминиевых деталей, а также элементов из высоколегированной стали. Кроме того, он нужен для быстрой резки различных металлов, в том числе и самых тугоплавких. Незаменим аргон и при выполнении дуговой электросварки тонкостенных металлов и изделий.
Также аргон применяется в химической промышленности для получения сверхчистых веществ и используется в электроэнергетике для наполнения газоразрядных ламп в процессе сборки ответственных узлов.

Об основных качествах аргона, а также о сферах его применения будет подробно рассказано в этой статье.
Аргон: технические характеристики
Аргон представляет собой бесцветный газ, который не оказывает никакого действия на органы вкуса и обоняния. Этот одноатомный элемент является одним из самых распространённых инертных газообразных веществ на земле.
Аргон был открыт в конце XIX века британским учёным Джоном Стреттом. Исследователь проводил опыты по выделению азота из воздуха. В результате экспериментов было выяснено, что азот полученный таким образом имеет немного большую плотность, чем в случае, когда для получения этого газа использовались органические вещества. Учёный предположил, что азот из атмосферы содержит примесь неизвестного на тот момент газообразного вещества. Впоследствии, эти догадки были подтверждены, и аргон был получен в чистом виде и тщательно исследован.
Учёных, которые пытались произвести различные опыты с аргоном, ошеломил тот факт, что этот газ не вступал в реакцию с другими химическими элементами. Таким образом удалось впервые получить благородный газ с подобными характеристиками.
Несмотря на отсутствие соединений аргон, как и другие вещества, обладает физическими свойствами. К наиболее важным характеристикам газа относятся:
Аргон практически не растворяется в воде, а также абсолютно безопасен в плане пожарной активности. Этот газ не ядовит, поэтому при работе с ним не требуется использовать каких-либо средств защиты.
Где применяется аргон
Аргон получил большое распространение в промышленности. Инертные свойства этого газа особенно востребованы в различных производственных процессах, где необходимо вытеснить один из самых активных элементов – кислород. Использование аргона очень дёшево, в сравнении с другими инертными летучими веществами, поэтому газ незаменим в том случае, когда требуется защитная среда при сваривании металлов, а также вытеснение влаги и кислорода в ёмкостях, где хранятся пищевые продукты.
Наполнение колб ламп накаливания инертным газом, позволяет значительно увеличить ресурс работы осветительного прибора. Кроме повышенного срока использования такие элементы обладают большей яркостью. Используется инертный газ и при производстве люминесцентных ламп. Применение аргона позволяет облегчить запуск разряда электрической дуги, а также значительно увеличить ресурс электродов.
При изготовлении стеклопакетов, инертным газом заполняются полости между стёклами, что позволяет значительно улучшить теплоизоляционные свойства. Учитывая тот факт, что аргон является абсолютно прозрачным, использование его никак не ограниченно даже при изготовлении многослойных конструкций.

Инертный газ аргон используется также в установках плазменной резки металлов. Преимущество использования этого газа заключается в том, что для возникновения дуги не требуется слишком высокого напряжения, поэтому такие установки могут иметь очень простую конструкцию. При генерации плазмы с использованием аргона образуется минимальное количество вредных газообразных веществ во время выполнения резки, поэтому этот метод идеально подходит для ручных приборов.
Благодаря возможности образовывать плазму при относительно невысоком напряжении, этот благородный газ используется в медицине для проведения аргоновой коагуляции. Такой метод успешно используется для удаления новообразований, а также для остановки кровотечений.
Аргон применяется и в химической промышленности. Благодаря отсутствию взаимодействия с другими элементами этот газ используется для получения сверхчистых веществ, а также для их анализа. В металлургической промышленности благородный газ позволяет обрабатывать такие металлы, как: титан, тантал, ниобий, бериллий, цирконий и др. Кроме этого, газ используется для перемешивания расплавленных веществ и снижения окисления хрома при производстве хромированной стали.
Способы получения аргона
Аргон является третьим по распространённости газом в земной атмосфере, поэтому наиболее логичным способом является добывание его из воздуха. Для этой цели используются специальные низкотемпературные ректификационные аппараты.
Процесс отделения инертного вещества осуществляется в такой последовательности:
Температура кипения аргона в ректификационной установке составляет минус 185,3˚С. При этом, кислород кипит при температуре на 3 градуса выше, а азот – на 13˚С ниже этого показателя. По причине небольшого отличия в переходе из одного агрегатного состояния в другое, на первом этапе отделения аргона смесь содержит большое количество жидкого кислорода. На заключительной стадии получения аргона производится отделение благородного газа из кислородно-аргоновой смеси. Процесс доочистки, как правило, осуществляется с помощью электролитического водорода. В результате реакции в контактном аппарате с кислородом образуется водяной пар, который затем утилизируется через влагоотделитель.
Аргон может быть получен не только из атмосферного воздуха. При некоторых производственных процессах этот газ может являться сопутствующим продуктом. Например, при производстве аммиака, аргон является примесью азота и является совершенно ненужным элементом, поэтому полученный таким образом газ имеет очень низкую себестоимость, в сравнении с криогенным аргоном.
Правила хранения и транспортировки
Хранение и перевозка газа осуществляется в специальных металлических баллонах. Несмотря на то, что аргон является инертным газом, к ёмкостям всё равно предъявляются определённые технические требования, нарушение которых приведёт к невозможности использовать сосуд в дальнейшем. Кроме этого, утечка благородного газа в закрытом помещении может вызвать тошноту и потерю сознания у людей, ведь этот газ тяжелее воздуха и способен вытеснить необходимый для дыхания кислород.
Баллоны, используемые для хранения и транспортировки аргона, представляют собой цилиндрические ёмкости, которые могут быть разделены на следующие категории:
Стандартное давление в аргоновом баллоне составляет 150 атм, но в ёмкостях объёмом 40 литров разрешается хранить газ давлением до 200 атм. На ёмкости для хранения аргона наносится информация о дате изготовления и аттестации, а также такие параметры, как вес и объём.
Транспортировка аргона должна осуществляться по правилам. Автомобили должны маркироваться специальным знаком, которые указывает на перевозку нетоксичных и невзрывоопасных веществ. Все документы оформляются в строгом соответствии с правилами ДОПОГ.
Кроме этого, при перевозке аргона необходимо:
При перевозке аргона в количестве до 18 баллонов (объём 40 л) груз не является опасным, поэтому специальное разрешение не требуется. Тем не менее, даже при перемещении небольших партий следует придерживаться вышеописанных правил транспортировки ёмкостей с этим газом.
Как добывают аргон
Ar не поддается изменениям в процессе его использования и всегда возвращается в атмосферу. Поэтому ученые считают данный источник неисчерпаемым. Он добывается как сопутствующий продукт при разделении воздуха на кислород и азот посредством низкотемпературной ректификации.
Для реализации этого метода применяются специальные воздухоразделительные аппараты, состоящие из колонн высокого, низкого давления и конденсатора-испарителя. В результате процесса ректификации (разделения) получается аргон с небольшими примесями (3-10%) азота и кислорода. Чтобы произвести очистку, примеси убираются с помощью дополнительных химических реакций. Современные технологии позволяют достичь 99,99% чистоты данного продукта.

Представлены установки по производству данного химического элемента.
Хранится и транспортируется газ аргон в стальных баллонах (ГОСТ 949-73), которые имеют серый окрас с полосой и соответствующей надписью зеленого цвета. При этом процесс наполнения емкости должен полностью соответствовать технологическим нормам и правилам безопасности. Детальную информацию о специфике заполнения газовых баллонов можно прочитать в статье: баллоны со сварочной смесью – технические особенности и правила эксплуатации.
История открытия
История открытия аргона начинается в 1785 году, когда английский физик и химик Генри Кавендиш, изучая состав воздуха, решил установить, весь ли азот воздуха окисляется.
Дальнейшая история открытия аргона связана с именем Рэлея, который несколько лет посвятил исследованиям плотности газов, особенно азота.
У известного уже в то время английского химика Уильяма Рамзая также не было готового ответа, но он предложил Рэлею своё сотрудничество. Интуиция побудила Рамзая предположить, что азот воздуха содержит примеси неизвестного и более тяжёлого газа, а Дьюар обратил внимание Рэлея на описание старинных опытов Кавендиша (которые уже были к этому времени опубликованы).
Большую роль в изучении нового газа сыграл спектральный анализ. Спектр выделенного из воздуха газа с его характерными оранжевыми, синими и зелёными линиями резко отличался от спектров уже известных газов. Уильям Крукс, один из виднейших спектроскопистов того времени, насчитал в его спектре почти 200 линий. Уровень развития спектрального анализа на то время не дал возможности определить, одному или нескольким элементам принадлежал наблюдаемый спектр. Несколько лет спустя выяснилось, что Рамзай и Рэлей держали в своих руках не одного незнакомца, а нескольких — целую плеяду инертных газов.

Распространение в природе
Содержание аргона в мировой материи оценивается приблизительно в 0,02 % по массе.
Аргон (вместе с неоном) наблюдается на некоторых звёздах и в планетарных туманностях. В целом его в космосе больше, чем кальция, фосфора, хлора, в то время как на Земле существуют обратные отношения.
Аргон — третий по содержанию после азота и кислорода компонент воздуха, его среднестатистическое содержание в атмосфере Земли составляет 0,934 % по объёму и 1,288 % по массе, его запасы в атмосфере оцениваются в 4·1014 т.

Свойства аргона (таблица): температура, плотность, давление и пр.
206* Ковалентный радиус аргона согласно [1] составляет 106±10 пм.
401* Плотность аргона согласно [3] и [4] [Россия] составляет 0,0017839 г/см3 (при 0 °C /20 °C и иных стандартных условиях, состояние вещества – газ).
402* Температура плавления аргона согласно [3] и [4] составляет -189,35 °C (83,8 K, -308,83 °F) и -189,6 °C (83,55 K, -309,28 °F) соответственно.
403* Температура кипения аргона согласно [3] и [4] составляет -185,85 °C (87,3 K, -302,53 °F) и -185,9 °C (87,25 K, -302,62 °F) соответственно.
407* Удельная теплота плавления (энтальпия плавления ΔHпл) аргона согласно [3] и [4] составляет 7,05 кДж/моль и 1,19 кДж/моль соответственно.
408* Удельная теплота испарения (энтальпия кипения ΔHкип) аргона согласно [3] и [4] составляет 6,45 кДж/моль и 6,51 кДж/моль соответственно.
410* Молярная теплоемкость аргона [3] составляет 20,79 Дж/(K·моль).
Химические свойства

Классификация аргона по сортам
Аргон обеспечивает хорошую защиту сварочной ванны. В зависимости от назначения и содержания этот газ делится на три сорта. Высший сорт аргона (99,99% Ar) используется для сварки, химически активных металлов, циркония, титановых сплавов, молибдена, сплавов на их основе, ответственных конструкций из нержавеющих сталей. Первый сорт аргона (99,98% Ar) применяется для сварки неплавящимся электродом, магния, алюминия, магниевых и алюминиевых сплавов, менее чувствительных к примесям кислорода и азота. Второй сорт аргона (99,95% Ar) используется для сварки нержавеющих сталей, жаропрочных сплавов и чистого алюминия. Для сварки могут также использоваться смеси аргона с другими газами (кислородом, углекислым газом).
Аргон – это инертный газ с одноатомной структурой,
Который имеет температуру кипения в условиях нормального давления ниже, чем у кислорода. Средняя температура кипения аргона составляет около ста восьмидесяти градусов по Цельсию.
Изотопы
Аргон представлен в земной атмосфере тремя стабильными изотопами: 36Ar (0,337 %), 38Ar (0,063 %), 40Ar (99,600 %). Почти вся масса тяжёлого изотопа 40Ar возникла на Земле в результате распада радиоактивного изотопа калия 40K (содержание этого изотопа в изверженных породах в среднем составляет 3,1 г/т). Распад радиоактивного калия идёт по двум направлениям одновременно:


Первый процесс (обычный β-распад) протекает в 88 % случаев и ведет к возникновению стабильного изотопа кальция. Во втором процессе, где участвуют 12 % атомов, происходит электронный захват, в результате чего образуется тяжёлый изотоп аргона. Одна тонна калия, содержащегося в горных породах или водах, в течение года генерирует приблизительно 3100 атомов аргона. Таким образом, в минералах, содержащих калий, постепенно накапливается 40Ar, что позволяет измерять возраст горных пород; калий-аргоновый метод является одним из основных методов ядерной геохронологии. Вероятные источники происхождения изотопов 36Ar и 38Ar — неустойчивые продукты спонтанного деления тяжёлых ядер, а также реакции захвата нейтронов и альфа-частиц ядрами лёгких элементов, содержащихся в урано-ториевых минералах. Подавляющая часть космического аргона состоит из изотопов 36Ar и 38Ar. Это вызвано тем обстоятельством, что калий распространён в космосе примерно в 50 000 раз меньше, чем аргон (на Земле калий преобладает над аргоном в 660 раз). Примечателен произведенный геохимиками подсчёт: вычтя из аргона земной атмосферы радиогенный 40Ar, они получили изотопный состав, очень близкий к составу космического аргона.
Физические свойства
Аргон — одноатомный газ с температурой кипения (при нормальном давлении) −185,9 °C (немного ниже, чем у кислорода, но немного выше, чем у азота). В 100 мл воды при 20 °C растворяется 3,3 мл аргона, в некоторых органических растворителях аргон растворяется значительно лучше, чем в воде.
Химические свойства
Пока известны только 2 химических соединения аргона — гидрофторид аргона и CU(Ar)O, которые существуют при очень низких температурах. Кроме того, аргон образует эксимерные молекулы, то есть молекулы, у которых устойчивы возбужденные электронные состояния и неустойчиво основное состояние. Есть основания считать, что исключительно нестойкое соединение Hg—Ar, образующееся в электрическом разряде, — это подлинно химическое (валентное) соединение. Не исключено, что будут получены другие валентные соединения аргона с фтором и кислородом, которые тоже должны быть крайне неустойчивыми. Например, при электрическом возбуждении смеси аргона и хлора возможна газофазная реакция с образованием ArCl.
Соединение CU(Ar)O получено из соединения урана с углеродом и кислородом CUO. Вероятно существование соединений со связями Ar-Si и Ar-C: FArSiF3 и FArCCH.
Производство аргона
Технический газ аргон получают в качестве побочного продукта производственного процесса, в ходе которого кислород отделяют от азота. Для этого применяются специальные камеры с использованием воздухоразделительных аппаратов с двукратной ректификацией. Аргон обладает большими летучими свойствами, чем кислород, и меньшими, чем азот. Поэтому в процессе разделения воздуха на кислород и азот аргон остается в средней фракции. Из средней точки верхней колонны аппарата аргон направляют в специальные камеры для сжатия и хранения.
При первичном отборе массовая доля аргона в отобранной фракции составляет ничтожно малые показатели, всего около пяти процентов. Это так называемый сырой аргон. После последующей конденсации и очистки удается получить чистый аргон с массовой долей содержания его во фракции около 99,99 процентов. Практикуется так же способ извлечения аргона в процессе утилизации отходов аммиачного производства. В этом случае аргон получают из азота, оставшегося после связывания его с молекулами водорода.
Заправка аргоном баллонов
Предлагаем технический аргон. Заправляем баллоны на любых площадках и в производственных цехах.
Гарантируем высокое качество – сварочный аргон имеет сертификат РОСС RU.AЯ02.Н40876 и изготавливается по ГОСТу 10157-79.
При хранении и перевозке газа используются баллоны из стали объемом 40, 10 и 5 л, вся тара соответствует ГОСТу 949-73.
Доставка аргона и хранение
Транспортировка и хранение аргона допускается только в специализированных емкостях, газовых баллонах. В большинстве случаев для этого применяются сорокалитровые газовые баллоны. Баллоны с аргоном окрашиваются в серый цвет. Поперек баллона наносится зеленая полоса и надпись аналогичного цвета. Стандартное давление в баллонах с аргоном составляет сто пятьдесят атмосфер. В ряде случаев для снижения затрат на перевозку, аргон транспортируется в сжиженном состоянии. При этом его закачивают в специализированные ёмкости и сосуды Дюара. Также можно использовать и специализированные цистерны. Аргон не является взрывоопасным веществом. Меры предосторожности при его транспортировке в основном сводятся к тому, чтобы обеспечить сохранность самого технического газа, так как он обладает большой летучестью.
Аргон в сварочном процессе
В сварочных процессах аргон применяется при сварке ответственных узлов и агрегатов, которые нуждаются в повышенной защите от коррозийных процессов. Есть также такие сплавы и металлы, которые без применения аргона не могут быть обработаны при помощи сварочных операций. В частности, такие металлы, как тантал, ниобий, цирконий, гафний, вольфрам, уран, торий, титан, не могут подвергаться обработке без дополнительной защиты их при помощи инертного газа аргона.
При сварке в аргоне не применяются различные флюсы и электродные покрытия. Сварочные швы после такой обработки получаются совершенно чистыми и ровными. Они не нуждаются в дополнительной обработке в виде зачистки от остатков сварочного материала и шлаков. В ходе работ струя аргона полностью удаляет не только воздух из места сварки, но и все остаточные продукты.
Применение
Применения аргона:
Биологическая роль
Аргон не играет никакой биологической роли.
Физиологическое действие
Инертные газы обладают физиологическим действием, которое проявляется в их наркотическом воздействии на организм. Наркотический эффект от вдыхания аргона проявляется только при барометрическом давлении свыше 0,2 МПа.. Содержание аргона в высоких концентрациях во вдыхаемом воздухе может вызвать головокружение, тошноту, рвоту, потерю сознания и смерть от асфиксии (в результате кислородного голодания).
Периодическая система химических элементов Менделеева
Классификация хим. элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона/
Периодическая система элементов
Химические семейства элементов периодической таблицы
Где применяется аргон?
Аргон получил большое распространение в промышленности. Инертные свойства этого газа особенно востребованы в различных производственных процессах, где необходимо вытеснить один из самых активных элементов – кислород. Использование аргона очень дёшево, в сравнении с другими инертными летучими веществами, поэтому газ незаменим в том случае, когда требуется защитная среда при сваривании металлов, а также вытеснение влаги и кислорода в ёмкостях, где хранятся пищевые продукты.
Наполнение колб ламп накаливания инертным газом, позволяет значительно увеличить ресурс работы осветительного прибора. Кроме повышенного срока использования такие элементы обладают большей яркостью. Используется инертный газ и при производстве люминесцентных ламп. Применение аргона позволяет облегчить запуск разряда электрической дуги, а также значительно увеличить ресурс электродов.
При изготовлении стеклопакетов, инертным газом заполняются полости между стёклами, что позволяет значительно улучшить теплоизоляционные свойства. Учитывая тот факт, что аргон является абсолютно прозрачным, использование его никак не ограниченно даже при изготовлении многослойных конструкций.

Инертный газ аргон используется также в установках плазменной резки металлов. Преимущество использования этого газа заключается в том, что для возникновения дуги не требуется слишком высокого напряжения, поэтому такие установки могут иметь очень простую конструкцию. При генерации плазмы с использованием аргона образуется минимальное количество вредных газообразных веществ во время выполнения резки, поэтому этот метод идеально подходит для ручных приборов.
Благодаря возможности образовывать плазму при относительно невысоком напряжении, этот благородный газ используется в медицине для проведения аргоновой коагуляции. Такой метод успешно используется для удаления новообразований, а также для остановки кровотечений.
Аргон применяется и в химической промышленности. Благодаря отсутствию взаимодействия с другими элементами этот газ используется для получения сверхчистых веществ, а также для их анализа. В металлургической промышленности благородный газ позволяет обрабатывать такие металлы, как: титан, тантал, ниобий, бериллий, цирконий и др. Кроме этого, газ используется для перемешивания расплавленных веществ и снижения окисления хрома при производстве хромированной стали.
Способы получения аргона
Аргон является третьим по распространённости газом в земной атмосфере, поэтому наиболее логичным способом является добывание его из воздуха. Для этой цели используются специальные низкотемпературные ректификационные аппараты.
Процесс отделения инертного вещества осуществляется в такой последовательности:
Температура кипения аргона в ректификационной установке составляет минус 185,3˚С. При этом, кислород кипит при температуре на 3 градуса выше, а азот – на 13˚С ниже этого показателя. По причине небольшого отличия в переходе из одного агрегатного состояния в другое, на первом этапе отделения аргона смесь содержит большое количество жидкого кислорода. На заключительной стадии получения аргона производится отделение благородного газа из кислородно-аргоновой смеси. Процесс доочистки, как правило, осуществляется с помощью электролитического водорода. В результате реакции в контактном аппарате с кислородом образуется водяной пар, который затем утилизируется через влагоотделитель.
Аргон может быть получен не только из атмосферного воздуха. При некоторых производственных процессах этот газ может являться сопутствующим продуктом. Например, при производстве аммиака, аргон является примесью азота и является совершенно ненужным элементом, поэтому полученный таким образом газ имеет очень низкую себестоимость, в сравнении с криогенным аргоном.
Меры безопасности
Применение технического газа аргона не требует специальных мер предосторожности. Этот газ обладает высокими экологическими свойствами. Это природный газ, который не претерпевает никаких технологических изменений. При этом аргон не отличается повышенной взрывоопасностью. Технология транспортировки и хранения газовых баллонов, наполненных аргоном, соответствует требованиям, применяемым для остальных технических газов.
Читайте также:

