Методы изучения мутаций кратко
Обновлено: 03.07.2024
Методы определения генетических мутаций
Существуют различные методы, позволяющие выявлять генетические мутации. Блоттинг по Саузерну, описанный выше, используют для определения крупных геномных мутаций. В других методах применяют ПЦР-амплифицированную или клонированную ДНК Мутации могут быть обнаружены непосредственно с помощью секвенирования (определения первичной структуры макромолекул ДНК) или с использованием радиоизотопных и флюоресцентных систем.
Они также могут быть выявлены при сравнении последовательности опухолевой ДНК с ДНК, выделенной из нормальных тканей, или путем сравнения с последовательностью нормальной ДНК, описанной в литературе (например, в базах данных, размещенных в Интернете).
Анализ конформационного полиморфизма одноцепочечной ДНК — радиоизотопная методика определения мутаций, основанная на изменении формы (конформации) мутантной ДНК, которые могут быть выявлены при электрофорезе. Для этого нормальную и опухолевую ДНК клонируют с помощью ПЦР, денатурируют и исследуют с помощью гель-электрофреза. Мутантная ДНК меняет свою конформацию, принимая форму, отличную от нормальной, и приобретает отличную от нормальной подвижность при электрофорезе.
Эти изменения легко определяются при радиоавтографии. Рисунок ниже иллюстрирует методику анализа конформационного полиморфизма одноцепочечной (однонитевой) ДНК.
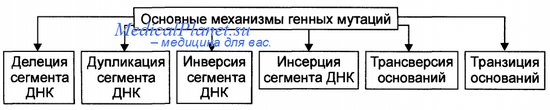
Виды и механизмы генных мутаций
Денатурационная высокоэффективная жидкостная хроматография — новый метод выявления мутаций, не требующий применения радиоактивных веществ. При этом исследовании нормальную и опухолевую ДНК амплифицируют (клонируют) с помощью ПЦР, смешивают и денатурируют для образования смеси одноцепочечных молекул ДНК. Затем проводится медленный отжиг, в результате которого вновь образуется двунитевая ДНК.
При спаривании нити нормальной ДНК с нитью опухолевой в месте мутации происходит нарушение спаривания — так называемый гетеродуплскс. Этот гетеродуплекс обладает температурой плавления, отличающейся от таковой для нормальной и опухолевой ДНК, т. с. гомодуплексных молекул, и благодаря этому его можно легко определить с помощью хроматографии.
Другие методы выявления мутаций — денатурирующий градиентный гель-электрофорез, аллель-специфический олигонуклеотидный анализ и аллель-специфическая амплификация — основаны на выявлении разницы в последовательностях нормальной и опухолевой ДНК.

Каждый из этих методов (за исключением прямого секвенирования) представляет собой средство скрининга на наличие мутации, но не определяет ее тип или характер нарушения последовательности. В настоящее время разработаны приборы и методы, позволяющие исследовать крупные фрагменты генома и экспоненциально повышающие наши возможности в выявлении мутаций.
К ним относятся молекулярно-генетический анализ ДНК (microarray analysis) с помощью генных чипов, или биочипов, и трансгеномная система WAVE DNA Fragmentation Analysis System, разработанная в Калифорнии компанией Transgenomic.
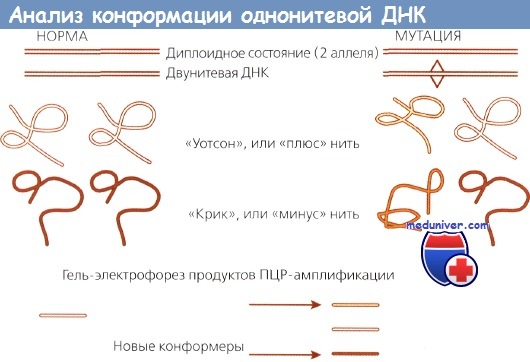
Анализ конформации однонитевой ДНК.
Слева - нормальные аллели имеют одинаковую последовательность и, соответственно, одинаковую конформацию, образуют две одинаковые полоски.
Справа представлен мутантный аллель. Темный и светлый отрезки имеют несколько различающуюся последовательность и в связи с этим мигрируют в геле с разной скоростью.
В результате образуются четыре полоски. Эта техника чувствительна для определения различий в несколько пар оснований.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021

ДНК находится в клетке внутри ядра. Она особым образом организована в виде хромосом – эти нитеподобные структуры можно рассмотреть в микроскоп с достаточно большим увеличением. Внутри хромосомы ДНК намотана на белки – гистоны. Когда гены неактивны, они расположены очень компактно, а во время считывания генетического материала молекула ДНК расплетается.
- 22 пары аутосом одинаковы у мужчин и женщин. В каждой паре хромосомы имеют одинаковую длину и содержат одинаковые наборы генов.
- Одна пара половых хромосом. У женщин это две X-хромосомы. Одна из них неактивна и плотно свернута – ее называют тельцем Барра. У мужчин одна половая хромосома представлена X-хромосомой, а вторая – Y-хромосомой, она меньше по размерам.
Методы исследования хромосом
Для исследования кариотипа применяют специальный метод – световую микроскопию дифференциально окрашенных метафазных хромосом культивированных лимфоцитов периферической крови.
Этот анализ применяется для диагностики различных хромосомных заболеваний. Он позволяет выявлять такие нарушения, как:
- Грубые изменения в кариотипе – изменение количества хромосом. Например, при синдроме Дауна в клетках ребенка присутствует лишняя хромосома №21.
- Присутствие в организме клеток с разными кариотипами. Это явление называется мозаицизмом.
- Хромосомные аберрации – нарушение структуры хромосом, внутрихромосомные и межхромосомные перестройки. Сюда относятся делеции (утрата участка хромосомы), дупликации (удвоение участка хромосомы), инверсии (поворот участка хромосомы на 180 градусов), транслокации (перенос участка одной хромосомы в другую).

Однако с помощью исследования кариотипа можно выявить не все генетические нарушения. Оно не способно обнаружить такие изменения, как:

Для получения дополнительной информации, не видимой в световой микроскоп, используют хромосомный микроматричный анализ (ХМА). С его помощью можно изучить все клинически значимые участки генома и выявить изменения в количестве и структуре хромосом, а именно микрополомки (микроделеции и микродупликации).
Во время хромосомного микроматричного анализа применяют технологию полногеномной амплификации и гибридизации фрагментов опытной ДНК с олигонуклеотидами, нанесенными на микроматрицу. Если объяснять простыми словами, то сначала ДНК, которую необходимо изучить, копируют, чтобы увеличить ее количество, а затем смешивают ее со специальными ДНК-микрочипами, которые помогают выявлять различные нарушения.
С помощью ХМА можно выявлять:
- изменения числа хромосом;
- дупликации и делеции, в том числе микродупликации и микроделеции;
- отсутствие гетерозиготности – утрату одной из двух копий гена. Это явление имеет важное значение в онкологии, при болезнях импринтинга (когда активность гена зависит от того, от какого из родителей он получен), аутосомно-рецессивных заболеваниях (связанных с рецессивными генами – о них мы поговорим ниже), близкородственных браках;
- однородительские дисомии, когда в геноме ребенка присутствуют две хромосомы от одного родителя.
Однако, как и предыдущий метод, хромосомный микроматричный анализ имеет некоторые ограничения. Он не позволяет выявлять или ограничен в выявлении таких аномалий, как:
Мутации в генах и заболевания, к которым они способны приводить
Все внешние признаки и особенности работы организма, которые человек получает от родителей, передаются с помощью генов. Это важнейшее свойство всех живых организмов называется наследственностью. В зависимости от того, как проявляются гены в тех или иных признаках, их делят на две большие группы.
Как выявляют рецессивные мутации?
Для выявления мутаций, которые передаются рецессивно, используют целый ряд исследований.
Если неизвестно, какую нужно выявить мутацию, то используют специальные панели.
Не в каждой семье можно отследить все возможные рецессивные заболевания. Тогда на помощь приходит секвенирование экзома – тест для определения генетических повреждений (мутаций) в ДНК путем исследования в одном тесте практически всех областей генома, кодирующих белки, изменения которых являются причиной наследственных болезней.
Секвенирование следующего поколения-NGS – определение последовательности нуклеотидов в геномной ДНК или в совокупности информационных РНК (транскриптоме) путем амплификации (копирования) множества коротких участков генов. Это разнообразие генных фрагментов в итоге покрывает всю совокупность целевых генов или, при необходимости, весь геном.

Анализ позволяет выявить точечные мутации, вставки, делеции, инверсии и перестановки в экзоме. Анализ не позволяет выявить большие перестройки; мутации с изменением числа копий (CNV); мутации, вовлеченные в трехаллельное наследование; мутации митохондриального генома; эпигенетические эффекты; большие тринуклеотидные повторы; рецессивные мутации, связанные с Х-хромосомой, у женщин при заболеваниях, связанных с неравномерной Х-деактивацией, фенокопии и однородительские дисомии, и гены, имеющие близкие по структуре псевдогены, могут не распознаваться.
Что делать, если в семье есть наследственное заболевание?
Существуют два способа выявить наследственные генетические мутации у эмбриона:
Предимплантационное генетическое тестирование (ПГТ) в цикле ЭКО. Это диагностика генетических заболеваний у эмбриона человека перед имплантацией в слизистую оболочку матки, то есть до начала беременности. Обычно для анализа проводится биопсия одного бластомера (клетки зародыша) у эмбриона на стадии дробления (4–10 бластомеров). Существует несколько видов ПГТ: на хромосомные отклонения, на моногенные заболевания и на структурные хромосомные перестройки. Данные Simon с соавторами (2018) говорят о том, что в случае проведения ЭКО с ПГТ у пациентки 38–40 лет результативность ЭКО составляет 60%. Но при исследовании эмбриона есть ряд ограничений. Так, из-за ограниченного числа клеток можно не определить мозаицизм.
Если нет возможности провести ЭКО с ПГТ, то используют второй вариант – исследование плодного материала во время беременности.
Для забора плодного материала используют инвазивные методы:
- биопсия хориона – когда берут клетки из плаценты;
- амниоцентез – когда берут клетки амниотической жидкости.
Далее эти клетки исследуют при помощи одного или нескольких генетических тестов (которые имеют свои ограничения). Проведение инвазивных методов может быть связано с риском для беременности порядка 1%.
Таким образом, проведя дополнительные исследования, можно значительно снизить риск рождения ребенка с генетическим заболеванием в конкретной семье. Но привести этот риск к нулю на сегодняшний день, к сожалению, невозможно, так как любой генетический тест имеет ряд ограничений, что делает невозможным исключить абсолютно все генетические болезни.

Автор статьи
Пелина Ангелина Георгиевна
Ведёт генетическое обследование доноров Репробанка, осуществляет подбор доноров для пар, имеющих ранее рождённых детей с установленной генетической патологией.
Читайте также:
- Положение о школе молодых родителей в школе
- Сценарий теремок про школу
- Мировоззренческие нравственные и духовные основы сознательного служения отечеству кратко
- Индивидуальный образовательный маршрут для ребенка с зпр в доу образец логопед
- Инструкция по охране труда при работе с пароконвектоматом в доу

