2 закон термодинамики кратко для презентации
Обновлено: 08.07.2024
Презентация на тему: " Второй закон термодинамики. Процессы ОбратимыеНеобратимые." — Транскрипт:
1 Второй закон термодинамики
3 Обратимый процесс Это процесс, который может происходить как в прямом, так и в обратном направлении Обратимый процесс – это идеализация реального процесса. Обратимый процесс – это идеализация реального процесса. Все макроскопические процессы проходят в определенном направлении
4 Необратимый процесс Процесс, обратный которому самопроизвольно не происходит Все макроскопические процессы являются необратимыми
5 Примеры Кусок льда, внесенный в комнату, не отдает энергию окружающей среде и не охлаждается Маятник самостоятельно не наращивает амплитуду колебаний
6 Ни охлаждение льда в первом случае, ни увеличение амплитуды во втором не противоречит ни закону сохранения энергии, ни законам механики. Оно противоречит лишь второму закону термодинамики
7 Второй закон термодинамики В циклически действующем тепловом двигателе невозможно преобразовать все количество теплоты, полученное от нагревателя, в механическую работу
8 Формулировка Р. Клаузиуса Невозможно перевести тепло от более холодной системы к более горячей при отсутствии одновременных изменений в обоих системах или окружающих телах
9 Формулировка У. Кельвина Невозможно осуществить такой периодический процесс, единственным результатом которого было бы совершение работы за счет теплоты взятой от одного источника
10 Статистическое истолкование второго закона термодинамики Изолированная система самопроизвольно переходит из менее вероятного состояния в более вероятное, или Замкнутая система многих частиц самопроизвольно переходит из более упорядоченного состояния в менее упорядоченное
11 Используемая литература Физика. Молекулярная физика и термодинамика. 10 класс. Г. Я. Мякишев, А. З. Синяков, 2002 г. Дрофа
Свидетельство и скидка на обучение каждому участнику
Зарегистрироваться 15–17 марта 2022 г.

Описание презентации по отдельным слайдам:

Второй закон термодинамики Презентация разработана преподавателем КС и ПТ Каракашевой И.В. Санкт – Петербург 2016

Цели урока Образовательные: познакомить учащихся со вторым законом термодинамики, его статистическим характером; обеспечить усвоение понятий, связанных с использованием законов термодинамики; актуализировать знания о строении вещества; расширить общий кругозор учащихся Развивающие: создать условия для развития коммуникативных навыков; создать условия для развития аналитических способностей учащихся, умения анализировать, сопоставлять, сравнивать , обобщать, делать выводы; создать условия для развития памяти, внимания, воображения Воспитательные: способствовать развитию умения отстаивать свою точку зрения; способствовать развитию культуры взаимоотношений при работе в коллективе *

Ответьте на вопросы 1. Вспомните формулировку первого закона термодинамики. 2. Допускает ли первый закон термодинамики самопроизвольный переход тепла от менее нагретого тела к более нагретому? 3. Наблюдаются ли такие процессы в природе?

Первый закон термодинамики Первый закон термодинамики устанавливает связь между количеством теплоты Q, полученной системой, изменением ΔU ее внутренней энергии и работой A, совершенной над внешними телами: Q = ΔU + A. Согласно этому закону, энергия не может быть создана или уничтожена; она передается от одной системы к другой и превращается из одной формы в другую. Процессы, нарушающие первый закон термодинамики, никогда не наблюдались. На рисунке изображены устройства, запрещенные первым законом термодинамики.

Первый закон термодинамики Циклически работающие тепловые машины, запрещаемые первым законом термодинамики: 1 – вечный двигатель 1 рода, совершающий работу без потребления энергии извне; 2 – тепловая машина с коэффициентом полезного действия η > 1

Невозможность создания вечного двигателя Задолго до открытия закона сохранения энергии Французская Академия наук приняла в 1775г. решение не рассматривать проектов вечных двигателей первого рода. Под вечным двигателем первого рода понимают устройство, которое могло бы совершать неограниченное количество работы без затраты топлива или каких-либо других материалов. Вечные двигатели обычно конструируют на основе использования следующих приёмов или их комбинаций: 1) Подъем воды с помощью архимедова винта; 2) Подъем воды с помощью капилляров; 3) Использование колеса с неуравновешивающимися грузами; 4) Природные магниты; 5) Электромагнетизм; 6) Пар или сжатый воздух.

Необратимые процессы Первый закон термодинамики не устанавливает направления тепловых процессов. Тепловые процессы, которые могут протекать только в одном направлении, называются необратимыми. Например: 1. При тепловом контакте двух тел с разными температурами тепловой поток всегда направлен от более теплого тела к более холодному. Никогда не наблюдается самопроизвольный процесс передачи тепла от тела с низкой температурой к телу с более высокой температурой, т.е. процесс теплообмена при конечной разности температур является необратимым. 2. Процесс диффузии. Открыв пузырёк с духами, мы быстро почувствуем запах духов. Молекулы ароматического вещества благодаря тепловому движению проникают в пространство между молекулами воздуха. Трудно представить, чтобы все они вновь собрались в пузырьке. Все реальные процессы необратимы

Обратимые процессы Обратимыми процессами называют процессы перехода системы из одного равновесного состояния в другое, которые можно провести в обратном направлении через ту же последовательность промежуточных равновесных состояний. При этом сама система и окружающие тела возвращаются к исходному состоянию. Равновесное состояние — это состояние, при котором температура и давление во всех точках системы одинаковы. Обратимый процесс должен протекать очень медленно, чтобы каждое промежуточное состояние было равновесным. Круговой процесс, состоящий из двух изотерм и двух адиабат (цикл Карно) является единственным обратимым круговым процессом, при котором рабочее тело приводится в тепловой контакт только с двумя тепловыми резервуарами. Все остальные круговые процессы, проводимые с двумя тепловыми резервуарами, необратимы.

Обратимые процессы Произвольный обратимый цикл как последовательность малых изотермических и адиабатических участков

Второй закон термодинамики Первый закон термодинамики не может отличить обратимые процессы от необратимых. Он просто требует от термодинамического процесса определенного энергетического баланса и ничего не говорит о том, возможен такой процесс или нет. Направление самопроизвольно протекающих процессов устанавливает второй закон термодинамики. Он может быть сформулирован в виде запрета на определенные виды термодинамических процессов.

Второй закон термодинамики Формулировка У.Кельвина (1851 г.) Невозможно осуществить такой периодический процесс, единственным результатом которого было бы совершение работы за счет теплоты взятой от одного источника

Второй закон термодинамики Формулировка У.Кельвина (1851 г.) Гипотетическую тепловую машину, в которой мог бы происходить такой процесс, называют вечным двигателем второго рода. В земных условиях такая машина могла бы отбирать тепловую энергию, например, у Мирового океана и полностью превращать ее в работу. Масса воды в Мировом океане составляет примерно 1021 кг, и при ее охлаждении на один градус выделилось бы огромное количество энергии (≈ 1024 Дж), эквивалентное полному сжиганию 1017 кг угля. Ежегодно вырабатываемая на Земле энергия приблизительно в 104 раз меньше. Поэтому вечный двигатель второго рода был бы для человечества не менее привлекателен, чем вечный двигатель первого рода, запрещенный первым законом термодинамики.

Второй закон термодинамики Формулировка Р. Клаузиуса (1850 г.) Невозможен процесс, единственным результатом которого была бы передача энергии путем теплообмена от тела с низкой температурой к телу с более высокой температурой.

Второй закон термодинамики Процессы, не противоречащие первому закону термодинамики, но запрещаемые вторым законом: 1 – вечный двигатель второго рода; 2 – самопроизвольный переход тепла от холодного тела к более теплому (идеальная холодильная машина)

Второй закон термодинамики Статистический характер Констатируя факт необратимости процессов в природе, второй закон не дает ему никакого объяснения. Необратимость макропроцессов вроде парадоксальна: ведь все микропроцессы обратимы. В микромире нет сил трения; все силы – электромагнитные, зависят только от взаимного положения частиц и поэтому обратимы во времени. Уравнения движения молекулы тоже обратимы во времени, т.к. содержат только силы, зависящие от расстояний. Одному и тому же макросостоянию системы отвечает огромное число микроскопических состояний. Переход одной молекулы на место другой – уже изменение микросостояния системы, но это не приводит к изменению макросостояния


Второй закон термодинамики Статистический характер Л.Больцман высказал предположение, что все микросостояния замкнутой системы равновероятны. Микросостояния непрерывно сменяют друг друга, а макросостояние остается неизменным. Чем больше микросостояний реализуют данное макросостояние, тем оно более вероятно. Т.о., эволюция системы происходит в направлении от маловероятных состояний к состояниям более вероятным. Обратный процесс не является невозможным, просто он чрезвычайно маловероятен.

Второй закон термодинамики Статистический характер Так, состояние газа, при котором молекулы движутся хаотично, является наиболее вероятным, наиболее вероятным является и равномерное распределение молекул по объёму Однако возможно, что благодаря случайным перемещениям молекул все они окажутся в какой-то части сосуда, но вероятность такого состояния чрезвычайно мала. Соответственно не противоречит законам природы даже такой процесс, в результате которого при случайном движении молекул воздуха все они соберутся в одной половине класса, а учащиеся в другой половине класса задохнутся. Но реально это событие никогда не происходило в прошлом и не произойдёт в будущем.


Границы применимости второго закона термодинамики Закон справедлив только для систем с огромным числом частиц ( в системах с малым числом частиц могут наблюдаться случайные отклонения от равновесного состояния) Такие случайные отклонения системы от равновесия называются флуктуациями. Именно флуктуациями плотности газа в областях порядка длины световой волны объясняются рассеяние света в атмосфере Земли и голубой цвет неба. Флуктуации давления в малых объёмах объясняют броуновское движение.

Ответьте на вопросы 1. Какие процессы называются необратимыми? Назовите наиболее типичные необратимые процессы. 2. Как формулируется второй закон термодинамики? 3. Какое состояние газа является наиболее вероятным и соответствует равновесному состоянию?

№ слайда 1

№ слайда 2
1. Два положения второго закона термодинамики Различные формы передачи энергии неравноценны. Энергия теплового движения стремиться в большей степени, чем другие виды энергии, сохраниться за счет какой-либо другой энергии. Так, естественные процессы имеют определённую направленность, а именно они протекают в сторону достижения системой равновесного состояния. На практике не обнаружено случаев самопроизвольного перехода теплоты от тела с более низкой температурой к телу с более высокой температурой.

№ слайда 3
Второй закон термодинамики обобщает особенности теплоты как формы передачи энергии. Он выражает закон о существовании энтропии и определяет закономерности её изменения при протекании обратимых и необратимых процессов в изолированных системах. 1 положение: теплота не может переходить самопроизвольно от менее нагретого тела к более нагретому. 2 положение: только часть подведенной теплоты может переведена в работу, а остальная же часть отводится в холодильник.

№ слайда 4
Круговые процессы тепловых машин Процесс в котором газ пройдя ряд последовательных состояний, возвращается в исходное состояние называется круговым процессом или циклом.
№ слайда 5
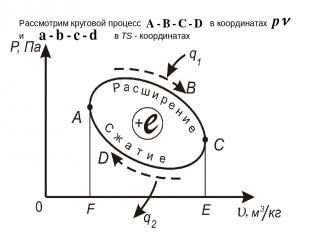
Рассмотрим круговой процесс в координатах и в TS - координатах
№ слайда 6
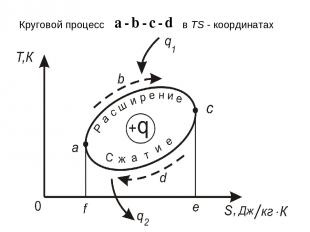
Круговой процесс в TS - координатах

№ слайда 7
На участке A-B-C рабочее тело получает от нагревателя (источника теплоты) некоторое количество теплоты, в результате чего совершает работу расширения . Затем на участке сжатия оно возвра- щается в исходное положение, определяемое точкой А. Для осуществления этого процесса от рабочего тела необходимо отвести определенное количество теплоты. Работа сжатия на участке отрицательная. Следовательно, работа цикла равна равная площади , т.е. площади цикла.

№ слайда 8
Если в круговом процессе линия расширения лежит выше линии сжатия, то он называется прямым. По этому циклу работают все тепловые двигатели. Если линия расширения лежит ниже линии сжатия, то такой круговой процесс называется обратным. По этому циклу работают все холодильные установки и тепловые насосы.

№ слайда 9
В координатах на участке , протекающем при , к рабочему телу от источника теплоты подводиться количество теплоты равное площади Для возвращения в исходное состояние необходимо отвести от рабочего тела количество теплоты равное площади .Отсюда следует, что количество теплоты, превращенной в цикле в работу, равно равное площади .

№ слайда 10
Таким образом, для осуществления кругового процесса необходимо наличие трех элементов: источника теплоты (нагревателя) с температурой , охладителя с температурой и рабочего тела, которое последова- тельно вступает в теплообмен с нагревателем и охладителем.

№ слайда 11
2. Термический КПД цикла. Холодильный коэффициент. Основной теплотехнической характе- ристикой цикла является термический коэффициент полезного действия . Термический КПД показывает какая часть затраченной теплоты превращается в работу. Он равен отношению теплоты затраченной на получение полезной работы ко всей затраченной теплоте.

№ слайда 12
Термический КПД равен: Термическим КПД оценивается степень совершенства цикла теплового двигателя. Чем выше КПД, тем больше работа, полученная при заданном подводе теплоты , т.е. экономичность двигателя выше.

№ слайда 13
Холодильный коэффициент Работа холодильных машин оценивается холодильным коэффициентом. Холодильный коэффициент это есть отношение отведенной теплоты к затраченной на это работе
№ слайда 14
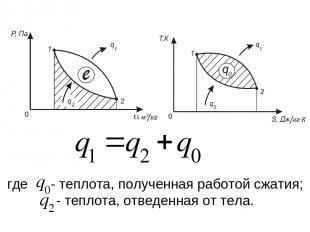
где - теплота, полученная работой сжатия; - теплота, отведенная от тела.
№ слайда 15
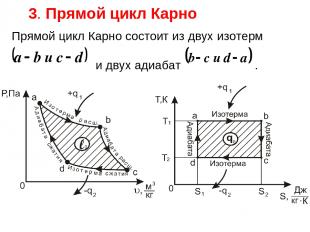
3. Прямой цикл Карно Прямой цикл Карно состоит из двух изотерм и двух адиабат .

№ слайда 16
На участке расширения к рабочему телу подводиться от нагревателя количество теплоты при температуре . Далее на участке происходит адиабатное расширение от температуры до На участке происходит изотермическое сжатие. При этом от рабочего тела отводится к охладителю количество теплоты при температуре .

№ слайда 17
В результате дальнейшего адиабатного сжатия на участке рабочее тело возвращается в исходное состояние. На участках изменение внутренней энергии равно нулю, а подведенная (отведенная) теплота равна работе. На участках нет подвода (отвода) теплоты, а работа совершается за счет внутренней энергии.
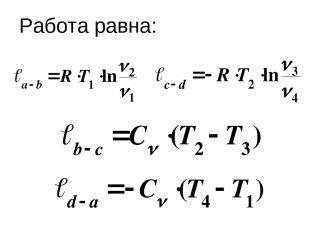
№ слайда 18

№ слайда 19
Термический КПД прямого цикла Карно равен:
№ слайда 20
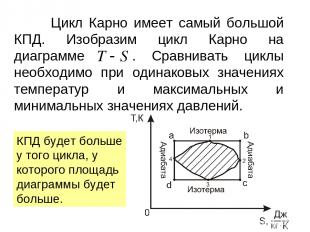
Цикл Карно имеет самый большой КПД. Изобразим цикл Карно на диаграмме . Сравнивать циклы необходимо при одинаковых значениях температур и максимальных и минимальных значениях давлений. КПД будет больше у того цикла, у которого площадь диаграммы будет больше.

№ слайда 21
Полученные уравнения позволяют сделать следующие выводы: Термический КПД зависит только от температур ; 2. Чем разность больше между тем выше ; 3. Т.к. , то не может быть больше 1, он всегда меньше 1; 4. не зависит от природы рабочего тела.
№ слайда 22
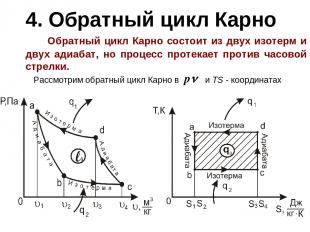
4. Обратный цикл Карно Обратный цикл Карно состоит из двух изотерм и двух адиабат, но процесс протекает против часовой стрелки. Рассмотрим обратный цикл Карно в и TS - координатах

№ слайда 23
- адиабатное расширение сжатого газа. Температура резко понижается; - рабочее тело продолжает расширяться в изотермическом процессе; - теплота, отбираемая от охладителя; - адиабатное сжатие газа. Температура газа значительно повышается и становится выше, чем температура окружающей среды; - охлаждение нагретого газа в изотермическом процессе с отводом теплоты .

№ слайда 24

Данная презентация подготовлена для учащихся 10 класса по теме "Второй закон термодинамики". Её можно использовать при объяснении нового материала по термодинамики. Добавлены картинки учёных, визуально быстро воспринимаются. Есть определения, которые учащиеся должны знать. Презентация легко читается.

ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ
Необратимые

ОБРАТИМЫЙ ПРОЦЕСС
- Это процесс, который может происходить как в прямом, так и в обратном направлении
- Обратимый процесс – это идеализация реального процесса.
- Все макроскопические процессы проходят в определенном направлении
НЕОБРАТИМЫЙ ПРОЦЕСС
Ни охлаждение льда в первом случае, ни увеличение амплитуды во втором не противоречит ни закону сохранения энергии, ни законам механики. Оно противоречит лишь второму закону термодинамики

ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ
В циклически действующем тепловом двигателе невозможно преобразовать все количество теплоты, полученное от нагревателя, в механическую работу
Читайте также:

