Таргетная терапия в онкологии доклад
Обновлено: 02.05.2024
Сегодня поиск лекарственных средств идёт целенаправленно и в клинической практике уже используются три варианта таргетного воздействия:
- Действие на определённые клеточные мишени, в числе которых рецепторы половых гормонов, гены и внутриклеточные ферменты.
- Повреждение обеспечивающих нормальную жизнедеятельность раковой опухоли внеклеточных структур, например, питающих опухоль сосудов.
- Выключение передачи внутриклеточных биохимических сигналов, которые позволяют раку жить и размножаться, в цепочке биохимических реакций — сигнального пути.
Таргетная терапия входит в лекарственное противоопухолевое лечение, но постепенно отделяется от понятия химиотерапии, поскольку механизм действия иной, но результат общий — уничтожение рака. Лекарства эти применяются только вместе с цитостатиками и усиливают их эффективность.
Преимущества таргетной терапии
Можно выделить следующие преимущества таргетных препаратов: [5]
Препараты для таргетной терапии
В настоящее время существует довольно много разных таргетных препаратов. Одни уже давно внедрены в клиническую практику, другие недавно закончили или все еще проходят испытания. В зависимости от эффектов, их можно разделить, на несколько групп: [4,5]
- В каждой клетке человека работают так называемые сигнальные пути — каскады химических реакций, итогом которых является то или иное событие. Таргетные препараты могут блокировать звенья в сигнальных путях, отвечающих за размножение клеток.
- Некоторые препараты изменяют важные белки таким образом, что клетка погибает.
- Злокачественная опухоль активно растет и распространяется по организму, поэтому ей нужно много кислорода и питательных веществ. Раковые клетки выделяют вещества, которые стимулируют ангиогенез — рост новых сосудов. Существуют антиангиогенные таргетные препараты, которые могут их заблокировать.
- Воздействуя на некоторые молекулы, можно активировать иммунитет, заставить его распознавать и убивать раковые клетки.
- Есть таргетные препараты, которые вводят в раковые клетки токсины (при этом не затрагивая здоровые клетки), уничтожающие их.
При каких онкозаболеваниях применяют таргетную терапию?
Таргетная терапия в лечении рака молочной железы
Гормональные препараты, созданные для лечения рака молочной железы, весьма похожи на настоящие гормоны, но несут в себе не программу жизни рака, а программу его смерти, и гормональный рецептор активно выбирает не родной гормон, а лекарство. Сегодня наряду с тамоксифеном используются антиэстрогены торемифен (фарестон) и фульвестрант (фазлодекс).
Вторую группу таргетных гормональных средств составляют ингибиторы фермента ароматазы, превращающего один вид полового гормона в другой. Ароматаза находится в жировой клетчатке и синтезируется яичниками, выключение её с помощью лекарственного препарата нарушает синтез гормона, в котором нуждаются раковые клетки. [1]
Лечение герцептином
Чувствительность к химиотерапии можно предсказать по наличию специфического гена HER2-neu — гена множественной лекарственной резистентности. Обнаружение этого гена говорит о том, что опухоль может не реагировать на присутствие лекарства-убийцы.
Раковая клетка пытается избежать гибели несколькими способами, одновременно включая механизмы:
- быстрого выведения химиопрепаратов в межклеточное пространство;
- обезвреживая цитостатик специальными белками;
- быстро восстанавливая повреждения;
- изменяя мишень для препарата, предлагая ему похожий белок, не имеющий принципиального значения для дальнейшей жизнедеятельности;
- изменяя роль ключевых генов, контролирующих клеточный апоптоз (гибель), которые больше не могут запустить фатальные изменения.
Найден ключевой ген рака молочной железы, получивший название HER 2, и заставляющий рецепторы на клеточной поверхности избыточно активно захватывать факторы клеточного роста, что приводит к неуправляемому делению. В некоторых случаях ген амплифицируется, то есть образует в ДНК не одну, а целый пучок генетических копий.
Помогает работе герцептина ещё один таргетный препарат перьета (пертузумаб) — белок, синтезируемый иммунными клетками, или моноклональное антитело. Перьета на поверхности раковой клетки соединяется с определённым рецептором, не позволяя фактору роста проникнуть внутрь и активировать ген HER2. Перьета вводится вместе с герцептином и химиопрепаратом доцетакселом.
Аналогично герцептину работает лапатиниб (тайверб), применяемый во второй очереди после герцептина с перьетой. [2,7]

Таргетная терапия при метастатическом раке легкого
Таргетные препараты при немелкоклеточном раке легкого могут применяться в сочетании с химиопрепаратами или самостоятельно. Применяются препараты, которые блокируют ангиогенез (рамицирумаб, бевацизумаб), мутантные белки, заставляющие раковые клетки размножаться: EGFR (афатиниб, эрлотиниб, гефитиниб), ALK (бригатиниб, алектиниб, церитиниб, кризотиниб), BRAF (траметиниб, дабрафениб). [7]
Таргетная терапия при меланоме
Исследования показывают, что примерно в половине всех меланом клетки имеют мутацию в гене BRAF. Из-за этого в них образуется одноименный мутантный белок, и они быстро размножаются. В таких случаях эффективны таргетные препараты из группы ингибиторов BRAF: дабрафениб, вемурафениб.
В тандеме с геном BRAF работает ген MEK. Если в нем обнаружена мутация, врач может назначить ингибиторы MEK: кобиметиниб и траметиниб.
Некоторые меланомы (на участках кожи, на которые постоянно воздействуют солнечные лучи, на ладонях и подошвах, слизистых оболочках, под ногтями) имеют мутацию в гене C-KIT. При этом могут помочь препараты иматиниб и нилотиниб. [2,7]
Таргетная терапия при раке поджелудочной железы
На поздних стадиях рака поджелудочной железы некоторым пациентам назначают химиотерапию в сочетании с эрлотинибом, таргетным препаратом, который блокирует рецептор эпидермального фактора роста (EGFR). [7]
Таргетная терапия при колоректальном раке
При раке толстой и прямой кишки применяются три группы таргетных препаратов: [5,7]
- Ингибиторы фактор роста эндотелия сосудов (VEGF), белка, который вырабатывается раковыми клетками и стимулирует ангиогенез: рамуцирумаб, бевацизумаб.
- Ингибиторы рецепторов эпидермального фактора роста, которые находятся на поверхности раковых клеток и, находясь в активном состоянии, заставляют их размножаться: панитумумаб, цетуксимаб.
- Ингибиторы киназы — белка-фермента, который выполняет разные функции, в том числе стимулирует клеточный рост: регорафениб.
Таргетная терапия при раке желудка
Примерно в 1 из 5 случаев в клетках злокачественных опухолей желудка содержится повышенное количество белка HER2-neu (или только HER2), который стимулирует их размножение. В таких случаях применяют таргетный препарат трастузумаб (Герцептин). Также при раке желудка применяют ингибитор ангиогенеза рамуцирумаб (Цирамза). [7]
Таргетная терапия при раке почки
При раке почек применяют: [2,7]
- Таргетные препараты, которые блокируют ангиогенез: бевацизумаб.
- Таргетные препараты, которые блокируют белки-тирозинкиназы: сорафениб, сунитиниб, пазопаниб, акситиниб, кабозантиниб, ленватиниб.
- Таргетные препараты, которые блокируют белок mTOR: темсиролимус, эверолимус.
Отзыв пациента о таргетной терапии
-
— 6 900 руб.
- Проведение внутрипузырной химиотерапии (без стоимости лекарственных препаратов) — 26 400 руб.
- Проведение внутрибрюшинной химиотерапии (без стоимости лекарственных препаратов) — 24 100 руб.
- Проведение иммунотерапии (без стоимости лекарственных препаратов) — 19 000 руб.
- Проведение интратекальной химиотерапии — 26 600 руб.
- Проведение гипертермической интраперитонеальной химиотерапии — 352 000 руб.
- Проведение химиотерапии с использованием инфузионной помпы 1 сутки (без стоимости лекарственных препаратов) — 22 600 руб.
- Проведение анти PD-1 терапии — 423 500 руб.

О таргетных препаратах в онкологии, лечении различных видах опухолей препаратами таргетной терапии рассказывает онколог-химиотерапевт, к.м.н., врач высшей категории Анна Игоревна Буйнякова.
За последнее десятилетие в лечении онкологических пациентов был получен значительный прорыв.
Эра химиотерапии претерпела важные изменения. Раньше назначение противоопухолевой терапии основывалось на главных фенотипических характеристиках, таких как: локализация первичной опухоли, гистологический тип и степень ее дифференцировки, общее состояние больного, характер распространения опухолевого процесса и т.д.
К существенным недостаткам химиотерапии следует отнести ограниченную эффективность цитостатиков; диапазон их активности колеблется от 20 до 80%.
Максимальная эффективность наблюдается у ограниченной группы препаратов, таких как Таксаны, производные и препараты Платины. Поэтому сегодня в помощь врачу и пациенту есть препараты таргетной терапии.
Появление новых эффективных препаратов для лечения пациентов с онкологическим диагнозом расширяет возможности терапии. Сегодня мы используем комбинации определенных таргетных и химиопрепаратов, имеющих разные точки приложения, но обладающих высоким синергизмом противоопухолевого действия.
В современной онкологии без знания молекулярно-генетических характеристик опухоли не обойтись. Оно позволяет индивидуализировать лечение и улучшить качество жизни, а по некоторым нозологическим формам значительно увеличить ее продолжительность. И речь идет не о месяцах, а о годах, отвоеванных у болезни. Лечение таргетными препаратами обладает принципиально иными механизмами воздействия на опухоль.
Большинство рецепторов в опухоли – это факторы роста, представленные тирозинкиназными рецепторами, каждый из которых имеет экстрацеллюлярную часть - часть вне клетки, ответственную за соединение с фактором роста или другим лигандом - рецептором, трансмембранную часть (в толще стенки клетки) и интрацеллюлярную часть (в глубине клетки), представленную ферментом тирозинкиназой С.
На все эти части рецептора в той или иной форме воздействуют таргетные препараты, блокируя или разрушая их. Так погибает опухолевая клетка.
Выключение функции рецептора возможно за счет блокирования экстрацеллюлярной части рецептора моноклональными антителами или ингибирования активности тирозинкиназы С.
Пришло время признать, что таргетные препараты в онкологии как в монорежиме, так и в комбинации с химиотерапией могут обладать высокой противоопухолевой активностью.
Но наряду с этим нормальные ткани также могут экспрессировать аналогичные рецепторы, в связи с чем может наблюдаться ряд побочных эффектов, отличных от наблюдаемых при стандартной химиотерапии. Но этого не стоит бояться, так как все побочные эффекты лечения известны, тщательно изучены и успешно корректируются либо снижением дозы, либо индивидуальным назначением симптоматической терапии.
Некоторое таргетные препараты при раке выпускаются в таблетированной форме, что очень удобно для применения на дому и для коррекции дозировки с целью контроля побочных реакций.
Наряду с гормональным или химиотерапевтическим лечением данный вид терапии основан на приёме специальных медикаментозных препаратов. Ключевым отличием таргетного воздействия является то, что разрушительный эффект оказывается исключительно на злокачественные клетки. Также таргетная терапия может блокировать процессы канцерогенеза (размножения клеток рака). Рассмотрим особенности и возможные направления применения данного метода в онкологии.
Развитие таргетной терапии и преимущества метода
Рак – это бич современного общества, а потому процесс борьбы с онкологическими заболеваниями никогда не прекращается. Непосредственно при исследовании таргетного воздействия ищут новые комбинации препаратов и генерируют действующие вещества, находящие и разрушающие злокачественного образования. На сегодняшний день таргетная терапия осуществляется в следующих формах:
- воздействие на конкретные клеточные компоненты (рецепторы половых гормонов, элементы ДНК, ферменты);
- повреждение структур, отвечающих за жизнедеятельность новообразований, к примеру, сосудистой системы, питающей клетки;
- блокировка внутриклеточных биохимических сигналов, также отвечающих за развитие и распространение рака по организму.
Однако полного разделения таргетного воздействия и химиотерапии на данный момент не произошло, т.к. новые препараты, используемые в борьбе с раком, всё также сочетаются с цитостатиками для усиления эффективности. Потому и полного отсутствия побочных эффектов, в частности, проявляющихся в клеточной биохимии, гарантировать нельзя.
Преимущества таргетной терапии
Принято сравнивать данный метод с другими терапевтическими подходами к борьбе с раком. Выделяют следующие преимущества от использования таргетных средств:
Назначение этого метода, как единственного способа лечения, либо в комплексе с химиотерапией, может произвести только специалист. Зачастую это делается на консилиуме при поддержке коллег, изучивших клиническую картину пациента.
Стоит отметить, что этот подход к борьбе с раковыми опухолями актуален практически для каждого пациента. Необходимо провести лишь специализированные исследования, которые позволят отобрать наиболее эффективные действующие вещества под каждый конкретный случай заболевания.
Разнообразие таргетных препаратов
Сегодня существует множество таргетных средств для осуществления точечного лечения различных форм рака. Некоторые активно используются в медицинской практике, другие же еще не связаны с онкологией, поскольку лишь тестируются или проходят клинические испытания. Исходя из эффекта, оказываемого в процессе лечения теми или иными таргетными средствами, все они делятся на следующие группы:
- блокираторы звеньев в сигнальных путях, обеспечивающих процесс клеточного размножения;
- программаторы белков, меняющие структуру клеток таким образом, чтобы они самоуничтожались;
- антиангиогенные таргетные препараты, направленные на блокировку роста сосудов, подающих к очагам рака кислород и прочие необходимые компоненты;
- активаторы иммунной защиты, программирующие ряд молекул на уничтожение клеток рака;
- поставщики токсинов в злокачественные клетки, не затрагивающие здоровые объекты.
Конкретный способ борьбы с раком может определить исключительно лечащий врач, имеющий полное представление об особенностях развивающейся опухоли. Его рекомендации следует исполнять беспрекословно, избегая какого-либо самолечения. Любые народные средства или препараты, помогающие знакомым и родственникам, лишь отнимут время, которое может быть потрачено лечащим врачом с пользой.
Виды рака, поддающиеся таргетной терапии
При раке молочной железы
Прямое воздействие оказывается на гормональный рецептор, расположенный внутри железы. Тот, в свою очередь, функционирует в сочетании с половыми гормонами, находящимися в крови. Применяемый препарат подменяет гормон, таким образом рак уничтожается стандартным функционалом организма. Также возможна подмена половых гормонов в целях блокировки продуцирования веществ, необходимых клеткам рака.
При раке легкого
В данном случае таргетная терапия часто сочетается с химиотерапией, но может быть и одиночным методом. Суть таргетных препаратов заключается в том, чтобы заблокировать ангиогинез, исключить из работы органа мутантные белки, приводящие к тому, что клетки рака активно размножаются.
При колоректальном раке
При лечении формы рака, поражающей толстую и прямую кишку, применяются препараты, воздействующие на следующие элементы:
- эндотелий сосудов, питающих раковые клетки, а также белок, стимулирующий ангиогенез;
- рецепторы эпидермального роста, расположенные на поверхности злокачественного образования;
- киназу – ферментный белок с разным функциями.
В зависимости от индивидуальных показаний лечение может осуществляться как в комплексе, так и по одному из направлений.
При раке почки
Опять же, когда раком поражаются почки, таргетные препараты нацелены на блокировку ангиогинеза, а также белков тирозинкиназы и mTOR.
Внимание! Это далеко не весь перечень опухолей, которые поддаются лечению посредством таргетной терапии. В сети Интернет вы можете найти обширный перечень таргетных препаратов, подходящих для каждого конкретного случая. Однако назначение на лечение может дать исключительно профильный специалист после тщательного осмотра, лабораторных исследований и составления оптимального плана приёма препаратов.
Возможные побочные эффекты таргетной терапии
Как уже было сказано, таргетная терапия отличается от химиотерапии тем, что оказывает минимум негативного воздействия на здоровые клетки организма. Если при лечении в комплексе с химиотерапией появление побочных эффектов очевидно, то самостоятельное применение таргетных препаратов вызывает иной спектр негативных проявлений.
- Сорафениб может поражать ладони и подошвы (эритродизестезия), вызывать артериальную гипертензию, диарею и т.д.
- Ленватиниб к вышеперечисленному может добавить протеинурию, ухудшить аппетит, вызвать тромбоцитопению и т.д.
- Вандетаниб – привести к образованию сыпи, помутнению роговицы глаза, спровоцировать различные аномалии на электрокардиограмме и т.д.
Во избежание подобных эффектов, на определённое время лечение любой формы рака может быть приостановлено, либо специалист уменьшит дозировку, негативно влияющего на организм препарата. Также может последовать отказ от химиотерапии, как сопутствующего метода. Для улучшения самочувствия и восстановления пораженных побочными эффектами участков могут быть назначены сопроводительные препараты.
Чтобы можно было проконтролировать приём медикаментов, когда осуществляется лечение посредством таргетной терапии, пациент госпитализируется. Если выраженные побочные эффекты отсутствуют, а больной легко переносит все действующие вещества, то в дальнейшем лечебный процесс проводится амбулаторно.
Поддержка больных
Также при борьбе с раковыми заболеваниями одной из ключевых задач врача и самого пациента является формирование положительного психоэмоционального фона. Независимо от того, какой метод воздействия избран, будь то таргетная терапия или облучение раковых клеток, недопустимо настраиваться на отрицательный результат.
Квалифицированные специалисты способствуют улучшению настроения и общего самочувствия пациентов следующим образом:
При этом больной должен постоянно находиться в благоприятных условиях. Насколько бы эффективна ни была таргетная терапия – положительный настрой вносит весомый вклад в конечный результат лечебного процесса.
Реабилитационный процесс
Как такового, восстановления после таргетной терапии нет, поскольку она не имеет выраженного побочного действия, что было сказано ранее. Однако стоит помнить, что таргетная терапия неизменно связана с действующими веществами химиотерапевтического формата, а потому при восстановлении пациентов, прошедших комплекс приёма таких средств актуальны все рекомендации, касающиеся второго метода. Об этих и других нюансах лечебного процесса читайте в статьях нашего сайта.
Зачастую сразу после выписки пациенты могут приступать к рабочему процессу, если, конечно же, речь не идёт о финишных стадиях развития раковой опухоли. В таком случае таргетная терапия изначально направлена лишь на продление срока жизни и улучшение состояния пациента.
Обращение в Центр профессора Капранова
Предлагаем пройти обследование в Центре эндоваскулярной хирургии. Обращайтесь в наше учреждение в Москве, чтобы получить компетентную помощь от высококвалифицированных врачей различного профиля.
Основные преимущества обращения за помощью в Центр профессора Капранова:
- возможность прохождения всестороннего обследования и всех лабораторных/аппаратных анализов на месте;
- огромный опыт каждого практикующего врача, дающего максимально обширные рекомендации и формирующего оптимальный план лечебного процесса;
- комфортные условия пребывания пациентов (палаты, процедурные кабинеты, прочая инфраструктура центра);
- ответственный медперсонал, который большую часть времени следит за самочувствием пациентов и оказывает им необходимую поддержку.
Важно! В нашем Центре любой лечебный процесс осуществляется с применением исключительно сертифицированных медпрепаратов. Каждое лекарственно средство закупается у надёжных поставщиков с обязательным предоставлением сертификата качества. Речь идёт только о проверенных препаратах, прошедших клинические испытания.
На сайте можно прочитать ряд статей, посвященных каждому заболеванию в рамках нашего профиля. Из этих материалов вы узнаете о способах борьбы с патологиями, опухолями и прочими заболеваниями. Пользовательские отзывы подробнее расскажут о наших технических возможностях и качественном уровне обслуживания в Центре. Оставьте и свой комментарий, можно и с конструктивной критикой, которая поможет нам улучшить сервис.
Ценовая политика предоставляемых услуг является конкурентной. Конечную стоимость обслуживания мы формируем на основании индивидуальных особенностей заболевания и личных потребностей пациента. Никогда не назначаются лишние процедуры или принудительные операции, если можно добиться положительного эффекта и без хирургического вмешательства. Будьте здоровы, а мы постараемся вам в этом помочь!
Основные направления деятельности центра эндоваскулярной хирургии а также другие популярные материалы:
Эмболизация сосудов при лечении миомы матки
Цена проведения эмболизации миомы матки в Москве
Цена эмболизация артерий простаты при аденоме
Автор: Капранов С.А
Доктор медицинских наук, профессор, дважды Лауреат Государственных Премий Правительства Российской Федерации в области науки и техники, Лауреат Премии Ленинского Комсомола, автор более 350 научных работ по медицине, 7 монографий, и 10 патентов на изобретения по медицине
Сегодня поиск лекарственных средств идёт целенаправленно и в клинической практике уже используются три варианта таргетного воздействия:
- Действие на определённые клеточные мишени, в числе которых рецепторы половых гормонов, гены и внутриклеточные ферменты.
- Повреждение обеспечивающих нормальную жизнедеятельность раковой опухоли внеклеточных структур, например, питающих опухоль сосудов.
- Выключение передачи внутриклеточных биохимических сигналов, которые позволяют раку жить и размножаться, в цепочке биохимических реакций — сигнального пути.
Таргетная терапия входит в лекарственное противоопухолевое лечение, но постепенно отделяется от понятия химиотерапии, поскольку механизм действия иной, но результат общий — уничтожение рака. Лекарства эти применяются только вместе с цитостатиками и усиливают их эффективность.
Преимущества таргетной терапии
Можно выделить следующие преимущества таргетных препаратов: [5]
Препараты для таргетной терапии
В настоящее время существует довольно много разных таргетных препаратов. Одни уже давно внедрены в клиническую практику, другие недавно закончили или все еще проходят испытания. В зависимости от эффектов, их можно разделить, на несколько групп: [4,5]
- В каждой клетке человека работают так называемые сигнальные пути — каскады химических реакций, итогом которых является то или иное событие. Таргетные препараты могут блокировать звенья в сигнальных путях, отвечающих за размножение клеток.
- Некоторые препараты изменяют важные белки таким образом, что клетка погибает.
- Злокачественная опухоль активно растет и распространяется по организму, поэтому ей нужно много кислорода и питательных веществ. Раковые клетки выделяют вещества, которые стимулируют ангиогенез — рост новых сосудов. Существуют антиангиогенные таргетные препараты, которые могут их заблокировать.
- Воздействуя на некоторые молекулы, можно активировать иммунитет, заставить его распознавать и убивать раковые клетки.
- Есть таргетные препараты, которые вводят в раковые клетки токсины (при этом не затрагивая здоровые клетки), уничтожающие их.
При каких онкозаболеваниях применяют таргетную терапию?

Таргетная терапия в лечении рака молочной железы
Гормональные препараты, созданные для лечения рака молочной железы, весьма похожи на настоящие гормоны, но несут в себе не программу жизни рака, а программу его смерти, и гормональный рецептор активно выбирает не родной гормон, а лекарство. Сегодня наряду с тамоксифеном используются антиэстрогены торемифен (фарестон) и фульвестрант (фазлодекс).
Вторую группу таргетных гормональных средств составляют ингибиторы фермента ароматазы, превращающего один вид полового гормона в другой. Ароматаза находится в жировой клетчатке и синтезируется яичниками, выключение её с помощью лекарственного препарата нарушает синтез гормона, в котором нуждаются раковые клетки. [1]
Лечение герцептином
Чувствительность к химиотерапии можно предсказать по наличию специфического гена HER2-neu — гена множественной лекарственной резистентности. Обнаружение этого гена говорит о том, что опухоль может не реагировать на присутствие лекарства-убийцы.
Раковая клетка пытается избежать гибели несколькими способами, одновременно включая механизмы:
- быстрого выведения химиопрепаратов в межклеточное пространство;
- обезвреживая цитостатик специальными белками;
- быстро восстанавливая повреждения;
- изменяя мишень для препарата, предлагая ему похожий белок, не имеющий принципиального значения для дальнейшей жизнедеятельности;
- изменяя роль ключевых генов, контролирующих клеточный апоптоз (гибель), которые больше не могут запустить фатальные изменения.
Найден ключевой ген рака молочной железы, получивший название HER 2, и заставляющий рецепторы на клеточной поверхности избыточно активно захватывать факторы клеточного роста, что приводит к неуправляемому делению. В некоторых случаях ген амплифицируется, то есть образует в ДНК не одну, а целый пучок генетических копий.
Помогает работе герцептина ещё один таргетный препарат перьета (пертузумаб) — белок, синтезируемый иммунными клетками, или моноклональное антитело. Перьета на поверхности раковой клетки соединяется с определённым рецептором, не позволяя фактору роста проникнуть внутрь и активировать ген HER2. Перьета вводится вместе с герцептином и химиопрепаратом доцетакселом.
Аналогично герцептину работает лапатиниб (тайверб), применяемый во второй очереди после герцептина с перьетой. [2,7]

Таргетная терапия при метастатическом раке легкого
Таргетные препараты при немелкоклеточном раке легкого могут применяться в сочетании с химиопрепаратами или самостоятельно. Применяются препараты, которые блокируют ангиогенез (рамицирумаб, бевацизумаб), мутантные белки, заставляющие раковые клетки размножаться: EGFR (афатиниб, эрлотиниб, гефитиниб), ALK (бригатиниб, алектиниб, церитиниб, кризотиниб), BRAF (траметиниб, дабрафениб). [7]
Таргетная терапия при меланоме
Исследования показывают, что примерно в половине всех меланом клетки имеют мутацию в гене BRAF. Из-за этого в них образуется одноименный мутантный белок, и они быстро размножаются. В таких случаях эффективны таргетные препараты из группы ингибиторов BRAF: дабрафениб, вемурафениб.
В тандеме с геном BRAF работает ген MEK. Если в нем обнаружена мутация, врач может назначить ингибиторы MEK: кобиметиниб и траметиниб.
Некоторые меланомы (на участках кожи, на которые постоянно воздействуют солнечные лучи, на ладонях и подошвах, слизистых оболочках, под ногтями) имеют мутацию в гене C-KIT. При этом могут помочь препараты иматиниб и нилотиниб. [2,7]

Таргетная терапия при раке поджелудочной железы
На поздних стадиях рака поджелудочной железы некоторым пациентам назначают химиотерапию в сочетании с эрлотинибом, таргетным препаратом, который блокирует рецептор эпидермального фактора роста (EGFR). [7]
Таргетная терапия при колоректальном раке
При раке толстой и прямой кишки применяются три группы таргетных препаратов: [5,7]
- Ингибиторы фактор роста эндотелия сосудов (VEGF), белка, который вырабатывается раковыми клетками и стимулирует ангиогенез: рамуцирумаб, бевацизумаб.
- Ингибиторы рецепторов эпидермального фактора роста, которые находятся на поверхности раковых клеток и, находясь в активном состоянии, заставляют их размножаться: панитумумаб, цетуксимаб.
- Ингибиторы киназы — белка-фермента, который выполняет разные функции, в том числе стимулирует клеточный рост: регорафениб.
Таргетная терапия при раке желудка
Примерно в 1 из 5 случаев в клетках злокачественных опухолей желудка содержится повышенное количество белка HER2-neu (или только HER2), который стимулирует их размножение. В таких случаях применяют таргетный препарат трастузумаб (Герцептин). Также при раке желудка применяют ингибитор ангиогенеза рамуцирумаб (Цирамза). [7]
Таргетная терапия при раке почки
При раке почек применяют: [2,7]
- Таргетные препараты, которые блокируют ангиогенез: бевацизумаб.
- Таргетные препараты, которые блокируют белки-тирозинкиназы: сорафениб, сунитиниб, пазопаниб, акситиниб, кабозантиниб, ленватиниб.
- Таргетные препараты, которые блокируют белок mTOR: темсиролимус, эверолимус.
Отзыв пациента о таргетной терапии
-
— 6 900 руб.
- Проведение внутрипузырной химиотерапии (без стоимости лекарственных препаратов) — 26 400 руб.
- Проведение внутрибрюшинной химиотерапии (без стоимости лекарственных препаратов) — 24 100 руб.
- Проведение иммунотерапии (без стоимости лекарственных препаратов) — 19 000 руб.
- Проведение интратекальной химиотерапии — 26 600 руб.
- Проведение гипертермической интраперитонеальной химиотерапии — 352 000 руб.
- Проведение химиотерапии с использованием инфузионной помпы 1 сутки (без стоимости лекарственных препаратов) — 22 600 руб.
- Проведение анти PD-1 терапии — 423 500 руб.

Таргетная терапия – это специальные лекарства, которые уничтожают определенные типы раковых клеток. Они воздействуют исключительно на вещества, благодаря которым некоторые виды онкологии растут и распространяются по организму.
Чем таргетная терапия отличается от химиотерапии?
Подобные вещества, так же как и другие используемые для лечения рака лекарства, технически считаются химиотерапией, но принцип их действия отличается:
Как работает таргетная терапия?
Таргетные препараты предназначены для воздействия на определенные вещества в раковых клетках: избыток некоторых белков, а также соединения или изменения генов, которые отсутствуют в нормальных тканях.
Такие лекарства умеют:
- блокировать или отключать сигналы, которые стимулируют рост и деление клеток;
- останавливать рост новых кровеносных сосудов, необходимых новообразованию для питания;
- изменять содержащиеся в опухолевых клетках белки, благодаря чему они перестают размножаться и погибают;
- активировать собственную иммунную систему человека – направлять ее на борьбу с раком;
- переносить в онкологические клетки токсины – убивающие их ядовитые вещества, не опасные для здоровых тканей.
Виды таргетной терапии
Существует несколько типов препаратов, каждый из которых выполняет определенную задачу.
Ингибиторы ангиогенеза: блокируют образование новых кровеносных сосудов, которые необходимы новообразованию для питания и быстрого роста – например, бевацизумаб, применяющийся при нескольких видах рака.
Моноклональные антитела: доставляют в опухолевую клетку молекулы, которые ее убивают. Одни их виды называют таргетной терапией, поскольку у них есть конкретная цель в онкологической клетке, которую они стремятся найти и атаковать. Другие действуют как иммунотерапия, стимулирующая иммунную систему и помогающая ей обнаруживать онкологию и бороться с ней. К таким лекарствам относят трастузумаб, работающий при некоторых типах новообразований молочной железы, и цетуксимаб, назначающийся пациентам с опухолями прямой кишки, легких, головы и шеи.
Ингибиторы протеасом: нарушают нормальную работу клеток, что приводит к их гибели. Их примером является бортезомиб, применяющийся при множественной миеломе – заболевании кроветворной системы.
Ингибиторы сигнальной трансдукции: блокируют активность молекул, передающих сигналы между клетками. Так работает препарат иматиниб, применяющийся при некоторых типах хронической лейкемии – поражении костного мозга, приводящем к образованию измененных клеток крови.
Как принимают таргетную терапию?
На сегодняшний день существует несколько форм, в которых выпускаются подобные препараты. Их можно принимать внутрь, как обычные таблетки, капсулы или сиропы, либо внутривенно.
Лекарства доставляют в организм через обычный катетер – тонкую мягкую пластиковую трубку в кровеносном сосуде, или центральный венозный, так называемый порт – устанавливаемое под кожу устройство. Они вводятся специалистом за несколько минут или часов.
Оральная таргетная терапия обычно принимается по четкому графику дома. Каждый пациент получает четкие инструкции о том, сколько, когда и как это нужно делать. Дозы средства рассчитываются таким образом, чтобы в организме постоянно присутствовало необходимое количество данных веществ, уничтожающих раковые клетки.
Любой малейший сбой или отклонение от схемы может повлиять на эффективность лечения.
О каждом пропуске или задержке в приеме препарата нужно сообщить врачу, который решит, как действовать в данной ситуации.
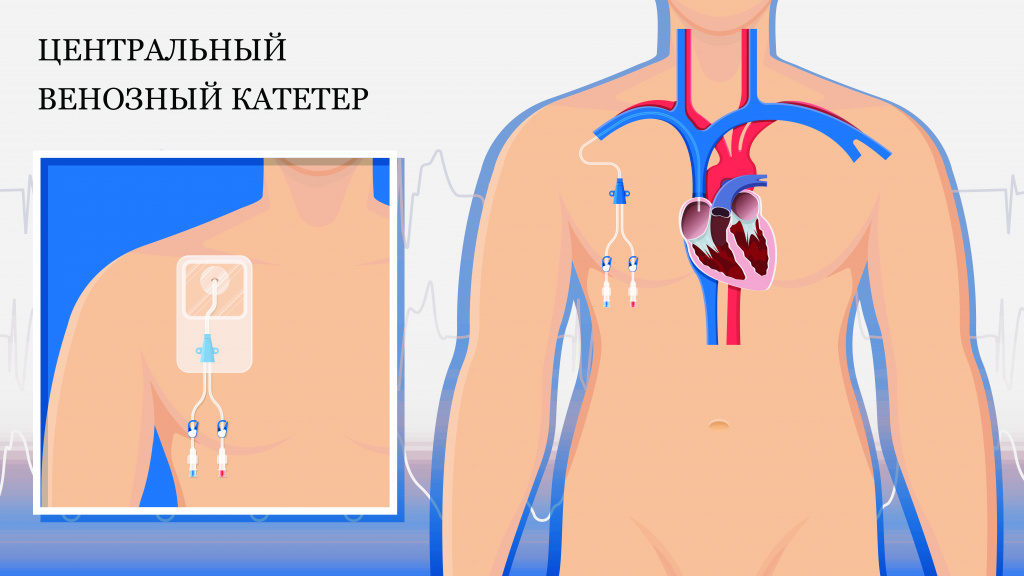
Порты для таргетной и химиотерапии
Центральный венозный катетер, или порт – удобное решение для онкобольных, которым нужно регулярно получать внутривенное лечение и сдавать кровь. С течением времени состояние их сосудов ухудшается из-за постоянных проколов, а попытки введения препаратов превращаются в пытку как для пациентов, так и для медицинского персонала.
Практически незаметное устройство, обычно устанавливаемое под кожу чуть ниже ключицы, эту проблему решает – его обладатели не испытывают проблем со сдачей анализов и доставкой в организм препаратов.
Преимуществ у портов много: они позволяют сократить количество уколов, избежать дискомфорта при проведении химио- или таргетной терапии, и уменьшить риски попадания препаратов на кожу, а значит и ее раздражения.
К их минусам можно отнести вероятность засорения катетера, появление в нем сгустков крови, его перекручивание либо смещение. Избежать неприятных последствий не сложно – достаточно строго следовать инструкциям по очистке, тщательно мыть руки, стараться избегать по нему ударов и не заниматься контактными видами спорта.
Побочные эффекты таргетной терапии
Проблемы с кожей
Самая распространенная из них – сыпь, обычно возникающая голове, лице, шее, груди и верхней части спины.
Чаще всего она начинается с покраснения и припухлостей на первых же неделях лечения, а примерно через месяц кожа покрывается корками, становится пересушенной и красной. У некоторых людей появляются круглые, плоские или выпуклые пятна или гнойные прыщи.
Сыпь вызывает зуд и жжение и нередко приводит к заметному изменению внешности, но обычно полностью проходит примерно через месяц после отмены таргетных препаратов.
Сухость, приводящая к ломкости, зуду, шелушению и даже трещинам – еще одна распространенная проблема, которая возникает практически у всех пациентов, получающих лечение на протяжении полугода.
Некоторые вещества могут вызвать покраснение и болезненность кутикулы, а также появление вокруг ногтей на руках и ногах отечных красных язв, которые нередко инфицируются.
Ладонно-подошвенный синдром – поражение кожи на ладонях и подошвах стоп, связан со многими препаратами для лечения рака, включая химио- и некоторые виды таргетной терапии. Его причина до сих пор точно не известна – возможно, все дело в повреждении крошечных кровеносных сосудов в конечностях или окружающих их тканей. Обычно он развивается в течение первых 2-6 недель лечения, а его первыми симптомами становятся повышенная чувствительность, покалывание или онемение. Затем пострадавшие области опухают, краснеют, как при солнечном ожоге, шелушатся, трескаются и покрываются волдырями.
Применение некоторых средств может привести к ухудшению качества волос – их сухости, ломкости, истончению и появлению залысин.
У части пациентов кожа или волосы темнеют или приобретают желтоватый оттенок.
Кроме того, возможно пересыхание, покраснение и ощущение жжения в области век и глаз.
При появлении сыпи или любых других проблем с кожей необходимо сразу же сообщить об этом врачу-онкологу, поскольку при отсутствии правильного лечения у пациента могут развиться инфекции, требующие отсрочки или даже прекращения терапии.
- Часть препаратов, особенно те, что относятся к ингибиторам ангиогенеза, могут повышать кровяное давление. Некоторым пациентам приходится принимать специальные лекарства, снижающие его уровень до безопасного.
- Некоторые вещества препятствуют росту новых кровеносных сосудов, что может привести к появлению синяков и кровотечений, а также медленному заживлению ран.
- Повреждения сердца: возникают при сочетании таргетных средств с химиотерапией.
- Аутоиммунные реакции – атака организма на собственные здоровые ткани: легких, кишечника, печени, кожи, глаз, нервов, желез или другие органы происходит из-за ослабления иммунной системы.
- Отеки лица, особенно в областях вокруг глаз: обычно проходят сами, а в тяжелых случаях снимаются обычными мочегонными.
Таргетная терапия различных видов рака
Данные препараты подходят не для всех пациентов – они помогают только в том случае, если в раковых клетках человека присутствуют определенные изменения. Перед назначением лечения врачи проводят биопсию – изымают небольшую частичку новообразования и передают ее в лабораторию, где она тщательно исследуется. Если специалистам удается найти особенности опухоли, для которых уже созданы лекарства, их применяют – часто одновременно с химиотерапией или другими видами вмешательства.
Таргетная терапия рака гортани
Для лечения некоторых запущенных форм онкологии горла и гортани используется Цетуксимаб (Эрбитукс), блокирующий EGFR – белок, который помогает опухолевым клеткам быстро расти. Его можно комбинировать с лучевой или химиотерапией.
Таргетная терапия рака желчных протоков
На сегодняшний день при данном типе онкологии используется 2 типа препаратов:
- Пемигатиниб и Инфигратиниб (Труселтик): блокируют белок FGFR2 в раковых клетках желчных протоков и препятствуют их росту и распространению в другие ткани.
- Ивосидениб (Тибсово): работает против измененного гена IDH1, который воздействует на одноименный белок, необходимый для нормального созревания клеток.
Таргетная терапия немелкоклеточного рака легкого
Для пациентов с немелкоклеточной онкологией легких создано множество таргетных препаратов:
Таргетная терапия рака молочной железы
Примерно у 1 из 5 женщин с раком груди опухолевые клетки содержат на своей поверхности слишком много стимулирующего их рост белка – HER2. Эти HER2-положительные новообразования быстро развиваются и распространяются по организму. Для их лечения применяются:
- моноклональные антитела Трастузумаб (Герцептин), Пертузумаб (Перьета) и Маргетуксимб (Маргенза);
- моноклональные антитела, связанные с химиотерапевтическим препаратом, доставляющие его непосредственно к белку HER2 на онкологической клетке: Адо-трастузумаб эмтанзин (Кадсила) и Фам-трастузумаб дерукстекан (Энхерту);
- Лапатиниб, Нератиниб (Нерлинкс) и Тукатиниб (Тукиса), блокирующие передачу сигнала о быстром росте от HER2.
Примерно 2 из 3 случаев рака молочной железы чувствительны к гормонам – веществам, которые создаются нашими железами, через кровоток попадают в органы и сообщают им, как действовать – работать или отдыхать, выделять что-то или поглощать. В таких ситуациях применяется гормональная терапия:
Олапариб (Линпарза) и Талазопариб (Талценна): блокируют белки PARP, необходимые для восстановления поврежденной ДНК, что часто приводит к гибели раковых клеток.
Сацитузумаб говитекан: моноклональное антитело, присоединенное к химиотерапевтическому препарату. Лекарство работает в случае избытка в опухоли белка Trop-2, помогающего ей быстро расти и распространяться по организму.
Таргетная терапия рака печени
Для пациентов с раком печени есть несколько типов таргетных препаратов:
- Так называемые ингибиторы, или блокаторы киназ – белков, расположенных на поверхности клетки или рядом с ней, которые передают важные управляющие ею сигналы: например, к ускорению роста или созданию новых кровеносных сосудов. К ним относят Сорафениб (Нексавар), Ленватиниб (Ленвима), Регорафениб (Стиварга) и Кабозантиниб (Кабометикс).
- Моноклональные антитела – искусственные версии белков иммунной системы, предназначенные для прикрепления к определенной цели. Ими являются Бевацизумаб (Авастин) и Рамуцирумаб (Цирамза), предотвращающие развитие сосудов, необходимых для питания быстро растущей опухоли.
Таргетная терапия рака пищевода
При лечении рака пищевода используется несколько типов таргетных препаратов.
Некоторые типы опухолей содержат слишком много белка HER2, который способствует быстрому росту онкологических клеток. Такие заболевания называются HER2-положительными. Против них можно применять:
Таргетная терапия рака поджелудочной железы
Для лечения онкологии поджелудочной железы используются:
- Эрлотиниб: препарат, нацеленный на белок EGFR, который помогает раковым клеткам расти.
- Олапариб (Линпарза): затрудняет восстановление поврежденной ДНК опухолевых клеток, в которых содержится измененный ген BRCA.
- Ларотректиниб (Витракви) и Энтректиниб: применяются при запущенных новообразованиях с измененным геном NTRK, которым не помогают другие методы терапии.
Таргетная терапия рака почки
Врачи применяют 2 типа таргетных препаратов для лечения рака почки. Их назначают пациентам с запущенным заболеванием для снижения скорости разрастания опухоли или уменьшения ее размеров.
- Сунитиниб (Сутент), Сорафениб (Нексавар), Кабозантиниб (Кабометикс), Ленватиниб (Ленвима), Бевацизумаб (Авастин), Акситиниб (Инлита), Тивозаниб (Фотивда), Белзутифан (Велирег) и Пазопаниб (Вотриент): предотвращают образование новых кровеносных сосудов, необходимых для питания увеличивающегося новообразования, и блокируют вещества, необходимые для роста и выживания онкологических клеток.
- Темсиролимус (Торисел) и Эверолимус (Афинитор) – работают против белка mTOR, который помогает клеткам развиваться и делиться.
Таргетная терапия рака предстательной железы
При лечении онкологии простаты используются Рукабариб (Рубрака) и Олапариб (Линпарза) – так называемые ингибиторы PARP. Данные лекарства не позволяют восстанавливаться поврежденной ДНК в клетках новообразований, что приводит к их гибели.
Таргетная терапия саркомы матки
Пазопаниб (Вотриент): назначается при лейомиосаркоме – опасной для жизни опухоли гладкой мускулатуры матки, которая распространилась по организму или вернулась после проведенного лечения.
Таргетная терапия рака щитовидной железы
В случае папиллярного или фолликулярного рака щитовидной железы применяют 3 типа препаратов:
- Ленватиниб (Ленвима) и Сорафениб (Нексавар): не позволяют образовываться новым кровеносным сосудам, без которых опухоль не может быстро увеличиваться, и блокируют необходимые для ускоренного развития онкологических клеток белки.
- Сельперкатиниб (Ретевмо) – атакует белок RET, который помогает клеткам расти.
- Ларотректиниб (Витракви) и Энтректиниб (Розлитрек): работают против измененного гена NTRK, благодаря которому новообразование быстро прогрессирует.
При медуллярном раке используются:
- Вандетаниб (Капрелса) и Кабозантиниб (Кометрик), которые предотвращают стремительный рост клеток и создание новых кровеносных сосудов.
- Сельперкатиниб (Ретевмо) и Пралсетиниб (Гаврето): противодействуют белку RET, стимулирующему развитие аномальных клеток.
При анапластических новообразованиях применяются:
- Дабрафениб (Тафинлар) и Траметиниб (Мекинист), нацеленные на ускоряющие увеличение новообразования белки BRAF и МЕК соответственно.
- А также Сельперкатиниб, Ларотректиниб и Энтректиниб.
Таргетная терапия рака яичников
Пациенткам с онкологией яичников могут назначаться:
- Бевацизумаб (Авастин), который блокирует белок VEGF и не позволяет образовываться новым сосудам, необходимым для роста опухоли.
- Олапариб (Линпарза), Рукапариб (Рубрака) и Нирапариб (Зеджула): не позволяют раковым клеткам восстанавливать повреждения ДНК – молекулы, в которой зашифрована вся информация об организме, что приводит к их гибели.
- Ларотректиниб (Витракви) и Энтректиниб (Розлитрек): работают против измененного гена NTRK, благодаря которому клетки новообразования растут очень быстро.
Читайте также:

