Острый лимфобластный лейкоз доклад
Обновлено: 30.06.2024
Острый лимфобластный лейкоз – это злокачественная патология костного мозга и крови, которая заключается в продуцировании кроветворным органом бластных (незрелых) лейкоцитов. Эти клетки неспособны выполнять свою функцию и постепенно вытесняют нормальные клетки, что приводит к катастрофическому падению иммунитета, анемии, инфекционным воспалительным процессам, кровотечениям и другим нарушениям нормальной жизнедеятельности организма. Заболевание развивается очень быстро и при отсутствии квалифицированной медицинской помощи в течение нескольких месяцев приводит к летальному исходу.
Общепринятая классификация острых лимфобластных лейкозов (ОЛЛ) подразделяет их на две группы, в зависимости от типа пораженных лейкоцитов.
- В-клеточный (до 85% всех случаев) наиболее характерен для детского возраста, причем пик заболеваемости приходится на 3-й год жизни. Взрослые заболевают крайне редко. Вторая группа риска – это люди старше 60 лет, но среди пожилых людей заболеваемость в 5-6 раз ниже, чем у детей
- Т-клеточный (15-20% случаев) характеризуется более тяжелым течением и высокой агрессивностью. Наибольшее количество заболевших приходится на 15-летний возраст.
Симптомы
Первые проявления острого лимфоидного лейкоза неспецифичны и характерны для многих заболеваний:
- бледность кожных покровов из-за развивающейся анемии;
- вялость, упадок сил, сонливость;
- частые инфекционные заболевания из-за снижения иммунитета;
- повышенная температура тела.
С развитием болезни, увеличением в крови количества бластных лимфоцитов и недостатком здоровых клеток появляются более выраженные симптомы:
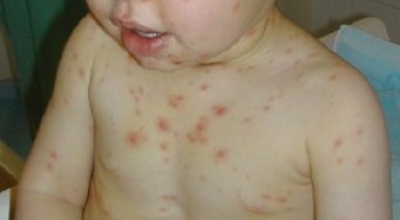
- кровоточивость слизистых оболочек;
- синяки, точечные кожные кровоизлияния;
- длительное заживление даже небольших царапин и ранок, сопровождающееся инфицированием, воспалениями, нагноениями;
- боли в конечностях, вызванные ростом опухоли костного мозга;
- увеличение размеров печени, селезенки, лимфоузлов, приводящие к болям в животе;
- затрудненное дыхание, одышка;
- паралич лицевого нерва, ухудшение зрения, рвота из-за поражения мозговых оболочек.
В каждом отдельном случае формируется индивидуальный симптомокомплекс, в который перечисленные признаки могут входить частично или полностью.
Причины и факторы риска
- радиоактивное излучение любой природы, в том числе во время лечения других форм рака;
- некоторые химические соединения – бензол, определенные препараты химиотерапии;
- вирусные инфекции (Эпштейна-Барр, HTLV);
- унаследованная предрасположенность.
Острый лимфоцитарный лейкоз часто развивается у детей, реже – у людей старше 60 лет, совсем редко – у взрослых. Представители белой расы заболевают чаще темнокожих, мужчины – несколько чаще женщин.
Стадии
Поскольку при онкозаболеваниях крови опухоль, как таковая, не развивается, то общие критерии стадийности для оценки их течения не подходят. Начальной стадией острого лимфобластного лейкоза считают период от появления злокачественного клона до появления выраженных симптомов. Далее выделяют следующие этапы.
- Первая атака, или дебют. В это время заболевание стремительно развивается, пациент обращается к врачу, его помещают в гематологический стационар и проводят индукционную терапию.
- Ремиссия. Она может быть полной, со снижением уровня бластных лейкоцитов менее 5% и наличием в миелограмме всех здоровых ростков кроветворения, и частичной, при которой улучшение показателей крови является временным и через определенный период прекращается.
- Рецидив. Состояние наступает после ремиссии и характеризуется возвратом признаков заболевания с повышением уровня бластоза выше 5%. Выделяют ранний (с ремиссией менее года) и поздний (с ремиссией дольше года) рецидив острого лимфобластного лейкоза.
Иногда после нескольких ремиссий и рецидивов у пациента наступает терминальная стадия, при которой проводимая терапия не дает никаких результатов. После этого неизбежно наступает летальный исход. У большинства больных результаты лечения оказываются более благоприятными, и после ремиссии, как правило, происходит выздоровление.
Диагностика
Чтобы диагностировать острый лимфоцитарный лейкоз, необходим ряд лабораторных анализов и инструментальных исследований.
Общий анализ крови обязательно проводят с подсчетом лейкоцитарной формулы, чтобы выявить первичные признаки болезни.
Биохимический анализ крови проводят для уточнения состояния внутренних органов, в частности – печени и почек.
Биопсия костного мозга из подвздошной кости предоставляет материал для основных исследований.
Рентген грудной клетки необходим для выявления увеличенных лимфоузлов, а также для определения воспалительного процесса в легких.
В процессе лечения может появиться необходимость в дальнейших диагностических и мониторинговых исследованиях.
Лечение
Стратегию лечения острого лимфобластного лейкоза разрабатывает и утверждает консилиум, в который входят медики нескольких специализаций: онколог общего профиля, химиотерапевт, радиолог, гематолог, другие специалисты. Как правило, пациенту назначают комплекс мероприятий, включающий наиболее эффективные методики.
Химиотерапия является ключевым методом при онкозаболеваниях крови и костного мозга. Современные препараты эффективно уничтожают злокачественные клетки либо угнетают их рост и деление. В зависимости от показаний, каждому пациенту разрабатывают индивидуальный курс с несколькими разными химиопрепаратами. Если они не оказывают желаемого эффекта, назначения корректируют с учетом новых данных.
Лучевая терапия используется в качестве вспомогательного метода при лечении некоторых подвидов заболевания. Наиболее часто она предшествует хирургической операции по пересадке костного мозга, когда требуется тотальное уничтожение опухолевых клеток.
Лечение состоит из нескольких этапов:
- подготовительного, необходимого для снижения количества лейкозных клеток в крови;
- индукции ремиссии – интенсивного курса, целью которого является максимально возможное уничтожение опухоли;
- консолидации, направленной на закрепление результата и уничтожение остаточных очагов;
- реиндукции, или повторении индукции, чтобы полностью исключить вероятность рецидива;
- поддерживающей терапии, которая при успешном лечении продолжается около двух лет и состоит из небольших доз цитостатиков.
Между этапами делаются перерывы, необходимые для восстановления организма после воздействия тяжелых препаратов.
Прогнозы
При остром лимфобластном лейкозе прогноз зависит, в первую очередь, от возраста пациента. У детей выздоровление наступает в 80-90% случаев. Для взрослых этот показатель в настоящее время составляет 40-45%, причем у более молодых пациентов шансы существенно выше, чем у людей старше 60 лет. Не следует забывать, что за последние годы онкологи добились существенных успехов в лечении заболеваний крови. Ежегодно появляются новые, все более эффективные и безопасные химиопрепараты направленного действия.
Профилактика
Специальных мер для предупреждения острого лимфоидного лейкоза не существует. Чтобы снизить риски заболевания, необходимо придерживаться здорового образа жизни, укреплять естественный иммунитет, избегать радиационных и канцерогенных воздействий.
Реабилитация
В течение реабилитационного периода пациент нуждается в полном восстановлении функций организма, для чего необходимо:
- поддерживать и укреплять иммунную систему;
- восстанавливать кишечную микрофлору;
- выводить из организма токсины, образовавшиеся после распада патогенных клеток;
- укреплять нервную систему, бороться со стрессами и депрессивными состояниями.
Диагностика и лечение острого лимфобластного лейкоза в Москве
- лечение у онкологов, химиотерапевтов, гематологов высокой квалификации;
- диагностику с использованием новейшего медицинского оборудования;
- пребывание в комфортабельной палате стационара под круглосуточным наблюдением;
- медицинский сервис в соответствии с жесткими стандартами мировой медицины.
Позвоните нам, чтобы выяснить интересующие вас подробности и записаться на консультацию.
Вопросы и ответы
Сколько живут при остром лимфобластном лейкозе?
Заболевание отличается стремительным течением, поэтому без медицинской помощи летальный исход наступает в течение нескольких месяцев. При своевременно начатом лечении шансы прожить более 7 лет имеются у 80-90% детей и около 40% взрослых.
Сколько времени продолжается лечение острого лимфобластного лейкоза?
- Подготовительный этап лечения продолжается 1-2 недели.
- Индукция – до 8 недель.
- Консолидация – до 4 месяцев.
- Реиндукция – несколько месяцев.
- Поддерживающая терапия – до полутора лет.
Общая продолжительность лечения составляет примерно два или два с половиной года.
Как понять, что у тебя острый лимфобластный лейкоз?
Если у вас появились:
- симптомы общего недомогания – вялость, слабость, повышенная температура;
- кровотечения из носа, десен, других слизистых оболочек;
- плохо заживающие ранки на коже;
- сильная потливость по ночам –
необходимо как можно скорее обратиться к онкологу или гематологу и сделать анализы. Перечисленные симптомы далеко не всегда свидетельствуют о начале острого лимфобластного лейкоза, однако это заболевание развивается стремительно и агрессивно. Для успеха лечения дорог буквально каждый день.

Острый лимфобластный лейкоз является самой распостраненной формой и составляет 80% от всех лейкозов у детей. А если говорить о всей детской онкологии, то количество острых лимфобластных лейкозов – составляет практически одну третью часть среди всех форм онкологических заболеваний у детей и подростков.
По статистике в Германии в Детском Раковом Регистре ежегодно регистрируется около 500 детей и подростков в возрасте от 0 до 14 лет с диагнозом острый лимфобластный лейкоз. А общее количество заболевших в возрасте до полных 18 лет ежегодно составляет примерно от 550 до 600 человек.
Согласно мировой статистике, 3,3-4,7 детей из 100 тысяч заболевают лейкемией в возрасте до 15 лет. Около 40-46 % случаев приходится на детей 2-6 лет.
Именно поэтому не смотря на недостаток знаний о данном заболевании крайне важно его изучение.
Материалы и методы:
Для исследования была отобрана группа из 40 пациентов с диагнозом острый лимфобластный лейкоз.
Определение заболевания:
Острый лимфобластный лейкоз относится к группе клинически гетерогенных клональных злокачественных новообразований из лимфоидных клеток-предшественников, имеющих определённые генетические и иммунофенотипические характеристики. До 80% всех лейкемий у детей имеют лимфоидное происхождение, из них большая часть - 80% приходится на опухоли из предшественников В-лимфоцитов, 1% - состоят из зрелых В-клеток, около 15% происходят из Т-лимфоцитов и менее 5% имеют неопределённое клеточное происхождение.
Не установлено ни одной безусловно вызывающей лейкоз причины. Существует 3 теории происхождения заболевания: инфекционная, опухолевая и теория системно-пролиферативной природы лейкозов.
Сторонники инфекционной теории разделяются на 3 группы: одни считают, что возбудителем лейкоза могут быть различные микробы, вызывающие однотипную реакцию со стороны крови; другие стоят на точке зрения туберкулезной этиологии лейкоза; наконец, третьи придерживаются вирусной теории лейкоза.
Наиболее обоснованной является опухолевая теория, которая поддерживается большинством современных авторов. Доказательства сторонников этой теории основываются на общих закономерностях развития злокачественных опухолей и лейкозов, нередко их сочетаний, аналогичных нарушениях обменных процессов, клеточной анаплазии, однотипности наследственных влияний и гормональных нарушений — все это свидетельствует о патогенетической общности лейкозов и злокачественных новообразований.
Третья теория происхождения лейкоза — системно-пролиферативная — несколько сходна с опухолевой теорией и рассматривает патологический процесс как следствие нарушения патогенетических механизмов, регулирующих пролиферацию и созревание элементов крови. Причиной этих нарушений считают различные экзогенные и эндогенные факторы. К первой группе относят патогенное влияние вирусов (специфический вирус пролиферации), канцерогенные вещества и ионизирующую радиацию. Ко второй группе можно отнести влияние эндокринных нарушений в организме.
Основным звеном в развитии острого лимфобластного лейкоза является то, что различные неблагоприятные факторы приводят к мутациям в клетках кроветворения. При этом клетки реагируют неудержимым ростом, невозможностью дифференцировки и изменением скорости нормального созревания. Поэтому все клетки, которые составляют лейкемическую опухоль, являются потомком одной стволовой клетки или клетки-предшественницы любого направления кроветворения. Клеточный субстрат при этом представлен бластами.
Такие опухоли обладают способностью расти вне органов гемопоэза, они неравноценны и представляют разные этапы прогрессии. Происходит нарастание процесса в виде выхода бластных элементов в периферическую кровь, перехода от лейкопении к лейкоцитозу.
Говоря об остром лимфолейкозе, патогенез до настоящего времени до конца не выяснен. Существует только ряд теорий.
1.этап повышенной мутабельности нормальных клеток;
4.этап независимой прогрессии.
2. Стволовая клетка, подвергающаяся мутации с измененным геном - генотипом, воспроизводит себе подобные патологические клоны, на первом этапе опухолевой прогрессии опухоль моноклональная (доброкачественная).
3. Второй этап – поликлональной трансформации (злокачественный). Клоны клеток, прилежащие к стволовой клетке более дифференцированы и менее злокачественны, а клоны клеток, все дальше отстоящие от стволовой, менее дифференцированы и более злокачественны. С каждым последующим клоном растет нестабильность генетического аппарата клеток (клеточный полиморфизм, нарушается созревание, возникают атипичные элементы).
4. Пролиферация патологических клеток, идет в режиме геометрической прогрессии, подчиняясь закону митотического деления клеток. Мутантный клон автономен от каких-либо регулирующих воздействий организма и достаточно быстро вытесняет нормальные гемопоэтические клетки, замещая собой весь гемопоэз с последующим развитием синдромов: анемический, геморрагический и вторичного иммунодефицита.
Статистические данные:
Процентное соотношение возраста пациентов.
Вывод: из 40 детей в отделении онкогематологии, наиболее подвержены заболеванию дети от 1 года до 7 лет.
Процентное соотношение мальчиков и девочек.
Вывод: из 40 исследуемых, мальчики - 25 человек болеют острым лимфобластным лейкозом чаще, чем девочки - 15 человек.
Соотношение сельских и городских детей.
Вывод: 29 человек - городские жители, жители села составляют- 11 человек, так как в городах неблагоприятная экологическая обстановка.
Клинический случай:
Пациентка Х, 3,5 лет. Диагноз: острый лимфобластный лейкоз.
Пациентка часто болела ОРЗ и ОРВИ в период с 1 года до 2х лет. За 2 месяца до постановки диагноза родители отмечали обострение ситуации, часто беспокоила высокая температура (38.6), кашель, насморк. Лечение проходила в стационаре Ординской ЦРБ, назначались курсы антибактериальной и противовирусной терапии с периодичностью раз в 2 недели. К началу мая появились быстрая утомляемость, вялость, бледность кожи, по анализам крови была диагностирована анемия и пациентку направили на консультацию к гематологу. К 22.05.19 состояние стало ухудшаться, появилась геморрагическая сыпь на ногах и теле, печень и селезенка увеличены, с 23.05.19 больная госпитализирована в Ординскую ЦРБ, затем переведена в ОРИТ Кунгурской больницы. ОАК от 23.05.19 Hb- 52 г/л; Эр- 2,0; Тр-19; Л-0,5; лимфоциты- 92. После чего пациентка переведена в онкологическое отделение ПКДКБ с 24.05.19.
Для подтверждения диагноза оценивались показатели ОАК, миелограммы, проводились иммунофенотипирование клеток костного мозга, определение транслокаций методом ПЦР, кариологическое исследование, исследование ликвора.
ОАК: на момент поступления в ПКДКБ от 23.05.19 Hb- 52 г/л; Эр- 2,0; Тр-19; Л-0,5; ; Эо - ; Баз -; м/ц -; ю -; п/я-1; с/я-67; мон-1; лимфоциты- 31. В процессе терапии показатели ОАК изменялись в широких пределах.
На 36-й день: от 03.07.19 Hb- 100 г/л; Эр- 3,28; Ht-28,8; MCV-88,0; Тр-279;Л-7,08; Эо - ; Баз-1; м/ц-2; ю-3; п/я-6; с/я-35; мон-5;лимфоциты-48; СОЭ-20.
ОАК от 11.11.19 Hb- 105 г/л; Эр- 3,14; Ht-28,5; MCV-90,7; Тр-104; Л-3,51; Эо - ; Баз-0,02; мон-0,06;лимфоциты-79,9; СОЭ-12.
Миелограмма от 13.05.19 Пунктат малоклеточный. Все ростки костного мозга угнетены. Гипопластическое состояние костного мозга.
Миелограмма: от 27.05.19 Костный мозг малоклеточный. Бластные клетки выше нормы. Заключение: бластная гиперплазия костного мозга.
Миелограмма от 02.10.19 Костный мозг многоклеточный. Бласты в пределах нормы. Гранулоцитарный росток незначительно сужен, эритроцитарный- расширен.
Кариологическое исследование от 30.05.19 (результат от 11.06.19). Обнаружен гиперплоидный клон с модальным числом хромосом- 52, что характерно для ОЛЛ из клеток-предшественников В-лимфоцитов.
Также была выявлена отягощенная наследственность ребенка в сфере онкологических заболеваний.
Числовые изменения кариотипа имеют большое значение для прогнозирования острого лимфобластного лейкоза. Вариант острого лимфобластного лейкоза со значительным увеличением числа хромосом (более 50) имеет относительно благоприятный прогноз: 80—90 % больных переживает пятилетний срок с момента постановки диагноза, однако выявление некоторых структурных перестроек в клетках лейкозного клона с такими числовыми нарушениями может ухудшить прогноз.
Проанализировав полученные результаты, можно сделать вывод, что острый лимфобластный лейкоз в онкологии у детей занимает одно из первых мест. Особенно подвержены дети в возрасте от 1 года до 7 лет. Самый маленький процент заболеваемости у детей до года.
Мальчики более подвержены данному заболеванию, чем девочки, то есть у мальчиков острый лимфобластный лейкоз встречается в 1,63 раза чаще, чем у девочек.
Большое значение в возникновении острого лимфобластного лейкоза имеют различные канцерогенные вещества. Именно это может объяснять более частое возникновение заболевания у городских жителей.
Рассмотренный ранее клинический случай доказывает волнообразность течения данного заболевания. Также прослеживается характерная длительность заболевания. В данном случае довольно ярко видна клиническая картина острого лимфобластного лейкоза, подкрепляемая типичными данными лабораторных исследований.
Учитывая высокий процент встречаемости острого лимфобластного лейкоза среди онкологических заболеваний у детей, вопрос изучения этого вида патологии остается актуальным и требует дальнейших исследований.
Список литературы:
Asnani, M., Exons of Leukemia Suppressor Genes: Creative Assembly Required / M. Asnani, A. Thomas-Tikhonenko // Trends in Cancer – 2018. – Vol. 4. – P. 796-798.
Румянцева А.Г. – Гематология/онкология детского возраста. Практическое руководство по детским болезням. – М.: - 2014. – т. 4.
Частота встречаемости и факторы риска
На долю ОЛЛ приходится 75-80% всех опухолевых заболеваний кроветворной системы у детей и примерно 25% всех детских онкозаболеваний вообще (примерно 4 случая на 100 тысяч детей в год). Именно ОЛЛ – самое распространенное онкологическое заболевание у детей. Чаще всего ОЛЛ возникает в возрасте до 14 лет; пик детской заболеваемости приходится на возраст 2-5 лет. У мальчиков эта болезнь встречается немного чаще, чем у девочек.
Вероятность возникновения ОЛЛ несколько повышена у людей, ранее получавших лечение от какой-либо другой болезни (обычно злокачественной опухоли) с использованием облучения или определенных видов цитостатической химиотерапии. Также риск ОЛЛ повышен у детей с некоторыми генетическими нарушениями – например, с синдромом Дауна, нейрофиброматозом типа I или рядом первичных иммунодефицитных состояний.
Риск заболеть для ребенка выше среднего, если у его брата- или сестры-близнеца уже был диагностирован лейкоз. Другие случаи, когда в одной и той же семье ОЛЛ возникает более чем у одного ребенка, бывают, но исключительно редки.
Впрочем, в большинстве случаев ОЛЛ не удается обнаружить никакого известного фактора риска, и причины, вызвавшие болезнь, остаются неизвестными.
Признаки и симптомы
ОЛЛ характеризуется множеством различных признаков и у разных больных может проявляться совершенно по-разному. Большинство наблюдаемых симптомов, однако, обусловлено тяжелыми нарушениями кроветворения: избыток аномальных бластных клеток при ОЛЛ сочетается с недостаточным количеством нормальных функциональных клеток крови.
Обычно наблюдаются слабость, бледность, снижение аппетита, потеря веса, учащенное сердцебиение (тахикардия) – проявления анемии и опухолевой интоксикации. Недостаток тромбоцитов проявляется мелкими кровоизлияниями на коже и слизистых оболочках, кровотечениями из десен, носовыми и кишечными кровотечениями, кровоподтеками, синяками. Из-за накопления бластных клеток часто увеличиваются лимфоузлы – в частности, шейные, подмышечные, паховые. Нередко увеличиваются также печень и селезенка - как говорят, возникает гепатоспленомегалия.
Часто наблюдаются боли в костях и суставах, иногда возникают патологические (то есть вызванные заболеванием) переломы костей. Из-за недостаточного количества нормальных зрелых лейкоцитов возможны частые инфекции. Повышение температуры может наблюдаться как в связи с возникшей на фоне лейкоза инфекцией, так и из-за опухолевой интоксикации. Иногда одним из проявлений острого лейкоза является продолжительная ангина, плохо поддающаяся терапии антибиотиками.
В некоторых случаях ОЛЛ вызывает изменения и в других органах: глазах, почках, яичках у мальчиков и яичниках у девочек, причем у мальчиков поражение половых органов наблюдается чаще. Может возникнуть поражение центральной нервной системы - нейролейкемия.
Так как все наблюдаемые симптомы могут быть связаны и с другими заболеваниями и не специфичны для ОЛЛ, перед началом лечения необходима лабораторная диагностика, которая в срочном порядке производится в больничных условиях.
Диагностика
При ОЛЛ возникают изменения в обычном клиническом анализе крови: как правило, понижены уровни эритроцитов и тромбоцитов, появляются бластные клетки. Очень высокий лейкоцитоз (гиперлейкоцитоз) возможен, но, вопреки распространенному мнению, наблюдается далеко не во всегда. В целом же надежно поставить диагноз можно только при исследовании образца костного мозга; для этой цели необходима костномозговая пункция.
В ходе диагностики ОЛЛ также необходимо исследовать состояние центральной нервной системы. Анализ спинномозговой жидкости (ликвора) позволяет определить, нет ли у больного поражения центральной нервной системы – нейролейкемии. Образец ликвора для анализа получают посредством пункции спинномозгового канала.
Возможны и дополнительные диагностические процедуры для исследования пораженных лимфоузлов и внутренних органов – компьютерная томография (КТ), ультразвуковое исследование (УЗИ) и так далее.
Диагностические исследования позволяют для каждого конкретного больного определить ту или иную группу риска, от которой зависят прогноз заболевания и планируемое лечение. Так, говорят о стандартном, промежуточном, высоком риске и т. д. Отнесение к той или иной группе в рамках конкретного протокола лечения зависит от многих факторов. Перечислим некоторые из них.
Возраст больного: менее благоприятным считается возраст до 1 года или старше 10 лет.
Количество лейкоцитов: риск увеличивается при очень высоком лейкоцитозе в момент постановки диагноза.
Распространение ОЛЛ в другие органы, помимо костного мозга (например, возникновение нейролейкемии), определяет более высокий риск.
При раннем или повторном рецидиве риск повышается.
Кроме того, выбор стратегии лечения зависит от варианта лейкоза (В- или Т-клеточный ОЛЛ), а также от цитогенетических аномалий в лейкемических клетках, связанных с числом хромосом и транслокациями. Некоторые из них достоверно влияют на течение болезни и ход терапии, другие только изучаются. Так, филадельфийская хромосома – транслокация t(9;22) – требует подключения к терапии дополнительных таргетных лекарств. Транслокация t(4;11) часто требует трансплантации костного мозга. В то же время, например, транслокация t(12;21) обычно связана с относительно хорошим прогнозом.
Лечение
Как упомянуто в предыдущем разделе, современное лечение ОЛЛ основано на разделении пациентов на группы риска – в зависимости от того, насколько вероятно у них достижение и сохранение ремиссии при одинаковой терапии. Соответственно, пациенты, относящиеся к группам более высокого риска (то есть те, у кого изначальный прогноз хуже), получают более интенсивную терапию, а в группах более низкого риска можно использовать менее интенсивную терапию и тем самым избегать излишней токсичности и тяжелых осложнений.
Терапия ОЛЛ, как правило, состоит из трех этапов:
Индукция ремиссии (то есть терапия, направленная на достижение ремиссии) проводится в течение нескольких первых недель лечения. Под ремиссией здесь подразумеваеся содержание менее 5% бластных клеток в костном мозге и отсутствие их в обычной (периферической) крови в сочетании с признаками восстановления нормального кроветворения.
В ходе индукции проводится интенсивная многокомпонентная химиотерапия лекарствами-цитостатиками, которые вызывают разрушение лейкемических клеток. На этом этапе могут применяться, в зависимости от протокола, такие лекарства, как гормоны-глюкокортикостероиды, аспарагиназа и пэгаспаргаза, винкристин, даунорубицин, другие препараты. Индукция позволяет достигнуть ремиссии более чем у 95% детей и у 75-90% взрослых с ОЛЛ. Принципиально важно посредством лабораторных анализов оценить ответ на терапию индукции: в случае плохого ответа (к контрольному сроку не удалось достичь нужных результатов) пациент переводится в группу более высокого риска.
Консолидация (закрепление) ремиссии направлена на уничтожение остаточных аномальных бластных клеток во избежание рецидива заболевания. Общая продолжительность этого этапа измеряется месяцами и сильно зависит от конкретного протокола лечения. В ходе курсов терапии на этапе консолидации могут использоваться, опять-таки в зависимости от конкретного протокола, метотрексат, аспарагиназа, 6-меркаптопурин, винкристин, глюкокортикостероиды, даунорубицин и ряд других лекарств в зависимости от протокола и терапевтической группы.
На этапах индукции и консолидации введение химиотерапевтических препаратов производится в основном внутривенно, в условиях больничного стационара или стационара одного дня.
Поддерживающая терапия проводится для поддержания ремиссии, то есть для дополнительного снижения риска рецидива после этапов индукции и консолидации. Продолжительность поддерживающей терапии – полтора-два года. На этом этапе основными препаратами являются 6-меркаптопурин и метотрексат.
Поддерживающая терапия представляет собой этап наименее интенсивного лечения. Ребенок живет дома, постоянное пребывание или ежедневные визиты в больницу не требуется.
Если требуется лечение или профилактика нейролейкемии на перечисленных этапах, химиопрепараты вводятся интратекально, то есть в спинномозговой канал посредством люмбальных пункций. Иногда лекарства вводят в желудочки (особые полости) головного мозга через специальный резервуар Оммайя, который устанавливается под кожей головы. Для интратекального введения при ОЛЛ используются метотрексат, цитарабин и гормоны-глюкокортикостероиды. У некоторых пациентов применяется и облучение головы – краниальное облучение.
К сожалению, несмотря на все перечисленные меры, иногда возникает рецидив ОЛЛ – костномозговой, экстрамедуллярный (то есть вне костного мозга – например, с поражением центральной нервной системы или яичек) или комбинированный. В этом случае проводится противорецидивная терапия. Выбор метода лечения рецидива зависит от сроков его возникновения (ранний или поздний) и от того, является ли рецидив костномозговым или экстрамедуллярным. При раннем рецидиве шансы на успех одной только лекарственной терапии значительно снижаются и практически всегда планируется трансплантация.
В ходе лечения ОЛЛ может применяться трансплантация костного мозга от родственного или неродственного донора. Если по плану лечения предусмотрена трансплантация, то ее проводят после достижения ремиссии. Как правило, трансплантация показана только при высоком риске (например, после раннего рецидива или при плохом ответе на терапию индукции), поскольку это очень тяжелое лечение, а хорошие результаты стандартной терапии при ОЛЛ в среднем вероятны, особенно у детей.
Химиотерапия ОЛЛ высокоэффективна, но зачастую тяжело переносится и может быть связана с серьезными побочными эффектами. Так, в процессе лечения подавляется кроветворение и бывают необходимы переливания компонентов донорской крови – тромбоцитов во избежание кровотечений при очень низком уровне собственных тромбоцитов больного, эритроцитов для борьбы с анемией. Переливания донорских гранулоцитов применяются только в редких случаях при тяжелых инфекционных осложнениях.
Поскольку и лейкоз сам по себе, и используемая при его лечении химиотерапия резко снижают сопротивляемость организма различным инфекциям, больным во время лечения необходимы эффективные антибактериальные и противогрибковые лекарства для профилактики и терапии инфекционных осложнений. Опасны как обычные, так и оппортунистические инфекции.
Интенсивное лечение ОЛЛ накладывает серьезные ограничения на образ жизни больного. Необходимо соблюдать определенную диету и строгие гигиенические требования. Во избежание инфекций ограничиваются контакты с внешним миром. При очень низком уровне тромбоцитов нельзя не только допускать травмы, но даже, например, чистить зубы зубной щеткой, чтобы не спровоцировать кровотечение из десен. После достижения ремиссии строгость этих ограничений постепенно снижается. Врачи и медсестры сообщают каждому больному, что ему можно и что нельзя на текущем этапе лечения.
Прогноз
Без лечения ОЛЛ приводит к гибели больного в течение нескольких месяцев. Однако использование современных протоколов лечения дает при ОЛЛ очень хороший результат: можно вылечить 85-90% больных детей. У взрослых, особенно пожилых, результаты хуже, но, тем не менее, примерно у 40% взрослых больных удается достичь долговременной ремиссии – то есть отсутствия рецидивов болезни в течение многих лет.
Острый лимфобластный лейкоз – злокачественное поражение системы кроветворения, сопровождающееся неконтролируемым увеличением количества лимфобластов. Проявляется анемией, симптомами интоксикации, увеличением лимфоузлов, печени и селезенки, повышенной кровоточивостью и дыхательными расстройствами. Из-за снижения иммунитета при остром лимфобластном лейкозе часто развиваются инфекционные заболевания. Возможно поражение ЦНС. Диагноз выставляется на основании клинических симптомов и данных лабораторных исследований. Лечение – химиотерапия, радиотерапия, пересадка костного мозга.
МКБ-10
Общие сведения
В соответствии с классификацией ВОЗ различают четыре типа ОЛЛ: пре-пре-В-клеточный, пре-В-клеточный, В-клеточный и Т-клеточный. В-клеточные острые лимфобластные лейкозы составляют 80-85% от общего количества случаев заболевания. Первый пик заболеваемости приходится на возраст 3 года. В последующем вероятность развития ОЛЛ повышается после 60 лет. Т-клеточный лейкоз составляет 15-20% от общего количества случаев болезни. Пик заболеваемости приходится на возраст 15 лет.

Причины острого лимфобластного лейкоза
Непосредственной причиной острого лимфобластного лейкоза является образование злокачественного клона – группы клеток, обладающих способностью к неконтролируемому размножению. Клон образуется в результате хромосомных аберраций: транслокации (обмена участками между двумя хромосомами), делеции (утраты участка хромосомы), инверсии (переворота участка хромосомы) или амплификации (образования дополнительных копий участка хромосомы). Предполагается, что генетические нарушения, вызывающие развитие острого лимфобластного лейкоза, возникают еще во внутриутробном периоде, однако для завершения процесса формирования злокачественного клона нередко требуются дополнительные внешние обстоятельства.
В числе факторов риска возникновения острого лимфобластного лейкоза обычно в первую очередь указывают лучевые воздействия: проживание в зоне с повышенным уровнем ионизирующей радиации, радиотерапию при лечении других онкологических заболеваний, многочисленные рентгенологические исследования, в том числе во внутриутробном периоде. Уровень связи, а также доказанность наличия зависимости между различными лучевыми воздействиями и развитием острого лимфобластного лейкоза сильно различаются.
Так, взаимосвязь между лейкозами и лучевой терапией в наши дни считается доказанной. Риск возникновения острого лимфобластного лейкоза после радиотерапии составляет 10%. У 85% пациентов болезнь диагностируется в течение 10 лет после окончания курса лучевой терапии. Связь между рентгенологическими исследованиями и развитием острого лимфобластного лейкоза в настоящее время остается на уровне предположений. Достоверных статистических данных, подтверждающих эту теорию, пока не существует.
Вероятность развития острого лимфобластного лейкоза повышается при контакте матери с некоторыми токсическими веществами в период гестации, при некоторых генетических аномалиях (анемии Фанкони, синдроме Дауна, синдроме Швахмана, синдроме Клайнфельтера, синдроме Вискотта-Олдрича, нейрофиброматозе, целиакии, наследственно обусловленных иммунных нарушениях), наличии онкологических заболеваний в семейном анамнезе и приеме цитостатиков. Некоторые специалисты отмечают возможное негативное влияние курения.
Симптомы острого лимфобластного лейкоза
Болезнь развивается стремительно. К моменту постановки диагноза суммарная масса лимфобластов в организме может составлять 3-4% от общей массы тела, что обусловлено бурной пролиферацией клеток злокачественного клона на протяжении 1-3 предыдущих месяцев. В течение недели количество клеток увеличивается примерно вдвое. Различают несколько синдромов, характерных для острого лимфобластного лейкоза: интоксикационный, гиперпластический, анемический, геморрагический, инфекционный.
Интоксикационный синдром включает в себя слабость, утомляемость, лихорадку и потерю веса. Повышение температуры может провоцироваться как основным заболеванием, так и инфекционными осложнениями, которые особенно часто развиваются при наличии нейтропении. Гиперпластический синдром при остром лимфобластном лейкозе проявляется увеличением лимфоузлов, печени и селезенки (в результате лейкемической инфильтрации паренхимы органов). При увеличении паренхиматозных органов могут появляться боли в животе. Увеличение объема костного мозга, инфильтрация надкостницы и тканей суставных капсул могут становиться причиной ломящих костно-суставных болей.
О наличии анемического синдрома свидетельствуют слабость, головокружения, бледность кожи и учащение сердечных сокращений. Причиной развития геморрагического синдрома при остром лимфобластном лейкозе становятся тромбоцитопения и тромбозы мелких сосудов. На коже и слизистых выявляются петехии и экхимозы. При ушибах легко возникают обширные подкожные кровоизлияния. Наблюдаются повышенная кровоточивость из ран и царапин, кровоизлияния в сетчатку, десневые и носовые кровотечения. У некоторых больных острым лимфобластным лейкозом возникают желудочно-кишечные кровотечения, сопровождающиеся кровавой рвотой и дегтеобразным стулом.
Иммунные нарушения при остром лимфобластном лейкозе проявляются частым инфицированием ран, царапин и следов от уколов. Могут развиваться различные бактериальные, вирусные и грибковые инфекции. При увеличении лимфатических узлов средостения отмечаются нарушения дыхания, обусловленные уменьшением объема легких. Дыхательная недостаточность чаще обнаруживается при Т-клеточном остром лимфобластном лейкозе. Нейролейкозы, спровоцированные инфильтрацией оболочек спинного и головного мозга, чаще отмечаются во время рецидивов.
При вовлечении ЦНС выявляются положительные менингеальные симптомы и признаки повышения внутричерепного давления (отек дисков зрительных нервов, головная боль, тошнота и рвота). Иногда поражение ЦНС при остром лимфобластном лейкозе протекает бессимптомно и диагностируется только после исследования цереброспинальной жидкости. У 5-30% мальчиков появляются инфильтраты в яичках. У пациентов обоих полов на коже и слизистых оболочках могут возникать багрово-синюшные инфильтраты (лейкемиды). В редких случаях наблюдаются выпотной перикардит и нарушения функции почек. Описаны случаи поражений кишечника.
С учетом особенностей клинической симптоматики можно выделить четыре периода развития острого лимфобластного лейкоза: начальный, разгара, ремиссии, терминальный. Продолжительность начального периода составляет 1-3 месяца. Преобладает неспецифическая симптоматика: вялость, утомляемость, ухудшение аппетита, субфебрилитет и нарастающая бледность кожи. Возможны головные боли, боли в животе, костях и суставах. В период разгара острого лимфобластного лейкоза выявляются все перечисленные выше характерные синдромы. В период ремиссии проявления болезни исчезают. Терминальный период характеризуется прогрессирующим ухудшением состояния больного и завершается летальным исходом.
Диагностика острого лимфобластного лейкоза
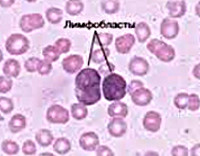
Диагноз выставляют с учетом клинических признаков, результатов анализа периферической крови и данных миелограммы. В периферической крови пациентов с острым лимфобластным лейкозом выявляются анемия, тромбоцитопения, повышение СОЭ и изменение количества лейкоцитов (обычно – лейкоцитоз). Лимфобласты составляют 15-20 и более процентов от общего количества лейкоцитов. Количество нейтрофилов снижено. В миелограмме преобладают бластные клетки, определяется выраженное угнетение эритроидного, нейтрофильного и тромбоцитарного ростка.
В программу обследования при остром лимфобластном лейкозе входят люмбальная пункция (для исключения нейролейкоза), УЗИ органов брюшной полости (для оценки состояния паренхиматозных органов и лимфатических узлов), рентгенография грудной клетки (для обнаружения увеличенных лимфоузлов средостения) и биохимический анализ крови (для выявления нарушений функции печени и почек). Дифференциальный диагноз острого лимфобластного лейкоза проводят с другими лейкозами, отравлениями, состояниями при тяжелых инфекционных заболеваниях, инфекционным лимфоцитозом и инфекционным мононуклеозом.
Лечение и прогноз при остром лимфобластном лейкозе
Основой терапии являются химиопрепараты. Выделяют два этапа лечения ОЛЛ: этап интенсивной терапии и этап поддерживающей терапии. Этап интенсивной терапии острого лимфобластного лейкоза включает в себя две фазы и длится около полугода. В первой фазе осуществляют внутривенную полихимиотерапию для достижения ремиссии. О состоянии ремиссии свидетельствуют нормализация кроветворения, наличие не более 5% бластов в костном мозге и отсутствие бластов в периферической крови. Во второй фазе проводят мероприятия для продления ремиссии, замедления или прекращения пролиферации клеток злокачественного клона. Введение препаратов также осуществляют внутривенно.
Продолжительность этапа поддерживающей терапии при остром лимфобластном лейкозе составляет около 2 лет. В этот период больного выписывают на амбулаторное лечение, назначают препараты для перорального приема, осуществляют регулярные обследования для контроля над состоянием костного мозга и периферической крови. План лечения острого лимфобластного лейкоза составляют индивидуально с учетом уровня риска у конкретного больного. Наряду с химиотерапией используют иммунохимиотерапию, радиотерапию и другие методики. При низкой эффективности лечения и высоком риске развития рецидивов осуществляют трансплантацию костного мозга. Средняя пятилетняя выживаемость при В-клеточном остром лимфобластном лейкозе в детском возрасте составляет 80-85%, во взрослом – 35-40%. При Т-лимфобластном лейкозе прогноз менее благоприятен.

Острым лимфобластным лейкозом (общепринятая аббревиатура — ОЛЛ) называют злокачественное заболевание крови и костного мозга, при котором кроветворный орган неконтролируемо продуцирует незрелые (бластные) лимфоциты. Это приводит к резкому ухудшению состояния больного, повышает риск кровотечений и восприимчивость к инфекциям. Наиболее часто болезнь поражает детей в возрасте от года до шести лет, причём у мальчиков она встречается чаще, чем у девочек. Взрослые страдают от ОЛЛ на порядок реже детей, причём самые высокие показатели заболеваемости — у пожилых людей старше 60 лет.
По типу поражённых лимфоцитов клинические случаи подразделяются на:
- В-клеточные, на долю которых приходится до 85% больных, у которых кроветворный орган активно продуцирует незрелые В-клетки (в здоровом организме вырабатывающие антитела к патогенам);
- Т-клеточные, составляющие до 15% пациентов, у которых продуцируются незрелые Т-клетки (в норме отвечающие за регуляцию производства антител).
Острый лимфобластный лейкоз В-типа наиболее часто поражает маленьких детей и людей старшей возрастной группы. Основную группу риска ОЛЛ Т-типа составляют подростки 14-15 лет.
Симптомы
Первые признаки заболевания развиваются с увеличением в составе крови незрелых лимфоцитов:
- бледность кожи;
- быстрая утомляемость;
- повышенная температура тела;
- чрезмерное выделение пота, особенно по ночам;
- частые простуды;
- кровоподтёки и синяки на коже;
- потеря веса без видимых причин.
По мере распространения лейкозных клеток развиваются симптомы острого лимфоцитарного лейкоза, свидетельствующие о поражении других органов:
- головные боли, нарушения зрения и слуха, ухудшение координации движений, онемение лицевых мышц при проникновении в головной мозг и нервную систему;
- боли в костях и суставах при тотальном поражении костного мозга;
- боли в правом подреберье при метастазировании в печень и селезёнку.
Могут встречаться и другие проявления болезни, в зависимости от локализации повреждений.
Причины и факторы риска
Онкогематологи связывают появление злокачественных клонов, дающих начало острому лимфобластному лейкозу, с рядом провоцирующих факторов.
- Радиоактивное излучение, в том числе лучевая терапия по поводу другого онкозаболевания.
- Некоторые инфекционные заболевания.
- Длительный контакт с канцерогенными химическими соединениями.
- Наличие близких родственников, страдавших аналогичной онкопатологией.
- Заболевания, связанные с генетическими отклонениями.
- Курение табака.
У детей болезнь может развиваться, если мать испытывала воздействие одного или нескольких перечисленных факторов во время беременности.
Стадии
Различают следующие стадии заболевания.
- Начало. Характеризуется общим ухудшением самочувствия, появлением первых неспецифических признаков — бледности, быстрой утомляемости, появлении болей в мышцах и костях.
- Разгар. Характерные для онкопатологии симптомы ярко выражены, состояние больного резко ухудшается.
- Ремиссия. Самочувствие больного улучшается, клинико-гематологические показатели возвращаются к норме.
- Рецидив. После ремиссии количество бластных лимфоцитов вновь возрастает, возвращаются патологические симптомы.
- Терминальная стадия. Заболевание быстро прогрессирует, поражаются жизненно важные органы. Наиболее частое завершение — летальный исход.
Диагностика
Поскольку заболевание развивается очень быстро, то при обращении к онкологу или онкогематологу симптомы острого лимфоидного лейкоза у него уже, как правило, ярко выражены. Однако для подтверждения диагноза и для определения методов лечения необходимы лабораторные анализы, а также проведение инструментальных исследований:
- общий и биохимический анализы крови;
- миелограмма — исследование клеток костного мозга, цитохимический анализ, иммунофенотипирование;
- пункция спинного мозга с гистологическим и цитологическим исследованием биоптата;
- УЗИ внутренних органов и лимфоузлов;
- рентген грудной клетки;
- ЭКГ и другие исследования согласно симптоматике.
Лечение
Как правило, схема лечения острого лимфобластного лейкоза включает три основных этапа.
Индукция. Продолжительность составляет несколько недель. Интенсивная химиотерапия направлена на уничтожение злокачественных лимфоцитов. К окончанию этапа в костном мозге должно быть не более 5% незрелых клеток.
- Консолидация. Усилия онкологов направлены на закрепление достигнутого результата и предотвращение рецидива острого лимфобластного лейкоза. Для этого пациенту курсами вводят химиотерапевтические средства. На этом этапе возможна пересадка здоровых стволовых клеток для восстановления кроветворной функции. При отсутствии стойкой ремиссии и высокой угрозе рецидива может быть назначена пересадка костного мозга.
- Поддерживающая терапия. Как правило, этот этап подразумевает амбулаторное лечение, но он не менее важен, чем предыдущие для достижения стойкой ремиссии. Пациенту назначают пероральные химиотерапевтические препараты, он регулярно проходит обследования, выполняет все назначения онкогематолога.
На всех этапах лечение сопровождается приёмом антимикробных средств, переливаниями тромбоцитной массы и крови. Периодически проводится дезинтоксикация организма, чтобы очистить кровь от продуктов распада лейкозных клеток.
Прогнозы
При остром лимфобластном лейкозе прогноз благоприятен для 80-90% детей. У взрослых шансы на полное излечение достигают 40-45%, причём с возрастом они понижаются. Существенное влияние на успех лечения оказывает уровень бластных лимфоцитов в крови пациента на момент начала лечения, наличие у него хромосомных аномалий, а также распространение болезни в тканях головного мозга.
Профилактика
На сегодняшний день не существует специальных профилактических мер для безусловного предупреждения острого лимфобластного лейкоза. Общие рекомендации заключаются в поддержании здорового образа жизни, исключении курения, минимизации контактов с канцерогенными соединениями.
Реабилитация
Восстановление после химиотерапии ничем не отличается от аналогичных мер при остром нелимфобластном лейкозе и включает:
- меры, необходимые для активации собственной иммунной системы;
- приём пробиотиков и выполнение рекомендаций врача по сбалансированному питанию;
- выведение токсинов из организма;
- антистрессовую терапию, избавление от депрессивного состояния.
Важно, чтобы пациент выполнял все рекомендации онкогематолога.
Диагностика и лечение острого лимфобластного лейкоза в Москве
Квалифицированная диагностика острого лимфобластного лейкоза проводится в московской клинике Института ядерной медицины. Современное лечебно-диагностическое оборудование и высокая квалификация врачей-онкологов позволяют использовать для лечения онкозаболеваний передовые методы мировой практики с максимально высокой результативностью.
Вопросы и ответы
Какова продолжительность жизни при остром лимфобластном лейкозе?
При отсутствии лечения больной с ОЛЛ может прожить не более нескольких месяцев. Современные методики позволяют добиться полного выздоровления для 90% детей. У взрослых результативность терапии менее высока, однако у каждого пациента есть шансы, и необходимо их полностью использовать.
Нужна ли пересадка костного мозга при остром лимфобластном лейкозе?
Трансплантация костного мозга проводится только после наступления ремиссии при наличии показаний — при плохом ответе на индукционную терапию или из-за быстрого наступления рецидива. Как правило, у детей необходимости в пересадке не возникает. Костный мозг может быть взят у родственного либо у неродственного донора.
Можно ли вылечить острый лимфобластный лейкоз после рецидива?
Лечение при рецидиве заболевания зависит от локализации поражения — находится ли источник в костном мозге или вне его — например, в центральной нервной системе. Кроме того, имеет значение срок его развития — ранний либо поздний. Наиболее высоки шансы на успех при позднем рецидиве.
Читайте также:

