Лечение генами фантастика или реальность доклад
Обновлено: 05.07.2024
Трансфекция клеток
Методы генной терапии
Существует два основных подхода, различающиеся природой клеток-мишеней: 1. Фетальная, при которой чужеродную ДНК вводят в зиготу (оплодотворённую яйцеклетку) или эмбрион на ранней стадии развития; при этом ожидается, что введённый материал попадёт во все клетки реципиента (и даже в половые клетки, обеспечив тем самым передачу следующему поколению). В нашей стране она фактически запрещена ; 2. Соматическая, при которой генетический материал вводят уже родившемуся в неполовые клетки и он не передаётся половым клеткам. Генная терапия in vivo основана на прямом введении клонированных (размноженных) и определенным образом упакованных последовательностей ДНК в определённые ткани больного. Особенно перспективным для лечения генных болезней in vivo представляется введение генов с помощью аэрозольных или инъецируемых вакцин. Аэрозольная генотерапия разрабатывается, как правило, для лечения лёгочных заболеваний (муковисцидоз, рак лёгких). Разработке программы генной терапии предшествует много этапов. Это и тщательный анализ тканеспецифической экспрессии соответствующего гена (т. е., синтеза на матрице гена какого-то белка в определённой ткани), и идентификация первичного биохимического дефекта, и исследование структуры, функции и внутриклеточного распределения его белкового продукта, а также биохимический анализ патологического процесса. Все эти данные учитываются при составлении соответствующего медицинского протокола.
Прямая доставка и клеточные носители терапевтических генов
Судьба гена после его попадания в клетку
Заключение
Обзор данных позволяет прийти к заключению, что, несмотря на усилия многих лабораторий мира, все уже известные и испытанные in vivoи in vitro векторные системы далеки от совершенства . Если проблема доставки чужеродной ДНК in vitro практически решена, а ее доставка в клетки-мишени разных тканей in vivo успешно решается (главным образом путем создания конструкций, несущих рецепторные белки, в том числе и антигены, специфичные для тех или иных тканей), то другие характеристики существующих векторных систем – стабильность интеграции, регулируемая экспрессия, безопасность – все еще нуждаются в серьезных доработках. Прежде всего, это касается стабильности интеграции. До настоящего времени интеграция в геном достигалась только при использовании ретровирусных либо аденоассоциированных векторов. Повысить эффективность стабильной интеграции можно путем совершенствования генных конструкций типа рецептор-опосредованных систем либо путем создания достаточно стабильных эписомных векторов (то есть ДНК-структур, способных к длительному пребыванию внутри ядер). В последнее время особое внимание уделяется созданию векторов на базе искусственных хромосом млекопитающих. Благодаря наличию основных структурных элементов обычных хромосом такие мини-хромосомы длительно удерживаются в клетках и способны нести полноразмерные (геномные) гены и их естественные регуляторные элементы, которые необходимы для правильной работы гена, в нужной ткани и в должное время. Генная и клеточная терапия открывает блестящие перспективы для восстановления утраченных клеток и тканей и генно-инженерного конструирования органов, что, несомненно, существенно расширит арсенал методов для медико-биологических исследований и создаст новые возможности для сохранения и продления жизни человека .
ФГБУ "Московский научно-исследовательский онкологический институт им. П.А. Герцена" Минздравсоцразвития России
ФГБУ "Московский научно-исследовательский онкологический институт им. П.А. Герцена" Минздрава России
Генная терапия — новое направление в медицине
Журнал: Онкология. Журнал им. П.А. Герцена. 2016;5(2): 64-72





ФГБУ "Московский научно-исследовательский онкологический институт им. П.А. Герцена" Минздравсоцразвития России
ФГБУ "Московский научно-исследовательский онкологический институт им. П.А. Герцена" Минздрава России
Достижения молекулярной биологии и генетики в изучении тонкой структуры генов эукариот, картирование генов на хромосомах млекопитающих, их идентификация и клонирование, обнаружение мутаций в генах, ассоциированных с наследственными и приобретенными заболеваниями, наряду с бурным ростом в области биотехнологий, клеточных технологий и успехами генной инженерии привели к тому, что в конце прошлого века начался бум в исследованиях по анализу молекулярно-биохимических дефектов, ассоциированных с определенной патологией, который привел к пониманию того, что большинство грозных заболеваний человека сопровождается серьезными изменениями в генетическом аппарате клетки. Особенно выражены и наиболее исследованы эти изменения при злокачественных новообразованиях. Из этих данных следует логичный вывод о том, что наиболее радикальным способом борьбы с заболеваниями, вызываемыми изменениями в генетическом аппарате клеток, должны быть мероприятия, направленные непосредственно на причину заболевания, а не ее последствия.
Генная терапия — это лечение наследственных, мультифакториальных и ненаследственных (инфекционных, злокачественных и др.) заболеваний путем введения генов в соматические клетки пациентов с целью направленного изменения генных дефектов или придания клеткам новых свойств.
В 1976 г. в Университете Пенсильвания, США, Уильям Андерсон предложил использование вирусов в качестве носителей ДНК, а в 1990 г. этот исследователь в клинике Университета Пенсильвания ввел больной Ашанти ДеСильва с синдромом комбинированного иммунодефицита (СКИД) генетически модифицированные геном аденозиндезаминазы ее собственные лимфоциты, в последующие 3 года провел 23 внутривенных трансфузии и получил длительную ремиссию, а затем выздоровление.
В 1990—1999 гг. Департамент здравоохранения США за год после выздоровления Ашанти создает свыше сотни лабораторий по генной терапии, проводит более 400 клинических исследований по генной терапии, в которых принимает участие свыше 4 тыс. пациентов. Однако в 1999 г. в госпитале Университета Пенсильвании, США, происходит событие, которое резко затормозило исследования по генной терапии в США. Это — внезапная смерть 17-летнего Джесси Гелзингер в процессе лечения наследственного заболевания печени.
В то же время метод генной терапии все шире распространялся по миру и к настоящему моменту в мире проведено и проводится более 2210 клинических испытаний по генной терапии. География их широка и разнообразна. Это — Америка (63,9%), Европа (24,1%), Азия (6,0%), Австралия (1,5%), международные (4,2%) [1]. По странам имеется распределение, свидетельствующее о том, что эта технология наиболее развита в США и ряде Европейских стран.
Спектр заболеваний, при которых проводятся клинические испытания по генной терапии, также чрезвычайно широк (табл. 1). Независимо от нозологии, в области соматической генной терапии имеются общие задачи. Это:

Таблица 1. Клинические испытания в области генной терапии
— выбор наиболее эффективного для лечения гена;
— разработка способов доставки требуемого гена в нужные клетки;
— изучение и обеспечение эффективных подходов и способов нужной регуляции гена;
— вопросы длительности существования и экспрессии введенного гена;
— обеспечение безопасности больного.
Типы генов, используемых при генной терапии, разнообразны, и их выбор определяется патогенетическими механизмами развития заболевания, идентификацией наиболее болезнетворных генов.
Наиболее простая задача в выборе гена стоит при моногенных наследственных заболеваниях, то есть там, где показано, что определенный дефект в данном гене вызывает патологический процесс. Совершенно другая задача по степени сложности в выборе гена для терапии стоит при многофакториальных заболеваниях, таких как злокачественные новообразования, кардиоваскулярные болезни, при которых в патогенезе заболеваний, во-первых, пока много неясного, во-вторых, задействован ряд генов.
Для эффективной работы выбранный терапевтический ген снабжают сигнальными (регулирующими) элементами, которые необходимы для синтеза полноценной мРНК и целевого белка, а также позволяют управлять специфичностью экспрессии в определенном типе клеток или ткани, длительностью функционирования и нужной регуляцией гена в клетке (рис. 1) [2, 3].

Рис. 1. Схема генно-терапевтической конструкции.
Специфичность экспрессии генов в заданной клетке достигается конструированием векторов, несущих терапевтические гены под контролем промоторов, работающих только в данном типе клеток. К настоящему моменту выявлен ряд тканеспецифичных промоторов, обеспечивающих селективную экспрессию терапевтических трансгенов в клетках определенных органов. В экспериментальной генной терапии сердечно-сосудистых заболеваний в настоящее время используют промоторы, которые обеспечивают преимущественную экспрессию трансгена в миокарде (SM22α-промотор и др.) [4]. Разработан целый ряд тканеспецифичных промоторных систем, в которых использованы гены, высокоэкспрессированные, главным образом, в опухолевых клетках: простатспецифический и простатспецифический мембранный антигены при раке предстательной железы [5], гены, кодирующие сурфактантные белки, А и В, при раке легкого [6, 7], ген мембранно-связанного муцина MUC1/DF3 при раке молочный железы, трахеи, легкого, тонкого или толстого кишечника [8], ген α-фетопротеина — белка, синтезируемого в печени, при раке печени [9], промоторы гена сурвивина человека (hSurv) и гена обратной транскриптазы теломеразы человека (hTERT), обеспечивающих экспрессию трансгена в клетках широкого спектра опухолей [10, 11] (табл. 2).

Таблица 2. Опухолеспецифичные промоторы
Поскольку тканеспецифичные промоторы обладают общим недостатком — низким уровнем экспрессии гетерологичных генов, а также ограниченной областью применения, обусловленной их тканеспецифичностью, в настоящее время идет активный поиск промоторов генов человека, не обладающих тканевой специфичностью — универсальных или гибридных промоторов, направленных исключительно на пролиферирующие клетки и не затрагивающих нормальные дифференцированные клетки.
Одной из сложнейших проблем в генной терапии является доставка требуемого гена в нужные ткани при минимизации его контакта с биологическими средами организма до достижения клетки-мишени, а также обеспечение доставки гена в нужную клетку с целью его эффективной и безопасной работы в ней.

Рис. 2. Системы доставки генетического материала в клетку. (Адаптировано по: Thomas SM, Grandis JR. The Current State of Head and Neck Cancer Gene Therapy. 2009; Y20: 1565—1575 [12])
Альтернативным способом доставки терапевтических генов является использование векторов вирусной, бактериальной и химической природы. Вектор должен эффективно и специфически трансфицировать/трансдуцировать делящиеся и неделящиеся таргетные клетки, экспрессировать трансген в адекватных количествах в течение длительного времени, производиться легко и рентабельно по количеству и качеству, не быть иммуногенным и использоваться для повторного введения гена, являться безопасным при введении и не иметь побочных эффектов.
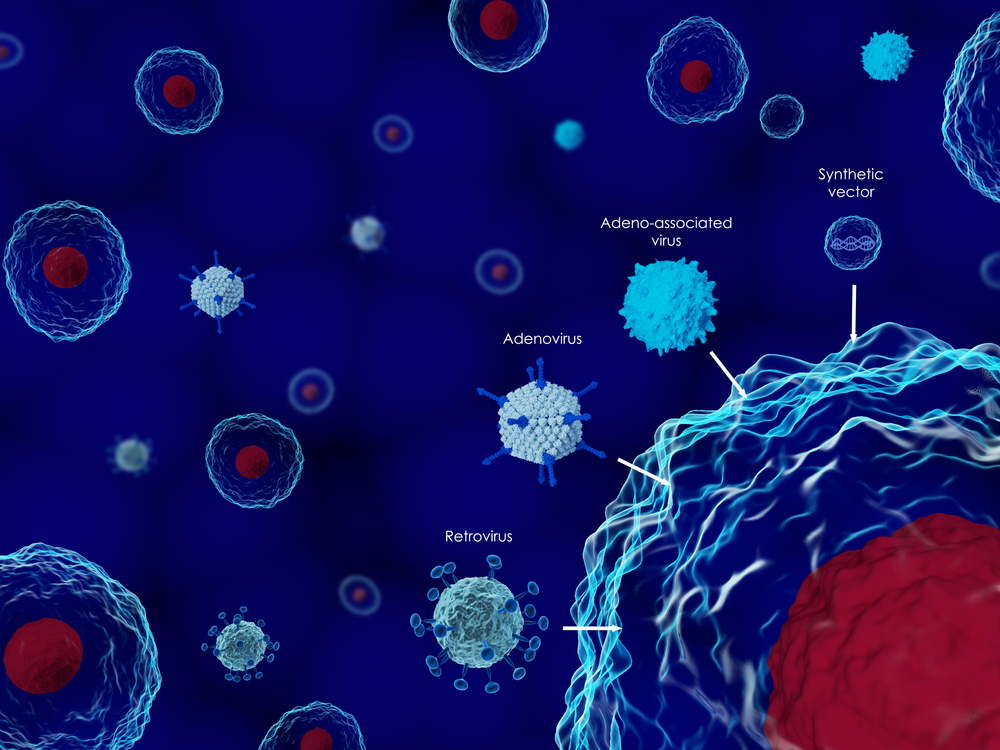
В качестве векторов для доставки генетического материала в клетку-мишень используют самые разнообразные вирусы, но наиболее распространены векторы на основе аденовируса (ADV), аденоассоциированного вируса, ретро- (RV), лентивируса (LV) и вируса простого герпеса (HSV) (табл. 3). При этом нативные полные вирусные частицы никогда не используются в качестве векторов, так как в этом случае есть опасность встраивания их генетического материала в клетки хозяина с целью приобретения метаболических и биосинтетических продуктов для вирусной транскрипции и репликации. Поэтому вирусы предварительно подвергаются существенной генетической модификации, приводящей к утере их репликационной способности и повышению тропизма к тканям и клеткам.

Таблица 3. Вирусные векторы для генной терапии
Вирусные векторы достаточно хорошо изучены, они имеют высокую эффективность трансфекции in vivo, для их наработки существуют коммерческие паковочные клеточные линии. Векторы на основе аденовируса и аденоассоциированных вирусов не встраиваются в геном клетки, а остаются эпихромосомными. Это уменьшает опасность мутагенеза, который может быть индуцирован при внедрении вируса в геном. При конструировании специфически направленных аденовирусных векторов эффективной оказалась замена вирусных промоторов, контролирующих основные транскрипционные области, так называемыми транскрипционными регуляторами, в результате чего экспрессия гена и репликация вируса происходят преимущественно в целевых клетках [14, 15].
Ретровирусные векторы интегрируют в геном хозяина, что при генной терапии обеспечивает стабильность и стойкую экспрессию трансгена в дочерних клетках, однако несет риск инсерционного мутагенеза, который может вызывать инактивацию генов-супрессоров опухолевого роста или активации онкогенов [16].
Несмотря на описанные недостатки, вирусный метод доставки трансгенов в клетки успешно развивается и в настоящее время является доминирующим: около 70% клинических исследований посвящено изучению генетических конструкций, снабженных вирусными векторами.
В то же время в последние годы активно разрабатываются невирусные системы доставки генетического материала с использованием высокомолекулярных химических соединений для конденсации с ДНК: липидсвязанные комплексы — липоплексы либо поликатионные комплексы, имитирующие поверхность вируса — полиплексы (табл. 4). Эти наночастицы защищают плазмидную ДНК в межклеточном пространстве от деградации нуклеазами и облегчают проникновение в клетки-мишени. Положительно заряженные комплексы связываются со специфическими рецепторами (при наличии на их поверхности макромолекул, обладающих свойствами специфического лиганда) или непосредственно с поверхностью клетки. Комплексы проникают в клетку по механизму эндоцитоза. После высвобождения из эндосомы и разборки комплекса нуклеиновая кислота проникает через поры в ядро клетки [20].

Таблица 4. Невирусные векторы для генной терапии
Невирусные системы на основе катионных липидов или полимеров имеют ряд преимуществ перед вирусными системами доставки: большой объем несущей ДНК, отсутствие какой-либо вирусной составляющей, а следовательно, низкая иммуногенность, высокая технологичность производства. Однако низкая трансфицирующая способность невирусных векторов и недостаток информации о безопасности у человека тормозят развитие исследований в этом направлении, только 5,2% приходится на клинические испытания, где в качестве системы доставки терапевтических генов используют липоплексы или полиплексы.
К настоящему моменту сформировалось два типа геннотерапевтического воздействия: индивидуализированный подход ex vivo — трансфекция стволовых гемопоэтических клеток, полученных из периферической крови и трансплантированных затем больному, и in vivo — трансфекция клеток внутри организма, куда генетический материал в составе вектора доставляется в результате внутривенной или внутриартериальной (в печеночную артерию) инфузии, внутримышечного, подкожного, интратуморального, интраназального или сублингвального введения. В практике лечения сердечно-сосудистых заболеваний испытываются прямые игольные инъекции конструкций в миокард, введение вирусных векторов при помощи разнообразных катетеров, использование стентов с покрытиями, обеспечивающими дозированный выход лекарственного средства. В онкологии используют, как правило, внутриопухолевое введение целевого гена в составе различных векторов.

Таблица 5. Подходы к генной терапии онкологических заболеваний
Представления о патогенезе злокачественных новообразований, в основе которого, в том числе, лежат активация онкогенов и инактивация генов-супрессоров опухолевого роста, позволяют искать пути подавления или восстановления функции этих генов.
К настоящему моменту известно более 24 генов-супрессоров, среди них наиболее изученным является ген р53, контролирующий клеточный цикл и поврежденный в ≈50% опухолей человека [21]. Так, коррекционная замена мутантного гена p53 в опухолевых клетках геном дикого типа (не содержащим мутаций) с помощью методов генотерапии приводила к восстановлению функций белка p53 и инициации процессов, запускающих программированную гибель злокачественных клеток. Клинические испытания аденовирусного вектора Ad-p53 показали, что восстановление дикого типа р53 путем доставки гена при помощи дефектного по репликации Ad приводило к значительному противоопухолевому эффекту на фоне низкой общей токсичности [22]. Более того, восстановление р53 сопровождалось увеличением чувствительности опухолевых клеток к химио- и радиотерапии [23].
Наиболее успешным онколитическим препаратом является OncoVexGMCSF на основе вируса простого герпеса, который проходит II/III фазы клинических испытаний для лечения меланомы, рака молочной железы, опухолей головы и шеи. В геноме этого вируса сохранен ген тимидинкиназы для проведения GDEPT, но удалены обе копии ICP34.5 гена, отвечающего за вирусную репликацию в нормальных клетках, а в область ICP47 встроен ген GM-CSF. Продуцируемый GM-CSF привлекает дендритные клетки (DC) и может стимулировать выброс цитотоксических Т-лимфоцитов [35].
Следует отметить, что современная стратегия развития иммунотерапии рака на фоне расширяющихся знаний о функционировании иммунной системы и формировании иммунного ответа является главной предпосылкой для усовершенствования подходов к лечению с привлечением инновационных лекарственных средств, созданных методами генной инженерии, таких как генные вакцины.
Исследования в этой области ведутся в трех направлениях: модификация опухолевых клеток для придания им большей иммуногенности, введение генов опухолеассоциированных антигенов в дендритные клетки, геномодификация лимфоцитов для повышения цитотоксического ответа.
Метод, известный как технология химерных антигенных рецепторов, или CAR-технология (от англ. chimeric antigen receptor), в настоящее время является одним из наиболее перспективных и быстро развивающихся направлений в области иммунотерапии злокачественных новообразований [42]. Эта технология заключается в выделении из периферической крови пациента Т-лимфоцитов и их двухкомпонентной модификации в условиях ex vivo: присоединение к их поверхности рецептора, распознающего экспрессируемый большинством лейкемических клеток белок CD19, и введение мощного внутриклеточного механизма, запускающего активный рост и деление клеток в ответ на их взаимодействие с белком-мишенью. Такие генномодифицированные Т-лимфоциты возвращают в кровоток пациента. Предварительные результаты исследований свидетельствуют о том, что этот подход позволяет получить хорошие результаты у 2/3 пациентов, не ответивших на традиционные методы лечения [43—45].

Таблица 6. Официнальные препараты для генной терапии различных заболеваний
Заключение
Таким образом, использование метода генной терапии может быть результатом уже не столь отдаленного будущего, но говорить о реальных перспективах этого направления в медицине, по-видимому, пока преждевременно. Несмотря на то, что большинство клинических испытаний свидетельствует об относительной безопасности геннотерапевтических препаратов, требуется время для окончательного доказательства их эффективности. Возможно, в будущем метод генной терапии станет основным в лечении наследственных заболеваний, а для заболеваний онкологического профиля генная терапия будет рассматриваться как часть комплексного противоопухолевого лечения.
Управление по контролю качества пищевых продуктов и медикаментов США (FDA) 24 мая 2019 года одобрило использование генно-терапевтического препарата Zolgensma для лечения спинальной мышечной атрофии 1-го типа у детей в возрасте до двух лет. Рассказываем, что такое генная терапия и почему она может стать лекарством будущего.
Генно-терапевтический подход к лечению наследственных заболеваний разрабатывается уже 40 лет. Основная технология генной терапии основана на замещении гена с мутацией правильно функционирующей копией этого гена. Но есть еще две стратегии: выключение неправильно работающего гена и введение нового гена, который поможет организму победить заболевание.
Надо подчеркнуть принципиальное отличие генной терапии от редактирования генома, которое сейчас тоже активно разрабатывается для лечения наследственных заболеваний. Генная терапия доставляет ген в клетки, чтобы компенсировать дефектный ген. Но при этом не происходит удаление дефектной ДНК из клеток. При редактировании генома происходит удаление или изменение дефектной ДНК в клетках пациента.
Для доставки генная терапия использует различные вирусы, которые транспортируют ген специфично в определённый орган. Вирусы - внутриклеточные паразиты, они встраивают свою генетическую информацию в ДНК клетки и таким образом заставляют клетку делать копии вирусной ДНК. Это оказалось очень полезным свойством для генной терапии. Перед использованием вирусы делают безвредными, чтобы они не могли вызывать заболевание, но могли доставить ген в клетки.
В зависимости от цели генная терапия бывает соматической и фетальной. В первом случае вирус с геном вводят в клетки тела, во втором – в эмбрион на ранней стадии развития. В результате фетальной генной терапии генетический материал попадает во все клетки и может быть передан детям.
В ходе клинических испытаний препарат Zolgensma показал хорошие результаты у пациентов со спинальной мышечной атрофией: из 21 пациентов 19 смогли начать двигать головой и самостоятельно сидеть.
Спинальная мышечная атрофия - наследственное заболевание, к развитию которого приводят мутации в гене SMN1. При этом заболевании из-за нарушения работы нервных клеток спинного мозга развивается слабость мышц и их атрофия. Дети теряют способность ходить, а по мере развития заболевания - самостоятельно дышать. Более 90% случаев заболевания заканчиваются смертью детей до 2-х лет.
Препараты генной терапии могут стать эффективным средством лечения многих наследственных заболеваний, для которых не существовало лечения до этого. Так, в ближайшее время ожидает одобрения международного регулятора еще один новый генно-терапевтический препарат для лечения талассемии и серповидноклеточной анемии. Оба этих заболевания связаны с мутациями, результатом которых является синтез неправильно работающего гемоглобина – белка, переносящего кислород в крови.
Прежде всего, препараты генной терапии разрабатываются для заболеваний, причиной которых является одна в мутация в одном гене. Таких болезней 10 000. В связи с большими затратами на разработку генно-терапевтических препаратов, они очень дорогие. Но постепенно отработка технологии позволит значительно снизить стоимость таких лекарств и сделать их доступными большинству пациентов.

Генная терапия — это лечение наследственных, мультифакториальных и ненаследственных (инфекционных, злокачественных и др.) заболеваний путем введения генов в соматические клетки пациентов с целью направленного изменения генных дефектов или придания клеткам новых свойств.
Последние достижения в области генетической терапии приближают нас к тому дню, когда CRISPR, технология генетического редактирования, будет способна лечить широкий спектр заболеваний среди большого числа пациентов.
В октябре 2020 года были объявлены лауреаты Нобелевской премии по химии - французский микробиолог ЭмануэльШарпентье и американский биохимик Дженнифер Дадна - за их новаторскую работу по разработке метода редактирования генов на основе CRISPR, которую они ведут с 2012 года. Система CRISPR произвела революцию в области генной инженерии и сможет найти применение в лечении различных заболеваний. Поиск безопасных и эффективных способов внесения изменений в геном человека может привести к излечению от наследственных генетических заболеваний и даже послужить средством лечения рака.
Следующим шагом стал поиск способа воспроизводства этого процесса у человека, при помощи создания сегментов ДНК, которые могли бы обнаруживать определенные поврежденные последовательности ДНК, а затем изменять или удалять их из генома.
Само собой разумеется, что если РНК, управляющая ножницами, или процесс разрезания ДНК недостаточно точны, это может иметь серьезные и неожиданные последствия, такие как опасные мутации и рак. Еще одной проблемой при применении данного метода является то, что и РНК-мессенджер, и белок Cas9 представляют собой довольно крупные молекулы, что затрудняет их размещение в нужном месте.
Настоящий эксперимент основан на иммунологических открытиях, совершенных такими компаниями, как Gilead и Novartis, которые производят препараты для лечения CAR (химерный антигенный рецептор) -T-клеток. В рамках лечения новая ДНК вводится в Т-клетки иммунной системы, чтобы помочь им убить раковые опухоли. Это длительный процесс, требующий от пациентов посещения лаборатории и не допускающий массового производства.
С другой стороны, CRISPR Therapeutics находится на переднем крае разработки аллогенных методов лечения, основанных на использовании клеток от здоровых доноров. Риск использования чужеродных донорских клеток заключается в том, что организм реципиента отвергнет их и вызовет болезнь трансплантат против хозяина (GvHD), которая может быть фатальной.
CRISPR Therapeutics и другая биотехнологическая компания под названием AllogenicTherapeutics надеются показать, что этого не произойдет в результате разрабатываемых ими методов лечения. Создание готовых лекарств на клеточном уровне, несомненно, будет значительно дешевле для медицинской промышленности и принесет пользу пациентам, поскольку их доступность во всем мире увеличивается.
В долгосрочной перспективе использование CRISPR с целью замены дефектной ДНК в сочетании с CAR-T (действием иммунной системы, способным разрушать существующие опухоли) сможет стать оптимальной комбинацией, когда речь идет об излечения рака.

Подробнее
Медицинский лекторий

Коронавирус и пустота. Взаимоотношения в эпоху ковида

Щитовидная железа : мифы и реальность

Постковидный синдром. Что же делать дальше?



Утренние привычки для хорошего пищеварения

Как быстро еда попадает в грудное молоко при грудном вскармливании?

Ученые сообщили о способности оливкового масла продлевать жизнь

Врач назвала очищающий кишечник продукт

Врач рассказала, нужно ли заставлять себя есть при коронавирусе

Сила любви: Врач объяснил, что поможет не заболеть коронавирусом на Новый год
Читайте также:

