Ядро как динамическая система протонов и нейтронов кратко
Обновлено: 04.07.2024
Альварес · Беккерель · Быть · А. Бор · Н. Бор · Чедвик · Кокрофт · Ir. Кюри · Пт. Кюри · Пи. Кюри · Склодовская-Кюри · Дэвиссон · Ферми · Хан · Дженсен · Лоуренс · Mayer · Meitner · Олифант · Оппенгеймер · Proca · Перселл · Раби · Резерфорд · Soddy · Strassmann · Witecki · Сцилард · Кассир · Томсон · Уолтон · Вигнер
Модель атомного ядра, показывающая его как компактный пучок двух типов нуклоны: протоны (красный) и нейтроны (синий). На этой диаграмме протоны и нейтроны выглядят как склеенные вместе маленькие шарики, но на самом деле это ядро (в понимании современного ядерная физика) нельзя так объяснить, а только с помощью квантовая механика. В ядре, которое занимает определенную уровень энергии (например, основное состояние), можно сказать, что каждый нуклон занимает несколько мест.
В атомное ядро это небольшая плотная область, состоящая из протоны и нейтроны в центре атом, открытый в 1911 г. Эрнест Резерфорд на основе 1909 г. Эксперимент с золотой фольгой Гейгера – Марсдена. После открытия нейтрона в 1932 году модели ядра, состоящего из протонов и нейтронов, были быстро разработаны. Дмитрий Иваненко [1] и Вернер Гейзенберг. [2] [3] [4] [5] [6] Атом состоит из положительно заряженного ядра и облака отрицательно заряженных. электроны окружающие его, связанные вместе электростатическая сила. Почти все масса атома находится в ядре, с очень малым вкладом электронное облако. Протоны и нейтроны связаны вместе, чтобы образовать ядро. ядерная сила.
Диаметр ядра находится в диапазоне 1.7566 FM ( 1.7566 × 10 −15 м ) за водород (диаметр одиночного протона) примерно до 11.7142 FM за уран. [7] Эти размеры намного меньше диаметра самого атома (ядро + электронное облако) примерно в 26 634 раза (радиус атома урана составляет примерно 156 вечера ( 156 × 10 −12 м )) [8] примерно до 60 250 (атомный радиус водорода около 52.92 вечера ). [а]
Раздел физики, связанный с изучением и пониманием атомного ядра, включая его состав и силы, связывающие его вместе, называется ядерная физика.
Содержание
Вступление
История
Ядро было открыто в 1911 году в результате Эрнест Резерфордусилия по тестированию Томсона "сливовый пудинг модель"атома. [9] Электрон был уже открыт J.J. Томсон сам. Зная, что атомы электрически нейтральны, Дж. Дж. Томсон предположил, что также должен быть положительный заряд. В своей модели сливового пудинга Томсон предположил, что атом состоит из отрицательных электронов, случайно разбросанных внутри сферы с положительным зарядом. Эрнест Резерфорд позже разработал эксперимент со своим партнером по исследованиям. Ганс Гейгер и с помощью Эрнест Марсден, что связано с отклонением альфа-частицы (ядра гелия), направленные на тонкий лист металлической фольги. Он рассудил, что, если бы модель Дж. Дж. Томсона была верной, положительно заряженные альфа-частицы могли бы легко проходить через фольгу с очень небольшим отклонением их траектории, поскольку фольга должна действовать как электрически нейтральная, если отрицательный и положительный заряды так тесно смешаны, чтобы создавать он кажется нейтральным. К его удивлению, многие частицы отклонились на очень большие углы. Поскольку масса альфа-частицы примерно в 8000 раз больше массы электрона, стало очевидно, что должна присутствовать очень сильная сила, если она может отклонять массивные и быстро движущиеся альфа-частицы. Он понял, что модель сливового пудинга не может быть точной и что отклонения альфа-частиц можно объяснить только в том случае, если положительный и отрицательный заряды будут отделены друг от друга и что масса атома представляет собой концентрированную точку положительного заряда. Это оправдало идею ядерного атома с плотным центром положительного заряда и массы.
Этимология
Ядерный макияж
Образное изображение гелий-4 атом с электронным облаком в оттенках серого. В ядре два протона и два нейтрона изображены красным и синим цветом. Это изображение показывает частицы как отдельные, тогда как в реальном атоме гелия протоны накладываются друг на друга в пространстве и, скорее всего, находятся в самом центре ядра, и то же самое верно для двух нейтронов. Таким образом, все четыре частицы, скорее всего, находятся в одном и том же пространстве, в центральной точке. Классические изображения отдельных частиц не могут моделировать известные распределения заряда в очень маленьких ядрах. Более точное изображение - пространственное распределение нуклонов в ядре гелия гораздо ближе к гелиевому. электронное облако показано здесь, хотя и в гораздо меньшем масштабе, чем на вымышленном изображении ядра.
Ядро атома состоит из нейтронов и протонов, которые, в свою очередь, являются проявлением более элементарных частиц, называемых кварки, которые проводятся совместно ядерная мощная сила в определенных устойчивых сочетаниях адроны, называется барионы. Сильная ядерная сила распространяется достаточно далеко от каждого бариона, чтобы связывать нейтроны и протоны вместе против отталкивающей электрической силы между положительно заряженными протонами. Ядерное сильное взаимодействие имеет очень короткий радиус действия и практически падает до нуля сразу за краем ядра. Коллективное действие положительно заряженного ядра заключается в удержании электрически отрицательно заряженных электронов на их орбитах вокруг ядра. Набор отрицательно заряженных электронов, вращающихся вокруг ядра, демонстрирует сродство к определенным конфигурациям и количеству электронов, которые делают их орбиты стабильными. Который химический элемент представляет собой атом определяется количеством протоны в ядре; нейтральный атом будет иметь такое же количество электронов, вращающихся вокруг этого ядра. Отдельные химические элементы могут создавать более стабильные электронные конфигурации, объединяясь для обмена своими электронами. Это совместное использование электронов для создания стабильных электронных орбит вокруг ядра, которое представляется нам химическим составом нашего макромира.
Протоны определяют весь заряд ядра и, следовательно, его химическая идентичность. Нейтроны электрически нейтральны, но вносят вклад в массу ядра почти в той же степени, что и протоны. Нейтроны могут объяснить явление изотопы (один и тот же атомный номер с разной атомной массой). Основная роль нейтронов - уменьшить электростатическое отталкивание внутри ядра.
Состав и форма
Протоны и нейтроны фермионы, с разными значениями сильный изоспин квантовое число, поэтому два протона и два нейтрона могут находиться в одном пространстве волновая функция поскольку они не являются идентичными квантовыми объектами. Иногда их рассматривают как два разных квантовых состояния одной и той же частицы. нуклон. [12] [13] Два фермиона, такие как два протона или два нейтрона, или протон + нейтрон (дейтрон) могут проявлять бозонный поведение, когда они становятся слабо связанными парами, имеющими целочисленный спин.
В редком случае гиперядро, треть барион называется гиперон, содержащий один или несколько странные кварки и / или другой необычный кварк (ы), также могут иметь общую волновую функцию. Однако ядро этого типа крайне нестабильно и не встречается на Земле, за исключением экспериментов по физике высоких энергий.
Нейтрон имеет положительно заряженное ядро радиусом ≈ 0,3 фм, окруженное компенсирующим отрицательным зарядом с радиусом от 0,3 до 2 фм. Протон имеет примерно экспоненциально затухающее распределение положительного заряда со среднеквадратичным радиусом около 0,8 фм. [14]
Ядра могут быть сферическими, шарообразными (вытянутая деформация), дискообразными (сплющенная деформация), трехосными (комбинация сплюснутой и вытянутой деформации) или грушевидными. [15] [16]
Ядра связаны остаточной сильной силой (ядерная сила). Остаточная сильная сила - это незначительный остаток сильное взаимодействие который связывает кварки вместе с образованием протонов и нейтронов. Эта сила намного слабее между нейтронов и протонов, потому что они в основном нейтрализуются в них, так же, как электромагнитные силы между нейтральные атомы (например, силы Ван дер Ваальса которые действуют между двумя атомами инертного газа) намного слабее, чем электромагнитные силы, которые удерживают части атомов вместе внутри (например, силы, удерживающие электроны в атоме инертного газа, связанном с его ядром).
Ядерная сила очень притягивает на расстоянии типичного разделения нуклонов, и это подавляет отталкивание между протонами из-за электромагнитной силы, позволяя ядрам существовать. Однако остаточная сильная сила имеет ограниченный диапазон, потому что она быстро спадает с расстоянием (см. Потенциал Юкавы); таким образом, только ядра, меньшие определенного размера, могут быть полностью стабильными. Самое крупное из известных полностью стабильных ядер (т.е.устойчивых к альфа-, бета- и гамма-распадам) является свинец-208 который содержит в общей сложности 208 нуклонов (126 нейтронов и 82 протона). Ядра, размер которых превышает этот максимум, нестабильны и имеют тенденцию быть все более короткоживущими с большим числом нуклонов. Однако, висмут-209 также устойчив к бета-распаду и имеет самый длинный период полураспада до альфа-распада из всех известных изотопов, который, по оценкам, в миллиард раз превышает возраст Вселенной.
Остаточная сильная сила эффективна на очень коротком расстоянии (обычно только несколько фемтометры (FM); примерно один или два диаметра нуклона) и вызывает притяжение между любой парой нуклонов. Например, между протоны и нейтроны сформировать [НП] дейтрон, а также между протонами и протонами, и нейтронами и нейтронами.
Ядра гало и пределы диапазона ядерных сил
Эффективный абсолютный предел диапазона ядерная сила (также известный как остаточный сильная сила) представлен ядра гало Такие как литий-11 или бор-14, в котором динейтроны, или другие скопления нейтронов, орбита на расстояниях около 10 фм (примерно похоже на 8 фм радиус ядра урана-238). Эти ядра не являются максимально плотными. Ядра гало образуются на крайних краях диаграммы нуклидов - нейтронной и протонной - и все они нестабильны с короткими периодами полураспада, измеряемыми в миллисекунды; например, литий-11 имеет период полураспада 8,8 мс .
Ядерные модели
Хотя стандартная модель физики, как широко считается, полностью описывают состав и поведение ядра, делать предсказания на основе теории гораздо труднее, чем для большинства других областей физика элементарных частиц. Это связано с двумя причинами:
- В принципе, физика ядра может быть полностью выведена из квантовая хромодинамика (QCD). Однако на практике современные вычислительные и математические подходы к решению КХД в низкоэнергетических системах, таких как ядра, чрезвычайно ограничены. Это связано с фаза перехода что происходит между высокоэнергетическими кварк материя и низкоэнергетические адронный материя, которая оказывает пертурбативные техники непригодным для использования, что затрудняет построение точной модели силы между нуклонами. Современные подходы ограничиваются либо феноменологическими моделями, такими как потенциал Аргонна v18, либо киральная эффективная теория поля. [17]
- Даже если ядерное взаимодействие хорошо ограничено, для точного вычисления свойств ядер требуется значительная вычислительная мощность. ab initio. События в теория многих тел сделали это возможным для многих маломассивных и относительно стабильных ядер, но необходимы дальнейшие улучшения как в вычислительной мощности, так и в математических подходах, прежде чем можно будет заняться тяжелыми ядрами или очень нестабильными ядрами.
Исторически эксперименты сравнивали с относительно грубыми моделями, которые неизбежно несовершенны. Ни одна из этих моделей не может полностью объяснить экспериментальные данные о структуре ядра. [18]
В ядерный радиус (р) считается одной из основных величин, которую должна предсказывать любая модель. Для стабильных ядер (не ядер гало или других нестабильных искаженных ядер) ядерный радиус примерно пропорционален кубическому корню из массовое число (А) ядра, особенно в ядрах, содержащих много нуклонов, поскольку они располагаются в более сферических конфигурациях:
Стабильное ядро имеет приблизительно постоянную плотность, и поэтому радиус ядра R можно аппроксимировать следующей формулой:
Другими словами, упаковка протонов и нейтронов в ядре дает примерно тот же общий размер получается при упаковке твердых сфер постоянного размера (например, шариков) в плотный сферический или почти сферический мешок (некоторые стабильные ядра не совсем сферические, но, как известно, вытянутый). [20]
Модель жидкой капли
Члены полуэмпирической формулы массы, которые можно использовать для аппроксимации энергии связи многих ядер, рассматриваются как сумма пяти типов энергий (см. Ниже). Тогда картина ядра как капли несжимаемой жидкости примерно объясняет наблюдаемое изменение энергии связи ядра:
Объемная энергия. Когда совокупность нуклонов одинакового размера упаковывается в наименьший объем, каждый внутренний нуклон имеет определенное количество других нуклонов, контактирующих с ним. Итак, эта ядерная энергия пропорциональна объему.
Поверхностная энергия. Нуклон на поверхности ядра взаимодействует с меньшим количеством других нуклонов, чем нуклон внутри ядра, и, следовательно, его энергия связи меньше. Этот член поверхностной энергии учитывает это, поэтому он отрицателен и пропорционален площади поверхности.
Кулон Энергия. Электрическое отталкивание между каждой парой протонов в ядре способствует уменьшению его энергии связи.
Асимметрия энергии (также называемый Паули Энергия). Энергия, связанная с Принцип исключения Паули. Если бы не кулоновская энергия, наиболее стабильная форма ядерной материи имела бы такое же количество нейтронов, что и протоны, поскольку неравное количество нейтронов и протонов подразумевает заполнение более высоких уровней энергии для одного типа частиц, в то время как более низкие уровни энергии остаются вакантными для другой тип.
Парная энергия. Энергия, которая представляет собой поправочный член, возникающий из-за тенденции появления пар протонов и пар нейтронов. Четное число частиц более стабильно, чем нечетное.
Модели оболочек и другие квантовые модели
В приведенных выше моделях нуклоны могут занимать орбитали парами, так как они являются фермионами, что позволяет объяснить даже странно Z и N последствия хорошо известно из экспериментов. Точная природа и емкость ядерных оболочек отличаются от таковых электронов на атомных орбиталях, прежде всего потому, что потенциальная яма, в которой движутся нуклоны (особенно в более крупных ядрах), сильно отличается от центральной электромагнитной потенциальной ямы, которая связывает электроны в атомах. Некоторое сходство с моделями атомной орбиты можно увидеть в небольшом атомном ядре, таком как ядро гелий-4, в котором два протона и два нейтрона по отдельности занимают 1s-орбитали, аналогичные 1s-орбитали для двух электронов в атоме гелия, и достигают необычной стабильности по той же причине. Ядра с пятью нуклонами крайне нестабильны и недолговечны, однако, гелий-3с 3 нуклонами очень устойчива даже при отсутствии замкнутой орбитальной оболочки 1s. Еще одно ядро с тремя нуклонами, тритон водород-3 нестабилен и при изоляции распадается на гелий-3. Слабая ядерная стабильность с двумя нуклонами на 1s-орбитали обнаружена в дейтроне. водород-2, с одним нуклоном в каждой из протонных и нейтронных потенциальных ям. В то время как каждый нуклон является фермионом, дейтрон является бозоном и, следовательно, не следует исключению Паули для плотной упаковки внутри оболочки. Литий-6 с 6 нуклонами очень стабильна без замкнутой второй орбитали оболочки 1p. Для легких ядер с полным числом нуклонов от 1 до 6 только ядра с числом 5 не демонстрируют каких-либо признаков стабильности. Наблюдения бета-стабильности легких ядер вне закрытых оболочек показывают, что ядерная стабильность намного сложнее, чем простое замыкание оболочечных орбиталей с помощью магические числа протонов и нейтронов.
Для более крупных ядер оболочки, занятые нуклонами, начинают значительно отличаться от электронных оболочек, но, тем не менее, современная ядерная теория предсказывает магические числа заполненных ядерных оболочек как для протонов, так и для нейтронов. Закрытие стабильных оболочек предсказывает необычно стабильные конфигурации, аналогичные благородной группе почти инертных газов в химии. Примером может служить устойчивость замкнутой оболочки из 50 протонов, что позволяет банка иметь 10 стабильных изотопов, больше, чем любой другой элемент. Точно так же расстояние от закрытия оболочки объясняет необычную нестабильность изотопов, которые имеют далеко не стабильное количество этих частиц, таких как радиоактивные элементы 43 (технеций) и 61 (прометий), каждому из которых предшествует и следует 17 или более стабильных элементов.
Однако существуют проблемы с моделью оболочек, когда делается попытка учесть ядерные свойства вдали от закрытых оболочек. Это привело к сложному постфактум искажения формы потенциальной ямы, чтобы соответствовать экспериментальным данным, но остается вопрос, действительно ли эти математические манипуляции соответствуют пространственным деформациям в реальных ядрах. Проблемы с оболочечной моделью привели к тому, что некоторые предложили реалистичные двух- и трехчастичные ядерные силовые эффекты с участием кластеров нуклонов, а затем на этой основе построили ядро. Три таких кластерных модели - это модель 1936 г. Резонирующая структура группы модель Джона Уиллера Модель плотноупакованного сферона Линуса Полинга и 2D модель Изинга МакГрегора. [18]
Согласованность между моделями

Большая часть массы всех элементов на Земле сосредоточена в элементарных частицах, называемых протонами и нейтронами (общее название – нуклоны). Поговорим кратко о протонах и нейтронах в составе атомных ядер.
Протоны и нейтроны
В самом начале XXв в опытах Э. Резерфорда было установлено, что практически вся масса и положительный заряд атома сосредоточен в компактном ядре. Вокруг ядра по весьма далеким (по отношению к размеру ядра) орбитам вращаются электроны. Атом в целом нейтрален, потому, что заряд электронов и ядра одинаков.
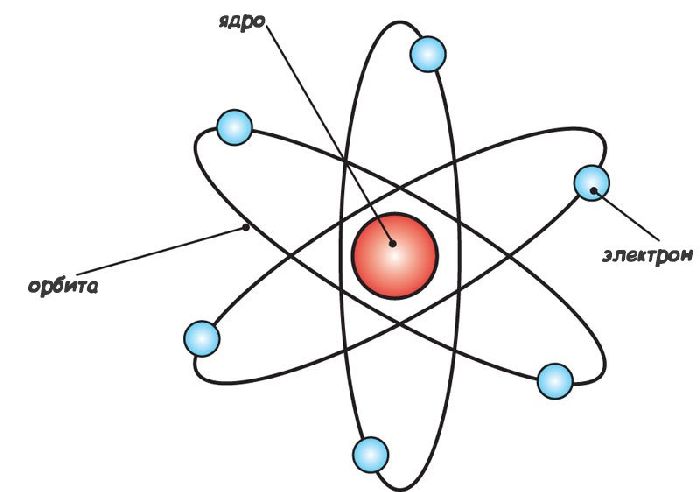
Рис. 1. Планетарная модель атома.
Дальнейшие опыты Э. Резерфорда привели в 1919 г к открытию протона, и к пониманию, что весь положительный заряд ядра обеспечивается наличием в его составе протонов. Протон – это достаточно тяжелая частица, тяжелее электрона в 1830 раз, что примерно равно одной атомной единице массы. Его положительный заряд по модулю равен заряду электрона. Ядро самого легкого элемента – водорода – имеет единичный заряд, и состоит из одного протона, вокруг которого обращается один электрон.
В 1930 году Д. Чедвиком был открыт нейтрон. Это еще одна элементарная частица, почти с такой же массой, как у протона, но не имеющая заряда, и входящая в состав ядер.
Ядерные Силы
Возникает вопрос – если протоны обеспечивают положительный заряд ядра, то почему существуют ядра элементов с зарядом больше единицы ? Ведь протоны, заряженные одинаково, должны отталкиваться друг от друга!
Нуклоны удерживает вместе особое Сильное (или ядерное) взаимодействие. Особенность ядерного взаимодействия в том, что его переносчики (глюоны и составленные из них пионы) – не только переносят сильное взаимодействие, но и сами в нем участвуют. Поэтому они не могут далеко удаляться друг от друга, и радиус действия ядерных сил не превышает размеры ядер. Эти силы значительно больше кулоновских сил отталкивания, и поэтому ядра, содержащие много положительных протонов стабильны.
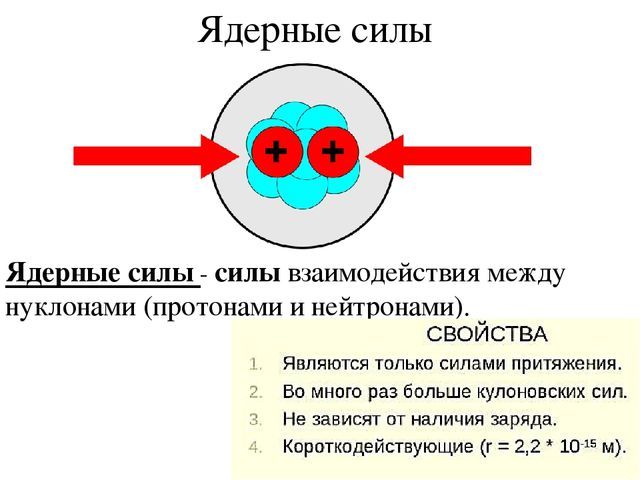
Рис. 2. Ядерные силы.
Эти же силы определяют стабильность нейтрона в составе ядер. Свободный нейтрон – это нестабильная частица с периодом полураспада около 600 сек. Ядерные взаимодействия делают распад нейтрона в ядрах с малым их числом $N$ энергетически невыгодным.
Протонно-нейтронная модель ядра
Таким образом, в состав атомного ядра входят протоны и нейтроны, которые удерживаются вместе короткодействующим Сильным взаимодействием. Число протонов в ядре $Z$ соответствует номеру элемента в Периодической Системе Менделеева. Общее число нуклонов в ядре $A$ соответствует массовому числу элемента:
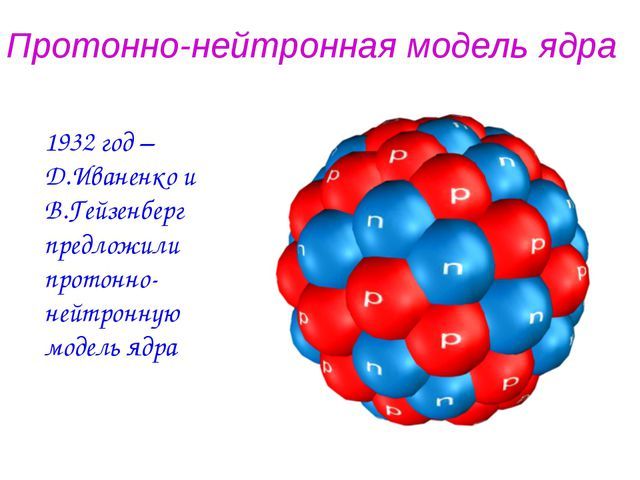
Рис. 3. Протонно-нейтронная модель ядра.
Чем больше протонов в ядре – тем больше силы кулоновского отталкивания, и тем менее стабильно ядро. Наличие $N$ нейтронов в ядре стабилизирует его.
Для тяжелых элементов, содержащих в ядре много протонов, число нейтронов должно быть еще больше. Так, например, ядро наиболее распространенного в природе свинца-208 содержит 82 протона и 126 нейтронов. Однако, если число нейтронов становится слишком большим, становится энергетически выгоден распад нейтрона, а с распадом нейтрона уменьшаются ядерные силы, и ядро распадается. Именно поэтому наиболее стабильными являются ядра со средним числом нейтронов и протонов.
Что мы узнали?
Ядро атома состоит из элементарных частиц – протонов и нейтронов, которые удерживаются вместе особыми ядерными силами. Число протонов в ядре соответствует номеру элемента в Периодической системе. Общее число нуклонов – соответствует массовому числу.

Из этого видеоурока учащиеся узнают, из каких частиц состоит атомное ядро. Познакомятся с протонно-нейтронной моделью строения атомного ядра. Узнают, какие силы удерживают протоны и нейтроны в ядрах атомов. А также мы поговорим об обменной модели ядерного взаимодействия.

В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобретя в каталоге.
Получите невероятные возможности



Конспект урока "Строение атомного ядра. Ядерные силы"
На одном из прошлых уроков мы с вами рассматривали опыты Резерфорда по рассеиванию альфа-частиц, на основании которых им была предложена ядерная модель атома. Согласно ей, в центре атома находится положительно заряженное ядро, в котором сосредоточена практически вся масса атома, а вокруг ядра по замкнутым траекториям вращаются электроны. Однако ещё долгое время для учёных оставался загадкой состав атомного ядра, хотя к 20-годам ХХ века физики уже не сомневались в том, что ядра атомов, как и сами атомы, имеют сложную структуру.
В настоящее время твёрдо установлено, что атомные ядра различных элементов состоят из частиц двух видов −− протонов и нейтронов. Но обо всём по порядку.
Итак, первым, кто выдвинул теорию о том, что в состав ядер атомов всех химических элементов входит ядро атома водорода, был Эрнест Резерфорд. Он также дал название этой частице — протон, что в переводе с греческого означало первый, основной. Основанием для такого предположения стало то, что массы атомов химических элементов превышают массу атома водорода в целое число раз. Чтобы подтвердить своё предположение Резерфорд в 1919 году поставил опыт по исследованию взаимодействия ядра атома азота с альфа-частицей.
Прибор Резерфорда состоял из вакуумированной камеры, в которой был расположен контейнер с источником альфа-частиц. Окно камеры было закрыто металлической фольгой, толщина которой подбиралась так, чтобы альфа-частицы не могли через неё проникнуть. За окном располагался экран, покрытый сернистым цинком. С помощью микроскопа можно было наблюдать сцинтилляции (световые вспышки) в точках попадания на экран тяжёлых заряженных частиц.
При заполнении камеры азотом низкого давления на экране возникали световые вспышки, указывающие на появление потока каких-то частиц, проникающих через фольгу, практически полностью задерживающую альфа-частицы.
Исследования действия на частицы, выбиваемые из ядер азота, электрических и магнитных полей показали, что они обладают положительным элементарным зарядом и их масса равна массе ядра атома водорода:
Такое совпадение зарядов двух не похожих друг на друга частиц — протона и электрона, вызывает удивление и остаётся одной из фундаментальных загадок современной физики.
Впоследствии опыт был выполнен с целым рядом других газообразных веществ. Во всех случаях было обнаружено, что из их ядер альфа-частицы выбивают протоны. Таким образом, показано, что протоны входят в состав ядер атомов.
А так, как атом в целом электрически нейтрален, то число протонов в ядре равно числу электронов в атомной оболочке, которое определяется порядковым номером элемента в периодической системе элементов Менделеева. Его мы с вами будем называть зарядовым числом и обозначать большой латинской буквой Z. Ставится зарядовое число внизу перед буквенным обозначением элемента.
После открытия протона было высказано предположение, что ядра атомов состоят только из них. Однако оно оказалось несостоятельным, так как отношение заряда ядра к его массе не остаётся постоянным для разных ядер, как это было бы, если бы в состав ядер входили одни протоны.
Более того, при переходе к тяжёлым ядрам масса ядра растёт быстрее, чем его заряд. В связи с этим в 1920 году Эрнест Резерфорд высказал гипотезу о существовании в составе ядер жёстко связанной компактной протон-электронной пары, представляющей собой электрически нейтральное образование — частицу с массой, приблизительно равной массе протона. Он даже придумал название этой гипотетической частице — нейтрон. Это была очень красивая, но, как выяснилось впоследствии, ошибочная идея, так как было доказано, что электрон не может входить в состав атомного ядра.
Однако идея о существовании тяжёлой нейтральной частицы казалась Резерфорду настолько привлекательной, что он незамедлительно предложил группе своих учеников во главе с Джеймсом Чедвиком заняться её поиском. Лишь через 12 лет, в 1932 году, Чедвику удалось найти эту частицу.
Оказалось, что при облучении бериллия альфа-частицами возникает сильное проникающее излучение, способное преодолеть слой свинца толщиной до 20 см и не ионизирующее газ в счётчике Гейгера.
Так был открыт нейтрон — тяжёлая элементарная частица, не имеющая электрического заряда, с массой, практически равной массе протона:
Дальнейшие изучения свойств нейтронов показали, что они устойчивы только в ядре. В свободном же состоянии, то есть в не ядра, в течение примерно четырнадцати минут и сорока двух секунд нейтрон распадается на протон, электрон и электронное антинейтрино — нейтральную частицу.
Практически сразу же после открытия нейтрона советским физиком Дмитрием Иваненко и немецким учёным Вернером Гейзенбергом была предложена протонно-нейтронная модель строения атомного ядра, которая полностью подтвердилась последующими исследованиями.
Согласно этой модели, ядра всех химических элементов (за исключением водорода) состоят из двух видов частиц: протонов и нейтронов.
Общее число нуклонов в ядре называют массовым числом и обозначают латинской буквой А. Оно ставится вверху перед буквенным обозначением химического элемента.
Из-за малости масс частиц в ядерной физике массовое число принято выражать не в килограммах, а в атомных единицах массы (сокращённо, а. е. м.) и округлять до целых чисел. Одна атомная единица массы (1 а. е. м.) равна 1/12 части массы атома углерода, что составляет порядка 1,66 ∙ 10 –27 кг.
Число нейтронов в ядре обозначают большой латинской буквой N. Нетрудно догадаться, что оно равно разнице между массовым и зарядовым числами:
N = A – Z.
В общем случае любой химический элемент периодической таблицы Менделеева можно представить в виде символа Z A X, где под иксом подразумевается символ химического элемента.
Следует обратить внимание на то, что плотность ядерного вещества не зависит от размеров ядра, так как объем ядра пропорционален массовому числу.
Отметим также то, что в ядрах одного химического элемента всегда содержится одно и то же количество протонов, а число нейтронов может быть различным. Например, в ядрах атома лития всегда содержится три протона, а вот число нейтронов колеблется от одного до десяти.
Из всех известных на сегодняшний день изотопов (а они есть у всех химических элементов) только изотопы водорода имеют свои названия.
На основании многих экспериментов было установлено, что изотопы одинаково вступают в химические реакции и образуют одинаковые соединения. Это говорило о том, что химические свойства элементов определяются не атомной массой, а зарядовым числом ядра. Действительно, например, нуклиды трития () и гелия два-три () имеют близкие по величине атомные массы, но принципиально разные химические свойства.
Предложенная Иваненко и Гейзенбергом протонно-нейтронная модель строения ядра впоследствии была полностью подтверждена экспериментально и в настоящее время является общепризнанной. Однако эта модель породила ряд новых противоречий. Дело в том, между протонами, находящимися в ядре атома, действуют огромные силы электростатического отталкивания — порядка 230 Н, что, согласить, слишком много для частиц с массой порядка 10 –27 кг.
Причина устойчивости ядра кроется в существовании, кроме сил электростатического отталкивания между протонами, ядерных сил притяжения между нуклонами, которые примерно в 100 раз превышают кулоновские силы. Это самые мощные силы из всех сил, существующих в природе. Вследствие этого они представляют собой проявление самого интенсивного из всех известных в физике видов взаимодействия — так называемого сильного взаимодействия.
Важной особенностью ядерных сил является их короткодействие: они заметно проявляются лишь на расстояниях, сравнимых с размерами ядра (10 –13 — 10 –12 см). На бо́льших расстояниях преобладает действие сравнительно медленно убывающих кулоновских сил.
Многочисленные опытные данные также показали, что ядерные силы не являются центральными, а также то, что им присуща зарядовая независимость, то есть протоны и нейтроны в ядре взаимодействуют между собой и друг с другом совершенно одинаково.
Ядерные силы обладают и свойством насыщения. Иными словами, каждый нуклон в ядре взаимодействует не со всеми нуклонами ядра, а с их конечным числом — ближайшими соседями.
Ещё одной важной особенностью ядерных сил является то, что они являются так называемыми обменными силами. Они имеют квантовый характер, поэтому у них нет аналога в обычной физике.
Взаимодействие между нуклонами возникает вследствие обмена между ними некоторой третьей виртуальной частицей. Названа она была так, из-за того, что время её жизни чрезвычайно мало. Вследствие этого она не может быть обнаружена экспериментально.
В результате многолетних исследований в космическом излучении в 1947 году были обнаружены частицы, которые могут реализовать ядерное взаимодействие.
Их назвали π-мезонами или пионами. Их изучение показало, что масса пионов примерно в 280 раз больше массы электрона. Помимо этого, было обнаружено, что существует три вида пи-мезонов: положительные и отрицательные, время жизни которых порядка 26 нс и нейтральные, время жизни которых около 8,5 ∙ 10 –17 с. Таким образом, взаимодействие между однородными нуклонами осуществляется нейтральными пионами, а взаимодействие между различными нуклонами — заряженными π-мезонами.
АТОМНОГО ЯДРА СТРОЕНИЕ. Ядро представляет собой центральную часть атома (см. также АТОМА СТРОЕНИЕ). В нем сосредоточены положительный электрический заряд и основная часть массы атома; по сравнению с радиусом электронных орбит размеры ядра чрезвычайно малы: 10 –15 –10 –14 м. Ядра всех атомов состоят из протонов и нейтронов, имеющих почти одинаковую массу, но лишь протон несет электрический заряд. Полное число протонов называется атомным номером Z атома, который совпадает с числом электронов в нейтральном атоме. Ядерные частицы (протоны и нейтроны), называемые нуклонами, удерживаются вместе очень большими силами; по своей природе эти силы не могут быть ни электрическими, ни гравитационными, а по величине они на много порядков превышают силы, связывающие электроны с ядром.
Первое представление об истинных размерах ядра давали опыты Резерфорда по рассеянию альфа-частиц в тонких металлических фольгах. Частицы глубоко проникали сквозь электронные оболочки и отклонялись, приближаясь к заряженному ядру. Эти опыты явно свидетельствовали о малых размерах центрального ядра и указали на способ определения ядерного заряда. Резерфорд установил, что альфа-частицы приближаются к центру положительного заряда на расстояние примерно 10 –14 м, а это позволило ему сделать вывод, что таков максимально возможный радиус ядра.
На основе таких предположений Бор построил свою квантовую теорию атома, успешно объяснившую дискретные спектральные линии, фотоэффект, рентгеновское излучение и периодическую систему элементов. Однако в теории Бора ядро рассматривалось как положительный точечный заряд.
Ядра большинства атомов оказались не только очень малы – на них никак не действовали такие средства возбуждения оптических явлений, как дуговой искровой разряд, пламя и т.п. Указанием на наличие некой внутренней структуры ядра явилось открытие в 1896 А.Беккерелем радиоактивности. Оказалось, что уран, а затем и радий, полоний, радон и т.п. испускают не только коротковолновое электромагнитное излучение, рентгеновское излучение и электроны (бета-лучи), но и более тяжелые частицы (альфа-лучи), а они могли исходить лишь из массивной части атома. Резерфорд использовал альфа-частицы радия в своих опытах по рассеянию, которые послужили основой формирования представлений о ядерном атоме. (В то время было известно, что альфа-частицы – это атомы гелия, лишенные своих электронов; но на вопрос – почему некоторые тяжелые атомы спонтанно испускают их, ответа еще не было, как не было и точного представления о размерах ядра.)
Открытие изотопов.
Сравнивая на своем масс-спектрографе массу атома неона с известными массами других элементов, Томсон в 1912 неожиданно обнаружил, что неону вместо одной соответствуют две параболы. Расчеты масс частиц показали, что одна из парабол отвечает частицам с массой 20, а другая – с массой 22. Это явилось первым свидетельством того, что атомы определенного химического элемента могут иметь различные массовые числа. Поскольку измеренное (среднее) массовое число оказалось равным 20,2, Томсон высказал предположение, что неон состоит из атомов двух типов, на 90% с массой 20 и на 10% с массой 22. Поскольку оба типа атомов в природе существуют в виде смеси и их нельзя разделить химическим путем, массовое число неона оказывается равным 20,2.
Наличие двух типов атомов неона наводило на мысль о том, что и другие элементы могут представлять собой смеси атомов. Последующие масс-спектрометрические измерения показали, что большинство природных элементов представляют собой смеси от двух до десяти различных сортов атомов. Атомы одного и того же элемента с различной массой называют изотопами. У некоторых элементов существует только один изотоп, что требовало теоретического объяснения, как и факт разной распространенности элементов, а также существование радиоактивности лишь у определенных веществ.
Отметим, что в атомную единицу массы входит масса одного электрона, а масса самого легкого изотопа водорода почти на 1% больше 1 а.е.м.
Открытие нейтрона.
Открытие изотопов не прояснило вопрос о строении ядра. К этому времени были известны лишь протоны – ядра водорода и электроны, а потому естественной была попытка объяснить существование изотопов различными комбинациями этих положительно и отрицательно заряженных частиц. Можно было бы думать, что ядра содержат А протонов, где А – массовое число, и А - Z электронов. При этом полный положительный заряд совпадает с атомным номером Z.
Лишь спустя десятилетие, после того как естественная радиоактивность была глубоко исследована, а радиоактивное излучение стали широко применять, чтобы вызывать искусственное превращение атомов, было надежно установлено существование новой составной части ядра. В 1930 В.Боте и Г.Беккер из Гисенского университета проводили облучение лития и бериллия альфа-частицами и с помощью счетчика Гейгера регистрировали возникающее при этом проникающее излучение. Поскольку на это излучение не оказывали влияния электрические и магнитные поля и оно обладало большой проникающей способностью, авторы пришли к выводу, что испускается жесткое гамма-излучение. В 1932 Ф.Жолио и И.Кюри повторили опыты с бериллием, пропуская такое проникающее излучение через парафиновый блок. Они обнаружили, что из парафина выходят протоны с необычно высокой энергией, и заключили, что, проходя через парафин, гамма-излучение в результате рассеяния порождает протоны. (В 1923 было установлено, что рентгеновские лучи рассеиваются на электронах, давая комптоновский эффект.)
Дж.Чедвик повторил эксперимент. Он также использовал парафин и с помощью ионизационной камеры (рис. 1), в которой собирался заряд, возникающий при выбивании электронов из атомов, измерял пробег протонов отдачи.
Чедвик использовал также газообразный азот (в камере Вильсона, где вдоль следа заряженной частицы происходит конденсация водяных капелек) для поглощения излучения и измерения пробега атомов отдачи азота. Применив к результатам обоих экспериментов законы сохранения энергии и импульса, он пришел к выводу, что обнаруженное нейтральное излучение – это не гамма-излучение, а поток частиц с массой, близкой к массе протона. Чедвик показал также, что известные источники гамма-излучения не выбивают протонов.
Тем самым было подтверждено существование новой частицы, которую теперь называют нейтроном. Расщепление металлического бериллия происходило следующим образом:
Альфа-частицы 4 2He (заряд 2, массовое число 4) сталкивались с ядрами бериллия (заряд 4, массовое число 9), в результате чего возникали углерод и нейтрон.
Открытие нейтрона явилось важным шагом вперед. Наблюдаемые характеристики ядер теперь можно было интерпретировать, рассматривая нейтроны и протоны как составные части ядер. На рис. 2 схематически показана структура нескольких легких ядер.
Нейтрон, как теперь известно, на 0,1% тяжелее протона. Свободные нейтроны (вне ядра) претерпевают радиоактивный распад, превращаясь в протон и электрон. Это напоминает о первоначальной гипотезе составной нейтральной частицы. Однако внутри стабильного ядра нейтроны связаны с протонами и самопроизвольно не распадаются.
Ядерная связь.
Первоначальное предположение Праута о том, что все атомные массы должны быть целыми кратными массы атома водорода, очень близко к истине, в частности, применительно к изотопам. Отклонения крайне малы, всегда не более 1%, а в большинстве случаев не более 0,1%. Детальное изучение масс изотопов доведено до высочайшей степени совершенства: погрешность измерения в настоящее время, как правило, не превышает нескольких миллионных.
Установлено, что число нейтронов примерно совпадает с числом протонов в атоме, т.е.
В действительности в более тяжелых ядрах имеется некоторый избыток нейтронов. Поскольку нейтрон не заряжен, силы, удерживающие нейтроны и протоны в ядре, по своей природе не являются электростатическими; кроме того, одноименные заряды отталкиваются. То обстоятельство, что ядра очень трудно расщепить, указывает на существование больших сил ядерного притяжения. Несмотря на малость расстояний, гравитационное притяжение между нуклонами все же слишком слабо, чтобы обеспечить стабильность ядра.
Согласно Эйнштейну, полная энергия изолированной системы сохраняется, а масса является одной из форм энергии: E = mc 2 . Чтобы расщепить такую связанную систему, как ядро стабильного атома, на составляющие ее нейтроны и протоны, ей необходимо сообщить энергию. Это означает, что масса нейтронов и протонов превышает массу ядра на величину
где Mp и Mn – массы свободного протона и нейтрона, а MA,Z – масса ядра с зарядом Z и массовым числом А. Эта разница масс, выраженная в единицах энергии, называется энергией связи. Коэффициент для пересчета таков:
1 а.е.м. = 931,14 МэВ,
где 1 МэВ = 10 6 эВ. Таким образом, энергия связи EB = D Mc 2 есть энергия, необходимая для расщепления ядра на отдельные нейтроны и протоны.
Средняя энергия связи, приходящаяся на один нуклон, EB/A, довольно регулярно изменяется с увеличением числа нуклонов в ядре (рис. 3). Самым легким ядром после протона является дейтрон 2 1H, расщепление которого требует энергии 2,2 МэВ, т.е. 1,1 МэВ на нуклон. Альфа-частица 4 2He связана гораздо сильнее, чем ее соседи: ее энергия связи составляет 28 МэВ. У ядер с массовым числом, превышающим 20, средняя энергия связи, приходящаяся на нуклон, остается почти постоянной, равной примерно 8 МэВ.
Энергия связи ядер на много порядков величины превышает энергию связи валентных электронов в атоме и атомов в молекуле. Чтобы удалить из атома водорода его единственный электрон, достаточно энергии 13,5 эВ; для удаления же внутренних электронов в свинце, связанных наиболее прочно, необходима энергия, равная 0,1 МэВ. Следовательно, все ядерные процессы связаны с энергиями, значительно превышающими те, с которыми мы имеем дело в обычных химических реакциях или при обычных температурах и давлениях.
Естественная радиоактивность.
С явления естественной радиоактивности началась ядерная физика. Альфа-, бета- и гамма-излучения, испускаемые ураном, имеют ядерное происхождение, тогда как оптические и рентгеновские спектры соответствуют электронной структуре атома. Альфа-частицы оказались ядрами гелия. Бета-частицы по своему заряду и массе идентичны электронам оболочки атома, однако их ядерное происхождение было четко продемонстрировано изменением заряда распадающегося ядра. Кроме того, энергия гамма-излучения значительно превышает энергию, которую могут излучать электроны из внешней оболочки атома, следовательно, это проникающее излучение имеет ядерное происхождение.
Важная роль радиоактивности в физике ядра связана с тем, что радиоактивное излучение несет информацию о типах частиц и энергетических уровней ядра. Например, испускание альфа-частиц из ядра и относительная устойчивость образования из двух протонов и двух нейтронов косвенно указывает на возможность существования альфа-частиц внутри ядра.
Различие между естественной и искусственно наведенной радиоактивностью не очень существенно для понимания строения ядра, однако изучение естественных радиоактивных рядов позволило сделать важные выводы относительно возраста Земли и использовать такие элементы в качестве источников бомбардирующих частиц задолго до того, как были изобретены ускорители частиц.
Искусственные превращения ядер.
Опыты с естественно радиоактивными элементами показали, что на скорость радиоактивного распада нельзя повлиять обычными физическими средствами: теплом, давлением и т.п. Таким образом, поначалу казалось, что нет какого-либо эффективного метода исследования структуры естественно стабильных изотопов. Однако в 1919 Резерфорд обнаружил, что ядра можно расщеплять, бомбардируя их альфа-частицами. Первым расщепленным элементом был азот, который в виде газа заполнял камеру Вильсона. Альфа-частицы, испускаемые ториевым источником, сталкивались с ядрами азота, поглощались ими, в результате чего испускались быстрые протоны. При этом происходила реакция
В результате такой реакции атом азота превращается в атом кислорода. В этом примере энергии связи ядер аналогичны теплу, которое выделяется при химической реакции, хотя и значительно превышают его. Впоследствии аналогичные результаты были получены и с многими другими элементами. Используя различные методы, можно измерить энергии и углы вылета испускаемых заряженных частиц, что обеспечивает проведение количественных экспериментов.
Следующим шагом явилось открытие, сделанное Дж.Кокрофтом и Э.Уолтоном в 1932. Они установили, что искусственно ускоренные пучки протонов с энергией 120 кэВ (т.е. значительно меньшей, чем у альфа-частиц в опытах Резерфорда) способны вызывать расщепление атомов лития в процессе
Два ядра гелия (альфа-частицы) одновременно вылетают в противоположные стороны. Причина, по которой эта реакция протекает при низкой энергии, заключается в прочной связи альфа-частиц; при добавлении протона к массе ядра 7 Li сообщается энергия, которая почти равнозначна массам двух альфа-частиц. Остальная энергия, необходимая для протекания реакции, черпается из кинетической энергии бомбардирующих протонов.
Энергетические уровни ядер и ядерные модели.
Изучение ядерных реакций убедительно продемонстрировало существование энергетических уровней ядер. Эти уровни представляют собой состояния ядра с определенной энергией, которым приписаны определенные квантовые числа, как и энергетическим уровням атома (см. также АТОМА СТРОЕНИЕ). По аналогии с оптической спектроскопией исследование излучений, испускаемых ядром при переходах между энергетическими уровнями, называется ядерной спектроскопией. Однако, как можно видеть из рис. 4, расстояние между энергетическими уровнями ядер значительно больше, чем между электронными уровнями атомов, а к ядерным излучениям, кроме электромагнитного, относятся также излучения электронов, протонов, альфа-частиц и частиц других типов.
О существовании у ядра дискретных энергетических уровней свидетельствует то, что возбуждение ядра, приводящее к испусканию излучения, происходит лишь при определенных энергиях бомбардирующих частиц, а также то, что энергии испускаемых частиц соответствуют переходам между определенными уровнями. Например, можно измерить число протонов, образующихся при бомбардировке бора-10 моноэнергетическими дейтронами в результате реакции
В 1932 Дж.Бартлетт заметил, что все стабильные ядра, расположенные между 4 He и 16 О, относятся к последовательности
4 He + n + p + n + p +.
тогда как между 16 О и 36 Аr аналогичная последовательность приобретает вид
16 O + n + n + p + p + n + n +.
Составное ядро и модель капли.
Размеры и форма ядра.
Впервые размеры ядра правильно оценил Резерфорд, использовав для этой цели рассеяние альфа-частиц. Его первые эксперименты показали, что размеры заряженной части ядра – порядка 10 –14 м. Более поздние и более точные эксперименты позволили установить, что радиус ядра приблизительно пропорционален А 1/3 и, следовательно, плотность ядерного вещества почти постоянна. (Она колоссальна: 100 000 т/мм 3 .)
С открытием нейтрона стало ясно, что он представляет собой идеальное средство исследования ядра, поскольку нейтральные частицы, проходя на значительном удалении от ядра, не испытывают отклонения под действием заряда ядра. Другими словами, нейтрон сталкивается с ядром, если расстояние между их центрами оказывается меньше суммы их радиусов, а в противном случае не отклоняется. Опыты по рассеянию пучка нейтронов показали, что радиус ядра (в предположении сферической формы) равен:
R = r0A 1/3 ,
Ядерные силы и мезоны.
Хотя существование пи-мезонов и ободрило сторонников теории Юкавы, на ее основе оказалось весьма трудно правильно предсказать такие детальные свойства ядерных сил, как их насыщение, энергии связи и энергии ядерных уровней. Трудности математического характера не позволили точно установить, что именно предсказывает эта теория. Ситуация еще более усложнилась после открытия новых типов мезонов, которые, как считается, имеют отношение к ядерным силам. См. также МОМЕНТЫ АТОМОВ И ЯДЕР; УСКОРИТЕЛЬ ЧАСТИЦ; ЧАСТИЦЫ ЭЛЕМЕНТАРНЫЕ; РАДИОАКТИВНОСТЬ.
Айзенбуд Л., Вигнер Е. Структура ядра. М., 1959
Престон М. Физика ядра. М., 1964
Кук Ш. Структура атомных ядер. М., 1967
Лейн А. Теория ядра. М., 1967
Федянин В. К. Электромагнитная структура ядер и нуклонов. М., 1967
Широков Ю.М., Юдин Н.П. Ядерная физика. М., 1980
Робертсон Б. Современная физика в прикладных науках. М., 1985
Читайте также:

