В чем отличие между молекулами горячей и холодной воды кратко
Обновлено: 02.07.2024
Молекулярная структура воды уникальна. Удивительным образом здесь сочетается несочетаемое: подвижность жидкого вещества и прочный кристаллический материал, который мы называем льдом. Разумеется, молекулы меняются в различных агрегатных состояниях: газообразном, твердом и жидком.
Сегодня подробно расскажем про строение молекул воды, которая оказывает столь важное влияние на все живое на планете и на само качество нашей жизни.
Молекулярная структура воды
Длительный период времени ученые описывали молекулярную структуру воды простым соединением без возможности комплексных взаимодействий с другими веществами. И наконец, вода была поставлена в один ряд со сложными веществами химиком Лавуазье в 1783 г.
Молекулярный состав воды определяется тремя атомами; из них два атома водорода и один атом кислорода, имеющие между собой ковалентную связь.
Химическая формула воды: H₂O.
Основные характеристики ковалентной связи выражены такими понятиями, как направленность, насыщаемость, полярность, поляризуемость. Эти параметры являются химическими и физическими свойствами соединений.
Форма молекулы воды похожа на равнобедренный треугольник с двумя атомами водорода в основании (по одному атому в каждом углу). Между атомами кислорода и водорода наблюдается полярная связь, которая объясняется свойством кислорода сильнее (по сравнению с водородом) притягивать электроны.
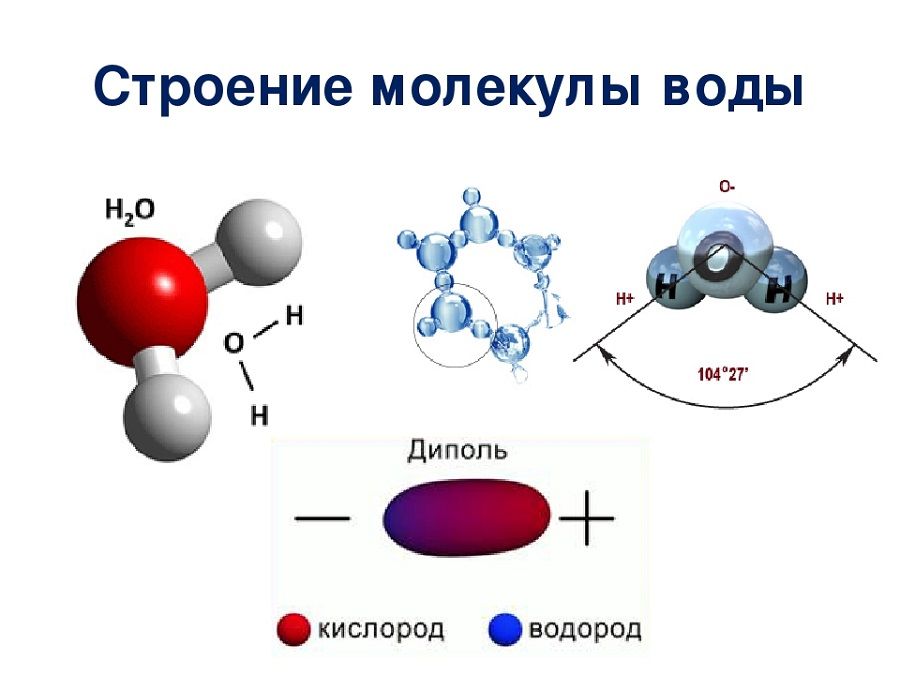
Молекулярная структура воды
Межъядерные расстояния О—Н близки к 0,1 нм, расстояние между ядрами атомов водорода равно 0,15 нм, угол между связями Н—О—Н равен 104,5°.
Молекулярная структура воды подразумевает наличие двух положительно и двух отрицательно заряженных полюса, этим можно объяснить ее проявление в качестве диполя (в большинстве случаев).
Показатели эффективных зарядов на атомах равны ±0,17 от заряда электрона.
Наличие водородной связи наделяет воду в жидком состоянии свойством осуществлять ассоциацию молекул (соединять их в сложные вещества).
Особое внимание водородная связь заслужила благодаря своей не сильно высокой устойчивости.
Кроме того, водородная связь оказывает прямое влияние на способность воды растворять вещества, так как конкретно от соединения водородных связей с растворителем зависят характеристики растворимости. Именно взаимодействием водородных связей с содержащими ОН-группы веществами (сахар, глюкоза, спирт, карбоновые кислоты) можно объяснить их отличный уровень растворения в воде.
Димер — это водородная связь двух молекул H2O.
Каждая молекула имеет способность формировать четыре водородные связи: две между неподеленными парами ее атома кислорода и атомами водорода соседних молекул и еще две – между атомами водорода и атомами кислорода двух соседних молекул.
Границы энергии водородной связи могут варьироваться от 17 до 33 кДж/моль.
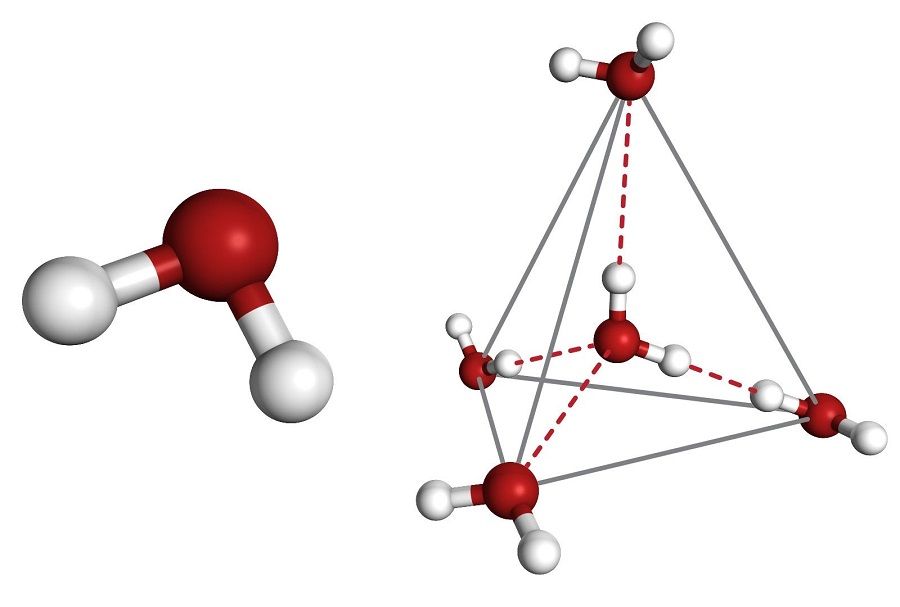
Молекулярная структура воды
Различают несколько состояний воды:
Жидкое. Основное состояние в нормальных условиях.
Твердое. Это лед, а также в форме кристаллов – иней или снег.
Газообразное — водяной пар.
Три исследования, которые помогут остановить старение
Такой простой элемент как вода всегда считался жизненно важным и необходимым. Но вместе с тем, то количество мифов о воде, научных фактов и мнений, которые ежедневно навязывают, а потом опровергают, побуждает искать ответы на вопросы. Чтобы помочь вам, мы с командой подготовили вебинар и подарок: 3 уникальных материала, основанные на опыте наших экспертов о продлении молодости с помощью воды. После прохождения нашего бесплатного вебинара вы узнаете:

практикующий врач терапевт-диетолог, натуропат
Сразу после регистрации вы получите подборку исследований:
Старение: остановить нельзя смириться К каким выводам пришли ученые 21 века, изучая воду и ее способность продлевать молодость
На самом деле, мы ничего не знаем о воде Важная информация для продления молодости, которую нам могли рассказать еще в школе
Водородная вода - самое мощное природное средство для продления молодости Почему вода, обогащенная водородом, считается самым эффективным, безопасным и доступным способом продлить молодость
Узнайте, как вода может заботиться о вашем здоровье, молодости и красоте на бесплатном вебинаре врача-диетолога Артёма Хачатряна!
Выделяют также и переходные состояния воды, которые обусловлены ее замерзанием или испарением.
Удивительно и в то же время вполне естественно, что можно наблюдать соседство и даже взаимодействие воды, одновременно находящейся в разных агрегатных состояниях: озера с ледниками, айсберги в океане, облака на небе, состоящие из водяного пара и капель жидкой воды.
Ознакомимся подробнее с особенностями каждого агрегатного состояния воды.
Молекулярная структура воды в различных агрегатных состояниях
Вода в ее естественном жидком состоянии содержит одиночные (моногидроли), двойные (дигидроли) и тройные (тригидроли) молекулы. Их соотношение и количество определяется температурой и влияет на то, в каком из трех состояний вода находится в текущий момент.
Пар включает одну H₂O-гидроль (моногидроль). Пар образуется при нагревании, которое способствует активному движению молекул, что, в свою очередь, нарушает связь между ними. Моногидроли в газообразном состоянии не соединены между собой.
Две молекулы H₂O обозначают жидкое состояние – дигидроль. В данном случае молекулы соединены, но между ними есть пустоты.
Три молекулы H₂O включает лед. Его твердость можно объяснить очень плотной связью между тригидролями.
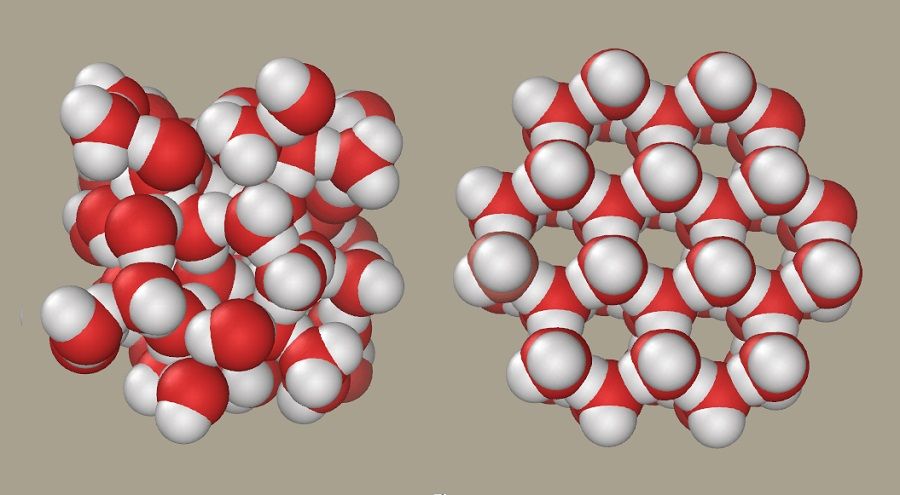
Молекулярная структура воды в различных агрегатных состояниях
Также существуют еще и переходные состояния жидкости, такие как испарение или замерзание. Попробуем понять, есть ли отличия между льдом и водой на уровне молекулярного строения. При замерзании вода приобретает структуру кристалла, например, в форме тетраэдра, тригональной и моноклинной сингонии, куба.
Различия в молекулярной структуре воды и льда есть в первую очередь в плотности: кристаллы по своему строению объемные, но менее плотные. Но главное, что отличает их друг от друга, – это водородные связи, которые выражаются разными видами, количеством и силой.
Как правило, молекулы воды не имеют сильного притяжения и определенного порядка расположения, благодаря чему, собственно, жидкость обладает свойством текучести. Структура льда своей формой кристаллической решетки говорит о значительной силе притяжения между молекулами.
Состав не меняется ни в одном агрегатном состоянии. К отличиям также можно отнести разное поведение молекул воды и льда во время движения и их строение.
Популярным остается вопрос, отличаются ли по объему и составу молекул холодная и горячая вода. Как уже говорилось выше, состав воды всегда один и тот же. Конкретно в горячем и холодном состоянии молекулы жидкости отличаются расположением. Объем также разный, это объясняется тем, что молекулярная структура холодной воды упорядочена, а горячей – хаотична.
При таянии температура льда постоянна. Только когда агрегатное состояние полностью сменится, стрелка термометра начнет подниматься вверх. Во время таяния льда выделяется энергия, равная 25 000 Дж/кг, ее называют удельной теплотой плавления (лямбда воды).
Твердая – это замерзшая вода. При замерзании расстояние между ее молекулами увеличивается, за счет чего уже в состоянии льда ее плотность уменьшается, однако объем при этом становится больше.
Молекулярная структура воды наделяет ее специфической особенностью – расширяться при низких температурах, в то время как большинство веществ, наоборот, сжимаются.
Интересно! Все мы привыкли, что основное состояние воды жидкое. Однако большая часть запасов воды на планете Земля хранится в состоянии льда. Ледники занимают 11 % всей сухой поверхности земного шара.
Вода в жидком состоянии на Земле находится не только в реках и океанах. Осадки в виде дождя, маленькие капельки, спрятанные в облаках, – это все тоже жидкость.
В мире почти не существует женщин, которые бы ни разу не сидели на диете. Рано или поздно с желанием скинуть пару килограммов сталкивается каждая.
Чтобы заветная цифра на весах скорее появилась, внедрите в свою жизнь 3 здоровые и супер простые привычки: мы подготовили с экспертами документ, где подробно описываем их.


Практикующий врач терапевт- диетолог, натуропат
Также встретить воду в жидком состоянии можно под землей, куда она уходит через почву, образуя подземные скопления, из которых состоит основной объем запасов питьевой воды.
В жидком виде вода обладает свойством прилипания к твердым веществам, легко увлажняя их поверхность.
Из жидкого состояния она без труда, при определенных показателях температуры и давления, превращается в газ (пар) или лед.
Физическое превращение воды из жидкости в газ называют испарением, ввиду того что газообразное состояние воды называется паром.
Закипает жидкая пресная вода при 100 °C (градусах Цельсия), или 212 °F (градусах Фаренгейта), в условиях нормального атмосферного давления. При снижении давления (в горах, например) значение температуры кипения увеличивается.
Рассмотрим, какие существуют процессы перехода воды из одного агрегатного состояния в другое:
кипение и парообразование — превращение воды в пар;
конденсация — обратный процесс, пар становится водой;
кристаллизация — вода превращается в лед;
плавление – наоборот, лед становится водой;
сублимация – процесс преобразования льда в пар;
десублимация – превращение пара в лед (иней).
Показатели перехода воды в разные агрегатные состояния лед/вода и вода/пар условились определять соответственно как 0 и 100 градусов по Цельсию при условии атмосферного давления 760 мм рт. ст., или 101 325 Па.
Составляющие элементы молекулярной структуры воды
В естественном состоянии вода представляет собой бесцветную, безвкусную, ничем не пахнущую жидкость.
Она обладает способностью растворять огромное количество веществ. В природных условиях вода содержит растворенные в ней газы и соли.
Вода в чистом виде считается неплохим изолятором, при условии, что концентрация протонов и гидроксильных ионов в ней равна 10–7 моль/л. Но в таком виде ее можно встретить редко: в жидкости практически всегда присутствуют растворенные вещества с положительными и отрицательным ионами, которые, в свою очередь, наделяют ее свойствами проводить ток. Именно на основании степени электропроводности можно судить о чистоте воды.
Даже активное воздействие других веществ на воду не способно изменить ее состав, что является важным свойством для всего живого на планете. Так как полезные вещества, попадающие в организм с помощью жидкости, передаются в неизменном виде.
Также вода отлично справляется с функцией поглощения инфракрасных и микроволновых лучей. По мере прохождения всех этапов гидрологического цикла (круговорота воды в природе – испарение, конденсация и выпадение осадков) вода может насыщаться различными химическими элементами, среди которых выделяют 6 категорий.
Рассмотрим информацию в таблице № 1.
Na, K, Mg, Ca, анионы: Cl, HCO3 и SO4. Эти компоненты находятся в воде в наибольшем по сравнению с другими количестве.
Растворенные газы
Кислород, азот, сероводород, углекислый газ и прочие. Количество каждого газа в воде напрямую зависит от ее температуры.
Биогенные элементы
Главными из них являются фосфор и азот, которые поступают в жидкость из осадков.
Микроэлементы
Их насчитывается около 30 видов: бром, селен, медь, цинк и т. д. Концентрации их в составе воды очень малы и колеблются от 0,1 до микрограмма на 1 литр.
Органические вещества
Спирты, углеводы, альдегиды, фенолы, пептиды и прочее.
Тяжелые металлы и продукты нефтепереработки.
В современном мире для очистки воды от вредных веществ используют эффективные надежные способы.
В зависимости от концентрации магния или катионов кальция вода бывает мягкой и жесткой соответственно.
По молекулярной структуре воды и изотопному составу ее определяют как легкую, тяжелую и сверхтяжелую. Данная характеристика в основном зависит от количества изотопов водорода в молекуле воды.
Ответ на такой вопрос наверно больше основывается на смекалке ведь по сути при нагревании воды, её объем увеличивается, но это происходит не за счет изменения самих молекул, а в связи с увеличением между ними расстояния.
Поэтому можно сказать, что по своим химическому составу молекулы в горячей воде ничем не отличаются от молекул холодной воды.
Ни какой разницы химического состава между молекулами холодного и горячего вещества нет. И у воды нет. Есть только скорость движения молекул. У "горячих" молекул скорость больше. И толкаются они друг с другом сильнее, потому-то и объем горячего вещества больше. И у воды, тоже.
Еще у "горячих" молекул заселяются более высокие колебательные уровни. То есть атомы колеблются быстрее и имеют большую колебательную энергию.
Я вообще могу долго не пить, как верблюд. Да, водой считается только чистая питьевая вода, чай без сахара - уже не вода, тем более суп.
Я раньше (всю жизнь) вообще не пила воду. Чай, потом кофе, что еще? Вода была только кипяченая, вкус противный. И ничего.
А сейчас придерживаюсь водной диеты, впихиваю в себя 8 стаканов воды в день. Другой жидкости - чай, кофе, уже не хочется. Правда, часто не получается 8, стаканов 5-6 выпиваю. Радуюсь, хоть немножко к норме потребления приблизилась.
Не для всякой жидкости, а только для той, которая способна смачивать стенки сосуда. Со ртутью всё будет наоборот - в центре окажется ртуть, а не газ.
Причина простая: поверхностное натяжение. Жидкость в сосуде принимает форму, при которой минимальна поверхностная энергия жидкости, и не штука догадаться, что это возможно именно при сферической форме воздушного пузыря.
А вот что он будет именно в центре сосуда - не факт. Такой пузыть в невесомости находится в состоянии безразличного равновесия. Коль скоро его расстояние до стенок достаточно велико (слой жидкости достаточно толстый), не видно причин, по которым предпочтительным окажется положение в центре сферы. "Отталкиваться от стенки" пузыть может только если он подойдёт к ней на расстояние порядка межмолеклярного взаимодействия, когда начнёт нарушаться его сферическая форма.
Как известно, диффузия при более высокой температуре происходит быстрее. Из этого следует, что скорость перемещения молекул и температура глубоко взаимосвязаны между собой. Если увеличить температуру, то скорость движения молекул увеличится, если уменьшить – понизится.
Таким образом, делаем вывод: температура тела напрямую зависит от скорости перемещения молекул.
Горячая вода состоит из абсолютно таких же молекул, как и холодная. Разница между ними состоит лишь в скорости передвижения молекул.
Молекула горячей воды не чем не отличается от молекулы холодной воды.
Молекула горячей воды быстрее движется, чем молекула холодной воды.
Согласно уравнению молекулярно-кинетической теории, средняя кинетическая энергия молекул Ек зависит от температуры следующим образом Ек= 3 *k *T/2. Чем больше температура, тем быстрее двигаются молекулы.
Как написать хороший ответ? Как написать хороший ответ?
- Написать правильный и достоверный ответ;
- Отвечать подробно и ясно, чтобы ответ принес наибольшую пользу;
- Писать грамотно, поскольку ответы без грамматических, орфографических и пунктуационных ошибок лучше воспринимаются.
Мореплаватель — имя существительное, употребляется в мужском роде. К нему может быть несколько синонимов.
1. Моряк. Старый моряк смотрел вдаль, думая о предстоящем опасном путешествии;
2. Аргонавт. На аргонавте были старые потертые штаны, а его рубашка пропиталась запахом моря и соли;
3. Мореход. Опытный мореход знал, что на этом месте погибло уже много кораблей, ведь под водой скрывались острые скалы;
4. Морской волк. Старый морской волк был рад, ведь ему предстояло отчалить в долгое плавание.
Читайте также:

