Спектральный анализ физика 9 класс кратко
Обновлено: 05.07.2024
Спектральный анализ — совокупность методов качественного и количественного определения состава объекта, основанная на изучении спектров взаимодействия материи с излучением, включая спектры электромагнитного излучения, акустических волн, распределения по массам и энергиям элементарных частиц и др.
В зависимости от целей анализа и типов спектров выделяют несколько методов спектрального анализа. Атомный и молекулярный спектральные анализы позволяют определять элементный и молекулярный состав вещества, соответственно. В эмиссионном и абсорбционном методах состав определяется по спектрам испускания и поглощения.
Масс-спектрометрический анализ осуществляется по спектрам масс атомарных или молекулярных ионов и позволяет определять изотопный состав объекта.
Содержание
История
Вскоре выяснялось, что одна из самых отчётливых линий всегда появляется в присутствии натрия. В 1859 году Г. Кирхгоф и Р. Бунзен после серии экспериментов заключили: каждый химический элемент имеет свой неповторимый линейчатый спектр, и по спектру небесных светил можно сделать выводы о составе их вещества. С этого момента в науке появился спектральный анализ, мощный метод дистанционного определения химического состава.
Для проверки метода в 1868 году Парижская академия наук организовала экспедицию в Индию, где предстояло полное солнечное затмение. Там учёные обнаружили: все тёмные линии в момент затмения, когда спектр излучения сменил спектр поглощения солнечной короны, стали, как и было предсказано, яркими на тёмном фоне.
Природа каждой из линий, их связь с химическими элементами выяснялись постепенно. В 1860 году Кирхгоф и Бунзен при помощи спектрального анализа открыли цезий, а в 1861 году — рубидий. А гелий был открыт на Солнце на 27 лет ранее, чем на Земле (1868 и 1895 годы соответственно).
Принцип работы
Атомы каждого химического элемента имеют строго определённые резонансные частоты, в результате чего именно на этих частотах они излучают или поглощают свет. Это приводит к тому, что в спектроскопе на спектрах видны линии (тёмные или светлые) в определённых местах, характерных для каждого вещества. Интенсивность линий зависит от количества вещества и его состояния. В количественном спектральном анализе определяют содержание исследуемого вещества по относительной или абсолютной интенсивностям линий или полос в спектрах.
Оптический спектральный анализ характеризуется относительной простотой выполнения, отсутствием сложной подготовки проб к анализу, незначительным количеством вещества (10—30 мг), необходимого для анализа на большое число элементов.
Атомарные спектры (поглощения или испускания) получают переведением вещества в парообразное состояние путём нагревания пробы до 1000—10000 °C. В качестве источников возбуждения атомов при эмиссионном анализе токопроводящих материалов применяют искру, дугу переменного тока; при этом пробу помещают в кратер одного из угольных электродов. Для анализа растворов широко используют пламя или плазму различных газов.
Применение
В последнее время, наибольшее распространение получили эмиссионные и масс-спектрометрические методы спектрального анализа, основанные на возбуждении атомов и их ионизации в аргоновой плазме индукционных разрядов, а также в лазерной искре.
Спектральный анализ — чувствительный метод и широко применяется в аналитической химии, астрофизике, металлургии, машиностроении, геологической разведке и других отраслях науки.
В теории обработки сигналов, спектральный анализ также означает анализ распределения энергии сигнала (например, звукового) по частотам, волновым числам и т. п.
Метод определения химического состава вещества по его линейчатому спектру называется спектральным анализом.
2. Как проводится спектральный анализ?
Исследуемое вещество в виде порошка или аэрозоля помещают в высокотемпературный источник света - пламя или электрический разряд, из-за чего оно переходит в состояние атомарного газа и у него возбуждаются атомы, которые испускают или поглощают электромагнитное излучение в строго определенных диапазонах частот. Затем полученную с помощью спектографа фотографию спектра атомов анализируют.
3. Как по полученным в эксперименте фотографиям исследуемого образца определяют, какие химические элементы входят в его состав?
По расположению линий в спектре узнают из каких элементов состоит данное вещество.
4. Можно ли по спектру образца определить количество каждого из входящих в него химических элементов?
Сравнивая относительные интенсивности линий спектра оценивают количественное содержание элементов.
5. Расскажите о применении спектрального анализа.
Спектральный анализ применяется в металлургии, машиностроении, атомной индустрии, геологии, археологии, криминалистике и др. сферах. Особенно интересно использование спектрального анализа в астрономии, с помощью него определяют химический состав звезд и атмосфер планет, их температуру. По смещениям спектральных линий галактик научились определять их скорость.
1. Что такое спектральный анализ?
Спектральным анализом называется метод определения химического состава вещества по его линейчатому спектру
2. Как проводится спектральный анализ?
Для проведения спектрального анализа исследуемое вещество приводят в состояние атомарного газа (атомизируют).
Одновременно с этим возбуждают атомы, т. е. сообщают им дополнительную энергию.
Для атомизации и возбуждения используют высокотемпературные источники света: пламя или электрические разряды.
В них помещают образец исследуемого вещества в виде порошка или аэрозоля раствора, т. е. мельчайших капелек раствора, распылённого в воздухе.
Затем с помощью спектрографа получают фотографию спектров атомов элементов, входящих в состав данного вещества.
3. Как по полученным в эксперименте фотографиям исследуемого образца определяют, какие химические элементы входят в его состав?
В настоящее время существуют таблицы спектров всех химических элементов.
Отыскав в таблице точно такие же спектры, какие были получены при анализе исследуемого образца, узнают, какие химические элементы входят в его состав.
Спектральный анализ отличается высокой чувствительностью.
С его помощью можно обнаружить наличие химического элемента, масса которого в данном образце не превышает 10 -10 г.
4. Можно ли по спектру образца определить количество каждого из входящих в него химических элементов?
В процессе спектральныого анализа путём сравнения интенсивности линий определяют количество каждого химического элемента в образце.
5. Где применяется спектральный анализ?
Спектральный анализ используется для контроля состава вещества в металлургии, машиностроении и атомной индустрии.
Этот метод применяется также в геологии, археологии, криминалистике и многих других сферах деятельности.
В астрономии методом спектрального анализа определяют химический состав атмосфер планет и звёзд, температуру звёзд и магнитную индукцию их полей.
По смещению спектральных линий в спектрах галактик была определена их скорость, и на основании этого сделан вывод о расширении нашей Вселенной.

Ни один из источников не дает монохроматического света, т.е. света строго определенной длины волны. В этом можно убедиться на опытах по разложению света в спектр с помощью призмы, а также опыты по интерференции и дифракции.
Та энергия, которую несет с собой свет от источника, определенным образом распределена по волнам всех длин, входящим в состав светового пучка.
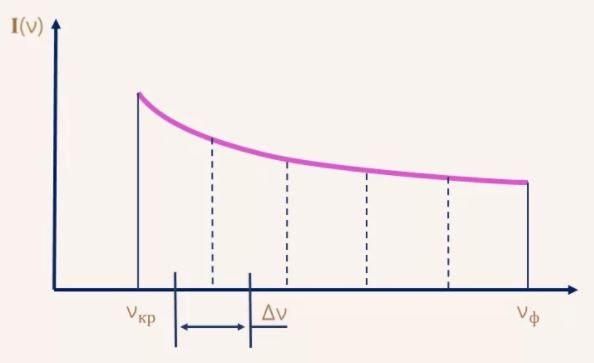
Для характеристики распределения излучения по частотам нужно ввести новую величину: интенсивность, приходящуюся на единичный интервал частот. Эту величину называют спектральной плотностью интенсивности излучения.
Спектральную плотность потока излучения можно найти экспериментально. Для этого надо с помощью призмы получить спектр излучения, например, электрической дуги, и измерить плотность потока излучения, приходящегося на небольшие спектральные интервалы шириной Δν.
Полагаться на глаз при оценке распределения энергии нельзя. Глаз обладает избирательной чувствительностью к свету: максимум его чувствительности лежит в желто-зеленой области спектра. Лучше всего воспользоваться свойством черного тела почти полностью поглощать свет всех длин волн. При этом энергия излучения (т.е. света) вызывает нагревание тела. Поэтому достаточно измерить температуру тела и по ней судить о количестве поглощенной в единицу времени энергии.
Спектры излучения
Спектральный состав излучения атомов различных веществ весьма разнообразен. Тем не менее, все спектры можно разделить на три сильно отличающихся друг от друга типа.
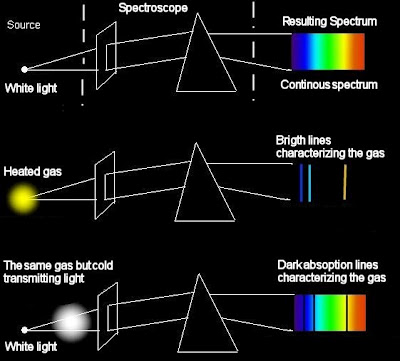
Сплошной (непрерывный) спектр
Накаленные твердые и жидкие тела и газы (при большом давлении) испускают свет, разложение которого дает сплошной спектр, в котором спектральные цвета непрерывно переходят один в другой. Характер непрерывного спектра и сам факт его существования определяются не только свойствами отдельных излучающих атомов, но и взаимодействием атомов друг с другом. Сплошные спектры одинаковы для разных веществ, и поэтому их нельзя использовать для определения состава вещества.
Линейчатый (атомный) спектр
Возбужденные атомы разреженных газов или паров испускают свет, разложение которого дает линейчатый спектр,состоящий из отдельных цветных линий. Каждый химический элемент имеет характерный для него линейчатый спектр. Атомы таких веществ не взаимодействуют друг с другом и излучают свет только определенных длин волн. Изолированные атомы данного химического элемента излучают строго определенные длины волн. Это позволяет по спектральным линиям судить о химическом составе источника света.

Обычно для наблюдения линейчатых спектров используют свечение паров вещества в пламени или свечение газового разряда в трубке, наполненной исследуемым газом. При увеличении плотности атомарного газа отдельные спектральные линии расширяются и, при очень большой плотности газа, когда взаимодействие атомов становится существенным, эти линии перекрывают друг друга, образуя непрерывный спектр.
Молекулярный (полосатый) спектр
Спектр молекулы состоит из большого числа отдельных линий, сливающихся в полосы, четкие с одного края и размытые с другого. В отличие от линейчатых спектров полосатые спектры создаются не атомами, а молекулами, не связанными или слабо связанными друг с другом. Серии очень близких линий группируются на отдельных участках спектра и заполняют целые полосы.
 |
| Спектр угольной дуги (полосы молекул CN и C2) |
 |
| Спектр испускания паров молекулы йода |
 |
| Спектр молекулы Н2 |
В 1860 г. немецкие ученые Г. Кирхгоф и Р. Бунзен, изучая спектры металлов, установили следующие факты:
1) каждый металл имеет свой спектр;
2) спектр каждого металла строго постоянен;
3) введение в пламя горелки любой соли одного и того же металла всегда приводит к появлению одинакового спектра;
4) при внесении в пламя смеси солей нескольких металлов в спектре одновременно появляются все их линии;
5) яркость спектральных линий зависит от концентрации элемента в данном веществе.
Спектры поглощения
Если белый свет от источника, дающей сплошной спектр, пропускается через пары исследуемого вещества и затем разлагается в спектр, то на фоне сплошного спектра наблюдаются темные линии поглощения в тех же сам ых местах, где находились бы линии спектра испускания паров исследуемого элемента. Такие спектры получили название атомных спектров поглощения.
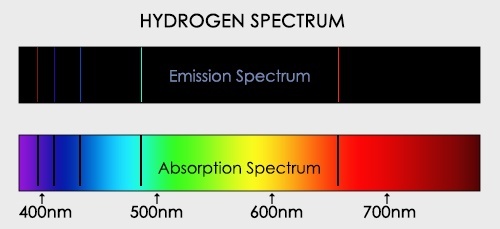
Все вещества, атомы которых находятся в возбужденном состоянии, излучают световые волны, энергия которых определенным образом распределена по длинам волн. Поглощение света веществом также зависит от длины волны. Атомы поглощают излучение лишь тех длин волн, которые они могут испускать при данной температуре.
Спектральный анализ
Спектральным анализом называется метод изучения химического состава вещества, основанный на исследовании его спектров. Отдельные линии в спектрах различных элементов могут совпадать, но в целом спектр каждого элемента является его индивидуальной характеристикой.
Спектральный анализ сыграл большую роль в науке. Например, в спектре Солнца (1814) были открыты фраунгоферовы темные линии, происхождение которых объясняется следующим образом. Солнце, являясь раскаленным газовым шаром (Т ~ 6000 °С), испускает сплошной спектр. Солнечные лучи проходят через атмосферу Солнца (солнечную корону, температура которой ~2000— 3000 °С. Корона поглощает из сплошного спектра излучение определенной частоты, а на Земле регистрируется солнечный спектр поглощения, по которому можно определить, какие химические элементы присутствуют в короне Солнца. По спектрам поглощения на Солнце были обнаружены все земные элементы, а также неизвестный ранее элемент, который назвали гелий. Через 26 лет (1894) открыли гелий на Земле. Благодаря спектральному анализу на Земле было открыто еще 25 химических элементов.
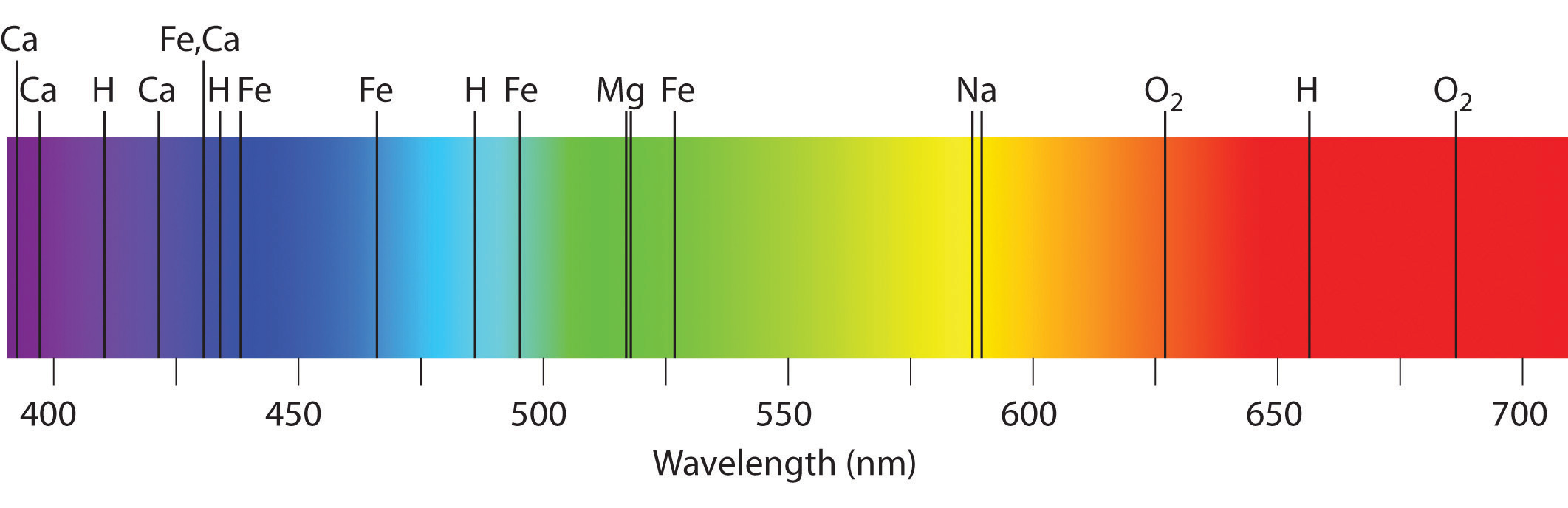
Фраунгоферовы линии дают информацию не только о химическом составе звезды, но и о ее температуре и давлении на поверхности. Более того, спектральный анализ Солнца и звезд показал, что входящие в их состав химические элементы имеются и на Земле, т.е. вещество Вселенной состоит из одного и того же набора элементов.
Спектральные аппараты
Спектроскопом называется прибор, с помощью которого визуально исследуется спектральный состав света, испускаемого некоторым источником. Если регистрация спектра происходит на фотопластинке, то прибор называется спектрографом.
Для точного исследования спектров такие простые приспособления, как узкая щель, ограничивающая световой пучок, и призма, уже недостаточны. Необходимы приборы, дающие четкий спектр, т.е. приборы, хорошо разделяющие волны различной длины и не допускающие перекрытия отдельных участков спектра. Такие приборы называют спектральными аппаратами. Чаще всего основной частью спектрального аппарата является призма или дифракционная решетка.

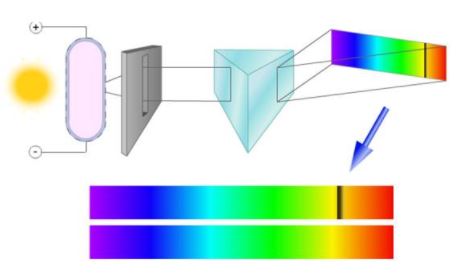
Рассмотрим схему устройства призменного спектрального аппарата. Исследуемое излучение поступает вначале в часть прибора, называемую коллиматором. Коллиматор представляет собой трубу, на одном конце которой имеется ширма с узкой щелью, а на другом - собирающая линза. Щель находится на фокусном расстоянии от линзы. Поэтому расходящийся световой пучок, попадающий на линзу из щели, выходит из нее параллельным пучком и падает на призму.
Так как разным частотам соответствуют различные показатели преломления, то из призмы выходят параллельные пучки, не совпадающие по направлению. Они падают на линзу. На фокусном расстоянии этой линзы располагается экран - матовое стекло или фотопластинка. Линза фокусирует параллельные пучки лучей на экране, и вместо одного изображения щели получается целый ряд изображений. Каждой частоте (узкому спектральному интервалу) соответствует свое изображение. Все эти изображения вместе и образуют спектр.
Описанный прибор называется спектрографом . Если вместо второй линзы и экрана используется зрительная труба для визуального наблюдения спектров, то прибор называется спектроскопом .
Применение спектрального анализа
Линейчатые спектры играют особо важную роль, потому что их структура прямо связана со строением атома. Ведь эти спектры создаются атомами, не испытывающими внешних воздействий. Состав сложных, главным образом органических смесей анализируется по их молекулярным спектрам.
С помощью спектрального анализа можно обнаружить данный элемент в составе сложного вещества , если даже его масса не превышает 10 -10 г. Линии, присущие данному элементу, позволяют качественно судить о его наличии. Яркость линий дает возможность (при соблюдении стандартных условий возбуждения) количественно судить о наличии того или иного элемента.
Спектральный анализ можно проводить и по спектрам поглощения. В астрофизике по спектрам можно определить многие физические характеристики объектов : температуру, давление, скорость движения, магнитную индукцию и др. с помощью спектрального анализа определяют химический состав руд и минералов.
Основные направления применения спектрального анализа таковы: физико-химические исследования; машиностроение, металлургия; атомная индустрия; астрономия, астрофизика; криминалистика.
Современные технологии создания новейших строительных материалов (металлопластиковые, пластиковые) непосредственно взаимосвязаны с такими фундаментальными науками как химия, физика. Данные науки используют современные методы исследования веществ. Поэтому спектральный анализ можно применять для определения химического состав состава строительных материалов по их спектрам.

Посмотрев данный видеоурок, вы узнаете, какие тела дают сплошной спектр и от каких источников получают линейчатые спектры. Так же мы выясним, чем различаются линейчатые спектры испускания и поглощения. Познакомимся с методом спектрального анализа и узнаем, какие открытия были сделаны с помощью этого метода.

В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобретя в каталоге.
Получите невероятные возможности



Конспект урока "Типы оптических спектров. Спектральный анализ"
На прошлом уроке мы с вами говорили о дисперсии света. Напомним, что дисперсией называется зависимость показателя преломления вещества и скорости света в нём от частоты падающего света.
Как показали опыты Ньютона, белый свет является сложным: пройдя через призму он разлагается на пучки различных цветов, которые образуют на экране разноцветную полоску, называемую спектром. И хотя, перечисляя цвета спектра, обычно называют семь цветов, начиная с красного и заканчивая фиолетовым, на самом деле один цвет переходит в другой постепенно.
Исследования, проведённые при помощи специального чувствительного термометра, показали, что спектр излучения нагретых тел, кроме видимых лучей, содержит ещё и невидимые лучи. Открыты они были в тысяча восьмисотом году английским астрономом Уильямом Гершелем. Одновременно с изучением Солнца, он искал способы уменьшения нагревания инструментов для наблюдения. Для этого Гершель помещал края термометров, у которых резервуар с ртутью был затемнён сажей, в различные участки спектра.

Какого же было его удивление, когда он обнаружил, что максимум тепла находится за насыщенным красным цветом. Из-за повышенной способности лучей нагревать тела, они были названы тепловыми, а затем (уже учитывая их расположение в спектре) — инфракрасными. Сейчас достоверно известно, что в инфракрасном диапазоне светится вся наша планета и все предметы на ней, даже лёд.
В 1801 году немецким физиком Иоганном Вильгельмом Риттером был обнаружен ещё один вид невидимого излучения, располагавшийся перед фиолетовой областью видимого спектра. Это — известное вам ультрафиолетовое излучение, обладающее сильным физиологическим воздействием.
Поскольку в спектрах нагретых тел нет пустых промежутков, то такие спектры являются непрерывными или, как их ещё называют, сплошными. Их дают раскалённые твёрдые тела и жидкости, а также пары́ и газы, находящиеся под очень большим давлением.

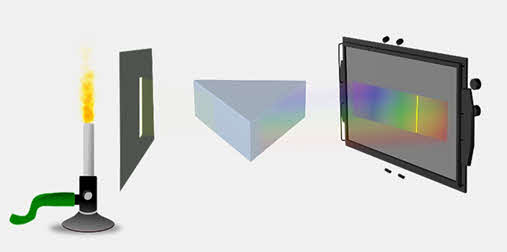
Например, сплошной спектр можно увидеть, направив спектроскоп на свет раскалённой спирали электрической лампочки или пламя свечи.

В середине девятнадцатого века немецкий физик Роберт Вильгельм Бунзен изобрёл специальную газовую горелку, называемую нами горелкой Бунзена. Вы спросите, а причём тут спектр?
Дело в том, что вещества, внесённые в пламя горелки, превращались в пар и окрашивали пламя в различные цвета. Например, медь окрашивала пламя в зелёный цвет, поваренная соль — в жёлтый, а литий — в малиново-красный.

Так вот, немецкий физик Густав Роберт Кирхгоф предложил пропускать такой свет пламени через призму. Например, если в пламя горелки внести кусочек поваренной соли, то на бледном фоне сплошного спектра горелки возникнет яркая жёлтая линия, которую дают пары натрия.
Если же в пламя горелки внести литий или стронций, то пламя окрасится в малиново-красный цвет. Однако спектры паров лития и стронция будут существенно различаться. После прохождения через призму свет литиевого пламени даёт две линии — яркую малиновую и слабую оранжевую. А вот стронций — голубую, две красные и оранжевую линии.
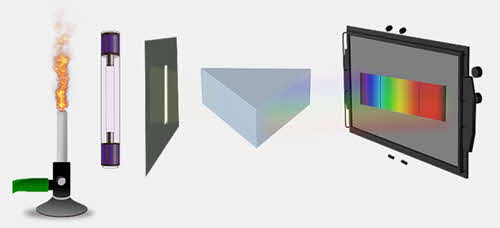
Характерный спектр, также состоящий из набора отдельных цветных линий, даёт свечение газового разряда в трубке, содержащей исследуемый газ. Например, спектр испускания атомарного водорода содержит четыре цветные линии различной яркости, которые разделены широкими тёмными промежутками.

Спектр испускания гелия включает уже семь цветных линий.
Таким образом, спектры испускания различных веществ, находящихся в атомарном состоянии, представляют собой набор отдельных цветных линий на чёрном фоне. Такие спектры получили название линейчатых спектров испускания.

Как показали тщательные измерения, атомы каждого химического элемента испускают излучение, спектр которого не похож на спектры других элементов. Как не бывает людей с одинаковыми отпечатками пальцев, окраской радужной оболочки глаз, или китов с одинаковой окраской хвостового плавника, так и не существует двух химических элементов, атомы которых излучали бы одинаковый набор спектральных линий. Поэтому для каждого химического элемента составлена специальная таблица, в которой указаны характерные для него линии и их яркость.
Все описанные нами спектры получались при разложении излучаемого света самосветящимися телами. Такие спектры получили название спектров испускания. Но кроме них существуют ещё и так называемые спектры поглощения. Чтобы пронаблюдать такой спектр видоизменим предыдущий опыт. Поместим перед ненагретыми парами водорода источник света, дающий непрерывный спектр. При этом на экране, установленным за призмой, будем наблюдать сплошной спектр, перерезанный тёмными линиями. Эти линии получили название линий поглощения, а сам спектр — линейчатого спектра поглощения.
В 1859 году Роберт Бунзен и Густав Кирхгоф установили, что линии поглощения находятся в тех же участках спектра, где должны быть расположены яркие линии в линейчатом спектре испускания, присущие данному газу. На основе этих наблюдений Кирхгоф сформулировал закон обратимости спектральных линий: атомы менее нагретых тел поглощают из сплошного спектра только те частоты, которые в других условиях они испускают.

Эта закономерность даёт возможность обнаружить те или иные элементы в данном веществе.
Кстати впервые линейчатый спектр поглощения наблюдал ещё в 1802 году английский врач и химик Уильям Хайд Волластон. Изучая непрерывный спектр Солнца, он обнаружил в нем несколько резких тёмных линий. Однако учёный не придал им особого значения, считая, что их появление зависит от внешних причин. Только через двенадцать лет немецкий физик Йозеф Фраунгофер, продолжая исследования тёмных линий в спектре Солнца (а их насчитывается около 20 тысяч), убедился, что их причина не оптический обман, а сама природа солнечного света. Впоследствии эти линии были названы фраунгоферовыми линиями солнечного спектра.
Таким образом, анализ линейчатых спектров излучения и поглощения позволяет расшифровать состав излучающего вещества.
Метод определения химического состава вещества по его спектру называют спектральным анализом. Данный метод был разработан в тысяча восемьсот пятьдесят девятом году уже известными нам Робертом Бунзеном и Густавом Кирхгофом, что ознаменовало появление нового раздела физики — спектроскопии, изучающей спектры электромагнитного излучения.
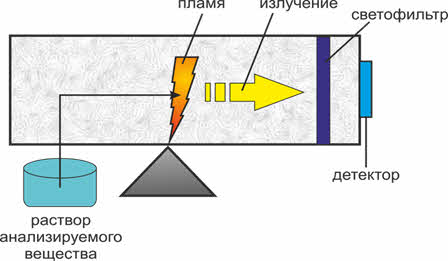
При выполнении спектрального анализа вещества с неизвестным химическим составом его сначала приводят в атомарное состояние и сообщают атомам большую энергию. Для этого, чаще всего, используются высокотемпературные источники света. В них помещается исследуемое вещество в виде порошка или аэрозоля, а затем при помощи спектрографа получают фотографию спектров. Сравнивая полученный линейчатый спектр с известными спектрами химических элементов, можно определить, какие элементы имеются в составе исследуемого вещества.
Благодаря относительной простоте и достаточной универсальности спектральный анализ является основным методом для контроля состава вещества в машиностроении и металлургии, атомной индустрии. С его помощью определяется химический состав руд и минералов, определяется возраст археологических находок, используется и в криминалистике.
Спектральный анализ в астрофизике даёт возможность определять не только химический состав звёзд и газопылевых облаков, но и некоторые другие физические характеристики, например, температуру, давление, скорость движения небесного тела и индукцию его магнитного поля. Именно благодаря спектральному анализу было открыто смещение спектральных линий в спектрах галактик, что свидетельствовало о расширении нашей Вселенной.
Читайте также:
- Что такое семейники в биологии 7 класс кратко
- Как вы думаете почему идеи з фрейда имеют довольно широкое распространение в наше время кратко
- В чем вы видите основные причины кризисного состояния окружающей среды в нашей стране кратко
- Мастер класс по проектной деятельности в основной школе
- Что такое молоко кратко