Почему кость относят к соединительной ткани кратко
Обновлено: 07.07.2024
Для цитирования: Дыдыкина И.С., Дыдыкина П.С., Наумов А.В. От знаний о структуре костной ткани к выбору средств влияния на нее. РМЖ. 2015;7:388.
Изменения в структуре питания и образе жизни, а также увеличение продолжительности жизни во многом определяют рост числа больных с заболеваниями костно-мышечной системы, в т. ч. в молодом возрасте. Интерес к структуре костной ткани не ослабевает на протяжении последних 50 лет и продиктован желанием, потребностью и необходимостью понять, что же определяет качество, прочность и целостность кости. Внедрение новейших технологий визуализации и диагностики состояния кости, успешное лечение ранее неизлечимых заболеваний с использованием генно-инженерных биологических препаратов позволяют изменить ход болезни, улучшить продолжительность и качество жизни больных. Однако эффект лечения, прогноз на будущее при использовании современных дорогостоящих технологий в онкологии, ревматологии, травматологии-ортопедии, стоматологии и других областях медицины определяются качеством костной ткани.
Костная ткань – разновидность соединительной ткани, формируется из мезодермы и состоит из клеток (остеокластов, остеобластов, остеоцитов), межклеточного неминерализованного органического матрикса (остеоида) и основного минерализованного межклеточного вещества. Органический матрикс (или остеоид) на 90% состоит из коллагена. Коллагеновые волокна в основном расположены параллельно направлению наиболее вероятных механических нагрузок на кость и обеспечивают ее упругость и эластичность. Фибриллы коллагена формируют пластины, которые расположены либо параллельно друг другу вдоль трабекул, либо концентрически вокруг кровеносных сосудов, образуя при этом гаверсовы каналы, соединенные между собой поперечными (фолькманновскими) каналами. При ускоренном метаболизме, на фоне хронических воспалительных или эндокринных заболеваний геометрия костной ткани нарушается.
Неколлагеновая часть матрикса представлена витамин К-зависимыми глютамилпротеинами (остеокальцином), матричными протеинами, остеопонтином, остеонектином, фибронектином, а также фосфопротеидами, сиалопротеидами и белками сывороточного происхождения. Минеральные вещества в составе основного вещества органического матрикса кости представлены кристаллами, главным образом гидроксиапатитом Ca10(PO4)6(OH)2. Соотношение кальций/фосфор в норме составляет 1,3:2,0. В кости обнаружены ионы Mg2+, Na+, K+, SO42-, HCO3-, гидроксильные и другие ионы, которые могут принимать участие в образовании кристаллов. Для нормальной минерализации кости необходимы активность остеобластов, поддержание определенных концентраций Са2+ и РО43- и микроэлементов (магния, марганца, цинка, селена, бора) во внеклеточной и периостальной жидкости [1]. Исследования последних лет показали, что для поддержания структуры костной ткани также необходимы витамины A, C, E, K. Дефицит этих веществ замедляет формирование костной массы в детстве и подростковом возрасте, способствует ее ускоренной потере в пожилом возрасте [2, 3].
Кость постоянно обновляется и каждые 30 лет изменяется почти полностью. При этом в ней происходят 2 противоположно направленных процесса – резорбция и восстановление. Соотношение этих процессов называется ремоделированием костной ткани. В первые 20 лет жизни преобладает формирование кости, и достигается пик костной массы, до 30–35-летнего возраста отмечается период более или менее устойчивого состояния, а затем начинается естественное постепенное снижение плотности костной массы. Скорость потери зависит от возраста, наступления андро- и менопаузы, сопутствующих заболеваний, приема лекарственных препаратов и влияния негативных факторов, таких как хроническое воспаление, ожирение, малоподвижный образ жизни, злоупотребление алкоголем, курение и многое другое.
Резорбцию активируют паратиреоидный гормон, инсулиноподобный фактор роста, интерлейкины-1 и -6, простагландины, кальцитриол, фактор некроза опухоли–α, тормозят этот процесс эстрогены. Установлено, что остеобласты и Т-лимфоциты секретируют лиганды рецепторов активатора нуклеарного фактора κВ (RANKL), и до определенного момента молекулы RANKL могут оставаться связанными с поверхностью остеобластов или стромальных клеток. В свою очередь из стволовой клетки костного мозга образуются предшественники остеокластов. Они имеют мембранные рецепторы, называемые рецепторами активатора нуклеарного фактора κВ (RANK). На следующем этапе RANKL связывается с RANK-рецептором, это приводит к слиянию нескольких предшественников остеокластов в одну крупную структуру и формированию зрелых многоядерных остеокластов. В образовавшихся зрелых активных остеокластах имеются лизосомы, содержащие большое количество гидролитических ферментов (катепсины К, D, B, кислая фосфатаза, эстераза, гликозидаза и др.), которые резорбируют костную ткань. Кроме того, катепсин К активирует матриксную металлопротеиназу-9, которая участвует в деградации коллагена и протеогликанов межклеточного матрикса. В этот период в остеокластах растет активность карбоангидразы и Н+/К+-АТФ-азы. Развивающийся ацидоз способствует дальнейшей активации лизосомных ферментов и разрушению минерального компонента кости.
На стадии образования остеокластов из предшественников процесс может блокироваться белком остеопротегерином, который, свободно перемещаясь, способен связывать RANKL и таким образом предотвращать взаимодействие RANKL с RANK-рецепторами. Остеопротегерин – гликопротеин с молекулярной массой 60–120 кДа, относится к семейству рецепторов фактора некроза опухоли. Ингибируя связывание RANK с RANKL, остеопротегерин подавляет мобилизацию, пролиферацию и активацию остеокластов.
Принципиальным отличием современных лекарственных средств для лечения остеопороза (ОП), таких как деносумаб (ингибитор RANKL), ромосозумаб (антитела к склеростину) и аденокатиб (ингибитор катепсина К), является таргетное воздействие на определенные мишени и механизмы патогенеза ремоделирования костной ткани.
ОП – системное заболевание скелета из группы метаболических остеопатий, которое характеризуется уменьшением костной массы и нарушением микроархитектоники костной ткани, что приводит к снижению прочности кости и, следовательно, к повышению риска возникновения переломов [4]. Заболевание встречается во всех возрастных группах, диагностируется как у женщин, так и у мужчин. Остеопоротические переломы представляют огромную социальную и экономическую проблему, являются причиной низкого качества жизни больных, инвалидизации и преждевременной смерти. Специалисты отмечают, что ОП можно предупредить и излечить. Определены факторы риска и механизмы патогенеза заболевания, разработаны методы диагностики, первичной и вторичной профилактики болезни, совершенствуются способы лечения [5, 6].
При изучении остеогенеза и формирования качественной структуры кости установлено, что ведущая роль принадлежит обеспечению организма не только витаминами и белком, но и макро- и микроэлементами [5, 7–9]. Субклинический дефицит, обусловленный недостаточным потреблением с пищей или пониженной абсорбцией этих веществ, может стать причиной (фактором) снижения минеральной плотности кости.
Особое значение имеют такие эссенциальные микроэлементы, как медь, цинк, марганец и условно эссенциальный – бор. Медь, марганец, цинк, являясь кофакторами ферментов, ответственных за синтез коллагена и гликозаминогликанов, непосредственно участвуют в синтезе костного матрикса [10].
Значение меди для организма состоит в том, что она является компонентом ферментов, обладающих окислительно-восстановительной активностью и участвующих в метаболизме железа, стимулировании усвоения белков и углеводов, процессах обеспечения тканей организма человека кислородом. Медь – кофактор для лизилоксидазы, необходима для межмолекулярной связи коллагена и эластина, основной компонент миелиновой оболочки, участвует в образовании коллагена, минерализации скелета, синтезе эритроцитов, образовании пигментов кожи. Клинические проявления недостаточного потребления меди – нарушения формирования и функции сердечно-сосудистой системы, скелета, развитие дисплазии соединительной ткани. Дефицит меди влечет за собой угнетение роста кости и ОП, что наблюдается при болезни Менкина, заключающейся во врожденной неспособности поглощать медь [17]. Суточная потребность колеблется от 0,9 до 3,0 мг. Физиологическая потребность для взрослых составляет 1,0 мг/сут, для детей – от 0,5 до 1,0 мг/сут. Пищевыми источниками меди являются шоколад, какао, печень, орехи, семечки, грибы, моллюски, лосось, шпинат [16].
Недостаточное потребление марганца (поступление в организм) вызывает замедление роста, нарушения в репродуктивной системе, повышенную хрупкость кости, нарушения углеводного и липидного обмена. Связано это с тем, что марганец принимает непосредственное участие в образовании костной и соединительной ткани, входит в состав ферментов, включающихся в метаболизм аминокислот, углеводов, катехоламинов. Микроэлемент необходим для синтеза холестерина и нуклеотидов. Пищевыми источниками являются зеленые листовые овощи, продукты из неочищенного зерна (пшеница, рис), орехи, чай. Среднее потребление микроэлемента с продуктами питания колеблется от 1 до 10 мг/сут. Установленный уровень потребности составляет 2–5 мг/сут. Физиологическая потребность для взрослых – 2 мг/сут [16].
Бор оказывает непосредственное влияние на метаболизм витамина D, а также снижает избыточную активность паратиреоидного гормона, который, как известно, ответственен за обмен кальция, фосфора, магния. Улучшает абсорбцию кальция, уменьшает риск развития дефицита холекальциферола, способствует предотвращению ОП. Это позволяет полагать, что влияние бора на метаболизм костной ткани аналогично действию витамина D. Бор содержится в корневых овощах, винограде, грушах, яблоках, орехах, пиве [16, 18]. Суточная потребность составляет 2–3 мг.
Сведения об исследовании микроэлементов при остеопении и ОП ограничены и противоречивы [19–22]. Особый интерес представляет работа коллектива соавторов из центров Франции, Италии и Северной Ирландии по изучению взаимосвязи между показателями нутритивного статуса цинка и биохимических маркеров ремоделирования кости у европейцев в возрасте 55–87 лет. Рандомизированное двойное слепое многоцентровое проспективное исследование (ZENITH) продолжительностью 6 мес. включало 387 здоровых мужчин и женщин. У всех определялись концентрация цинка в крови и моче, костно-специфическая щелочная фосфатаза и остеокальцин в сыворотке крови, пиридинолин и дезоксипиридинолин в моче. Установлено, что у большинства пациентов ремоделирование было нормальным, без преобладания процессов формирования или резорбции кости. Усвоение цинка отрицательно коррелировало с концентрацией пиридинолина и дезоксипиридинолина в моче, не установлено корреляции с маркерами формирования кости. Прослеживалась тенденция отрицательной корреляции цинка в сыворотке с дезоксипиридинолином в моче (r=-0,211; р=0,080). Цинк в эритроцитах имел отрицательную корреляцию с остеокальцином в сыворотке (r=-0,090; р=0,0001). После учета вмешивающихся факторов (возраст, пол, исследовательский центр) осталась единственная статистически значимая корреляция между остеокальцином в сыворотке и цинком в эритроцитах (b=-0,124; р=0,011). Таким образом, были получены некоторые данные о взаимосвязи между нутритивным статусом цинка и ремоделированием кости у здоровых взрослых [23]. Турецкие ученые установили, что концентрация магния и цинка у женщин с ОП была значимо ниже, чем у женщин с остеопенией и здоровых женщин; в свою очередь концентрация магния и цинка у женщин с остеопенией была статистически значимо ниже, чем у здоровых женщин. Статистически значимого различия между группами по концентрации меди не получено. Высказано мнение о том, что поступление микроэлементов, в особенности магния, цинка и, вероятно, меди, может оказать благоприятное воздействие на плотность костной ткани [24].
Связь между статусом остеотропных микроэлементов, характеристикой костной ткани и возможностью коррекции дефицита потребления с помощью лекарственных средств, в состав которых входят соли кальция и микроэлементы, изучена отечественными педиатрами у 100 подростков [25]. При обследовании выявлены сдвиги в содержании бора, меди, марганца и цинка, а у 46 подростков обнаружена остеопения. Авторам удалось установить взаимосвязь между содержанием микроэлементов в волосах и минеральной плотностью кости, проанализировать возможность воспроизведения состояния минеральной плотности через комплекс исследуемых микроэлементов.
В открытом проспективном наблюдении сделана попытка оценить эффективность комбинированного препарата Кальцемин для коррекции микроэлементоза и кальциевого обмена. Для этого подросткам 1-й группы назначался Кальцемин Адванс по 1 таблетке 2 р./сут (что составляло 1000 мг кальция, 400 МЕ холекальциферола, 80 мг магния, 15 мг цинка, 2 мг меди, 3,6 мг марганца и 500 мкг бората натрия), а 2-й группы – одна из лекарственных форм Кальцемина в индивидуальной дозе в зависимости от суточного потребления кальция с продуктами питания и возрастной суточной потребности, а также от наличия факторов риска остеопении и выраженности микроэлементоза, подтвержденного лабораторно. Продолжительность приема препарата составляла не менее 8–12 мес. Исследование содержания микроэлементов проводилось до назначения препарата и после окончания приема. Авторы сделали вывод, что для коррекции остеопении и профилактики ее развития целесообразно назначение комбинированных препаратов, содержащих не только кальций и витамин D3, но и микроэлементы. Применение Кальцемина позволяет корректировать содержание микроэлементов, улучшить качество костной ткани.
Эффективность Кальцемин Адванса изучена в открытом контролируемом исследовании, в которое было включено 100 женщин в возрасте от 45 до 65 лет с остеопенией. Пациентки были случайно разделены на 2 сопоставимые по основным показателям группы: 1-я группа – 50 человек, получавшие Кальцемин Адванс (по 1 таблетке 2 р./сут, что составляло 1000 мг кальция, 400 МЕ холекальциферола, 80 мг магния, 15 мг цинка, 2 мг меди, 3,6 мг марганца и 500 мкг бората натрия); 2–я группа (контрольная) – 50 женщин, не получавшие медикаментозного лечения, которым были даны рекомендации по питанию. Продолжительность исследования составила 1 год. Анализ минеральной плотности через 12 мес. наблюдения показал, что в группе, получавшей терапию Кальцемином Адванс, отмечалось стабильное состояние минеральной плотности кости, в то время как в контрольной группе она уменьшилась во всех исследуемых зонах, особенно в поясничном отделе позвоночника. Подводя итоги исследования по применению комбинированного препарата Кальцемин Адванс в течение 1 года у женщин с остеопенией, авторы сделали вывод о том, что препарат оказывает стабилизирующее влияние на минеральную плотность кости, его длительное использование не вызывает гиперкальциемии и повышения экскреции кальция с мочой, хорошо переносится. Это позволяет рекомендовать Кальцемин Адванс для профилактики постменопаузального ОП и восполнения дефицита микроэлементов [26].
Ткань как совокупность клеток и межклеточного вещества. Типы и виды тканей, их свойства. Межклеточные взаимодействия.
В организме взрослого человека различают около 200 типов клеток. Группы клеток, имеющие одинаковое или сходное строение, связанные единством происхождения и приспособленные к выполнению определенных функций, образуют ткани. Это следующий уровень иерархической структуры организма человека – переход с клеточного уровня на тканевой (смотри рисунок 1.3.2).
Любая ткань представляет собой совокупность клеток и межклеточного вещества, которого может быть много (кровь, лимфа, рыхлая соединительная ткань) или мало (покровный эпителий).
Клетки каждой ткани (и некоторых органов) имеют собственное название: клетки нервной ткани называются нейронами, клетки костной ткани – остеоцитами, печени – гепатоцитами и так далее.
Межклеточное вещество химически представляет собой систему, состоящую из биополимеров в высокой концентрации и молекул воды. В нем расположены структурные элементы: волокна коллагена, эластина, кровеносные и лимфатические капилляры, нервные волокна и чувствительные окончания (болевые, температурные и другие рецепторы). Это обеспечивает необходимые условия для нормальной жизнедеятельности тканей и выполнения ими своих функций.
Всего выделяют четыре типа тканей: эпителиальную, соединительную (включая кровь и лимфу), мышечную и нервную (смотри рисунок 1.5.1).
Эпителиальная ткань, или эпителий, покрывает тело, выстилает внутренние поверхности органов (желудка, кишечника, мочевого пузыря и других) и полостей (брюшной, плевральной), а также образует большинство желез. В соответствии с этим различают покровный и железистый эпителий.
Покровный эпителий (вид А на рисунке 1.5.1) образует пласты клеток (1), тесно – практически без межклеточного вещества – прилегающие друг к другу. Он бывает однослойным или многослойным. Покровный эпителий является пограничной тканью и выполняет основные функции: защита от внешних воздействий и участие в обмене веществ организма с окружающей средой – всасывание компонентов пищи и выделение продуктов обмена (экскреция). Покровный эпителий обладает гибкостью, обеспечивая подвижность внутренних органов (например, сокращения сердца, растяжение желудка, перистальтику кишечника, расширение легких и так далее).
Железистый эпителий состоит из клеток, внутри которых находятся гранулы с секретом (от латинского secretio – отделение). Эти клетки осуществляют синтез и выделение многих веществ, важных для организма. Путем секреции образуются слюна, желудочный и кишечный сок, желчь, молоко, гормоны и другие биологически активные соединения. Железистый эпителий может образовывать самостоятельные органы – железы (например, поджелудочная железа, щитовидная железа, железы внутренней секреции, или эндокринные железы, выделяющие непосредственно в кровь гормоны, выполняющие в организме регулирующие функции и другие), а может являться частью других органов (например, железы желудка).
Соединительная ткань (виды Б и В на рисунке 1.5.1) отличается большим разнообразием клеток (1) и обилием межклеточного субстрата, состоящего из волокон (2) и аморфного вещества (3). Волокнистая соединительная ткань может быть рыхлой и плотной. Рыхлая соединительная ткань (вид Б) присутствует во всех органах, она окружает кровеносные и лимфатические сосуды. Плотная соединительная ткань выполняет механическую, опорную, формообразующую и защитную функции. Кроме того, существует еще очень плотная соединительная ткань (вид В), из нее состоят сухожилия и фиброзные мембраны (твердая мозговая оболочка, надкостница и другие). Соединительная ткань не только выполняет механические функции, но и активно участвует в обмене веществ, выработке иммунных тел, процессах регенерации и заживления ран, обеспечивает адаптацию к меняющимся условиям существования.
К соединительной ткани относится и жировая ткань (вид Г на рисунке 1.5.1). В ней депонируются (откладываются) жиры, при распаде которых высвобождается большое количество энергии.
Важную роль в организме играют скелетные (хрящевая и костная) соединительные ткани. Они выполняют, главным образом, опорную, механическую и защитную функции.
Хрящевая ткань (вид Д) состоит из клеток (1) и большого количества упругого межклеточного вещества (2), она образует межпозвоночные диски, некоторые компоненты суставов, трахеи, бронхов. Хрящевая ткань не имеет кровеносных сосудов и получает необходимые вещества, поглощая их из окружающих тканей.
Костная ткань (вид Е) состоит их костных пластинок, внутри которых лежат клетки. Клетки соединены друг с другом многочисленными отростками. Костная ткань отличается твердостью и из этой ткани построены кости скелета.
Разновидностью соединительной ткани является и кровь. В нашем представлении кровь – это нечто очень важное для организма и, в то же время, сложное для понимания. Кровь (вид Ж на рисунке 1.5.1) состоит из межклеточного вещества – плазмы (1) и взвешенных в ней форменных элементов (2) – эритроцитов, лейкоцитов, тромбоцитов (на рисунке 1.5.2 даны их фотографии, полученные при помощи электронного микроскопа). Все форменные элементы развиваются из общей клетки-предшественницы. Подробнее свойства и функции крови рассматриваются в разделе 1.5.2.3.
Клетки мышечной ткани (рисунок 1.3.1 и виды З и И на рисунке 1.5.1) обладают способностью сокращаться. Так как для сокращения требуется много энергии, клетки мышечной ткани отличаются повышенным содержанием митохондрий.
Различают два основных типа мышечной ткани – гладкую (вид З на рисунке 1.5.1), которая присутствует в стенках многих, и, как правило полых, внутренних органов (сосуды, кишечник, протоки желез и другие), и поперечно-полосатую (вид И на рисунке 1.5.1) , к которой относятся сердечная и скелетная мышечные ткани. Пучки мышечной ткани образуют мышцы. Они окружены прослойками соединительной ткани и пронизаны нервами, кровеносными и лимфатическими сосудами (смотри рисунок 1.3.1).
Нервная ткань (вид К на рисунке 1.5.1) состоит из нервных клеток (нейронов) (1) и межклеточного вещества (2) с различными клеточными элементами (3), называемыми в совокупности нейроглией (от греческого glia – клей). Основным свойством нейронов (нейрон обозначен цифрой 7 на рисунке 1.3.4) является способность воспринимать раздражение, возбуждаться, вырабатывать импульс и передавать его далее по цепи. Они синтезируют и выделяют биологически активные вещества – посредники (медиаторы).
Нервная система регулирует функции всех тканей и органов, объединяет их в единый организм путем передачи информации по всем звеньям и осуществляет связь с окружающей средой.
Обобщающие сведения по тканям приведены в таблице 1.5.1.
Таблица 1.5.1. Ткани, их строение и функции
Сохранение формы и выполнение специфических функций тканью генетически запрограммировано: дочерним клеткам посредством ДНК передается способность к выполнению специфических функций и к дифференцированию. О регуляции экспрессии генов, как основе дифференцировки, было сказано в разделе 1.3.4.
Дифференцировка – это биохимический процесс, при котором относительно однородные клетки, возникшие из общей клетки-предшественницы, превращаются во все более специализированные, специфические типы клеток, формирующие ткани или органы. Большинство дифференцированных клеток обычно сохраняет свои специфические признаки даже в новом окружении.
В 1952 году ученые из Чикагского университета осуществили разделение клеток куриного эмбриона, выращивая (инкубируя) их в растворе фермента при осторожном помешивании. Однако клетки не оставались разделенными, а начинали объединяться в новые колонии. Более того, при смешивании печеночных клеток с клетками сетчатки глаза образование клеточных агрегатов происходило так, что клетки сетчатки всегда перемещались во внутреннюю часть клеточной массы.
Взаимодействия клеток. Что же позволяет тканям не рассыпаться при малейшем внешнем воздействии? И чем обеспечивается слаженная работа клеток и выполнение ими специфических функций?
Множество наблюдений доказывает наличие способности у клеток распознавать друг друга и соответствующим образом реагировать. Взаимодействие – это не только способность передавать сигналы от одной клетки к другой, но и способность действовать совместно, то есть синхронно. На поверхности каждой клетки располагаются рецепторы (смотри раздел 1.3.2), благодаря которым каждая клетка распознает другую себе подобную. И функционируют эти “детекторные устройства” согласно правилу “ключ – замок” – этот механизм неоднократно упоминается в книге.
Давайте немного поговорим о том, как клетки взаимодействуют друг с другом. Известно два основных способа межклеточного взаимодействия: диффузионное и адгезивное. Диффузионное – это взаимодействие на основе межклеточных каналов, пор в мембранах соседних клеток, расположенных строго напротив друг друга. Адгезивное (от латинского adhaesio – прилипание, слипание) – механическое соединение клеток, длительное и стабильное удерживание их на близком расстоянии друг от друга. В главе, посвященной строению клетки, описаны различные виды межклеточных соединений (десмосомы, синапсы и другие). Это является основой для организации клеток в различные многоклеточные структуры (ткани, органы).
Каждая клетка ткани не только соединяется с соседними клетками, но и взаимодействует с межклеточным веществом, получая с его помощью питательные вещества, сигнальные молекулы (гормоны, медиаторы) и так далее. Посредством химических веществ, доставляемых ко всем тканям и органам тела, осуществляется гуморальный тип регуляции (от латинского humor – жидкость).
Другой путь регуляции, как уже упоминалось выше, осуществляется с помощью нервной системы. Нервные импульсы всегда достигают цели в сотни или тысячи раз быстрее доставки к органам или тканям химических веществ. Нервный и гуморальный способы регуляции функций органов и систем тесно между собой взаимосвязаны. Однако само образование большинства химических веществ и выделение их в кровь находятся под постоянным контролем нервной системы.
Клетка, ткань – это первые уровни организации живых организмов, но и на этих этапах можно выделить общие механизмы регуляции, обеспечивающие жизнедеятельность органов, систем органов и организма в целом.
Соединительные ткани играют огромную роль в строении организма, хотя и не отвечают напрямую за функционирование органов. Однако без их вспомогательной роли системы органов работать не смогут, да и процентное соотношение этих тканей в организме велико. Соединительные ткани — внутренние, нигде не взаимодействуют с внешней средой.
Клетки соединительных тканей разнятся по форме, а находящееся между ними межклеточное вещество, как правило, очень развито. В крови и лимфе оно жидкое, подвижное, в костях гораздо более плотное. Несмотря на вроде бы радикальные различия во внешнем виде и строении собственно соединительной ткани (волокно, жир), скелетной ткани (кость, хрящ) и крови с лимфой, все они происходят из зародышевого листка мезодермы.
Функции соединительной ткани
1. Пластическая — обеспечивает процесс регенерации, без нее живые организмы не имели бы возможности устранить повреждения, заживить раны.
2. Защитная — состоит в механической защите (за это отвечает костная ткань) и обезвреживании различных веществ, проникающих снаружи или образующихся внутри (иммунная защита).
3. Трофическая — связана с питанием тканевых структур, с обменом веществ и поддержанием в организме неизменного состава внутренней среды.
4. Опорная — реализуется благодаря минерализации межклеточного вещества скелетных тканей и эластичным волокнам, образующим волокнистые основы всех органов.
Виды соединительной ткани
1. Рыхлая волокнистая соединительная ткань есть во всех органах, имеет клетки разных форм, причем они преобладают над межклеточной жидкостью. Формирует футляры сосудов, нервов, входит в состав кожи.
3. Жировая ткань имеет сходство с рыхлой волокнистой, клетки ее заполняет жир. Находится в подкожно-жировом слое, внутри органов. Делится на белую (хранит воду, энергию, витамины) и бурую (очень важна для младенцев, потому что отвечает за теплообразование).
4. Кровь — жидкая ткань, заполняющая сердечно-сосудистую систему, переносящая, словно река, кислород, углекислый газ, комплекс различных элементов и гормонов. Клеточные элементы крови: белые лейкоциты, красные эритроциты и кровяные пластинки тромбоциты. Желтовато-соломенная водянистая плазма — межклеточная жидкость крови, составляющая 50–60 процентов объема.
5. Лимфа — еще одна жидкая ткань. Она омывает лимфатические сосуды, узлы и попадает в кровь. Подобно крови, состоит из плазмы (где меньше белков, чем в плазме крови) и клеток: лимфоцитов, моноцитов и др., но не содержит эритроцитов.
6. Хрящевая ткань — отличается значительным преобладанием матрикса, межклеточного вещества. На хондроциты (зрелые клетки) и хондробласты (незрелые, основа для формирования хондроцитов) отводится всего 10 процентов объема. Клетки разбросаны, они напоминают островки в океане, только океан этот не текучий, а плотный. Упругость хряща зависит от присутствия в нем воды, связанной со сложными белками протеогликанами. Хрящевые ткани делятся на три подвида. Первый, гиалиновый хрящ имеется в составе ребер, грудины, суставных поверхностей костей, воздухоносных полостей (хрящи носа, гортани). Эластический хрящ — также в составе гортани, наружного уха и слухового прохода. Наконец, волокнистый хрящ, содержащий пучки коллагеновых волокон, — в составе межпозвонковых дисков и связок.
7. Костная ткань — строится из костных пластинок, заполненных межклеточным веществом (и здесь важны коллагеновые волокна) и клетками, которые соединяются отростками. Содержит значительное количество фосфатов кальция и магния. Интересно, что у молодых организмов костная ткань достаточно мягкая и гибкая, но с возрастом становится все более твердой, теряет эластичность. Имеет три вида клеток: остеоциты (зрелые, связанные костными канальцами), остеобласты (молодые, продуцирующие органические вещества, например, коллаген) и остеокласты (крупные многоядерные, находящиеся на поверхности костной ткани и обеспечивающие разрушение кости или хряща).
Хочешь сдать экзамен на отлично? Жми сюда - онлайн тесты по биологии

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Соединительная ткань (textus connectivus) представляет собой большую группу тканей, включающую собственно соединительные ткани (рыхлая и плотная волокнистые), ткани со специальными свойствами (ретикулярная, жировая), жидкие (кровь) и скелетные (костная и хрящевая). Эти ткани выполняют многие функции: опорную, механическую (собственно соединительные ткани, хрящ, кость), трофическую (питательную), защитную (фагоцитоз и транспорт иммунокомпетентных клеток и антител). Соединительные ткани сформированы из многочисленных клеток и межклеточного вещества, состоящего из протеогликанов и гликопротеинов (адгезивных белков), а также различных волокон (коллагеновых, эластических, ретикулярных).
Все виды соединительной ткани являются производными мезенхимы, которая, в свою очередь, образуется из мезодермы
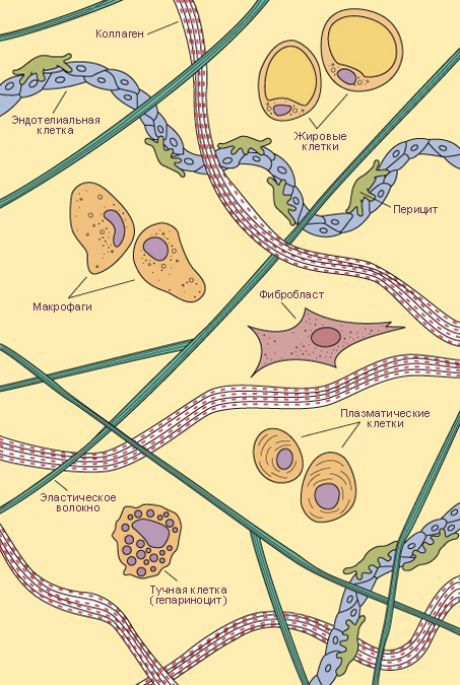

[1], [2], [3]
Клетки соединительной ткани
Фибробласты являются основными клетками соединительной ткани. Они веретенообразные, от поверхности фибробластов отходят тонкие короткие и длинные отростки. Количество фибробластов в разных типах соединительной ткани различное, особенно много их в рыхлой волокнистой соединительной ткани. Фибробласты имеют овальное ядро, заполненное мелкими глыбками хроматина, четко различимыми ядрышком и базофильной цитоплазмой, содержащей множество свободных и прикрепленных рибосом.

[4], [5], [6]
Волокнистые соединительные ткани
Волокнистые соединительные ткани включают рыхлую и плотную волокнистые соединительные ткани. Плотная волокнистая соединительная ткань, в свою очередь, имеет две разновидности - неоформленную и оформленную плотную соединительную ткань.

[7], [8], [9], [10], [11], [12]
Ткани со специальными свойствами
К соединительным тканям со специальными свойствами относятся жировая, ретикулярная и слизистая. Они расположены лишь в определенных органах и участках тела и характеризуются особыми чертами строения и своеобразными функциями.

[13], [14], [15]
Кровь
Плазма крови представляет собой жидкость, остающуюся после удаления из нее форменных элементов - клеток. Она содержит 90-93 % воды, 7-8 % различных белковых веществ (альбумины, глобулины, липопротеиды, фибриноген), 0,9 % солей, 0,1 % глюкозы. В плазме крови имеются также ферменты, гормоны, витамины и другие необходимые организму вещества. Белки плазмы участвуют в процессе свертывания крови, обеспечивают постоянство ее реакции (рН 7,36), давления в сосудах, вязкость крови, препятствуют оседанию эритроцитов. В плазме крови содержатся иммуноглобулины (антитела), участвующие в защитных реакциях организма.
Содержание глюкозы в крови у здорового человека составляет 80-120 мг% (4,44-6,66 ммоль/л). Резкое уменьшение количества глюкозы (до 2,22 ммоль/л) приводит к резкому повышению возбудимости клеток мозга. Дальнейшее снижение содержания глюкозы в крови ведет к нарушению дыхания, кровообращения, сознания и может быть смертельным для человека.

[16], [17], [18], [19], [20]
Читайте также:

