Кратко опишите что собой представляет феррит аустенит цементит ледебурит перлит
Обновлено: 05.07.2024
Фазовые диаграммы представляют собой изображение зон существования фаз, которые имеются в сплаве при различных условиях (температура, давление, химсостав).
Диаграмма железо углерод описывает подходящие условия для существования двух или более фаз в равновесии. Популярная аналогия: фазовая диаграмма воды описывает точку (тройную точку), в которой вода может сосуществовать в трёх разных фазах одновременно. Это происходит при температуре чуть выше точки замерзания (0,01 ° C) и при давлении 0,006 атм.
Существует четыре основных применения фазовых диаграмм:
- Разработка новых сплавов на основе требований применения.
- Производство этих сплавов.
- Разработка и контроль соответствующих процедур термообработки, которые предназначены для улучшения химических, физических и механических свойств сплавов.
- Устранение проблем, возникающих при применении новых сплавов, что в конечном итоге улучшает предсказуемость свойств продукта.
При разработке сплава фазовые диаграммы помогают предотвращать проектирование чрезмерно большого количества вариантов, сокращая затраты и время обработки. Они также помогают разрабатывать альтернативные сплавы или такие же, но с альтернативными легирующими элементами.
Компонентный состав
Диаграмма железо-углерод была разработана, чтобы показать микроструктурное состояние металла как функцию температуры и содержания углерода. Она показывает, что, в зависимости от интенсивности охлаждения стали, в ней могут возникать очень разные микроструктуры.
Когда металл расплавлен, то есть находится в жидком состоянии, решётчатые структуры отсутствуют. Атомы могут свободно перемещаться во всех направлениях. Чтобы достичь желаемых кристаллических структур, необходимо, чтобы металл медленно и полностью остыл при комнатной температуре. Промежуточные термические обработки положительно влияют на формирование кристаллических структур.
По вертикальной оси диаграммы железо-углерод располагается шкала температур в °C. Металл показан здесь от твердого до жидкого состояния. Например, чистое железо начинает плавиться при 1147°C. Температура устойчивого состояния расплава - 1536 °C.
По горизонтальной оси указывается процентное содержание углерода в металле.
Диаграмма показывает участки, в которых металл находится только в состоянии. расплава, феррита или аустенита. Остальные зоны характеризуются определённым сочетанием свойств. Это, например, расплав и аустенит, аустенит и феррит, феррит и перлит.
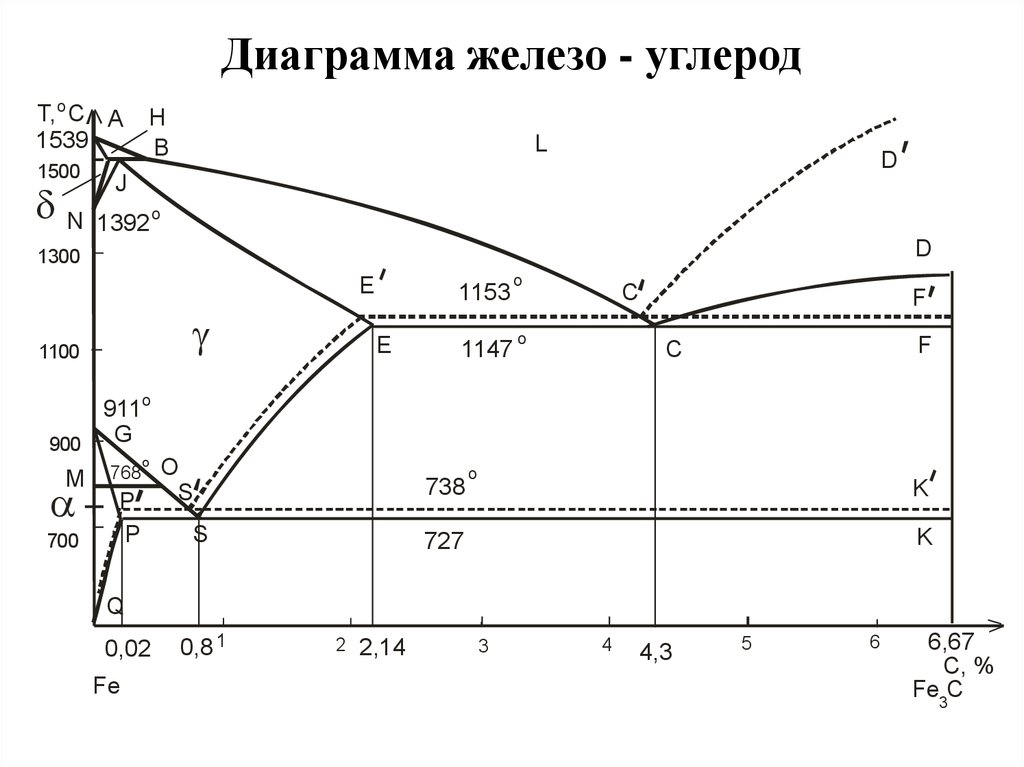
Обозначение точек пересечения заглавными буквами на линиях преобразования предназначено для лучшего понимания. Они указывают на переход в другое состояние или условие.
Диаграмма предполагает постоянное охлаждение металлов. Если металл медленно охлаждать, образуются крупные зёрна, если же металл остывает быстро, то размеры зёрен уменьшаются. Тип зерна металла определяет его прочностные свойства. Крупнозернистый материал имеет меньшую прочность, но его можно сделать более мелким и, следовательно, более прочным путём термической обработки или пластического деформирования (упрочнением). Самый высокий уровень прочности имеет именно мелкозернистый металл.
Выполним краткую характеристику основных химических компонентов диаграммы.
Железо
Железо образует кубическую пространственную решётку. Атомы железа расположены по углам этой решётки. Количество углерода, которое может быть растворено в железе, зависит от модификации железа, потому что разные формы кристаллической решетки железа (например, кубическая пространственно-центрированная и кубическая гранецентрированная) имеют межстраничные промежутки разного размера.
Второстепенную роль играет дельта-смешанный кристалл, который имеет объемно-центрированные атомы, но существует только в высоколегированных сталях. Эти кристаллы образуются в диапазоне температур от 1536 °C (точка плавления чистого железа) до 1392 °C.
Альфа-смешанный кристалл существует как объемно-центрированная кубическая решетка. Эти структуры образуются в чистом железе до температуры 911 °C.
В гамма смешанном кристалла атомы железа гранецентрированы, и это означает, что они расположены в середине каждой грани куба. Эти кристаллы образуются при температурах от 1392 °C до 911 °C в чистом железе.
Углерод
В низких концентрациях, углерод не образует твёрдого химического соединения с железом, но откладывается в промежутках кристаллической решетки железа.
Углерод в железе является примесью внедренияи может существовать в форме гранецентрированную или объемно-центрированной кубической решётки. Диаграмма состояния сплавов железо-углерод устанавливает области стабильного существования твёрдого раствора с α, γ и δ фазами железа.
Описанные выше кристаллические решётки имеют различную растворимость углерода в зависимости от температуры. Углерод осаждается в междуузельных пространствах кристаллической решётки, при этом гранецентрированная кубическая решетка, также называемая аустенитом, имеет растворимость не более чем в сто раз выше, чем кристаллы феррита.
Цементит
Цементит - метастабильная фаза сплава с фиксированным составом, имеющий химическую формулу Fe3C. При комнатной температуре цементит очень медленно разлагается на железо и углерод (графит).
Некоторые другие факторы (например, высокие температуры и добавление определенных легирующих элементов) могут влиять на это разложение, поскольку они способствуют образованию графита.
Цементит твёрдый и хрупкий, что делает его пригодным для упрочнения сталей (существует специальная технология химико-термической обработки стали, которая называется цементацией). Механические свойства цементита зависят от его микроструктуры, а также от условий связи с ферритом.
Жидкий раствор Fe-C на диаграмме обозначается выше линии L (ликвидус). Поскольку δ-феррит плавится при 1538 °C, очевидно, что температура плавления железа снижается с увеличением содержания углерода.
Перлит
Зёрна перлита включают в себя структурные объединения, где все образовавшиеся пластины между собой параллельны. При возрастании числа перлитных конкреций рост размеров пластин приостанавливается, а сами они могут изменить направление своего движения. С уменьшением температуры колонии перлита превращаются в шаровидные мелкозернистые образования.
Ледебурит в сталях
Ледебурит - один из основных структурных компонентов железоуглеродистых сплавов и является эвтектическую смесью аустенита и цементита, которая образуется при 1145°C и ниже (для чистых железоуглеродистых сплавов). Аустенит превращается в ферритно-цементитную смесь при температурах ниже 723°C. В сталях ледебурит, состоящий из аустенита и карбидов, образуется только при очень высоком содержании компонентов сплава и углерода (0,7…1,0%); такие стали (называются ледебуритовыми сталями.
Метастабильная нелегированная эвтектика ледебурита Fe – Fe3C классифицируется как квазирегулярная. Доказано, что после зарождения Fe3C рост пластин цементита происходит быстро, в результате на стыках образуется аустенит, и возникает взаимосвязь ориентации. Fe3C и аустенит также растут совместно и образуют стержневую структуру, которая располагается перпендикулярно пластинам цементита. Эти два режима роста образуют квазирегулярную структуру, но рост по краю происходит быстрее, чем по бокам, и доминирует в структуре. Эксперименты по направленной кристаллизации показали, что рабочая точка на кривой роста квазирегулярной структуры близка к точке экстремума. Такую квазирегулярную структуру можно модифицировать закалкой, но модификация примесей пока не исследовалась.
Структурная подложка сталей ледебуритного класса имеет доэвтектические компоненты, включающие перлит, ледебурит и шаровидный графит. Легированный слой состоит из дендритов и междендритов. В чугуне с шаровидным графитом конкреции графита постепенно растворяются в ванне расплава, и в то же время под действием гидродинамических сил и сил текучести перемещаются к поверхности.

Фазы в системе “железо-углерод”
Фазы - это физически однородные состояния сплава. Фаза имеет точный химический состав - определенное расположение и связь между атомами. Такая структура атомов придает разные свойства различным фазам.
Некоторые специальные сплавы могут существовать в нескольких фазах, что достигается нагревом металла до определенных температур и использованием разных процедур термообработки.
Жидкая
Существует при температуре, которая превышает 1457 o C. Фазовое превращение при этой температуре означает полное плавление, поэтому на диаграмме жидкая фаза всегда обозначается линией L.
Феррит
На диаграмме присутствует в трёх разных фазах:
- Фаза дельта-феррита (δ-Fe) представляет собой твердый раствор C в δ-Fe (ОЦК) в высокотемпературной области диаграммы. Раствор стабилен при температуре выше 1400 °C и плавится при температуре выше 1539 °C. Структурно подобен α-ферриту;
- Фаза гамма-феррита (γ-Fe) является твёрдым раствором C в γ-Fe, который называют аустенитом. Нестабилен ниже температуры 910 °C, превращаясь в δ-феррит при 1395 ° C.. Максимальная растворимость углерода составляет около 2,1% при 1147 °C. Аустенит мягок и пластичен, не обладает магнитными свойствами;
- Фаза альфа-феррита (α-Fe) представляет собой твердый раствор C в α-Fe с ОЦК-решёткой. Считается самой стабильной формой железа при комнатной температуре. Максимальная растворимость углерода составляет около 0,02% при 727 °C. Мягче аустенита, магнитен.
Аустенит в сталях
Аустенит всегда присутствует в нержавеющих сталях, которые содержат от 16 до 26 процентов хрома и до 35 процентов никеля. Аустенитные стали, помимо высокой коррозионной стойкостью, не закаливаются при термической обработке и немагнитны.

Формы существования цементита важны для определения коррозионной стойкости сталей. Доказано, что цементит (Fe3C) увеличивает скорость коррозии, причём этот эффект более выражен, когда он образует когерентную сеть на поверхности. В нормализованных сталях цементит образует когерентную сетку, а в отпущенном мартенсите - нет. Поэтому цементит влияет на скорость коррозии нормализованной, но не закалённой стали.
В целом скорость коррозии углеродистой стали снижается с увеличением содержания хрома из-за образования защитного оксида хрома. Однако, когда хром соединяется с углеродом с образованием карбида хрома, положительный эффект хрома теряется.
Влияние микроструктуры различных низколегированных сталей, показанное на этой модели, распространяется только на условия, в которых не образуются защитные плёнки. Более того, образование карбидной сетки на поверхности нормализованной стали - процесс, зависящий от времени.
Узловые критические точки

В этих точках происходят эвтектические реакции, при которых жидкая фаза затвердевает и превращается в смесь двух твердых фаз. Это происходит при охлаждении жидкого сплава эвтектического состава до его эвтектической температуры.
Сплавы, образующиеся на этом этапе, известны как эвтектические сплавы. Слева от этой точки сплавы называются заэвтектическими, а справа – заэвтектическими.
Значение линий диаграммы
Границы, пересекающиеся друг с другом, отмечают определенные области на диаграмме. Внутри каждой зоны может существовать отдельная фаза или две фазы. На границе происходит фазовый переход. Эти области являются фазовыми полями, они указывают фазы, присутствующие для определенного состава и температуры сплава.
На диаграмме имеется несколько характерных линий, обозначаемых как A1, A2, A3, A4 и ACM. При повышении или понижении температуры металла на этих границах происходит фазовый переход. Обычно при нагревании сплава его температура повышается, но вдоль этих линий нагрев приводит к перестройке структуры в другую фазу, и, таким образом, температура перестаёт расти до тех пор, пока фаза полностью не изменится. Этот процесс называется термической остановкой.
Элементы легированной стали - никель, марганец, хром, и молибден - влияют на положение этих границ на фазовой диаграмме. Границы могут сдвигаться в любом направлении в зависимости от используемого элемента. Например, на диаграмме состояния железа и углерода добавление никеля понижает границу A3, а добавление хрома увеличивает её.
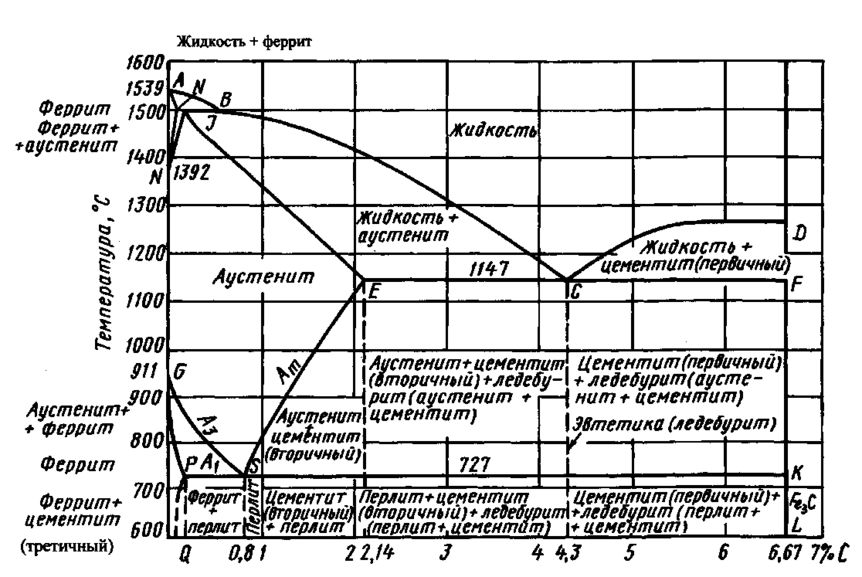
К основным составляющим структуры различных чугунов, определяющим их свойства, помимо графита относят феррит, цементит, перлит, аустенит, ледебурит. Феррит —твердый раствор углерода (до 0,02%) в α -железе. Железо существует в виде различных разновидностей (α, β, ү и δ-аллотропных модификаций), различающихся по кристаллической структуре или по магнитным свойствам. Устойчивым при обычной температуре и нагреве вплоть до 769°С является α-железо, обладающее магнитными свойствами. При более высоких температурах (до 910°С) происходит переход его в β-железо, а в интервале температур 910—1440°С устойчиво ү-железо, отличающееся от α -модификации структурой и не обладающее магнитными свойствами. Структуру с ү-модификацией железа можно получить (и сохранить в отливке при обычной температуре) путем быстрого охлаждения с температуры 910—1140°С.
В феррите могут быть растворены также кремний, марганец, фосфор и другие элементы. Феррит мягок и пластичен, если не содержит легирующих примесей, повышающих его прочность, твердость, хрупкость.
Цементит (карбид железа) представляет собой химическое соединение (Fe3C), содержащее 93,33% железа и 6,67% углерода; является наиболее твердой и хрупкой составляющей чугунов.
Перлит — эвтектоидная механическая смесь цементита и феррита. Мельчайшие частицы цементита, находящиеся в пластичной массе феррита, придают этой смеси хорошие прочностные свойства. В перлите содержится 0,83% углерода.
Аустенит — твердый раствор углерода (до 2,14%) в ү-железе. Аустенит немагнитен.
Ледебурит — эвтектическая механическая смесь аустенита и цементита, образующаяся при температурах ниже 1145°С. Содержание углерода в ледебурите 4,3%. При нормальной температуре ледебурит представляет собой смесь цементита и перлита.
На процесс формирования структуры чугунных отливок оказывает влияние ряд факторов; к наиболее существенным из них относят химический состав чугуна, температуру перегрева его перед заливкой в форму и скорость охлаждения отливки. Структуру металла готовой отливки можно изменять термической обработкой.
По химическому составу чугуны разделяют на нелегированные и легированные. Обычно в чугунах содержится (помимо железа) 2,4—3,6% углерода, 0,5—3% кремния, 0,2—1,0% марганца, 0,04—0,8% фосфора, 0,02— 0,2% серы. Как основные, так и легирующие элементы оказывают различное влияние на графитизацию чугуна. В приведенном ниже ряду элементы расположены в зависимости от их влияния на графитизацию (слева — способствующие графитизации, справа — тормозящие ее, в середине — не оказывающие на этот процесс существенного влияния): Al, С, Si, Ti, Ni, Cu, Р Со, Zr, Nb, W, Мп, Mo, S, Cr, V, Те, Mg, Sr, B.
Таким образом, постоянные компоненты чугуна С и Si оказывают сильное графитизирующее действие, а Мп и S тормозят выделение свободного графита. Большое влияние суммарного содержания углерода и кремния на структуру чугуна показано многими исследователями. Предложены структурные диаграммы, типа приведенной на рис. 5.2 диаграммы Маурера. Наклонные линии делят диаграмму на пять областей, каждой из который соответствует определенная структура чугуна: I — белый чугун (перлит+цементит), IIа— половинчатый чугун (перлит+цементит+феррит), II — серый перлитный чугун (феррит+графит), 116— серый перлитно-ферритный чугун (перлит4-феррит+графит), III — серый ферритный чугун (феррит+графит). Схематическое изображение этих структур показано на рис. 5.3. Из диаграммы (см. рис. 5.2) следует, например, что при одном и том же содержании углерода (3,0%) будет получаться белый чугун, если содержание кремния не превышает 0,8%, серый перлитный — при 1,1 до 2% Si и при 2,8% и более — серый ферритный чугун. Таким образом, регулируя суммарное количество углерода и кремния в расплаве чугуна, а также скорость охлаждения его в форме, можно получать отливки с различной структурой.

Рис. 5.2. Диаграмма Маурера:
I — белый чугун (перлит + цементит), IIа — половинчатый чугун (перлит + цементит + феррит), II — серый перлитный чугун (феррит + + графит), IIб — серый перлитно-ферритный чугун (перлит + феррит + графит), III — серый ферритный чугун (феррит + графит)
Внимательно всмотревшись в излом металла, ясно можно увидеть, что он представляет собой нагромождение (совокупность) отдельных кристаллов (зерен), крепко сцепленных между собой. Мельчайшей частицей металла, как и всякого другого вещества, является атом. В элементарных ячейках, из которых состоят кристаллы железа, атомы расположены в определенном порядке. Это расположение изменяется в зависимости от температуры нагрева. При любой температуре ниже 910° атомы в ячейках кристаллов располагаются в виде куба, образуя так называемую кристаллическую решетку альфа-железа. В этом кубе восемь атомов расположены в углах решетки и один в центре.
При нагреве свыше 910° происходит перегруппировка атомов и кристаллическая решетка представляет собою форму куба с четырнадцатью атомами; условно ее называют решеткой гамма-железа. При температуре 1390° решетка гамма-железа перестраивается в решетку с девятью атомами, носящую название дельта-железо. Эта решетка отличается от решетки альфа-железа несколько большим расстоянием между центрами атомов и сохраняется до момента расплавления железа, т. е. до 1535° (Рис. 1).
Перестройка кристаллической решетки при медленном охлаждении происходит в обратном порядке: дельта-железо при 1390° превращается в гамма-железо, а гамма-железо при 898° превращается в альфа-железо.
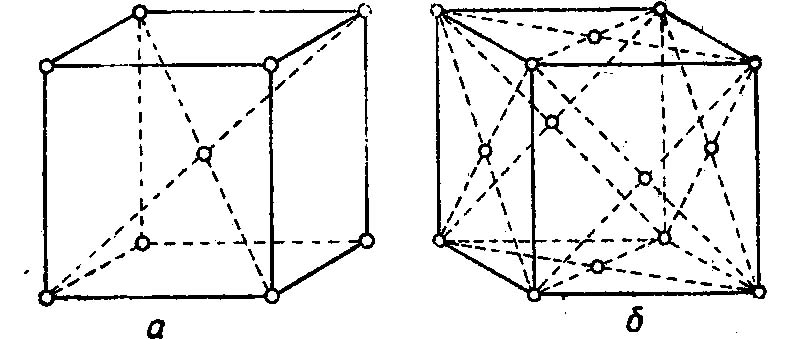
Рис. 1. Строение кристаллической решетки: а — альфа и дельта железа; б — гамма железа.
Критические точки превращения
На рис.2 показаны кривые охлаждения и нагревания чистого железа. Как видно из этих кривых, в процессе перестройки одной решетки в другую, а также при расплавлении и затвердевании железа происходят температурные остановки, являющиеся результатом выделения дополнительного количества тепла при охлаждении и поглощении дополнительного количества тепла при нагревании.
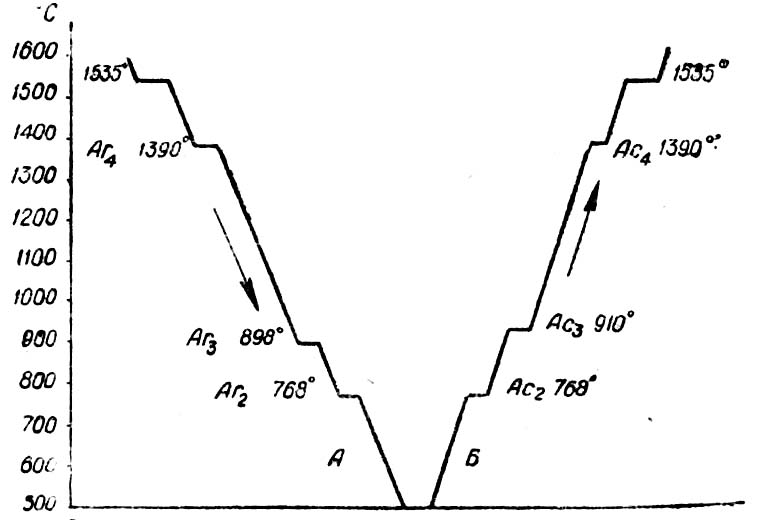
Рис. 2. Кривые охлаждения и нагрева чистого железа.
Температурные остановки, при которых происходят перестройки решеток, называются критическими температурами или критическими точками и обозначаются Аrпри охлаждении и Ас при нагревании. В точках Аr2и Ас2,не происходит перестройка атомной решетки, а изменяются магнитные свойства железа. При температуре выше 768° железо теряет способность притягиваться магнитом. При очень малой скорости нагревания и охлаждения критические точки А с3и Аr3не совпадают друг с другом на 12°. При увеличении скорости охлаждения несовпадение критических точек увеличивается, так как температура значительно снижается и железо переохлаждается. Это явление, носит название гистерезис.
При нагревании и охлаждении стали происходит также перестройка атомной решетки, но температуры критических точек не постоянны. Они зависят от содержания углерода и легирующих примесей в стали, а также от скорости нагревания и охлаждения.
На рис. 3 представлена диаграмма состояния углеродистой стали при медленном охлаждении и нагревании.
Рис.3. Диаграмма состояния углеродистых сталей.
Структура стали
Структурой стали называется внутреннее ее строение. Углерод в стали находится в виде химического соединения с железом, и это соединение называется — цементит. Кроме цементита, в стали имеется феррит, представляющий собой почти чистое железо. В зависимости от содержания углерода большая или меньшая часть феррита находится в механической смеси с цементитом, образуя новую структуру — перлит. Если небольшой кусок металла прошлифовать, отполировать и протравить в специальном реактиве, то под микроскопом можно различить структуры. Ниже приводится описание структур железоуглеродистых сплавов.
Аустенит представляет собою твердый раствор углерода и других элементов в гамма-железе. Наибольшее содержание углерода, которое может раствориться в ау-стените — это 2%. Аустенит образуется при затвердевании жидкой стали и при нагреве твердой стали выше критических температур.
В обычных сталях аустенит устойчив только лишь при температуре выше критических точек. При охлаждении, даже самом быстром, с этих температур аустенит превращается в другие структуры. При комнатной температуре аустенит полностью сохраняется в ряде марок нержавеющих сталей, в высокомарганцовистой стали и в незначительном количестве остается при закалке некоторых марок инструментальной и конструкционной сталей.
Аустенит мягок, пластичен, тягуч, мало упруг. Твердость его по Бринелю находится в пределах 170—220.
Аустенит немагнитен, обладает невысокой электропроводностью.
Феррит представляет собой твердый раствор углерода и других элементов в альфа-железе. Наибольшее содержание углерода, которое может раствориться в феррите, это 0,04%. Феррит устойчив при температурах ниже критической точки AC1. Он выделяется из аустенита при медленном охлаждении последнего ниже A6i. Феррит мягок, сильно тягуч. Твердость HB= 60—100. Феррит магнитен до 768°. Свыше этой температуры он теряет магнитные свойства.
Цементит представляет собой химическое соединение железа с углеродом Fe3C—карбид железа. Цементит содержит углерода 6,67%. Выделяется из жидкого и твердого раствора при медленном охлаждении. Цементит весьма тверд и хрупок. Твердость его НB= 800—820. Он магнитен до 210°. Выше этой температуры цементит теряет магнитные свойства.
Перлит представляет собой механическую смесь феррита и цементита. Он образуется из аустенита при медленном его охлаждении. Температура превращения аустенита в перлит 723°С. При весьма медленном переходе через эту температуру цементит образуется в виде зерен (глобулей), и тогда перлит называется зернистым. При более быстром охлаждении цементит приобретает форму пластинок, и такой перлит называется пластинчатым. При весьма быстром охлаждении в результате значительного переохлаждения аустенита вместо перлита получаются другие структуры, о которых речь будет ниже.
Перлит магнитен, прочен и пластичен. Твердость его находится в пределах от 160 до 230 кг/мм 2 по Бринелю. При обработке резанием наиболее чистую поверхность дает структура зернистого перлита.
Мартенсит образуется в результате весьма быстрого охлаждения (закалки) аустенита. При быстром охлаждении успевает произойти перестройка кристаллической решетки гамма-железа в решетку альфа-железа, выделение же углерода в карбид железа не успевает произойти, и он весь остается растворенным в решетке альфа-железа. Так как нормально альфа-железо может растворить в себе не более 0,04% углерода, то такой раствор называют пересыщенным. Он отличается весьма большой твердостью (свыше Rc= 60) и хрупкостью. Следует указать, что решетка альфа-железа, получающаяся в результате закалки, имеет искаженную форму. Так, размеры ее граней не одинаковы — в одном направлении они удлинены за счет других (см. рис. 4). Такая решетка называется тетрагональной. Чем больше в стали углерода, тем больше тетрагональность решетки и тем более велики внутренние напряжения. При нагревании до температур 100—200° тетрагональность мартенсита уменьшается, форма кристаллической его решетки приближается к форме правильного куба, и вместе с этим уменьшаются внутренние напряжения. Мартенсит магнитен.
Рис. 4. Строение кристаллической решетки стали, закаленной на мартенсит.
Троостит представляет собой высокодисперсную (мелкораздробленную) смесь феррита и карбидов. Он образуется при охлаждении аустенита с замедленной против закалки скоростью или в результате нагрева (отпуска) мартенсита в пределах 250—400°.
При нагреве закаленной стали происходит постепенное выделение углерода из кристаллической решетки с образованием карбидов. Троостит менее прочен, более пластичен, чем мартенсит. Твердость его НB330—400. При охлаждении аустенита в горячих средах в интервале 250—400° (изотермическое превращение аустенита) происходит образование игольчатого троостита, несколько более прочного, чем обычный троостит.
Сорбит представляет собой дисперсную смесь феррита и карбидов. Он образуется при охлаждении аустенита с небольшой скоростью или при нагреве (отпуске) мартенсита до 400—650°. Карбиды сорбита более крупные, чем троостита. Сорбит пластичен, вязок и магнитен. Твердость НВ 270—320.
Ледебурит представляет собой эвтектическую смесь аустенита и цементита. Он содержит углерода 4 3% Образуется ледебурит при затвердевании жидкого сплава с содержанием углерода свыше 2%. Ледебурит хрупок.
На рис. 5. представлены фотоснимки структур стали с различным содержанием углерода.
Структура стали с содержанием углерода 0,83% состоит из сплошного перлита и называется эвтектоидной; при меньшем содержании углерода структура стали состоит из перлита и феррита и носит название доэвтектоидной, а при большем содержании углерода — из перлита и цементита и называется заэвтектоидной. Температура 723°, при которой перлит переходит в аустенит, также называется критической и обозначается Ас.
Для того чтобы доэвтектоидную и эвтектоидную сталь полностью отжечь, нормализовать или закалить, их нужно нагреть до такой температуры, при которой они перешли бы в аустенитное состояние.
Рис. 5. Микроструктура отожженной углеродистой стали:
а - с содержанием углерода -0,1%
б - с содержанием углерода -0,85%
в - с содержанием углерода -1,1%
Превращения, происходящие в стали при нагревании
По диаграмме на рис. 3 можно проследить за изменениями структуры трех разных марок стали при нагревании:
- Сталь с содержанием углерода 0,83%. Структура стали представляет собой перлит. При температуре 723° в точке Aс1 перлит переходит в аустенит.
- Сталь с содержанием углерода 0,4%. Структура стали представляет собой перлит и феррит. При температуре 723° в точке К1 перлит переходит в аустенит, и по мере повышения температуры происходит растворение свободного феррита в аустените. При пересечении линии GS в точке К2 закончится растворение феррита и структура будет полностью состоять из аустенита. Для этой стали точка К1на диаграмме будет нижней критической точкой Ас1,а К2— верхней критической точкой Ас1,.
- Сталь с содержанием углерода 1,2%. Структура стали представляет собой перлит и цементит. При температуре 723° в точке Pi перлит переходит в аустенит, и при дальнейшем повышении температуры происходит постепенное растворение цементита в аустените. При пересечении линии SEв точке Р2 это растворение закончится. Для этой стали точка Р1 явится нижней критической точкой Ас1, а точка Ρ2 — верхней критической точкой, которая для заэвтектоидных сталей обозначается Асm.
Линия на диаграмме, обозначенная буквами GS, соответствует окончанию растворения феррита в аустените в доэвтектоидных сталях, а линия SE соответствует окончанию растворения цементита в аустените в заэвтектоидных сталях.
Следует указать, что заэвтектоидные стали при операциях термической обработки не нагревают выше линии Аcт(такая высокая температура нагрева приведет к перегреву и ухудшению свойств стали), а ограничиваются нагревом выше первой критической точки ACl, что полностью обеспечивает получение необходимых свойств.
Превращения, происходящие в стали при медленном охлаждении
В сталях, нагретых до аустенитного состояния, при весьма медленном охлаждении произойдут обратные превращения, а именно:
а) в стали с содержанием углерода 0,83% аустенит превратится в перлит;
б) в стали с содержанием углерода 0,4% сначала из аустенита начнет выделяться феррит, а затем в районе температуры 700° оставшийся аустенит превратится в перлит и
в) в стали с содержанием углерода 1,2% сначала из аустенита выделится цементит, а затем в районе температуры 700° оставшийся аустенит превратится в перлит.
Даже при весьма медленном охлаждении температура распада аустенита не совпадает с теми температурами, при которых аустенит образовался при нагревании. Чем скорость охлаждения больше, тем больше становится гистерезис, т. е. разница между критическими температурами (точками) при нагревании и охлаждении.
Превращения, происходящие в стали при быстром охлаждении
Как указывалось выше, при быстром охлаждении не успевает произойти превращение аустенита в перлит с выделением избыточного феррита или цементита, а в зависимости от скорости охлаждения аустенит превращается в новые структуры - мартенсит, троостит или сорбит. Сталь с этими структурами отличается от сталей со структурами перлита и феррита повышенной твердостью, прочностью и уменьшенной пластичностью. Если углеродистую сталь, нагретую выше критических температур, охладить очень быстро, то аустенит превратится в мартенсит и это превращение начнется лишь при температуре около 200°. При несколько меньшей скорости охлаждения образуется структура троостит, а при еще меньшей — сорбит.
В производственных условиях при охлаждении углеродистой инструментальной стали в воде образуется мартенсит, при охлаждении в масле — троостит и при охлаждении в струе воздуха -сорбит. На рис. 6 показаны микроструктуры закаленной стали.
Рис. 6. Микроструктура закаленной стали:
а — игольчатый мартенсит;
В легированных сталях, благодаря присутствию специальных элементов, для образования мартенсита не требуется столь большой скорости охлаждения, как для углеродистых сталей, и мартенсит образуется при охлаждении в масле, а для быстрорежущих сталей — и при охлаждении на воздухе.
Троостит и сорбит можно получить не только в результате ускоренного охлаждения, нои путем нагрева закаленной стали, имеющей структуру мартенсита, до температуры ниже Aс1, т. е. путем отпуска стали. В этом случае троостит получается при нагреве стали до 400°, а сорбит—при нагреве до 650°. При нагреве до промежуточных температур получаются смешанные структуры: при нагреве от 250—400° — мартенсит и троостит и при нагреве от 400—650° — троостит и сорбит. В производственных условиях троостит и сорбит получают путем отпуска закаленной стали.
Превращения, происходящие в стали при охлаждении в среде, имеющей температуру выше 200° (изотермическое превращение)
Если деталь, нагретую выше критической точки, поместить в среду, имеющую температуру от 700 до примерно 200°, и выдержать в ней до выравнивания температуры по всему сечению, то аустенит превратится в ту структуру, которая соответствует превращению при данной температуре.
О поведении стали при изотермической обработке, выборе температуры и времени выдержки судят по кривым изотермического превращения, построенным для разных марок стали.
Рис. 7. Диаграмма изотермического превращения аустенита углеродистой стали.
На рис. 7 дан вид диаграммы изотермического превращения в стали. На горизонтальной оси отложено время начала и конца превращения, а на вертикальной— температура, при которой оно происходит. Линия А с соответствует переходу аустенита в перлит, а линия Мн — образованию мартенсита из аустенита. На кривой I начинаются, а на кривой II заканчиваются структурные превращения.
Если углеродистую инструментальную сталь, нагретую до 800°, поместить в масло, расплавленную соль или щелочь при температуре 250°, в ней образуется игольчатый троостит с высокой твердостью Rc=45—55. Если эту же сталь охладить в среде, имеющей температуру свыше 600°, в ней образуется перлит и такая сталь легко обрабатывается на станках. При охлаждении стали в среде с промежуточными температурами образуются структуры троостита и сорбита с соответствующей твердостью.
Изотермический отжиг нашел большое применение при термической обработке инструментальных сталей как процесс, резко уменьшающий время по сравнению с другими видами отжига.
Изотермическая закалка в инструментальном деле применяется редко из-за недостаточной для инструмента твердости, достигаемой при этом процессе.
Источник:
Остапенко Н.Н.,Крапивницкий Н.Н. Технология металлов. М. Высшая школа,1970г.
Каменичный И.С. Практика термической обработки инструмента. Киев, 1959 г.
Диаграмма железо-углерод – это графическое отображение структуры сплавов, состоящих только из железа и углерода, в зависимости от исходной средней концентрации углерода и текущей температуры сплава. Диаграмма железо-углерод позволяет понять процессы, происходящие при термообработке стали.

Диаграмма железо-углерод (железо-цементит). Упрощенная

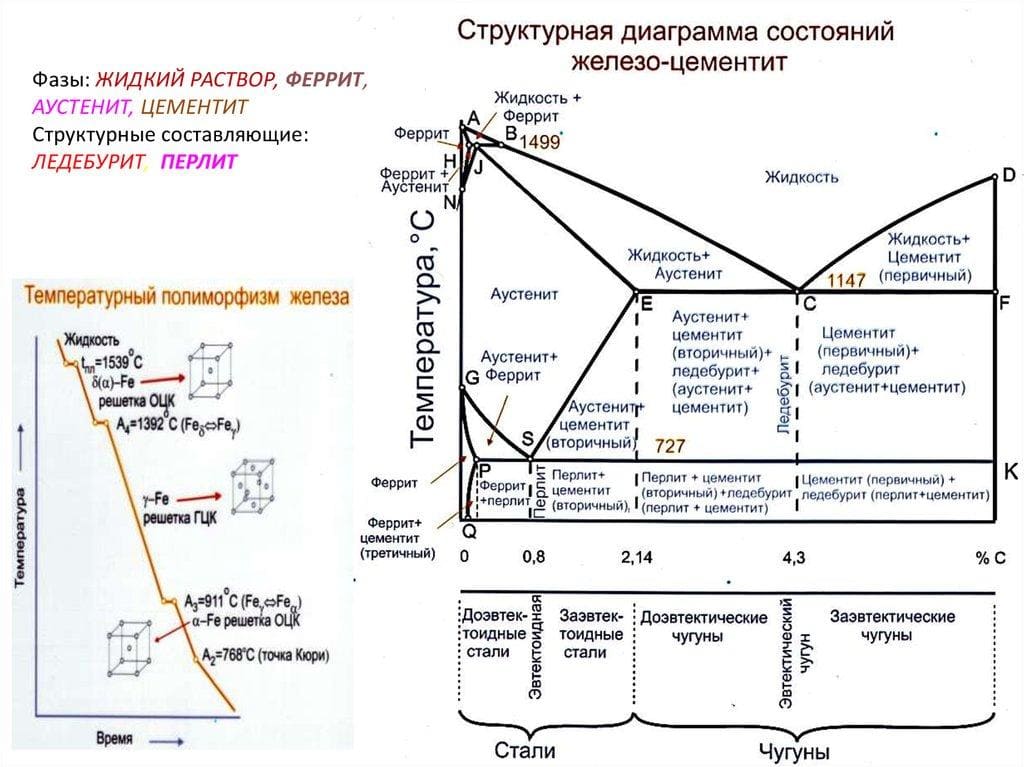
Структуры на диаграмме железо-углерод
Напомним о 2 кристаллических формах железа:
Полиморфное превращение одной формы в другую при проведении термообработки сталей происходит при прохождении сплавами линии GSK.
Выделим 4 фазы в системе железо-углерод:
- Жидкая фаза. Концентрация углерода не ограничена;
- Феррит – это твёрдый раствор углерода в α-железе. Максимальная концентрация углерода – всего лишь 0,025% (точка P). При комнатной температуре – не выше 0,006%. Феррит мягок и пластичен.
- Аустенит – твёрдый раствор углерода в γ-железе. Максимальная концентрация углерода — 2,14 % (точка E). Аустенит имеет невысокую твёрдость, пластичен, не магнитится.
- Цементит — химическое соединение железа с углеродом (карбид железа, Fe 3 C). Концентрация углерода, соответственно, постоянная – 6,67 % углерода. Цементит очень твёрд, хрупок, непластичен.
В зависимости от условий образования выделяют:
- первичный цементит (образуется из жидкости);
- вторичный цементит (выделяется из аустенита вокруг его зерен);
- третичный цементит (выделяется из феррита по границам его зерен);
- эвтектоидный цементит (является составной частью перлита);
- эвтектический цементит (является составной частью ледебурита).
Необходимо так же выделить 2 структурные составляющие железоуглеродистых сплавов:

Структура перлита. Ф — феррит, Ц — цементит
Железо при этом переходит из γ-формы в α-форму. Механические свойства сильно зависят от размера (дисперсности) частичек, из которых состоит данный перлит.
- Ледебурит (эвтектика) – механическая смесь 2 фаз – пластинок/зерен аустенита и цементита. Ледебурит образуется из жидкой фазы с концентрацией углерода 4,3% при прохождении ниже линии ECF:

Структура ледебурита. Ц — цементит, А — аустенит.
Повторяясь, напомним, что при прохождении сплавов ниже линии PSK (727°С) аустенит, входящий в состав ледебурита, претерпевает перлитное превращение, разделяясь на феррит и цементит. Ледебурит тверд и хрупок.
При комнатной температуре железоуглеродистые сплавы могут иметь различную структуру, а значит и свойства, хотя и состоят всегда всего из 2 фаз: феррита и цементита.

Некоторые элементы диаграммы железо-углерод
Выделим несколько границ на диаграмме железо-углерод:
- линия ACD. Линия ликвидус. При охлаждении сплавов ниже нее начинается их кристаллизация;
- линия AECF. Линия солидус. При охлаждении сплавов ниже нее весь сплав переходит в твердое состояние;
- линия ECF. Иногда называется линией ледебуритного превращения. При охлаждении сплавов с содержанием углерода выше 2,14% ниже нее жидкая фаза превращается в ледебурит;
- линия PSK. Линия перлитного превращения. При охлаждении сплавов ниже нее аустенит превращается в перлит.
Отметим несколько важных точек на диаграмме:
Часто значения температур, при которых происходят структурные изменения конкретного сплава обозначают буквами A:
Поскольку температуры фазовых переходов при нагреве и охлаждении слегка отличаются, то часто вводят дополнительные буквенные обозначения:
Чтение диаграммы железо-углерод
Состав сплава с данным исходным содержанием углерода при заданной температуре мы можем увидеть, двигаясь по вертикальной линии, соответствующей содержанию углерода в сплаве.
Рассмотрим, например, область AEC. С ней соседствуют области аустенита AESG и жидкой фазы. Сплавы в ней состоят из жидкой фазы и образующегося твердого аустенита. Как определить концентрацию углерода в разных фазах для данного сплава? Рассмотрим для примера сплав с исходной концентрацией углерода 2,5% при температуре 1250°С.
Пересечение этой же горизонтальной прямой с линией AС, граничащей с областью жидкой фазы, покажет концентрацию углерода в жидкой фазе при данной температуре (~3.5%).
Именно таким образом мы можем определить концентрацию углерода в фазах любого сплава при заданной температуре:
- в жидкой фазе и аустените в области AEC;
- в жидкой фазе в области CDF (концентрация углерода в цементите, конечно, постоянна – 6,67%);
- в аустените в области SEFK;
- в феррите в области QPKL;
- в феррите и аустените в области GPS.
Как видим, при концентрации углерода выше 2,14% насыщение охлаждаемого расплава углеродом всегда стремится к 4,3% (по линиям AC и DC) по мере приближения к температуре 1147°С (уровень ECF). Далее происходит превращение жидкости в ледебурит (эвтектику). Естественно, с этим же средним содержанием углерода.
Классификация железоуглеродистых сплавов
Классификация железоуглеродистых сплавов в зависимости от концентрации углерода в сплаве:
Чугуны же выделяет наличие ледебурита, придающего им хрупкость. Поэтому чугуны не могут подвергаться ковке. Зато обладают лучшими литейными свойствами (чем стали), обусловленными наличием легкоплавкого ледебурита.
Термообработка сталей в ООО КВАДРО
Наше предприятие уже почти четверть века производит на заказ термообработку металлов в Санкт-Петербурге. Заказать термообработку у нас Вы можете, оставив Вашу заявку на электронной почте или позвонив нам.
Мы производим термообработку сталей (в т.ч. нержавеющих, инструментальных и т.п.) по чертежам Заказчика или заданным режимам , а так же иных металлов и сплавов (алюминиевых и титановых, латуней и бронз, и т.д.).
Основные виды термической обработки металлов, осуществляемые на нашем предприятии на заказ:
Напоминаем так же, что у нас вы можете воспользоваться широким спектром методов металлообработки, включая фрезерные работы и токарную обработку.
Читайте также:

