Что такое клетки спутницы кратко
Обновлено: 14.05.2024
Кле́тки-спу́тницы, или сопровожда́ющие кле́тки [1] — паренхимные клетки флоэмы покрытосеменных [1] растений, тяжи которых примыкают к боковым стенкам члеников ситовидных трубок, соединяясь с ними полуситовидными полями [2] (т.е. в стенке членика развивается ситовидное поле, а в сопровождающей клетке — простая пора [3] ).
Сопровождающие клетки осуществляют передачу нуклеиновых кислот и энергии в виде АТФ в ситовидную трубку, лишённую ядра, полностью управляя её деятельностью [4] и участвуя таким образом в нисходящем токе веществ. В связи с этим они имеют крупные, часто полиплоидные ядра и митохондрии [2] .
У голосеменных роль сопровождающих паренхимных клеток выполняют клетки Страсбургера [1] .
Напишите отзыв о статье "Клетки-спутницы"
Примечания
Литература
Отрывок, характеризующий Клетки-спутницы
Немец, закрыв глаза, показывал, что не понимает.
– Хочешь, возьми себе, – говорил офицер, подавая девушке яблоко. Девушка улыбнулась и взяла. Несвицкий, как и все, бывшие на мосту, не спускал глаз с женщин, пока они не проехали. Когда они проехали, опять шли такие же солдаты, с такими же разговорами, и, наконец, все остановились. Как это часто бывает, на выезде моста замялись лошади в ротной повозке, и вся толпа должна была ждать.
– И что становятся? Порядку то нет! – говорили солдаты. – Куда прешь? Чорт! Нет того, чтобы подождать. Хуже того будет, как он мост подожжет. Вишь, и офицера то приперли, – говорили с разных сторон остановившиеся толпы, оглядывая друг друга, и всё жались вперед к выходу.
Оглянувшись под мост на воды Энса, Несвицкий вдруг услышал еще новый для него звук, быстро приближающегося… чего то большого и чего то шлепнувшегося в воду.
– Ишь ты, куда фатает! – строго сказал близко стоявший солдат, оглядываясь на звук.
– Подбадривает, чтобы скорей проходили, – сказал другой неспокойно.
Толпа опять тронулась. Несвицкий понял, что это было ядро.
– Эй, казак, подавай лошадь! – сказал он. – Ну, вы! сторонись! посторонись! дорогу!
Он с большим усилием добрался до лошади. Не переставая кричать, он тронулся вперед. Солдаты пожались, чтобы дать ему дорогу, но снова опять нажали на него так, что отдавили ему ногу, и ближайшие не были виноваты, потому что их давили еще сильнее.
– Несвицкий! Несвицкий! Ты, г'ожа! – послышался в это время сзади хриплый голос.
Несвицкий оглянулся и увидал в пятнадцати шагах отделенного от него живою массой двигающейся пехоты красного, черного, лохматого, в фуражке на затылке и в молодецки накинутом на плече ментике Ваську Денисова.
– Вели ты им, чег'тям, дьяволам, дать дог'огу, – кричал. Денисов, видимо находясь в припадке горячности, блестя и поводя своими черными, как уголь, глазами в воспаленных белках и махая невынутою из ножен саблей, которую он держал такою же красною, как и лицо, голою маленькою рукой.

Кле́тки-спу́тницы, или сопровожда́ющие кле́тки [1] — паренхимные клетки флоэмы покрытосеменных [1] растений, тяжи которых примыкают к боковым стенкам члеников ситовидных трубок, соединяясь с ними полуситовидными полями [2] (т.е. в стенке членика развивается ситовидное поле, а в сопровождающей клетке — простая пора [3] ).
Сопровождающие клетки осуществляют передачу нуклеиновых кислот и энергии в виде АТФ в ситовидную трубку, лишённую ядра, полностью управляя её деятельностью [4] и участвуя таким образом в нисходящем токе веществ. В связи с этим они имеют крупные, часто полиплоидные ядра и митохондрии [2] .
У голосеменных роль сопровождающих паренхимных клеток выполняют клетки Страсбургера [1] .
Мезофилл. Эндодерма. Перицикл. Клетки-спутницы.
Мезофилл. Эта выполняющая ткань располагается между двумя слоями эпидермиса листа и состоит из модифицированных паренхимиых клеток, осуществляющих фотосинтез. Фотосинтетическую паренхиму иногда называют хлоренхимой. Цитоплазма клеток хлоренхимы содержит большое число хлоропластов, в которых и протекают реакции фотосинтеза. У двудольных растений мезофилл состоит из двух четко различающихся слоев: верхний слой составляет палисадная паренхима, клетки которой имеют столбчатую форму, а нижний — губчатая паренхима с клетками неправильной формы, содержащими меньше хлоропластов. Фотосинтез идет главным образом в палисадной паренхиме, а воздухоносные межклетники губчатой паренхимы обеспечивают интенсивный газообмен.
Эндодерма
Эндодермой называется слой клеток, окружающий проводящую ткань растения.
Его можно рассматривать как самый внутренний слой коры. Обычно клетки эндодермы парснхимныс, но они могут быть и модифицированы как в физиологическом, так и в структурном отношениях. В корнях, где эндодерма состоит из одного слоя клеток, она выражена более отчетливо, чем в стеблях, потому что в каждой такой клетке имеется поясок Каспари — опоясывающая клетку полоска суберина (вещества, близкого по своей природе к жирам). На более поздней стадии может происходить дальнейшее утолщение клеточной стенки. О структуре и функции эндодермы корня см. гл. 13.
В стеблях двудольных проводящие пучки образуют кольцо, эндодерма же, состоящая из одного или нескольких слоев клеток, располагается снаружи от этого кольца, непосредственно примыкая к нему. Нередко при этом эндодерма по своему виду не отличается от остальной коры, но иногда в ней накапливаются крахмальные зерна, и тогда она превращается в так называемое крахмалоносное влагалище, которое легко сделать видимым, окрасив препарат иодом. Эти крахмальные зерна могут поддействием силы тяжести оседать в клетках, в силу чего эндодерма играет важную роль в геотропической реакции, так же, как и клетки корневого чехлика (гл. 16).
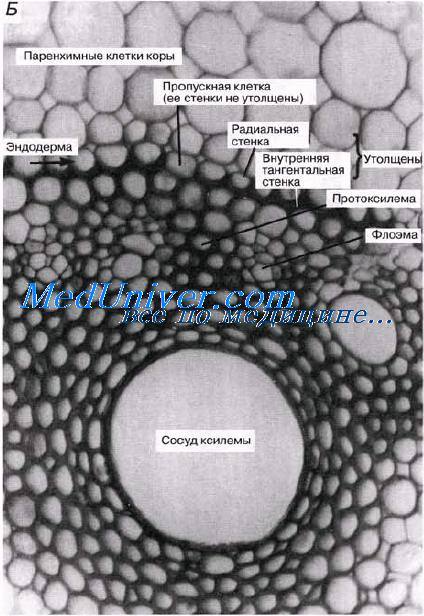
Перицикл.
В корне между центральной проводящей тканью (центральным цилиндром) и эндодермой располагается перицикл — слой, состоящий из одного или нескольких рядов клеток. Перицикл сохраняет мсристсматичсскую активность: в нем закладываются боковые корни. У растений, корням которых свойствен вторичный рост, перицикл участвует в этом вторичном росте. В стеблях, как правило, аналогичного слоя нет.
Клетки-спутницы.
Так называются специализированные паренхимные клетки, примыкающие к ситовидным трубкам и участвующие в их работе. Метаболически клетки-спутницы весьма активны; от обычных паренхимных клеток их отличают более плотная цитоплазма и более мелкие вакуоли. О происхождении, строении и функции клеток-спутниц мы будем говорить в соответствующей статье
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Обзор
Автор
Редакторы
- Иммунология
- Медицина
- Наука из первых рук
- Нейробиология
- Нейродегенерация
- Стволовые клетки
- Эмбриология

Стволовые клетки взрослого организма
Стволовые клетки (СК) находятся в организме в строго определенных местах, которые, благодаря окружающим клеткам и внеклеточному матриксу [1], обеспечивают правильное функционирование стволовых клеток. Такие места называются клеточной нишей [2]. В костном мозге есть два типа СК: кроветворные, способные дифференцироваться во все клетки крови, и мезенхимные (МСК), дающие начало костной, хрящевой и жировой тканям и составляющие важную часть стромы кроветворения (ниши кроветворной СК), но ни при каких обстоятельствах не способные дифференцироваться в клетки крови.
Самые первые — стволовые клетки крови
Ниже в иерархии стоят олигопотентные клетки-предшественницы — родоначальницы только нескольких линий клеток крови, таких как общие миелоидные предшественники (дающие моноциты, мегакариоциты, эритроциты) и общие лимфоидные предшественники (дающие В-, Т- и НК-клетки ).
Еще более низкую ступень в иерархии занимает отдел уни- и бипотентных клеток-предшественниц, способных дифференцироваться только в одном или двух направлениях.
Самые популярные — мезенхимные стволовые клетки
Большой медицинский потенциал сподвиг Бигильдеева А.Е. с соавторами досконально изучить этот тип клеток при помощи генетического штрихкодирования клеточных популяций [6]. При извлечении МСК из костного мозга [7] в каждую клетку вносят метку — небольшой уникальный фрагмент ДНК, который встраивается в геном клетки и потому будет находиться в геномах всех ее потомков. Анализ этих меток после роста в чашке Петри позволяет определить, потомки каких клеток размножились сильнее, а каких — не оставили потомков.
Оказалось, что популяция МСК гетерогенна и представлена множеством клеточных клонов (потомков одной исходной клетки), различающихся по способности к делению и дифференцировке. При многократном пересеве культуры ее клональный состав значительно меняется из-за ухода потомков клеток, не способных к долгому размножению. МСК с высокой способностью к размножению чаще выявляются на ранних этапах культивирования вне организма, и в поликлональной популяции МСК содержится лишь небольшое количество таких клеток. В связи с этим в подходах регенеративной медицины, требующих активного размножения клеток, рекомендуется применять МСК ранних пассажей (то есть те, что жили в чашке Петри недолго). Благодаря подобным исследованиям становится ясно, что хранить в замороженном виде МСК в больших количествах невозможно: для этого придется их долго культивировать, и они могут утратить требуемые стволовые свойства. Тут можно обратиться к более ранним стволовым клеткам, каких во взрослом организме уже не остается.
Эмбриональные стволовые клетки
Некоторые стволовые клетки функционируют не просто в особом месте организма, но и в строго определенное время. Тотипотентностью — способностью дифференцироваться во все клетки организма и экстраэмбриональные ткани — обладает только зигота, но уже после нескольких делений это свойство утрачивается навсегда. На стадии бластоцисты происходит первая специализация клеток эмбриона: выделяются клетки трофобласта (наружный слой, который затем образует экстраэмбриональные ткани) и клетки внутренней клеточной массы, из которых разовьется весь организм (рис. 1). Последние при культивировании в чашке Петри называются эмбриональными стволовыми клетками (ЭСК). Впервые удалось вывести этот тип клеток в культуру в 1981 году [8]. Добавляя в культуральную среду определенные белки — факторы роста, — удается долго поддерживать ЭСК в недифференцированном плюрипотентном состоянии. ЭСК активно размножаются, сохраняя при этом свои свойства, что позволяет получать большое количество клеток для исследовательских задач и для применения в медицине.

Рисунок 1. Первые пять дней развития эмбриона человека. 1 — Оплодотворение; 2 — деление (дочерние клетки называются бластомерами); 3 — компактизация (образование плотных контактов между бластомерами); 4 — дифференцировка на внутренний и внешний слои; 5 — образование полости (бластоцеля), внешнего слоя клеток (трофобласта) и внутренней клеточной массы, которую можно извлечь для культивирования в чашке Петри и получить таким образом ЭСК (фото автора статьи).
Существуют разные протоколы перепрограммирования — как со вставкой ДНК прямо в геном клетки (подходят только для исследовательских целей), так и не оставляющие следов в геноме (подходят и для медицинского применения ИПСК). Получение ИПСК с помощью доставки репрограммирующих факторов в вирусных векторах (например, лентивирусных, относящихся к тому же семейству вирусов, что и ВИЧ), которые встраиваются в геном клетки, широко распространено в лабораторной практике ввиду высокой эффективности, методологической простоты и дешевизны.
С одной стороны, проблема решается прочно укоренившейся в мире практикой клинических исследований, доказывающих эффективность и оправданность применения разрабатываемых лекарств на людях . С другой стороны, заметно помочь в разработке препаратов могут модели заболеваний на основе ИПСК, несущих связанные с развитием той или иной болезни мутации, из клеточного материала пациентов с установленным диагнозом. ИПСК представляют собой практически бесконечный источник клеточного материала и могут превращаться в любой тип клеток взрослого организма, в том числе в предшественников нейронов, зрелые нейроны и кардиомиоциты. Разработка таких моделей наследственных заболеваний позволит изучать функции продуктов мутантных генов в клетке и механизмы развития патологии. Дифференцированные производные ИПСК можно использовать для скрининга новых лекарственных препаратов (рис. 2).

Для создания модели заболевания на основе ИПСК необходимо превратить их в тот тип клеток, который повреждается при изучаемой патологии. Наиболее востребованы модели нейродегенеративных и кардиологических заболеваний, ведь в этих случаях поврежденные ткани напрямую не доступны исследователям. Для запуска дифференцировки в нужную сторону необходимо воспроизвести в чашке Петри те же условия, с которыми клетка сталкивается в организме. Рассмотрим, как можно получить клетки нервной системы — нейроны, производящие дофамин (а именно они погибают при болезни Паркинсона [14], [15]).
Дифференцировка в клетки нервной системы: трудно, долго, красиво
Тут мы должны слегка углубиться в эмбриологию, ведь нужно будет имитировать все изменения в окружении клетки, происходящие от стадии бластоцисты до формирования головного мозга. Придется учитывать и механические воздействия на клетку, и своевременное появление определенных белков — факторов дифференцировки, — и их концентрацию, и состав солей в окружающей клетку среде, и особенности поверхности, к которой клетка прикреплена.
Перед запуском ИПСК в дифференцировку важно убедиться, что клетки растут в оптимальной плотности: они должны занимать почти всю площадь чашки Петри. Это необходимо, чтобы на старте превращения клетки давили друг на друга ровно так, как это происходит на первом этапе формирования нервной системы эмбриона — при развитии нервной трубки. Клетки, которые находятся на дне нервной бороздки, испытывают давление из-за активного размножения соседних клеток и изгибания самой бороздки в трубку, а клетки, расположенные сверху, наоборот, испытывают растяжение и превращаются в нервный гребень. Из нервного гребня впоследствии развивается множество типов клеток, в том числе и волосяные луковицы, а из клеток, находящихся на дне нервной бороздки, образуется центральная нервная система (рис. 3).

Рисунок 3. Последовательные стадии развития нервной системы (ранние этапы). Первоначально будущие клетки нервной системы изменяют форму и характерным образом располагаются друг относительно друга — получается нервная пластинка. Затем она изгибается, превращаясь в нервную бороздку, где на клетки действуют механические силы. Наконец, нервная бороздка замыкается в нервную трубку. Красные стрелки показывают механические силы, действующие на клетки. Нейрональные розетки — аналог нервной трубки в чашке Петри. Увеличение 100× (фото автора статьи).

Поскольку при нейродегенеративных заболеваниях, в том числе и при болезни Паркинсона, гибнут именно зрелые нейроны у взрослых людей, а не их размножающиеся предшественники, для моделирования болезни правильно брать как раз зрелые нейроны, чтобы с большей достоверностью повторить развитие патологических процессов. С другой стороны, можно изучать особенности дифференцировки нейронов и выяснять, что и как на эту дифференцировку влияет. Аналогичные подходы можно применить при получении кардиомиоцитов — клеток сердца, изучать которые прямо в организме тоже непросто.

Рисунок 5. Зрелые нейроны, полученные путем дифференцировки из клеток-предшественниц. Различные структуры нейронов флуоресцентно окрашены: бета-III-тубулин (присутствует во всех типах нейронов; окрашен зелёным), тирозингидроксилаза (фермент, участвующий в синтезе дофамина; характерен для нейронов, выделяющих дофамин; окрашен желто-зеленым), ядра клеток (окрашены синим). Увеличение 100×.
фотография из диссертации автора статьи [18]
Дифференцировка в клетки сердца
Получение ИПСК от пациента и их последующая направленная дифференцировка в кардиомиоциты открывают новые возможности для изучения патогенеза наследственных сердечно-сосудистых заболеваний, в частности гипертрофической кардиомиопатии, от которой до сих пор не разработано эффективного лечения. При этом заболевании утолщаются стенки левого желудочка и межжелудочковой перегородки, развиваются сердечная недостаточность и аритмия, возрастает риск внезапной сердечной смерти. Гипертрофическая кардиомиопатия — одна из самых распространенных сердечно-сосудистых патологий: 1 случай на 500 человек. Елена Дементьева с коллегами создала модель этого заболевания на основе пациентспецифичных ИПСК [19]. Исследовав геном пациента с гипертрофической кардиомиопатией, коллектив обнаружил мутацию R326Q в гене MYBPC3, кодирующем миозин-связывающий белок С. Этот белок расположен в саркомере и играет важную роль в сокращении кардиомиоцита. ИПСК пациента и здорового донора (в качестве контроля) превратили в клетки сердца, которые воспроизводили такие признаки гипертрофической кардиомиопатии, как нарушение динамики потоков ионов кальция и их повышенное внутриклеточное содержание.
Таким образом, описанная клеточная модель для изучения гипертрофической кардиомиопатии представляет собой кардиомиоциты, полученные в результате направленной дифференцировки ИПСК пациента с этой болезнью.
3D-дифференцировка: миниорганы в пробирке
Исследования последних лет, связанные с созданием 3D-органоидов (Еремеев А.В. с соавторами [20]) из ЭСК или ИПСК, существенно облегчили исследования в области моделирования органогенеза человека in vitro и стали мощным инструментом для исследования механизмов развития патологий сложных органов, равно как и разработки новых подходов к их терапии. В последние годы были созданы многоклеточные органоиды мозга человека [21], толстой кишки [22], почек, сетчатки, печени. Разумеется, пока 3D-модели многоклеточных органов на основе 2D-культур имеют свои ограничения и лишь условно имитируют их сложную архитектонику [23], [24].
Применение плюрипотентных стволовых клеток в медицине
Для решения проблем, выявленных в предыдущей серии трансплантаций, запустили TRANSEURO — клиническое исследование в Европе, в ходе которого в 2014–2016 годах 11 пациентам трансплантировали предшественников нейронов, вырабатывающих дофамин. Однако из-за источника клеток — эмбрионов человека — возникли как этические, так и чисто технические трудности, связанные с получением фетального материала и невозможностью его стандартизации для клинического применения. Из-за сбоев в поставке ткани для трансплантации из 90 запланированных операций по подсадке таких клеток осуществили только 20, и на данный момент проект остановлен. Для того чтобы обойти эти сложности, активно разрабатывают эффективные методы дифференцировки ЭСК и ИПСК для дальнейшего их применения в клинической практике.
В качестве альтернативы Киотский университет запустил проект Stock, нацеленный на создание банка разных линий ИПСК, типированных по иммунологическим параметрам совместимости (как это делается при пересадке органов). Было подсчитано, что 50 линий ИПСК, специально отобранных по этому принципу, позволят охватить 73% населения Японии. Но не стόит забывать, что развитию иммунного ответа могут способствовать и клетки врожденной иммунной системы, такие как макрофаги и естественные киллеры.
Клеточная терапия с использованием стволовых клеток различного происхождения набирает обороты в мировой практике. Такой подход клеточной терапии, как пересадка костного мозга, уже давно прижился в клинической практике. Терапия МСК не всегда дает хорошие результаты. Однако в случае реэпителизации поврежденных кожных покровов (например, при синдроме диабетической стопы) эффективность применения МСК уже показана в клинических исследованиях [28].
В клинику готовы войти и производные плюрипотентных стволовых клеток (ЭСК и ИПСК). Полученные из ЭСК олигодендроциты [29] и клетки поджелудочной железы [30], производящие инсулин, находятся на финальных этапах клинических испытаний. В случае олигодендроцитов был заявлен 15-летний срок наблюдения за пациентами после подсадки клеток в спинной мозг. Этот срок еще не истек, но негативных последствий для пациентов до сих пор не обнаружено. Начались клинические исследования клеточных продуктов для терапии таких сложных и тяжелых заболеваний, как дистрофия сетчатки и болезнь Паркинсона [31]. Многие исследования направлены на то, чтобы уменьшить или полностью исключить иммуносупрессию при пересадке дифференцированных производных ЭСК и ИПСК. Благодаря стволовым клеткам перед нами открывается огромное поле возможностей, но впереди еще большее поле научной работы.
Словарик
ИПСК (индуцированные плюрипотентные стволовые клетки) полученный в пробирке аналог ЭСК, обладающий точно такими же морфологическими и функциональными свойствами. МСК (мезенхимные стволовые клетки) мультипотентные стволовые клетки, способные дифференцироваться в остеобласты (клетки костной ткани), хондроциты (хрящевые клетки) и адипоциты (жировые клетки). СК (стволовая клетка) неспециализированные клетки, присутствующие в организме многоклеточных животных и способные к самообновлению и дифференцировке в соответствующие специализированные клетки. СКК (стволовая клетка крови) мультипотентные стволовые клетки, дающие начало всем клеткам крови как миелоидного, так и лимфоидного рядов. ЭСК (эмбриональные стволовые клетки) плюрипотентные стволовые клетки, полученные из внутренней клеточной массы бластоцисты, культивируемые in vitro. HLA (лейкоцитарный антиген человека) система тканевой совместимости человека; представляет собой белки на поверхности клеток, позволяющие клеткам крови различать свои и чужеродные ткани.
Читайте также:

