Что такое ферменты и какова их роль в химических реакциях кратко
Обновлено: 04.07.2024
Ферменты — это молекулы белка, синтезируемые живыми клетками, которые являются также катализаторами химических реакций, протекающих в организме.
Исходя из определения фермента, можно утверждать, что в любом организме регулярно продуцируется различные ферменты — их количество может достигать несколько сотен. Ферменты играют огромную роль в обеспечении жизнедеятельности организма. В частности, ускоряют химические реакции. В этом плане ферменты выступают биологическими катализаторами, ускоряя и упрощая процесс протекания химической реакции.
Но ферменты — это не то же самое, что химические катализаторы, так как не меняют направление химической реакции и не расходуются в ходе ее протекания.
Так что такое фермент?
Ферменты выступают в качестве биокатализаторов, то есть веществ, облегчающих протекание химической реакции и провоцирующих увеличение ее скорости.
Одна из функций ферментов — поддержание жизнеспособности организмов.
Яркий пример работы ферментов — сладковатый вкус во рту, который возникает при пережевывании продуктов, содержащих крахмал. Этот вкус появляется благодаря ферменту амилазе — этот фермент есть в слюне и помогает расщеплять крахмал. Сам по себе крахмал не имеет вкуса, однако продукты его распада — декстрина, глюкоза и мальтоза — дают сладковатый привкус.
У всех ферментов наблюдается глобулярная структура, но кроме того — еще и третичная, и четвертичная.
- простые. Они состоят из белка;
- сложные. Они состоят белков и отдельных дополнительных веществ.
Также сложные ферменты могут иметь в составе белковую и небелковую части. Белковая часть — это апофермент, добавочная часть — кофермент. Коферментам могут выступать витамины групп Е, К и В.
Механизмы действия ферментов
У всех ферментов одни и те же принципы и механизмы действия. Взаимодействие с субстратом у фермента происходит посредством отдельного активного центра, а не всей молекулы. Результатом такого взаимодействия является фермент или субстратный комплекс. По завершении реакции происходит достаточно быстрый распад этого комплекса. Фермент, это то, что важно, остается неизменным, поэтому он может вступать во взаимодействие с новой молекулой.
Ферменты участвуют в образовании молекулы пептидной связи. Это происходит в результате взаимодействия между собой двух молекул в активном центре фермента. Далее новое вещество, называемый дипептидом, уходит из активного центра фермента, так как структурно уже ему не соответствует.
Высокая степень специфичности действия — одна из особенностей фермента. Отдельный фермент отвечает за ускорение одного типа реакции.
Факторы, влияющие на активность ферментов
Есть несколько факторов, влияющих на активность ферментов:
- Температура. Если она повышается, то возрастает скорость химической реакции. Таким образом повышается и скорость молекул, что приводит к увеличению шансов их столкновения друг с другом.
Все это, соответственно, приводит к увеличению шансов, что между молекулами пройдет реакция. Температура, повышающая активность фермента, называется оптимальной.
При выходе температуры реакции за границы оптимального диапазона снижается скорость реакции и происходит процесс денатурации белка. Скорость реакции снижается при снижении температуры и причина этого — в инактивации фермента.
Чтобы продукты хранились дольше, используется способ быстрого замораживания. При таком замораживании рост и развитие микроорганизмов прекращается, а ферменты внутри микроорганизмов — инактивируются. Это предотвращает разложение продуктов питания.
- pHсреда. Другими словами, активность ферментов находится в прямой зависимости от концентрации ионов водорода. Оптимальный уровень pH среды — нейтральное значение около 7.
Есть ферменты, способные работать в кислой среде (пепсин). Этот фермент находится в сильнокислой среде желудка.
- Ингибиторы и инактиваторы. В случаях, когда ферменты подвергаются воздействию ингибиторов и инактиваторов, к примеру, ионов металлов (Mg, Mn, Zn), происходит инактивация первых. Прочие ионы тяжелых металлов подавляют активность ферментов и денатурируют белки.
Согласно устоявшейся классификации, все ферменты делятся на 6 групп и имеют довольно сложные названия. Для облегчения их использования ферменты стали называть по имени субстрата, добавляя к названию окончание —аза.
К примеру, есть субстрат лактоза. Фермент его будет называться лактаза.
Фермент способен к преобразованию вещества. В случае субстрата сахарозы ферментом, который его расщепляет, является сахараза. По этой же логике ферменты, расщепляющие протеины, называются протеиназы.
Использование ферментов в практических целях
Ферменты нашли практическое применение почти во всех областях и сферах человеческой деятельности. Даже вне живых клеток они способны проявлять свои уникальные свойства. В медицине активно используют такие ферменты как амилаза, липаза, протеаза — они включаются в состав комбинированных препаратов (фестала, панзинорма), лечащих заболевания желудочно-кишечного тракта. Ферменты также применяют для устранения тромбов в кровеносных сосудах и в процессе лечения гнойных ран.
В случае лечения онкологических заболеваний повсеместно используется энзимотерапия и ферментотерапия.
В пищевой промышленности используют амилазу, которая помогает расщеплять крахмал. В этой же области используют протеиназу, которая участвует в процессе расщепления белков, и липазу, которая расщепляет жиры.
Кажется, что ферменты обладают исключительно полезными свойствами. Однако они могут приносить и вред — когда их слишком много или мало. Пример — энзимопатология или взаимосвязь между болезнью и недостаточным синтезом какого-либо фермента.
Причина фенилкетонурии — утрата клетками печени способности синтезировать фермент, который катализирует превращение фенилаланина в тирозин.

Ферменты – это особый вид протеинов, которым природой отведена роль катализаторов разных химических процессов.
Этот термин постоянно на слуху, правда, далеко не все понимают, что такое фермент или энзим, какие функции выполняет это вещество, а также чем отличаются ферменты от энзимов и отличаются ли вообще. Все это сейчас и узнаем.
История открытия
Структура: цепь из тысяч аминокислот

Все ферменты являются белками, но не все белки – ферменты. Как и другие протеины, энзимы состоят из аминокислот. И что интересно, на создание каждого фермента уходит от ста до миллиона аминокислот, нанизанных, словно жемчуг на нить. Но эта нить не бывает ровной – обычно изогнута в сотни раз. Таким образом, создается трехмерная уникальная для каждого фермента структура. Меж тем, молекула энзима – сравнительно крупное образование, и лишь небольшая часть его структуры, так называемый активный центр, участвует в биохимических реакциях.
Биохимические свойства
Хотя при участии ферментов в природе происходит огромное количество реакций, но все они могут быть разделены на 6 категорий. Соответственно, каждая из этих шести реакций протекает под влиянием определенного типа ферментов.
Реакции при участии энзимов:
Ферменты, участвующие в этих реакциях, называются оксидоредуктазами. В качестве примера можно вспомнить как, алкогольдегидрогеназы преобразуют первичные спирты в альдегид.
Ферменты, благодаря которым происходят эти реакции, называются трансферазами. Они обладают умением перемещать функциональные группы от одной молекулы к другой. Так происходит, например, когда аланинаминотрансферазы перемещают альфа-аминогруппы между аланином и аспартатом. Также трансферазы перемещают фосфатные группы между АТФ и другими соединениями, а из остатков глюкозы создают дисахариды.

Гидролазы, участвующие в реакции, умеют разрывать одинарные связи, добавляя элементы воды.
Этот вид реакций негидролитическим путем происходит при участии лиазы.
Во многих химических реакциях положение функциональной группы изменяется в пределах молекулы, но сама молекула состоит из того же количества и типов атомов, что были до начала реакции. Иными словами, субстрат и продукт реакции являются изомерами. Такого типа трансформации возможны под влиянием ферментов изомеразы.
- Образование одинарной связи с устранением элемента воды.
Гидролазы разрушают связь, добавляя в молекулу элементы воды. Лиазы осуществляют обратную реакцию, удаляя водную часть из функциональных групп. Таким образом, создают простую связь.
Как работают в организме
Ферменты ускоряют практически все химические реакции, происходящие в клетках. Они имеют жизненно важное значение для человека, облегчают пищеварение и ускоряют метаболизм.
Гипер- и гипоактивность
Бывают случаи, когда энзимы выполняют свои функции с неправильной интенсивностью. Чрезмерная активность вызывает чрезмерное формирование продукта реакции и дефицит субстрата. В результате – ухудшение самочувствия и серьезные болезни. Причиной гиперактивности энзима может быть как генетическое нарушение, так и избыток витаминов или микроэлементов, используемых в реакции.
Гипоактивность ферментов может даже стать причиной смерти, когда, например, энзимы не выводят из организма токсины либо возникает дефицит АТФ. Причиной такого состояния также могут быть мутированные гены или, наоборот, гиповитаминоз и дефицит других питательных веществ. Кроме того, пониженная температура тела аналогично замедляет функционирование энзимов.
Катализатор и не только

Сегодня можно часто услышать о пользе ферментов. Но что такое эти вещества, от которых зависит работоспособность нашего организма?
Энзимы – это биологические молекулы, жизненный цикл которых не определяется рамками от рождения и смерти. Они просто работают в организме до тех пор, пока не растворятся. Как правило, это происходит под воздействием других ферментов.
В процессе биохимической реакции они не становятся частью конечного продукта. Когда реакция завершена, фермент покидает субстрат. После этого вещество готово снова приступить к работе, но уже на другой молекуле. И так продолжается столько, сколько необходимо организму.
Ферменты в качестве катализаторов ускоряют процессы метаболизма и другие реакции.
Как правило, эти процессы состоят из определенных этапов, каждый из которых требует работы определенного энзима. Без этого цикл преобразования или ускорения не сможет завершиться.
Пожалуй, из всех функций ферментов наиболее известна – роль катализатора. Это значит, что энзимы комбинируют химические реагенты таким образом, чтобы снизить энергетические затраты, необходимые для более быстрого формирования продукта. Без этих веществ химические реакции протекали бы в сотни раз медленнее. Но на этом способности энзимов не исчерпываются. Все живые организмы содержат энергию, необходимую им для продолжения жизни. Аденозинтрифосфат, или АТФ, это своего рода заряженная батарейка, которая снабжает клетки энергией. Но функционирование АТФ невозможно без ферментов. И главный энзим, производящий АТФ, – синтаза. Для каждой молекулы глюкозы, которая трансформируется в энергию, синтаза производит около 32-34 молекул АТФ.
Факторы, определяющие активность энзимов
Поскольку энзим способен ускорять реакции во много раз, его активность определяется так называемым числом оборотов. Этот термин обозначает количество молекул субстрата (реагирующего вещества), которую способна трансформировать 1 молекула фермента за 1 минуту. Однако существует ряд факторов, определяющих скорость реакции:

Увеличение концентрации субстрата ведет к ускорению реакции. Чем больше молекул действующего вещества, тем быстрее протекает реакция, поскольку задействовано больше активных центров. Однако ускорения возможно только до тех пор, пока не задействуются все молекулы фермента. После этого, даже повышение концентрации субстрата не приведет к ускорению реакции.
Обычно повышение температуры ведет к ускорению реакций. Это правило работает для большинства ферментативных реакций, но только до тех пор, пока температура не поднимется выше 40 градусов по Цельсию. После этой отметки скорость реакции, наоборот, начинает резко снижаться. Если температура опустится ниже критической отметки, скорость ферментативных реакций повысится снова. Если температура продолжает расти, ковалентные связи рушатся, а каталитическая активность фермента теряется навсегда.
На скорость ферментативных реакций также влияет показатель рН. Для каждого фермента существует свой оптимальный уровень кислотности, при котором реакция проходит наиболее адекватно. Изменение уровня рН сказывается на активности фермента, а значит, и скорости реакции. Если изменения слишком велики, субстрат теряет способность связываться с активным ядром, а энзим больше не может катализировать реакцию. С восстановлением необходимого уровня рН, активность фермента также восстанавливается.
Ферменты для пищеварения
Ферменты, присутствующие в человеческом организме, можно разделить на 2 группы:
За что отвечают пищеварительные – понятно из названия. Но и здесь срабатывает принцип селективности: определенный тип ферментов влияет только на один вид пищи. Поэтому для улучшения пищеварения можно прибегнуть к маленькой хитрости. Если организм плохо переваривает что-то из еды, значит надо дополнить рацион продуктом, содержащим фермент, который способен расщепить трудно перевариваемую пищу.
Пищевые ферменты – катализаторы, которые расщепляют продукты питания до состояния, в котором организм способен поглощать из них полезные вещества. Пищеварительные энзимы бывают нескольких типов. В человеческом организме разные виды ферментов содержатся на разных участках пищеварительного тракта.
Ротовая полость
На этом этапе на пищу воздействует альфа-амилаза. Она расщепляет углеводы, крахмалы и глюкозу, которые содержатся в картофеле, фруктах, овощах и других продуктах питания.
Желудок
Здесь пепсин расщепляет белки до состояния пептидов, а желатиназа – желатин и коллаген, содержащиеся в мясе.
Поджелудочная железа
- трипсин – отвечает за расщепление белков;
- альфа-химотрипсин – помогает усвоению протеинов;
- эластазы – расщепляют некоторые виды белков;
- нуклеазы – помогают расщеплять нуклеиновые кислоты;
- стеапсин – способствует усвоению жирной пищи;
- амилаза – отвечает за усвоение крахмалов;
- липаза – расщепляет жиры (липиды), содержащиеся в молочных продуктах, орехах, маслах и мясе.
Тонкая кишка
Толстый кишечник

Здесь функции ферментов выполняют:
- кишечная палочка – отвечает за переваривание лактозы;
- лактобактерии – влияют на лактозу и некоторые другие углеводы.
Кроме названных энзимов, существуют еще:
- диастаза – переваривает растительный крахмал;
- инвертаза – расщепляет сахарозу (столовый сахар);
- глюкоамилаза – превращает крахмал в глюкозу;
- альфа-галактозидаза – способствует перевариванию бобов, семян, соевых продуктов, корневых овощей и листовых;
- бромелайн – фермент, полученный из ананасов, способствует расщеплению разных видов белков, эффективен при разных уровнях кислотности среды, обладает противовоспалительными свойствами;
- папаин – фермент, выделенный из сырой папайи, способствует расщеплению мелких и крупных протеинов, эффективен в широком диапазоне субстратов и кислотности.
- целлюлаза – расщепляет целлюлозу, растительные волокна (в человеческом организме не обнаружена);
- эндопротеаза – расщепляет пептидные связи;
- экстракт бычьей желчи – энзим животного происхождения, стимулирует моторику кишечника;
- панкреатин – фермент животного происхождения, ускоряет переваривание жиров и белков;
- панкрелипаза – животный фермент, способствует усвоению белков, углеводов и липидов;
- пектиназа – расщепляет полисахариды, содержащиеся во фруктах;
- фитаза – способствует усвоению фитиновой кислоты, кальция, цинка, меди, марганца и других минералов;
- ксиланаза – расщепляет глюкозу из зерновых.
Катализаторы в продуктах
Ферменты имеют решающее значение для здоровья, поскольку помогают организму расщеплять пищевые компоненты до состояния, пригодного для использования питательных веществ. Кишечник и поджелудочная железа производят широкий спектр ферментов. Но кроме этого, многие из полезных веществ, способствующих пищеварению, содержатся также и в некоторых продуктах.
Например, абрикосы содержат в себе смесь полезных энзимов, в том числе инвертазу, которая отвечает за расщепление глюкозы и способствует быстрому высвобождению энергии.
Натуральным источником липазы (способствует более быстрому перевариванию липидов) может послужить авокадо. В организме это вещество производит поджелудочная железа. Но дабы облегчить жизнь этому органу, можно побаловать себя, например, салатом с авокадо – вкусно и полезно.
Кроме того, что банан, пожалуй, самый известный источник калия, он также поставляет в организм амилазу и мальтазу. Амилаза содержится также в хлебе, картофеле, крупах. Мальтаза способствует расщеплению мальтозы, так называемого солодового сахара, который в обилии представлен в пиве и кукурузном сиропе.
Другой экзотический фрукт – ананас содержит в себе целый набор энзимов, в том числе и бромелайн. А он, согласно некоторым исследованиям, еще и обладает противораковыми и противовоспалительными свойствами.
Экстремофилы и промышленность
Экстремофилы – это вещества, способны сохранять жизнедеятельность в экстремальных условиях.
Живые организмы, а также ферменты, позволяющие им функционировать, были найдены в гейзерах, где температура близка к точке кипения, и глубоко во льдах, а также в условиях крайней солености (Долина Смерти в США). Кроме того, ученые находили энзимы, для которых уровень рН, как оказалось, также не принципиальное требование для эффективной работы. Исследователи с особым интересом изучают ферменты-экстремофилы, как вещества, которые могут быть широко использованы в промышленности. Хотя и сегодня энзимы уже нашли свое применение в индустрии как биологически и экологически чистые вещества. К применению энзимов прибегают в пищевой промышленности, косметологии, производстве бытовой химии.
- Коровкин Б. Ф. – Ферменты в жизни человека / Б. Ф. Коровкин. – М.: Медицина, 2016 г. – 770 c.
Специальность: инфекционист, гастроэнтеролог, пульмонолог .
Общий стаж: 35 лет .
Образование: 1975-1982, 1ММИ, сан-гиг, высшая квалификация, врач-инфекционист .

Рис. 1 — Брожение с использованием дрожжей – типичный пример ферментативной реакции
Человечество давно пользуется полезными свойствами этих ферментов. Например, уже много веков из молока с помощью сычужного фермента делают сыр.
Ферменты отличаются от катализаторов тем, что действуют в живом организме, тогда как катализаторы – в неживой природе. Отрасль биохимии, которая изучает эти важнейшие для жизни вещества, называется энзимологией.
Общие свойства ферментов
Ферменты представляют собой молекулы белковой природы, которые взаимодействуют с различными веществами, ускоряя их химическое превращение по определенному пути. При этом они не расходуются. В каждом ферменте есть активный центр, присоединяющийся к субстрату, и каталитический участок, запускающий ту или иную химическую реакцию. Эти вещества ускоряют протекающие в организме биохимические реакции без повышения температуры.
Основные свойства ферментов:
- специфичность: способность фермента действовать только на специфический субстрат, например, липазы – на жиры;
- каталитическая эффективность: способность ферментативных белков ускорять биологические реакции в сотни и тысячи раз;
- способность к регуляции: в каждой клетке выработка и активность ферментов определяется своеобразной цепью превращений, влияющей на способность этих белков вновь синтезироваться.
Классификация
В зависимости от роли в химических реакциях, различаются такие классы ферментов:
Классы
Особенности
Катализируют окисление своих субстратов, перенося электроны или атомы водорода
Участвуют в переносе химических групп из одного вещества в другое
Расщепляют крупные молекулы на более мелкие, добавляя к ним молекулы воды
Катализируют расщепление молекулярных связей без процесса гидролиза
Активируют перестановку атомов в молекуле
Образуют связи с атомами углерода, используя энергию АТФ.
В живом организме все ферменты делятся на внутри- и внеклеточные. К внутриклеточным относятся, например, ферменты печени, участвующие в реакциях обезвреживания различных веществ, поступающих с кровью. Они обнаруживаются в крови при повреждении органа, что помогает в диагностике его заболеваний.
Внутриклеточные ферменты, которые являются маркерами повреждения внутренних органов:
- печень – аланинаминотрансефраза, аспартатаминотрансфераза, гамма-глютамилтранспептидаза, сорбитдегидрогеназа;
- почки – щелочная фосфатаза;
- предстательная железа – кислая фосфатаза;
- сердечная мышца – лактатдегидрогеназа
Внеклеточные ферменты выделяются железами во внешнюю среду. Основные из них секретируются клетками слюнных желез, желудочной стенки, поджелудочной железы, кишечника и активно участвуют в пищеварении.
Пищеварительные ферменты
Пищеварительные ферменты – это белки, которые ускоряют расщепление крупных молекул, входящих в состав пищи. Они разделяют такие молекулы на более мелкие фрагменты, которые легче усваиваются клетками. Основные типы пищеварительных ферментов – протеазы, липазы, амилазы.
При ферментативном расщеплении питательных веществ выделяется энергия, которая расходуется для процессов обмена веществ и жизнедеятельности. Без участия ферментов, подобные процессы происходили бы слишком медленно, не обеспечивая организм достаточным энергетическим запасом.
Кроме того, участие ферментов в процессе пищеварения обеспечивает распад питательных веществ до молекул, способных проходить через клетки кишечной стенки и поступать в кровь.
Амилаза
Амилаза вырабатывается слюнными железами. Она действует на крахмал пищи, состоящий из длинной цепи молекул глюкозы. В результате действия этого фермента образуются участки, состоящие из двух соединенных молекул глюкозы, то есть фруктоза, и другие короткоцепочечные углеводы. В дальнейшем они метаболизируются до глюкозы в кишечнике и оттуда всасываются в кровь.
Слюнные железы расщепляют только часть крахмала. Амилаза слюны активна в течение короткого времени, пока пища прожевывается. После попадания в желудок фермент инактивируется его кислым содержимым. Большая часть крахмала расщепляется уже в 12-перстной кишке под действием панкреатической амилазы, вырабатываемой поджелудочной железой.
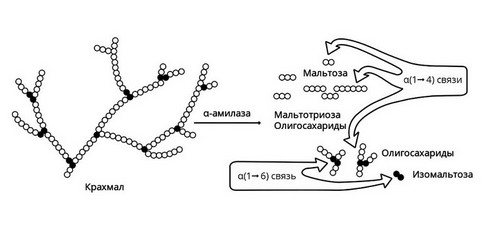
Рис. 2 — Амилаза начинает расщепление крахмала
Короткие углеводы, образовавшиеся под действием панкреатической амилазы, попадают в тонкий кишечник. Здесь с помощью мальтазы, лактазы, сахаразы, декстриназы они расщепляются до молекул глюкозы. Нерасщепляющаяся ферментами клетчатка выводится из кишечника с каловыми массами.
Протеазы
Белки или протеины - существенная часть человеческого рациона. Для их расщепления необходимы ферменты – протеазы. Они различаются по месту синтеза, субстратам и другим характеристикам. Некоторые из них активны в желудке, например, пепсин. Другие вырабатываются поджелудочной железой и активны в просвете кишечника. В самой железе выделяется неактивный предшественник фермента – химотрипсиноген, который начинает действовать только после смешивания с кислым пищевым содержимым, превращаясь в химотрипсин. Такой механизм помогает избежать самоповреждения протеазами клеток поджелудочной железы.
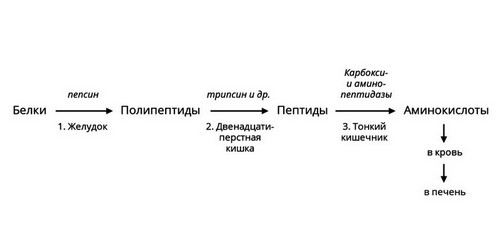
Рис. 3 — Ферментативное расщепление белков
Протеазы расщепляют пищевые белки на более мелкие фрагменты – полипептиды. Ферменты – пептидазы разрушают их до аминокислот, которые усваиваются в кишечнике.
Липазы
Пищевые жиры разрушаются ферментами-липазами, которые также вырабатываются поджелудочной железой. Они расщепляют молекулы жира на жирные кислоты и глицерин. Такая реакция требует наличия в просвете 12-перстной кишки желчи, образующейся в печени.
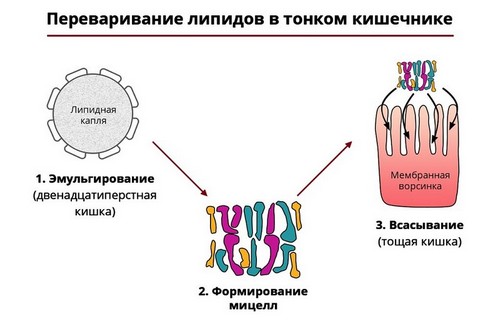
Рис. 4 — Ферментативный гидролиз жиров
Для многих людей с нарушением пищеварения, прежде всего с заболеваниями поджелудочной железы, назначение ферментов обеспечивает функциональную поддержку органа и ускоряет процессы выздоровления. После купирования приступа панкреатита или другой острой ситуации прием ферментов можно прекратить, так как организм самостоятельно восстанавливает их секрецию.
Длительный прием ферментативных препаратов необходим лишь при тяжелой внешнесекреторной недостаточности поджелудочной железы.
Показания для использования этого лекарства:
- хронический панкреатит, муковисцидоз и другие причины недостаточной секреции ферментов поджелудочной железы;
- воспалительные заболевания печени, желудка, кишечника, особенно после операций на них, для более быстрого восстановления пищеварительной системы;
- погрешности в питании;
- нарушение функции жевания, например, при стоматологических заболеваниях или малоподвижности пациента.
Прием пищеварительных ферментов с заместительной целью помогает избежать вздутия живота, жидкого стула, болей в животе. Кроме того, при тяжелых хронических заболеваниях поджелудочной железы Микразим полностью принимает на себя функцию по расщеплению питательных веществ. Поэтому они могут беспрепятственно усваиваться в кишечнике. Это особенно важно для детей, страдающих муковисцидозом.
Важно: перед применением ознакомьтесь с инструкцией или проконсультируйтесь с лечащим врачом.

Все биологические и химические процессы в клетках, благодаря ферментам, происходят при огромной скорости реакций. При этом сам фермент в этих процессах остается неизменным.
Ферменты — это.
Прежде чем приступить к лекции по теме ферментов, преподаватель одного из ВУЗов предложил студентам, для большего восприятия, послушать небольшую старинную притчу.
Перед смертью арабский старец разделил стадо из 17 верблюдов с чудесной белой шерстью на части, и в качестве наследства распределил между сыновьями. Старшему из сыновей завещал половину стада, средний — получал треть стада, младший сын получил – девятую часть.
После смерти отца перед сыновьями возникла проблема, как же разделить это количество верблюдов согласно завещанию, ведь число 17 нельзя поделить на 2 части, 3, либо 9 частей.
В это время по пустыне шел нищий, но мудрый монах (дервиш), ведя на поводке старого, черного, тощего верблюда. Заметив грустных братьев, поинтересовался чем те озабочены. И когда братья рассказали о полученном наследстве, которое не могут поделить, дервиш решил подарить им своего старого верблюда.
Когда верблюдов стало 18, их легко разделили. Старшему досталось – 9, средний получил – 6, а младший – 2. Черный верблюд дервиша остался лишним, и братья вернули его хозяину.
В этом случае роль ферментативного катализатора сыграл черный верблюд, но остался в прежнем статусе – собственностью дервиша.
Ферменты, либо энзимы, это молекулы белка, синтезируемые клетками организма. В составе каждой клетки имеется более сотни разновидностей энзимов.
При их помощи, в различных показателях температуры (5-40 градусов), характерных для определенного живого организма, реакции биохимических процессов протекают с очень большой скоростью.
Чтобы эти же процессы протекали не в живом организме, понадобились бы иные условия и критически высокая температура. Наши клетки бы в таких условиях погибли, так как для обеспечения их жизнедеятельности недопустимы какие-либо изменения в условиях их физиологического существования.
Благодаря своим свойствам ферменты получили статус биокатализаторов, веществ, ускоряющих процессы биохимических реакций в клетках, без которых они протекали бы в сотни, а то и в миллионы раз медленней.
Особенности и свойства ферментов
Первым это сделал в средине 20-х годов прошлого столетия американский ученый Д.Самнер, выделив кристаллы энзима, разлагающего мочевину – уреазу.
Лишь спустя десятилетия, пройдя длительный путь эволюции (что это?), удалось получить несколько разновидностей кристаллических ферментов и доказать их белковую природу.
Какими же свойствами обладают ферменты?
Несмотря на их огромное разнообразие, все ферменты на основании строения молекулярной кристаллической решетки разделяют на группы простых и сложных белков.
В основе сложной формы энзимов, кроме белковой фракции, присутствует так называемый кофактор, в виде добавочной небелковой группы происхождения, к примеру – различные варианты витамин.
В молекулярном составе простых белков (однокомпонентных) выделяется особая молекулярная часть энзимов, называемая активным центром. Он обеспечивает специфичность и каталитическую функцию фермента, благодаря уникальному сочетанию аминокислотных остатков.
Вступая в контакт с субстратом, реакция образует своеобразный комплекс с последующим его распадом на энзимы и вещества, образуемые после процессов реакции. По пространственной конфигурации субстрата и активного ферментативного центра они имеют точное соответствие, подобно тому как ключ подходит к отверстию в замке.
Наиболее эффективная активность ферментов, как, впрочем, и всех белков, отмечается лишь в нормальных естественных условиях и зависит от конкретных обстоятельств.
- Температуры — многие из ферментов проявляют активность лишь при определенных температурных показателях. К примеру, каталитическая активность (при среднем значении повышенной температуры до 50 С) увеличивается вдвое при каждом повышении температуры на 10 С. Но если температура превысит среднестатистическое значение, молекулярная структура белка нарушается и активность ферментативных реакций снижается.
- Определенного значения водородного показателя (рН), который индивидуален для каждого энзима и обеспечивает развитие его максимальной активности.
- Концентрации. Зависимости ферментативной реакции от количественной концентрации фермента и субстрата.
- Специфичности. Все энзимы специфичны к своему конкретному субстрату и катализируют, как правило, лишь одну определенную реакцию.
Именно ферментативная специфичность и тип катализирующей реакции лежат в основе классификации ферментов.
Классификация ферментов
Изначально многие ферменты носили упрощенные названия, не связанные часто с типом катализируемых реакций. Лишь в середине прошлого столетия была разработана и предложена систематическая номенклатура (что это такое?) и классификация ферментов на шесть главных классов.
Почти 3000 ферментов были распределены с учетом реакционной и субстратной составляющей и принципа катализирующего действия.
- Ферменты, входящие в класс оксидоредуктазы, катализируют различные окислительно-восстановительные реакции.
- Энзимы класса трансферазы ускоряют процессы переноса большинства функциональных кислотных группировок.
- Принадлежность к классу гидролазы характеризуется способностью расщепления веществ, состоящих из атомов различных химических соединений посредством обязательного наличия воды.
- Катализаторы группы лиазы расщепляют вещества без наличия жидкости, участвуют в процессах разрыва или присоединения веществ с кратными связями.
- Ферменты, относящиеся к группе изомеразы, обладают способностью превращения одних веществ в другие.
- Белковые фракции лигазы способны ускорять синтез различных сложных веществ (неорганических и органических групп) из простых веществ.
Для удобства пользования длинные названия ферментов заменили на более короткое рабочее обозначение, с опознавательным окончанием – аза, включающее название субстрата и тип ускоряемой реакции. Всем ферментам был присвоен классификационный шифр – КФ, включающий 4 цифры.
Первая – обозначает принадлежность к классу. Две последующих определяют тип подкласса и подподкласса. Последняя – порядковый номер элемента в определенном подклассе (к примеру, дегидрогеназа – КФ 1.3 99.3).
Практическая значимость энзимов
Практическую значимость ферментов трудно переоценить. Они применяются практически везде.
Используются для изготовления колбас, консервов, сыров и копченостей. Применяются для обработки зерновых культур и приготовления кормов. В кожевенной промышленности смягчают кожу. Являются составляющим компонентом чистящих средств, участвуют в огромном количестве химических процессов в различных производственных областях.
В медицине служат своеобразным диагностическим маркером развития патологических процессов – дисбаланс и признаки активности энзимов способствуют распознаванию природы различных заболеваний в организме.
Существование всего живого на земле обеспечивают процессы биохимических реакций с участием ферментативного катализа. Ферменты по праву считают основным источником здоровья и жизни любых живых организмов.
Эта статья относится к рубрикам:
Комментарии и отзывы (1)
Тяжело все это для восприятия, но вот одно я понял, мы состоим из совокупности элементарных организмов. Есть одноклеточные, а мы состоим из огромного числа клеток, а если бы не существовали ферменты, то химия не перешла бы в биологию и никакой жизни бы не было.

Ферме́нты, или энзи́мы (от лат. fermentum , греч. ζύμη , ἔνζυμον — закваска) — обычно белковые молекулы или молекулы РНК (рибозимы) или их комплексы, ускоряющие (катализирующие) химические реакции в живых системах. Реагенты в реакции, катализируемой ферментами, называются субстратами, а получающиеся вещества — продуктами. Ферменты специфичны к субстратам (АТФаза катализирует расщепление только АТФ, а киназа фосфорилазы фосфорилирует только фосфорилазу).
Ферментативная активность может регулироваться активаторами и ингибиторами (активаторы — повышают, ингибиторы — понижают).
Белковые ферменты синтезируются на рибосомах, а РНК — в ядре.
Наука о ферментах называется энзимологией, а не ферментологией (чтобы не смешивать корни слов латинского и греческого языков).
Содержание
История изучения
Термин фермент предложен в XVII веке химиком ван Гельмонтом при обсуждении механизмов пищеварения.
В кон. ХVIII — нач. XIX вв. уже было известно, что мясо переваривается желудочным соком, а крахмал превращается в сахар под действием слюны. Однако механизм этих явлений был неизвестен [1] .
В XIX в. Луи Пастер, изучая превращение углеводов в этиловый спирт под действием дрожжей, пришёл к выводу, что этот процесс (брожение) катализируется некой жизненной силой, находящейся в дрожжевых клетках.
Каталитическая активность РНК впервые была обнаружена в 1980-е годы у пре-рРНК Томасом Чеком, изучавшим сплайсинг РНК у инфузории Tetrahymena thermophila. Рибозимом оказался участок молекулы пре-рРНК Tetrahymena, кодируемый интроном внехромосомного гена рДНК; этот участок осуществлял аутосплайсинг, то есть сам вырезал себя при созревании рРНК.
Функции ферментов
Ферменты присутствуют во всех живых клетках и способствуют превращению одних веществ (субстратов) в другие (продукты). Ферменты выступают в роли катализаторов практически во всех биохимических реакциях, протекающих в живых организмах — ими катализируется более 4000 разных биохимических реакций [2] . Ферменты играют важнейшую роль во всех процессах жизнедеятельности, направляя и регулируя обмен веществ организма.
Например, одна молекула фермента ренина, содержащегося в слизистой оболочке желудка телёнка, створаживает около 10 6 молекул казеиногена молока за 10 мин при температуре 37 °C.
При этом эффективность ферментов значительно выше эффективности небелковых катализаторов — ферменты ускоряют реакцию в миллионы и миллиарды раз, небелковые катализаторы — в сотни и тысячи раз. См. также Каталитически совершенный фермент
Классификация ферментов
По типу катализируемых реакций ферменты подразделяются на 6 классов согласно иерархической классификации ферментов (КФ, EC — Enzyme Comission code). Классификация была предложена Международным союзом биохимии и молекулярной биологии (International Union of Biochemistry and Molecular Biology). Каждый класс содержит подклассы, так что фермент описывается совокупностью четырёх чисел, разделённых точками. Например, пепсин имеет название ЕС 3.4.23.1. Первое число грубо описывает механизм реакции, катализируемой ферментом:
- КФ 1: Оксидоредуктазы, катализирующие окисление или восстановление. Пример: каталаза, алкогольдегидрогеназа.
- КФ 2: Трансферазы, катализирующие перенос химических групп с одной молекулы субстрата на другую. Среди трансфераз особо выделяют киназы, переносящие фосфатную группу, как правило, с молекулы АТФ.
- КФ 3: Гидролазы, катализирующие гидролиз химических связей. Пример: эстеразы, пепсин, трипсин, амилаза, липопротеинлипаза.
- КФ 4: Лиазы, катализирующие разрыв химических связей без гидролиза с образованием двойной связи в одном из продуктов.
- КФ 5: Изомеразы, катализирующие структурные или геометрические изменения в молекуле субстрата.
- КФ 6: Лигазы, катализирующие образование химических связей между субстратами за счёт гидролиза АТФ. Пример: ДНК-полимераза.
Будучи катализаторами, ферменты ускоряют как прямую, так и обратную реакции, поэтому, например, лиазы способны катализировать и обратную реакцию — присоединение по двойным связям.
Соглашения о наименовании ферментов
Обычно ферменты именуют по типу катализируемой реакции, добавляя суффикс -аза к названию субстрата (например, лактаза — фермент, участвующий в превращении лактозы). Таким образом, у различных ферментов, выполняющих одну функцию, будет одинаковое название. Такие ферменты различают по другим свойствам, например, по оптимальному pH (щелочная фосфатаза) или локализации в клетке (мембранная АТФаза).
Кинетические исследования

Кривая насыщения химической реакции, иллюстрирующая соотношение между концентрацией субстрата [S] и скоростью реакции v
В 1972—1973 г.г. была создана первая квантово-механическая модель ферментативного катализа (авторы М. В. Волькенштейн, Р. Р. Догонадзе, З. Д. Урушадзе и др.) [3] [4] [5] [6] .
Структура и механизм действия ферментов
Активность ферментов определяется их трёхмерной структурой [7] .
Как и все белки, ферменты синтезируются в виде линейной цепочки аминокислот, которая сворачивается определённым образом. Каждая последовательность аминокислот сворачивается особым образом, и получающаяся молекула (белковая глобула) обладает уникальными свойствами. Несколько белковых цепей могут объединяться в белковый комплекс. Третичная структура белков разрушается при нагревании или воздействии некоторых химических веществ.
Активный центр ферментов
В активном центре условно выделяют [8] :
Чтобы катализировать реакцию, фермент должен связаться с одним или несколькими субстратами. Белковая цепь фермента сворачивается таким образом, что на поверхности глобулы образуется щель, или впадина, где связываются субстраты. Эта область называется сайтом связывания субстрата. Обычно он совпадает с активным центром фермента или находится вблизи него. Некоторые ферменты содержат также сайты связывания кофакторов или ионов металлов.
Фермент, соединяясь с субстратом:
Обычно присоединение фермента к субстрату происходит за счет ионных или водородных связей, редко — за счет ковалентных. В конце реакции её продукт (или продукты) отделяются от фермента.
В результате фермент снижает энергию активации реакции. Это происходит потому, что в присутствии фермента реакция идет по другому пути (фактически происходит другая реакция), например:
В отсутствие фермента:
В присутствии фермента:
где А, В — субстраты, АВ — продукт реакции, Ф — фермент.
Ферменты не могут самостоятельно обеспечивать энергией эндергонические реакции (для протекания которых требуется энергия). Поэтому ферменты, осуществляющие такие реакции, сопрягают их с экзергоническими реакциями, идущими с выделением большего количества энергии. Например, реакции синтеза биополимеров часто сопрягаются с реакцией гидролиза АТФ.
Для активных центров некоторых ферментов характерно явление кооперативности.
Специфичность
Ферменты обычно проявляют высокую специфичность по отношению к своим субстратам (субстратная специфичность). Это достигается частичной комплементарностью формы, распределения зарядов и гидрофобных областей на молекуле субстрата и в центре связывания субстрата на ферменте. Ферменты обычно демонстрируют также высокий уровень стереоспецифичности (образуют в качестве продукта только один из возможных стереоизомеров или используют в качестве субстрата только один стереоизомер), региоселективности (образуют или разрывают химическую связь только в одном из возможных положений субстрата) и хемоселективности (катализируют только одну химическую реакцию из нескольких возможных для данных условий). Несмотря на общий высокий уровень специфичности, степень субстратной и реакционной специфичности ферментов может быть различной. Например, эндопептидаза трипсин разрывает пептидную связь только после аргинина или лизина, если за ними не следует пролин, а пепсин гораздо менее специфичен и может разрывать пептидную связь, следующую за многими аминокислотами.




Более реалистичная ситуация в случае индуцированного соответствия. Неправильные субстраты — слишком большие или слишком маленькие — не подходят к активному центру
Модель индуцированного соответствия
Модификации
Многие ферменты после синтеза белковой цепи претерпевают модификации, без которых фермент не проявляет свою активность в полной мере. Такие модификации называются посттрансляционными модификациями (процессингом). Один из самых распространенных типов модификации — присоединение химических групп к боковым остаткам полипептидной цепи. Например, присоединение остатка фосфорной кислоты называется фосфорилированием, оно катализируется ферментом киназой. Многие ферменты эукариот гликозилированы, то есть модифицированы олигомерами углеводной природы.
Кофакторы ферментов
Некоторые ферменты выполняют каталитическую функцию сами по себе, безо всяких дополнительных компонентов. Однако есть ферменты, которым для осуществления катализа необходимы компоненты небелковой природы. Кофакторы могут быть как неорганическими молекулами (ионы металлов, железо-серные кластеры и др.), так и органическими (например, флавин или гем). Органические кофакторы, прочно связанные с ферментом, называют также простетическими группами. Кофакторы органической природы, способные отделяться от фермента, называют коферментами.
Фермент, который требует наличия кофактора для проявления каталитической активности, но не связан с ним, называется апо-фермент. Апо-фермент в комплексе с кофактором носит название холо-фермента. Большинство кофакторов связано с ферментом нековалентными, но довольно прочными взаимодействиями. Есть и такие простетические группы, которые связаны с ферментом ковалентно, например, тиаминпирофосфат в пируватдегидрогеназе.
Регуляция работы ферментов
У некоторых ферментов есть сайты связывания малых молекул, они могут быть субстратами или продуктами метаболического пути, в который входит фермент. Они уменьшают или увеличивают активность фермента, что создает возможность для обратной связи.
Ингибирование конечным продуктом
Метаболический путь — цепочка последовательных ферментативных реакций. Часто конечный продукт метаболического пути является ингибитором фермента, ускоряющего первую из реакций данного метаболического пути. Если конечного продукта слишком много, то он действует как ингибитор для самого первого фермента, а если после этого конечного продукта стало слишком мало, то первый фермент опять активируется. Таким образом, ингибирование конечным продуктом по принципу отрицательной обратной связи — важный способ поддержания гомеостаза (относительного постоянства условий внутренней среды организма).
Влияние условий среды на активность ферментов
Активность ферментов зависит от условий в клетке или организме — давления, кислотности среды, температуры, концентрации растворённых солей (ионной силы раствора) и др.
Множественные формы ферментов
Множественные формы ферментов можно разделить на две категории:
- Изоферменты
- Собственно множественные формы (истинные)
Изоферменты — это ферменты, синтез которых кодируется разными генами, у них разная первичная структура и разные свойства, но они катализируют одну и ту же реакцию. Виды изоферментов:
- Органные — ферменты гликолиза в печени и мышцах.
- Клеточные — малатдегидрогеназа цитоплазматическая и митохондриальная (ферменты разные, но катализируют одну и ту же реакцию).
- Гибридные — ферменты с четвертичной структурой, образуются в результате нековалентного связывания отдельных субъединиц (лактатдегидрогеназа — 4 субъединицы 2 типов).
- Мутантные — образуются в результате единичной мутации гена.
- Аллоферменты — кодируются разными аллелями одного и того же гена.
Собственно множественные формы (истинные) — это ферменты, синтез которых кодируется одним и тем же аллелем одного и того же гена, у них одинаковая первичная структура и свойства, но после синтеза на рибосомах они подвергаются модификации и становятся разными, хотя и катализируют одну и ту же реакцию.
Изоферменты разные на генетическом уровне и отличаются от первичной последовательности, а истинные множественные формы становятся разными на посттрансляционном уровне.
Медицинское значение
Если происходит мутация в гене, кодирующем определенный фермент, может измениться аминокислотная последовательность фермента. При этом в результате большинства мутаций его каталитическая активность снижается или полностью пропадает. Если организм получает два таких мутантных гена (по одному от каждого из родителей), в организме перестает идти химическая реакция, которую катализирует данный фермент. Например, появление альбиносов связано с прекращением выработки фермента тирозиназы, отвечающего за одну из стадий синтеза темного пигмента меланина. Фенилкетонурия связана с пониженной или отсутствующей активностью фермента фенилаланин-4-гидроксилазы в печени.
В настоящее время известны сотни наследственных заболеваний, связанные с дефектами ферментов. Разработаны методы лечения и профилактики многих из таких болезней.
Практическое использование
Ферменты широко используются в народном хозяйстве — пищевой, текстильной промышленности, в фармакологии и медицине. Большинство лекарств влияют на течение ферментативных процессов в организме, запуская или приостанавливая те или иные реакции.
Ещё шире область использования ферментов в научных исследованиях и в медицине.
Читайте также:

