Что такое бужирование кишечника и как оно проводится кратко
Обновлено: 02.07.2024
Проблема образования стриктур межкишечных анастомозов и их лечения становится все более актуальной. Это обусловлено увеличением количества тяжелых операций на толстой и тонкой кишке в связи с ростом онкологических и воспалительных заболеваний кишечника с первичным наложением анастомоза или реконструктивных операций после первичных обструктивных резекций или резекций с формированием первичной стомы. Технические сложности хирургической операции, преклонный возраст больных, наличие сопутствующих заболеваний делают эндоскопический способ лечения рубцовых стриктур толстокишечных анастомозов предпочтительным.
Острая кишечная непроходимость — это острая ситуация, требующая немедленного медицинского вмешательства. Чаще всего причиной подобного состояния является колоректальный рак [1—4]. Также к кишечной непроходимости могут приводить рубцовые стриктуры после перенесенных операций, лучевая терапия, воспалительные заболевания кишечника, дивертикулиты, ишемическое повреждение [3—13]. Самой частой причиной формирования послеоперационных межкишечных стриктур является рубцовое или воспалительное сужение зоны анастомоза, который формируется забрюшинно в дистальной трети прямой кишки [3, 8—13]. До конца не ясны механизмы, приводящие к формированию стриктуры зоны анастомоза в послеоперационном периоде, однако ишемия и повреждение слизистой оболочки считаются ведущими в патофизиологической схеме формирования стриктур [15—17]. Известно, что частоту возникновения стриктур увеличивает использование скрепок при аппаратном формировании анастомоза по сравнению с методикой формирования анастомоза ручным способом [18, 19].
Развитие стриктуры в послеоперационном периоде не является редким случаем, она может формироваться у 30% пациентов, и зависит это от техники или вида операции, локализации анастомоза [12—14], а также от наличия или отсутствия стомы.
После формирования анастомоза могут появиться клинические признаки частичной или полной кишечной непроходимости. Эндоскопическим признаком сформировавшейся стриктуры является невозможность завести 12-миллиметровый гибкий эндоскоп за зону сужения [20—21].
В течение длительного времени все стриктуры подлежали хирургическому лечению с резекцией зоны анастомоза и последующим повторным наложением анастомоза [8]. На сегодняшний день известно, что стриктуры, требующие хирургической коррекции, развиваются лишь в 5—20% случаев. Остальные ситуации поддаются эндоскопическому лечению.
Баллонная дилатация
Эндоскопическая баллонная дилатация является методом выбора при лечении доброкачественных межкишечных стриктур. Впервые данная методика была использована для лечения доброкачественных колоректальных стриктур в 1984 г. [22].
Методика выполнения данной манипуляции стандартная. Для установки баллонов необходимо использование эндоскопа экспертного класса с широким рабочим каналом. Для визуализации стриктуры (ширина просвета, протяженность) в просвет кишки по катетеру вводится водорастворимый контраст (гастрографин). Затем с помощью проводника в область стриктуры устанавливался катетер 7 °F. Далее в область стриктуры вводится гидростатический баллон, с помощью которого под рентгенологическим контролем производится 1—2 этапа дилатации (длительность каждого этапа — 30 с). В зависимости от диаметра стриктуры используются баллоны (с максимальным диаметром 20 мм), которые в процессе заполняются водой. Баллоны при раздувании оказывают давление на зону стриктуры. В течение 2—3 сеансов используются баллоны все большего диаметра, что позволяет расширить просвет анастомоза на длительный срок. Тем не менее результаты лечения можно прогнозировать только после выполнения первого этапа дилатации.
Удовлетворительным результатом проведенной процедуры является свободное движение баллона через зону стриктуры и дальнейшее проведение аппарата по кишке за область стеноза. Клинически эффективность оценивалась в течение 48 ч и определялась как устранение симптомов непроходимости после технически удачно проведенной процедуры. Рестенозирование определялось как возвращение кишечной симптоматики в течение периода наблюдения. Также метод расценивался как неэффективный, если после баллонной дилатации требовалось другое эндоскопическое или хирургическое лечение.
В исследовании G. Vanbiervliet и соавт. [23] было отобрано 29 пациентов, получавших терапию с помощью баллонной дилатации. Пациенты находились под наблюдением в течение 13 лет (1999—2013). По результатам исследования было выявлено, что технически дилатацию удалось выполнить в 98,5% случаев, при этом клинический эффект был достигнут у 89,1% пациентов. Реобструкция возникла у 54,4% пациентов. Осложнения в виде перфорации отмечались после 2 (3,1%) процедур, при этом одна перфорация была выявлена в области поперечной ободочной кишки и потребовала хирургического вмешательства; вторая перфорация была скорректирована консервативно, с применением антибиотиков. В одном случае (1,5%) отмечалось формирование свища. Таким образом, метод был расценен как эффективный и безопасный, риск развития осложнений был связан лишь с наличием протяженной стриктуры.
В исследование К. Suchan и соавт. [11] было включено 94 пациента с послеоперационными анастомотическими стриктурами. Среди них дилатация оказалась успешной у 59% пациентов, которые исходно были прооперированы по поводу рака, и у 88% пациентов, перенесших резекцию по поводу доброкачественных заболеваний. Осложнения отмечались у 17 пациентов, при этом преимущественно у пациентов, исходно перенесших резекцию по поводу рака (у 16 пациентов). Основным по частоте осложнением был рестеноз (n=10) только после исходных резекций по поводу рака (р=0,05). Это потребовало хирургического лечения у 8 пациентов. С течением времени сведения о результатах этого метода лечения менялись [24].
Несмотря на безопасность и почти 80-процентную эффективность, данная методика нередко требует нескольких этапов лечения в связи с высокой частотой рецидивов стриктур [25].
Оценив полученные результаты, удалось выявить некоторые предикторы эффективности данного метода:
— ширина просвета стриктуры менее 10 мм;
— протяженность стриктуры не более 4 см;
— стриктура сформировалась в зоне послеоперационного анастомоза.
Также были выявлены предикторы неэффективности данной методики:
— полная обструкция просвета;
— формирование свищей в области стриктуры;
— активное воспаление в области стриктуры;
— недавно перенесенное хирургическое вмешательство с воздействием на область стриктуры;
— формирование плотного изгиба в зоне стриктуры;
Таким образом, высокая эффективность и низкий риск развития осложнений делают баллонную дилатацию методом выбора при лечении стриктур межкишечных анастомозов [11].
Саморасширяющийся металлический стент
Саморасширяющийся металлический стент (SEMS) считается методом лечения доброкачественных межкишечных стриктур [26]. В отличие от непокрытых стентов полностью покрытые SEMS имеют ряд преимуществ в процессе лечения. В частности, при установке стента одновременно с наложением анастомоза реакция местных тканей проявляется в значительно меньшей степени, чем при обычном формировании анастомоза с помощью сшивающего аппарата, поэтому SEMS могут использоваться в случае осложнений, таких как кишечные стриктуры, свищи, перфорации и другие повреждения ЖКТ [27, 28]. Однако установка постоянного SEMS связана с возможным возникновением ряда осложнений, таких как образование новых стриктур или перфорации. Лишь в небольшом числе исследований сообщалось о достижении полного эффекта у пациентов с доброкачественными стриктурами, которым был установлен SEMS.
В одном из недавних исследований, в которое были включены 43 пациента, сообщалось об эффективности подобного лечения. Все пациенты наблюдались в течение 6 лет. В процессе наблюдения оценивались эффективность стентирования, технические характеристики, возможности извлечения стента, безопасность, а также частота рецидивирования стриктур. В результате установка стента прошла успешно у всех пациентов. Клинический эффект был получен у 81% пациентов, миграция стента наблюдалась у 63%. Средняя продолжительность стояния стента составила 21 день. Важно отметить, что рецидив симптомов кишечной непроходимости наблюдался у 53% пациентов независимо от возникновения такого состояния, как миграция стента. Авторы резюмировали, что установка полностью покрытых SEMS безопасна и эффективна при лечении доброкачественных колоректальных стриктур с клиническими проявлениями кишечной непроходимости, несмотря на высокий процент спонтанной миграции стентов [29]. Данное исследование не может четко определить предикторы эффективности и неэффективности лечения, оно показывает, что пациентам с рефрактерными стриктурами, перенесшим несколько сеансов баллонной дилатации, может быть показан этот метод лечения. Однако необходимо учитывать, что применение данной методики может быть ограничено в связи с высокой стоимостью стентов.
Биоразлагаемые стенты
В последнее время для лечения доброкачественный стриктур используются биоразлагаемые стенты. Ранее поли-L-молочный стент и полидиоксаноновый стент в основном использовались для расширения стриктур пищевода.
Полидиоксаноновый стент является полукристаллическим биоразлагаемым полимером, который разлагается путем гидролиза при низких значениях рН. Ни один из продуктов разложения не является вредным. Длительный эффект, сохраняющийся до момента разложения стента, делает стентирование методом выбора в случае неэффективности баллонной дилатации у пациентов со стриктурой пищевода [30, 31]. В настоящее время предпринимаются попытки применения биоразлагаемых стентов у пациентов с колоректальными стриктурами. Использование биоразлагаемого стента оправдано, если стриктура находится близко к анусу (так как стент негибкий) и имеется возможность его надежно зафиксировать [32]. В другое исследование были включены 11 пациентов с послеоперационными стриктурами, располагающимися на расстоянии не более 20 см от ануса, рефрактерными к механическому бужированию или баллонной дилатации (не менее 3 этапов). У 5 была достигнута полная ремиссия и отсутствие симптомов. У 2 возникла необходимость в хирургическом лечении. Таким образом, эффективность данной методики составила 45% [33] при ее безопасности. Несмотря на риск возможной миграции стента, при использовании стентов с большим диаметром и при отсутствии его миграции могут быть достигнуты хорошие результаты в лечении доброкачественных колоректальных стриктур. Однако, как и в случае с саморасширяющимися стентами, применение методики может быть ограничено высокой стоимостью биоразлагаемого стента (до 1000 $).
Электрокоагуляция
Широко распространенной, доступной и эффективной методикой лечения доброкачественных стриктур является электрокоагуляция пораженной зоны. Так, в исследование G. Brandimarte и соавт. [34] были включены 39 пациентов, у которых были выявлены послеоперационные стриктуры в 7—12 см от края ануса. При проведении процедуры сфинктеротом располагался центрально, после чего бимодально подавался ток и в области стриктуры выполнялись 6 радиальных надрезов. Длина и глубина надрезов определялись в соответствии с размерами стриктуры (в качестве измерительного прибора использовались открытые биопсийные щипцы размером 8 мм). После процедуры пациенты находились под наблюдением 8—43 мес (в среднем 25 мес). Каких-либо осложнений, а также рецидива стриктуры выявлено не было ни в одном случае.
Еще в одном исследовании были оценены результаты, полученные на протяжении 12 лет у 60 пациентов. По поводу доброкачественных стриктур анастомозов всем пациентам производилась электрокоагуляция. Осложнений во время процедуры не отмечалось. Рестенозирование было выявлено лишь у 3 пациентов, впоследствии благополучно пролеченных с помощью еще одного сеанса электрокоагуляции.
В исследовании В.В. Веселова и соавт. [35] электрокоагуляция с применением шаровых электродов использовалась в рамках комплексной терапии стриктур межкишечных анастомозов. С помощью электрокоагуляции создавался узкий раневой канал (до 5 мм), который в дальнейшем бужировался с помощью различных методов (баллонная дилатация, аппаратное бужирование, механическое бужирование). Из 26 пациентов, которым было проведено лечение, удовлетворительные результаты были получены у 20 (ширина просвета в зоне стриктуры более 10 мм).
Таким образом, данная процедура может быть рекомендована в при плотных фиброзных стриктурах, а также в случае невозможности проведения или неэффективности баллонной дилатации [22, 36].
Лазерная коагуляция
Одной из первых попыток лечения доброкачественных толстокишечных стриктур можно считать попытку применения лазерной коагуляции. Так, в исследование А. Löffler и соавт.[37] были включены 22 пациента с послеоперационными стриктурами, локализующимися в ректосигмоидном отделе. После выполнения лазерной коагуляции результаты были превосходны у 21 пациента (у 1 пациента потребовалось расширение стриктуры под анестезией до 1,8 см, однако впоследствии наблюдался рецидив заболевания). Дальнейшего распространения методика не получила в связи с высокой себестоимостью.
Бужирование
Аппаратное бужирование
В качестве еще одной методики эндоскопического лечения стриктур межкишечных анастомозов можно использовать эндоскопическое (аппаратное) бужирование. Данная методика предусматривает последовательную смену аппаратов с увеличением их диаметра от 6 до 18 мм. В исследование было включено 15 пациентов. В 6 случаях было достаточно одного этапа лечения, а в 9 других случаях понадобилось от 2 до 5 этапов вмешательства [35]. Данный метод может быть рекомендован, если стриктура анастомоза слишком плотная и не позволяет выполнить баллонную дилатацию.
Комбинированные методики лечения
— электродеструкция и аппаратное бужирование (15 больных);
— электродеструкция и механическое бужирование (7 больных);
— электродеструкция, аппаратное и механическое бужирование (4 больных).
При электродеструкции стриктуры с аппаратным бужированием для достижения необходимой ширины просвета кишки в зоне анастомоза в 6 случаях достаточно было одного этапа лечения, а в 9 других случаях понадобилось от 2 до 5 этапов вмешательства. При комбинации электрокоагуляции и механического бужирования в 5 случаях коррекция стриктуры была достигнута за один этап бужирования, в 2 — в несколько этапов — 5 и 7 соответственно. В одном случае, при комбинации эндоскопического пособия и механического бужирования, произошла перфорация стенки кишки в зоне сигморектального анастомоза (на 9 см от анального канала), которая потребовала оперативного вмешательства в объеме ушивания перфоративного отверстия. Наряду с электродеструкцией стриктуры в 4 наблюдениях для достижения лечебного эффекта проводилось как аппаратное, так и механическое бужирование. Во всех случаях манипуляция проводилась многоэтапно. Таким образом, из 26 пациентов, которым проводилась эндоскопическая коррекция по поводу стриктур межкишечных анастомозов, у 20 пациентов результаты расценены как удовлетворительные после первого курса бужирования и у одного — после второго курса. У 5 пациентов результаты эндоскопического лечения рубцовых стриктур межкишечных анастомозов признаны неудовлетворительными. Следует отметить, что у всех 5 пациентов с неудовлетворительными результатами эндоскопического лечения протяженность рубцовых стриктур составляла от 12 до 20 мм. У пациентов с удовлетворительными результатами лечения протяженность стриктур составляла: в 1 случае — 9 мм, в 4 — 5—6 мм и в 16 — 2—4 мм.
Заключение
В течение длительного времени при обнаружении межкишечных стриктур отсутствовали альтернативы хирургическому лечению. На сегодняшний день развитие эндоскопических технологий позволяет выполнять малоинвазивные манипуляции для лечения стриктур межкишечных анастомозов. Учитывая большое количество возможных методов, можно выбрать наилучшую тактику лечения в каждом конкретном случае.
Таким образом, эндоскопическое лечение стриктур анастомозов является эффективной методикой в большинстве случаев. Оно наиболее предпочтительно, так как позволяет избежать серьезных осложнений. Единственное часто встречающееся осложнение после эндоскопического лечения — рестеноз — наблюдается после резекции по поводу злокачественных новообразований. Однако в подавляющем большинстве случаев рестеноз успешно устраняется с помощью повторного эндоскопического лечения. Необходимо продолжение исследований, направленных на изучение условий и закономерностей при проведении эндоскопического лечения, а также эффективности и показаний к применению различных методов эндоскопического лечения стриктур межкишечных анастомозов.
Очень важно, чтобы каждый пациент выписываясь из стационара после операции,научился ухаживать за стомой и следить за ее состоянием. В частности, следить следует за видоизменением стомы, не допуская ее сужения (стеноза). Для того чтобы не довести стому до состояния стеноза, необходимо в домашних условиях проводить бужирование.
Что такое бужирование?
Это механическое расширение и растягивание отверстия стомы, которое пациент может проделывать как самостоятельно, так и с помощью родственников (либо специалистов в стенах стационара). Техника бужирования очень проста.
На кисть руки надевается тонкая медицинская резиновая перчатка, продающаяся в любой аптеке. Один из пальцев (начинать можно с мизинца) обильно смазывается вазелином и вводится в стому на глубину 3 4 см, при этом им производятся вращательные движения, а также движения вверх вниз.
Этот страх понятен, поэтому первое бужирование необходимо проводить под контролем опытного специалиста. Стоматерапевт в доступной форме объяснит вам необоснованность ваших страхов. Во первых, слизистая стомы не имеет нервных окончаний, следовательно, с ее стороны болевых ощущений пациент испытывать не может.
Если же кожа заросла настолько, что растягивается болезненно и с трудом – это повод к оперативному вмешательству (реконструкции стомы). Не стоит также опасаться появления небольшого кровотечения в процессе бужирования.
В том же случае, если палец (даже мизинец) в стому ввести не удается, следует срочно обратиться к вашему стоматерапевту (либо к хирургу). Помните, что успех послеоперационного периода во многом зависит не только от профессионализма врачей, но и от вас самих.
Эндоскопическое бужирование – это малоинвазивное вмешательство, нацеленное на увеличение просвета анастомоза или полого органа (желудка, пищевода, толстой кишки, желчных протоков) для восстановления его проходимости. Предполагает введение в суженный участок специального инструмента – бужа. При восстановлении просвета толстой кишки, желчных протоков, пищевода и желудка процесс бужирования отличается высокой безопасностью, поскольку врач идеально контролирует процесс благодаря высокоточной оптике современного японского эндоскопа.
Эндоскопическое бужирование пищевода, желудка, других полых органов и анастомозов проходит с минимальным дискомфортом. Процедура демонстрирует длительный терапевтический эффект.
Цель бужирования
Главная цель эндоскопического лечебного бужирования – восстановление нормального просвета полых органов и анастомозов.
Процедура позволяет вернуть возможность самостоятельного питания пациентам с серьёзными стенозами, а также устранить риск развития кишечной непроходимости.
В онкологии бужирование пищевода является частью комплексной терапии опухолевых стенозов. Процедура позволяет временно расширить просвет в области увеличивающегося новообразования перед выполнением брахитерапии и установкой стента.
Показания к бужированию
Расширение просвета анастомозов и полых органов (желчных протоков, толстой кишки, желудка, пищевода) методом бужирования обычно проводится в случае обнаружения послеожоговых и пептических стриктур, нарушения проходимости на фоне ахалазии кардии, прогрессирующих опухолях.
Бужирование показано при:
- сужении пищеводных анастомозов;
- стриктурах низкорасположенных кишечных анастомозов;
- рубцовых сужениях пищевода (II-IV стадии);
- рубцовых сужениях анального канала, дистальных отделов сигмовидной или прямой кишки.
Порядок выполнения бужирования
Бужирование органов ЖКТ выполняется в несколько этапов:
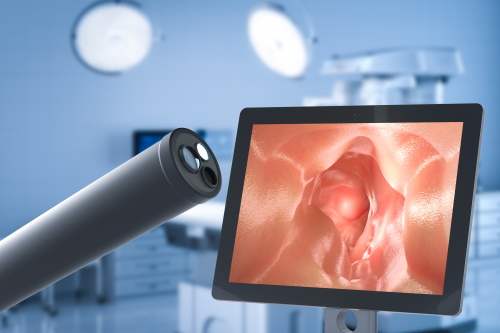
- Введение эндоскопа в пищевод. Врач осматривает ткани, обнаруживает сужение, оценивает его размер при помощи видеокамеры, которая расположена на конце гибкого эндоскопа, и передаёт изображение на монитор высокого разрешения.
- Подбор и первичный ввод бужа. В зависимости от размера стриктуры врач подбирает самый небольшой по диаметру буж и вводит его в просвет, используя для этого канал эндоскопа. Этот процесс называется пробным бужированием. Врач аккуратно проталкивает буж по всей длине сужения, увеличивая просвет органа или анастомоза. Для закрепления результата врач повторяет процедуру.
- Повторное введение бужа. Врач берёт буж большего диаметра, а затем проталкивает его по всей длине сужения. Это ведёт к ещё большему расширению просвета. Специалист повторяет процедуру несколько раз.
Завершение процедуры. Сформировав просвет необходимого диаметра, врач извлекает эндоскоп и приводит пациента в чувство.
Подготовка к бужированию
Перед бужированием анального канала и нижних отделов ЖКТ в вечер перед процедурой необходимо провести очистку кишечника. Для этого может быть использована медицинская клизма или слабительные средства. В последнем случае следует проконсультироваться с врачом.
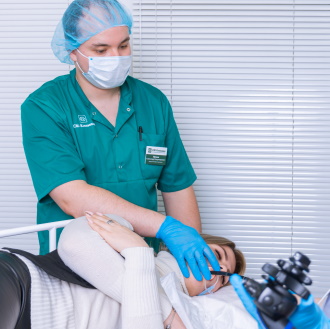
Процедура бужирования во сне
Медикаментозный сон предполагает использование безопасных седативных препаратов, которые имеют минимальный список противопоказаний и достаточно легко переносятся организмом. Вмешательство проходит под контролем врача-анестезиолога. Он индивидуально подбирает препараты и дозировку для каждого пациента.
- Консультации врачей. Выполняется бужирование по направлению лечащего врача. Его можно получить, записавшись на приём. Также перед процедурой пациенту необходимо проконсультироваться с терапевтом, анестезиологом и другими специалистами.
- Лабораторные анализы. Перед бужированием пациентам назначают общий анализ крови, коагулограмму, БАК, устанавливают группу и резус-фактор, а также другие исследования, которые позволят исключить противопоказания.
- Инструментальные исследования. Пациентам старше 50 лет и тем, кто страдает от сердечно-сосудистых заболеваний, рекомендуется выполнение ЭКГ. Также может быть назначена рентген ОГК и другие обследования.
Анализ на госпитальные инфекции. Процедура бужирования органов ЖКТ и другие эндоскопические вмешательства предполагает сдачу анализов на гепатит, ВИЧ и сифилис.

Полезная информация
Срок и характер терапии зависят от клинической картины и особенностей строения организма пациента. Как правило, лечение включает несколько сеансов бужирования и динамическое наблюдение.
- Основная терапия. Как правило, для расширения просвета полого органа в 15 мм и анастомоза в 20 мм необходимо от 4 до 5 процедур. Сеансы выполняются раз в 3-4 дня.
- Поддерживающая терапия. После завершения основной терапии бужирование выполняется 1 раз в 7 дней. Это необходимо для достижения стабильного результата. Постепенно перерывы между сеансами увеличиваются до 2-3 недель, а если врач отмечает отсутствие сужения – до 4 недель. Поддерживающая терапия может длиться от 3 месяцев до полугода.
- Динамическое наблюдение. После окончания поддерживающей терапии пациенту необходимо проходить ежегодное эндоскопическое обследование.
Периодичность регулярных обследований устанавливает лечащий врач. Если основная и поддерживающая терапии показали успешный результат, повторное лечение обычно не требуется.
Эндоскопические способы бужирования малотравматичны, поэтому имеют незначительный список противопоказаний. Процедура не проводится пациентам, страдающим от:
- свищей желудочно-кишечного тракта;
- кровотечений из органов ЖКТ;
- острых инфекционных заболеваний;
- обострения эзофагита;
- ряда злокачественных новообразований;
- плохой свёртываемости крови;
- полной кишечной непроходимости;
- критического стеноза;
- физических, химических и пептических повреждений слизистой (свежих);
- аневризмы аорты;
- инфаркта миокарда и инсульта.
Бужирование также имеет некоторые ограничения, к которым относятся:
- серьёзные искривления позвоночного столба;
- тяжёлые психические заболевания;
- наличие крупного зоба;
- гемофилия;
- тяжёлая сердечно-лёгочной недостаточностьи.
Выберите специалиста в удобной для вас клинике:
Статьи


Все материалы данного сайта являются объектами авторского права (в том числе дизайн). Запрещается копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного письменного согласия правообладателя. Указание ссылки на источник информации является обязательным.
Диагностика сужений прямой кишки. Лечение сужений прямой кишки.
Для диагностики врожденных стриктур применяются известные в проктологии методы исследования. Уровень и характер сужения могут быть определены с помощью зонда или другого инструмента — зажима Кохера, Пеана, при исследовании пальцем хирурга, а также с помощью анускопа, ректального зеркала, ректороманоскопа, рентгенологического исследования.
Начинать исследование нужно пальцем. При этом наилучшим образом определяется высота расположения стриктуры, ее плотность, растяжимость, иногда протяженность, состояние сфинктера и стенки кишки ниже стриктуры, а если удастся проникнуть выше сужения, то и состояние вышележащего отдела кишки.
Зонд и другие малого диаметра инструменты могут оказать некоторую помощь в диагностике характера сужения только при очень узком просвете его. Может быть установлена протяженность стриктуры. Более объемистые инструменты — детское ректальное зеркало, детский ректороманоскоп, анускоп, как правило, дают возможность осмотреть только нижний отдел кишки до места сужения и видеть просвет рубцового кольца.
Проникнуть этими инструментами выше сужения обычно не удается. С помощью рентгенографии можно получить точные данные о месте расположения стриктуры, ее протяженности, о состоянии вышерасположенных отделов толстой кишки.
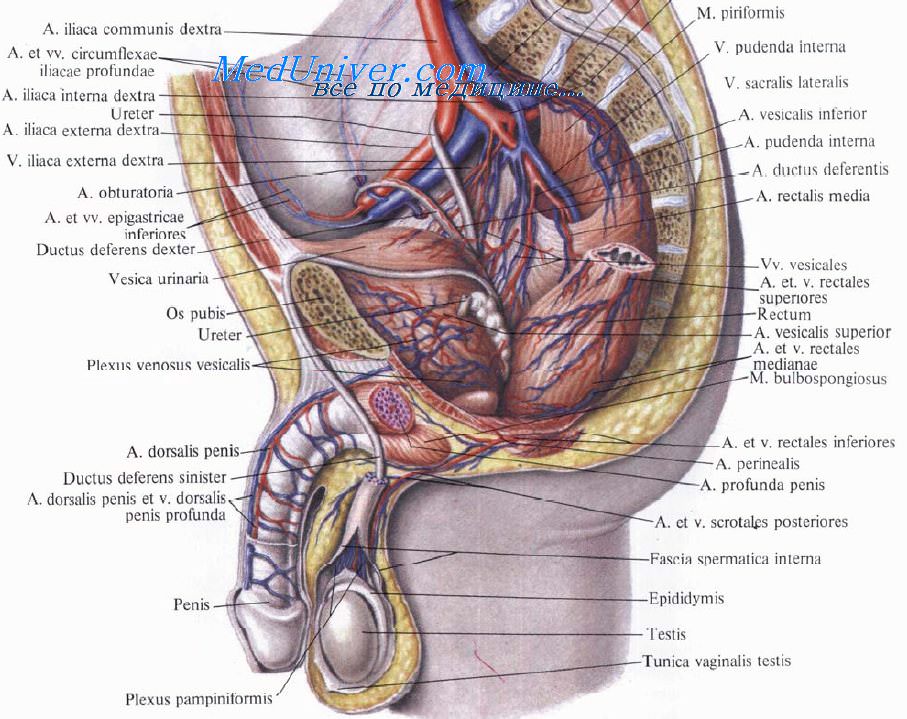
-- картинку можно увеличить --
Методы лечения врожденных стриктур прямой кишки варьируют в зависимости от возраста пациента, высоты расположения, протяженности стриктуры и других данных, характеризующих это врожденное уродство.
Наиболее распространенным методом лечения врожденных стриктур в раннем детском возрасте является бужирование. Для этой цели применяются расширители Гегара, специальные дилятаторы Brown, Schoen, пальцы медицинского работника или матери ребенка. Лучше всего обучить мать и она будет в домашних условиях бужировать пальцем задний проход у своего ребенка систематически, с любовью и настойчивостью.
Для бужирования пальцем на руку надевают резиновую перчатку. Палец смазывают вазелином и постепенно вводят в задний проход больного. Вначале нужно использовать мизинец, затем — средние пальцы и под конец даже большой палец руки.
В зависимости от первичного диаметра просвета сужения, плотности и протяженности суживающего кольца бужирование приходится применять на протяжении недель, месяцев, а иногда, с перерывами, в течение нескольких лет.
При плотных, нерастяжимых, рубцовых стриктурах показано оперативное лечение. Оно может быть применено в виде следующих основных вмешательств:
1) рассечение стриктуры в одном или в двух направлениях с последующим систематическим бужированием до полного заживления получившейся на месте рассечения раны (ран);
2) продольное рассечение стриктуры в одном или двух направлениях с последующим зашиванием полученной раны (ран) в поперечном направлении;
3) иссечение со стороны просвета кишки всего суживающего кольца с последующим сшиванием выше- и нижележащих здоровых участков стенки прямой кишки; эта операция легко выполнима лишь при расположении суживающего кольца не выше как на 4 см от заднего прохода — операция Гартмана;
4) резекция всей толщи стенки кишки вместе со стенозирующим ее рубцом с последующим сшиванием конец в конец всех слоев кишки; эта операция выполняется через брюшную полость при, расположении суживающего; кольца более чем на 5—6 см от заднего прохода.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

