Технология обогащения марганцевых руд реферат
Обновлено: 05.07.2024
Ма́рганец — элемент побочной подгруппы седьмой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 25. Обозначается символом Mn (лат. Manganum , ма́нганум , в составе формул по-русски читается как марганец , например, KMnO4 — калий марганец о четыре ; но нередко читают и как манган ). Простое вещество марганец (CAS-номер: 7439-96-5) — металл серебристо-белого цвета. Известны пять аллотропных модификаций марганца — четыре с кубической и одна с тетрагональной кристаллической решёткой.
Марганец твердый хрупкий металл. Известны четыре кубические модификации металлического марганца. При температурах от комнатной и до 710°C устойчив a-Mn, параметр решетки а = 0,89125 нм, плотность 7,44 кг/дм3. В интервале температур 710-1090°C существует b-Mn, параметр решетки а = 0,6300 нм; при температурах 1090-1137°C — g-Mn, параметр решетки а = 0,38550 нм. Наконец, при температуре от 1137°C и до температуры плавления (1244°C) устойчив d-Mn с параметром решетки а = 0,30750 нм. Модификации a, b, и d хрупкие, g-Mn пластичен. Температура кипения марганца около 2080°C.
На воздухе марганец окисляется, в результате чего его поверхность покрывается плотной оксидной пленкой, которая предохраняет металл от дальнейшего окисления. При прокаливании на воздухе выше 800°C марганец покрывается окалиной, состоящей из внешнего слоя Mn3O4 и внутреннего слоя состава MnO.
Марганец образует несколько оксидов: MnO, Mn3O4, Mn2O3, MnO2 и Mn2O7. Все они, кроме Mn2O7, представляющего собой при комнатной температуре маслянистую зеленую жидкость с температурой плавления 5,9°C, твердые кристаллические вещества.
Монооксид марганца MnO образуется при разложении солей двухвалентного марганца (карбоната и других) при температуре около 300°C в инертной атмосфере:
MnCO3 = MnO + CO2
Этот оксид обладает полупроводниковыми свойствами. При разложении MnOОН можно получить Mn2O3. Этот же оксид марганца образуется при нагревании MnO2 на воздухе при температуре примерно 600°C:
4MnO2 = 2Mn2O3 + O2
Оксид Mn2O3 восстанавливается водородом до MnO, а под действием разбавленных серной и азотной кислот переходит в диоксид марганца MnO2.
Если MnO2 прокаливать при температуре около 950°C, то наблюдается отщепление кислорода и образование оксида марганца состава Mn3O4:
3MnO2 = Mn3O4 + O2
Этот оксид можно представить как MnO·Mn2О3, и по свойствам Mn3О4 соответствует смеси этих оксидов.
Диоксид марганца MnO2 — наиболее распространенное природное соединение марганца в природе, существующее в нескольких полиморфных формах. Так называемая b-модификация MnO2 — это уже упоминавшийся минерал пиролюзит. Ромбическая модификация диоксида марганца, g-MnO2 также встречается в природе. Это — минерал рамсделит (другое название — полианит).
Диоксид марганца нестехиометричен, в его решетке всегда наблюдается дефицит кислорода. Если оксиды марганца, отвечающие его более низким степеням окисления, чем +4, — основные, то диоксид марганца обладает амфотерными свойствами. При 170°C MnO2 можно восстановить водородом до MnO.
Если к перманганату калия KMnO4 добавить концентрированную серную кислоту, то образуется кислотный оксид Mn2O7, обладающий сильными окислительными свойствами:
2KMnO4 + 2H3SO4 = 2KHSO4 + Mn2O7 + H3O.
Mn2O7 — кислотный оксид, ему отвечает сильная, не существующая в свободном состоянии марганцовая кислота НMnO4.
При взаимодействии марганца с галогенами образуются дигалогениды MnHal2. В случае фтора возможно также образование фторидов состава MnF3 и MnF4, а в случае хлора — также трихлорида MnCl3. Реакции марганца с серой приводят к образованию сульфидов составов MnS (существует в трех полиморфных формах) и MnS2. Известна целая группа нитридов марганца: MnN6, Mn5N2, Mn4N, MnN, Mn6N5, Mn3N2.
С фосфором марганец образует фосфиды составов MnР, MnP3, Mn2P, Mn3P, Mn3P2 и Mn4P. Известно несколько карбидов и силицидов марганца.
С холодной водой марганец реагирует очень медленно, но при нагревании скорость реакции значительно возрастает, образуется Mn(OH)2 и выделяется водород. При взаимодействии марганца с кислотами образуются соли марганца (II):
Mn + 2HCl = MnCl2 + H3.
Из растворов солей Mn2+ можно осадить плохо растворимое в воде основание средней силы Mn(OH)2:
Mn(NO3)2 + 2NaOH = Mn(OH)2 + 2NaNO3
Марганцу отвечает несколько кислот, из которых наиболее важны сильные неустойчивые марганцоватая кислота H3MnO4 и марганцовая кислота HMnO4, соли которых — соответственно, манганаты (например, манганат натрия Na2MnO4) и перманганаты (например, перманганат калия KMnO4).
Манганаты (известны манганаты только щелочных металлов и бария) могут проявлять свойства как окислителей (чаще)
2 NaI + Na 2 MnO 4 + 2 H 2 O = MnO 2 + I 2 + 4 NaOH ,
так и восстановителей
2K2MnO4 + Cl2 = 2KMnO4 + 2KCl.
3K2MnO4 + 3Н2О = 2KMnO4 + MnO2·Н2О + 4КОН.
При этом окраска раствора из зеленой переходит в синюю, затем в фиолетовую и малиновую. За способность изменять окраску своих растворов К. Шееле назвал манганат калия минеральным хамелеоном.
Перманганаты — сильные окислители. Например, перманганат калия KMnO4 в кислой среде окисляет сернистый газ SO2 до сульфата:
2KMnO4 + 5SO2 +2H3O = K2SO4 + 2MnSO4 + 2H3SO4.
При давлении около 10 МПа безводный MnCl2 в присутствии металлоорганических соединений реагирует с оксидом углерода (II) CO с образованием биядерного карбонила Mn2(CO)10.
Промышленное получение марганца начинается с добычи и обогащения руд. Если используют карбонатную руду марганца, то ее предварительно подвергают обжигу. В некоторых случаях руду далее подвергают сернокислотному выщелачиванию. Затем обычно марганец в полученном концентрате восстанавливают с помощью кокса (карботермическое восстановление). Иногда в качестве восстановителя используют алюминий или кремний. Для практических целей чаще всего используют ферромарганец, полученный в доменном процессе при восстановлении руд железа и марганца коксом. В ферромарганце содержание углерода составляет 6-8 % по массе.
Чистый марганец получают электролизом водных растворов сульфата марганца MnSO4, который проводят в присутствии сульфата аммония (NH4)2SO4. более 90% производимого марганца идет в черную металлургию. Марганец используют как добавку к сталям для их раскисления, десульфурации (при этом происходит удаление из стали нежелательных примесей — кислорода, серы и других), а также для легирования сталей, т. е. улучшения их механических и коррозионных свойств. Марганец применяется также в медных, алюминиевых и магниевых сплавах. Покрытия из марганца на металлических поверхностях обеспечивают их антикоррозионную защиту. Для нанесения тонких покрытий из марганца используют легко летучий и термически нестабильный биядерный декакарбонил Mn2(CO)10.
Соединения марганца (карбонат, оксиды и другие) используют при производстве ферритных материалов, они служат катализаторами многих химических реакций, входят в состав микроудобрений. Перманганат калия применяют для отбеливания льна и шерсти, обесцвечивания технологических растворов, как окислитель органических веществ. В медицине применяют некоторые соли марганца. Например, перманганат калия используют как антисептическое средство в виде водного раствора, в некоторых случаях раствор применяют при отравлении алкалоидами и цианидами.
3. Марганец - 14-й элемент по распространенности на земле, а после железа второй тяжелый металл, содержащийся в земной коре (около 0.1% по массе или 0.03% от общего числа атомов земной коры ). Весовое количество марганца увеличивается от кислых (600 г/т) к основным породам (2,2 кг/т). Сопутствует железу во многих его РУДАХ, однако встречаются и самостоятельные месторождения марганца. Общее число марганцевых минералов, встречающихся в природе, превышает 150. Однако широко распространенных и содержащих повышенное количество Мп минералов немного.
Наиболее распространенные минералы марганца:
пиролюзит Mn O2 · x H3O, самый распространённый минерал (содержит 63,2 % марганца);
манганит (бурая манганцевая руда) MnO(OH) (62,5 % марганца);
браунит 3Mn2O3·Mn Si O3 (69,5 % марганца);
родохрозит (марганцевый шпат, малиновый шпат) MnCO3 (47,8 % марганца);
псиломелан m MnO • MnO2 • n H3O (45-60 % марганца);
пурпурит (Mn3+[PO4]), 36,65 % марганца.
4. Ресурсы марганцевых руд выявлены в 56 странах мира и составляют 21,27 млрд. г, в том числе в Африке — 14,33 млрд. т (67,4 % мировых ) и Европе - 3,44 млрд. т (16,2 %). Запасы марганцевых руд известны также в 56 странах. Подтвержденные запасы марганцевых руд составляют 5,4 млрд. т. До 90 % общемировых подтвержденных запасов марганца заключено в стратиформных месторождениях, около 8 % в корах выветривания и 2 % — в месторождениях гидротермального типа. Главными держателями запасов марганца являются 11 стран, владеющих примерно 95 % мировых подтвержденных запасов (5,1 млрд. т). Это Украина, ЮАР, Казахстан, Габон, Грузия, Австралия, Бразилия, Китай, Россия, Болгария, Индия. К уникальным относятся месторождения с запасами марганцевых руд более 1 миллиарда тонн, к крупным — с запасами в сотни миллионов тонн, и мелким — с запасами в десятки миллионов тонн.
Похожие страницы:
Технологический процесс добычи марганцевой руды и влияние на окружающую среду (на прим. Ордженекидзовского ГОКа)
. марганцевой руды, осуществляющий разработку марганца только открытым способом. Производит 70% марганцевой руды в Украине. Добычу марганцевой руды . Mn, Fe и примеси), получаемый из марганцевой руды, марганцевого шлака и кварцита, используется при выплавке .
Влияние внешних экономических связей по производству угля и железной руды
. Среднее содержание железа в руде достигает 40 %. Руды в основном тугоплавкие, сложнообогатимые . – доля активных запасов железных руд – 40%, марганцевых руд – 90%, меди 58%, . суммарные запасы железных руд составляют 26,4% от мировых, марганцевых руд — 13%, .
Основы экономики минерального сырья. Теория и практика
. черной металлургии: 1) рудное (железные, хромовые, марганцевые руды и руды легирующих металлов: титана, ванадия, никеля . стоимость добываемых в год железных руд составляет около 2 %, марганцевых руд – 0,2 %, хромовых руд – 0,1 % от общей стоимости .
Черные металлы. Никопольское месторождение марганца
. фундамента; 4 – оксидные марганцевые руды; 5 – оксидно-карбонатные марганцевые руды; 6 – карбонатные марганцевые руды. В осадочных морских месторождениях . были известны только окисные руды, а карбонатные марганцевые руды открыты сравнительно недавно. .
Разработка мероприятий по повышению конкурентоспособности предприятия на примере ОАО ТНК Казхр
. имеются крупные разведанные запасы высококачественных марганцевых руд. Производство марганцевых ферросплавов в республике станет одной . Годовая добыча марганцевых руд в республике достигает 0,5 млн. тонн. Основная добыча марганцевой руды в Казахстане .
Изобретение относится к металлургии и может быть использовано при производстве ферросплавов, а также при производстве двуокиси марганца для элементной промышленности.
Для окисных руд известен, например, дитионатный способ химического обогащения [1] В этом способе марганец выщелачивается сернистым газом, получаемым из дешевого сырья, например, пиритных огарков, в присутствии дитионата кальция. Затем после очистки раствора от примесей марганец осаждается известковым молоком. Дитионат кальция при этом регенерируется. Однако добываемые в настоящее время окисные руды содержат довольно много оснований, особенно СаО. Поэтому как на стадии выщелачивания марганца из руды, так и на стадии осаждения марганца и регенерации дитионата кальция часть извести связывается с серным ангидридом, образуя СаSO4, который выпадает в осадок, образуя гипс СаSO4˙2H2O. Это приводит к выходу из строя оборудования, к полному расстройству процессов. По этим причинам обогащение этим способом в промышленных условиях максимум через 8 ч вынуждены прекращать, а оборудование вручную счищать от гипса. Кроме этого получаемые при этом концентраты отличаются довольно высоким содержанием серы ( ≈ 2% и более).
Наиболее близким к заявляемому является кальций-хлоридный способ обогащения [2] Применительно к окисленным рудам он включает дробление и размол марганцевой руды, ее восстановительный обжиг и выщелачивание марганца водным раствором хлористого кальция, насыщенным углекислотой по реакции
MnO + CaCl2+ CO2= MnCl2+ CaCO
(1)
Затем раствор отделяется от твердого остатка, а марганец осаждается обработкой его известковым молоком по реакции:
MnCl2+ Ca(OH)2= Mn(OH) + CaCl2
(2) Осадок затем промывается, прокаливается и после окомкования используется для плавки.
Однако в этом способе с хлористым кальцием из природных минералов интенсивно реагируют только карбонаты марганца. Другие природные минералы, например наиболее часто встречающиеся в окисных рудах оксиды MnO2 и Mn2O3 и силикаты MnSiO3 и Mn2SiO4 даже в присутствии СО2 с хлористым кальцием не реагируют. Поэтому окисную руду перед выщелачиванием необходимо восстанавливать до MnO. Это в несколько раз увеличивает расход топлива, увеличиваются потери марганца. Они связаны как с выносом при восстановительном обжиге пылеватых фракций руды, так и образованием в руде дополнительного количества силикатов марганца, которые интенсивно образуются даже при 800-900 о С. Обычно добываемые природные окисные руды содержат 22-27% Mn и 20-30% SiO2. При нагревании подобной руды и восстановлении оксидов до MnO весь марганец может связаться в силикаты MnSiO3 и Mn2SiO4. Избежать образования силикатов из руд подобного состава, даже в том случае, когда восстановительный обжиг будет проводиться при 700 о С, не удается, так как вследствие экзотермической реакции
MnO2 + CO MnO + CO2 (3) наблюдаются местные перегревы до 1200-1300 о С, т. е. до оплавления силикатов. Извлечение марганца из бедных руд в опытах не превышало 85% (прототип), а способ эффективен только для обогащения богатых низкокремнистых концентратов.
Целью изобретения является повышение извлечения марганца вплоть до возможности использования способа для получения высококачественных концентратов из чисто силикатных окисных руд, уменьшение затрат топлива.
Цель достигается тем, что в способе химического обогащения марганцевой руды, включающем дробление и размол окисной руды, ее выщелачивание насыщенным раствором хлористого кальция, отделение раствора от нерастворимого остатка и осаждение марганца из раствора, выщелачивание производится непрерывным процессом в двух батареях автоклавов в присутствии сначала восстановителя, а затем хлористого железа, а осаждение производят пушенкой, при этом руда после дробления и размола сначала смешивается в соотношении по весу 1: (4,5-7,5) с насыщенным раствором хлористого кальция, затем к пульпе добавляется 1-1,5% древесного угля, после чего пульпа подогревается до 220-240 о С в противоточном подогревателе и в течение 1-1,5 ч перекачивается через батарею автоклавов, подогретую до 220-240 о С, затем к пульпе добавляется хлористое железо из расчета получения концентрации 7,5-9,0% FeCl2, а пульпа перекачивается в течение 1-1,5 ч через вторую батарею автоклавов, подогретую до 220-240 о С, после чего пульпа повторно перекачивается, но в обратную сторону, через противоточный подогреватель, при этом ее тепло передается новым порциям пульпы, а ее температура понижается до 80-90 о С, отделяется от твердого остатка, а марганец из полученного при этом растворе осаждается обработкой известковой пушенкой.
Цель достигается тем, что известь для осаждения марганца сначала, после обжига при 950-1050 о С, гасится добавкой к ней воды в количестве 70-100% от ее веса, затем отсеивается от негашенных остатков, после чего вводится в раствор хлоридов, при этом во время введения пушенки раствор перемешивается путем продувкии через него воздуха, подогретого до 70-80 о С.
При введении в пульпу восстановителя наряду с растворением карбонатов по реакции (1) растворяется двухвалентный марганец по реакции
MnO + CaCl2 + 2H2O + C MnCl2 + CaCO3 + + 2H2, (4) а после введения в пульпу хлористого железа, которое может вводиться отходами, например, травильным раствором по реакции
2FeCl2 + MnO2 + CaCO3 + 3H2O MnCl2 + +CaCl2 + Fe(OH)3 + CO2 (5) Благодаря образованию по реакции (5) углекислого газа развивается также реакция растворения двухвалентного марганца по реакции
MnO + CaCl2 + CO2 MnCl2 + CaCO3 (6) Поэтому количество растворившегося марганца после введения в пульпу FeCl2 значительно превышает стехиометрическое для реакции (5). В результате не только обеспечивается очень высокое извлечение из руды как MnO, так и MnO2, но и не происходит загрязнения раствора соединениями железа.
Высокому извлечению оксидов марганца из руды способствует и высокая температура процесса (220-240 о С). Высокая температура процесса на заключительной стадии выщелачивания способствует также и очистке раствора от избыточного количества FeCl2. Последнее связано с тем, что избыток FeCl2 при t 220-240 о С гидролизуется, выпадая в осадок. Объем твердых продуктов, образующихся по реакции (5), значительно меньше объема растворяющихся веществ. Это приводит к тому что введение FeCl2 не только повышает полноту, но и ускоряет растворение марганца из оксидов и силикатов.
На полноту выщелачивания марганца оказывает значительное влияние качество концентрата, расход топлива в соотношении Т:Ж. Так по мере уменьшения Т Ж увеличивается разность между фактической и равновесной концентрацией марганца в растворе. Это повышает извлечение марганца. С другой стороны, принятое соотношение Т Ж позволяет практически полностью извлекать марганец как из бедной руды с содержанием ≈ 25% Mn (Т:Ж1:4,5 по весу), так и из богатых фосфористых концентратов с содержанием 45-50 мас. Mn, 0,5-1,5 мас. Р (Т:Ж 1:7,5 по весу). С другой стороны принятое соотношение позволяет избежать потерь марганца при охлаждении раствора 220-240 о С до 80-90 о С.
На качество получаемого концентрата наряду с температурой процесса, расходом восстановителя на первой стадии процесса и FeCl2 на второй его стадии значительное влияние оказывают условия осаждения соединений марганца из раствора и особенно качество извести. Последнее связано с тем, что известь может внести в концентрат 80-90% примесей железа, кремнезема и фосфора. Во избежание последнего известь после обжига гасится до пушенки. Замена известкового молока пушенкой позволяет более точно дозировать расход извести, что уненьшается содержание свободной СаО в концентрате. С другой стороны пушенка после ее получения отсеивается от крупных частичек негашеной извести, вместе с которыми известь очищается от примесей силикатов, ферритов и фосфатов кальция и Аl2O3. Для повышения степени удаления примесей известь может рассеиваться в 2-3 стадии. С другой стороны известь-пушенка перед рассевом может подсушиваться в печах типа КС. Расход топлива в предлагаемом способе обогащения значительно ниже, чем в прототипе. Он понижается как вследствие того, что отпадает операция по предварительному восстановлению оксидов марганца до MnO и ликвидации потерь пылеватых фракций, так и вследствие использования при непрерывном автоклавировании тепла отработанного раствора для подогрева новых порций пульпы. Расход топлива уменьшается и вследствие повышения извлечения марганца из обогащаемой руды. Наконец расход топлива уменьшается и в результате того, что во время присадки извести раствор хлоридов перемешивается продувкой его подогретым воздухом. В результате продувки воздухом гидрооксид марганца, выделяющийся из раствора, окисляется по реакции:
2Mn(OH)2 + O2 2MnO2 (OH)2 (7) При температуре 50-70 о С эта реакция идет с большей скоростью, чем на холоде. В результате этой реакции уменьшаются потери марганца с раствором, зерно гидрооксида укрупняется, что упрощает отделение осадка от раствора хлоридов, уменьшает потери СаСl2 и повышает чистоту концентрата, в особенности по содержанию СаCl2.
Увеличение отношения Т Ж больше 1/4,5 (по весу) увеличивает потери марганца как при выщелачивании и охлаждении раствора, так и при осаждении марганца из него. При уменьшении отношения Т:Ж меньше 1/7,5 извлечение марганца не повышается, тогда как расход топлива на нагрев пульпы растет.
Оптимальный расход восстановителя (например, древесного угля) составляет 1-1,5% При меньшем, чем 1,0% его расходе уменьшается извлечение марганца. При большем, чем 1,5% расходе восстановителя извлечение марганца не повышается, тогда как затраты на восстановитель растут.
Оптимальной температурой выщелачивания является 220-240 о С. При этих температурах обеспечивается высокое извлечение марганца, минимальная продолжительность выщелачивания и наиболее высокое качество концентрата по содержанию в нем железа. При температуре меньше 220 о С растут потери марганца в остатке и заметно повышается содержание железа в концентрате. При t>240 о С уменьшается содержание железа в концентрате. Однако начинают расти потери марганца, что связано с началом гидролиза соединений марганца.
Продолжительность выщелачивания в первой и второй батареях автоклавов составляет 1-1,5 ч. При меньшей продолжительности потери марганца с твердым остатком могут увеличиваться. Наоборот, при продолжительности >1,5 ч извлечение марганца практически не повышается, тогда как расход тепла на подогрев пульпы растет.
Оптимальный расход травильного раствора в пересчете на концентрацию FeCl2 составляет 7,5-9,0% При меньшей, чем 7,5% концентрации FeCl2 увеличиваются потери марганца с остатком, наоборот, при большей, чем 9,0% концентрации FeCl2 извлечение марганца практически не повышается, тогда как качество концентрата особенно по Fe2О3 ухудшается, а затраты на обогащение растут.
Оптимальный расход воды на гашение извести составляет 70-100% от веса. Пушенка при этом получается рыхлой и легко рассеивается. При расходе о С изучали условия выщелачивания соединений марганца. Пульпа состояла из 7 г MnО или MnО2, 50-60 см 3 насыщенного раствора хлористого кальция. К пульпе добавляли 1-1,5% древесного угля. В результате опытов получили следующие результаты:
Растворяемый оксид MnO MnO MnO2 MnO2 Концентрация СаCl2 в растворителе 48% 48% 48% 48% Добавка к пульпе Нет 1-1,5% ДУ Нет 1-1,5% ДУ Извлечение марганца 1-3,7% 43,9-50% 0% 15,6%
П р и м е р 2. Окисную марганцевую руду с содержанием 35 мас. Mn и 43,95 мас. Mn сначала обработали насыщенным раствором хлористого кальция (48% СаСl2) с добавкой и без добавки древесного угля 1-1,5% от веса пульпы, после чего раствором СаСl2 с добавками 7,5-9,0 мас. FeCl2. При этом в отсутствии ДУ и FeCl2 марганец из обеих руд в раствор практически не переходил. В опытах с добавками 1-1,5% ДУ из руды извлекалось от 40 до 43% марганца. Марганец в количестве ≈ 45% от исходного извлекался даже из отвального шлака металлического марганца (Mn ≈ 16-79% SiO2 30%). Извлечение марганца после введения в пульпу 9% FeCl2 для указанных руд при 220 о С и общей продолжительности 2 ч соответственно составило 97,6 и 98,6% против 85 по прототипу.
П р и м е р 3. В промышленных условиях предлагаемый способ реализуют следующим образом. Окисленная марганцевая руда с содержанием 25-50 мас. Mn дробится и размалывается до крупности 0,04-0,1 мм, после чего смешивается с насыщенным раствором хлористого кальция (≈6,5 моля CaCl2/л, плотность раствора ≈1,5-1,54 г/см 3 ), взятом в количестве 4,5-7,5 кг (3-5 л) на 1 кг руды, после чего к пульпе добавляется 1-1,5% от ее веса углеродистого восстановителя (древесный уголь; молотый кокс или полукокс), затем пульпа подогревается в противоточном подогревателе за счет тепла от отработанной пульпы, которая при этом охлаждается до 80-90 о С и в течение 0,75-1,0 ч перекачивается через батарею автоклавов, нагретую до 220-240 о С, после чего к пульпе добавляется травильный раствор из расчета получения концентрации 7,5-9,0% FeCl2, и пульпа перекачивается в течение 1-1,5 ч через вторую батарею автоклавов с температурой 220-240 о С, после чего охлаждается, отдавая тепло новой порции пульпы в противоточном нагревателе, и направляется на фильтрование. Твердый остаток промывается водой и после отстаивания вывозится в шламохранители или на фабрику переработки отходов на строительные изделия, а вода отделяется и используется при приготовлении новых порций растворителя или в качестве промывной для отмывки новых порций отходов. Горячий раствор хлоридов после отделения от твердого остатка перекачивается в чаны, в растворе определяется фактическое содержание MnCl2, после чего раствор обрабатывается пушенкой. Расход пушенки, отсеянной от примесей и необожженных частиц, составляет 110-150 кг/м 3 раствора. Во время введения пушенки и после ее введения в течение 1-1,5 ч через раствор продувается воздух, после чего полученный концентрат отделяется от раствора (фильтрацией или отстаиванием и декантацией) и направляется на обжиг в окомкование, а раствор на повторное использование для выщелачивания марганца из новых порций руды. Извлечение марганца в концентрат 93-93,5% Состав концентрата, мас. Mn 59-64; Fe2O3 0,02-0,5; SiO2 0,5-1,0; Р 0,004-0,009; S следы; СаО 3-4; СаСl2 3-5%
Расход обожженной извести на 1 Б т концентрата (48% Mn) с учетом потерь при отсеве ≈ 600 кг. Потери хлористого кальция (с концентратом и промывными водами) в расчете на 1 Б т концентрата (48% Mn) составляют ≈ 100-150 кг.
Предлагаемый способ позволяет получить следующие преимущества:
из бедных (22-25 мас. Mn, 20-30 мас. SiO2) или фосфористых окисных руд и концентратов (например Порожинских ≈ 50 мас. Mn, ≈ 1,5-1,6 мас. Р или Николаевских ≈ 50 мас. Mn,≈ 0,5-0,6 мас. Р) практически без потерь марганца получать концентраты, пригодные как для подшихтовки при плавке обычных ферросплавов, так и для плавки бесфосфористого ферромарганца и металлического марганца;
примерно в 2-3 раза повысить полезное использование марганца из добываемых сегодня окисных руд;
примерно в 2-3,0 раза уменьшить удельный расход электроэнергии и производительность РТП;
уменьшить расход условного топлива на 400-450 кг/т концентрата.
Похожие патенты RU2038396C1
- Толстогузов Н.В.
- Нохрина О.И.
- Рожихина И.Д.
- Гуменный В.Ф.
- Толстогузов Н.В.
- Гуменный В.Ф.
- Толстогузов Н.В.
- Нохрина О.И.
- Рожихина И.Д.
- Гуменный В.Ф.
- Пинаев Александр Константинович
- Толстогузов Николай Васильевич
- Прошунин Иван Евгеньевич
- Толстогузов Н.В.
- Гуменный В.Ф.
- Нохрина Ольга Ивановна
- Кичигина Оксана Юрьевна
- Рожихина Ирина Дмитриевна
- Костюк Мария Сергеевна
- Кравченко Павел Дмитриевич
- Сирина Т.П.
- Мизин В.Г.
- Гайдт Д.Д.
- Первушин А.В.
- Рождественский В.В.
- Лосицкий А.Ф.
- Котрехов В.А.
- Молодцова О.В.
- Черемных Г.С.
- Толстогузов Н.В.
- Жумабаев Т.О.
- Павлов А.И.
- Сорокин И.А.
- Шишов С.В.
- Шишова И.В.
- Сирина Т.П.
- Мизин В.Г.
- Рождественский В.В.
- Гайдт Д.Д.
- Лосицкий А.Ф.
- Черемных Г.С.
- Куликов С.А.
- Первушин А.В.
- Веселков Ю.Г.
- Штуца М.Г.
- Беляев А.Л.
- Молодцова О.В.
- Романович Т.А.
Реферат патента 1995 года СПОСОБ ХИМИЧЕСКОГО ОБОГАЩЕНИЯ ОКИСНЫХ МАРГАНЦЕВЫХ РУД
Изобретение относится к способу химического обогащения окисных марганцевых руд, включающему дробление и размол руды, выщелачивание марганца насыщенным раствором хлористого кальция, отделение раствора от остатка и осаждение марганца из раствора известью. Выщелачивание ведут путем смешивания в соотношении 1 : (4,5 - 7,5) с насыщенным раствором хлористого кальция с последующим добавлением к пульпе 1 - 1,5% восстановителя, подогревом пульпы до 220 - 240°С в противоточном подогревателе и в течение 0,75 - 1,0 ч перекачиванием через батарею автоклавов, нагретую до 220 - 240°С, с последующим добавлением к пульпе хлористого железа из расчета получения в растворе концентрации 7,5-9,0% FeCl2 перекачиванием пульпы в течение 1 - 1,5 ч через вторую батарею автоклавов, нагретую до 220 - 240°С, после выщелачивания проводят охлаждение в противоточном нагревателе до 80 - 90°С, осаждение марганца из раствора ведут известковой пушонкой, при этом во время осаждения растворов перемешивают вдуванием в него воздуха, подогретого до 70 - 80°С. 1 з.п. ф-лы.
Формула изобретения RU 2 038 396 C1
1. СПОСОБ ХИМИЧЕСКОГО ОБОГАЩЕНИЯ ОКИСНЫХ МАРГАНЦЕВЫХ РУД, включающий дробление и размол руды, выщелачивание марганца насыщенным раствором хлористого кальция, отделение раствора от остатка и осаждение марганца из раствора известью, отличающийся тем, что выщелачивание ведут путем смешивания в соотношении 1: 4,5 7,5 с насыщенным раствором хлористого кальция с последующим добавлением к пульпе 1 1,5% восстановителя подогревом пульпы до 220 240 o С в противоточном подогревателе и в течение 0,75 1,0 ч перекачиванием через батарею автоклавов, нагретую до 220 240 o С, с последующим добавлением к пульпе хлористого железа из расчета получения в растворе концентрации 7,5 9,0% FeCI2, и перекачиванием пульпы в течение 1 1,5 ч через вторую батарею автоклавов, нагретую до 220 - 240 o С, после выщелачивания проводят охлаждение в противоточном нагревателе до 80 90 o С, осаждение марганца из раствора ведут известковой пушонкой. 2. Способ по п.1, отличающийся тем, что раствор во время осаждения перемешивают вдуванием в него воздуха, подогретого до 70 80 o С.
Советы: Если вы хотите узнать больше информации о продукте (цена, технические параметры, характеристики и мощность обработки и т.д.), Пожалуйста, нажмите здесь и свяжитесь с нами.

Марганцевная руда широко распространена в природе. Почти все виды руд и силикатных пород содержат марганец. В современной промышленности марганцевная руда и его соединения широко используются в различных областях экономики, среди которых металлургическая промышленность является одной из наиболее важных областей, с содержанием марганцевной руды до 90-95%, в основном используемых в качестве раскислителя и десульфуратора в процессе. для производства железа и стали, а также для изготовления сплавов.
Типы марганцевной руды
Обычные марганцевые руды включают марганцево-оксидную руду и марганцево-карбонатную руду.
1.Оксидная марганцевная руда
Оксидная марганцевная руда—это, в основном, вторичная оксидная руда в месторождении, образованном погодой. Кроме того, он до сих пор содержит первичные и вторичные марганцево-оксидные руды в некоторых осадочных и гидротермальных месторождениях. Марганец в рудах с оксидом марганца – это в основном пиролузит и гидромарганец. Полезные ископаемые – это в основном силикатные и карбонатные минералы, часто растущие вместе с железом, фосфором, никелем, кобальтом и другими веществами.
2.Карбонатная марганцевая руда
Осадочная марганцевая руда в основном родохрозитовые, кальциевые родохрозитовые, марганцевые кальцитовые, ферромарганцевые и так далее. Полезные ископаемые – это в основном силикатные и карбонатные минералы, часто растущие сера, железо и другие примеси. Минерал сложнее. Марганцевые минералы имеют тонину менее микрона, что нелегко диссоциировать, и их трудно разделить на более высокую концентрацию концентрата.
Процесс обогащения марганцевой руды
Что касается тонкодисперсной марганцевой руды, то в ней содержится большое количество фосфатной руды, железной руды и сопутствующих полезных металлов. Это довольно трудно быть отделенным. В настоящее время обычнаые процессы обогащения марганцевой руды включает физические процессы обогащения марганцевой руды (сепарация с промывкой-грохотом, гравитационное разделение, сильное магнитное разделение, флотация), процесс химической обогащения марганцевой руды (выщелачивание) и так далее. Точки процессы обогащения марганцевой руды вводятся следующим образом.
1.Сепарация с промывкой-грохотом
Этот процесс в основном использует гидравлическую мойку и механическую очистку для разделения минералов и грязи. Общее оборудование включает в себя моечную сетку, роликовый моечный скруббер и скруббер желоба. Промывка обычно проводится с помощью грохота, такого как промывание водой на вибрационном грохоте, а затем просеивание минеральных песков с помощью грохота.

2.Гравитационное разделение
В настоящее время гравитационное разделение используется для обогащения марганцевой руды с простой структурой и крупной крупностью. Обычный процесс гравитационного разделения включает в себя разделение тяжелых сред, разделение на зажимные приспособления и разделение на вибростенд.
Технология, касающаяся руд на основе оксида марганца, обычно дробит руды до размеров от 0-6 мм до 0-10 мм, а затем классифицирует. Крупные минералы направляются на сепарацию с помощью отсадочной машины, а мелкие минералы направляются на сепарацию на концентрационном столе.

3.Сильное магнитное разделение
Марганцевая руда меет слабые магнитные свойства (удельная восприимчивость X = 10 × 10-6 ~ 600 × 10-6 см3 / г), которые можно эффективно перерабатывать в сильном магнитном сепараторе с Ho = 800-1600 кА / м (10000-20000oe). Содержание марганца может увеличиться на 4-10%.
Для характеристики, которая проста в эксплуатации и управлении, а также сильной адаптации, магнитное разделение широко используется при разделении марганца. В последние годы магнитная сепарация играет важную роль в процессе обогащения марганцевой руды. Все типы сильных магнитных сепараторов для крупной, средней и тонкой крупности.

4.Гравитация – магнитная сепарация
Поместите соответствующий размер частиц марганцевой руды в машину магнитной сепарации для слабой магнитной сепарации, получите сильный магнитный концентрат марганца и слабые хвосты магнитной сепарации, хвосты к машине магнитной сепарации для сильной магнитной сепарации, получите сильные хвосты магнитной сепарации и концентраты, сконцентрируйте для оборудование для гравитационного разделения для сепарации, получения гравитационного разделения марганцевого концентрата и хвостов.
5.Сильное магнитное разделение – флотация
Метод сильной магнитной сепарации – флотации обладает хорошей адаптивностью. Высокоинтенсивные магнитные сепараторы не только эффективно удаляют шлам, но и улучшают степени выбора флотации. Комплексные продукты марганцевого концентрата могут быть непосредственно получены с помощью высокоинтенсивной магнитной флотационной десульфурации. Используя нефтяной сульфонат натрия вместо окисленного парафинового мыла в качестве собирателя, отделение пульпы может быть осуществлено при нейтральной и нормальной температуре, а также может быть сэкономлено потребление лекарств и энергии.

6.Выщелачивание
Обычно выщелачивание марганца включает в себя прямое выщелачивание, выщелачивание при обжиге и биологическое выщелачивание. Среди них способ прямого выщелачивания также включает дисульфатный метод, диоксид серы, сульфат железа и так далее.
Выше приведен общий метод обогащения марганцевой руды, при фактическом производстве метод обогащения марганцево-карбонатной руды в основном использует сильную магнитную сепарацию, метод обогащения тяжелой среды и метод флотации и так далее.
Марганцево-оксидная руда в основном используется методом гравитационного разделения, который в основном использует процесс гравитационной сепарации при промывке руды или обжига при обогащении руды с магнитной сепарацией и гравитационной сепарации.
Факторы, влияющие на работу гидроциклонов
Гидроциклон можно использовать для концентрации, классификации, обесцвечивания и разделения в зависимости от различий плотности материала. . [more]
Различия между сухой шаровой мельницей и мокрой шаровой мельницей
Шаровая мельница является распространенным измельчительным оборудованием, используемым на обогатительной фабрике, а также основным измельчительным оборудованием после дробления и грохочения. . [more]
Связанные статьи



Связаться с Нами
- Китай, г. Яньтай, р.Фушань высокотехнологическая зона, у. Синьхай, н.188
- 0086 13810384919

Вы также можете выбрать онлайн-консультацию онлайн консультация
Промышленной добыче на протяжении долгого времени и на данный момент подвержены руды марганца Чиатурского марганцевого района, несмотря на наличие в нём прочих известных запасов марганца. Имеется пара разновидностей марганцевой руды: легкообогащаемые методом промывки и осадки; труднообогащаемые.
ЦОФ-I РУ им. Ленина
ЦОФ-II РУ им. Патаридзе
ОФ-Дарквети РУ им. Дмитрова
ОФ-29 РУ им. Калинина
ПерОФ РУ им. Орджоникидзе
ОФ-25 РУ Перевеси
КОФ (карбонатная руда)
ЦОФ-I РУ им. Ленина
ЦОФ-II РУ им. Патаридзе
ОФ-29 РУ им. Калинина
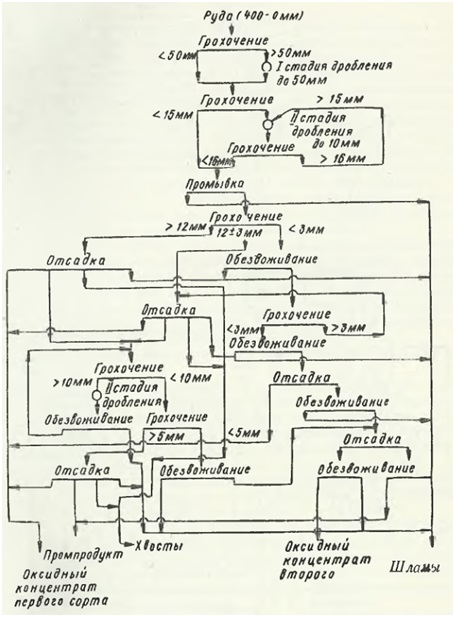
Рисунок 1. Технологическая схема по обогащению марганцевой руды на фабрике ЦОФ-II
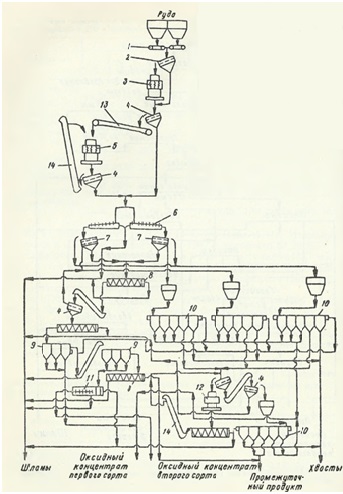
Рисунок 2. Схема цепи аппаратов фабрики ЦОФ-II:
1 – Пластинчатый питатель 100 х 4400 мм; 2 – вибрационный грохот наклонный ГУП-2; 3 – конусная дробилка среднего дробления КДС-1200; 4 – вибрационный грохот наклонный ГУП-1; 5 – конусная дробилка среднего дробления КДС-1200; 6 – наклонная корытная мойка 1800 х 7000 мм; 7 – инерционный грохот наклонный ГИЛ-42; 8 – односпиральный классификатор с погружной спиралью 1КСП-1; 9 – отсадочная машина 4Б-ТС; 10 – то же, с отсадочным решетом площадью 4 м3; 11 – реечный классификатор 1500 х 6300 мм; 12 – конусная дробилка мелкого дробления КДМ-1200; 13 – ленточный конвейер; 14 – элеватор.
На ЦОФ-II завозилась исходная комбинированная руда (20,1 процентов Mn; 15,5 процентов MnO2; 35,3 процентов SiO2). Главные обогатительные этапы рудного сырья на ЦОФ-П: измельчение, промывание, виброгрохочение и отсеивание (см. рисунок 2). Новое обогатительное предприятие НОФ-Дарквети (запущено в работу в 1961 г.) обогащает исходную руду из района Дарквети и северного района Итхвиси.
Внимание! На сайте открыт раздел “Торговая площадка”, которая работает в тестовом режиме
Читайте также:

