Современные остеопластические материалы используемые при зубосохраняющих операциях реферат
Обновлено: 02.07.2024
Это актуальное решение для всех, кто связан с хирургической стоматологией.
Стоматологи давно на практике знакомы с использованием костного материала. Он помогает с проведением операций по остеопластике. Это значит, восстанавливают альвеолярный гребень, если его объём утрачен. Потом разрушение костной ткани замедляется, предотвращается целый ряд негативных последствий, возникающих на фоне изменений во внешнем виде ухудшения здоровья. Процедура становится актуальной, если человеку не хватает костной ткани, а в ближайшее время ставят имплантаты. Материалы, позволяющие провести такие операции, обладают собственной спецификой.
Об основных характеристиках, имеющих значение для стоматологии
Высокое качество – главное требование, которое в стоматологии предъявляют к остеопластическим материалам. Для этой продукции значение имеют и другие параметры:
- Дефект костной ткани полностью заполняют, что позволяет избавиться от проблем.
- Ткани, в которые ставят имплантат, полностью совместимы с такими материалами.
- Пористость, что способствует эффективному прорастанию новой ткани.
- Эффективность при любых обстоятельствах.
- Безопасность, которой отличается искусственная костная ткань. Запрещено применять составы, способные причинить вред человеку.
Остеопластические материалы представлены на современном рынке в большом количестве. Надо учесть все нюансы, описанные выше, чтобы сделать правильный выбор. Надо выбрать состав, который допускает применение сразу после покупки. Высокая адгезия обеспечит плотное прилегание к кости, насколько это возможно.
На чём основана классификация?
По сути, любой из остеопластических материалов – разновидность имплантата, способствующего прорастанию кости. Активность, которую они обеспечивают, бывает остеогенной, остеоиндуктивной, остеокондуктивной.

Выделяют четыре группы материалов, в зависимости от происхождения:
- Синтетические, с кальциевыми солями.
- Ксеногенные, донором для которых выступили животные.
- Аллогенные – предполагают выбор других людей в качестве доноров.
- Аутогенные. Донор – сам пациент.
Каждая группа отличается своими особенностями, заслуживающими отдельного рассмотрения.
Аутогенная группа
Разновидность костнозамещающих материалов, которая встречается на практике чаще остальных. Для получения применяют внеротовые или внутриротовые донорские участки. Потом материалы пересаживают в принимающий участок. Были проведены многочисленные клинические исследований, после которых выяснили, что послеоперационные и другие дефекты заполняются максимально быстро, если пользоваться данной разновидностью материала. Новообразованная ткань не приводит к появлению конфликтов.
Иммунная несовместимость отсутствует. Сам материал пластичный. Отличается небольшими финансовыми затратами во время забора.
Происхождение такой ткани тоже бывает двух видов – эктомезенхимальное или мембранное, либо эндоходральное или хрящевое. Без недостатков тоже не обходится:
- Оперативное вмешательство отнимает достаточно много времени.
- Получение аутоматериала связано с некоторой травматичностью.
- Есть вероятность инфицирования.
Аутокость часто заменяют ксено- или аллокостями. Тогда вероятность усадки материала сводится к нулю.
Об аллогенных разновидностях
Для синус лифтинга. Его пока не применяют на территории России из-за требований законодательства. Аллогенные материалы – ещё одна разновидность костных имплантатов. Их получают из мёртвых человеческих тел, одновременно подвергая специальной обработке. Примеры – из деминерализованной лиофилизированной кости, либо губчатые и кортикальные части подвздошных костей.

По сравнению с аутоматериалами эта группа обладает следующими преимуществами:
- Гарантия быстрого ангиогенеза за счёт микро- и макропористой структуры.
- Оперативное вмешательство не требует много времени.
- По отношению к реципиентному ложу адгезия очень хорошая.
- Получение материала не связано с высокой травмоопасностью.
- Остеоиндуктивный потенциал, выраженный достаточно ярко.
Недостатком считаются не только проблемы этического характера. Есть вероятность переноса различного вида инфекций на пациента.
Особенности ксеногенных групп
Имплантация редко предполагает выбор именно этой разновидности на практике. Зато они способствуют сохранению структуры костей с минеральной точки зрения, а ещё материал отличается остеокондуктивными свойствами. Источник для получения – костная ткань млекопитающих. Многие животные кости обладают структурой, похожей на человеческий организм. Поэтому в стоматологической практике не отказываются от таких решений. Деантигенизация и специальная обработка стали важными требованиями.
Только при таком подходе получается устранять любые нежелательные реакции.
Обработка ксеногенного материала предполагает сохранение высоких, либо низких температур. Энзимные технологии тоже продолжают широко использовать на практике. Деантигенизация проводится двумя основными методами. Повышение температуры до 700-1000 градусов при обработке – одно из самых эффективных решений. Это приводит к испарению всех веществ органического происхождения. Усадка у ксенокостей отсутствует. Разрушение и восстановление костной ткани – процессы, которые проходят синхронно, за счёт чего объём при восстановлении не утрачивается. Искусственные костные гранулы замещаются натуральными материалами.
Синтетического происхождения
В основе этого материала всегда – кальциевые соли. Если в вертикальной или горизонтальной плоскости требуется нарастить большой объём, допустимо сочетание с аутогенной костью. Главное – чтобы соотношение между составными частями было равным. Отличная альтернатива для других решений на современном рынке. Некоторые признаки даже превосходят аналогичные разработки естественного происхождения. Например, вероятность заражения практически сведена к минимуму, необходимость в заборе костных тканей отпадает.
Свойства остеоиндукции у синтетических материалов отсутствуют, что считают главным недостатком по сравнению с другими подобными разработками. То есть, эктопическое формирование у костной ткани может отсутствовать. Поэтому к составу надо добавлять компоненты, стимулирующие данный процесс. Тогда и появление соответствующих характеристик не заставит себя ждать.
Что надо сделать перед тем, как увеличить костную ткань?
Обычно речь идёт об устранении моляров и предмоляров. После этого кость не испытывает дополнительных нагрузок, что со временем может приводить к дистрофии. Пародонтальная ткань может столкнуться с развитием воспалительных процессов, что тоже усложняет установку имплантатов.
Поэтому так важно придерживаться индивидуального подхода, когда занимаются подбором методики. При необходимости назначается инструментальная диагностика, ротовая полость тщательно осматривается лечащим врачом. Даётся оценка её текущего состояния. Иногда бывает так, что оперативное вмешательство уже идёт, но возникла необходимость выбрать другую технологию. Специалисту должны быть известны все методы остеопластики, чтобы они правильно применялись на практике.
Разновидности современных процедур
Предлагаем описание основных технологий по остеопластике. Они помогут разобраться в том, когда и какой вариант выбирать в зависимости от сложившихся обстоятельств.
Одно из оперативных вмешательств для верхней челюсти. Помогает увеличивать костную ткань наверху при обнаружении дефицита.

Один зуб переносится с одного места на другое. Это нужно, чтобы восполнить дефект – не важно, функционального он характера или визуального. Трансплантация зубов мудрости или восьмых моляров – решение, которое выбирает большинство пациентов. Костная ткань увеличивается по ширине в результате.
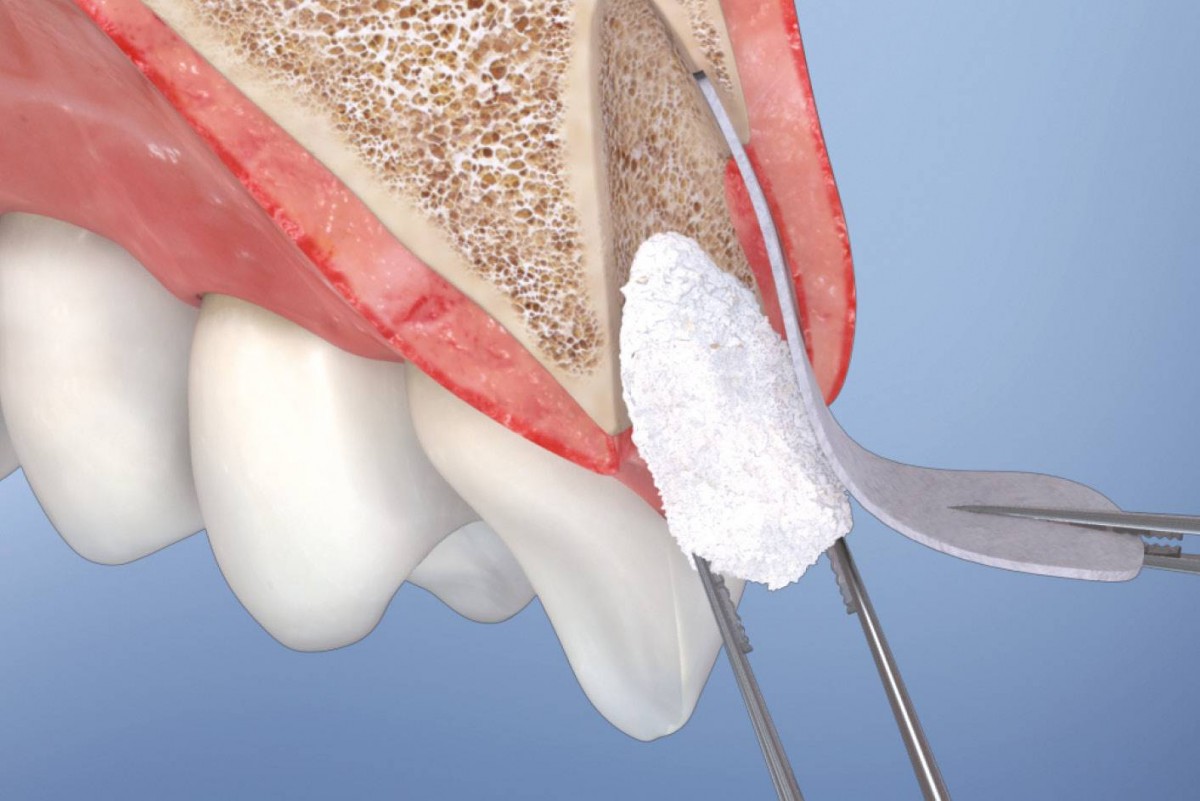
Материалы синтетического происхождения способствуют эффективному увеличению костных тканей. Барьерные мембраны выбирают, когда надо зафиксировать пересаженные костные ткани, либо обеспечить дополнительную защиту после избавления от моляров. Аллотрансплантаты станут оптимальными, если больше интересует возможность восстановления. Аутотрансплантаты самые распространённые среди материалов.
С точки зрения техники и инструментов остеопластические операции отличаются повышенной сложностью. Без грамотного подхода оперативные вмешательства могут быть связаны с некоторыми негативными эффектами. Обращаться надо только в клиники, которые уже зарекомендовали себя на практике. Тогда вероятность проблем и спорных ситуаций меньше.
Остеопластика – это реконструктивно-восстановительная операция, позволяющая нарастить объем альвеолярного гребня, остановить атрофию кости, заполнить имеющиеся дефекты ткани. Нередко костнопластические операции проводят перед имплантацией, чтобы обеспечить объем кости, необходимый для нормального приживления титанового имплантата. Существует два варианта проведения костной пластики – как самостоятельная операция и одновременно с имплантацией. Выбор зависит от клинической картины и выбранного протокола имплантации.
Особенности костнопластических материалов в стоматологии
В стоматологической практике применяют различные остеопластические материалы. Они могут отличаться по виду, происхождению, но должны обладать определенными характеристиками:
- Безопасность. Вживление остеопластического материала не должно нести рисков для здоровья пациента.
- Хорошая приживаемость. Для наращивания кости применяют не только донорскую кость, но и синтетические материалы. Важно, чтобы они хорошо приживались, имели минимальный риск отторжения.
- Пористость. Благодаря пористой структуре остеопластических материалов, собственная кость может прорастать через него.
- Биосовместимость. Искусственные материалы должны быть совместимы с тканями организма.
- Высокая адгезия. Благодаря высокой адгезии костнопластический материал полностью заполняет дефект. Также эта характеристика обеспечивает плотное прилегание и хорошую приживаемость имплантата.
- Остеогенность. После вживления костнопластический материал должен инициировать рост собственных жизнеспособных остеогенных клеток.
- Остеоиндукция. Это способность вживляемого материала воздействовать на мезенхимальные стволовые клетки. В результате такого стимулирующего воздействия начинает расти собственная ткань.
- Остеокондукция. После вживления костный имплант формирует матрикс – пассивный каркас, который способствует наращиванию новой ткани. Со временем имплантированный граф, обладающий остеокондуктивными свойствами, резорбируется. Например, хорошими показателями остеокондукции обладает собственная губчатая кость пациента.
Классификация костнопластических материалов
В современной стоматологии применяют большое количество разнообразных остеопластических материалов. Они отличаются по своему происхождению и свойствам. По происхождению выделяют четыре основных группы материалов:
- Аутогенные. В качестве материала для подсадки применяют собственную кость пациента.
- Аллогенные. Донором костной ткани выступает другой человек.
- Ксеногенные. Кость для подсадки берут у животного.
- Синтетические. Искусственные материалы на основе кальциевых солей.
Свои особенности имеет каждая группа материалов. Поэтому при выборе хирург опирается на клиническую картину.
Аутогенные
Аутотрансплантанты в стоматологии используют часто, так как этот тип материалов обладает лучшими характеристиками. Для пересадки используют небольшие фрагменты собственной кости пациента. В зависимости от того, откуда трансплантолог делает забор костной ткани, она может быть хрящевого или эктомезенхимального происхождения.
Лучший вариант для подсадки – губчатая кость. Она обладает остеогенными, остеоиндуктивными и остеокондуктивными характеристиками, отлично приживается. Применение собственной кости для подсадки имеет свои ограничения:
- Дополнительное вмешательство по забору костного материала. Это приводит к необходимости делать еще один надрез, увеличивает болезненность;
- Дефицит кости в месте забора. В донорском месте образуется дефицит костной ткани. Со временем он восстанавливается, но врач должен внимательно выбирать место для забора ткани. Количество донорских мест и объем костной ткани, которую можно пересадить с минимальным риском для здоровья пациента ограничены;
- Риск осложнений. Забор собственной ткани усложняет остеопластическую операцию. Риск развития осложнений при выборе этого метода может достигать 20%.
Основное преимущество аутокости – отсутствие иммуногенности. Так как у подсаживаемого материала нет иммунной несовместимости с тканями человека, риска отторжения аутотрансплантанта практически нет. Заживление проходит быстро, без выраженной боли. Через несколько месяцев в месте вживления трансплантата начинает расти молодая костная ткань.
Недостатки применения аутокости привели к применению других донорских материалов для подсадки.
Аллогенные
Аллогенные материалы – это кортикальная и губчатая костная ткань. После забора донорского материала его обрабатывают. Таким образом он становится пригодным к трансплантации.
В качестве аллоимплантатов применяют:
- Свежую или свежезамороженную кость, обработанную для хранения. Основной недостаток обработанной ткани – риск возникновения токсических реакций на применяемые средства;
- Лиофилизированную кость – минерализованная ткань, полностью лишенная живых клеток. Такой материал обладает хорошей остеокондукцией;
- Деминерализованные костные аллотрансплантаты, изготовленные методом полной, частичной или поверхностной декальцинации. Такой материал обладает хорошими остеокондуктивными и остеоиндуктивными свойствами;
- Биокомпозитные материалы, которые включают в себя компоненты кости и биоактивные субстанции.
Применение аллотрансплантатов позволяет быстро нарастить объем костной ткани без дополнительного травмирования пациента. После трансплантации достаточно быстро начинается рост собственной молодой кости.
Ксеногенные
Ксенокость получают из костей млекопитающих. Такие трансплантаты отличаются хорошими остеокондуктивными свойствами. Для того чтобы ксенокость можно было использовать для подсадки человеку, ее обрабатывают. Благодаря этому получается в значительной степени риск развития иммунного или аллергического ответа организма на подсадку чужеродного материала.
В зависимости от способа обработки выделяют несколько видов ксеноматериалов:
- С низкотемпературной обработкой;
- С высокотемпературной обработкой;
- С обработкой с использованием энзимных технологий.
Деантигенизация – обязательный этап обработки. С ее помощью из кости удаляют иммуногенные компоненты. При этом биологические и биохимические свойства материала остаются неизменными.
Синтетические
Синтетические остеопластические материалы делают на основе фосфатов кальция – гидроксиапатита, трикальцийфосфата, карбонат-замещенного ГА. Они отличаются высокой функцией клеток, участвующих в ремоделировании кости. Их применение позволяет минимизировать риски, связанные с использованием ауто- и аллотрансплантатов.
Синтетические материалы обладают необходимой биологической активностью. Они проявляют остеокондуктивные и остеоиндуктивные свойства. Остеокондуктивные материалы образуют пассивный матрикс, который со временем резорбирует, полностью замещаясь новой костной тканью. Для придания необходимых свойств в материал вводят дополнительные компоненты: коллаген, факторы роста, антибактериальные и кортикостероидные препараты.
Методы остеопластики
Чтобы имплантат мог стабилизироваться, необходимы адекватная ширина и высота костной ткани. После того, как зуб утрачивается, на кость нет необходимого физиологического давления. Начинаются атрофические процессы. Чем меньше объем альвеолярного отростка, тем сложнее провести успешную имплантацию, так как при установке внутрикостного имплантата есть риск перфорировать дно верхнечелюстной пазухи.
Костная пластика позволяет нарастить необходимый объем кости и успешно вживить имплант. На практике чаще всего применяют следующие методы костной пластики:
Хирург выбирает подходящий метод остеопластики на основе клинической картины и результатов исследования. Также индивидуально он выбирает и костнопластический материал, с которым будет работать.

3. Назарян, Р.С. Варианты отсроченных результатов операции резекции верхушки корня (клинические наблюдения)/ Назарян Р.С., Фоменко Ю.В., Щеблыкина Н.А., Колесова Т.А., Сухоставец Е.В.// Вестник проблем биологии и медицины. 2014. Т. 2. № 2 (108). С. 35-41.
Актуальность. Высокое распространение верхушечных деструктивных форм периодонтитов, а также их осложнений, создает большую проблему в стоматологии не только для пациентов, но и для врачей.Несмотря на современные методики лечения, большое количество средств и способов проведения зубосохраняющих оперативных вмешательств, данная проблема остается актуальной, так как не всегда удается добиться успеха в регенерации периапикальных тканей в исходе патологического процесса, а склонность организма к образованию кист и опухолевых процессов может приводить к рецидиву заболевания, даже спустя длительные сроки после проведения хирургических манипуляций [1,2,3].
Деструктивные формы хронического периодонтита (апикальные гранулемы, кисты) представляют большую проблему для организма. В ряде случаев воспалительный процесс способен распространяться не только на ткани зуба, но и на костную ткань вокруг верхушек корней даже соседних зубов, в результате чего возникает необходимость удаления нескольких зубов. Также в воспалительный деструктивный процесс могут вовлекаться соседние анатомические структуры – гайморова пазуха, нижнечелюстной канал, слюнные железы, что чревато грозными осложнениями [3,4].
Хронические очаги воспаления в периапикальных тканях могут быть причиной одонтогенных воспалительных процессов в челюстно-лицевой области, снижая резистентность и иммунологический статус организма, влиять на патогенез развития и течение заболеваний внутренних органов и
систем [2,3]. Причинами возникновения осложнений при лечении деструктивных форм периодонтита могут быть поздняя диагностика, ошибки и осложнения при эндодонтическом лечении, перегрузка при использовании данных зубов под опору, несвоевременное хирургическое вмешательство с возможным использованием остеогенных препаратов узконаправленного действия и т. д. [1,2].
Несмотря на значительный диапазон лечебных воздействий, не всегда удается получить желаемые результаты, что является основанием для поиска новых лечебных методов и средств реабилитации пациентов с указанной патологией. Одним из возможных перспективных направлений в хирургическом лечении радикулярных кист, для заполнения костного дефекта в периапикальной области зубов после оперативного вмешательства по резекции верхушки корня зуба, является использование остеопластических препаратов, однако современный рынок предлагает широкий выбор средств и препаратов [3,4].
Цель исследования. Определить эффективность современных остеопластических препаратов российского производства после проведения зубосохраняющей операции резекции верхушки корня зуба в сочетании с методами современных эндодонтических технологий.
Материалы и методы исследования. Исследование проведено на кафедре хирургической стоматологии и челюстно-лицевой хирургии Ставропольского государственного медицинского университета на базе ГКБСМП г. Ставрополя. В исследование включены 20 пациентов с диагнозом радикулярная киста, которым показана операция резекции верхушки корня зуба. Критериями исключения из исследования являлись противопоказания к рентгенологическому исследованию, беременность, кормление грудью, возраст более 60 лет, наличие тяжелой общесоматической патологии.
Пациентам проводился комплекс лечебных мероприятий, включая консервативные (первый этап) и хирургические методы лечения (второй этап). На первом этапе пациентам проводилось эндодонтическое лечение с использованием системы ProTaper (Dentsply, США), обтурация корневого канала производилась методом латеральной конденсации с использованиемсилера АН+ и гуттаперчевых штифтов и реставрация коронки фотокомпозитным материалом.
Хирургическое лечение заключалось в оперативном вмешательстве – цистэктомии с резекцией верхушки причинного корня и закрытии костных дефектов остеопластическим материалом. В зависимости от вида использованного препарата пациенты разделены на 2 группы (по 10 человек в каждой группе). Костный дефект заполнялся соответствующим препаратом в сочетании с обогащенной тромбоцитарной плазмой. Рана наглухо ушивалась синтетическим материалом.
Критериями оценки состояния костной структуры после операции явились: клиническое состояние до лечения; результаты рентгенологического исследования; мониторинг в течение года.
Результаты исследования. Послеоперационный период пациентов обеих групп протекал без особенностей, швы снимались на 10 сутки. В течение года пациенты не отмечали каких-либо жалоб. На рентгенограммах, через год отмечалось улучшение состояния структуры костной ткани.
В ближайшие дни после оперативного лечения у 67,9% 1 группы и 65,1% пациентов отсутствовал болевой синдром или отмечался небольшой дискомфорт (12,4%1 группы и 15,2% пациентов 2 группы), умеренная ноющая боль (у 3,7% пациентов 2 группы. Боль и отек исчезали к 3-4 суткам после операции у пациентов обеих групп.
У одного пациента 2 группы после операции в течение суток отмечалось повышение температуры тела до 37,5˚С. В одном случае после резекции верхушки корня 34 зуба наблюдались подслизистая гематома и нейропатия 3 ветви тройничного нерва слева, по поводу чего пациентка получила лечение с положительной динамикой.
При рентгенологическом исследовании через 1, 3, 6, 12 месяцев после лечения было отмечено увеличение плотности костной ткани по периферии очага деструкции – благоприятный признак, свидетельствующий о репаративномостеогенезе у пациентов обеих групп. Показатели плотности периапикального очага деструкции кости за указанные периоды наблюдения достоверно не различались.
В одном случае дважды оперированный зуб был удален через год. Зуб удален по месту жительства пациентки в поликлинике г. Ставрополя в связи с появлением боли, отека десны, на рентгенограмме отмечалось неполное заживление периапикального очага деструкции кости.
По статистике, заболевания, сопровождающиеся деструктивными изменениями костной ткани (например, доброкачественные опухоли или радикулярные кисты) занимают одно из первых мест в структуре челюстно-лицевых дефектов.
В связи с этим, наряду с оптимальным выбором новых хирургических техник, актуальным становится выбор остеопластических материалов. Общепризнанно, что остеопластика открывает максимальные возможности для реабилитации пациентов.
Современный ассортимент костных материалов для хирургической стоматологии подразделяется на несколько обширных групп. Среди них выделяются аутогенные, аллогенные, ксеногенные (Остеоматрикс), аллопластические (искусственно синтезированные заменители кости) и композиционные материалы.
Принадлежащие к перечисленным группам остеопластические материалы обладают уникальным набором преимуществ и недостатков, в зависимости от тех клинических требований, которые предъявлялись к ним.
Остеопластическим материалам должны быть присущи:
- остеогенность — способность инициировать рост костной ткани за счет особых жизнеспособных остеогенных клеток (аутокость)
- остеоиндукция — способность стимулировать рост ткани в результате действия материала на дифференцировку мезенхимальных стволовых клеток (протеины крови, ростовые факторы и другие биоактивные компоненты)
- остеокондукция — способность остеопластического материала играть роль пассивного каркаса (матрикса) для наращивания новой ткани с последующей резорбцией имплантированного графта.
Помимо этих ключевых свойств, следует принимать во внимание пористость (обеспечивающую прорастание новой костной ткани), биологическую и иммунологическую совместимость с организмом реципиента, инфекционную безопасность (стерильность), экономическую и физическую доступность.
Особое значение в нынешних реалиях приобрели религиозные, морально-этические и юридические аспекты, связанные с выбором костных материалов.
Аутогенные остеопластические материалы в стоматологии
По данным литературы, чаще всего в хирургической стоматологии используется аутопластический метод — пересадка кости, полученной из другой части тела самого пациента. Впервые аутогенный трансплантат испытан хирургом Уолтером в 1820.
Сторонники аутогенных графтов указывают на высокую остеогенность (за счет наличия клеток), остеокондукцию (благодаря содержанию минералов и коллагена) и остеоиндуктивные свойства (за счет неколлагеновых белков костного матрикса).
По своей структуре аутотрансплантаты могут быть кортикальными, губчатыми и губчато-кортикальными. Принято считать, что при использовании губчатых костных материалов происходит более быстрая и полноценная реваскуляризация трансплантата.
Это возможно благодаря содержанию плюрипотентных клеток, которые способны дифференцироваться и пролиферировать, участвуя в остеогенезе. В кортикальных графтах указанные процессы протекают медленно.
Ряд исследователей считают, что губчато-кортикальные фрагменты за счет прочной кортикальной части обладают достаточными механическими свойствами, а губчатая составляющая способствует повышению остеогенного потенциала.
Чаще всего внеротовыми участками для забора остеопластического материала служит нижняя челюсть, реже — тазовая кость, латеральный край лопатки или ребро. По мнению зарубежных специалистов, ткань из тазовой кости и челюсти отличается высоким регенеративным потенциалом и меньше поддается резобрции.
В любом случае, только для получения аутогенного остеопластического материала необходимо выполнять дополнительное вмешательство. Это означает привлечение анестезиологов и хирургов, дополнительные риски и затраты.
Если для выполнения остеопластики требуется получить внутриротовой трансплантат, оптимальным донорским участком является тело либо ветвь нижней челюсти, ретромолярная область, подбородочный симфиз и горб верхней челюсти.
Забор биоматериала производится под местной анестезией, что упрощает весь лечебный процесс, однако дополнительная травматизация и риски остаются.
Стоит упомянуть, что одной из основных причин отказа от данного вида остеопластики является страх пациентов перед хирургическим вмешательством и естественное желание закончить лечение с минимальной кровью (в буквальном смысле).
Несмотря на очевидные преимущества аутотрансплантатов (биосовместимость, инфекционную безопасность, регенеративный потенциал), они имеют существенный недостаток. Проблема заключается в резорбции трансплантата в динамике, преимущественно при использовании внеротовых графтов.
Нужно помнить о возрастных аспектах, переносимости дополнительного хирургического вмешательства у отдельных категорий пациентов.
Метод с осторожностью используется в пожилом и детском возрасте, в том числе из-за недостаточного количества кости и риска повреждения ростовых зон у детей.
Необходимость забора кости всегда сопряжена с дополнительным риском инфицирования донорского участка, кровопотерей, увеличением продолжительности послеоперационного периода, повышенной потребностью в обезболивающих препаратах, ростом медицинских расходов и др.
Потребность в преодолении этих недостатков аутотрансплантации обусловили быстрое развитие альтернативного метода — аллотрансплантации. Впервые в мире новаторский метод замещения костных дефектов, при котором донором выступает другой человек, использовали в 1880 году под руководством Уильяма Макьюэна.
Аллогенные костные материалы в хирургической стоматологии
Известно, что аллогенный трансплантат является остеокондуктивным, но ряд авторов указывают на остеоиндуктивные свойства, выраженность которых зависит от способа обработки (лиофилизация, замораживание, обработка формалином).
Аллотрансплантат деминерализованной лиофилизированной кости наряду с аллотрансплантатом деминерализованной кости (АДК) являются основными представителями этой группы остеопластических материалов.
Суть обработки графта заключается в том, что после деминерализации ткань становится более эластичной, благоприятствуя заполнению дефектов сложной формы и обеспечивая более плотный контакт с костным ложем.
Это является залогом успешной остеопластики.
Деминерализованную кость подвергают лиофилизации. Это процесс сублимации жидкости из предварительно замороженной ткани в вакууме. Такое обезвоживание осуществляется за счет стремления к поддержанию равновесной концентрации водяных паров в окружающем пространстве и ткани.
Исследования показали, что в процессе деминерализации происходит высвобождение коллагенового матрикса и костных морфогенетических белков — стимуляторов остеогенеза. Но остеогенный потенциал лиофилизированной и обработанной формалином кости может быть слабее, чем у АДК.
Экспериментальные исследования указывают на более высокую эффективность аллотрансплантатов, насыщенных гликозаминогликанами, ростовыми факторами и гидроксиапатитом. Однако сам этот метод остеопластики имеет принципиальные недостатки, в том числе недостаточную остеогенность и риск иммунных реакций.
В практике возникают сложности с получением и хранением аллогенного материала, требующего создания специальных банков. Хотя логистические проблемы частично разрешены коммерческими производителями, остается непредсказуемость результатов — это барьер, который сложно преодолеть.
При глубоком изучении свойств аллотрансплантатов выявляется зависимость остеоиндуктивного потенциала от целого набора факторов:
- возраст донора кости
- срок забора материала после смерти
- температурный режим хранения
- технология консервации образца и др.
Ксеногенные костные материалы в хирургической стоматологии
Одна из самых интересных категорий остеопластических материалов — ксеногенные, или принадлежащие представителям других биологических видов. Это доступные и массовые продукты животного происхождения, которые подвергаются тщательной многоступенчатой обработке перед имплантацией в человеческий организм.
Впервые ксеноматериалы были применены для остеопластики в 1668 году знаменитым хирургом ван Мегененом, однако технологическая отсталость медицины того времени вынудила отодвинуть их внедрение до второй половины XIX века.
Трансплантолог Леопольд Олье (1830-1900) обнаружил удивительную закономерность. Пересаживая костные графты от примитивных животных более высокоорганизованным видам, хирург достигал хороших прогнозируемых результатов — и наоборот. Эксперимент Олье продемонстрировал, что пластика костного дефекта у кошки материалом от кролика эффективнее, чем курице от кролика. Это стало откровением для ученых и новым толчком к изучению эффективности ксеноматериалов.
В настоящее время наиболее широко используется костная ткань свиней или крупного рогатого скота (Остеоматрикс), которая подвергается особой обработке — депротеинизации, удаляющей антигенные вещества. Это важнейшее условие успеха процедуры, поскольку реакция отторжения трансплантата часто приводит к провалу.
Иммуногенность потребовала разрабатывать новые методы очистки и производства ксеногенных трансплантатов. В зависимости от типа обработки их классифицируют:
- ксеноматериалы с низкотемпературной обработкой
- ксеноматериалы с высокотемпературной обработкой
- ксеноматериалы на основе энзимных технологий*
* - последние в процессе обработки очищаются при помощи ферментов и длительного промывания, сохраняя выраженные остеокондуктивные свойства.
После предварительной очистки ксеноматериал трансформируется в костный минерал, который с различной скоростью подвергается резорбции в организме пациента, но не обладает непосредственно остеоиндуктивными свойствами.
Согласно исследованиям, наличие микроскопических пор в структуре ксеноматериалов способствует быстрой реваскуляризации трансплантата.
В течение первых месяцев после операции поры наполняются мезенхимальными клетками и функциональными капиллярами. Этот момент является ключевой точкой для образования новой кости и резорбции имплантированного материала. Для полной резорбции и замещения графта требуется порядка 20-22 месяцев.
Несмотря на очевидные преимущества, использование ксеноматериалов в стоматологии и челюстно-лицевой хирургии остается ограниченным по ряду причин. Наличие гликозаминогликанов (теоретически!) не исключает вероятности передачи прионных белков, возбудителей фатальной болезни Крейтцфельдта-Якоба.
Здесь многое зависит от технологии обработки продукта. Например, остеопластические материалы Остеоматрикс проходят многостадийный контроль и агрессивный процесс обезвреживания, который полностью исключает проникновение патологических белков в организм пациента.
Синтетические остеопластические материалы в стоматологии
Синтетические вещества – интересный альтернативный материал в хирургической стоматологии и челюстно-лицевой хирургии с 1970-х годов, когда началось бурное развитие соответствующих направлении химии и химической технологии. Первой ласточкой был синтетический гидроксиапатит, предложенный Халбертом.
В результате проведенных сорок лет назад экспериментов было отмечено прорастание соединительной ткани в микропоры графта при отсутствии воспалительного процесса.
Но выраженного остеокондуктивного эффекта достичь не удалось из-за быстрой резорбции. Дальнейшие опыты показали, что скорость резорбции в значительной степени определяется плотностью и пористостью конкретного продукта.
Это искусственный аналог основного компонента неорганического костного матрикса, который принимает участие в обеспечении адгезии протеинов и клеток, ионном обмене. По данным отечественных исследований, синтетический гидроксиапатит индуцирует остеогенез и обладает остеокондуктивными свойствами.
Преимуществом гидроксиапатита является полная неиммуногенность и способность к постепенной резорбции при взаимодействии с живыми тканями.
Важной особенностью его является совместимость с минерализованными тканями организма. В процессе резорбции продукты распада кальций-фосфорных веществ, то есть ионы кальция и фосфора, метаболизируются естественным путем, без превышения норм содержания минералов в моче и сыворотке.
Современный выбор синтетических аллопластических материалов:
- Неорганические вещества: синтетический гидроксиапатит, трикальцийфосфат, кальция сульфат, биоактивное стекло, кальция карбонат
- Органические вещества: представлены полимерами животного и растительного происхождения
Несмотря на разнообразную химическую структуру, происхождение и способ получения, синтетические остеопластические материалы объединены рядом достоинств.
Они никогда не содержат потенциально опасных резидуальных протеинов, не содержат прионных или иных болезнетворных агентов, допускают регуляцию скорости резорбции и других характеристик на этапе производства, легко стандартизируются.
Наконец, синтетика практически исключает религиозные или этические проблемы, сопряженные с использование животного и трупного биоматериала.
Будущее синтетических биоматериалов видится в комбинировании разных веществ. В практической медицине множество примеров, когда композиционные материалы удачно совмещают положительные свойства своих компонентов.
Например, выделенный из губчатых костей человека высокоочищенный коллаген, сульфатированные гликозаминогликаны (сГАГ), деминерализованный костный матрикс с гиалуроновой кислотой, трикальцийфосфат с гидроксиапатитом и коллагеном, комплекс коллагена с гидроксиапатитом и другие комбинации.
Клинический опыт подтверждает, что при использовании композиционных остеопластических материалов удается достичь лучших результатов, чем при использовании отдельных их компонентов.
Стремление к усовершенствованию кальций-фосфатной керамики привело к созданию новых композиций из полимеров и кальция.
Сегодня в роли органической базы биорезорбтивных полимеров применяется коллаген, полигликолид и полилактид. Всего же зарубежные авторы классифицируют современные композиты на три группы со своеобразным химическим составом:
- композиции коллаген + гидроксиапатит
- композиции кальций-фосфаты + полимер
- композиции полимер + керамика
Собственно коллаген являет собой межклеточный протеин. Он отличается высокой биосовместимостью, способностью к биодеградации и активации взаимодействия между клетками костной ткани. Несмотря на эти неоспоримые преимущества, клиническое применение коллагена сопряжено с обычными рисками ксенотрансплантатов (инфицирование).
В связи с этим ведутся исследования в области альтернативным природных полимеров, таких как растительный альгинат и животный хитозан.
В зарубежной хирургической стоматологии широко применяют остеопластические материалы, содержащие искусственные биодеградируемые полимеры, такие как полилактид и полигликолид.
Читайте также:

