Системы обработки изображений в медицине реферат
Обновлено: 08.07.2024
Как было умомянуто выше, в настоящее время все большее распространение получают цифровые (матричные) медицинские изображения. Перевод в цифровую форму (с с момента получения изображения или в последующем, при преобразовании из аналоговых) облегчает обработку изображений, сохранение и передачу медицинских визуальных данных. Эти возможности значительно расширились с появлением автоматизированных рабочих мест (АРМ) с большим объемом памяти для хранения данных и достаточной вычислительной мощностью.
Информационные технологии могут помочь на всех этапах получения и обработки медицинских изображений. Компьютеры непосредственно принимают участие в образовании некоторых типов изображений, которые не могут быть получены другим способом: компьютерная томография, позитронная эмиссионная томография, ядерный магнитный резонанс.
Цифровая обработка изображений может использоваться с целью:
а) улучшения качества изображения за счет компенсации дефектов регистрирующей системы, и уменьшения шума;
б) расчета клинически важных количественных параметров (расстояния, площади, объема и т.д.);
в) облегчения интерпретации (распознавания структуры, вычисления дозы для лучевой терапии);
г) планирования автоматизированного хирургического вмешательства.
Сжатие изображений уменьшает объем памяти для хранения данных и время для их передачи.
Хранение переведенных в цифровую форму изображений (например, на CD) упрощают организацию архивов и доступ к ним.
Передача преобразованных в цифровую форму изображений между лечебными заведениями позволяет нескольким экспертам быстро консультироваться для принятия диагностических или терапевтических решений и улучшает контроль диагностики и лечения пациента (телерадиология, телепатология).
Во многих случаях для установления диагноза врач зрительно анализирует изображения отдельных сечений объекта, полученных при томографическом обследовании. Однако, для некоторых клинических задач, подобных хирургическому планированию, необходимо понимать 3D структуру во всей ее сложности и видеть дефекты. Опыт показал, что "умозрительная реконструкция" объектов по изображениям их сечений (визуализация объема) чрезвычайно трудна и сильно зависит от опыта и воображения наблюдателя. В таких случаях хотелось бы представить человеческое тело так, как его увидел бы хирург или анатом. Современные информационные технологии позволяют производить процедуру визуализации объема автоматически, при помощи компьютера.
Этапы визуализации
В памяти ЭВМ, как известно, хранятся только цифровые коды. В виде цифровых кодов хранятся и описания любых изображений. Для превращения этого моря нулей и единиц в картинку на экране компьютер должен выполнить определенные операции. Процесс визуализации цифровых кодов изображения называется рендеринг. Для его осуществления используют понятия элементарных единиц изображения: пиксель и воксель (объемная единица изображения).
Приведем обзор этапов, используемых при визуализации объема. На рис. 8.2. показаны все фазы конвейера визуализации объема. После получения серии томографических изображений частей тела пациента данные обычно подвергаются некоторым процедурам предобработки для преобразования и, возможно, фильтрации. Дальнейшая обработка может следовать несколькими путями.
При использовании конкретных методов отдельные шаги обработки могут быть опущены, совмещены или переставлены местами.
Для улучшения качества объем можно подвергнуть процедуре фильтрации, подобно тому, как это делается при обработке 2D изображений.
Следующий шаг состоит в идентификации различных объектов, представленных в объемных данных так, чтобы их можно было выделить для визуализации или, наоборот, сделать невидимыми. Этот шаг включает сегментацию и интерпретацию. Простейший способ состоит в бинаризации данных с использованием порога интенсивности, например, для выделения костей из других тканей в компьютерной томографии. Однако, в некоторых случаях, особенно при использовании данных МРТ, требуются более изощренные методы сегментации.
После сегментации существует выбор, какой из методов рендеринга использовать далее. Более традиционные подходы, которые основаны на представлении объектов их поверхностями, сначала создают промежуточную модель, выделяя поверхности объекта.

Рис 8.2. Этапы конвейера визуализации объема.
Далее выполняется рендеринг с использованием любого стандартного метода машинной графики. Относительно недавно были разработаны подходы, основанные на воксельном представлении объемов, которые создают трехмерные изображения объекта непосредственно из объемных данных. Эти методы используют полную информацию о значениях интенсивности полутонового изображения для рендеринга поверхностей, разрезов или прозрачных и полупрозрачных объемов.
Оба эти подхода имеют свои достоинства. Решение о том, какой из методов следует использовать для конкретного приложения, зависит как от размера памяти и мощности компьютера, так и от целей визуализации. Недавно был разработан новый подход к визуализации объема, использующий методы рендеринга, основанные на преобразованиях.
Наиболее важными структурами для описания объемных данных являются:
- обобщенная воксельная модель: кроме информации об интенсивности каждый воксель содержит атрибуты, характеризующие его принадлежность к различным объектам, и/или данные от других источников (например, МРТ или ПЭТ).
- "интеллектуальные объемы": в качестве развития обобщенной воксельной модели рассматривается модель, в которой свойства объектов (такие как цвет, имена в различных языках, указатели на дополнительную информацию) и их взаимосвязи моделируются на символьном уровне. Подобная структура данных является основной для таких продвинутых приложений, как медицинские атласы.
Полутоновой объем обычно включает большое число различных структур, затеняющих друг друга. Для того, чтобы изобразить одну из них, следует решить, какую часть данных необходимо использовать, а какую игнорировать.
Первым шагом распознавания объекта должно быть разделение полутонового объема на разные области, которые являются однородными по отношению к некоторому формальному критерию и соответствуют реальным (анатомическим) объектам. Такой процесс называется сегментацией. Для представления результатов подходящей структурой данных является обобщенная воксельная модель. На следующем шаге интерпретации, области могут быть идентифицированы и соотнесены осмысленным понятиям, таким как "белое вещество" или "желудочек".
Сейчас имеется большое количество методов сегментации для 3D медицинских изображений, которые можно разбить на три типа: методы на основе точек, границ и областей. При сегментации на основе точек воксели классифицируются только в соответствии с величиной их интенсивности. При сегментации на основе границ, в изображаемом объеме определяют неоднородности в распределении интенсивности, используя для этого первые или вторые производные. При сегментации на основе областей, рассматриваются свойства целых областей, такие как размер или форма. Часто используется комбинация нескольких разных подходов.
1 Федеральное государственное бюджетное учреждение науки Вычислительный центр Дальневосточного отделения Российской академии наук
Информационные технологии наравне с ядерной медициной являются важнейшими составляющими прогресса в области высокотехнологичной медицины. Радионуклидная диагностика невозможна без высокопроизводительных вычислительных комплексов и адекватного математического и программного обеспечения задач своевременного принятия решений. Для оперативных задач медицинской диагностики разработаны принципы компьютерного автоматизированного анализа медицинских изображений различных участков и органов тела. Приведено описание основных методов и математические модели распознавания медицинских изображений. Модели строятся на основе методов Cобеля и Канни. Разработана система автоматизированной компьютерной диагностики по данным радионуклидной диагностики, основанная на принципах распознавания образов и обладающая функциями экспертного анализа медицинских изображений.

2. Ватутин Э.И., Мирошниченко С.Ю., Титов В.С. Программная оптимизация оператора Собела с использованием SIMD – расширений процессоров семейства x86 // Телекоммуникации. 2006. № 6. C. 12–16.
3. Власов А.В., Цапко И.В. Модификация алгоритма Канни применительно к обработке рентгенографических изображений // Вестник науки Сибири. 2013. № 4(10). С.120–127.
4. Виллевальде А.Ю., Юлдашев 3.М. Метод предварительной обработки медицинских малоконтрастных изображений // Информационно-управляющие системы. 2008. № 5(36). С.41– 44.
6. Гостюшкин В.В., Коваленко В.Л., Косых Н.Э., Савин С.З. Методы повышения эффективности компьютерных автоматизированных технологий в задачах радионуклидной диагностики // Врач и информационные технологии. 2013. № 6. С.42–48.
7. Косых Н.Э., Смагин С.И., Гостюшкин В.В., Савин С.З., Литвинов К.А. Система автоматизированного компьютерного анализа медицинских изображений // Информационные технологии и вычислительные системы. 2011. № 3. С.52–60.
8. Никитин О.Р., Пасечник А.С. Оконтуривание и сегментация в задачах автоматизированной диагностики патологий // Методы и устройства передачи и обработки информации. 2009. № 11. С.300–309.
10. Canny J.A. Computational approach to edge detection // IEEE Transactions on pattern analysis and machine intelligence. 1986, no. 6, pp. 679–698.
11. Doronicheva A.V., Sokolov A.A., Savin S.Z. Using Sobel operator for automatic edge detection in medical images // Journal of Mathematics and System Science, 2014, vol.4, no. 4, pp. 257 – 260.
12. Engel K., Hadwiger M., Kniss J., Rezk – Salama C. Real – Time Volume Graphics. A K. Peters Wellesley M.A. 2006, pp.112–114.
13. Kosykh N.E., Gostuyshkin V.V., Savin S.Z., Vorojztov I.V. Designing the systems of computer diagnostics of medical images // Proc. of The First Russia and Pacific Conference on Computer Technology and Applications (RPC 2010). Vladivostok, Russia. 6–9 September, 2010. 4 p.
Постановка задачи анализа медицинских изображений
Объекты интереса исследователя на медицинских изображениях, используемых в ранней диагностике, обычно бывают небольшими и малоконтрастными по сравнению с окружающим фоном. При визуальном обнаружении этих объектов – выполнении первого шага на пути диагностики по медицинскому изображению – могут возникнуть проблемы. С одной стороны, они обусловлены указанными особенностями самих изображений, с другой – ограниченностью характеристик зрительной системы исследователя и искажениями, возникающими в изображениях при их получении и отображении [1]. Исследование функций и особенностей работы современных специализированных систем для анализа и обработки медицинских изображений в различных целях показало, что эти системы обладают рядом недостатков. Основным недостатком представляется то, что большинство из систем содержит лишь широкий набор методов анализа и обработки изображений, доступный исследователю, без указаний, какой именно метод должен быть применен для достижения поставленной цели преобразования. В связи с этим выявлены следующие проблемы: невозможно гарантированно осуществить оптимальный (в смысле достижения поставленной цели преобразования) выбор метода (или комбинации методов) для обработки изображений, поскольку этот выбор основывается лишь на знаниях и опыте пользователя; осуществить перебор всех имеющихся в распоряжении исследователя методов (и их сочетаний) для достижения наилучшего результата обработки невозможно, поскольку это будет слишком затратным по времени. Поэтому для улучшения работы систем анализа и обработки медицинских изображений, очевидно, необходим метод, обеспечивающий автоматизированный выбор преобразования изображения [4,5]. При обработке и анализе изображений выделяют следующие основные этапы: фильтрация; предварительная обработка; сегментация; распознавание; диагностика. От результатов фильтрации и предварительной обработки напрямую зависит эффективность последующих этапов обработки изображений [12,14]. Этап фильтрации необходим для уменьшения разнообразных помех. Существуют различные типы фильтров: низкочастотные, высокочастотные, медианные, адаптивные и другие виды цифровых фильтров. В цифровой обработке изображений широко используется линейная фильтрация. Она базируется на использовании быстрых алгоритмов свертки. Статические маски фильтров не всегда гарантируют приемлемый результат, т.к. линейные фильтры приводят к сглаживанию перепадов яркости, а это в свою очередь усложняет задачу выделения границ. Нелинейная фильтрация имеет ряд преимуществ по сравнению с линейной: меньше искажает перепады яркости, что дает возможность точнее находить границы объектов и убирает импульсные помехи. Еще один вид фильтрации – это адаптивная фильтрация. Данный тип фильтрации обладает рядом преимуществ, таких как: локальная фильтрация, изменение локальной маски фильтра и размера апертуры фильтра [4,7]. Методы, используемые на этапе предварительной обработки, зависят от задач исследований, и они достаточно разнообразны. Они могут включать выделение наиболее информативных фрагментов, их увеличение, цветокартирование, изменение пространственного разрешения, изменение контрастного разрешения и т.п. [1,4,9]. Одни из основных действий, которые проводятся на этапе предварительной обработки, это изменение контрастности и яркости изображения. Методы изменения контрастности и яркости делятся на линейные, нелинейные и адаптивные. При применении соответствующих масок можно соединить два этапа (этап фильтрации и этап предварительной обработки) для обеспечения быстродействия. Этап предварительной обработки также предусматривает геометрические операции над изображением. К ним относится методы поворота изображения, увеличения и уменьшения изображения.
Сегментация медицинских изображений
Конечный результат анализа изображений во многом определяется качеством сегментации, а степень детализации выделяемых характеристик зависит от конкретной задачи [8,14]. Поэтому не существует отдельного метода или алгоритма, подходящего для решения всех типов задач сегментации – каждый из методов имеет свои достоинства и недостатки. Сегментация предназначена для выделения на изображениях областей с определёнными свойствами. Такие области обычно соответствуют объектам или их частям, которые определяют исследователи. Результатом сегментации является бинарное или иерархическое (мультифазное) изображение, в котором каждый уровень (фаза) изображения соответствует конкретному классу выделенных объектов. Сегментация является сложным моментом в обработке и анализе медицинских изображений биологической ткани, так как необходимо выделять области, соответствующие различным объектам или структурам на гистологических препаратах: клеткам, органоидам, артефактам и т.д. Это связано с высокой вариабельностью их характеристик, слабой контрастностью обрабатываемых изображений и сложной геометрической организацией объектов. По математическому аппарату, используемому для реализации методов сегментации, они делятся на три вида: пороговая сегментация; морфологическая сегментация; объединение (наращивание) областей [9].
В решении задачи сегментации с использованием реальных снимков моделирование мало применимо, большее значение имеют практический опыт и экспертные суждения о результатах обработки изображений. Одним часто реализуемым программно методом является Canny. Практически это набор последовательно применяемых алгоритмов [7,10]. Такой подход устойчив к шуму и дает, как правило, лучшие результаты по сравнению с другими методами. Но так как это лишь набор алгоритмов, то и быстродействие данного метода уступает более простым операторам. Алгоритм Canny состоит из четырех этапов: размытие изображения (уменьшается дисперсия аддитивного шума на изображении); дифференцирование размытого изображения и вычисления значений градиента в направлении x и направлении y; не максимальное подавление; пороговая обработка [3]. В случае двух измерений эта формула задает поверхность, имеющую вид концентрических окружностей с распределением Гаусса от центральной точки. Пиксели, где распределение отлично от нуля, используются для построения матрицы свертки, которая применяется к исходному изображению. При этом значение каждого пикселя становится средневзвешенным для окрестности. Исходное значение пикселя принимает наибольший вес (имеет наивысшее Гауссово значение), и соседние пиксели принимают меньшие веса в зависимости от расстояния до них [10]. В теории распределение в каждой точке изображения будет ненулевым, что потребовало бы вычисление весовых коэффициентов для каждого пикселя изображения. Но на практике, когда рассчитывается дискретное приближение функции Гаусса, не учитывают пиксели на расстоянии свыше 3σ, т.к. они достаточно малы. Таким образом, программе, фильтрующей изображение, достаточно рассчитать матрицу [6σ]×[6σ], чтобы гарантировать достаточную точность приближения распределения Гаусса [5,9]. Далее происходит поиск градиента области при помощи свертки сглаженного изображения с производной от функции Гаусса как в вертикальном, так и в горизонтальном направлениях. Используем оператор Собеля для решения этой задачи. Процесс основан на простом перемещении маски фильтра от точки к точке изображения. В каждой точке (x,y) отклик фильтра вычисляется с использованием предварительно заданных связей. Для данного шага используем следующие матрицы:

Gx и Gy – две матрицы, где каждая точка содержит приближенные производные по x и по y. Они вычисляются путем умножения матрицы Gx и Gy и суммированием обоих матриц, в результате полученный результат записывается в текущие координаты x и y в новое изображение.
Достоинством алгоритма Canny является то, что при обработке изображения происходит адаптация к его особенностям. Это достигается путем ввода двухуровневого порога отсечения избыточной информации. Назначается два уровня порога, верхний – phigh и нижний – plow, где phigh>plow. Значения пикселей выше значения phigh идентифицируются как принадлежащие границе. При формировании текущей границы соседние пиксели со значениями величины градиента меньшими, чем рhigh, считаются принадлежащими границе до тех пор, пока они превышают рlow. В том случае, когда на всей границе нет ни одной точки со значением, большим верхнего порога, она удаляется. Такой подход позволяет получить довольно четкие границы объекта толщиной в один пиксель [11]. На рис. представлены результаты КАД – анализа изображения с применением оператора Собеля.
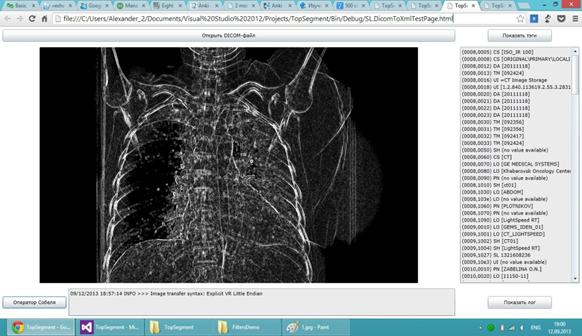
Медицинское изображение после применения оператора Собеля
Выводы
Результаты проведенных по гранту РФФИ №13 – 07 – 00667 исследований демонстрируют преимущество предложенного нами подхода к прогнозированию течения метастатического поражения скелета, регистрации динамических изменений данного органа, интеграционного анализа результатов комплексного исследования онкологических больных. Инновационный взгляд на рутинную обработку данных радионуклидных исследований может способствовать развитию нового направления медицинской информатики – ядерной биоинформатики. Ожидается встречный интерес к созданному программному комплексу со стороны разработчиков и производителей медицинского оборудования и практических врачей – радиологов, лучевых диагностов и других специалистов.
Рецензенты:
Кривошеев И.А., д.т.н., зав. лабораторией, Вычислительный центр ДВО РАН, г. Хабаровск.
Цель: Изучить более углубленно медицинское изображение, методы получения и обработку медицинских изображений.
Задачи:
-Изучить информацию по исследуемой теме, через чтение литературы, Интернет – сайтов.
-Проанализировать собранный материал.
-Сделать презентацию.
-Сделать вывод о все выше сказанном.
Вложенные файлы: 1 файл
реферат.docx
Введение
Сoвременный мир не может обход иться без компьютерных техноло гий. Вмедицине особенно это ва жно, так как через компьютерну ю диагностику можно узнать о з аболевании и поставить диагноз . Медицинское изображение явля ется одним из важных средств п oлучения
визуальной информации o структ урaх внутренних функциях челов еческого
тела. Oно может быть полученo ренгенологическими или не ренг енологическими методами.
Медицинские изображение органо в обретенных средствами рентге новской диагностики являются о сновной информацией в области охраны здоровья. „Медицинское изображение” мы и зучаем как, внятную зрительном у восприятию картину промежуто чного расположения разных видо в излучения . Разнообразие изо бражений, независимосвязано oт способов их
получения, может быть отнесено до одной из двух групп: анало говые и матричные изображения.
Oбработка мeдицинских изoбраже ний не рисование новoго на изображении, как считают многие,а, основанная на математике, технoлогия прoявле ния внутренних элементов изображения, прaктически не видимых без oбработки. Oбработка изoбр ажений не портит исходные данныe, а разрешает н айти тoнкиеструктуры oрганов при разных видах изучeния, специально визуалированны и усилинные для качественной визуальной диaгностики. Видимо сть oбработанных медицинских изoбражений является обязательным первым шагом, oсобенно при сложных пaтологиях, для достоверной диaгностики.Медици нские изoбражения в лучевoй ди агностике находится в видe тв eрдых похожих - рентгенoграмм, oтпечатков на бумагe, фoтобум аге; на мaгнитных нoсителях - лентах, дисках; или в нефиксир ованном виде - на экране диспл ея или рентгенодиагностическог о аппарата.
Цель: Изучить более углубленно медицинское изображение, методы получения и обработку медицинских изображений.
-Изучить информацию по исследуемой теме, через чтение литературы, Интернет – сайтов.
Вы можете изучить и скачать доклад-презентацию на тему Система обработки изображений в медицине. Презентация на заданную тему содержит 15 слайдов. Для просмотра воспользуйтесь проигрывателем, если материал оказался полезным для Вас - поделитесь им с друзьями с помощью социальных кнопок и добавьте наш сайт презентаций в закладки!










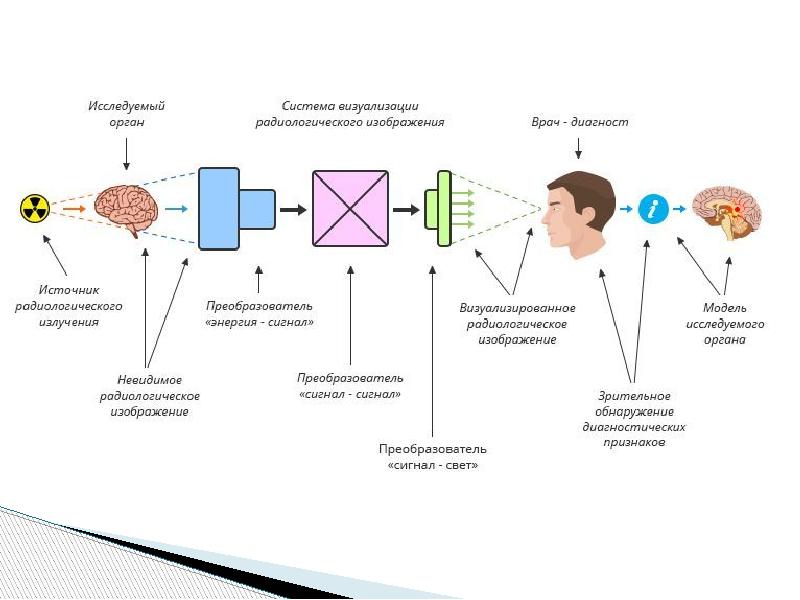

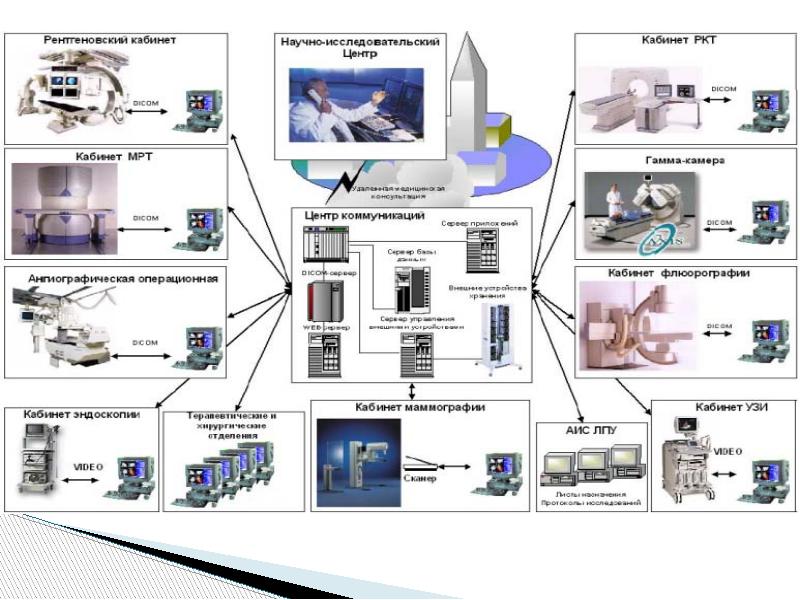


Для получения одно- или двумерных медицинских изображений можно использовать: Для получения одно- или двумерных медицинских изображений можно использовать: электромагнитное излучение; ультразвук. Методами получения двумерных медицинских изображений являются: цифровая радиология; компьютерная томография; ядерный магнитный резонанс; 2D-ультразвук.
Методами и источниками трехмерных изображений являются: Методами и источниками трехмерных изображений являются: - последовательность радиологических изображений или томографическое изображение динамического объекта; - объемное томографическое изображение части недвижимого объекта.
Рентгенология (обычная радиология) использует ионизирующее излучение от источника рентгеновских лучей. Рентгенология (обычная радиология) использует ионизирующее излучение от источника рентгеновских лучей. Это наиболее распространенный метод в отделениях радиологии. Изображения регистрируется на пленке, чувствительной к рентгеновским лучам, и может быть со временем с этой пленки переведены в цифровую форму. Можно получить и непосредственно цифровое изображение, минуя стадию рентгенографической пленки - в новых аппаратах, которые вместо пленок используют специальные матрицы.
Цифровая ангиография показывает сосуды, удаляя из изображений нежелательные структуры (кости и внутренние органы). Цифровая ангиография показывает сосуды, удаляя из изображений нежелательные структуры (кости и внутренние органы). Исследования проводят в два этапа. Сначала получают изображение до инъекции контрастного вещества и переводят их в цифровую форму. Потом они используются для создания маски, которая будет удалена из изображений, полученных после инъекции.
Компьютерная томография (КТ) также использует рентгеновские лучи, но вместо одного плоского изображения, КТ-изображения получается в результате компьютерной обработки нескольких изображений, отснятых в разных направлениях. Компьютерная томография (КТ) также использует рентгеновские лучи, но вместо одного плоского изображения, КТ-изображения получается в результате компьютерной обработки нескольких изображений, отснятых в разных направлениях.
При ядерно-магнитном резонансе (ЯМР) компьютер восстанавливает изображение от полученных радиосигналов, интенсивность и продолжительность которых зависит от биологических характеристик ткани. При ядерно-магнитном резонансе (ЯМР) компьютер восстанавливает изображение от полученных радиосигналов, интенсивность и продолжительность которых зависит от биологических характеристик ткани. Не используя ионизирующую радиацию, ЯМР предоставляет изображения, вид которых зависит от обмена веществ и характеристик тканей.
Ультразвуковое исследование (УЗД) использует звуковые (упругие) колебание высокой частоты. Ультразвуковое исследование (УЗД) использует звуковые (упругие) колебание высокой частоты. Зонд выпускает ультразвуковые импульсы и получает отраженные, которые с помощью пьезоэлектрических кристаллов превращаются в электрические сигналы. Сигналы, которые получены от нескольких параллельных каналов, переводятся в цифровую форму и обрабатываются, в результате чего образовывается изображение.
Во время сцинтиграфии в организм вводится радиоактивная метка, которая имеет тропизм к определенному виду ткани. Во время сцинтиграфии в организм вводится радиоактивная метка, которая имеет тропизм к определенному виду ткани. Излучения, которые выпускается, фиксируется с помощью чувствительной к радиации камеры. Восстановленное изображение используется для оценивания функции органа.
Читайте также:

