Реферат оперативное лечение циррозов печени портокавальные ангиоанастомозы виды и техника выполнения
Обновлено: 02.07.2024
В статье представлены наиболее важные заключения рабочего совещания Baveno VI по использованию инвазивных и неинвазивных методов диагностики и наблюдения пациентов с портальной гипертензией, профилактике декомпенсации, помощи при кровотечении, профилактик
Strategy of conducting patients with portal hypertension syndrome against the background of cirrhosis (according to materials of Baveno VI consensus, 2015)
The article highlights the most important conclusions of the working meeting of Baveno VI on use of invasive and non-invasive diagnostic methods and observation of patients with portal hypertension, prevention of decompensation, help in bleeding, prevention of complications.
Портальная гипертензия (ПГ) — гемодинамическое нарушение, связанное с наиболее тяжелыми осложнениями цирроза печени, включающими асцит, печеночную энцефалопатию и кровотечения из варикозно расширенных вен пищевода/желудка. Оценка диагностических подходов, дизайн и проведение надлежащих клинических исследований в лечении ПГ всегда были трудной задачей. Понимание этих трудностей обусловило проведение ряда встреч по консенсусу. Первая из них была организована A. Burroughs в городе Гронинген в 1986 г. [1]. За этой встречей последовал ряд других: в 1990 г. в городе Бавено (Италия) (Baveno I) [2], в 1995 году вновь в Бавено (Baveno II) [3, 4], в 1992 г. в Милане (Италия) [5], в 1996 г. в Рестоне (США) [6], в 2000 г. в Стрезе (Италия) (Baveno III) [7, 8], в 2005 г. в Бавено (Италия) (Baveno IV) [9, 10], в 2007 г. в Атланте [11], в 2010 г. в Стрезе (Италия) (Baveno V) [12, 13]. Цель встреч — анализ доказательств по течению синдрома портальной гипертензии и разработка рекомендации по ведению данной категории пациентов. Оценка уровня доказательств и рекомендации ранжированы согласно Оксфордской системе [14].
Скрининг на наличие портальной гипертензии
Критерии, позволяющие врачу заподозрить ХВКЗП
- Обнаружение при эластографии повышения плотности печени достаточно, чтобы заподозрить ХВКЗП у лиц без симптомов, но при наличии известных факторов хронического поражения печени; эластография часто дает ложноположительные результаты, поэтому ее рекомендуется выполнять дважды в разные дни в состоянии натощак (5; D).
- Значение эластографии менее 10 kPa при отсутствии других клинических признаков исключает наличие ХВКЗП, значения от 10 до 15 kPa позволяют заподозрить наличие ХВКЗП, однако требуют дальнейших обследований; значения более 15 kPa с большой степенью вероятности указывают на наличие ХВКЗП.
Критерии, позволяющие подтвердить ХВКЗП
- Биопсия печени с обнаружением выраженного фиброза или сформировавшегося цирроза (1b; A); определение относительной площади, занимаемой коллагеном, в печеночном биоптате позволяет количественно оценить выраженность фиброза и имеет прогностическое значение (2b; B).
- Эндоскопия верхних отделов желудочно-кишечного тракта: обнаружение варикозно расширенных вен (1b; A).
- Измерение печеночного венозного градиента давления (Hepatic venous pressure gradient — HVPG). Величина его более 5 мм рт. ст. указывает на синусоидальную портальную гипертензию (1b; A).
Диагностика клинически выраженной портальной гипертензии (КВПГ)
- У пациентов без признаков клинически выраженной портальной гипертензии нет варикозно расширенных вен пищевода/желудка (ВРВПЖ) и риск их развития в течение 5 лет низок (1b; A); измерение HVPG является золотым стандартом диагностики, при повышении этого показателя ≥ 10 мм рт. ст. (1b; A) ставят диагноз клинически выраженной портальной гипертензии.
- У больных с ХВКЗП вирусной этиологии достаточно использовать неинвазивные методики для определения группы риска по наличию КВПГ (пациентов, у кого высока вероятность обнаружения эндоскопических признаков портальной гипертензии). Для этой цели может быть использовано: определение плотности печени по данным эластографии, с подсчетом числа тромбоцитов и определением размеров селезенки. (Риск КВПГ высок при эластографии ≥ 20–25 кРа при как минимум двух определениях в разные дни в состоянии натощак. Следует быть внимательным при резких повышениях уровня АЛТ. Необходимо обратиться к рекомендациям Европейской ассоциации по изучению печени (European Association for the Study of the Liver, EASL) для правильной интерпретации критериев.)
- При заболевании печени другой этиологии значение величины эластографии для диагностики КВПГ подлежит уточнению (5; D).
- Методы визуализации, указывающие на наличие коллатерального кровотока, являются достаточными для подтверждения наличия КВПГ у больных ХВКЗП любой этиологии (2b; B).
Выявление пациентов с ХВКЗП, у которых можно избежать необходимости проведения эндоскопии с целью скрининга
- У больных с показателем эластографии менее 20 кРа и числом тромбоцитов более 150 000 риск наличия варикозных вен, требующих лечения, очень низок, и у таких пациентов можно избежать проведения эндоскопии (1b; A). Таких пациентов можно наблюдать, определяя им показатель эластографии и уровень тромбоцитов крови ежегодно (5; D).
- При увеличении плотности печени или снижении числа тромбоцитов пациентам необходимо проведение эзофагогастродуоденоскопии (ЭГДС) с целью скрининга (5; D).
Динамическое наблюдение пациентов с варикозным расширением вен пищевода/желудка
- У компенсированных больных при отсутствии признаков ВРВПЖ при скрининг-эндоскопии и с продолжающимся повреждением печени (прием алкоголя, отсутствие устойчивого вирусологического ответа при гепатите С) необходимо проведение ЭГДС с целью динамического наблюдения 1 раз в 2 года (5; D).
- У компенсированных больных с небольшим расширением вен и продолжающимся повреждением печени (прием алкоголя, отсутствие устойчивого вирусологического ответа при гепатите С) необходимо проведение ЭГДС с целью динамического наблюдения 1 раз в год (5; D).
- У компенсированных больных при отсутствии признаков ВРВПЖ при скрининг-эндоскопии, у которых этиологический фактор был удален (наличие устойчивого вирусологического ответа при гепатите С, длительная абстиненция у алкоголиков) и у которых нет ко-факторов (например, ожирения), ЭГДС с целью динамического наблюдения необходимо проводить 1 раз в 3 года (5; D).
- У компенсированных больных с небольшим расширением вен, у которых этиологический фактор был удален (достигнут устойчивый вирусологический ответ при гепатите С, длительная абстиненция у алкоголиков) и у кого нет ко-факторов (например, ожирения) необходимо проведение ЭГДС с целью динамического наблюдения 1 раз в 2 года (5; D).
Из-за разного прогноза пациенты с компенсированным циррозом должны быть разделены на тех, у кого есть признаки КВПГ, и тех, у кого их нет (1b; A). Цель лечения в первой подгруппе — профилактика развития КВПГ, а во второй — профилактика декомпенсации.
Профилактика развития КВПГ
- Изменение HVPG является приемлемым суррогатным маркером клинического исхода у больных с нехолестатическим циррозом (2b; B), значимым считается изменение HVPG на 10% и более (1b; A); этиотропное лечение может привести к уменьшению портальной гипертензии и предотвратить развитие осложнений у больных с сформировавшимся циррозом (1b; A); ожирение ухудшает естественное течение компенсированного цирроза любой этиологии (1b; A); алкогольная абстиненция должна поощряться у всех больных циррозом вне зависимости от его этиологии (2b; B); применение статинов является перспективным и должно быть изучено в клинических исследованиях III фазы (1b; A).
Профилактика декомпенсации
Е. А. Лялюкова, доктор медицинских наук, профессор
Что такое цирроз печени? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Цирроз печени (ЦП) — это хроническое дегенеративное заболевание печени, связанное с диффузным патологическим процессом, при котором нормальные клетки печени повреждаются, а затем замещаются рубцовой тканью, образуя избыточный фиброз и структурно-анатомические регенераторные узлы.
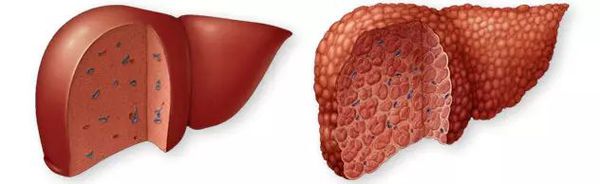
Этиология
По этиологическим характеристикам можно выделить:
- распространённые формы ЦП;
- редкие формы ЦП.
К распространённым относят вирусные (В, С, D), алкогольные и метаболические формы цирроза печени.
Редкими формами ЦП являются:
- аутоиммунные, лекарственные, токсические, первичные и вторичные билиарные циррозы;
- генетически обусловленные патологии — гемохроматоз (нарушение обмена железа), болезнь Вильсона — Коновалова, дефицит белка альфа-1-антитрипсина, гликогеноз IV типа (недостаток ферментов), галактоземия, наследственная тирозинемия и непереносимость фруктозы;
- нарушение венозного оттока из печени — венокклюзионные формы ЦП (болезнь Бадда — Киари);
- тяжёлая правожелудочковая сердечная недостаточность;
- флебопортальные циррозы (типа Банти).
Пути заражения
Заразиться циррозом печени нельзя. Однако, если он вызван вирусным гепатитом, то возбудитель может передаться через кровь, при половых контактах и от матери к ребёнку.
Основную роль в возникновении и развитии вирусного ЦП играют симптомные, малосимптомные и бессимптомные формы острого вирусного гепатита В, С, а также одновременное заболевание гепатитами В и D с последующим переходом в активный хронический вирусный гепатит. У большинства больных интервал между острым гепатитом С и клинически выраженными проявлениями ЦП превышает 30 лет. Только у мужчин, употребляющих более 50 г спирта в день, выраженные формы ЦП возникают через 13-15 лет.
Наиболее частыми причинами смерти больных ЦП является:
- большая печёночная недостаточность;
- кровотечение из варикозно расширенных вен пищевода;
- первичный рак печени;
- иммунопротективная недостаточность, влекущая за собой активизацию инфекционных (микробных) процессов, в первую очередь спонтанного бактериального перитонита и пневмонии, а также возникновение оксидативного стресса.
У больных в терминальной (заключительной) фазе заболеваний печени в основном наблюдаются декомпенсированные формы цирроза печени: асцит, варикозное расширение вен пищевода и желудка, энцефалопатия и желтуха.
Особенности цирроза печени у детей
Заболевание у детей встречается крайне редко и обычно связано:
- с аутоиммунным поражением печени;
- кардиогенными заболеваниями — лёгочной гипертензией и хронической сердечной недостаточностью;
- болезнью Бадда — Киари;
- врождёнными болезнями накопления — наследственным гемохроматозом, лизосомальными болезнями накопления, болезнью Вильсона — Коновалова;
- флебопортальным циррозом (типа Банти).
Прогноз у таких детей неблагоприятный, чаще всего они погибают, так как не успевают попасть к гепатологу и выяснить диагноз. Также они обычно страдают от множества сопутствующих болезней, в том числе от основного заболевания, ставшего причиной цирроза.
Проявления заболевания у детей и взрослых схожи. Единственный эффективный метод лечения цирроза у детей — это пересадка печени. Поэтому крайне важно вовремя диагностировать заболевание и встать в очередь на пересадку печени.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы цирроза печени
Цирроз печени в течение длительного времени может протекать латентно, т. е. бессимптомно.
Клиническая картина ЦП зависит от его формы и течения, активности основного заболевания, а также наличия или отсутствия печёночно-клеточной недостаточности, синдрома портальной гипертензии, холестаза и внепечёночных проявлений.
Основные общие симптомы, которые чаще всего встречаются при ЦП:
- повышенная утомляемость;
- похудение;
- нарушения сознания и поведения;
- ухудшение аппетита и чувство дискомфорта в животе;
- пожелтение кожи, белковых оболочек глаз и слизистой;
- осветление или обесцвечивание кала;
- потемнение мочи;
- болевые ощущения в животе;
- отёки;
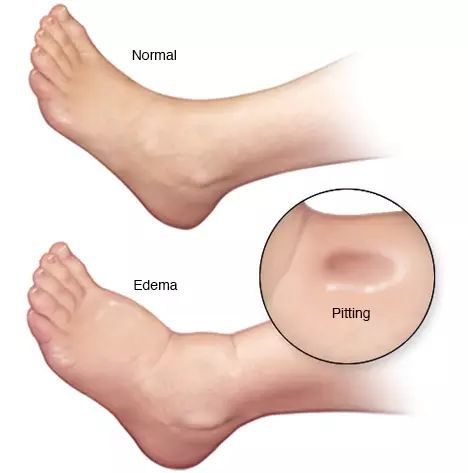
- асцит (скопление жидкости в брюшной полости);
- кровотечения из носа, желудочно-кишечного тракта, дёсен или геморроидальных узлов, а также подкожные кровоизлияния;
- часто возникающие бактериальные инфекции (например, органов дыхания);
- снижение полового влечения;
- кожный зуд.
Симптомы распространённых форм ЦП
При высокоактивном ЦП, кроме общей утомляемости, осветления стула и потемнения мочи, может возникать тупая боль в правом подреберье и вздутие живота.
Во время осмотра часто выявляют:
- субиктеричность (желтушность) склер;
- расширение вен брюшной стенки, напоминающее голову медузы;
- венозный шум при выслушивании в эпигастральной области живота (шум Крювелье — Баумгартена);
- серо-коричневатый цвет шеи;
- гинекомастию (увеличение грудных желёз);
- гипогонадизм (у мужчин);
- контрактуру Дюпюитрена (укорочение сухожилий ладоней).
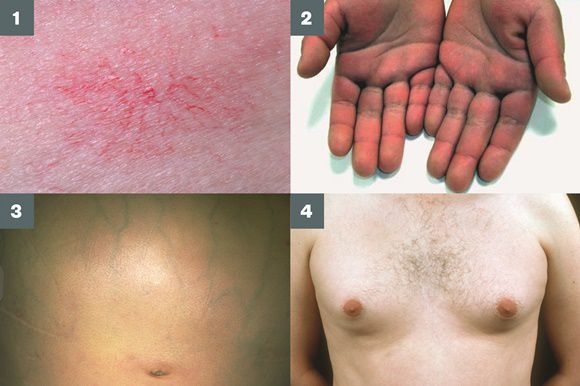
Три последних признака цирроза печени зачастую наблюдаются при алкогольных ЦП.
В области грудной клетки в 50-80% случаев наблюдаются телеангиэктазии кожи (расширения мелких сосудов), чаще при алкогольных ЦП. Пальпаторно печень отчётлива уплотнена, имеет неровный нижний край. Размеры печени различны — от значительного увеличения до уменьшения.
Часто при пальпации выявляется умеренно увеличенная селезёнка, причём её край может выступать из-под рёберной дуги на 1-3 см.
При развитии ЦП появляются симптомы белково-энергетической недостаточности, асцит, отёки, а также печёночный запах при тяжёлой печёночной недостаточности.
Симптомы при малоактивных и начальных стадиях ЦП
Данные формы ЦП зачастую протекают бессимптомно и выявляются в ходе периодических медицинских осмотров, диспансеризации, а также как случайная находка при обследовании пациента со смежной патологией или внепечёночными проявлениями.
При малоактивном ЦП, как правило, не возникают жалобы, связанные с печенью. Во время активного расспроса можно выявить весеннее снижение работоспособности, частые болезни, после которых возможны кровоточивость дёсен и потемнение мочи. Такие пациенты хуже, чем раньше, переносят длительные физические и нервно-психические нагрузки.
Желтухи и выраженного увеличения билирубина, за исключением периода интеркурентного острого гепатита, нет. Неяркая телеангиоэктазия кожи (сосудистые звёздочки) в области грудной клетки наблюдаются у 40-60% людей с ЦП.
Телеангиоэктазии кожи, плотная печень с фестончатым краем и умеренно увеличенная селезёнка — ценная клинико-диагностическая триада, которая с вероятностью 80-90% свидетельствует о ЦП или далеко зашедшем активном хроническом гепатите.
Патогенез цирроза печени
В основе патофизиологии цирроза лежит повреждение и некроз паренхимы (основной ткани) печени с деструкцией и гибелью гепатоцитов (клеток печени), а также системное поражение интерстициальной ткани.
При всех формах ЦП нарушается иммунологическое равновесие организма, преобладающими становятся аутоиммунные процессы: иммунная система человека принимает собственные клетки печени за чужеродные и повреждает их. В конечном итоге, это приводит к разрушению гепатоцитов и структуры печени в целом. Однако при этом каждая форма ЦП имеет свои патогенетические особенности:
- при вирусных гепатитах повреждающим агентом является сама вирусная частица, которая, размножаясь в клетке, разрушает её, вызывая цитолиз;
- при алкогольном ЦП прямое токсическое воздействие на мембраны гепатоцитов оказывает ацетальдегид с развитием алкогольной жировой болезни печени и алкогольного стеатогепатита;
- при метаболическом ЦП ведущую роль в патогенезе играет ожирение и сахарный диабет через стадию неалкогольного стеатогепатита с инсулинорезистентностью и последующей запрограммированной гибелью клеток печени.
В основе патогенеза более редких причин цирроза печени лежат ещё более частные механизмы развития повреждения и разрушения гепатоцитов и структуры печени:
- нарушение обмена и накопления железа при гемохроматозе;
- накопление меди при болезни Вильсона — Коновалова;
- окклюзия в системе воротной вены при гепатопортальном склерозе.
Цирроз формируется на протяжении многих лет. С течением времени происходят изменения генетического аппарата клеток печени, в результате чего появляются новые патологические клетки. Этот процесс в печени является иммуновоспалительным, он поддерживается чужеродными агентами, в роли которых могут выступать разные субстраты:
- вирус гепатита В;
- алкогольный гиалин;
- денатурированные белки;
- некоторые лекарственные средства;
- медьбелковые и железобелковые комплексы (ферритин).
В итоге повреждения паренхимы печени развивается гепатоцеллюлярная (печёночно-клеточная) недостаточность за счёт диффузного фиброза и трансформации ткани печени в анормальные узлы-регенераты. [3] [4] [5]
Классификация и стадии развития цирроза печени
В 1974 году на съезде гепатологов в Акапулько (Мексика) была принята единая морфологическая классификация, которую позже уточнили и несколько доработали эксперты ВОЗ. В настоящее время она является общепринятой.

Портальная гипертензия - повышение давления в венах брюшной полости вследствие нарушения венозного оттока через венозную систему печени. Следствием портальной гипертензии является варикозное расширение вен органов брюшной полости с истончением их стенок, что может привести к тяжелым кровотечениям, угрожающим жизни пациента.
Чаще всего портальная гипертензия развивается у больных с циррозом печени и является одним из факторов, приводящим к летальному исходу при данном заболевании. Для портальной гипертензии характерно расширение вен передней брюшной стенки, геморроидальных вен и вен пищевода. Печеночная недостаточность при циррозе печени приводит к недостаточной выработке белков свертывания крови, поэтому у этих пациентов повышенная кровоточивость. Этим обусловлена высокая летальность от кровотечений при портальной гипертензии. Даже при современном состоянии медицины летальность при кровотечении из варикозно расширенных вен составляет более 50%.
Лечение портальной гипертензии в Инновационном сосудистом центре
В Инновационном сосудистом центре для лечения портальной гипертензии применяются как классические операции по созданию сплено-ренальных анастомозов, так и экстренные эндоваскулярные операции трансъягулярного портокавального шунтирования (TIPS).
Эндоваскулярные операции выполняются на ангиографическом комплексе с дополнительным использованием визуализации воротной вены с помощью УЗИ навигации. Такие вмешательства проводятся под местной анестезией с внутривенной седацией.
Операции сплено-ренального анастомоза выполняются у сохранных пациентов, перенесших кровотечение из варикозно-расширенных вен пищевода. Такие вмешательства мы выполняем под наркозом через доступ в левой боковой стенке живота с переходом на грудную клетку. Подобные вмешательства позволяют избежать смертельно-опасных осложнений портальной гипертензии.
![При циррозе печени кровь скапливается в венах желудка, которые расширяются]()
Причины и факторы риска
Портальная гипертензия возникает, когда что-то препятствует кровотоку через печень, повышая давление внутри воротной вены. Эта обструкция (закупорка) может быть внутрипеченочной, подпеченочной (внепеченочной) или надпеченочной.
Внутрипеченочные причины портальной гипертензии
Основной причиной возникновения гипертензии является цирроз (в 70% случаев). Есть много причин возникновения цирроза, наиболее распространенной из них является злоупотребление алкоголем. Цирроз печени может вызвать обширный фиброз (рубцевание). Интенсивное рубцевание препятствует прохождению жидкостей через печень. Фиброз окружает сосуды в печени, что затрудняет кровообращение.
В качестве причины портальной гипертензии выступает большое количество болезней:
- Вирусный гепатит,
- Аутоиммунный гепатит,
- Фиброз печени,
- Опухолевый процесс в печени,
- Болезнь Вильсона, врожденное нарушение метаболизма меди,
- Гемохроматоз, избыточное накопление железа,
- Муковисцидоз, системное наследственное заболевание,
- Холангит, воспаление желчных протоков, связанное с инфекцией,
- Атрезия желчных путей, слабо образованные желчные протоки,
- Инфекции,
- Некоторые метаболические заболевания.
Подпеченочные причины портальной гипертензии
- Тромбоз воротной и селезёночной вены,
- Врожденные аномалии воротной вены, в частности атрезия,
- Сдавление воротной вены опухолью,
- Гематологические заболевания.
Надпеченочные причины портальной гипертензии
Эти причины вызваны обструкцией кровотока из печени в сердце и могут включать:
- Тромбоз печеночной вены, синдром Бадда-Киари,
- Травматический тромбоз нижней полой вены,
- Слипчивый перикардит, воспаление околосердечной сумки, характеризующееся увеличением проницаемости и расширением кровеносных сосудов.
Международные данные по распространенности портальной гипертензии неизвестны, хотя известно что 80% пациентов страдают от портальной гипертензии из-за внутрипеченочных причин, то есть цирроза печени.
Течение заболевания
Течение заболевания можно разбить на 4 стадии:
I стадия — начальная
Заболевание уже появилось, но ещё не может диагностироваться. Протекает бессимптомно, либо пациенты ощущают тяжесть в правом подреберье и легкое недомогание.
II стадия — умеренная
Появляются выраженные клинические симптомы заболевания. Боли в верхней половине живота, метеоризм, расстройства пищеварения (отрыжка, изжога, тяжесть в животе и т.д.), спленомегалия и гепатомегалия (увеличение печени).
III стадия — выраженная
Присутствуют все признаки и симптомы портальной гипертензии в резко выраженной форме.
IV стадия — стадия осложнений
Развивается напряженный асцит, плохо поддающийся терапии, повторяющиеся кровотечения, а также возможные осложнения.
Осложнения
Основные осложнения: желудочно-кишечные кровотечения, асцит и печеночная энцефалопатия (печеночная недостаточность, комплекс психических, нервных и мышечных нарушений).
Спленомегалия часто вызывает анемию, низкие показатели лейкоцитов и низкие показатели тромбоцитов.
Общими осложнениями, связанными с портальной гипертензией, являются аспирационная пневмония, сепсис, почечная недостаточность, кардиомиопатия, аритмии и гипотония.
Портальная гипертензия является опасным заболеванием, поскольку может вызвать кровотечение. Во многих случаях эпизоды кровотечения считаются неотложными медицинскими ситуациями, потому что смертность от варикозных кровотечений составляет около 50%. Варикоз пищевода очень распространен у людей с прогрессирующим циррозом, и считается, что у каждого из трех человек с варикозом развивается кровотечение.
Прогноз
Портальная гипертензия является осложнением основного заболевания печени. Это заболевание часто можно контролировать, а выживаемость зависит от сохранения функций печени. Чем хуже печень выполняет свои функции, тем хуже прогноз.
Более высокие показатели смертности и заболеваемости у пациентов с тяжелым и стойким желудочно-кишечным кровотечением. Смертность пациентов с диагнозом варикозного расширения вен пищевода составляет 30%.
Пациенты, которые имели хотя бы один эпизод кровотечения из-за варикоза пищевода, имеют 80% шансов повторного кровотечения в течение 1 года. У пациентов с варикозом пищевода осложнения иммунных, сердечно-сосудистых и легочных систем способствуют примерно 20-45% смертей.
Преимущества лечения в клинике
Диагностика
Когда кровь не может легко протекать через печень, она пытается обойти портальную систему, используя венозную систему, чтобы вернуться к сердцу. Возникают осложнения, связанные со снижением кровотока через печень и повышенным давлением внутри вен, что приводит к расширению вен. Варикоз может возникать в пищеводе, желудке и прямой кишке.
Когда кровь пытается найти другой путь к сердцу, открываются новые кровеносные сосуды. Среди них те, которые проходят вдоль стенки верхней части желудка и нижнего конца пищевода. Эти вены могут кровоточить. Кровотечение может быть мягким, в этом случае анемия является наиболее распространенным симптомом; либо серьезным, сопровождающееся кровавой рвотой или меленой (черным, смолистым стулом, который появляется из-за кровотечения из верхних отделов желудочно-кишечного тракта). Варикоз пищевода и желудка может привести к кровотечениям, угрожающим жизни.
Брюшная водянка — избыточное скопление жидкости внутри брюшины, обусловленное сочетанием факторов, включая повышенное давление в портальной системе, застой крови и уменьшение уровня белка в крови. Асцит может достигать огромных размеров, сдавливая диафрагму и мешая нормальному дыханию.
Обратимое расстройство нервной и психической деятельности при заболеваниях печени. Проявляется спутанностью сознания, раздражительностью и сонливостью из-за накопления токсических веществ из-за неспособность печени адекватно фильтровать их.
Увеличение селезенки основной симптом при внепеченочной гипертензии, часто сопровождается анемией и тромбоцитопенией (низким уровнем тромбоцитов в кровотоке).
Снижение количества лейкоцитов в крови увеличивает риск инфицирования. Спонтанный бактериальный перитонит наиболее частое инфекционное заболевание, сопровождающее цирроз и печеночную гипертензию. Сопровождается ознобом, лихорадкой и болью в животе.
Портальная гипертензия является опасным осложнением многих заболеваний печени и несет значительные риски для жизни. Диагностика данного заболевания основана на клинических данных, результатах ультразвуковых и эндоскопических исследований желудка.
Лабораторные исследования позволяют оценить функцию печени и почек, что влияет на прогноз заболевания. С целью подготовки к возможному вмешательству при портальной гипертензии используются методы визуализации сосудов воротной системы. Нами используются методы компьютерной томографии и магнито-резонансной диагностики вен брюшной полости.
В клинике применяются следующие диагностические методы:
Лечение
Лечение портальной гипертензии представляет собой сложную задачу. Сложность связана с тем, что развивающаяся печеночная недостаточность обуславливает плохую переносимость тяжелых сосудистых вмешательств. Однако в нашей клинике отработали технологии лечения портальной гипертензии с низким риском для жизни пациента.
Операции по поводу кровотечений из вен портальной системы
При кровотечениях из варикозно-расширенных вен пищевода нередко применяются методы прямого хирургического гемостаза - прошивание кровоточащих вен после рассечения желудка. Такие операции, выполняемые на фоне кровотечения, часто заканчиваются неблагоприятно для пациента. Летальность после таких операций составляет не менее 40%. Иногда общие хирурги дополняют эту операцию спленэктомией, исходя из соображений уменьшения притока крови из-за перевязки селезеночной артерии.
Специальный двухкомпонентный зонд позволяет плотно сжать верхний отдел желудка и нижний отдел пищевода, придавив расширенные вены. Наряду с другими мероприятиями (переливанием плазмы, крови и гемостатических препаратов) позволяет остановить тяжелое желудочно-кишечное кровотечение. Остановка кровотечения не устраняет его причины, поэтому неизбежен рецидив. Но использование этого зонда позволяет отложить вмешательство на портальной системе на более спокойный период и провести его в плановом порядке. Держать зонд в раздутом состоянии рекомендуется не более 6 часов, после чего распускать его на час. Общая продолжительность использования не должна превышать более 2 суток.
- Эмболизация вен пищевода и селезеночной артерии
Эндоваскулярная технология остановки кровотечения из варикозно-расширенных вен пищевода. Редко выполняется как самостоятельное вмешательство, так как требует чреспеченочного доступа, однако применяется совместно с созданием транспеченочного портокавального анастомоза (TIPS). В просвет варикозно-расширенных вен вводятся спирали и микроэмболы, которые блокируют кровоток в кровоточащих сосудах и способствуют остановке кровотечения.
Современный высокотехнологичный метод лечения портальной гипертензии, применяемый в экстренном порядке или как подготовка к пересадке печени. Смысл вмешательства заключается в создании искусственного соустья между ветвями воротной вены в толще печени и печеночной веной из системы нижней полой. В результате улучшается отток из воротной системы и снижается давления в варикозно-расширенных венах пищевода. Кровотечение быстро останавливается.
Российский научный центр хирургии им. Б.В. Петровского, РАМН
Российский научный центр хирургии им. Б.В. Петровского, РАМН
Российский научный центр хирургии им. акад. Б.В. Петровского РАМН, Москва
Российский научный центр хирургии им. Б.В. Петровского, РАМН
Российский научный центр хирургии им. акад. Б.В. Петровского РАМН, Москва
Современное состояние проблемы хирургического лечения больных портальной гипертензией
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2013;(2): 30-34
Шерцингер А. Г., Жигалова С. Б., Лебезев В. М., Манукьян Г. В., Киценко Е. А. Современное состояние проблемы хирургического лечения больных портальной гипертензией. Хирургия. Журнал им. Н.И. Пирогова. 2013;(2):30-34.
Shertsinger A G, Zhigalova S B, Lebezev V M, Manuk'ian G V, Kitsenko E A. Surgical treatment of portal hypertension: the state of art. Pirogov Russian Journal of Surgery = Khirurgiya. Zurnal im. N.I. Pirogova. 2013;(2):30-34. (In Russ.).
Российский научный центр хирургии им. Б.В. Петровского, РАМН





Статья посвящена одной из актуальных тем хирургии - лечению и профилактике кровотечений портального генеза. В последние годы отмечается рост числа диффузных заболеваний печени и хронических миелопролиферативных заболеваний крови, которые лежат в основе формирования синдрома портальной гипертензии и развития его осложнений. Авторы подробно описали современные подходы к лечению больных с этим тяжелым заболеванием. Предложенная тактика является дифференцированной. Способ лечения выбирается с учетом формы портальной гипертензии, функционального состояния печени, неотложности ситуации и тяжести кровопотери, локализации и степени варикозного расширения вен, состояния центральной гемодинамики, наличия сопутствующих заболеваний. Показано место малоинвазивных методов в алгоритме лечения. Доказана целесообразность разработки единой программы лечения больных портальной гипертензией в условиях специализированных клиник.
Российский научный центр хирургии им. Б.В. Петровского, РАМН
Российский научный центр хирургии им. Б.В. Петровского, РАМН
Российский научный центр хирургии им. акад. Б.В. Петровского РАМН, Москва
Российский научный центр хирургии им. Б.В. Петровского, РАМН
Российский научный центр хирургии им. акад. Б.В. Петровского РАМН, Москва
В последние годы стал очевидным факт увеличения количества больных портальной гипертензией. Если в 2006 г. в клинике находились на лечении
294 больных, то в 2011 г. - уже 365 больных.
Наблюдается рост количества больных внепеченочной портальной гипертензией за счет увеличения хронических миелопролиферативных заболеваний крови и тромбофилий [4]. Увеличивается число больных вирусным и алкогольным циррозом печени [7, 11, 18, 27, 29].
Основной причиной смерти больных портальной гипертензией являются кровотечения из варикозно-расширенных вен (ВРВ) пищевода и желудка. Известно, что летальность вследствие первого кровотечения составляет от 40 до 70% [1, 15, 20, 22, 25, 28, 32, 34, 35].
За многолетний период работы отделения экстренной хирургии и портальной гипертензии тактика лечения больных портальной гипертензией неоднократно пересматривалась. В первый период работы основным хирургическим пособием было прямое портокавальное шунтирование. Значительное количество послеоперационных осложнений в виде шунтовой энцефалопатии и высокая летальность заставили пересмотреть хирургическую тактику. Внедрение самых разнообразных операций азигопортального разобщения, таких как операции
М.Д. Пациоры, Берема-Крайля, Таннера, Сигиура, резекция пищевода и кардиального отдела желудка, позволило снизить процент гепатогенной энцефалопатии. Наряду с этим отмечено увеличение рецидивов пищеводно-желудочных кровотечений в отдаленном периоде наблюдения и летальности в ближайшем послеоперационном периоде вследствие увеличения количества гнойно-септических осложнений из-за большого и травматичного объема оперативных вмешательств [1, 8, 11] .
За последние годы, несмотря на увеличение количества тяжелобольных, прослеживается тенденция снижения летальности. Рациональный выбор вмешательства в зависимости от функционального состояния печени и локализации ВРВ, по отчетам работы отделения экстренной хирургии и портальной гипертензии, позволил снизить летальность за последние 5 лет при циррозе печени с 18,0 до 9,7% в группе больных с внепеченочной портальной гипертензией - с 4,8 до 1,1%.
На наш взгляд, снижение летальности связано с внедрением в клиническую практику новых малоинвазивных эндоскопических технологий. Доля эндоскопических вмешательств (лигирования и склерозирования) среди всех методов лечения за последние годы возросла с 52 до 63%. Внедрение методик эндоскопического лигирования и склерозирования послужило основанием для отказа от тяжелых травматичных операций, что положительно сказалось на результатах лечения.
Снижение летальности на фоне увеличения доли эндоскопических вмешательств наглядно демонстрирует приоритет эндоскопических методик в лечении ВРВ пищевода и желудка. Эндосклеротерапия и эндоскопическое лигирование стали широко применяться для остановки и профилактики кровотечений из ВРВ пищевода и желудка [2, 7, 12, 21, 23, 24, 26].
Анализ опыта работы предыдущих лет позволил сформулировать оптимальную, на наш взгляд, тактику, в которой четко разработаны показания к выбору того или иного способа хирургического или эндоскопического вмешательства. При этом в обязательном порядке учитываются форма портальной гипертензии, функциональное состояние печени у больных циррозом, неотложность ситуации и тяжесть кровопотери, локализация и степень ВРВ по данным эндоскопического обследования, состояние центральной и портальной гемодинамики; наличие сопутствующих заболеваний.
Выбор метода лечения больных внепеченочной портальной гипертензией
Первичная внепеченочная портальная гипертензия
У больных с врожденной аномалией развития воротной вены приоритетным является наложение любого вида сосудистого анастомоза (спленоренального или мезентерико-кавального; рис. 1, 2 и далее на цв. вклейке). Рисунок 1. Дистальный спленоренальный анастомоз W. Warren. Рисунок 2. Парциальный мезентерико-кавальный анастомоз с синтетической вставкой из политетрафторэтилена. Выполнение этой операции решает все проблемы с кровотечениями из ВРВ пищевода и желудка. Особенно хорошие результаты отмечены при портокавальном шунтировании в детском возрасте. После операции больные подлежат контрольному эндоскопическому обследованию с периодичностью 1 раз в 2 года, при котором хорошая функция анастомоза констатируется в случае исчезновения ВРВ. Эти пациенты практически здоровы и трудоспособны [5, 10].
Вторичная (приобретенная) внепеченочная портальная гипертензия
Данный контингент на 30% состоит из больных хроническими миелопролиферативными заболеваниями крови, на 60% - из больных наследственной (мутации генов свертывающей и противосвертывающей системы крови) или приобретенной (активация системы гемостаза при наличии провоцирующих факторов) тромбофилией. Остальные 10% приходятся на больных сегментарной внепеченочной портальной гипертензией на фоне изолированной окклюзии селезеночной вены.

Операцией выбора при тотальном тромбозе портальной системы является азигопортальное разобщение: операция М.Д. Пациоры с обязательной перевязкой всех коммуникантных вен желудка по большой и малой кривизне (рис. 3). Рисунок 3. Операция М.Д. Пациоры в сочетании с деваскуляризацией желудка.
Через 3-6 мес после операции при эндоскопическом контроле решается вопрос о необходимости выполнения эндоскопического лигирования ВРВ пищевода, оставшихся вне зоны открытой операции [8].
Все изложенное относится только к плановой ситуации. При развитии профузного кровотечения после верификации источника кровотечения первичный гемостаз достигается зондом-обтуратором, проводится трансфузионная терапия, желудок отмывается от крови. После этого выбирается вариант окончательного гемостаза в зависимости от распространенности ВРВ и локализации источника кровотечения. При локализации источника геморрагии в пищеводе возможно эндоскопическое лигирование, при подтекании крови в субкардии после удаления зонда Блейкмора хорошо зарекомендовало себя эндоскопическое склерозирование. Наличие больших стволов ВРВ в желудке, а также рецидив кровотечения после эндоскопического гемостаза в течение 1 сут являются показаниями к срочному хирургическому вмешательству - гастротомии с прошиванием ВРВ желудка и нижней трети пищевода. Не рекомендуется расширять объем оперативного вмешательства в экстренной ситуации и выполнять деваскуляризацию желудка. Цель операции - только гемостаз [2].
Сегментарная портальная гипертензия
Выбор метода лечения больных с изолированной окклюзией селезеночной вены, развитием порто-портальных анастомозов через фундальный отдел желудка и в экстренной и плановой ситуации однозначен - это спленэктомия. Проведение консервативных мероприятий, таких как тампонада зондом-обтуратором в момент кровотечения, бывает неэффективным. Риск развития кровотечения у больных изолированным ВРВ желудка очень высок. По данным S. Sarin и соавт. (2010), представленным на Согласительной конференции по портальной гипертензии, он составляет 78%, по нашим данным - 56,5% [19].
Все попытки эндоскопического гемостаза у больных изолированным ВРВ дна желудка в нашем исследовании потерпели неудачу. Склеротерапия варикозных узлов диаметром 12-15 мм окончилась рецидивом кровотечения. Введение 30-40 мл склерозанта паравазально не прерывает кровотока по варикозно-измененным венам. Во время гастротомии у больного после случайного прокалывания иглой блокированного сосуда произошло струйное кровотечение.
Эндоскопическое лигирование также оказалось малоэффективным. Так как диаметр латексных колец и нейлоновых петель не превышает 13 мм, основной проблемой при выполнении эндоскопического лигирования ВРВ дна желудка является неполный захват вены, кроме того, желудочный сок действует на латекс, что в конечном итоге приводит к раннему отторжению лигатур. Известны рекомендации японских авторов применять при лигированиии большую нейлоновую петлю с внутренним диаметром 4 см при захвате периферической части узла щипцами через второй канал эндоскопа [31, 35]. Однако они не нашли практического применения, так как стандартный лигатор не приспособлен для работы с таким диаметром петли.
Самым надежным методом профилактики кровотечения, позволяющим окончательно решить проблему сегментарной портальной гипертензии, является спленэктомия. Мы провели анализ лечения 23 больных сегментарной внепеченочной портальной гипертензией и варикозным расширением вен свода желудка, которым была выполнена спленэктомия. В 3 наблюдениях операцию дополнили дистальной резекцией поджелудочной железы при верификации опухоли дистального отдела поджелудочной железы. У 2 больных спленэктомия сочеталась с гастротомией, так как большой дефект на вене в своде желудка являлся источником продолжающегося кровотечения.
Выполнение операции М.Д. Пациоры без сплен- эктомии больным сегментарной портальной гипертензией дает кратковременный гемостатический эффект. Как показал наш опыт, после прошивания ВРВ свода желудка рядом с лигированными венами возникают новые узлы, что не позволяет решить проблему окончательного гемостаза. Данное явление легко объяснить. Прошивание ВРВ свода желудка перекрывает кровоток от селезенки, что ведет к образованию новых варикозных узлов в подслизистом слое.
Из 23 больных 22 были выписаны из клиники в удовлетворительном состоянии. Умер один больной, страдающий наследственной тромбофилией, от тромбоза легочных сосудов на 9-й день после спленэктомии. Это обстоятельство делает необходимым контроль коагулограммы и количества тромбоцитов после спленэктомии в ближайшем и отдаленном периодах, особенно у больных хроническими миелопролиферативными заболеваниями крови и тромбофилией. Летальность в этой группе больных составила 4,3%. Трехлетний период наблюдения за этими больными демонстрирует 100% гемостатический эффект и выживаемость.
Тактика лечения больных циррозом печени

Выбор метода лечения таких больных базируется на функциональном состоянии печени и наличии или отсутствии кровотечения. Всех больных мы разделили на 5 групп согласно критериям Г.В. Манукьяна [11] (см. таблицу).
Больные циррозом печени в компенсированной стадии подлежат профилактическому шунтированию, а именно выполнению дистального спленоренального или дозированного мезентерико-кавального анастомоза с диаметром синтетической вставки 9 мм. При невозможности выполнения декомпрессивного шунтирования следует производить операцию азигопортального разобщения с максимально возможной деваскуляризацией желудка [13, 17].
Основная масса больных группы В не переносит наложения портокавального анастомоза. Выбор метода лечения зависит от локализации и размера ВРВ. При локализации таких вен изолированно в пищеводе преимущества имеют эндоскопические методики, а именно эндоскопическое лигирование вен пищевода. При выявлении гастроэзофагеальных вен I типа альтернативой операции азигопортального разобщения является комбинированное эндоскопические лигирование ВРВ пищевода и желудка. В выборе преимущественного метода лечения определяющим является размер ВРВ [33].
При наличии гастроэзофагеальных вен II типа с формированием венозных конгломератов больших размеров выполнение эндоскопического лигирования чревато развитием большого количества осложнений. Приоритет в данном случае принадлежит операции азигопортального разобщения - гастротомии с прошиванием ВРВ желудка и дистального отдела пищевода в сочетании с полной деваскуляризацией желудка по большой и малой кривизне.
Выявление эктопических ВРВ желудка IV типа предусматривает выжидательную тактику - динамическое эндоскопическое наблюдение вследствие того, что вены этой локализации крайне редко осложняются кровотечением [6].
Ранее проведенные в клинике исследования еще раз подтвердили точку зрения, что при декомпенсированном циррозе печени в плановом порядке следует применять профилактические малоинвазивные методы лечения. Оперативное лечение для них непереносимо [3].
Развитие пищеводно-желудочного кровотечения делает условным распределение на группы по классификации Чайлда-Пью. Многие больные на фоне кровопотери переходят в низший класс, при этом выполнение оптимального лечения становится невозможным [11, 14].
Применение зонда-обтуратора и эндоскопических вмешательств с целью достижения первичного гемостаза позволяет отсрочить рецидив кровотечения и подготовить больного к более радикальному вмешательству. Отсутствие результатов от проводимого лечения диктует необходимость экстренного хирургического вмешательства - операции М.Д. Пациоры [2, 14].
Наиболее проблематичной при кровотечении, по нашему мнению, является группа больных субкомпенсированным циррозом печени.
При планировании профилактической операции больным этой группы большое значение имеет функциональный резерв организма. Нередко адекватно проведенное предоперационное лечение нормализует показатели функции печени, что позволяет отнести больных к группе А и соответственно выполнить шунтирующую операцию [11, 14].
Судьбу больного субкомпенсированным циррозом печени определяют сроки проведения гемостаза и лечение печеночной недостаточности. Алгоритм выбора метода лечения при пищеводно-желудочных кровотечениях остается таким же, как и в плановой группе В.
Тяжелая кровопотеря, промедление с проведением лечебных действий приводят больных в состояние печеночной недостаточности и комы. Эндоскопическое склерозирование источника кровотечения, выполненное своевременно, дает хороший результат, позволяет вывести больных из тяжелого состояния и подготовить их к более радикальному вмешательству, т.е. эндоскопические технологии в группе В-С являются основными мерами лечения и профилактики кровотечений из ВРВ пищевода и желудка [1, 6, 9, 30, 31].
В случае развития кровотечения у больных с декомпенсированным течением цирроза печени методом выбора должна быть только консервативная тактика, основу которой составляют тампонада ВРВ зондом-обтуратором, проведение грамотной инфузионно-трансфузионной терапии с учетом показателей центрального венозного давления, а также назначение гепатотропного и дезинтоксикационного лечения.
Выполнение эндоскопических вмешательств в этой группе больных приводит к развитию большого количества геморрагических осложнений на фоне исходной белково-энергетической недостаточности и кровопотери.
Дистрофические изменения миокарда, сердечная недостаточность и гипокинетический тип центральной гемодинамики у больных декомпенсированным циррозом печени приводят к застою в непарной и полунепарной венах, что усугубляет нарушение оттока крови из портальной системы. Выполнение любых вмешательств, в том числе малоинвазивных, в такой ситуации не имеет перспектив достижения стойкого гемостаза [2, 12, 16].
Таким образом, внедрение малоинвазивных эндоскопических вмешательств радикальным образом повлияло на результаты лечения больных с синдромом портальной гипертензии, но, несмотря на малоинвазивность, следует строго придерживаться наработанных установок при выполнении этих процедур. Разработка единой программы лечения больных портальной гипертензией возможна только в специализированных клиниках.
Читайте также:


