Реферат на тему раневая инфекция
Обновлено: 02.07.2024
Анаэробная раневая инфекция — инфекция с быстро прогрессирующим некрозом мягких тканей, обычно сопровождается образованием газа и тяжёлой интоксикацией; наиболее грозное и опасное осложнение ран любого генеза.
Этиология. Возбудители — Clostridium perfringens, Clostridium novyi (Clostridium oedematiens), Clostridium septicum, Clostridium histolyticum.
Предрасполагающие факторы • Обширные размозжения тканей, огнестрельные и оскольчатые ранения с обширными повреждениями, загрязнённые землёй и обрывками одежды • Местные или общие нарушения кровообращения: тугая повязка, перевязка или тромбоз сосудов, тяжёлая кровопотеря • Первичная хирургическая обработка сильно загрязнённой раны, выполненная позднее 6 ч с момента ранения • Неадекватно выполненная первичная хирургическая обработка раны • Пониженная реактивность организма: переутомление, истощение, длительное голодание, переохлаждение, лечение ГК.
Классификация • Преимущественное поражение мышц (клостридиальный миозит, классическая форма) • Преимущественное поражение подкожной клетчатки и соединительной ткани (клостридиальный целлюлит, или отёчно-токсическая форма) • Смешанная форма — в патологический процесс вовлечены все виды мягких тканей.
Клиническая картина • Инкубационный период — от 3–6 ч до 1–2 сут; молниеносные формы могут привести к смертельному исходу в течение первых двух дней • Основная жалоба: постоянно усиливающиеся непереносимые давящие боли в повреждённой области. Если больной получал наркотические анальгетики, болевой синдром может отсутствовать • Состояние пострадавшего прогрессивно ухудшается, что проявляется резкой слабостью, бледностью кожных покровов, усиленным потоотделением, чувством беспокойства. Частота пульса быстро нарастает, АД падает, температура тела остаётся неизменной или иногда повышается, сознание спутанное, бред. Развивается септический шок • Рана резко болезненна; нет гиперемии и гноетечения, характерных для других инфекционных процессов; серый налёт на поверхности раны; отделяемое серозное, жёлто-коричневого цвета с неприятным сладковато-гнилостным запахом. Возможно образование булл, заполненных геморрагическим содержимым. Прогрессивно увеличивается отёчность тканей, зона некроза расширяется. Позже, при пальпации краёв раны появляется крепитация.
Методы исследования • Лабораторные показатели. Уменьшение Ht, увеличение содержания билирубина за счёт гемолиза эритроцитов, лейкоцитоз с относительной и абсолютной лимфопенией • Микроскопия мазков: крупные грамположительные палочки • Рентгенологическое исследование. Характерная перистость, вызванная расхождением мягких тканей (мышц, клетчатки) под действием образующихся газов.
Лечение • Хирургическое лечение — широкое рассечение раны в сочетании с удалением омертвевших тканей. Одновременно начинают вводить больше антибиотиков широкого спектра действия (т.к. возможно сочетание клостридиальной инфекции с другими аэробами и анаэробами), например цефалоспорин 3 поколения или клиндамицин в сочетании с аминогликозидом; хлорамфеникол, ампициллин+сульбактам. При клостридиальном миозите, целлюлите эффективен бензилпенициллин (10–20 млн ЕД/сут в/в). В особо запущенных случаях (при поражении газовой гангреной конечности) выполняют ампутацию • Гипербарическая оксигенация (при давлении кислорода — 3,03 кПа) • Серотерапия — применение противогангренозных сывороток. Поливалентная сыворотка содержит в одной ампуле анатоксины против трёх видов возбудителей газовой гангрены (по 10 000 МЕ против Clostridium perfringens, Clostridium oedematiens, Clostridium septicum). Моновалентные сыворотки содержат анатоксины только одного вида по 10 000 МЕ. Лечебная доза сывороток — 150 000 МЕ (по 50 000 МЕ каждого вида). Перед введением основной дозы проводят внутрикожную пробу сывороткой, разведённой 1:100 с целью выявления гиперчувствительности к белку. Профилактически, поливалентную сыворотку в дозе 30 000 МЕ вводят в максимально ранние сроки п/к и/или в/м.
Прогноз зависит от характера раневого процесса, его локализации, срока с момента получения травмы до начала проведения целенаправленной терапии, скорости распространения инфекционного процесса за пределы раны, вида возбудителя. Без лечения летальный исход неизбежен. Даже при лечении, смертность всё равно остаётся высокой — 25–40%.
Профилактика. Главные условия успешной профилактики газовой гангрены — удаление всех нежизнеспособных тканей и своевременная первичная хирургическая обработка раны.
Синонимы • Газовая гангрена • Флегмона коричневая
МКБ-10. A48.0 Газовая гангрена
Код вставки на сайт
Анаэробная раневая инфекция — инфекция с быстро прогрессирующим некрозом мягких тканей, обычно сопровождается образованием газа и тяжёлой интоксикацией; наиболее грозное и опасное осложнение ран любого генеза.
Этиология. Возбудители — Clostridium perfringens, Clostridium novyi (Clostridium oedematiens), Clostridium septicum, Clostridium histolyticum.
Предрасполагающие факторы • Обширные размозжения тканей, огнестрельные и оскольчатые ранения с обширными повреждениями, загрязнённые землёй и обрывками одежды • Местные или общие нарушения кровообращения: тугая повязка, перевязка или тромбоз сосудов, тяжёлая кровопотеря • Первичная хирургическая обработка сильно загрязнённой раны, выполненная позднее 6 ч с момента ранения • Неадекватно выполненная первичная хирургическая обработка раны • Пониженная реактивность организма: переутомление, истощение, длительное голодание, переохлаждение, лечение ГК.
Классификация • Преимущественное поражение мышц (клостридиальный миозит, классическая форма) • Преимущественное поражение подкожной клетчатки и соединительной ткани (клостридиальный целлюлит, или отёчно-токсическая форма) • Смешанная форма — в патологический процесс вовлечены все виды мягких тканей.
Клиническая картина • Инкубационный период — от 3–6 ч до 1–2 сут; молниеносные формы могут привести к смертельному исходу в течение первых двух дней • Основная жалоба: постоянно усиливающиеся непереносимые давящие боли в повреждённой области. Если больной получал наркотические анальгетики, болевой синдром может отсутствовать • Состояние пострадавшего прогрессивно ухудшается, что проявляется резкой слабостью, бледностью кожных покровов, усиленным потоотделением, чувством беспокойства. Частота пульса быстро нарастает, АД падает, температура тела остаётся неизменной или иногда повышается, сознание спутанное, бред. Развивается септический шок • Рана резко болезненна; нет гиперемии и гноетечения, характерных для других инфекционных процессов; серый налёт на поверхности раны; отделяемое серозное, жёлто-коричневого цвета с неприятным сладковато-гнилостным запахом. Возможно образование булл, заполненных геморрагическим содержимым. Прогрессивно увеличивается отёчность тканей, зона некроза расширяется. Позже, при пальпации краёв раны появляется крепитация.
Методы исследования • Лабораторные показатели. Уменьшение Ht, увеличение содержания билирубина за счёт гемолиза эритроцитов, лейкоцитоз с относительной и абсолютной лимфопенией • Микроскопия мазков: крупные грамположительные палочки • Рентгенологическое исследование. Характерная перистость, вызванная расхождением мягких тканей (мышц, клетчатки) под действием образующихся газов.
Лечение • Хирургическое лечение — широкое рассечение раны в сочетании с удалением омертвевших тканей. Одновременно начинают вводить больше антибиотиков широкого спектра действия (т.к. возможно сочетание клостридиальной инфекции с другими аэробами и анаэробами), например цефалоспорин 3 поколения или клиндамицин в сочетании с аминогликозидом; хлорамфеникол, ампициллин+сульбактам. При клостридиальном миозите, целлюлите эффективен бензилпенициллин (10–20 млн ЕД/сут в/в). В особо запущенных случаях (при поражении газовой гангреной конечности) выполняют ампутацию • Гипербарическая оксигенация (при давлении кислорода — 3,03 кПа) • Серотерапия — применение противогангренозных сывороток. Поливалентная сыворотка содержит в одной ампуле анатоксины против трёх видов возбудителей газовой гангрены (по 10 000 МЕ против Clostridium perfringens, Clostridium oedematiens, Clostridium septicum). Моновалентные сыворотки содержат анатоксины только одного вида по 10 000 МЕ. Лечебная доза сывороток — 150 000 МЕ (по 50 000 МЕ каждого вида). Перед введением основной дозы проводят внутрикожную пробу сывороткой, разведённой 1:100 с целью выявления гиперчувствительности к белку. Профилактически, поливалентную сыворотку в дозе 30 000 МЕ вводят в максимально ранние сроки п/к и/или в/м.
Прогноз зависит от характера раневого процесса, его локализации, срока с момента получения травмы до начала проведения целенаправленной терапии, скорости распространения инфекционного процесса за пределы раны, вида возбудителя. Без лечения летальный исход неизбежен. Даже при лечении, смертность всё равно остаётся высокой — 25–40%.
Профилактика. Главные условия успешной профилактики газовой гангрены — удаление всех нежизнеспособных тканей и своевременная первичная хирургическая обработка раны.
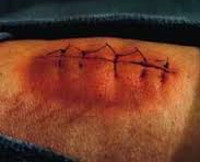
Раневая инфекция – это комплекс общих и местных патологических проявлений, возникающих при развитии инфекции в случайных или операционных ранах. Патология проявляется болью, ознобом, лихорадкой, увеличением регионарных лимфатических узлов и лейкоцитозом. Края раны отечные, гиперемированные. Наблюдается выделение серозного или гнойного отделяемого, в отдельных случаях образуются участки некроза. Диагноз выставляется на основании анамнеза, клинических признаков и результатов анализов. Лечение комплексное: вскрытие, перевязки, антибиотикотерапия.
МКБ-10
Общие сведения
Раневая инфекция – осложнение раневого процесса, обусловленное развитием патогенной микрофлоры в полости раны. Все раны, в том числе и операционные, как в гнойной хирургии, так и в травматологии считаются первично загрязненными, поскольку какое-то количество микробов попадает на раневую поверхность из воздуха даже при безукоризненном соблюдении правил асептики и антисептики. Случайные раны загрязнены сильнее, поэтому в таких случаях источником инфекции обычно является первичное микробное загрязнение. При операционных ранах на первый план выступает эндогенное (из внутренней среды организма) или внутригоспитальное (вторичное) инфицирование.

Причины
В большинстве случаев возбудителем инфекции в случайных ранах становится стафилококк. Редко в качестве основного возбудителя выступает протей, кишечная и синегнойная палочка. В 0,1% случаев встречается анаэробная инфекция. Через несколько дней пребывания в стационаре флора меняется, в ране начинают преобладать устойчивые к антибактериальной терапии грамотрицательные бактерии, которые обычно становятся причиной развития раневой инфекции при вторичном инфицировании как случайных, так и операционных ран.
Раневая инфекция развивается в случае, когда количество микробов в ране превышает некий критический уровень. При свежих травматических повреждениях у ранее здорового человека этот уровень составляет 100 тыс. микроорганизмов на 1 г ткани. При ухудшении общего состояния организма и определенных особенностях раны этот порог может существенно снижаться.
К числу местных факторов, повышающих вероятность развития раневой инфекции, относится присутствие в ране инородных тел, сгустков крови и некротических тканей. Также имеет значение плохая иммобилизация при транспортировке (становится причиной дополнительной травмы мягких тканей, вызывает ухудшение микроциркуляции, увеличение гематом и расширение зоны некроза), недостаточное кровоснабжение поврежденных тканей, большая глубина раны при малом диаметре раневого канала, наличие слепых карманов и боковых ходов.
Общее состояние организма может провоцировать развитие раневой инфекции при грубых расстройствах микроциркуляции (централизация кровообращения при травматическом шоке, гиповолемические расстройства), нарушениях иммунитета вследствие недостаточного питания, нервного истощения, химических и радиационных поражений, а также хронических соматических заболеваний. Особенно значимы в таких случаях злокачественные новообразования, лейкемия, уремия, цирроз, сахарный диабет и ожирение. Кроме того, снижение сопротивляемости инфекции наблюдается при проведении лучевой терапии и при приеме ряда лекарственных средств, в том числе – иммунодепрессантов, стероидов и больших доз антибиотиков.
Классификация
В зависимости от преобладания тех или иных клинических проявлений гнойные хирурги выделяют две общие формы раневой инфекции (сепсис без метастазов и сепсис с метастазами) и несколько местных. Общие формы протекают тяжелее местных, вероятность летального исхода при них повышается. Самой тяжелой формой раневой инфекции является сепсис с метастазами, который обычно развивается при резком снижении сопротивляемости организма и раневом истощении вследствие потери больших количеств белка.
К числу местных форм относятся:
- Инфекция раны. Является локализованным процессом, развивается в поврежденных тканях с пониженной сопротивляемостью. Зона инфицирования ограничена стенками раневого канала, между ней и нормальными живыми тканями есть четкая демаркационная линия.
- Околораневой абсцесс. Обычно соединен с раневым каналом, окружен соединительнотканной капсулой, отделяющей участок инфекции от здоровых тканей.
- Раневая флегмона. Возникает в случаях, когда инфекция выходит за пределы раны. Демаркационная линия исчезает, процесс захватывает прилежащие здоровые ткани и проявляет выраженную тенденцию к распространению.
- Гнойный затек. Развивается при недостаточном оттоке гноя вследствие неадекватного дренирования или зашивании раны наглухо без использования дренажа. В подобных случаях гной не может выйти наружу и начинает пассивно распространяться в ткани, образуя полости в межмышечных, межфасциальных и околокостных пространствах, а также в пространствах вокруг сосудов и нервов.
- Свищ. Образуется на поздних стадиях раневого процесса, в случаях, когда на поверхности рана закрывается грануляциями, а в глубине сохраняется очаг инфекции.
- Тромбофлебит. Развивается через 1-2 мес. после повреждения. Является опасным осложнением, обусловлен инфицированием тромба с последующим распространением инфекции по стенке вены.
- Лимфангит и лимфаденит. Возникают вследствие других раневых осложнений, исчезают после адекватной санации основного гнойного очага.
Симптомы раневой инфекции
Как правило, патология развивается спустя 3-7 дней с момента ранения. К числу общих признаков относится повышение температуры тела, учащение пульса, ознобы и признаки общей интоксикации (слабость, разбитость, головная боль, тошнота). В числе местных признаков – пять классических симптомов, которые были описаны еще во времена Древнего Рима врачом Аулусом Корнелиусом Сельсусом: боль (dolor), местное повышение температуры (calor), местное покраснение (rubor), отек, припухлость (tumor) и нарушение функции (functio laesa).
Характерной особенностью болей является их распирающий, пульсирующий характер. Края раны отечны, гиперемированы, в полости раны иногда имеются фибринозно-гнойные сгустки. Пальпация пораженной области болезненна. В остальном симптоматика может варьироваться в зависимости от формы раневой инфекции. При околораневом абсцессе отделяемое из раны нередко незначительное, наблюдается выраженная гиперемия краев раны, резкое напряжение тканей и увеличение окружности конечности. Образование абсцесса сопровождается снижением аппетита и гектической лихорадкой.
При раневых флегмонах выявляется существенное повышение местной температуры и резкое ухудшение состояния больного, однако рана выглядит относительно благополучно. Формирование гнойного затека также сопровождается значительным ухудшением состояния пациента при относительном благополучии в области раны. Температура повышается до 40 градусов и более, отмечаются ознобы, вялость, адинамия и снижение аппетита. Гнойное отделяемое отсутствует или незначительное, гной выделяется только при надавливании на окружающие ткани, иногда – удаленные от основного очага инфекции. При свищах общее состояние остается удовлетворительным или близким к удовлетворительному, на коже формируется свищевой ход, по которому оттекает гнойное отделяемое.
Осложнения
Осложнения обусловлены распространением инфекции. При гнойных тромбофлебитах общее состояние ухудшается, в зоне поражения определяются умеренные признаки воспаления, при расплавлении стенки вены возможно формирование флегмоны или абсцесса. Лимфангит и лимфаденит проявляются болезненностью, отечностью мягких тканей и гиперемией кожи в проекции лимфатических узлов и по ходу лимфатических сосудов. Отмечается ухудшение общего состояния, ознобы, гипертермия и повышенное потоотделение. При сепсисе состояние тяжелое, кожа бледная, наблюдается снижение АД, выраженная тахикардия, бессонница и нарастающая анемия.
Лечение раневой инфекции
Лечение заключается в широком вскрытии и дренировании гнойных очагов, а также промывании раны антисептиками. В последующем при перевязках используются сорбенты и протеолитические ферменты. В фазе регенерации основное внимание уделяется стимуляции иммунитета и защите нежных грануляций от случайного повреждения. В фазе эпителизации и рубцевания при больших, длительно незаживающих ранах выполняют кожную пластику.
Прогноз и профилактика
Прогноз определяется тяжестью патологии. При небольших ранах исход благоприятный, наблюдается полное заживление. При обширных глубоких ранах, развитии осложнений требуется длительное лечение, в ряде случаев возникает угроза для жизни. Профилактика раневой инфекции включает в себя раннее наложение асептической повязки и строгое соблюдение правил асептики и антисептики в ходе операций и перевязок. Необходима тщательная санация раневой полости с иссечением нежизнеспособных тканей, адекватным промыванием и дренированием. Пациентам назначают антибиотики, проводят борьбу с шоком, алиментарными нарушениями и белково-электролитными сдвигами.
Первичное микробное загрязнение раны реализуется в момент ранения. От нее нужно отличать вторичное микробное загрязнение, которое происходит при неаккуратном обращении с раной, отсутствии повязки или наличии нестерильной повязки.
Что же происходит с микробами попавшими в рану. Большая часть их погибает за счет фагоцитоза, а часть их приспосабливается. Через 1-2 недели в ране преобладает кокковая флора, так называемая микрофлора раны - эта та ассоциация микробов, которая осталась в ране спустя некоторое время после ранения вследствие естественного отбора.
Микробное загрязнением раны это еще не есть раневая инфекция.
Нагноение раны - это физиологическая мера организма, направленная на заживление раны; при нагноении раны микробы питаются мертвыми тканями, утилизируют их, вызывают развитие грануляций. Грануляции имеют мало форменных элементов, но имеют много сосудов, по которым прибывают фибробласты, которые затем становятся фиброцитами, составляющими основу рубцовой ткани.
От нагноения раны нужно отличать инфекции раны - результат взаимодействия микро - и макроорганизма, вызывающее воспаление и признаки общей реакции организма в виде болей, лихорадки, слабости, тошноты и соответствующей реакции крови. До сих пор эти термины часто смешиваются, а их необходимо различать.
Что же сопровождается инфекцию раны? Прежде всего, это гнйоно-резорбтивная лихорадка, характеризующаяся вечерними подъемами температуры тела и другими общими явлениями. Еще более грозное осложнение раневой инфекции это сепсис. Развивается в результате подавления ретикулоэндотелиальной системы. Лихорадка приобретает ремитирующий характер, в общем анализе крови наблюдается анемия, появление юных форм лейкоцитов. Развивается раневое истощение так называемая потеря гноя - это потеря больших количеств белка ( 120 г гноя = 10 белка), могут появляться гнойные метастазы. Реактивность падает настолько, что хирург вскрывает одни очаг, а в это время где-то в другом месте зреет другой очаг. Поэтому сейчас сепсис делят на две формы:
1. Сепсис без метастазов.
2. Сепсис с гнойными метастазами.
Местные формы инфекции.
Важной является профилактика раневой инфекции, которая должная совершаться на поле боя ( обработка краев раны, наложение асептической повязки, остановка кровотечения, даже с помощью жгута, транспортная иммобилизация). Но главная профилактика это проведение рациональной первичной хирургической обработки раны.
Существует военно-полевая хирургическая доктрина, которая гласит:
1. Все открытие огнестрельные повреждения микробно загрязненные и потенциально инфицированы.
2. Профилактикой является возможно ранняя первичная хирургическая обработка раны.
Первичная хирургическая обработка раны - это хирургическое вмешательство, направленное на предупреждение развития раневой инфекции и на восстановление разрушенных тканей.
Помощь на этапах медицинской эвакуации.
МПБ - иммобилизация (шины Дитерихса, шины Крамера).
МПП - введение антибиотиков, у слабых раненых переливание О(1) группы крови. В случае полного разможжения конечности проводится транспортная ампутация. Заполняется первичная медицинская карточка.
ОМедБ - операция первичной хирургической обработки раны по показаниям. Помещение раненых с анаэробной инфекцией в анаэробную палатку. При развитии гнойной инфекции раны выполняется вторичная хирургическая обработка раны - операция , направленная на ликвидацию развившейся раневой инфекции ( часто стафилококковая).
Однако после ранения нередко развивается анаэробная инфекция. Микроорганизмы вызывающие ее размножаются без доступа кислорода и сами образуют газы (газовая инфекция). Ранее называлась “бронзовая кожа”, самопроизвольная эмфизема, газовый нарыв и т.д.). микроорганизмы вызывающие анаэробное поражение открыты в 1894 году ( Вейнберг). В 1916 году (Себин) открыта Clostridium histoliticum.
Вообще же гноя при анаэробных инфекция не наблюдается, а выделяется водянистая жидкость. Замечено , что возбудители анаэробной инфекции могут обнаруживаться в 90% свежих случайных ран, инфекция развивается всего лишь у 1-2% лиц. То есть понятие анаэробной инфекции чисто клиническое.
Эти микробы выделяют экзотоксины, вызывающие сильную интоксикацию, эйфорию, бессонницу и пр. Развитию анаэробной инфекции способствует значительное разрушение тканей, особенно мягких; оказалось , что при огнестрельных переломах анаэробная инфекция развивается в 5 раз чаще. Также способствует наложение жгутов, массовое поступление раненных , осенне-зимний период, кровопотеря переутомление, наличие шока, загрязнение раны почвой. Летальность при анаэробной инфекции 15-50%.
1. По скорости распространения:
2. По клиническим проявлениям:
3. По глубине распространения
Инкубационный период короче, чем при гнойной инфекции, может встречаться молниеносные формы.
Начальные симптомы: боли в ране, нарастание отека ( симптом лигатуры Мельникова) конечности, конечность приобретает синюшную окраску, температура кожи понижается, частота пульса намного опережает температуру тела, изменения психики - эйфория, бессонница.
Кардиальные симптомы - появление подкожной эмфиземы ( покожная крепитация), желтушность кожи, мышцы в ране приобретают коричнево-красный цвет и не кровоточат.
Бактериологическое исследование не имеет решающего значения, главное - клиника.
Профилактика - своевременная и радикальная первичная хирургическая обработка раны.
К годы ВОВ встречался 0.6 - 0.7 на 100 тысяч раненых; летальность 75% в военное время, в мирное - 40-45%.
Возбудитель Clostridium tetani.
Патогенез - до конца не ясен. Считается, что возбудитель передвигается по нервной системе. Инкубационный период в среднем 2 недели, но может быть до 80 дней.
Начальный период - характеризуется 3 симптомами: тризм жевательной мускулатуры, ригидность затылочных мышц, дисфагия.
Период разгара болезни - те же симптомы и прибавляются судороги тонического характера, в особенности касающиеся крупных мышечных массивов (мышц спины). Опистотонус - больной стоит на затылке и пятках, плейростотонус - боковое искривление. Самое страшное это вовлечение в процесс дыхательной мускулатуры, когда развиваются апноэтические кризы - больной перестает дышать. В этом случае вводится литическая смесь:
Sol. Aminazini 2.5% - 2.0
Sol. Omnoponi 2% - 1.0
Sol. Promedoli 2% - 1.0
Sol. Dimedroli 1% - 2.0
Sol. Scopolamini 0.05% - 0.5
Эта смесь вводится внутримышечно 3-4 раза в сутки, а в тяжелых случаях показана миорелаксация с ИВЛ. Одновременно проводится лечение противостолбнячной сывороткой по 50 - 200 тыс антитоксических единиц внутривенно на физиологическом растворе 1 к 5. Питание через зонд антибиотики широкого спектра действия.
1. Для непривитых ранее вводится
а. 1 Мл анатоксина подкожно
б. Через 0.5 часа вводят 0.1 мл разведенной противостолбнячной сыворотки внутрикожно.
Через 20 минут смотрят папулу. Если она более 1 см, то реакция считается положительной и дальнейшее введение сыворотки делать не следует. При отрицательной реакции вводится 0.1 мл подкожно. Через 20 минут при отрицательной реакции общее введение сыворотки доводится до 3000 антитоксических единиц.
Инфекция у больных, раненых и пострадавших представляет собой реакцию организма на внедрение возбудителей. Далеко не всегда микробная контаминация (микробиологическое событие - МБС, микробное загрязнение) приводит к развитию инфекционного процесса. Это определяется целым рядом аспектов, в том числе типом и вирулентностью возбудителя, местным состоянием раны, иммунным статусом пациента и состоятельностью других компенсаторных реакций, особенно системы кровообращения. В качестве основных источников контаминации рассматривают внебольничную инфекцию, обитающую за пределами лечебного учреждения, микроорганизмы, представляющие естественный биоценоз организма человека и внутрибольничные или назокомиальные штаммы, находящиеся в среде обитания пациента (помещения, аппаратура и оснащение, персонал). В связи с тем, что госпитальные микроорганизмы являются длительно персистирующими в отделении, они обладают высокой степенью резистентности к используемым антимикробным химиопрепаратам. Этому процессу способствует неоправданно широкое назначение антибиотиков, недостаточные разовые и суточные дозы, нарушение правил асептики и антисептики, отсутствие эпидемиологического контроля и продуманной политики проведения эмпирической и этиотропной антибактериальной терапии.
Среди представителей раневой микробиоты наиболее часто встречаются:
грамположительные кокки (золотистый и эпидермальный стафилококки, А-, В-, С - и D-стрептококк и энтерококк, пневмококки);
грамположительные палочки (коринобактерии дифтерии);
грамотрицательные палочки - энтеробактерии (кишечная палочка, группа протея, клебсиелла, синегнойная палочка и др.);
Нередко микроорганизмы выступают в ассоциации со сменой "лидера" в составе раневой микробиоты непосредственно в процессе лечения. Это происходит и под воздействием антибактериальной терапии, когда лекарственная супрессия одних микроорганизмов приводит к размножению других.
МБС является начальным этапом развития инфекционных осложнений на местном уровне. В ответ на микробное загрязнение развивается местная воспалительная реакция. Она характеризуется всеми признаками воспаления, которое в данном случае имеет инфекционную природу.
Применительно к хирургической инфекции в качестве основных вариантов воспалительной реакции называют нагноение раны и собственно раневую инфекцию.
Нагноение раны представляет собой первую фазу раневого процесса, являясь закономерным составляющим воспаления по типу вторичного очищения в некротических тканях. Имеет место отграничение нежизнеспособных тканей. При отсутствии условий для оттока гноя создаются предпосылки для распространения воспаления инфекционного процесса за пределы мертвых тканей. Нагноение раны перерастает в раневую инфекцию. Отличительная особенность раневой инфекции - активное распространение (инвазия) процесса на жизнеспособные ткани. Следует считать, что в данном случае макроорганизм по тем или иным причинам неспособен локализовать микробную инвазию. Среди основных факторов, способствующих повышению риска инфекционных осложнений, называют возраст старше 60 лет, нарушения обмена и питания (ожирение, гипотрофия, сахарный диабет), нарушение систем противоинфекционной защиты (онкологические процессы, лучевая терапия, применение глюкокортикоидной терапии и т.д.), наркомания (в том числе алкоголизм), травматический шок, комбинированный характер поражения. Местные факторы, способствующие прогрессу инфекционного процесса, представлены большим объемом повреждения тканей, регионарными нарушениями перфузии. Основными клиническими проявлениями местных гнойных инфекционных осложнений являются флегмона, абсцесс и гнойный затек.
Аналогичная ситуация возникает и при других видах инфекционных осложнений, не связанных с хирургическими ранами или травмами. Частным вариантом инфекционных осложнений является катетерассоциированная инфекция. Это специальная форма локальной или генерализованной инфекции, возникающей на фоне нахождения в сосудистом русле катетера. Наиболее часто гнойно-воспалительный процесс возникает в месте прокола кожи, в катетерном тоннеле и окружающей его клетчатке, внутри собственно катетера и тромбах, образующихся на катетере. Среди факторов риска развития катетерассоциированных инфекционных осложнений выделяют нарушения асептики и других правил при установке катетера, подвижность его относительно кожи, несоблюдение персоналом правил при проведении инфузионно-трансфузионной терапии, болюсного введения лекарственных средств и ухода (перевязки, промывание, "гепариновый замок"), длительность нахождения, наличие у пациента бактериемии.
Любое из развивающихся в процессе проведения интенсивной терапии инфекционных осложнений (госпитальная пневмония, уроинфекция, инфицированные пролежни и т.д.) проходят этапы микробного загрязнения и местной воспалительной реакции.
При инвазивной и высокоинвазивной бактериальной инфекции, неспособности макроорганизма локализовать инфекционный очаг взаимодействие макро - и микроорганизма выходит за пределы местной воспалительной реакции. В характеристике таких состояний начинают играть важную роль следующие факторы микрофлоры: токсикогенность, инвазивность и патогенность. Токсикогенность - это способность вегетирующей флоры вырабатывать и выделять токсин. В зависимости от характера выработки токсины разделяют на экзотоксины, т.е. выделяемые микроорганизмами в процессе жизнедеятельности, и эндотоксины, накапливаемые в очаге при разрушении бактерии. Помимо токсинов интоксикационные эффекты микробной инвазии определяются ферментами. Последние нарушают структуру живых тканей, изменяют функциональную активность и метаболизм, приводя к образованию эндогенных токсических субстанций небактериального генеза, формируя фактор инвазивности и патогенности . Чем шире набор факторов патогенности у возбудителя, тем существенней нарушения жизнедеятельности организма пациента.
В определенных ситуациях организм не способен локализовать очаг. Попадание токсинов в кровь переводит процесс на системный уровень. Для характеристики таких состояний в 1992 г. на согласительной конференции Американской коллегии торакальных врачей и Общества интенсивной терапии сформулировано понятие системного ответа на воспаление (СОВ) или системной воспалительной реакции (СВР). Диагностика СОВ основывается на наличии у взрослого пациента с заболеванием или травмой следующих клинических симптомов: гипертермии выше 38 о С или ниже 36 о С, тахикардии выше 90 мин -1 , тахипноэ с частотой дыхания более 20 мин -1 , гиперлейкоцитозе свыше 12х10 9 или ниже 4х10 9 , или когда количество незрелых форм превышает 10%. Необходимость разделения микробиологического события и местной воспалительной реакции с клиническими признаками воспаления обусловлена различным значением упомянутых терминов. Первый из них отражает контаминацию тканей организма возбудителями, а второй - характеризует собственно реакцию организма в целом на инфекционный процесс.
2. Сепсис
При дальнейшем прогрессировании инфекционного процесса развивается состояние, называемое сепсисом. Сепсис как вариант генерализованного инфекционного заболевания описан достаточно давно. Вместе с тем его различные клинические манифестации, наблюдаемые при терапевтической, хирургической, гинекологической патологии, в неонаталогии и т.д., препятствовали формированию единых представлений о закономерностях возникновения и развития этого заболевания.
Сепсис, также как и системную воспалительную реакцию, следует считать результатом взаимодействия микро - и макроорганизма с отчетливой несостоятельностью последнего при избыточной микробной нагрузке. Организм при этом не способен стерилизовать свою внутреннюю среду на фоне высокой степени инвазивности, вирулентности и токсикогенности инфекции. Существующий септический очаг следует рассматривать как источник постоянного поступления интоксикантов (живых микроорганизмов, экзо - и эндотоксинов, других метаболитов) в системный кровоток. Аналогичная ситуация наблюдается и при формировании системного ответа на воспаление, однако там процесс не поражает органы, не имеющие прямой связи с очагом. При сепсисе же последовательно проявляется дисфункция, недостаточность и даже несостоятельность функциональных систем, обеспечивающих реакцию организма на имеющийся инфекционный очаг.
Классификация, предложенная согласительной комиссией, предполагает, что для постановки диагноза "сепсис" достаточно подтвердить факт микробного загрязнения и найти клиническое подтверждение развитию СОВ. В случае присоединении к признакам сепсиса синдрома полиорганной недостаточности (ПОН), состояние характеризуется как тяжелый сепсис ("сепсис-синдром").
Эти критерии, предложенные американским патологом Роджером Боном, вызвали широкую дискуссию, поскольку вступили в определенную конфронтацию с классическими представлениями о сепсисе. Последние утверждались на том, что при данной патологии как клинической форме инфекционного заболевания микробные очаги становятся местами бурного размножения и генерализации возбудителей с гематогенным и лимфогенным распространением и формированием отдаленных (септикопиемических) метастазов. В этой связи в основные критерии сепсиса входили высокая лихорадка и интоксикация, не исчезнувшие после санации очага, увеличение размеров селезенки, нарастающие явления полиорганной дисфункции, прогрессирующие истощение и белковая недостаточность, плотная бактериемия. Современные представления заключают, что все эти перечисленные критерии, безусловно, также характеризуют сепсис, однако постановка диагноза с их помощью просто запаздывает. Ранняя же констатация сепсиса как состояния, при котором велика опасность прорыва защитных барьеров с последующим развитием полиорганной недостаточности, пусть даже несколько преждевременная, позволяет максимально ускорить принятие стратегических и тактических решений по изменению лечебной тактики.
Правомочность такого подхода подтверждает и современная концепция патогенеза септического процесса, согласно которой основные патофизиологические реакции обусловлены не инфектом, а вызванной микробными токсинами системной воспалительной реакцией. Активация в ответ на чрезмерную микробную и токсиновую нагрузку системных защитных механизмов приводит к гиперпродукции медиаторов, которые вызывают и поддерживают воспалительную реакцию в условиях нарушения реактивности организма больного. Решающее значение приобретает возникновение условий, при которых организм не способен уничтожать микроорганизмы за пределами инфекционного очага. При этом происходит повышение активности циркулирующих иммунных комплексов. Последние не подвергаются адекватному разрушению и поглощению, а фиксируются на стенках лейкоцитов, эндотелиоцитов. Одновременно происходит активация протеолитических процессов с повышением концентрации лизосомальных ферментов и пептогидролаз. Продолжающаяся эндотоксическая агрессия приводит к снижению функциональных свойств макрофагов, угнетению гуморального иммунитета. Кроме всего прочего, септический очаг становится источником сенсибилизации организма с развитием механизмов поливалентной инфекционной аллергии в вариантах гипер - или гипоэргических анафилактоидных реакций. "Медиаторный пожар" приводит и к нарушениям в системе гемостаза и микроциркуляции. Первые из них укладываются в клинику ДВС-синдрома, который играет существенную роль в миграции, диссеминации и метастазировании микроорганизмов. Считается, что последние "путешествует" по организму именно на микросвертках и образуют новые очаги интоксикации. Одновременно с этим имеет место нарушение агрегационной способности эритроцитов, снижение их деформируемости, накопление патологических форм. Итогом совокупности описанных процессов является глубокое угнетение тканевого обмена, гиперкатаболизм с белковым истощением, дибаланс всех видов обмена. Практически нельзя назвать ни одного органа или системы, не вовлекаемых в септический процесс.
Диагностика сепсиса основывается на определении локализации септического очага, уточнении вида и характера возбудителей инфекции, а также путей генерализации, выраженности синдрома полиорганной недостаточности.
Одним из клинических признаков сепсиса является наличие очага септического процесса. В зависимости от его локализации выделяют мезенхимальную или флегмонозную форму, плевро-легочную, перитонеальную, билиарную, кишечную, ангиогенную формы, уросепсис. Вторым важным аспектом является констатация полиорганной недостаточности. При сепсисе критерии те же, наиболее принципиальными среди них являются:
а) для ЦНС - нарушение сознания менее 14 баллов по шкале комы Глазго, дезориентация, сонливость, спутанность сознания или возбуждение, неадекватность;
б) для системы дыхания - одышка с гипервентиляцией (респираторный алкалоз), клиника РДСВ, отек легких (в теминальной стадии);
в) для системы кровообращения - увеличение сердечного выброса сменяющееся депрессией миокарда, снижение МОК, гипотензия, тахикардия;
г) для системы выделения - олигурия (диурез 0,4, PaO2 / FiO2 40 в мин, ИВЛ > 3 дней при FiO2 > 0,4 и ПДКВ > 5 см вод. ст);
в) для системы кровообращения - гипотензия, АД 9 ). Рекомендуемый минимальный объем инфузионно-трансфузионной терапии составляет 1,5-2,0 л. Инфузию следует производить в центральную вену одновременно с мониторингом ЦВД, сердечного и минутного выброса, ДЗЛА, темпа диуреза. Волемическая поддержка создает благоприятный фон для применения сосудоактивных средств, из которых препаратом выбора следует считать дофамин, допамин, норадреналин, адреналин. Окончательный выбор препарата лучше осуществлять после получения данных, измеренных с помощью инвазивного мониторинга показателей центральной гемодинамики (катетер Swan-Ganz). Выбор препарата производят в зависимости от степени снижения контрактильной способности миокарда и выраженности вазоплегии. Одновременно это позволяет контролировать темп инфузионно-трансфузионной терапии, поскольку при отсутствии диуреза избыточное введение растворов может привести к гипергидратации, усугубить дыхательные расстройства. Использование коллоидных растворов следует ограничить (не более ½ общего объема), так как они могут накапливаться в интерстициальном пространстве и тем самым усиливать тканевую гипергидратацию. Критерием эффективности мероприятий по поддержанию сердечно-сосудистой системы является стабилизация интегральных показателей (АД, МОК), лучше в гипердинамическом режиме, восстановление удовлетворительного уровня микроциркуляции, диуреза. Гипердинамический тип кровообращения, достигаемый в опережающем режиме, позволяет компенсировать кислородную задолженность тканям, купировать последствия дыхательных расстройств и гиперметаболизма. С другой стороны, неэффективность перечисленных мер, сохранение недостаточности кровообращения является пусковым фактором для дополнительного повреждения органов и тканей с прогностически неблагоприятным исходом.
Следующий важный момент - поддержание адекватного газообмена. Нарушение дыхательных функции легких всегда наблюдается при септическом шоке. Различна степень выраженности этих нарушений. В зависимости от тяжести дыхательных расстройств используется кислородотерапия с помощью лицевой маски или носовых катетеров, неизвазивная механическая вентиляция легких, респираторная терапия с помощью современных аппаратов через интубационную (трахеотомическую) трубку. Основной задачей следует считать недопущение гипоксемии и гиперкапнии. Наиболее грозным осложнением септического шока является синдром острого повреждения легких. Применительно к септическому шоку принципиально важен выбор режимов и параметров респираторной терапии с минимальным негативным влиянием на гемодинамику.
Основной способ ограничения поступления микроорганизмов и токсических продуктов иного рода заключается в адекватном и своевременном дренировании септического очага. Данный шаг является важнейшим компонентом интенсивного лечения, позволяющим оборвать патологическую цепь событий. Отказ от оперативного вмешательства (дренирования) при установленном источнике септической интоксикации не позволяет надеяться на эффективность проводимой консервативной терапии.
Среди средств, которые снижают медиаторный ответ организма, ведущее место занимают иммуноглобулины. На сегодняшний день имеется опыт использования обогащенного иммуноглобулина G (Пентаглобина), обладающего максимальной эффективностью при инактивации эндотоксина грамотрицательных микроорганизмов. Средняя доза пентаглобина при септическом шоке составляет 5 мл/кг/сутки в течении 3 дней. Именно такая дозировка позволяет снизить выраженность токсикоза. Широкое использование пентаглобина ограничивает относительно высокая стоимость препарата. В настоящее время идет активная разработка моноклональных антител к цитокинам.
Использование методов экстракорпоральной гемокоррекции целесообразно для удаления токсических метаболитов и цитокинов, поддерживающих системную воспалительную реакцию после устранения причины генерализации инфекции. Методом выбора следует считать продленную гемофильтрацию (гемодиафильтрацию), применяемую тогда, когда собственные механизмы детоксикации оказываются несостоятельными.
Особенностью антибактериальной терапии септического шока является использование максимальных дозировок химиопрепаратов с широким спектром действия. Нередко при развитии септического шорка нет четких представлений относительно типа и вида возбудителей. В этой связи используют антибиотики резерва с доказанным эффектом относительно наиболее вероятных возбудителей шока - грамотрицательных микроорганизмов. С учетом временной ограниченности возможно применение деэскалационной схемы → назначение карбопенемов или цефалоспоринов IV поколения → получение результатов бактериологических исследований → назначение химиопрепаратов с более узким спектром действия. При подозрении на анаэробный характер инфекции дополнительно назначают метронидазол и клиндамицин.
Клиническими критериями эффективности проводимой интенсивной терапии септического шока принято считать улучшение уровня сознания, исчезновение периферического цианоза, уменьшение кожно-ректального градиента температур, уменьшение одышки, повышение адаптации к респиратору и повышение PaO2 , снижении тахикардии, стабилизация АД или сокращение темпа введения инотропов, восстановление МОК в гиперкинетическом режиме, рост общего периферического сопротивления, возрастание темпа диуреза.
Литература
1. "Неотложная медицинская помощь", под ред. Дж.Э. Тинтиналли, Рл. Кроума, Э. Руиза, перевод с английского д-ра мед. наук В.И. Кандрора, д. м. н. М.В. Неверовой, д-ра мед. наук А.В. Сучкова, к. м. н. А.В. Низового, Ю.Л. Амченкова; под ред.Д. м. н.В.Т. Ивашкина, Д.М. Н.П.Г. Брюсова; Москва "Медицина" 2001
2. Интенсивная терапия. Реанимация. Первая помощь: Учебное пособие / Под ред. В.Д. Малышева. - М.: Медицина. - 2000. - 464 с.: ил. - Учеб. лит. для слушателей системы последипломного образования. - ISBN 5-225-04560-Х
Читайте также:

