Реферат на тему эхокг в диагностике ибс
Обновлено: 07.07.2024
После первичных исследований врач строит план дальнейшего обследования и лечения больного, исходя из полученных первичных данных и априорной вероятности диагноза хронической ИБС (Таблица 4).
| Типичная стенокардия | Атипичная стенокардия | Боль некоронарного характера | ||||
| Возраст, лет | мужчины | женщины | мужчины | женщины | мужчины | женщины |
| 30—39 | 59 | 28 | 29 | 10 | 18 | 5 |
| 40—49 | 69 | 37 | 38 | 14 | 25 | 8 |
| 50—59 | 77 | 47 | 49 | 20 | 34 | 12 |
| 60—69 | 84 | 58 | 59 | 28 | 44 | 17 |
| 70—79 | 89 | 68 | 69 | 37 | 54 | 24 |
| >80 | 93 | 76 | 78 | 47 | 65 | 32 |
Если по результатам первичных исследований априорная вероятность хронической ИБС превышает 85% — дальнейшие исследования для уточнения диагноза можно не проводить, а приступать к стратификации риска осложнений и назначению лечения.
Если по результатам первичных исследований априорная вероятность хронической ИБС не превышает 15% — следует заподозрить функциональное заболевание сердца или некардиальные причины симптомов.
Пациентов с промежуточной априорной вероятностью ИБС (15—85%) направляют на дополнительные неинвазивные визуализирующие исследования (Таблица 5).
| Диагностика ИБС | ||
| Чувствительность (%) | Специфичность (%) | |
| Нагрузочная ЭКГ | 45—50 | 85—90 |
| Стресс-ЭхоКГ | 80—85 | 80—88 |
| Стресс-ОЭКТ | 73—92 | 63—87 |
| Стресс-ЭхоКГ с добутамином | 79—83 | 82—86 |
| Стресс-МРТ | 79—88 | 81—91 |
| Стресс-ЭхоКГ с вазодилататором | 72—79 | 92—95 |
| Стресс-ОЭКТ с вазодилататором | 90—91 | 75—84 |
| Стресс-МРТ с вазодилататором | 67—94 | 61—85 |
| МСКТ-ангиография КА | 95—99 | 64—83 |
| Стресс-ПЭТ с вазодилататором | 81—97 | 74—91 |
2.7.2. Нагрузочные ЭКГ-пробы
Нагрузочные пробы показаны всем пациентам с подозрением на стенокардию напряжения и априорной вероятностью ИБС 15—85%. Показания к проведению нагрузочных проб лицам с ранее установленным диагнозом ИБС: первоначальная и повторная стратификации риска осложнений, оценка эффективности медикаментозного и хирургического лечения.
Обычно проводят велоэргометрическую пробу (ВЭМ-проба) или тредмил-тест. Проба с ходьбой (тредмил-тест) более физиологична и чаще используется для верификации функционального класса пациентов с ИБС. Велоэргометрия информативнее при выявлении ИБС в неясных случаях, но при этом требует от пациента, как минимум, начальных навыков езды на велосипеде, труднее выполняется пожилыми пациентами и при сопутствующем ожирении.
Распространенность чреспищеводной стимуляции (ЧПЭС) предсердий в повседневной диагностике ИБС ниже, хотя этот метод сравним по информативности с ВЭМ-пробой и тредмил-тестом. Метод ЧПЭС является средством выбора при невозможности выполнения пациентом других нагрузочных проб из-за некардиальных факторов (заболевания опорно-двигательного аппарата, перемежающаяся хромота, склонность к выраженному повышению АД при динамической физической нагрузке, детренированность, дыхательная недостаточность).
Для определения суммарного риска по результатам нагрузочных проб используется тредмил-индекс — показатель, комбинирующий информацию, полученную при нагрузочном тестировании.
| Тредмил-индекс = А - [5 × В] – [4 × С] | А — продолжительность нагрузки в минутах |
| В — отклонение от изолинии сегмента ST в мм (в ходе нагрузки или после ее завершения) | |
| С — индекс стенокардии: 0 — стенокардии нет; 1 — стенокардия есть; 2 — стенокардия приводит к остановке исследования |
Тредмил-индекс в равной степени информативен у стационарных и амбулаторных больных, а также у мужчин и женщин, однако у пожилых пациентов его прогностическая ценность изучена недостаточно
Результаты тредмил-теста выражаются в метаболических единицах (оксигенация тканей в единицу времени), а велоэргометрии — в ваттах или двойном произведении (характеристики мышечной работы). Для пересчета этих единиц измерения и стандартизации результатов нагрузочных проб используют Таблицу 7 .
| Показатели | Функциональный класс стенокардии | |||||||||
| I | II | III | IV | |||||||
| Число МЕ (тредмил-тест) | >7,0 | 4,0—6,9 | 2,0—3,9 | 278 | 218—277 | 151—217 | 125 | 75—100 | 50 | 25 |
2.7.3. Фармакологические пробы
В основе метода — провокация приступа ишемии миокарда с помощью лекарственных средств с одновременной записью ЭКГ. В зависимости от вводимого препарата, различают пробы: с вазодилататором (дипиридамолом) или с инотропным средством (добутамином).
Указанные препараты вводят в условиях палаты интенсивной терапии внутривенно под строгим контролем АД и ЧСС, под непрерывным мониторированием ЭКГ.
Фармакологические пробы показаны для диагностики ИБС только при невозможности выполнения или неинформативности проб с физической нагрузкой. Для оценки эффективности лечения ИБС фармакологические пробы не используются.
Сочетание нагрузочной пробы с визуализирующими методами (ЭхоКГ, томография, радиоизотопная сцинтиграфия) существенно повышает ценность полученных результатов.
2.7.4. Стресс-эхокардиография
Один из самых востребованных и высокоинформативных методов неинвазивной диагностики ИБС. В основе метода лежит визуальное выявление локальной дисфункции левого желудочка во время физической нагрузки или фармакологической пробы. Стресс-ЭхоКГ превосходит обычную нагрузочную ЭКГ по диагностической ценности, обладает большей чувствительностью (80— 85%) и специфичностью (84—86%) в диагностике ИБС. Метод позволяет не только доказательно верифицировать ишемию, но и предварительно определить симптом-связанную коронарную артерию по локализации преходящей дисфункции левого желудочка. При технической возможности метод показан всем больным с доказанной ИБС для верификации симптом-связанной коронарной артерии, а также при сомнительных результатах обычной нагрузочной пробы в ходе первоначальной диагностики.
2.7.5. Радиоизотопные исследования
Перфузионная сцинтиграфия миокарда — чувствительный и высокоспецифичный метод исследования с высокой прогностической значимостью. Сочетание сцинтиграфии с физической нагрузкой или фармакологическими пробами (дозированное в/в введение добутамина, дипиридамола) намного повышает ценность полученных результатов.
Отсутствие существенных нарушений перфузии миокарда по данным нагрузочной сцинтиграфии говорит о хорошем прогнозе даже при доказанной ИБС.
Выявление существенных нарушений перфузии в ходе сцинтиграфических исследований у больных с ИБС говорит о неблагоприятном прогнозе и служат веским основанием для проведения КАГ с последующим решением вопроса о хирургической реваскуляризации миокарда.
Исследование перфузии миокарда показано всем пациентам с доказанной хронической ИБС для стратификации риска сердечно-сосудистых осложнений.
2.7.6. Томографические исследования
Мультиспиральная рентгенкомпьютерная томография коронарных артерий
После внутривенного введения рентгенконтрастного вещества можно визуализировать коронарные артерии и шунты к ним, довольно точно выявить атеросклеротические бляшки и определить степень внутрисосудистого стенозирования.
При диагностике ИБС в неясных случаях метод является альтернативой обычной инвазивной КАГ и может проводиться по тем же показаниям. Преимуществом метода является малоинвазивность. У пожилых пациентов с множественными кальцинированными внутрисосудистыми бляшками этот метод нередко приводит к гипердиагностике стенозирования коронарных артерий. При доказанной ИБС и выборе способа хирургической реваскуляризации — предпочтительнее проводить КАГ.
Электронно-лучевая томография коронарных артерий
Метод используется в диагностике атеросклероза коронарных артерий, — особенно при верификации многососудистого поражения и поражении ствола левой коронарной артерии. Однако для повсеместного применения этот метод пока малодоступен, дорог и имеет ряд ограничений. Целесообразность повсеместного проведения этого исследования при ИБС пока не доказана.
Другие методы томографической визуализации
Магнитно-резонансная томография сердца, однофотонная эмиссионная компьютерная томография, позитронно-эмиссионная томография сердца, — в покое и в комбинации со стрессовыми воздействиями, — доказали в эксперименте высокую чувствительность и специфичность при хронической ИБС, однако повсеместно они не проводятся.
2.8. Итоговая стратификация риска осложнений
Конечной целью неинвазивных диагностических исследований является распределение больных с доказанной ИБС в группы: с высоким, умеренным или низким риском тяжелых осложнений и фатальных исходов (Таблица 8).
Стратификация пациентов на группы риска имеет важное практическое значение, поскольку позволяет избежать ненужных дальнейших диагностических исследований и сократить медицинские расходы у одних пациентов, и активно направлять на КАГ и реваскуляризацию миокарда других больных.
- В группе с низким риском осложнений (предполагаемая ежегодная смертность 3%) следует направлять на КАГ без дальнейших неинвазивных исследований.
- У больных, отнесенных к группе умеренного риска (предполагаемая ежегодная смертность 1—3%) показания к КАГ определяют по дополнительным исследованиям (визуализирующие стресс-тесты, наличие левожелудочковой дисфункции).
| Низкий риск | Умеренный риск | Высокий риск | ||
| (ежегодная смертность 3%) | ||||
| Высокий тредмил-индекс (>5) | Незначительная/умеренная дисфункция ЛЖ в покое (ОФВ 35—49%) | Тяжелая дисфункция ЛЖ в покое (ОФВ 2 сегментах на фоне введения низких доз фамакологического препарата или при низкой ЧСС ( 1 КА (50—74%) | 23 | 93 |
| Поражение 1 КА (>95%) | 32 | 91 | ||
| Поражение 2 КА | 37 | 88 | ||
| Поражение 2 КА (оба стеноза >95%) | 42 | 86 | ||
| Поражение 1 КА, стеноз в проксимальном отделе ПНА >95% | 48 | 83 | ||
| Поражение 2 КА, стеноз ПНА >95% | 48 | 83 | ||
| Поражение 2 КА, стеноз в проксимальном отделе ПНА >95% | 56 | 79 | ||
| Поражение 3 КА | 56 | 79 | ||
| Поражение 3 КА, один из стенозов >95% | 63 | 73 | ||
| Поражение 3 КА, стеноз в проксимальном отделе ПНА 75% | 67 | 67 | ||
| Поражение 3 КА, стеноз в проксимальном отделе ПНА >95% | 74 | 59 |
2.9.2. Вентрикулография
Иногда коронароангиографию дополняют вентрикулографическим исследованием. Главное показание к проведению вентрикулографии — детальная оценка общей и локальной левожелудочковой сократимости. Значение выявленной при вентрикулографии левожелудочковой дисфункции очень важно для прогнозирования выживаемости больных со всеми формами ИБС. Вентрикулографию проводят при неинформативности эхокардиографического исследования.
2.9.3. Внутрикоронарное ультразвуковое исследование
Сравнительно новый метод диагностического исследования, дополняющий КАГ. Он свободен от некоторых недостатков КАГ, поскольку позволяет изучить поверхность и внутреннюю структуру атеросклеротических бляшек, выявить тромбоз коронарных артерий, исследовать состояние сосудистой стенки вокруг бляшек. Кроме того, с помощью ВкУЗИ удается точнее верифицировать бляшки сложной конфигурации, плохо поддающиеся количественной оценке при КАГ в обычных проекциях. Наибольшее значение метод имеет при выявлении нормальных или малоизмененных КА во время обычной КАГ. Исследование не показано к повсеместному применению при хронической ИБС.
Согласно современным рекомендациям, основная задача эхокардиографии (ЭхоКГ) при обследовании пациентов с ишемической болезнью сердца (ИБС) – исключить альтернативные, некоронарогенные заболевания, которые могут являться причиной стенокардии. Таким образом, несмотря на то что ЭхоКГ покоя является важным инструментом для оценки функциональных показателей и анатомии сердца, в большинстве случаев она не дает диагностической ценности в плане наличия самого заболевания – ИБС. Развитие современных ультразвуковых технологий, таких как тканевое доплеровское исследование (ТДИ), позволяет расширить возможности эхокардиографии у пациентов с ИБС путем оценки упруго-эластических свойств грудной аорты. Многочисленные исследования показывают достоверную корреляцию между наличием и выраженностью коронарного атеросклероза и изменениями упруго-эластических свойств грудной аорты. Коронарный атеросклероз является наиболее частой причиной ИБС. ТДИ является ультразвуковой технологией, которая используется для оценки скорости и направления движения тканей. С помощью данных ТДИ стало возможным оценивать степень упруго-эластических свойств грудной аорты и выделять изменения, характерные для пациентов с коронарным атеросклерозом. Комбинация М-режима и цветового доплеровского картирования (ЦДК), методика, использующаяся для оценки диастолической функции левого желудочка, позволяет оценивать скорость распространения потока (СРП) в нисходящем отделе грудной аорты, которая характеризует податливость стенок аорты.

1. Шальнова С.А., Деев А.Д. Ишемическая болезнь сердца в России: распространенность и лечение (по данным клинико-эпидемиологических исследований) // Терапевтический архив. 2011. №. 1. С. 7-12.
3. Moran A.E., Forouzanfar M.H., Roth G.A., Mensah G.A., Ezzati M., Murray C.J., Naghavi M. Temporal trends in ischemic heart disease mortality in 21 world regions, 1980 to 2010: the Global Burden of Disease 2010 study. Circulation. 2014. vol. 129. no. 14. P. 1483-1492.
4. Knuuti J., Wijns W., Saraste A., Capodanno D., Barbato E., Funck-Brentano C., Prescott E., Storey R., Deaton C., Cuisset T., Agewall S., Dickstein K., Edvardsen T., Escaned J., Gersh B., Svitil P., Gilard M., Hasdai D., Hatala R., Mahfoud F., Masip J., Muneretto C., Valgimigli M., Achenbach S., Bax J. 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur. Heart J. 2020. V. 41(3). Р. 407-477. DOI: 10.1093/eurheartj/ehz425.
6. Gatzka C.D., Cameron J.D., Kingwell B.A., Dart A.M. Relation between coronary artery disease, aortic stiffness, and left ventricular structure in a population sample. Hypertension. 1998. vol. 32. no. 3. P. 575-578.
8. Stefanadis C., Wooley C.F., Bush C.A., Kolibash A.J., Boudoulas H. Aortic distensibility abnormalities in coronary artery disease. The American journal of cardiology. 1987. vol.59. no. 15. P. 1300-1304.
10. Güngör B., Yılmaz H., Ekmekçi A., Özcan K.S., Tijani M., Alper A.T., Mutluer F.O., Gürkanet U. Aortic stiffness is increased in patients with premature coronary artery disease: a tissue Doppler imaging study. J. Cardiol. 2014. vol. 63. no. 3. P. 223–229.
11. Eryol N.K., Topsakal R., Ciçek Y., Abaci A., Oguzhan A., Basar E., Ergin A. Color Doppler tissue imaging in assessing the elastic properties of the aorta and in predicting coronary artery disease. Jpn. Heart J. 2002. vol. 43.no. 3. P. 219–230.
12. Воробьев А.С., Зимина В.Ю. Эхокардиография у детей и взрослых: руководство для врачей. М.: СпецЛит, 2015. 560 с.
13. Beresten N.F., Pavochkina E.S., Ozerskaya I.A., Medvedev M.V., Kitaev V.M. Remodeling of Arteries in Arterial Hypertension. New Diagnostic Approaches to Assess the Remodeling of Elastic Arteries. Biosciences Biotechnology Research Asia. 2016. vol. 13. no. 4. P. 2007-2013.
14. Rouska E.G. Evaluation of Left Ventricular Diastolic Function by Echocardiography. Rhythmos. 2013. vol. 8. no. 1. P. 4-16.
В настоящее время сердечно-сосудистые заболевания продолжают оставаться главной причиной инвалидности и смертности как в России, так и в мире 1. В России, по данным Росстата, в 2017 году смертность от сердечно-сосудистых заболеваний составила 50% от всех причин смерти (45% от всех причин смерти среди мужского населения и 55% среди женского населения). Смертность от ишемической болезни сердца (ИБС) занимает лидирующее место и составляет 47% в структуре смертности от сердечно-сосудистых заболеваний, 9% из которых составляет смертность от инфаркта миокарда, остальные 38% проходятся на долю хронической ИБС. Основной причиной ИБС является коронарный атеросклероз [2].
Эхокардиография покоя в настоящее время широко используется практически повсеместно, представляя собой безопасное, неинвазивное, безболезненное исследование без побочных действий и противопоказаний. Согласно рекомендациям Европейского общества кардиологов, основной целью данного исследования является исключение альтернативных некоронарогенных причин стенокардии. Эхокардиография покоя также может выявить снижение фракции выброса левого желудочка и нарушение локальной сократимости левого желудочка как признак ИБС [4]. Однако следует отметить, что эти нарушения встречаются не часто. По данным Lewis S.J. et al. [5], при исследовании 252 пациентов без анамнестических, клинических или электрокардиографических указаний на перенесенный инфаркт миокарда, которые впоследствии прошли коронарографию, нарушение локальной сократимости было выявлено у 31% пациентов.
Многочисленные исследования показывают, что изменение эластичности аорты коррелирует с наличием и выраженности коронарного атеросклероза, что доказывает ассоциированность этих процессов 7.
ТДИ является ультразвуковой технологией, которая используется для оценки скорости и направления движения тканей. С помощью данных ТДИ стало возможным оценивать степень упруго-эластических свойств грудной аорты и выделять изменения, характерные для пациентов с коронарным атеросклерозом [10; 11].
Проведение исследования с помощью ТДИ для оценки упруго-эластических свойств грудной аорты проводится в режимах: импульсно-волновой тканевой доплерографии (ИТД), цветового тканевого доплеровского изображения (ЦТДИ), одномерного тканевого доплеровского изображения (М-режим ТДИ) [12; 13].
Целью исследования явилось повышение информативности ультразвуковой диагностики упруго-эластических свойств грудной аорты у лиц с коронарным атеросклерозом.
Материалы и методы исследования
В исследование включены 109 пациентов, проходивших обследование и лечение в ГКБ им. С.П. Боткина ДЗ г. Москвы (2016-2019 гг.). По результатам инвазивной коронарографии пациенты разделены на 2 группы: 64 пациента с коронарным атеросклерозом и 45 пациентов без ангиографических признаков коронарного атеросклероза. Критерии включения: пациентами подписана форма информированного согласия; возраст 18 лет и старше; проведение инвазивной коронарографии в течение последних 6 месяцев. Критерии невключения: подтвержденные медицинской документацией осложнения коронарного атеросклероза, диагностированные в соответствии с международными рекомендациями (инфаркт миокарда); предшествующее оперативное лечение атеросклеротического поражения коронарных артерий; электрокардиостимуляция; постоянная форма фибрилляции предсердий; гемодинамически значимые клапанные пороки; неишемические кардиомиопатии; аневризма восходящего отдела аорты (> 45 мм); наличие зон нарушения локальной сократимости в покое; фракция выброса в покое 2 - Дд 2 )/4 х ПАД), модуль эластичности (жесткости) Петерсона (Ep = ПАД х Дд /∆Д), индекс жесткости (SI = ln(САД/ДАД) / [(Дс - Дд) /Дд]) (рис. 1).
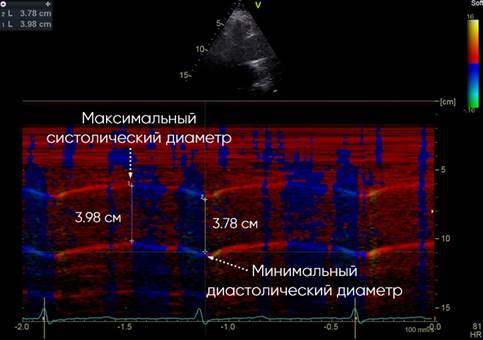
Рис. 1. М-режим ТДИ восходящего отдела аорты. Левая парастернальная позиция по длинной оси на уровне 3 см выше аортального клапана. Метки движения стенок устанавливаются в пограничных точках окрашивания движения стенок к датчику (1) в фазу изометрического расслабления ЛЖ, и от датчика (2) в фазу изометрического сокращения ЛЖ. Диаметр аорты измеряется по внутренним краям стенки
Анализ движения ближней стенки восходящего отдела грудной аорты проводится в режиме импульсно-волновой тканевой доплерографии с синхронной записью ЭКГ при задержке дыхания пациентом на протяжении 5–10 сердечных циклов. Контрольный объем размещается в области продольного среза восходящего отдела грудной аорты на участке на 3 см дистальнее фиброзного кольца аортального клапана при скорости развертки 50-100 мм/с. Точкой начала отсчета временных фаз считается первый антеградный систолический пик, соответствующий зубцу R ЭКГ. На каждом графике смещения доплеровских частот, отражающем скорости движения ближней стенки восходящего отдела грудной аорты, должны быть получены и выделены: S - скорость систолического смещения (см/с), А – скорость раннего диастолического смещения (см/с), E – скорость позднего диастолического смещения (см/с) (рис. 2).
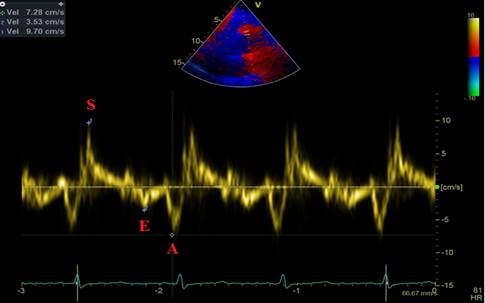
Рис. 2. Левая парастернальная позиция по длинной оси на уровне 3 см выше аортального клапана, ИТД ближней стенки восходящего отдела аорты. S - скорость систолического смещения. Е – скорость раннего диастолического смещения. А – скорость позднего диастолического смещения
Исследование потока нисходящего отдела грудной аорты. Для исследования используется стандартная супрастернальная эхокардиографическая позиция.
Курсор М-режима располагается параллельно потоку нисходящего отдела грудной аорты, и в сочетании с цветовым доплеровским картированием производится запись цветовой волны потока, получаемой с помощью элайзинг-эффекта, который достигается путем установки предела Найквиста 30-70 см/c.
Скорость распространения потока в цветовом М-режиме определяется как отношение расстояния между точками, отображающими начало и конец наклона цветовой волны потока, ко времени между двумя этими точками (рис. 3).
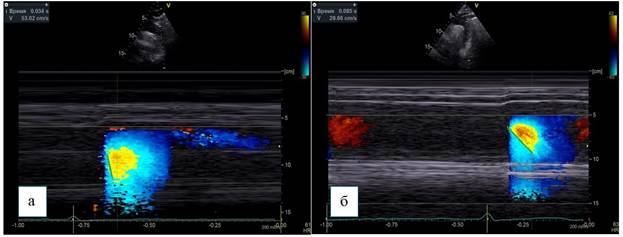
Рис. 3. Супрастернальная позиция, М-ЦДК нисходящего отдела грудной аорты.
Способ определения СРП:
а – пациент без коронарного атеросклероза, СРП – 530 мм/с,
б – пациент с коронарным атеросклерозом, СРП – 296 мм/c
Достоверность различий определялась по t-критерию Стьюдента для независимых выборок. Для определения корреляционных взаимосвязей использовался критерий корреляции рангов Пирсона. Результаты считались достоверными при р≤0,05. Статистическая обработка полученных данных была проведена с помощью программы Statistica 10.
Результаты исследования и их обсуждение
По результатам импульсно-волновой тканевой доплерографии ближней стенки восходящего отдела грудной аорты выявлено значимое снижение скорости систолического смещения S (8,13±2,77 см/с), скорости раннего диастолического смещения E (5,07±1,80 см/с) в группе пациентов с выявленным коронарным атеросклерозом (p=0,02 и p
Как проявляется ишемическая болезнь сердца до проведения эхокардиографии
- История болезни и физикальное обследование остаются краеугольным камнем для первоначальной оценки пациентов с известным или подозреваемым заболеванием коронарных артерий (ИБС).
- Однако анамнез у пациентов с ИБС может быть нетипичным. До 25% пожилых пациентов или пациентов с диабетом имеют безболевой инфаркт миокарда (ИМ); величина симптомов не коррелирует со степенью ИБС. Так с типичными симптомами
- У большинства пациентов с ОКС физическое обследование не дает отклонений.
- Электрокардиография (ЭКГ) может имитировать ишемическое повреждение при остром перикардите, аневризме левого желудочка и ранней реполяризации. Кроме того, приблизительно от 15% до 20% пациентов с ОКС имеют нормальную ЭКГ.
- Наконец, у пациентов Красноярска, поступающих в отделения неотложной помощи с болью в груди, 85% не имеют ОКС, но от 3% до 5% с острым инфарктом миокарда (ОИМ) выписываются домой.
- ИБС является наиболее распространенной клинической проблемой во взрослой кардиологии. Это затрагивает более 500 человек на 100000 населения России и являются основной причиной смерти в Красноярске.
- Ежегодно проводится не менее 5 миллионов посещений отделения неотложной помощи при болях в груди, и более 1 миллион людей в России испытывают новый или рецидивирующий ОИМ каждый год.
Показания класса I для использования при ишемической болезни сердца
Эхокардиография (ЭхоКГ) имеет важное дополнительное диагностическое и прогностическое значение для анамнеза, физического обследования и после снятия ЭКГ у пациентов с болью в груди, ОКС ((ОИМ с подъемом сегмента ST ( STEMI ), ИМ с подъемом сегмента без ST ( NSTEMI ) и нестабильная стенокардия (ИБС)) и у пациентов с известной хронической ИБС.
Диагностика ИБС: методы и основные диагностические особенности. Эхокардиография в покое
- Нарушения движения стенок являются непременным условием ишемии миокарда или ИМ.
- Левый желудочек (ЛЖ) разделен на 16 сегментов миокарда со специфическим артериальным снабжением.
- Каждый сегмент на эхокардиографии оценивается на основе внутреннего движения стенки и утолщения эндокарда по шкале от 1 до 5, где 1 = нормальный, 2 = гипокинетический, 3 = акинетический, 4 = дискинезический и 5 = аневризматический.
- Общая оценка движения стенок и индекс представляют собой сумму баллов каждого сегмента стены, деленную на общее количество набранных сегментов. Таким образом, нормальная общая оценка движения стенок и индекс составляют 16 и 1 соответственно. Чем выше балл и индекс, тем хуже степень и степень ишемии или ИМ.
- Независимо от аномалий движения стенки, склероз аортального клапана (особенно если смешанный нодулярный и диффузный склероз) и склероз митрального кольца являются прогностическими факторами возникновения ИБС.
- Сравнение отдыха с пиковым напряженным движением стенки приводит к четырем типам реакции на движение стенки и соответствующим клиническим сценариям: а) отсутствие или низкая вероятность возникновения ИБС, б) ишемия без ИМ, в) ишемический жизнеспособный миокард (оглушенный или спящий) или d ) ИМ с нежизнеспособным миокардом.
- Диагностическая точность стресс-эхокардиографии при обнаружении ИБС возрастает по мере того, как а) степень тяжести и степень увеличения ишемии, б) возрастает выраженность движения стенки или количества асинергических сегментов, и в) прогнозируемая максимальная частота сердечных сокращений составляет как достигнутая или превышенная

Эхокардиография в покое для пациентов, перенесших инфаркт миокарда: основные диагностические особенности
Спящий или оглушенный миокард
- Сравнение аномалий движения стенки покоя или дефектов перфузии по контрастному эхо-сигналу миокарда до и после реперфузионных вмешательств определяет степень спасенного миокарда с риском повторной ишемии или ИМ.
- После реперфузионной терапии оглушение миокарда может пройти в течение 3-5 дней. Таким образом, улучшение движения стенки левого желудочка и его функции при эхокардиографии после переднего ИМ может указывать на отсутствие необходимости длительной антикоагуляции.
- Постоянные значительные аномалии движения стенки с истончением или повышением эхогенности, аневризмой левого желудочка или ФВ левого желудочка ≤35% на эхокардиографии предполагают большой инфаркт миокарда. У этих пациентов необходима агрессивная терапия для снижения нагрузки после ремоделирования левого желудочка.
Ишемия после инфаркта миокарда
- Стенокардия после ИМ: преходящее или постоянное ухудшение аномалий движения стенки на эхокардиографии при ИМ или не связанных с инфаркзависимой артерией без повторного повышения изоферментов миокарда.
- Постинфарктное расширение: повторное повышение изоферментов миокарда в дополнение к новым или худшим нарушениям движения стенки.
- Расширение после постинфарктной зоны: увеличенная площадь истончения стенок в зоне инфаркта; он прогрессирует в течение 7 дней после ИМ. Это может привести к образованию аневризмы и / или тромба, разрыву стенки, рецидивирующей ишемии, сердечной недостаточности и желудочковой аритмии.
Правожелудочковый инфаркт на эхокардиографии
- Инфаркт правого желудочка встречается у 25–30% пациентов с задненижним инфарктом миокарда.
- Данные эхокардиограммы включают расширение и дисфункцию правого желудочка, аномальное движение свободной стенки правого желудочка, трикуспидальную регургитацию различной степени тяжести, парадоксальное движение межжелудочковой перегородки, дилатацию нижней полой вен (гипертензия в правом предсердии) и, редко, шунтирование из правого предсердия в левое предсердие через открытое овальное отверстие.
- Пациенты с ИМ правого желудочка имеют повышенную частоту сердечной недостаточности, механических осложнений и смертности, независимо от степени дисфункции левого желудочка.
Диастолическая дисфункция левого желудочка на эхокардиограмме
У пациентов с ИБС с клинической сердечной недостаточностью или без нее диастолическая дисфункция левого желудочка варьируется от нарушения расслабления до ослабления податливости левого желудочка.
Нарушение расслабления левого желудочка
Нарушение расслабления левого желудочка проявляется в уменьшении скорости E -волны, увеличении времени E -замедления (> 160 мсек), соотношении E / A IVRT ) до> 90 мсек.
Снижение релаксации левого желудочка
- Псевдонормальная схема митрального притока: увеличение скорости E , уменьшение скорости A , время замедления E (от 140 до 160 мсек) и отношение E / A составляет от 1,0 до 1,5.
- Ограничительная модель митрального притока: высокое отношение E / A (> 1,5), короткое время замедления E ( IVRT (
- Аномальный приток легочных вен: Уменьшенный или отсутствующий систолический приток в легочную вену, преобладающий диастолический приток и скорость изменения сокращения предсердия, более продолжительная, чем скорость митрального А. Ограничительный приток через митральный клапан и легочных вен является предиктором высокого давления наполнения левого желудочка или давления заклинивания в легочных капиллярах> 20 мм рт. ст. и является независимым предиктором сердечной смерти.
- Было показано, что снижение систолической и диастолической скоростей миокарда пульсовой волны базальных боковых и перегородочных стенок коррелирует с систолической и диастолической дисфункцией левого желудочка у пациентов после ИМ.
- Отсутствие увеличения систолических скоростей от базовой линии до пиковой дозы добутамина или пиковой нагрузки продемонстрировало высокую чувствительность и специфичность для выявления ишемии и, вероятно, превосходит развитие аномалий движения стенки.
- Скорость распространения цветового потока М-режима: скорость распространения цветовой М-волны при заполнения левого желудочка снижается (нормальный диапазон, 40-80 см/с) у пациентов с ишемической диастолической дисфункцией левого желудочка.
Перикардит при ИБС на эхокардиографии
- Перикардит возникает в течение 3–10 дней после ИМ, с частотой до 25% при больших инфарктах передней стенки (ниже у пациентов, получающих тромболитическую терапию, первичную ангиопластику или стентирование) и связан с небольшими или средними по размеру и обычно локализованными выпотами.
- Перикардит ≥2 недели после ИМ предполагает синдром Дресслера, который связан с периферическим выпотом перикарда от малого до большого размера и, редко вызывает тампонаду сердца.
- Эхокардиография является высокочувствительным для обнаружения локализованных или периферических выпотов перикарда после ИМ
Обнаружение механических осложнений после инфаркта миокарда, основные диагностические особенности
Ишемическая регургитация митрального клапана и разрыв папиллярных мышц
- Частота возникновения ишемической митральной регургитации (МР) у пациентов после ИМ составляет приблизительно 20%, аналогична при переднем и нижнем инфаркте и чаще всего бывает легкой или средней степени тяжести, но связана с повышенным кратковременным и долгосрочным смертность.
- При нижнем инфаркте миокарда ишемическая или инфарктированная заднемедиальная папиллярная мышца вызывает отсутствие и снижение подвижности медиальной половины, преимущественно задней створки митрального клапана, что приводит к неправильной адаптации створки, относительному западению передней створки или псевдопролапсу и эксцентрической направленной заднелатерально струе митральной недостаточности.
- При переднем инфаркте миокарда дилатация и дисфункция левого желудочка приводят к нисходящему и латеральному смещению обеих папиллярных мышц, неполной, но симметричной дислокации створок и центральной митральной регургитации на эхокардиографии.
- Когда разрыв папиллярной мышцы является частичным, на эхокардиографии может быть продемонстрировано западение одной или обоих митральных створок. После полного разрыва папиллярных мышц МР становится тяжелой, и вовлеченный митральный клапан с частью его папиллярной мышцы становится отслоенным или свободно выпадает в левое предсердие.
- Tрансторакальная эхокардиография недооценивает тяжесть эксцентричных струй митральной регургитации, следовательно, чреспищеводное исследование является тестом выбора, если клинически или обычная эхокардиограмма подозревают значительную МР.
Дефект межжелудочковой перегородки на ультразвуковом исследовании
- Дефекты межжелудочковой перегородки (ДМЖП) чаще всего встречаются в апикальной задней и апикальной передней зоне перегородки, часто со змеевидным кровотоком. Эхокардиограмма чаще всего показывает единичные дефекты.
- ДМЖП лучше всего визуализировать из длинной парастернальной и по короткой оси ниже уровня папиллярных мышц, а также с апикального или подреберного четырехкамерного доступа с передним или задним углом для переднего и заднего дефектов соответственно.
- Связанная с этим острая перегрузка правого желудочка приводит к дилатации и дисфункции правого желудочка, парадоксальному движению межжелудочковой перегородки, а также к легочной гипертензии и расширению правого предсердия.
- Чувствительность цветового допплера при эхокардиографии для обнаружения ДМЖП находится в диапазоне> 95%. Ширина цветной допплеровской струи коррелирует с размером дефекта при операции или патологии.
Разрыв свободной стенки на эхокардиограмме
Разрыв свободной стенки встречается чаще у пациентов с задне-боковым ИМ (окклюзия периферической артерии) и у пациентов с неудачной тромболитической терапией (5,9% против 0,5%). Он проявляется как гемоперикард (часто с внутриперикардиальной повышенной эхоплотностью или сгустками) и тампонадой сердца с частым сдавлением левых отделов сердца.
Псевдоаневризма на эхокардиограмме
Псевдоаневризма — это разрыв миокарда, содержащийся в перикардиальных спайках, которые образуют мешочек, который связывается с левым желудочком. Псевдоаневризма характеризуется узкой шейкой, с отношением диаметра шейки к максимальному размеру аневризмы
Эхокардиография в состоянии покоя и стресса после лечения острых коронарных синдромов и ИБС: основные диагностические и прогностические особенности
Априорно высокая претестовая вероятность стенозирующего коронарного атеросклероза у мужчин старше 40 лет при наличии типичных ангинозных болей показана в одной из известных таблиц Diamod GA еще в 1979
Рисунок 1. Претестовая вероятность ИБС у мужчин и женщин в зависимости от возраста и клинических проявлений (Diamond GA, 1979)
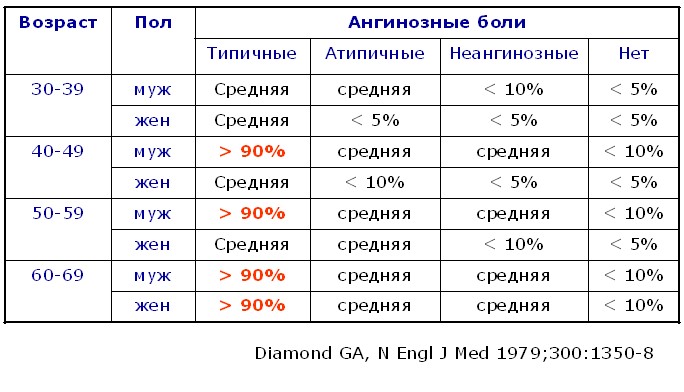
По сути мужчина старше 40 лет с факторами риска ИБС (гиперхолестеринемия, артериальная гипертензия, отягощенный семейный анамнез) может быть направлен на коронароангиографию для исключения стенозирующего коронарного атеросклероза без предварительного проведения нагрузочного теста. Однако эта таблица становится практически бесполезной при наличии у пациента с множественными факторами риска ИБС немой ишемии миокарда.
Алгоритм диагностики ИБС с использованием визуализирующих методик.
В самом начале этого алгоритма
Рисунок 2. Алгоритм диагностики ИБС
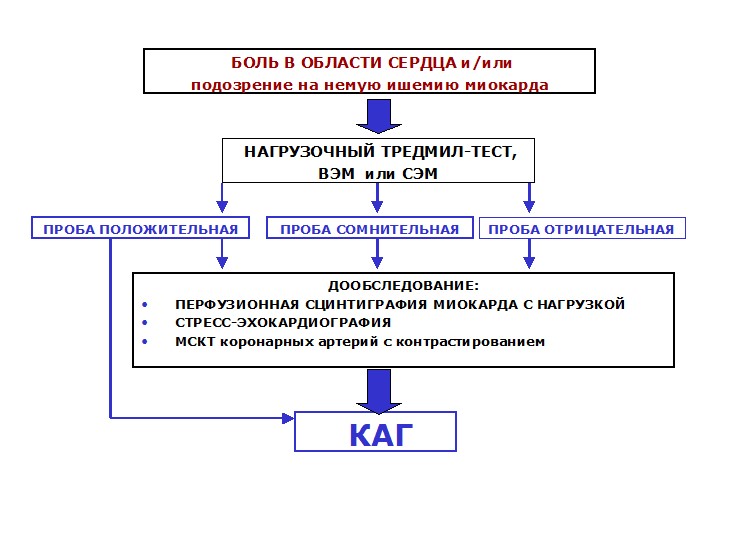
в зависимости от клинических проявлений ИБС мы имеем возможность выбора одного из трех вариантов нагрузочного теста:
- нагрузочный тредмил-тест;
- велоэргометрия;
- спироэргометрия.
Нагрузочный тредмил-тест по сути является универсальным скрининговым исследованием и подходит для любого пациента, независимо от возраста и физических возможностей, так как ходьба - наиболее физиологический вид физической активности.
В отличие от этого варианта стресс-системы,велоэргометр занимает гораздо меньше места, но не пригоден для тестирования пожилых людей с выраженной патологией суставов.
В том случае, когда мы подозреваем одышку как эквивалент стенокардии, мы используем особый метод скринингового стресс-теста – спироэргометрию.
К визуализирующим методикам относят три варианта инструментальной диагностики, которые при сомнительном результате нагрузочного теста могут быть доводом в пользу проведения коронароангиографии:
- мультиспиральная компьютерная томография коронарных артерий с контрастированием;
- перфузионная сцинтиграфия миокарда с нагрузкой;
- стресс-эхокардиография миокарда (с нагрузочной стресс-системой или с использованием добутамина).
Стоит вернуться к вопросу о том, какую динамику ЭКГ на сегодняшний день принято считать достоверным критерием ишемии миокарда, а какие электрокардиографические изменения могут косвенно свидетельствовать в пользу значимого стенозирующего коронарного атеросклероза.
В соответствии с критериями Darrow M, 2000
Рисунок 3. Наиболее специфичные ЭКГ-критерии ишемии миокарда
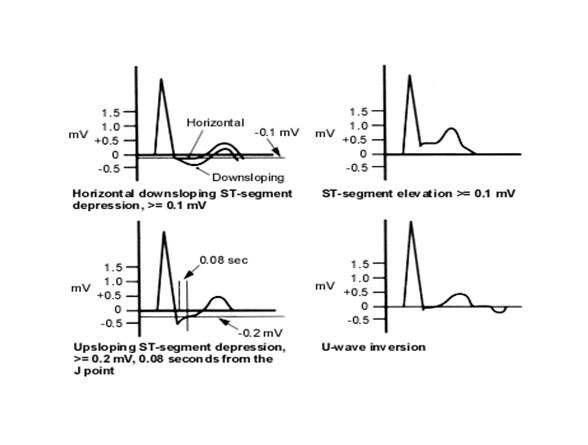
и современными пересмотрами, представленными в различных рекомендациях, наиболее достоверными критериями ишемии миокарда в настоящее время являются следующие ЭКГ-критерии:
и современными пересмотрами, представленными в различных рекомендациях, наиболее достоверными критериями ишемии миокарда в настоящее время являются следующие ЭКГ-критерии:
- горизонтальная депрессия сегмента ST не менее 1 мм;
- косонисходящая депрессия сегмента ST не менее 1 мм;
- медленная косовосходящая депрессия сегмента ST не менее 1.5 мм;
- элевация сегмента ST.
Использование визуализирующих методик возможно в ситуации, когда получен отрицательный результат нагрузочного теста, однако имеющиеся клинические данные и особенности анамнеза позволяют усомниться в высокой воспроизводимости и высокой чувствительности теста у данного больного. Особенностями нагрузочного тестирования, которые должны насторожить лечащего врача в вопросе достаточной воспроизводимости теста могут быть следующие результаты нагрузочного теста при нормальной динамике сегмента ST:
- снижение АД на пике нагрузки и в восстановительном периоде или выраженный симпатико-астенический тип реакции на нагрузку;
- индукция желудочковых нарушений сердечного ритма на пике нагрузки или в восстановительном периоде (стресс-индуцированные желудочковые нарушения сердечного ритма), особенно в сочетании с низкой толерантностью к физической нагрузке.
Возможности спироэргометрии как скринингового стресс-теста у пациентов с ИБС.
Для пациентов, предъявляющих жалобу на одышку, которая может быть расценена как эквивалент стенокардии, наиболее оптимальным вариантом скринингового нагрузочного теста является спироэргометрия. Это исследование является одномоментной оценкой функционального состояния сердечно-сосудистой системы, дыхательной системы и клеточного метаболизма. Полученные параметры позволяют оценить степень и место нарушений, а также определить прогноз дальнейшего течения имеющейся патологии.
Рисунок 4. Спироэргометрия
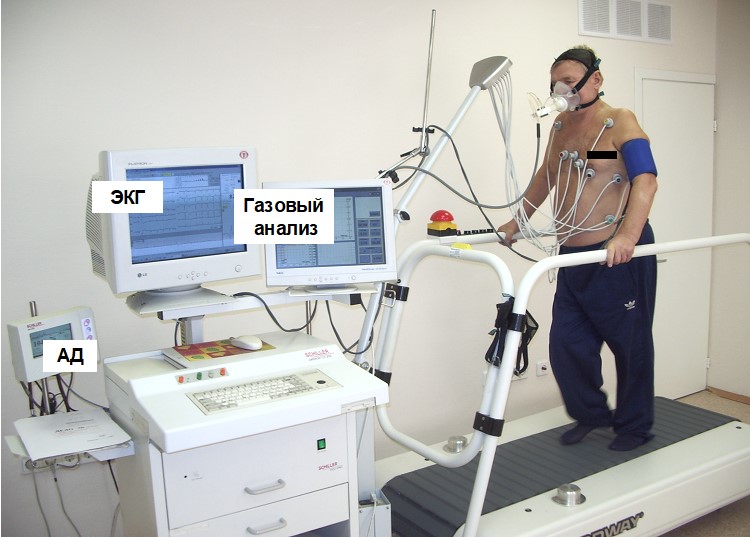
На самом деле, помимо скринингового исследования этот инструментальный метод является диагностическим методом с широким спектром возможностей
Рисунок 5. Показания к эргоспирометрии
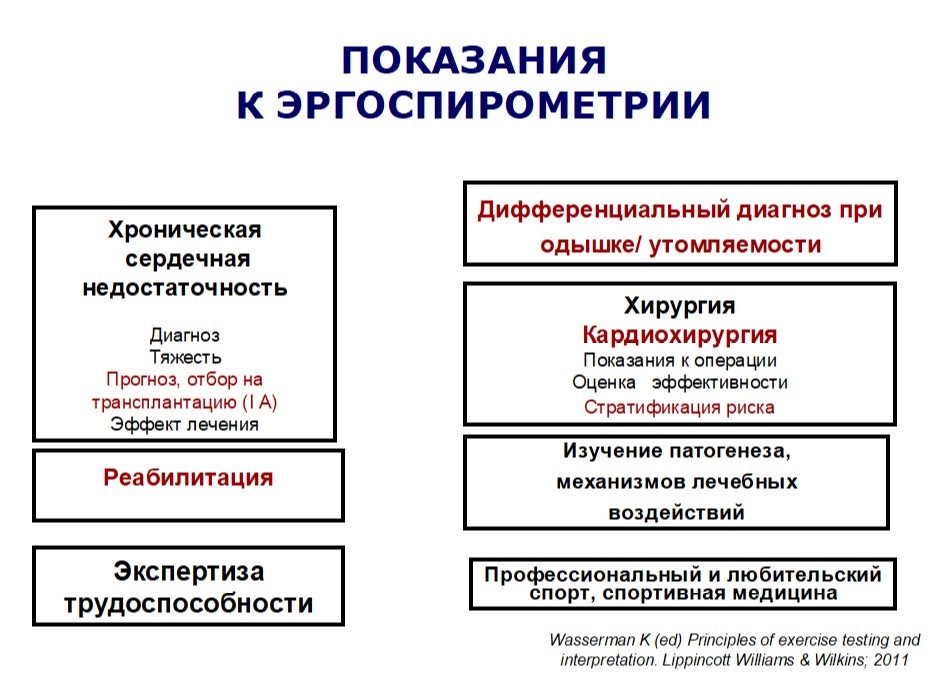
который позволяет его использовать в различных областях медицины. В частности, такой показатель, как пиковое потребление кислорода (VO2 peak), позволяет уточнить риск периоперационных осложнений
Рисунок 6. Прогностическое значение пикового потребления кислорода (VO2 peak).

При этом методика позволяет достоверно оценить тяжесть хронической сердечной недостаточности у пациентов с ИБС
Рисунок 7. Тяжесть хронической сердечной недостаточности у пациентов с ИБС.
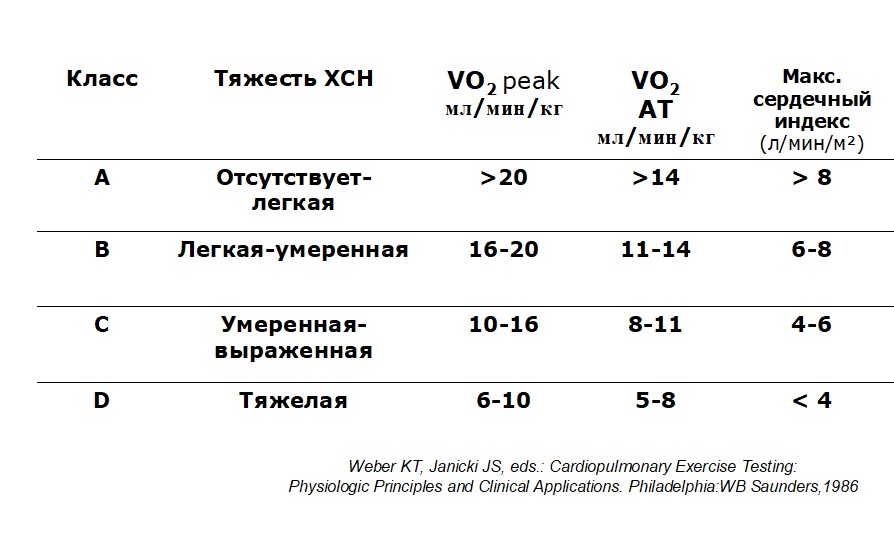
На сегодняшний день считается доказанным, что увеличение переносимости нагрузок на 1% приводит к снижению сердечно-сосудистой смертности на 2%, а VO2 peak является независимым предиктором смертности.
Вероятно, в практике любого врача-кардиолога имеются истории, демонстрирующие значимость визуализирующих методик в диагностическом алгоритме некоторых пациентов.
Показательной является история пациента К., 53 лет, который обратился в клинику кардиологии УКБ №1 в октябре 2016 года в связи с регистрацией парной желудочковой экстрасистолии на ЭКГ покоя. Из анамнеза было известно, что с 1996 года в анализе липидного спектра крови регистрировалась гиперхолестеринемия 9-12 ммоль/л. От приема статинов пациент отказывался. Ежедневно посещал фитнесс-клуб, и лишь при активном расспросе отмечал появление одышки в течение последнего года при длительной интенсивной ходьбе. Обращал также на себя внимание отягощенный семейный анамнез (у отца пациента имеется мультифокальный атеросклероз, клинически – немая ишемия миокарда).
Рисунок 8. Результаты холтеровского мониторирования пациента К., 53 лет (одиночная и парная желудочковая экстрасистолия).
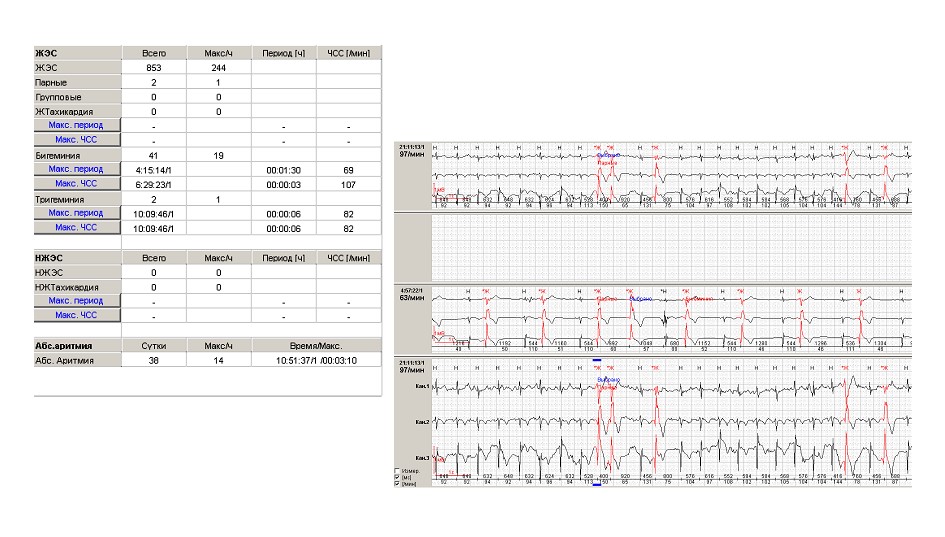
Перед проведением нагрузочного тредмил-теста обращала на себя внимание частая одиночная мономорфная желудочковая экстрасистолия с резким учащением на пике нагрузки
Рисунок 9. Стресс-индуцированная мономорфная желудочковая экстрасистолия у пациента К. во время нагрузочного тредмил-теста.
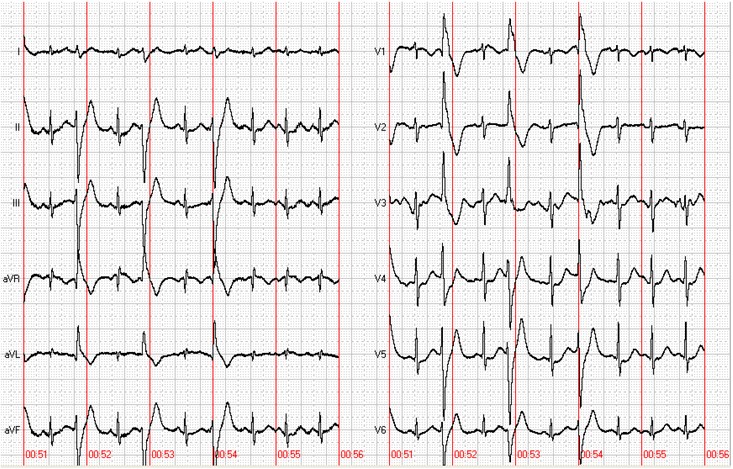
Рисунок 10. Ишемическая динамика сегмента ST у пациента К., 53 лет. А – ЭКГ на пике нагрузки; Б – появление косонисходящей депрессии сегмента ST в восстановительном периоде.
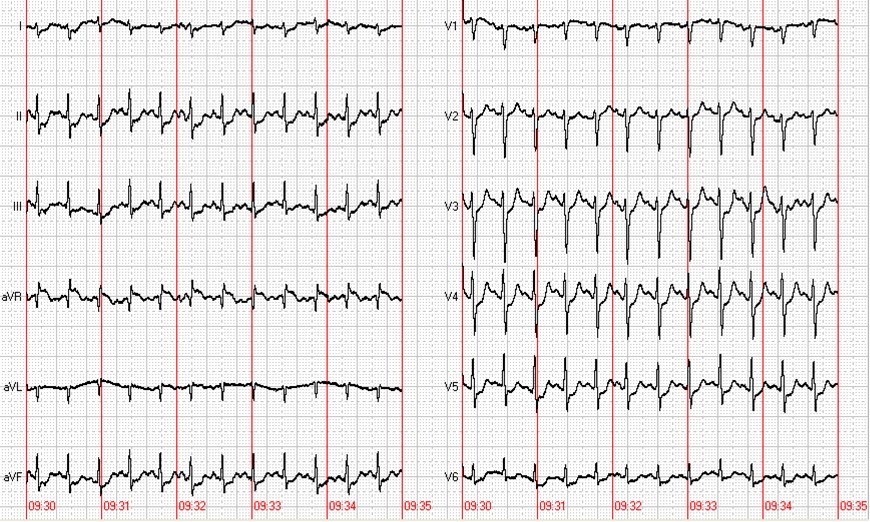
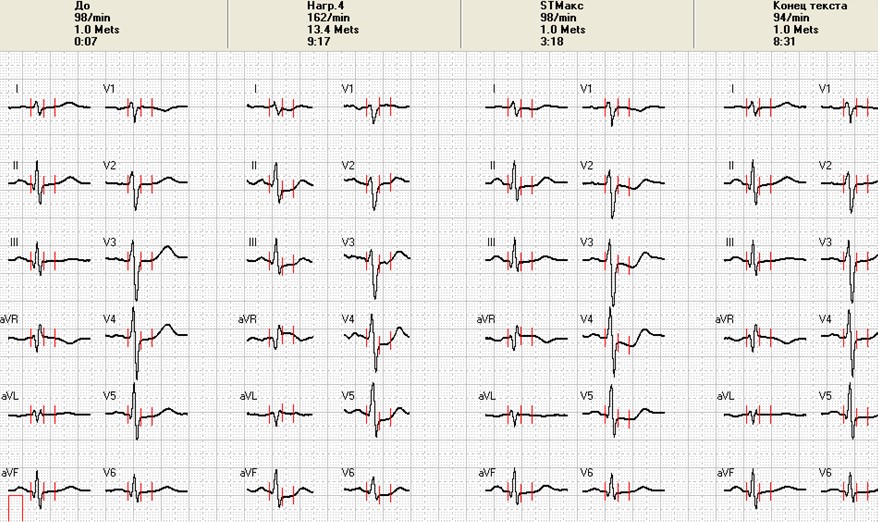
Поскольку от предложенной коронароангиографии пациент вновь отказался, была проведена мультиспиральная компьютерная томография коронарных артерий с контрастированием, которая продемонстрировала протяженный стеноз передней межжелудочковой артерии и окклюзию правой коронарной артерии
Рисунок 11. Стенозирующий атеросклероз коронарных артерий у больного К., 53 лет.
ПМЖВ в проксимальном сегменте имеет кальцинированную протяженную бляшку со стенозированием 50-75% (Указано стрелкой
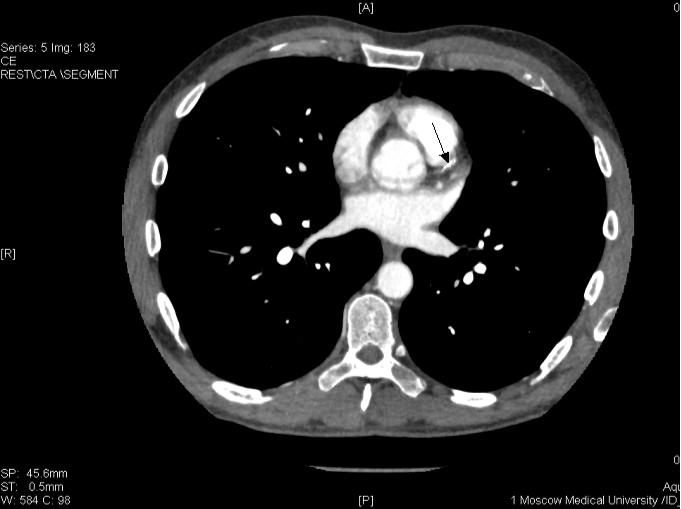
ПКА в проксимальном сегменте окклюзирована (указано стрелкой), дистальный отдел и ЗМЖВ заполняются контрастным веществом.
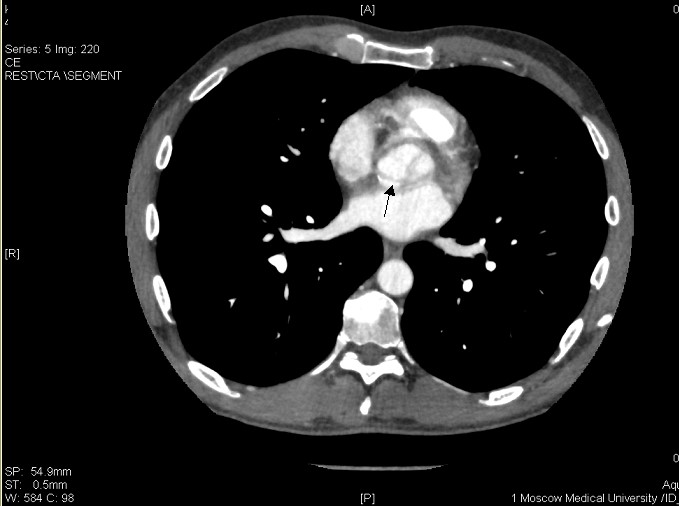
Предложенный случай демонстрирует полное соответствие скринингового тредмил-теста и результатов одной из визуализирующих методик, однако в практической кардиологии нередко имеются случаи рассогласования результатов этих методов исследования.
Довольно показательным в этом смысле является случай пациентки М., 63 лет, которая обратилась в клинику кардиологии УКБ №1 ПМГМУ им. И.М. Сеченова по поводу давящих болей в области сердца, возникающих при подъёме в гору в течение последних 6 месяцев. В анамнезе также обращал на себя внимание затяжной эпизод давящих болей в области сердца, возникший около 2 месяцев назад. При стационарном обследовании была выявлена умеренная гиперхолестеринемия (6.8 ммоль/л), лоцирована уплотненная аорта при проведении трансторакальной эхокардиографии. С учетом эпизода затяжных болей в области сердца пациентке была проведена перфузионная сцинтиграфия миокарда с нагрузкой, где выявлен дефект перфузии боковой стенки в покое с переходом на заднюю стенку при нагрузке
Рисунок 12. Результаты перфузионной сцинтиграфии пациентки М., 63 лет: дефект перфузии боковой стенки в покое с переходом на заднюю стенку при нагрузке.
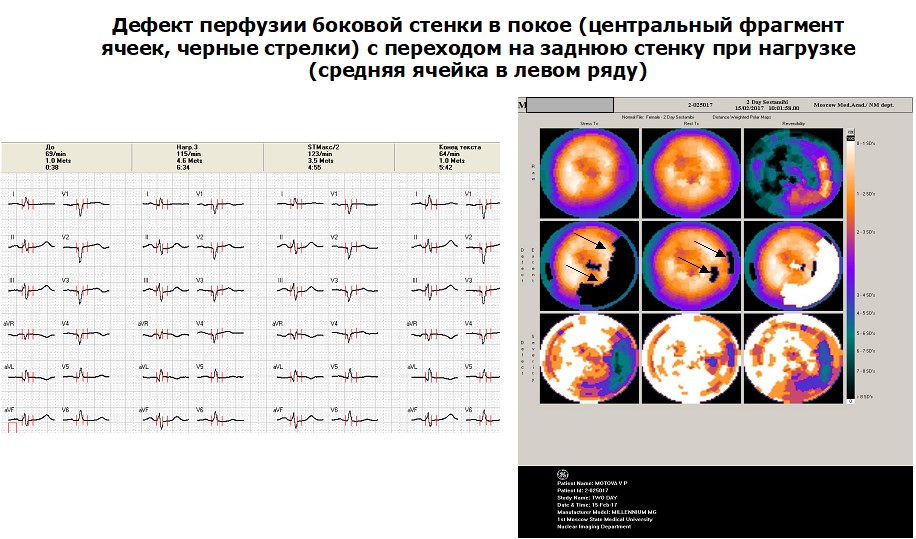
Также демонстративным является случай пациента Л., 54 лет, госпитализированного в стационар в декабре 2016 года с жалобами на давящий дискомфорт в области сердца, возникающий при ходьбе на 200 м с августа 2016 года и усилившийся в холодную погоду в декабре. При проведении трансторакальной эхокардиографии и нагрузочного тредмил-теста значимой патологии выявлено не было. Однако, с учетом наличия множественных факторов риска (мужской пол, возраст старше 40 лет, курение, гиперхолестеринемия 9 ммоль/л, отягощенный семейный анамнез, артериальная гипертензия) пациенту была проведена коронароангиография. Выявлен 90% стеноз передней межжелудочковой артерии (ПМЖА) и 70% стеноз диагональной артерии (ДА). После проведения стентирования ПМЖА на фоне терапии бисопрололом 5 мг/сут, клопидогрелем 75 мг/сут и аторвастатином 20 мг/сут в январе при ходьбе в холодную погоду пациент отметил возобновление болей в области сердца. Проведена перфузионная сцинтиграфия миокарда с нагрузкой
Рисунок 13. Результаты перфузионной сцинтиграфии миокарда пациента Л., 54 лет: стресс-индуцированный передне-боковой дефект перфузии на пике нагрузки при отсутствии значимой динамики сегмента ST.
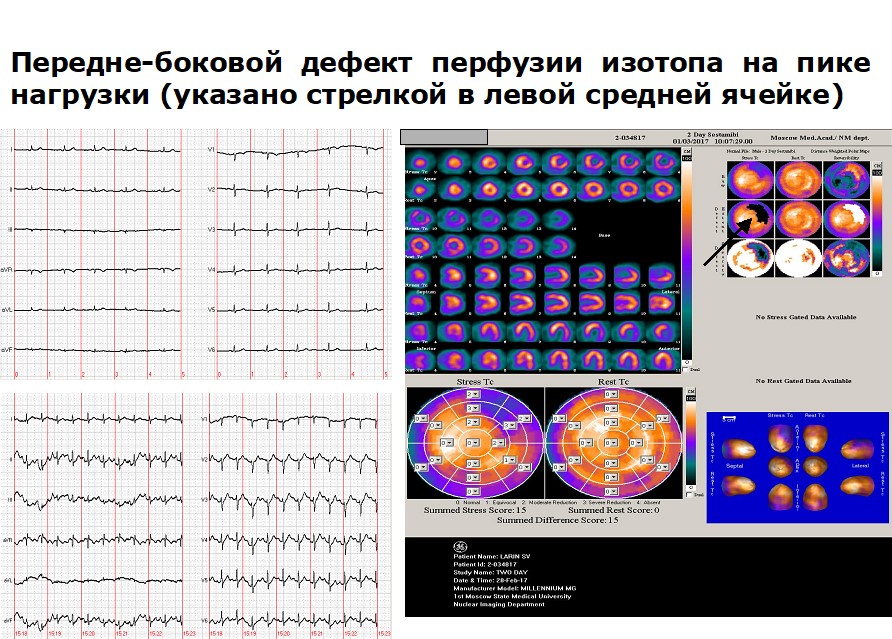
где выявлены симптомы стресс-индуцированной ишемии миокарда. После стентирования 70% стеноза ДА была получена положительная динамика контрольной перфузионной сцинтиграфии миокарда. Пациент также отметил полное отсутствие болей при ходьбе.
Довольно типичной является история пациента Д, 62 лет, который обратился на амбулаторную консультацию с жалобами на боли в икроножных мышцах при ходьбе. При проведении дуплексного сканирования артерий ног были выявлены множественные значимые стенозы артерий нижних конечностей, что позволяло расценить жалобы как проявление облитерирующего атеросклероза артерий нижних конечностей. У такого пациента, безусловно, было необходимо исключение гемодинамически значимого стенозирующего атеросклероза коронарных артерий и немой ишемии миокарда, однако при попытке проведения тредмил-теста проба была неинформативной: боли в ногах возникли при достижении 60% возрастной нормы. При проведении трансторакальной эхокардиографии была выявлена гипокинезия нижней стенки левого желудочка.
Для решения вопроса о мультифокальности и необходимости проведения коронароангиографии пациенту был проведен добутаминовый тест как вариант стресс-эхокардиографии. Появление двухфазной реакции сократимости (двухфазный добутаминовый ответ) для этого пациента позволило бы не только решить вопрос необходимости проведения коронароангиографии, но и оценить необходимость реваскуляризации миокарда.
Как известно, подтверждением наличия жизнеспособного миокарда является увеличение сократимости сегментов с исходной сниженной сократимостью в ответ на введение низких (5-10 мкг/кг/мин) доз добутамина с последующим ухудшением сократимости в тех же сегментах на фоне введения высоких (20 мкг/кг/мин) доз.
У пациента Д. проба была положительной: как видно из представленной иллюстрации
Рисунок 14. Положительный результат добутаминового теста у пациента Д., 62 лет
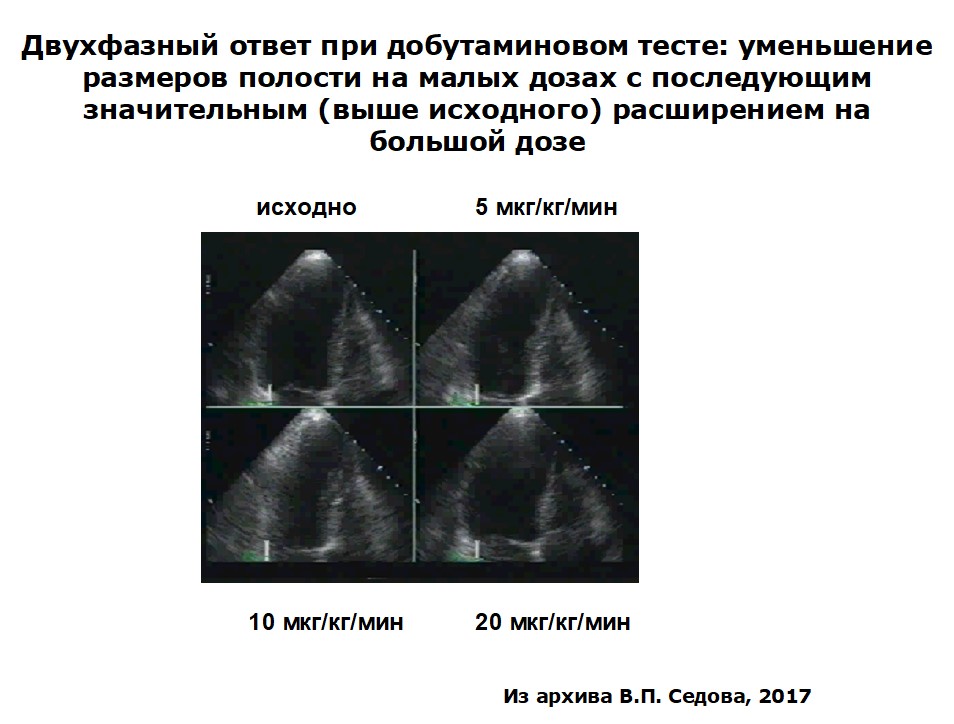
имеется сужение полости левого желудочка с последующим ее расширением, что является признаком последовательного улучшения, а затем ухудшения сократимости. При проведении коронароангиографии у пациента было выявлено гемодинамически значимое многососудистое поражение коронарных артерий, а в дальнейшем успешно проведено аорто-коронарное шунтирование.
Таким образом, на сегодняшний день можно сказать, что неинвазивная диагностика ИБС представляет собой отлаженный, но не всегда очевидный алгоритм. Чаще всего мы используем визуализирующие методики диагностики ИБС (перфузионную сцинтиграфию миокарда с нагрузкой, стресс-эхокардиографию, мультиспиральную компьютерную томографию) при сомнительном результате скринингового нагрузочного теста или при невозможности его проведения (пациенты с облитерирующим атеросклерозом артерий нижних конечностей). Однако отсутствие типичной ишемической динамики сегмента ST у пациента с несколькими факторами риска ИБС оправданно позволяет использовать визуализирующие методики диагностики, несмотря на отрицательный результат первичного теста, поскольку именно клинический статус пациента в сочетании с данными его анамнеза позволяют определить единственно верный для каждого конкретного пациента алгоритм диагностики.
Читайте также:

