Реферат коллигативные свойства растворов
Обновлено: 04.07.2024
Любому раствору характерны те или иные физические свойства, к которым относятся и коллигативные свойства растворов. Это такие свойства, на которые не оказывает влияние природа растворенного вещества, а зависят они исключительно от количества частиц этого растворенного вещества.
К коллигативным свойствам растворов относятся:
- Понижение давление паров
- Повышение температуры кипения
- Понижение температуры затвердевания (кристаллизации)
- Осмотическое давление раствора.
Рассмотрим подробнее каждое из перечисленных свойств.
Понижение давления паров
Давление насыщенного пара (т.е. пара, который пребывает в состоянии равновесия с жидкостью) над чистым растворителем называется давлением или упругостью насыщенного пара чистого растворителя.
Если в некотором растворителе растворить нелетучее вещество, то равновесное давление паров растворителя при этом понижается, т.к. присутствие какого – либо вещества, растворенного в этом растворителе, затрудняет переход частиц растворителя в паровую фазу.
Экспериментально доказано, что такое понижение давления паров напрямую зависит от количества растворенного вещества. В 1887 г. Ф.М. Рауль описал количественные закономерности коллигативных свойств растворов.
Первый закон Рауля
Первый закон Рауля заключается в следующем:
Давление пара раствора, содержащего нелетучее растворенное вещество, прямо пропорционально мольной доле растворителя в данном растворе:
p — давление пара над раствором, Па;
p0 — давление пара над чистым растворителем, Па;
χр-ль — мольная доля растворителя.
nв-ва и nр-ля – соответственно количество растворенного вещества и растворителя, моль.
Иногда Первому закону Рауля дают другую формулировку:
относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества:
При этом принимаем, что χв-ва + χр-ль= 1
Изотонический коэффициент Вант-Гоффа
Для растворов электролитов данное уравнение приобретает несколько иной вид, в его состав входит изотонический коэффициент i:
Δp — изменение давления паров раствора по сравнению с чистым растворителем;
i – изотонический коэффициент.
Изотонический коэффициент (или фактор Вант-Гоффа) — это параметр, не имеющий размерности, который характеризует поведение какого – либо вещества в растворе.
То есть, изотонический коэффициент показывает, разницу содержания частиц в растворе электролита по сравнению с раствором неэлектролита такой же концентрации. Он тесно связан связан с процессом диссоциации, точнее, со степенью диссоциации и выражается следующим выражением:
n – количество ионов, на которые диссоциирует вещество.
α – степень диссоциации.
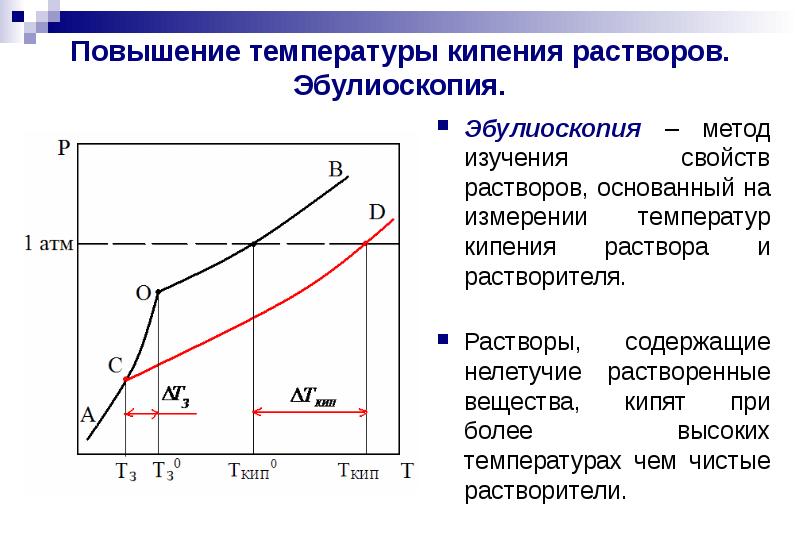
Повышение температуры кипения или понижение температуры затвердевания (кристаллизации). Второй закон Рауля
Равновесное давление паров жидкости имеет тенденцию к увеличению с ростом температуры, жидкость начинает кипеть, при уравнивании давления ее паров и внешнего давления.
При наличии нелетучего вещества, давление паров раствора снижается, и раствор будет закипать при более высокой температуре, по сравнению с температурой кипения чистого растворителя.
Температура замерзания жидкости также определяется той температурой, при которой давления паров жидкой и твердой фаз уравниваются.
Ф.М. Рауль доказал, что повышение температуры кипения, так же как и понижение температуры замерзания разбавленных растворов нелетучих веществ, прямо пропорционально моляльной концентрации раствора и не зависит от природы растворённого вещества. Это правило известно как Второй закон Рауля:
K — криоскопическая константа,
mв-ва — моляльность вещества в растворе.
Растворы электролитов не подчиняются Законам Рауля. Но для учёта всех несоответствий Вант-Гофф предложил ввести в приведённые уравнения поправку в виде изотонического коэффициента i, учитывающего процесс распада на ионы молекул растворённого вещества:
Осмотическое давление раствора
Некоторые материалы имеют способность к полупроницаемости, т.е. им свойственно пропускать частицы определенного вида и не пропускать частицы другого вида.
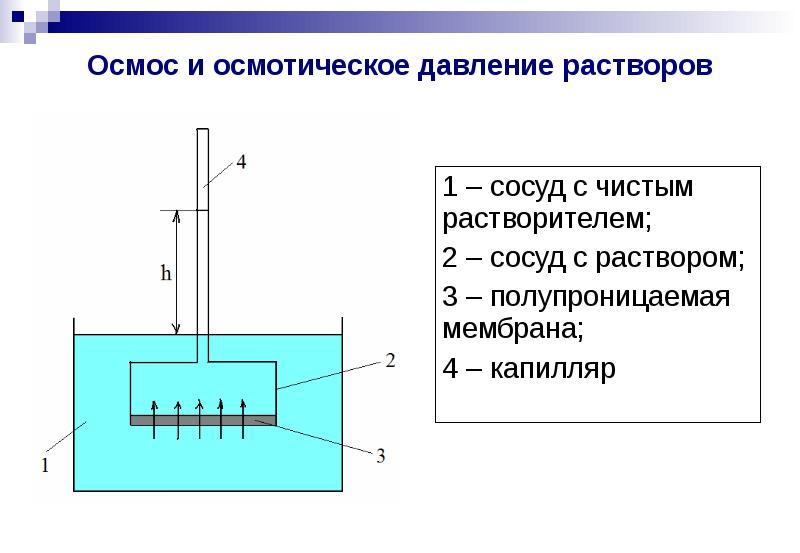
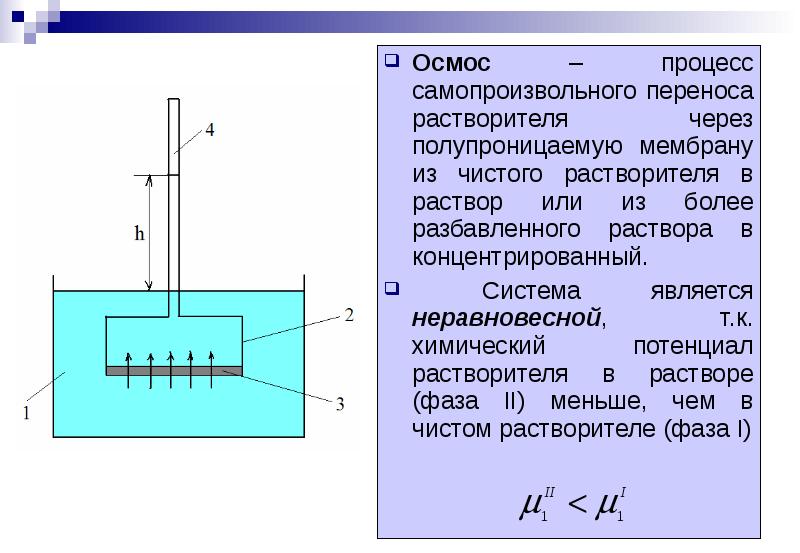
Перемещение молекул растворителя (но не растворенного, в нем вещества), через полупроницаемую мембрану в раствор с большей концентрацией из более разбавленного представляет собой такое явление как осмос.
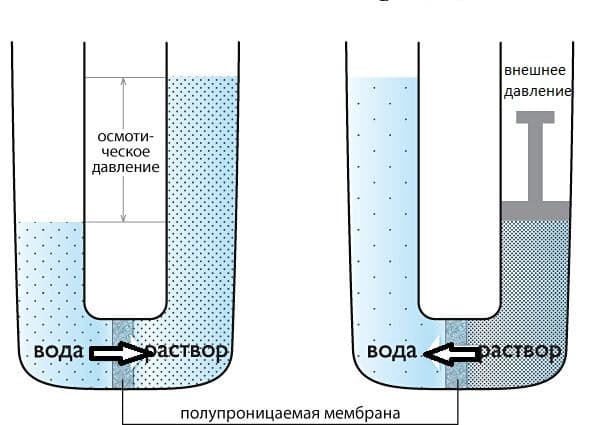
ОСМОС
Представим два таких раствора, которые разделены полупроницаемой мембраной, как показано на рисунке выше. Растворы стремятся к выравниванию концентраций, поэтому вода будет проникать в раствор, тем самым уменьшая его концентрацию.
Для того, чтобы осмос приостановить, необходимо приложить внешнее давление к раствору. Такое давление, которое требуется приложить, называется осмотическим давлением.
Осмотическое давление и концентрацию раствора неэлектролита позволяет связать уравнение Вант — Гоффа, которое напоминает уравнение идеального газа Клапейрона – Менделеева:
где C — молярная концентрация раствора, моль/м 3 ,
R — универсальная газовая постоянная (8,314 Дж/моль·К);
T — абсолютная температура раствора.
Преобразуем уравнение следующим образом:
C = n/V = m/(M·V)
π = т·R·T / M·V или
Для растворов электролитов осмотическое давление определяется уравнением, в которое входит изотонический коэффициент:
где i — изотонический коэффициент раствора.
Для растворов электролитов i > 1, а для растворов неэлектролитов i = 1.
Если полупроницаемой перегородкой разделены два раствора, имеющие одинаковое осмотическое давление, то перемещение растворителя через перегородку отсутствует. Такие растворы называются изотоническими.
Раствор, с меньшим осмотическим давлением, по сравнению с более концентрированным раствором, называют гипотоническим, а раствор с большей концентрацией – гипертоническим.
План:
1 Введение
2. Осмос
3.Осмотическое давление неэлектролитов Закон Вант - Гоффа
4.Осмотическое давление
5.Осмотическое давление электролитов, изотонический коэффициент
6.Гипо,- гипер- и изотонические растворы, их использование в медицинской практике
7.Заключение
8.Список литературыВведение
Коллигативные свойства растворов — это те свойства, которые при данных условиях оказываются равными и независимыми от химической природы растворённого вещества; свойства растворов, которые зависят лишь от количества кинетических единиц и от их теплового движения
Коллигативные свойства(хим.) — так называет В. Оствальд, по предложению Вундта, те свойства, которые приданных условиях и для данной группы тел оказываются равными и независимыми от их химической природы и большей или меньшей элементарной сложности. Таковы, напр.: равенство давлений газов (при данной температуре опыта), если они заключены в равные по объему приборы в равно молекулярных количествах (положение Авогадро-Ампера, см. соотв. статью); равенство давлений паров, т. е. температур кипения, итемператур замерзания жидких изосмотических (см.) растворов, образованных данной жидкостью и любыми растворенными в ней телами и т. д. К. свойствами мы почти исключительно пользуемся для установления молекулярных весов.
Весьма важным в биологическом отношении свойством растворов является осмос.
В природе часто растворы отделяются отрастворителя мембранами, проницаемыми лишь для частиц растворителя. В этом случае растворенное вещество диффундировать в растворитель не может, и будет наблюдаться только переход растворителя в раствор, т е растворитель будет перемещаться в обоих направлениях, но все же в раствор будет переходить его больше чем в обратном направлении. Так, например, если отверстие стеклянной трубки затянуть мембраной из целлофана иликоллодия, проницаемой для воды, но непроницаемой для сахарозы: трубку заполнить концентрированным раствором сахарозы и опустить в сосуд с водой, то спустя некоторое время отмечается значительное повышение уровня жидкости в трубке. Анализ содержимого во внешнем сосуде показывает отсутствие сахарозы. При этом происходит перемещение только молекул растворителя сквозь мембрану.
Осмос- это проникновениемолекул растворителя через полупроницаемую мембрану из растворителя в раствор.
Односторонние перемещение растворителя через мембрану можно объяснить тем что с поверхности мембраны снизу соприкасается больше молекул растворителя чем сверху, где часть объема занята молекулами растворенного вещества, не проникающего сквозь нее. Поэтому в единицу времени вверх будет переходить больше молекулрастворителя, чем в обратном направлении.
Механизм осмоса легко представить на основе изотермической перегонки. Пусть полупроницаемая мембрана, имеющая микропоры, разделяет растворитель и раствор с концентрацией С . В пору, ограниченную с одной стороны растворителем, а с другой раствором, идет испарение. Вследствие превышения по закону Рауля упругости насыщенного пара над раствором молекулы растворителя изпарообразной фазы концентрируются, переходя в раствор.
Если поместить в цилиндр концентрированный раствор какого либо вещества, например сахара, а поверх него осторожно налить слой более разбавленного раствора сахара то вначале сахар и вода будут распределены в объеме раствора неравномерно. Однако через некоторое время молекулы сахара и воды вновь равномерно распределятся по всему объему жидкости.
Этопроисходит потому, что молекулы сахара, беспорядочно двигаясь, проникают как из концентрированного раствора в разбавленный, так и в обратном направлении но при этом в течении любого промежутка времени из более концентрированного раствора в менее концентрированный переходит больше молекул сахара чем из разбавленного раствора в концентрированный. Точно так же.
- иметь представления о следующих понятиях и явлениях:
- осмос, осмотическое давление (закон Вант-Гоффа), его роль.
- закон Рауля о давлении паров растворителя над раствором и изменении температур кипения и замерзания растворов (следствия закона Рауля).
Коллигативные свойства – это свойства, которые не зависят от природы частиц растворенного вещества, а зависят только от концентрации частиц в растворе.
Коллигативными свойствами разбавленных растворов являются:
- осмотическое давление (Закон Вант-Гоффа)
- давление насыщенного пара растворителя над раствором (Закон Рауля)
- температура кипения раствора (1следствие из закона Рауля)
- температура кристаллизации раствора (2 следствие из закона Рауля)
Свойства неэлектролитов
Осмосом называется самопроизвольное перемещение молекул растворителя через полупроницаемую мембрану из раствора меньшей концентрации в раствор большей концентрации. В результате протекания осмоса возникает осмотическое давление раствора. Гипертоническим раствором называют тот раствор, у которого осмотическое давление больше. Гипотоническим раствором – раствор с меньшим осмотическим давлением. Изотоничные растворы – это растворы с одинаковой величиной осмотического давления.
| Растительная клетка (С >) (внутриклеточный раствор) |
| Мем-брана |
| Внешняя среда (С . Сm , где Dtкип = t кип р-ра – t кип н2o, 0 С ; Kэб – эбулиоскопическая константа растворителя (Kэб н2о ); Сm- моляльная концентрация растворенного вещества, моль/1000г растворителя.
II следствие закона Рауля: Понижение температуры замерзания раствора прямо пропорционально молярной концентрации растворенного вещества: Dtзам = Kкр . Сm , где Dt = t зам.н2о – t зам р-ра, 0 С; Kкр - криоскопическая константа растворителя (Ккр н2о =1,86); Сm- моляльная концентрация растворенного вещества, моль/1000г растворителя.
Эти уравнения справедливы только для растворов, в которых отсутствует взаимодействие частиц, т.е. для идеальных растворов. В реальных растворах имеют место межмолекулярные взаимодействия между молекулами вещества и растворителя, которые могут приводить либо к процессам диссоциации, либо к процессам ассоциации молекул. Диссоциация молекул вещества в водном растворе характерна для сильных электролитов. В результате диссоциации число частиц увеличивается. Доля (i) образовавшихся частиц определяется как отношение общего числа частиц к первоначальному числу молекул. Она зависит от степени диссоциации электролита и от числа частиц, на которые распадается молекула: i = (n -1)a + 1, i – получил название изотонический коэффициент, n – число частиц (ионов), на которые распадается молекула, a – степень диссоциации (в долях).
Примеры расчетов температур кипения, замерзания, осмотического давления растворов различных концентраций . Пример 1. Вычислить температуру замерзания, кипения раствора этилового спирта с процентной концентрацией (w), равной 40 %. Решение: Вычислим температуру замерзания раствора исходя из II следствия закона Рауля: Dtзам = Kкр . Сm, однако для решения необходимо перейти от одного вида концентрации к другому: w [m в-ва, г \ 100г р-ра] ® Сm[ n молей \ 1000 г р-ля ] 1. Перейдем от массы вещ-ва (m) к молям (n) через пропорцию: или по формуле х(n) = = моль/100р-ра, 2. Перейдем от массы раствора к массе растворителя: m р-ля = m р-ра - m в-ва = 100 – 40 = 60г р-ля 2. Через пропорцию выразим Сm : 0,87 молей С2Н5ОН содержит в 60 г растворителя
х (Сm) = = 14,5 молей/1000г р-ля 4. По формуле Dtзам = Kкр . Сm найдем Dt: Dt = 1,86 . 14,5 = 26,97 0 C 5. Dt = tзам н2о – tзамр-ра Þ tзам р-ра = tзам н2о – Dt = 0 - 26,97 = -26,97 0 C - температура замерзания 40 % раствора этилового спирта. Вычислим температуру кипения раствора исходя из I следствия закона Рауля: Dtкип = Kэб . Сm, Сm = 14,5 моль/1000р-ля (см. выше) Из формулы найдем Dt: Dt = 0,516 . 14,5 = 7,48 0 C Dt = tкипр-ра – tкип н2о Þ tкип р-ра = tкип н2о + Dtкип = 100 + 7,48 = 107,48 0 C- температура кипения 40% раствора этилового спирта. Решение: Для растворов электролитов Росм(NaCl ) = i·См·R·T Þ
См = (1) Условие изотоничности означает, что Росм(NaCl ) = Росм крови = 800 кПа, i = (n-1)·a + 1= (2 - 1) · 0,9 = 1,9 NaCl Û Na + +Cl - , где n = 2, a = 0,9
Подставим найденные значения в формулу (1) См = 0,17 моль/л – концентрация хлорида натрия, которая создает осмотическое давление 800 кПа. Вы можете изучить и скачать доклад-презентацию на тему Коллигативные свойства растворов. Презентация на заданную тему содержит 20 слайдов. Для просмотра воспользуйтесь проигрывателем, если материал оказался полезным для Вас - поделитесь им с друзьями с помощью социальных кнопок и добавьте наш сайт презентаций в закладки!
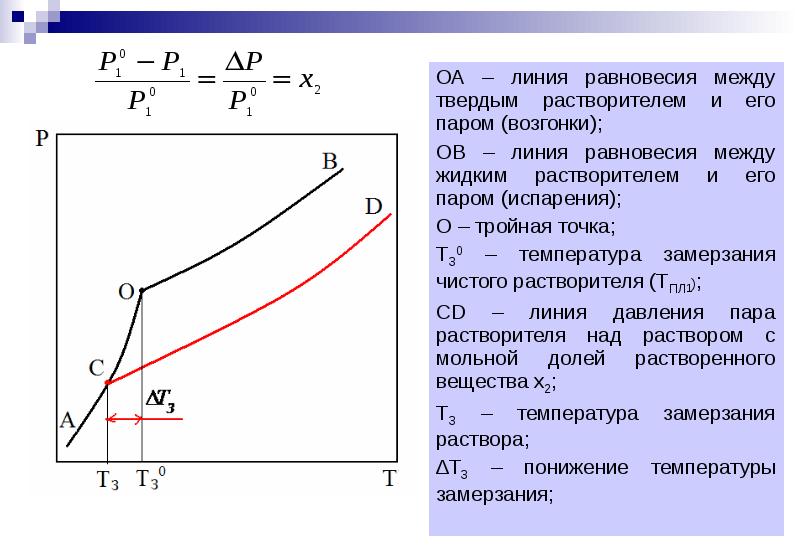
Коллигативными называются свойства растворов, зависящие от типа растворителя и концентрации растворенного вещества, но не зависящие от природы частиц растворенного вещества. Коллигативные свойства проявляются в условиях равновесия двух фаз: 1) относительное понижение давления пара растворителя над раствором; 2) понижение температуры замерзания раствора по сравнению с чистым растворителем; 3) повышение температуры кипения раствора; 4) осмотическое давление. Понижение температура замерзания растворов. Криоскопия. Криоскопия – метод изучения свойств растворов, основанный на измерении температур замерзания раствора и растворителя. При охлаждении разбавленного раствора до температуры замерзания из него начинает кристаллизоваться чистый растворитель. Температура замерзания ТЗ (ТПЛ ) – температура, при которой раствор данного состава находится в равновесии с кристаллами чистого растворителя. Растворы замерзают при более низких Т, чем чистый растворитель. Понижение ТЗ является следствием понижения давления пара растворителя над раствором. Читайте также:
|