Реферат 7 класс давление газа
Обновлено: 05.07.2024
Тип урока: комбинированный на основе исследовательской деятельности.
- установить причину существования давления в газах с точки зрения молекулярного строения вещества;
- выяснить:
- от чего зависит давление газа
- как можно его изменить.
- сформировать знания о давлении газа и природе возникновения давления на стенки сосуда, в котором находится газ;
- сформировать умение объяснять давление газа на основе учения о движении молекул, зависимости давления от объема при постоянной массе и температуре, а также и при изменении температуры;
- развить общеучебные знания и умения: наблюдать, делать выводы;
- способствовать привитию интереса к предмету, развития внимания, научного и логического мышления учащихся.
Оборудование и материалы к уроку: компьютер, экран, мультимедиапроектор, презентация к уроку, колба с пробкой, штатив, спиртовка, шприц, воздушный шар, пластиковая бутылка с пробкой.
- Проверка домашнего задания.
- Актуализация знаний.
- Объяснение нового материала.
- Закрепление пройденного материала на уроке.
- Итог урока. Домашнее задание.
Я предпочитаю то, что можно увидеть, услышать и изучить. (Гераклит) (Слайд 2)
– Это девиз нашего урока
– На прошлых уроках мы с вами узнали о давлении твердых тел, от каких физических величин зависит давление.
1. Повторение пройденного материала
1. Что такое давление?
2. От чего зависит давление твердого тела?
3. Как давление зависит от силы, приложенной перпендикулярно опоре? Каков характер этой зависимости?
4. Как давление зависит от площади опоры? Каков характер этой зависимости?
5. В чем причина давления твердого тела на опору?
Качественная задача.
Одинаковы ли силы, действующие на опору, и давление в обоих случаях? Почему?
Проверка знаний. Тестирование (проверка и взаимопроверка)
Тест
1. Физическая величина, имеющая размерность паскаль (Па), называется:
а) сила; б) масса; в) давление; г) плотность.
2. Силу давления увеличили в 2 раза. Как изменится давление?
а) уменьшится в 2 раза; б) останется прежним; в) увеличится в 4 раза; г) увеличится в 2 раза.
3. Давление можно рассчитать по формуле:
4. Какое давление на пол оказывает ковёр весом 200 Н, площадью 4 м 2 ?
а) 50 Па; б) 5 Па; в) 800Па; г) 80 Па.
5. Два тела равного веса поставлены на стол. Одинаковое ли давление они производят на стол?
2. Актуализация знаний (в форме беседы)
– Почему воздушные шары и мыльные пузыри круглые?
Учащиеся надувают воздушные шары.
– Чем мы заполнили шары? (Воздухом) Чем еще можно заполнить шары? (Газами)
– Предлагаю сжать шары. Что вам мешает сжать шары? Что действует на оболочку шара?
– Возьмите пластиковые бутылки, закройте пробкой и попробуйте сжать.
– О чем пойдет речь на уроке?
– Тема урока: Давление газа
3. Объяснение нового материала
Газы, в отличии от твёрдых тел и жидкостей, заполняют весь сосуд, в котором находятся.
Стремясь расшириться, газ оказывает давление на стенки, дно и крышку любого тела, с которым он соприкасается.
(Слайд 9) Картинки стальных баллонов, в которых находится газ; камеры автомобильной шины; мяча
Давление газа обусловлено иными причинами, чем давление твердого тела на опору.
Вывод: давление газа на стенки сосуда (и на помещенное в газ тело) вызывается ударами молекул газа.
Например, число ударов молекул воздуха, находящегося в комнате, о поверхность площадью 1 см 2 за 1 с выражается двадцатитрехзначным числом. Хотя сила удара отдельной молекулы мала, но действие всех молекул на стенки сосуда значительно, оно и создает давление газа.
Учащиеся самостоятельно работают с учебником. Читают опыт с резиновым шаром под колоколом. Как объяснить этот опыт? (стр.83 рис. 91)
Учащиеся объясняют опыт.
(Слайд 11) Просмотр видеофрагмента с объяснением опыта для закрепления материала.
(Слайд 12) Минутка отдыха. Зарядка для глаз.

(Слайд 14) ИМЕЮТ ЛИ ГАЗЫ ОБЪЁМ? ЛЕГКО ЛИ ИЗМЕНИТЬ ОБЪЁМ ГАЗОВ? ЗАНИМАЮТ ЛИ ГАЗЫ ВЕСЬ ПРЕДОСТАВЛЯЕМЫЙ ИМ ОБЪЁМ? ПОЧЕМУ?ПОЧЕМУ? ИМЕЮТ ЛИ ГАЗЫ ПОСТОЯННЫЙ ОБЪЁМ И СОБСТВЕННУЮ ФОРМУ? ПОЧЕМУ?

(Слайд 15) У учащихся сделаны модели из шприцов. Выполнение опыта.
Учащиеся делают вывод: при уменьшении объёма газа его давление увеличивается, а при увеличении объёма давление уменьшается при условии, что масса и температура газа остаются неизменными.
(Слайд 16) Опыт с колбой
– Как изменится давление газа, если нагреть его при постоянном объеме?
При нагревании давление газа в колбе будет постепенно возрастать до тех пор, пока пробка не вылетит из склянки.
Учащиеся делают вывод: давление газа в закрытом сосуде тем больше, чем выше температура газа,при условии, что масса газа и объём не изменяются. (Слайд 17)

Газы, заключенные в сосуде, можно сжимать или сдавливать, уменьшая при этом их объем. Сжатый газ равномерно распределяется во всех направлениях. Чем сильнее вы сжимаете газ, тем выше будет его давление.
Учащиеся делают вывод: давление газа тем больше, чем чаще и сильнее молекулы ударяют о стенки сосуда
4. Закрепление пройденного материала на уроке.
(Слайд 18) Подумай-ка
- молекулы начинают быстрее двигаться,
- молекулы начинают медленнее двигаться,
- среднее расстояние между молекулами газа уменьшается,
- среднее расстояние между молекулами газа увеличивается.
- Чем вызвано давление газа?
- Почему давление газа увеличивается при его сжатии и уменьшается при расширении?
- Когда давление газа больше: в холодном или горячем состоянии? Почему?
Ответ 1. Давление газа вызвано ударами молекул газа о стенки сосуда или о помещенное в газ тело
Ответ 2. При сжатии плотность газа увеличивается, из-за чего возрастает число ударов молекул о стенки сосуда. Следовательно, увеличивается и давление. При расширении плотность газа уменьшается, что влечет за собой уменьшение числа ударов молекул о стенки сосуда. Поэтому давление газа уменьшается
Ответ 3. Давление газа больше в горячем состоянии. Это связано с тем, что молекулы газа при повышении температуры начинают двигаться быстрее, из-за чего удары их становятся чаще и сильнее.
1. Почему при накачивании воздуха в шину автомобиля с каждым разом становится все труднее двигать ручку насоса?

2. Массы одного и того же газа, находящегося в разных закрытых сосудах при одинаковой температуре, одинаковы. В каком из сосудов давление газа наибольшее? Наименьшее? Ответ объясните

3. Объясните появление вмятины на мяче

Мяч при комнатной температуре

Мяч на снегу в морозный день
Решать загадки можно вечно.
Вселенная ведь бесконечна.
Спасибо всем нам за урок,
А главное, чтоб был он впрок!

Из курса физики 7 класса известно, что газ — это состояние вещества, при котором молекулы имеют достаточную скорость и энергию, чтобы преодолевать силы взаимного притяжения и удаляться друг от друга, заполняя весь предоставленный объём. Важнейшей характеристикой газа является давление. Рассмотрим эту тему подробнее, приведём формулу давления газа.
Давление в газах
Как известно из механики, давление — это мера распределения силы по некоторой площади. Она равна отношению величины силы, действующей на тело, к площади, на которой распределено действие.
Молекулы газа, заполняя предоставленный объём сосуда, непрерывно сталкиваются друг с другом и со стенками. Силы соударений отдельных молекул сливаются в одну общую силу. При этом из-за хаотичности движения молекул в любой точке газа есть молекулы, движущиеся во всех направлениях. А значит, эта сила есть в любой точке газа, и действует она также во всех направлениях. Причём, чем большую область мы будем рассматривать, тем больше в ней будет молекул, и тем большая сила будет действовать на границы этой области.
Получается, что в любой точке газа соударения молекул создают некоторую силу, пропорциональную площади, причём отношение этих двух величин постоянно. Это и есть давление газа.
Связь температуры и давления
Итак, давление газа создаётся хаотически движущимися молекулами в результате постоянных соударений. Следовательно, чем больше средняя скорость движения молекул, тем больше будет давление газа. А мера средней скорости молекул — это температура. Значит, если газ содержится в некотором постоянном объёме, то его давление будет пропорционально температуре. Данный закон был установлен в конце XVIII в. Ж. Шарлем и получил его имя.
Закон Шарля гласит, что отношение давления газа к его абсолютной температуре при неизменном объёме остаётся постоянным:
- $p$ — давление газа;
- $T$ — абсолютная температура газа.
Закон Шарля — это один из газовых законов молекулярно-кинетической теории (МКТ), связывающих макроскопические газовые параметры: давление, температуру и объём. Закон Шарля описывает ситуацию, когда объём газа постоянен.

Рис. 2. Газовые законы.
Основное уравнение МКТ
Поскольку давление газа обуславливается хаотическим движением молекул, то его величина может быть определена, исходя из концентрации молекул, массы и средней скорости молекулы:
- $p$ — давление газа;
- $n$ — число молекул в единице объёма (концентрация);
- $m_0$ — масса молекулы;
- $ v_^2$ — среднеквадратичная скорость молекулы.
Данное соотношение называется основным уравнением МКТ. Оно связывает средние параметры одной молекулы с давлением газа. Температура в эту формулу не входит, однако она неявно присутствует в ней в виде среднеквадратичной скорости, которая пропорциональна температуре.

Рис. 3. Молекулярно-кинетическая теория.
Что мы узнали?
Давление газа обуславливается постоянными ударами молекул газа о стенки сосуда и между собой. Давление при постоянном объёме растёт при росте температуры. Величина давления может быть определена с помощью основного уравнения МКТ.
Учение о свойствах вещества в различных агрегатных состояниях основывается на представлениях об атомно-молекулярном строении материального мира. В основе молекулярно-кинетической теории строения вещества (МКТ) лежат три основных положения:
- все вещества состоят из мельчайших частиц (молекул, атомов, элементарных частиц), между которыми есть промежутки;
- частицы находятся в непрерывном тепловом движении;
- между частицами вещества существуют силы взаимодействия (притяжения и отталкивания); природа этих сил электромагнитная.
Значит, агрегатное состояние вещества зависит от взаимного расположения молекул, расстояния между ними, сил взаимодействия между ними и характера их движения.
Сильнее всего проявляется взаимодействие частиц вещества в твердом состоянии. Расстояние между молекулами примерно равно их собственным размерам. Это приводит к достаточно сильному взаимодействию, что практически лишает частицы возможности двигаться: они колеблются около некоторого положения равновесия. Они сохраняют форму и объем.
Свойства жидкостей также объясняются их строением. Частицы вещества в жидкостях взаимодействуют менее интенсивно, чем в твердых телах, и поэтому могут скачками менять свое местоположение – жидкости не сохраняют свою форму – они текучи. Жидкости сохраняют объем.
Газ представляет собой собрание молекул, беспорядочно движущихся по всем направлениям независимо друг от друга. Газы не имеют собственной формы, занимают весь предоставляемый им объем и легко сжимаются.
Существует еще одно состояние вещества – плазма. Плазма — частично или полностью ионизованный газ, в котором плотности положительных и отрицательных зарядов практически одинаковы. При достаточно сильном нагревании любое вещество испаряется, превращаясь в газ. Если увеличивать температуру и дальше, резко усилится процесс термической ионизации, т. е. молекулы газа начнут распадаться на составляющие их атомы, которые затем превращаются в ионы.
Модель идеального газа. Связь между давлением и средней кинетической энергией.
Для выяснения закономерностей, которым подчиняется поведение вещества в газообразном состоянии, рассматривается идеализированная модель реальных газов – идеальный газ. Это такой газ, молекулы которого рассматриваются как материальные точки, не взаимодействующие друг с другом на расстоянии, но взаимодействующие друг с другом и со стенками сосуда при столкновениях.
Называется состояние веществ
. и давление. Жидкость есть агрегатное состояние вещества, сочетающее в себе черты твердого состояния (сохранение объема, определенная прочность на разрыв) и газообразного (изменчивость формы). Для жидкости характерны ближний порядок в расположении частиц (молекул, атомов) .
Идеальный газ
Идеальный газ – это модель, придуманная учеными для познания газов, которые мы наблюдаем в природе реально. Она может описывать не любой газ. Не применима, когда газ сильно сжат, когда газ переходит в жидкое состояние. Реальные газы ведут себя как идеальный, когда среднее расстояние между молекулами во много раз больше их размеров, т.е. при достаточно больших разрежениях.
Свойства идеального газа:
- расстояние между молекулами много больше размеров молекул;
- молекулы газа очень малы и представляют собой упругие шары;
- силы притяжения стремятся к нулю;
- взаимодействия между молекулами газа происходят только при соударениях, а соударения считаются абсолютно упругими;
- молекулы этого газа двигаются беспорядочно;
- движение молекул по законам Ньютона.
Давление – физическая величина, равная отношению силы F, действующей на элемент поверхности перпендикулярно к ней, к площади S этого элемента .
p = F/S Единица давления в СИ паскаль [Па]
До настоящего времени употребляются внесистемные единицы давления:
миллиметры ртутного столба
1 атм = = 760 мм рт. ст. = 1013 гПа.
Как возникает давление газа? Каждая молекула газа, ударяясь о стенку сосуда, в котором она находится, в течение малого промежутка времени действует на стенку с определенной силой. В результате беспорядочных ударов о стенку сила со стороны всех молекул на единицу площади стенки быстро меняется со временем относительно некоторой (средней) величины.
Давление газа
давление газа на стенку сосуда


Жидкостные манометры:
- открытый – для измерения небольших давлений выше атмосферного
- закрытый — для измерения небольших давлений ниже атмосферного, т.е. небольшого вакуума

Металлический манометр
Основной его частью является изогнутая трубка А, открытый конец которой припаян к трубке В, через которую поступает газ, а закрытый – соединен со стрелкой. Газ поступает через кран и трубку В в трубку А и разгибает её. Свободный конец трубки, перемещаясь, приводит в движение передающий механизм и стрелку. Шкала градуирована в единицах давления.


Основное уравнение молекулярно-кинетической теории идеального газа., Основное уравнение МКТ
. молекул газа находится в определённом объёме. Например, накачивая шину или сжимая её, мы заставляем газ сильнее давить на стенки камеры. Во-вторых, от того, какова температура газа. Обычно изменение давления . передавая ее окружающим телам, если газ сжимается. В частности, температура газа остается достаточно постоянной, если расширение или сжатие газа производится очень медленно, а передача теплоты .
- n = N/V – число молекул в единице объема, или концентрация молекул;
v 2 — средняя квадратичная скорость движения молекул.
Так как средняя кинетическая энергия поступательного движения молекул E = m 0 *v 2 /2, то домножив основное уравнение МКТ на 2, получим p = 2/3· n·(m0 · v 2 )/2 = 2/3·E·n
Давление газа равно 2/3 от средней кинетической энергии поступательного движения молекул, которые содержатся в единичном объеме газа.
Объединенный газовый закон.
термодинамическими параметрами газа.
объем V, давление р и температура Т.
В любом термодинамическом процессе изменяются параметры газа, определяющие его состояние.
объединенным газовым законом.
p = nkT
p = nkT
где n – концентрация молекул, N – общее число молекул, V – объем газа
Тогда получим или
Так как при постоянной массе газа N остается неизменным, то Nk – постоянное число, значит
При постоянной массе газа произведение объема на давление, деленное на абсолютную температуру газа, есть величина одинаковая для всех состояний этой массы газа.
Уравнение Клайперона можно записать в другой форме.
p = nkT,
Здесь N – число молекул в сосуде, ν – количество вещества, N А – постоянная Авогадро, m – масса газа в сосуде, M – молярная масса газа. В итоге получим:
универсальной (молярной) газовой постоянной
R = 8,31 Дж/моль·К
уравнением состояния идеального газа
Для одного моля любого газа это соотношение принимает вид: pV=RT
физический смысл молярной газовой постоянной
Запишем уравнение pV=RT для нагретого газа: p ( V + ΔV ) = R (T + 1)
и вычтем из этого равенства уравнение pV=RT , соответствующее состоянию газа до нагревания. Получим pΔV = R
ΔV = SΔh, где S – площадь основания цилиндра. Подставим в полученное уравнение:
pS = F – сила давления.
Понятие реального газа
. молярный объём. Вводя эти поправки - получим уравнение Ван-дер-Ваальса для моля газа (уравнение состояния идеальных газов): (p+a/V2m) (Vm-b)=RT 4. Изотермы Ван-дер-Ваальса Для исследования поведения реального газа рассмотрим изотермы Ван-дер-Ваальса - кривые .
Получим FΔh = R, а произведение силы на перемещение поршня FΔh = А – работа по перемещению поршня, совершаемая этой силой против внешних сил при расширении газа.
Таким образом, R = A .
Универсальная (молярная) газовая постоянная численно равна работе, которую совершает 1 моль газа при изобарном нагревании его на 1 К.
Примеры похожих учебных работ
Механика жидкостей и газов в законах и уравнениях
. чтобы Создать и поддерживать постоянным течение жидкости в трубе, необходимо наличие между кон-цами трубы разности давлений. Поскольку при уста-новившемся течении жидкость движется без ускоре-ния, необходимость действия сил давления указывает на то, .
Свойства и законы идеального газа
. закон Шарля, закон Гей-Люссака, закон Бойля-Мариотта, а также закон Авогадро, закон Дальтона. Закон Бойля-Мариотта. Изотерма ЗАКОН БОЙЛЯ -- МАРИОТТА, один из основных газовых законов, который описывает изотермические процессы в идеальных газах. .
Растворимость газов в нефти
. плохо растворяется азот. Растворимость газов повышается с ростом содержания в нефтях парафиновых углеводородов. При высоком содержании в нефти ароматических углеводородов ухудшается растворимость в ней газов. Малорастворимые газы (метан, азот) лучше .
Подсчет запасов и оценка ресурсов нефти и газа
. 120 км северо-восточнее г. Нарьян-Мара, административного центра округа, и в 80 км к северо-западу от п. Харьягинский. нефть газ месторождение геологический Непосредственно на территории рассматриваемой площади населенных .
Универсальная газовая постоянная. Основные законы идеального газа (2)
. — уравнение состояния идеального газа: pV = RT (для 1 моль газа) где R — универсальная газовая постоянная = pV/T Расчет показывает, что при атмосферном давлении 1 атм. = 101,3 кПа., объеме .
Законы идеальных газов
. долетев до стенки. Вместо сил, действующих на налетающие молекулы, можно по третьему закону Ньютона ввести равные молекулы пристеночного слоя. Пусть P- средняя сила давления газа .

Недавно мы рассмотрели такую величину, как давление на примере твердых тел. Но, оказывается, давление может создаваться и газами. На этом уроке мы рассмотрим, каким образом возникает давление газа и от чего зависит это давление.

В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобретя в каталоге.
Получите невероятные возможности



Конспект урока "Давление газа"
Давление газа
«Вызывает изумление
В этой теме речь пойдёт о том, каким образом могут оказывать давление газы.
В газах молекулы расположены друг от друга на большом расстоянии, поэтому, силы взаимного притяжения между молекулами практически отсутствуют. Известно также, что газы легко сжимаются. Молекулы газа двигаются беспорядочно, занимая весь предоставленный им объём. Молекулы сталкиваются не только друг с другом, но и ударяются о стенки сосуда. Именно эти удары и создают давление. Сила удара одной молекулы ничтожно мала, но ведь количество молекул даже в маленьком сосуде очень велико.

Рассмотрим классический опыт: возьмем завязанный шарик с небольшим количеством воздуха и накроем его стеклянным сосудом. Если выкачать из сосуда воздух, то объём воздушного шарика увеличится. Почему же это произошло? Дело в том, что изначально по шарику ударяли молекулы воздуха внутри сосуда, противодействуя ударам молекул внутри шарика. Таким образом, оболочка шарика сохраняла свой объём. Но когда воздух был откачен из сосуда, во много раз уменьшилось количество молекул воздуха внутри него. Ударов по шарику снаружи стало гораздо меньше, но вот количество молекул внутри шарика не изменилось. Это позволило газу внутри шарика расширяться до тех пор, пока давление газа внутри не стало равно давлению газа снаружи. Из этого можно сделать вывод, что при увеличении объёма, давление газа уменьшается. Но если мы вновь наполним сосуд воздухом, то шарик снова сдуется. Значит, при уменьшении объёма, давление увеличивается.
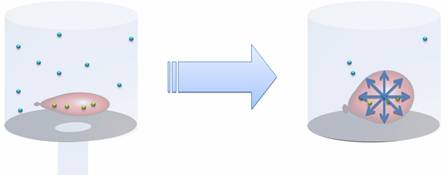
Следует понимать, что эти утверждения верны только в том случае, если речь идет о неизменной массе газа, находящейся при неизменной температуре. Также следует отметить: когда воздух был откачен из сосуда, форма шарика действительно стала шарообразной (а не вытянутой, как это было изначально). Это значит, что газ давит на оболочку шарика (или стенки сосуда) одинаково по всем направлениям. Это объясняется беспорядочным движением молекул. Они двигаются в случайных направлениях, но их число настолько велико, что можно с уверенностью сказать, что во всех направлениях летит одинаковое число молекул. В результате этого на каждый маленький кусочек площади поверхности шарика приходится одинаковое число ударов, то есть, создается одинаковое давление.
Проведем еще один опыт: возьмем цилиндр с подвижным поршнем и поместим туда некоторое количество газа.
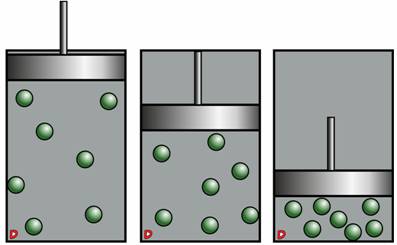
Если поршень будет двигаться, то можно изменять объём газа, при этом сохраняя его массу. Таким образом, плотность газа увеличиться, то есть на единицу объёма будет приходиться большее число молекул газа. В этом случае, они значительно чаще будут ударяться о стенки сосуда. То есть, таким способом можно увеличить давление. Это еще раз доказывает, что при уменьшении объёма газа постоянной массы и температуры, давление увеличивается, а при увеличении объёма – давление уменьшается.
Если плотно закрыть пластиковую бутылку и сжать её, то можно почувствовать значительное сопротивление – молекулы газа будут давить на стенки бутылки изнутри, не давая вам сжать её.
Поставим опыт: Не будем изменять ни массу газа, ни его объём, а просто нагреем газ в плотно закрытом сосуде. В этом случае давление газа увеличится. Это объясняется тем, что при увеличении температуры, молекулы газа начинают двигаться быстрее, а, следовательно, будут чаще ударяться о стенки сосуда. То есть, при увеличении температуры газа постоянной массы и объёма, давление газа увеличивается, и, наоборот, при уменьшении температуры, давление газа уменьшается. Если слегка заткнуть стеклянную бутылку пробкой и нагреть бутылку, то пробка выскочит из горлышка под давлением газа.
Зависимость давления газа от температуры нередко используется людьми. Например, чтобы поместить большое количество газа в сравнительно небольшой объём, газ охлаждают и закачивают в баллон. После того, как газ вновь нагревается, в баллоне создается очень высокое давление. Именно поэтому на таких баллонах, как правило, пишут предупреждения о том, чтобы баллон ни в коем случае не нагревали и не ударяли (это может привести к взрыву – настолько в баллоне высокое давление).

Примеров давления газа можно привести очень много: это и накачанный мяч, и накачанные шины автомобиля, и атмосферное давление.
Упражнение 1. Из баллона медленно выпустили половину газа и снова закрыли его. Как изменится давление в баллоне?
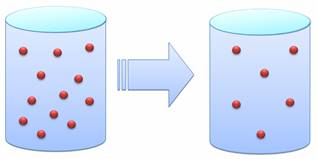
Поскольку молекул газа внутри баллона стало вдвое меньше, они вдвое меньше стали ударяться о стенки баллона. Следовательно, давление уменьшилось вдвое.
Упражнение 2. Одинаковые массы одного и того же газа находятся в двух баллонах: зеленом и синем. Известно, что температура и в том, и в другом баллоне одинакова. В каком баллоне давление будет больше?

По условию задачи, в обоих баллонах одинаковые условия. Из рисунка явно видно, что синий баллон больше зеленого. Поэтому давление в нем будет меньше, поскольку молекулы газа меньше будут ударяться о его стенки.
Упражнение 3. Воздушный шарик завязали и облили его ледяной водой. Из-за этого шарик немного сжался. Можете ли вы объяснить, почему это произошло?
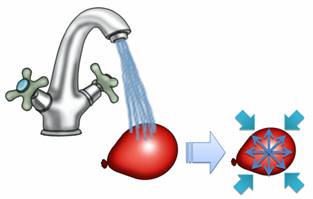
Из-за понижения температуры, давление внутри шарика уменьшилось. В результате внешнее давление сжимало шарик до тех пор, пока внутреннее давление вновь ни стало равным внешнему.
Основные выводы:
– Давление газа – это давление, которое создается в результате ударов молекул о стенки сосуда (или о какое-то другое тело).
– Давление газа одинаково по всем направлениям.
– При неизменной массе и температуре, давление газа тем больше, чем меньше его объём. И, наоборот, давление газа тем меньше, чем больше объём.
– При постоянной массе и объёме, давление можно изменить, изменяя температуру. При нагревании газа, его давление будет увеличиваться, а при охлаждении – наоборот, уменьшаться.
Читайте также:




