Причины возникновения гипертермии реферат
Обновлено: 05.07.2024
Злокачественная гипертермия (ЗГ) — это редкое, врожденное, опасное для жизни расстройство транспорта кальция в скелетных мышцах, сочетающееся с гиперметаболическим состоянием и чаще всего провоцируемое летучими анестезирующими веществами. По существующим оценкам, оно встречается примерно в 1 из 15 000 случаев наркоза.
Доля предрасположенных к этому лиц колеблется, по разным данным, от 1 на 20 до 1 на 5000 человек общей популяции. На детей в возрасте младше 5 лет приходится около половины всех случаев злокачественной гипертермии (ЗГ), а на представителей мужского пола — примерно 3/4 всех известных летальных исходов, связанных с этим расстройством. Ассоциация по злокачественной гипертермии в США находится по адресу: 32 South Main Street, Р. О. Box 1019, Sherbourne, New York 13 460; телефон: 607-674-2420; факс: 607-674-2060.
а) Этиология злокачественной гипертермии. Генетически предрасположенные лица могут страдать от ЗГ после экспозиции к скелетным миорелаксантам (сукцинилхолина хлориду, декаметонию, галламину, d-тубокурарину), всем ингаляционным и некоторым местным анестетикам (главным образом амидного типа, в частности лидокаину, мепивакаину и бупивакаину).
Известно о связи со злокачественной гипертермией (ЗГ) многих других медикаментов, но, судя по имеющимся данным, они редко индуцируют такой криз — скорее обостряют уже начавшийся.
Злокачественная гипертермия (ЗГ) наблюдается также при стрессе, высокой температуре окружающей среды, эмоциональном возбуждении, тяжелых физических нагрузках и инфекциях.
- Генетическая предрасположенность. Предрасположенность к злокачественной гипертермии (ЗГ), вероятно, обусловлена мутацией в гене рианодинового рецептора (RYR). Этот рецептор связан с кальциевым каналом саркоплазматиче-ского ретикулума. Ген RYR локализован в участке 12 - 13.2 хромосомы 19.
б) Патофизиология злокачественной гипертермией (ЗГ). Саркоплазматический ретикулум мышечной клетки в норме поглощает ионы кальция при расслаблении мышцы и высвобождает их в миоплазму во время сокращения. Хотя этот вопрос еще не до конца выяснен, считается, что ЗГ возникает из-за ослабленного поглощения кальция саркоплазматическим ретикулумом.
Повышение миоплазматического уровня Са2+ под действием индуцирующих средств запускает ряд аэробных и анаэробных метаболических процессов, приводящих к избыточному выделению тепла и СО2, а также образованию молочной кислоты. Все эти процессы становятся причиной злокачественной гипертермии (ЗГ).
в) Пробы на предрасположенность к злокачественной гипертермии (ЗГ). В США и Великобритании разработан и стандартизирован ряд инвазивных скрининговых проб на предрасположенность к злокачественной гипертермии (ЗГ). Мышечные биоптаты обрабатывают одним галотаном, одним кофеином или и тем и другим вместе. Ряд неинвазивных проб с эритроцитами (хрупкость), тромбоцитами (тест на нуклеотидное истощение) и мононуклеарными клетками не продемонстрировал достаточной чувствительности и специфичности для применения в клинических условиях.
Пробы на галотаново-кофеиновую контрактуру, по-видимому, более показательны в плане предрасположенности к злокачественной гипертермии (ЗГ), но в связи с относительной редкостью этой реакции (1:15 000 у детей и 1:50 000 у взрослых) практичность этих проб как скринингового метода спорна. Всеобщее внедрение и рутинное использование проб на злокачественную гипертермию (ЗГ) требует их дальнейшей доработки. Выявление клинических эпизодов злокачественной гипертермии (ЗГ) остается задачей анестезиолога во время хирургического вмешательства.
Ассоциация злокачественной гипертермии в США предлагает список центров, проводящих биопсию мышц для кофеиново-галотановой пробы.

г) Ранние признаки злокачественной гипертермии. Лечение ЗГ в значительной мере зависит от раннего выявления этой реакции путем внимательного рутинного мониторинга во время анестезии. Анестезиолог должен заподозрить злокачественную гипертермию (ЗГ) при наличии любого из следующих показателей.
1. Необъяснимая тахикардия.
2. Необъяснимые цианоз и тахипноэ.
3. Ригидность после введения сукцинилхолина или недостаточное расслабление жевательных мышц для интубации. Ригидность может развиться в любое время или вообще не возникнуть.
4. Более поздние признаки. К поздним симптомам относятся выраженная гипертермия, повышенное парциальное давление СО2 в конечной порции выдыхаемого воздуха и в смешанной венозной крови.
Нормальный анестезированный пациент не становится гипертермическим, если температура окружающей среды ниже 25,5 °С. Любое повышение его температуры более чем на 0,5 °С за 15 мин должно вызывать подозрение на ЗГ.
Лихорадка — один из поздних симптомов, связанных с неблагоприятным прогнозом, если лечение еще не начато. К другим признакам относятся гипотензия, комплексные аритмии, метаболический ацидоз, электролитный дисбаланс, гиперкалиемия, гиперкальциемия, острый некроз скелетных мышц, диссеминированное внутрисосудистое свертывание, почечная недостаточность и отек легких.
Злокачественная гипертермия (ЗГ) может также привести к гипоксемии и тяжелому дыхательному и метаболическому ацидозу. Анестезиолог должен определить газовый состав артериальной крови и уровни электролитов. Парциальное давление СО2 в венозной крови может служить даже более ранним диагностическим критерием. Полезны оксигенометрия и измерение парциального давления СО2 в конечной порции выдыхаемого воздуха.
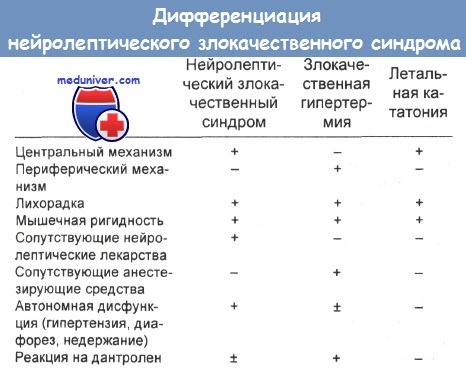
д) Дифференциальная диагностика злокачественной гипертермии (ЗГ) со злокачественным нейролептическим синдромом. Злокачественная гипертермия (ЗГ) появляется через считанные минуты после начала анестезии, а злокачественный нейролептический синдром (ЗНС) обычно развивается за более длительный период. ЗГ — генетическое расстройство, а у ЗНС нет специфической генетической составляющей. Вызывать ЗГ могут сукцинилхолин и общеанестезирующие средства; к пациентам со ЗНС применяли эти средства обычно без токсических последствий.
У пациентов с злокачественной гипертермией (ЗГ) не отмечалось индуцированного нейролептиками злокачественного нейролептического синдрома (ЗНС). В случае предрасположенности к ней нейролептическая аналгезия применялась успешно. Кураре и панкуроний приводят к вялости мышц при ЗНС, но не дают такого эффекта при злокачественной гипертермии (ЗГ).
Надо исключить другие причины синусовой тахикардии, например влияние антихолинергических средств, гиповолемию, гиповентиляцию, гипоксемию, слабый наркоз, тиреотоксический криз, порфирию и нераспознанную феохромоцитому. Среди аритмий отмечались бигеминия, желудочковые экстрасистолы и желудочковая тахикардия; все они могут быть последствиями гиперкалиемии, ацидоза, гипоксемии, гиперпирексемии и повышения уровня катехоламинов в миокарде. Желудочковая фибрилляция является терминальным симптомом.
е) Летальный исход при злокачественной гипертермии. Смерть может наступить в результате прогрессирования эктопической желудочковой аритмии до фибрилляции, острого диссеминированного внутрисосудистого свертывания, острого отека легких, острой миоглобинемии, почечной недостаточности или отека мозга с его смертью.

ж) Профилактика злокачественной гипертермии. Пациента, нуждающегося в дальнейшем обследовании и/или мышечной биопсии по поводу предрасположенности к злокачественной гипертермии (ЗГ), помогают выявить следующие вопросы.
1. Не умер ли кто-нибудь из родственников по неизвестной причине во время или сразу после операции, не было ли у него сильного жара во время нее?
2. Нет ли в анамнезе рецидивирующей лихорадки?
3. Не было ли аномальной регидности мышц, не говорил ли когда-либо дантист или хирург о необычной реакции на анестезию?
4. Нет ли в анамнезе мышечных спазмов или чрезмерной утомляемости в результате короткой, но интенсивной физической нагрузки?
5. Не было ли мышечной слабости после болезни или лихорадки и мышечной боли, внешне не связанной с болезнью?
6. Не выделялась ли красная или розовая моча, а если да, то когда?
7. Нет ли в анамнезе непереносимости физических нагрузок или жары?
8. Не избегает ли человек напитков, содержащих кофеин (кофе, чая, колы) в связи с отрицательной реакцией на них?
9. Нет ли в семейном анамнезе внезапных необъяснимых случаев смерти?
10. Нет ли в анамнезе ортопедических, мышечных или глазных расстройств, требующих лечения, например косоглазия у ребенка или грыжи?
11. Нет ли в анамнезе болезни Рейно или вегетативных дисфункций, таких как затрудненная терморегуляция или адаптация к жаре или холоду, или выраженных приливов крови к лицу?
12. Нет ли в анамнезе повышенного уровня креатинфосфокиназы?
13. Нет ли в анамнезе суставных аномалий (особенно в челюстном суставе) или кардиологических проблем, в частности аритмий или болезней миокарда?
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Гипертермия – типовая форма расстройства теплового обмена, возникающая в результате действия высокой температуры окружающей среды и/или нарушения процессов теплоотдачи организма. Характеризуется нарушением (срывом) механизмов теплорегуляции, проявляется повышением температуры тела выше нормы.
Прикрепленные файлы: 1 файл
Патология реферат.doc
Министерства Здравоохранения и Социального развития РФ
Кафедра патологической физиологии
студентка факультета фармации
и медицинской биологии
2 курса 2 группы
Гипертермия – типовая форма расстройства теплового обмена, возникающая в результате действия высокой температуры окружающей среды и/или нарушения процессов теплоотдачи организма. Характеризуется нарушением (срывом) механизмов теплорегуляции, проявляется повышением температуры тела выше нормы.
Причинами гипертермии являются:
• высокая температура окружающей среды;
• агенты, препятствующие реализации механизмов теплоотдачи организма;
• разобщители процессов окисления и фосфорилирования в митохондриях.
В реальной ситуации эти факторы могут действовать содружественно и повышать возможность возникновения гипертермии.
Снижение эффективности процессов теплоотдачи является следствием:
• первичного расстройства механизмов терморегуляции (например, при повреждении структур гипоталамуса, участвующих в регуляции температурного режима организма);
• нарушения процессов отдачи тепла в окружающую среду (например, у тучных людей, при снижении влагопроницаемости одежды, высокой влажности воздуха).
Разобщение процессов окисления и фосфорилирования в митохондриях клеток сопровождается увеличением образования доли свободной энергии, выделяющейся в виде тепла. При значительной степени разобщения может накапливаться тепло, которое организм не способен вывести, что и приводит к развитию гипертермии.
Разобщение окисления и фосфорилирования может быть вызвано:
• экзогенными факторами (например, при попадании в организм 2,4-ди-нитрофенола, дикумарола, олигомицина, амитала, препаратов, содержащих Са2+ и др.);
• эндогенными агентами (например, избытком йодсодержащих тиреоид-ных гормонов, катехоламинов, прогестерона, ВЖК и митохондриальными разобщителями - термогенинами).
Факторы риска гипертермии
Важными условиями (факторами риска), способствующими развитию гипертермии, являются:
• факторы, снижающие эффективность процессов теплоотдачи (значительная влажность воздуха, воздухо- и влагонепроницаемая одежда);
• воздействия, повышающие активность реакций теплопродукции (интенсивная мышечная работа);
• возраст (легче развивается гипертермия у детей и стариков, у которых понижена эффективность системы терморегуляции);
• некоторые заболевания (гипертоническая болезнь, сердечная недостаточность, эндокринопатии, гипертиреоз, ожирение, вегетососудистая дистония).
Воздействие на организм различных видов тепла реализуется по-разному. Конвекционное и кондукционное тепло вызывает вначале нагревание кожи, подкожной клетчатки и крови, циркулирующей в этих тканях, и лишь затем — внутренних органов и тканей. Радиационное тепло, к которому относится инфракрасное излучение, прогревает и поверхностные, и глубокие ткани одновременно.
Стадии гипертермии
В большинстве случаев указанные реакции препятствуют перегреванию организма и нарушению его жизнедеятельности. Однако нередко эти механизмы оказываются недостаточными, что сопровождается перенапряжением и срывом системы терморегуляции организма и развитием гипертермии. Иначе говоря, перегревание (в отличие от лихорадки) вызывает нарушение механизмов терморегуляции.
В ходе развития гипертермии условно выделяют две основные стадии:
• компенсации (адаптации);
• декомпенсации (деадаптации) механизмов терморегуляции организма.
• Иногда выделяют финальную стадию гипертермии — гипертермическую кому.
Механизм развития гипертермии включает комплекс адаптивных и патогенных реакций организма. На начальной стадии доминируют первые, на последующих (если компенсаторные и защитные реакции оказались недостаточными) — преобладают процессы повреждения. На каждой из стадий гипертермии в организме развиваются характерные метаболические, физико-химические, структурные и функциональные изменения.
Стадия компенсации гипертермии
Стадия компенсации гипертермии характеризуется активацией экстренных механизмов адаптации организма к перегреванию. Эти механизмы направлены на увеличение теплоотдачи и снижение теплопродукции. В результате температура тела хотя и повышается, но остаётся в пределах верхней границы нормального диапазона. Проявления гипертермии в значительной мере определяются температурой окружающей среды.
• При повышении внешней температуры до 30—31 °С происходят:
- расширение артериальных сосудов кожи и подкожной клетчатки, увеличивается их кровенаполнение;
- увеличение температуры поверхностных тканей.
Эти изменения направлены на отдачу организмом избытка тепла путём конвекции, теплопроведения и радиации. Однако по мере повышения температуры окружающей среды эффективность указанных механизмов теплоотдачи снижается.
• При внешней температуре, равной 32-33 °С и выше:
- Прекращается отдача тепла конвекцией и радиацией.
- Ведущее значение начинает приобретать теплоотдача путем потоотделения и испарения влаги с поверхности тела и дыхательных путей. При этом испарение 1 мл пота обеспечивает потерю примерно 0,6 ккал тепла. Существенно, что повышенное потоотделение активирует другие механизмы теплоотдачи в коже.
- Потовые железы наряду с экскрецией воды синтезируют и выделяют в кровь калликреин, расщепляющий глобулин. Это ведёт к образованию в крови каллидина, брадикинина и других кининов. Кинины, в свою очередь, обеспечивают двоякие эффекты:
- расширение артериол кожи и подкожной клетчатки;
- потенцирование потоотделения.
В целом, учитывая значительную поверхность кожи, эти эффекты кининов существенно увеличивают теплоотдачу организма, тормозя нарастание его температуры.
- На стадии компенсации также изменяются функции органов и физиологических систем. К этим изменениям относятся:
- увеличение ЧСС и минутного выброса сердца в связи с активацией симпатико-адреналовой системы;
- перераспределение кровотока с развитием феномена его централизации;
- тенденция к повышению АД. Причиной этого является повышение сердечного выброса крови;
- уменьшение объема альвеолярной вентиляции, потребления кислорода тканями и выделения ими углекислого газа. Это свидетельствует о снижении интенсивности окислительных процессов в организме.
- На стадии компенсации гипертермии развивается так называемый тепловой неврастенический синдром. Он характеризуется падением работоспособности, вялостью, слабостью и апатией, сонливостью, гиподинамией, нарушениями сна, раздражительностью, головными болями.
• При внешней температуре 38 - 39°С температура тела повышается на 1,5 - 2 °С по сравнению с нормой. Это сопровождается:
- расширением артериол и выраженной гиперемией кожи и слизистых оболочек;
- профузным потоотделением и тягостным ощущением жара;
- увеличением ударного и минутного выбросов сердца (в связи с дальнейшей активацией симпатико-адреналовой и гипоталамо-надпочечниковой систем);
- повышением систолического давления; диастолическое давление при этом продолжает снижаться в результате уменьшения тонуса стенок артериол;
- увеличением объёма лёгочной вентиляции, утилизации кислорода и выведения углекислоты; это свидетельствует об увеличении интенсивности окислительного метаболизма, но не о его энергетической эффективности;
- гипокапнией и развитием газового алкалоза в связи с гипервентиляцией лёгких; при выраженной гипертермии алкалоз быстро сменяется метаболическим ацидозом, что является результатом:
- нарушения кровообращения в тканях;
- развития циркуляторной и тканевой гипоксии;
- подавления активности ферментов, участвующих в обменных реакциях;
- гипогидратацией и увеличением вязкости крови, которые являются результатом значительного и длительного потоотделения;
- потерей водорастворимых витаминов;
- повышенным выведением из организма СГ, К+, Na+, Ca2+, Mg2+ и других ионов;
- при воздействии избыточного тепла развивается стресс-реакция, выражающаяся:
- активацией симпатико-адреналовой системы и повышением в крови уровня катехоламинов;
- увеличением выброса кортико- и тиролиберина, что ведёт к выбросу в кровь глюкокортикоидов и тиреоидных гормонов с развитием определяемых ими адаптивных реакций.
Стадия декомпенсации гипертермии
Стадия декомпенсации характеризуется срывом и неэффективностью как центральных, так и местных механизмов терморегуляции, что и приводит к нарушению температурного гомеостаза организма. Нарушение температурного гомеостаза организма является главным звеном патогенеза гипертермии на стадии декомпенсации.
• Температура внутренней среды организма может повыситься до 41 - 43 °С, поскольку тепловая нагрузка значительно преобладает над эффективностью механизмов теплоотдачи. В связи с этим наблюдается:
- сильное покраснение кожи, она становится сухой и горячей;
- потоотделение уменьшается, нередко отмечается лишь скудный липкий пот; сухость кожи считают важным признаком нарастающей гипертермии.
• Повышение температуры организма до 42 - 43 °С характеризуется изменениями функций органов и их систем.
- Усугубляются расстройства функции ССС и развивается так называемый гипертермический кардиоваскулярный синдром:
- нарастает тахикардия;
- снижается ударный выброс сердца;
- минутный выброс обеспечивается главным образом за счёт увеличенной ЧСС;
- систолическое давление может ненадолго возрастать, а диастолическое снижается;
- развиваются расстройства микроциркуляции;
- появляются признаки сладж-синдрома, диссеминированного внутрисосудис-того свёртывания белков крови (ДВС-синдром) и фибринолиза.
- Ацидоз. В связи с нарастанием ацидоза:
- увеличиваются вентиляция лёгких и выделение углекислоты;
- повышается потребление кислорода;
- снижается диссоциация НЬ02. Последнее в сочетании с циркуляторными расстройствами усугубляет состояние гипоксемии и гипоксии. Это, в свою очередь, обусловливает активацию гликолиза, нарастание расстройств энергообеспечения тканей и степени ацидоза.
- Развиваются существенные метаболические и физико- химические расстройства:
- теряются К+, Са2+, Na+, Mg2+ и другие ионы;
- из организма выводятся водорастворимые витамины;
- повышается вязкость крови.
- На стадии декомпенсации нарастают признаки истощения стресс-реакции и лежащая в основе этого надпочечниковая и тиреоидная недостаточность: наблюдаются гиподинамия, мышечная слабость, снижение сократительной функции миокарда, развитие гипотензии, вплоть до коллапса.
- В результате непосредственного патогенного действия тепла на клетки органов и тканей изменяются структура и функция белков, нуклеиновых кислот, липидов, мембран, кинетика ферментативных реакций.
- Увеличивается концентрация в плазме крови так называемых молекул средней массы (от 500 до 5000 Д). К ним относятся олигосахариды, полиамины, пептиды, нуклеотиды, глико- и нуклеопротеины. Указанные соединения обладают высокой цитотоксичностью.
- Появляются белки теплового шока.
- Существенно модифицируется физико-химическое состояние липидов клеток. В условиях гипертермии происходит:
- модификация липидов (в том числе необратимая) в связи с активацией сво-боднорадикальных и перекисных реакций;
- увеличение текучести мембранных липидов, что нарушает ультраструктуру и функциональные свойства мембран.
- Значительно повышается содержание в тканях мозга, печени, лёгких, мышц продуктов липопероксидации — диеновых конъюгатов и гидроперекисей липидов. Они выявляются как в первые 2—3 мин от начала воздействия теплового фактора, так и при развитии теплового удара. В последнем случае концентрация указанных агентов возрастает в 8—10 раз по сравнению с нормой. Одновременно с этим регистрируются признаки подавления антиоксидантных ферментов тканей.
- Увеличивается скорость метаболических реакций.
На стадии декомпенсации гипертермии самочувствие резко ухудшается, развивается нарастающая слабость, регистрируется сердцебиение, появляется пульсирующая головная боль, формируются ощущение сильной жары и чувство жажды, развивается сухость губ, полости рта и глотки, отмечается психическое возбуждение и двигательное беспокойство, нередко наблюдаются тошнота и рвота.
Злокачественная гипертермия – это состояние, характеризующееся острым гиперметаболизмом скелетных мышц. Возникает под действием препаратов для ингаляционного наркоза, кофеина, сукцинилхолина, стрессовых ситуаций. Проявляется в форме метаболических, кардиоваскулярных, мышечных нарушений. Позднее развивается ДВС–синдром, полиорганная недостаточность. Диагноз ставится на основании клинической картины, результатов анализа на КЩС и данных, полученных в ходе кофеин-галотанового теста. Лечение предполагает устранение всех возможных триггеров, введение раствора натрия гидрокарбоната, дантролена. Для снижения температуры тела используют физические методы.
МКБ-10
Общие сведения
Злокачественная гипертермия (ЗГ) – острое патологическое состояние, которое характеризуется значительным усилением метаболических процессов, протекающих в поперечнополосатой скелетной мускулатуре. Имеет фармакогенетическое происхождение. Частота встречаемости, по информации разных источников, варьирует в пределах 1 случая на 3-15 тысяч общих анестезий. У взрослых пациентов этот показатель составляет 1 случай на 50-100 тысяч анестезий. В реальности случаев больше, однако отследить все абортивные формы не представляется возможным. Кроме того, практикующие врачи не всегда предоставляют информацию о подобных осложнениях. У мужчин патология встречается в 4 раза чаще, чем у женщин.

Причины
Основная причина развития ЗГ – воздействие лекарственных препаратов и продуктов, обладающих триггерным действием. К числу лекарств, способных спровоцировать приступ, относят все ингаляционные анестетики, курареподобные миорелаксанты, кофеин. Присутствуют отрывочные данные о развитии патологии у людей, подвергшихся сильному психическому потрясению или физической нагрузке. Считается, что при этом происходит выработка симпатоадреналовых субстанций (адреналин, норадреналин), которые и приводят к развитию криза у предрасположенных к этому людей.
Более склонными к возникновению ЗГ считаются люди, имеющие доминантную мутацию гена рианодинового рецептора хромосомы 19. Однако известны случаи, когда при наличии явных предпосылок к возникновению гиперметаболических мышечных реакций, ген, ответственный за дефектный рецептор, у пациента отсутствовал. Предрасположенность к заболеванию обычно прослеживается у всех кровных родственников.
Патогенез
В основе патогенеза лежит увеличение длительности открытия мышечных кальциевых каналов. Это приводит к избыточному накоплению ионов кальция в саркоплазме. Нарушаются процессы поляризации и деполяризации, что становится причиной генерализованной мышечной контрактуры (ригидности). Истощаются запасы АТФ, расщепление которой приводит к усиленному потреблению клетками кислорода и выбросу тепловой энергии. Развивается тканевая гипоксия, в мышцах накапливается лактат, возникают явления рабдомиолиза. В плазме крови повышается концентрация ионов калия, кальция, магния, миоглобина и креатинфосфокиназы.
Первичное поражение затрагивает только скелетную мускулатуру. Однако накопление токсичных продуктов разрушения мышечной ткани в течение часа приводит к формированию полиорганной недостаточности, нарушению гемодинамики, критическим сдвигам кислотно-щелочного баланса. Может развиваться отек легких и головного мозга. Происходит запуск каскада воспалительных реакций окислительного типа. Возникает ДВС-синдром, который приводит к развитию скрытых внутренних и наружных кровотечений.
Классификация
Злокачественная гипертермия может протекать в нескольких клинических вариантах, которые различаются скоростью развития патологических процессов и временем, прошедшим от начала воздействия триггера до манифестации криза. Кроме того, присутствуют отличия в выраженности и наборе симптомов, тяжести течения. Различают следующие разновидности патологии:
- Классическая. Встречается в 20% случаев. Отличается развернутой клинической картиной, возникает непосредственно после введения препарата, обладающего триггерной активностью. Патология обычно развивается на операционном столе на глазах у анестезиолога, имеющего всё необходимое для купирования гипертермической реакции. Летальность сравнительно невысока, уровень смертности не превышает 5%.
- Абортивная. На ее долю приходится около 75% всех случаев. Отличается относительно легким течением, неполным набором клинической симптоматики. Во многих случаях значительного повышения температуры тела не происходит. Наиболее легкие варианты течения порой остаются незамеченными или ошибочно относятся к другим патологическим состояниям. Летальность – 2-4%.
- Отсроченная. Встречается в 5% случаев, развивается через сутки и более после контакта с провоцирующим фактором. Протекает сравнительно легко. Опасность для пациента заключается в том, что через 24 часа после операции контроль медиков за ним ослабевает. Злокачественная гипертермия на начальном этапе развития часто остается незамеченной или подвергается ошибочной диагностике.
Симптомы злокачественной гипертермии
Признаки ЗГ разделяются на ранние и поздние. Ранние возникают непосредственно при развитии криза, поздние – через 20 и более минут. Первым симптомом является спазм жевательных мышц, сменяющийся генерализованной мышечной контрактурой. Развивается респираторный ацидоз, CО2 в конце выдоха - более 55 мм рт. ст. Усиливается потоотделение, кожа приобретает мраморный оттенок. Увеличивается потребление кислорода. По мере усугубления метаболических нарушений происходят изменения в работе сердечно-сосудистой системы: колебания артериального давления, тахиаритмия.
Процессы миолиза и расщепления АТФ, развивающиеся в спазмированных мышцах, приводят к резкому росту температуры тела. Обычно этот показатель не превышает 40°C. Известны случаи лихорадки, достигавшей 43-45°C, что становилось причиной гибели больного. Из-за избыточного накопления калия усиливаются нарушения сердечного ритма. Моча становится темного цвета, концентрированной, может отмечаться анурия. Состояние обратимо, если лечебные мероприятия были начаты вовремя. В противном случае у больного развиваются осложнения.
Осложнения
Злокачественная гипертермия может становиться причиной инфаркта миокарда, полиорганной недостаточности, диссеминированного внутрисосудистого свертывания. Инфаркт развивается как следствие электролитных нарушений и генерализованного мышечного спазма. Объемные участки некроза миокарда приводят к возникновению кардиогенного шока и асистолии. Полиорганная недостаточность характеризуется нарушением функции жизненно важных структур, что в 80% случаев приводит к гибели больного. При ДВС-синдроме в сосудистом русле образуются микротромбы, которые способствуют усилению полиорганной недостаточности. В дальнейшем ресурс свертывающей системы истощается, возникают тяжелые кровотечения.
Диагностика
Диагностика уже развившейся ЗГ проводится на основании имеющихся симптомов, а также данных лабораторного обследования. Предрасположенность к возникновению криза определяется по результатам специфических методов тестирования. Алгоритм обследования пациента включает:
- Сбор анамнеза. Определить наличие предрасположенности к заболеванию можно при подготовке к операции. Для этого проводится тщательный опрос пациента и его родных. О высоком риске говорят, если среди кровных родственников больного присутствуют люди, ранее перенесшие гипертермический криз, внезапную смерть во время проведения наркоза, имеющие эпизоды необъяснимых судорог в анамнезе.
- Лабораторную диагностику. При ЗГ в крови обнаруживаются признаки метаболического ацидоза (pH менее 7,25, дефицит оснований более 8 ммоль/л), рост концентрации КФК до 20 тыс. Ед/л и более, концентрации ионов калия более 6 ммоль/л. Патологические изменения в плазме нарастают по мере развития процесса. Нормализация показателей происходит в течение суток с момента купирования криза.
- Кофеин-галотановый тест. Является специфическим анализом, выявляющим склонность к возникновению мышечной контрактуры. В ходе теста биоптат мышцы помещают в емкость, заполненную триггерными растворами. При наличии предрасположенности к ЗГ мышечная ткань сокращается, возникает контрактура. Тест проводится только пациентам, входящим в группу риска, поскольку процедура забора биоматериала отличается травматичностью.
- Генетическое обследование. Пациентам с отягощенным анамнезом показано генетическое исследование. Оно направлено на выявление гена, отвечающего за предрасположенность к развитию генерализованных мышечных контрактур. Положительным считается исследование, в ходе которого обнаруживаются мутации генов RYR1 и CACNA1S. В качестве общего скринингового метода генетический анализ не используется ввиду высокой стоимости и технической сложности работы.
Генетически обусловленные приступы ригидности скелетной мускулатуры должны дифференцироваться с анафилактическими реакциями, признаками недостаточной анальгезии, церебральной ишемией, тиреоидным кризом, злокачественным нейролептическим синдромом, недостаточностью вентиляции. Несомненный признак ЗГ – снижение выраженности симптомов вскоре после введения дантролена.
Лечение злокачественной гипертермии
Эффективность лечения напрямую зависит от времени, прошедшего с момента развития приступа до начала реанимационных мероприятий. В условиях операционной помощь больному оказывают на месте, прервав операцию. Если криз развился в палате, пациента экстренно транспортируют в ОРИТ. Оставление пациента в палате общего типа недопустимо. Лечение заключается в использовании неспециализированных и этиотропных фармакологических методов, аппаратном пособии, применении физических способов гипотермии. Основные мероприятия включают:
Прогноз и профилактика
Прогноз благоприятный, если злокачественная гипертермия была своевременно замечена и купирована. При длительном пребывании пациента в состоянии метаболического ацидоза и гипоксии возможно ишемическое поражение центральной и периферической нервной системы, нарушения в работе сердечно-сосудистого аппарата вплоть до атриовентрикулярной блокады, инфаркта миокарда, фибрилляции. При абортивной форме шансы на благополучный исход значительно выше, чем при классической.
Специфическая профилактика заключается в тщательном предоперационном обследовании, направленном на установление факта предрасположенности больного к мышечным контрактурам. Людям с подтвержденной генетической мутацией рекомендован отказ от кофе и кофеиносодержащих напитков, минимизация психологических стрессов в повседневной жизни.
1. Современные методы диагностики предрасположенности к злокачественной гипертермии/ Казанцева А.А., Лебединский К.М.// Анестезиология и реаниматология – 2014 - №4.
2. Злокачественная гипертермия: современные подходы к профилактике и лечению/ Ким Е.С., Горбачев В.И., Унжаков В.В.// Acta Biomedica Scientifica. – 2017.

В 2004 году исполнится 50 лет с тех пор, как ученые установили связь простуды и гриппа с вирусами. На сегодняшний день известно более 200 видов вирусов и микроорганизмов, относящихся к 20 семействам, вызывающих острые респираторные заболевания (ОРЗ), и этот список постепенно пополняется. У детей простуда — самая распространенная инфекционная патология.
Простудные заболевания при неправильно организованной и неадекватной помощи, в том числе при самолечении, нередко приводят к формированию группы часто болеющих детей, развитию хронических болезней желудочно-кишечного тракта, почек. Кроме того, ОРЗ являются причиной возникновения хронических очагов инфекции.
Наибольшее количество простудных заболеваний регистрируется в осенне-зимне-весенний период, причем развитию ОРЗ способствует не столько низкая температура воздуха, сколько ее сочетание с повышенной влажностью. Охлаждение организма происходит быстрее, когда поверхность кожи покрыта потом, так как при испарении влаги расходуется много тепла. При охлаждении любого участка тела (и особенно стоп) рефлекторно снижается температура слизистых оболочек верхних дыхательных путей (миндалин, слизистой оболочки носа и др.). В результате слизистая оболочка становится проницаемой для вирусов и болезнетворных микроорганизмов.
В отличие от взрослых у детей ввиду несовершенства механизма теплообмена простуда может наступить не только при переохлаждении, но и при перегревании. Особенно это касается детей раннего возраста. Известно, что 30-40% всех заболеваний у детей первого года жизни составляют ОРЗ.
Процессы теплообразования и теплоотдачи тесно связаны между собой, они помогают поддерживать постоянную температуру тела, и нарушение равновесия приводит к ослаблению местной защиты. В раннем возрасте у нетренированных и незакаленных детей механизмы образования тепла ослаблены, нервно-сосудистые реакции протекают нестабильно, что в условиях контакта с инфекцией приводит к развитию простуды. Следует, однако, отметить, что ребенок благодаря лабильности нервной регуляции быстрее, чем взрослый, приспосабливается к влиянию метеорологических факторов.
Если простуду без лихорадки у детей можно рассматривать как явление, не вызывающее беспокойства, то ОРЗ с лихорадкой и особенно с гипертермической реакцией угрожает ребенку развитием серьезных осложнений. Плохо переносят лихорадку дети с перинатальной энцефалопатией, врожденными пороками сердца, аритмиями, патологией ЦНС, наследственными метаболическими заболеваниями, фебрильными судорогами в анамнезе, родившиеся глубоко недоношенными. Тем не менее лихорадка в большинстве случаев носит защитный характер и ее опасность для организма ребенка преувеличивают из-за боязни возможных осложнений.
При большинстве простудных инфекций максимум температуры тела устанавливается в пределах 37-39°С, что не грозит серьезными расстройствами здоровья. Поэтому исходно здоровым детям с хорошей реактивностью и адекватной реакцией на воспалительный процесс в соответствии с критериями ВОЗ и отечественной педиатрической практикой не рекомендуется вводить жаропонижающие средства при температуре тела ниже 38,5-39,5°С [3, 6].
При гипертермическом синдроме, который признан абсолютным патологическим вариантом лихорадки, отмечается быстрое и неадекватное повышение температуры тела, сопровождающееся нарушениями микроциркуляции, метаболическими расстройствами и прогрессивно нарастающей дисфункцией жизненно важных органов. В основе расстройств лежит патологическая интеграция первично и вторично измененных образований ЦНС или патологическая система по Г. Н. Крыжановскому [9], деятельность которой имеет биологически отрицательное значение для организма. Гипертермический синдром требует обязательной медикаментозной коррекции, при этом не следует пренебрегать методами физического охлаждения.
Температура тела у больного ребенка контролируется каждые 30 мин. Лечебные мероприятия, направленные на борьбу с гипертермией, прекращаются после понижения температуры тела до 37,5°С, так как в дальнейшем она может понижаться без дополнительных вмешательств.
В патогенезе простудных заболеваний, помимо лихорадки, имеют значение воспалительные явления и болевые ощущения в зеве и носоглотке. В первые часы и дни болезни окончательный диагноз поставить трудно, а ребенку, особенно раннего возраста, нужна немедленная помощь. В связи с этим понятно, как важно иметь в своем арсенале эффективное лекарственное средство, обладающее комплексным воздействием и не вызывающее побочных эффектов. Поэтому при выборе препарата для снятия лихорадки лучше отдавать предпочтение средствам, обладающим жаропонижающим и одновременно противовоспалительным и обезболивающим действием. Этим требованиям при лечении простуды, осложненной лихорадкой, у детей отвечает ибупрофен (нурофен для детей), принцип действия которого основан на ингибировании циклооксигеназной активности.
Ибупрофен относится к нестероидным противовоспалительным средствам (НПВС). Обладая одновременно жаропонижающим, анальгетическим и противовоспалительным действием, НПВС не имеют гормональной активности, но благодаря угнетению синтеза простагландинов как в центральной нервной системе, так и на периферии оказывают необходимый комплексный эффект.
Парацетамол в отличие от ибупрофена обладает исключительно жаропонижающим действием. В настоящее время рекомендовано ограничить применение у детей ацетилсалициловой кислоты и метамизола, учитывая риск тяжелых осложнений. Производные пиразолона и парааминофенола, длительное время использовавшиеся в педиатрии, запрещены к применению у детей из-за существенных побочных действий [7, 10].
Данные о частоте использования жаропонижающих препаратов в России противоречивы. Тем не менее парацетамол при лечении простудных заболеваний, сопровождающихся лихорадкой, выписывают более 90% педиатров, ибупрофен — более 50%, ацетилсалициловую кислоту — около 30% [2, 5]. За рубежом с конца 80-х годов в качестве жаропонижающего лекарственного средства, составляющего альтернативу парацетамолу, в детской практике активно используют ибупрофен, который продается в аптеках без рецепта.
Нами было проведено изучение эффективности, безопасности и переносимости педиатрической суспензии ибупрофена (нурофена для детей). Спектр показаний к назначению препарата включает в себя инфекционно-воспалительную и поствакцинальную лихорадки, болевой синдром при отите, прорезывании и заболеваниях зубов, головную боль, растяжение связок и другие виды болей.
70 детей в возрасте от 6 месяцев до 12 лет (средний возраст 5,3+1,6 года, 29 девочек и 41 мальчик) имели симптомы простуды и гипертермическую температуру тела. Примерно у половины детей было отмечено наличие осложнений в виде отита, синусита и обструктивного бронхита. Все дети получали амбулаторно нурофен для детей.
Критерии включения в исследование: лихорадка выше 39,0°С у детей с благополучным преморбидным фоном и выше 38,0°С у детей из группы риска (фебрильные судороги в анамнезе, неврологическая патология, врожденный порок сердца), информированное письменное согласие родителей. Из исследования исключались больные дети, получавшие одновременно парацетамол, а также пациенты, у которых наблюдалась повышенная чувствительность к нурофену.
Нурофен для детей назначался в соответствии с общепринятыми рекомендациями в разовой дозе 10 мг/кг 3-4 раза в сутки при наличии лихорадки и болевого синдрома (головной и ушной боли, болях в горле, артралгий) в течение 3-7 дней.
Ежедневно регистрировалась информация о самочувствии ребенка, на фоне приема препарата многократно измерялась температура тела. Эффективность лечения детей оценивалась в соответствии с протоколом исследования на основании динамики клинических симптомов заболевания. Для характеристики отдельных клинических симптомов использовалась балльная шкала оценок. Переносимость нурофена для детей характеризовалась наличием или отсутствием побочных эффектов в ходе лечения.
Практически у всех детей с простудой разовый прием нурофена для детей приводил к снижению температуры тела на 1-1,5°С, исчезновению болевых ощущений в зеве. У больных детей из группы риска, когда препарат назначался при температуре тела менее 39,0°С, жаропонижающий эффект от действия нурофена для детей развивался через 30 мин после его приема. В течение 1,5 ч регистрировалось приблизительно равномерное снижение температуры тела, составляющее в целом 3,9% от исходной повышенной температуры тела. Отмечено, что за 90 мин у всех детей данной группы после использования нурофена для детей температура тела снижалась до 37,0-37,2°С.
Положительной стороной использования нурофена для детей является довольно стойкий жаропонижающий эффект, наблюдающийся у детей. В большинстве наблюдений после купирования гипертермии субфебрилитет, или температура тела в пределах 37-37,8°С держалась на протяжении 2-3 ч (см. рис.). Повторный подъем температуры тела являлся основанием для дальнейшего использования препарата. Регулярный, строго по часам, прием нурофена для детей, как это принято при курсовом лечении, нами не практиковался.
Проведенное нами сравнительное изучение, а также данные других авторов показали, что ибупрофен в дозе 10 мг/кг и парацетамол в дозе 15 мг/кг дают похожий обезболивающий результат — исчезают головные боли, боли в горле и артралгии. В обеих группах эффект был значительно более выражен, чем при приеме плацебо [6]. Так, у всех 6 детей с отитом, получавших нурофен для детей, отмечена положительная динамика по валидной шкале оценок.
Нурофен для детей в виде суспензии хорошо переносится, препарат безопасен и обладает приятным вкусом. Следует отметить, что при кратковременном применении ибупрофена риск развития нежелательных эффектов довольно низок [10].
Таким образом, проведенные наблюдения показали высокий жаропонижающий эффект, хорошую переносимость и безопасность суспензии нурофена для детей при лечении пациентов с простудными заболеваниями на фоне гипертермического и болевого синдромов. Нурофен для детей можно использовать в педиатрической практике в качестве безрецептурной формы.
Стойкий и длительный эффект нурофена для детей позволяет признать его высокоэффективным средством лечения простудных заболеваний, сопровождающихся гипертермическим синдромом. В последние годы ибупрофен рекомендован детям в качестве одного из основных жаропонижающих средств. Следует также отметить, что антипиретики необходимо назначать детям только в том случае, если лихорадка превышает допустимый предел и ведет к нарушению функций сердечно-сосудистой, центральной нервной и других систем [5, 7].
Читайте также:

