Особенности метаболизма миокарда реферат
Обновлено: 04.05.2024
Сердечная мышца обладает некоторыми характеристиками скелетной мышцы и некоторыми характеристиками гладкой мышцы. Из-за вязкости крови сокращения сердечной мышцы должны быть достаточно продолжи тельными, чтобы опустошить камеры сердца. Энергия запасается в эластичных стенках сосудов, благодаря которым кровь постоянно двигается по сосудам. Необходимо помнить, что ритмические сокращения скелетной мускулатуры также важны для циркуляции крови. Сердечная мышца обладает уникальным аэробным обменом. Способность получать энергию через анаэробный гликолиз в этой ткани ограничена. В состоянии покоя потребление кислорода на один грамм сердечной мышцы больше, чем потребление кислорода скелетной мышцы при тяжелой физической нагрузке. При физических нагрузках коронарный кровоток возрастает до 4-х раз, а сердечная мышца обладает уникальной способностью выделять кислород из крови.
На сердце лежит огромный объем работы. Подсчитано, что около 20% энергии в нормально работающем желудочке тратится на работу, не связанную с сокращением. Около 70% энергии тратится на механическую работу левого желудочка. Он работает автоматически и сокращается около одного раза (три раза во время тяжелой физической нагрузки) в секунду. Таким образом, его потребление кислорода даже в состоянии покоя в 4-5 раз больше, чем в скелетной мышце. Артериовенозное различие в давлении кислорода также выше. Основная часть объема клетки (20-30%) - это митохондрии, в то время как в остальных мышцах они занимают меньше 10% объема.
Поскольку сердечная мышца работает непрерывно, ее способность потреблять различные вещества меняется. Сердечная мышца обладает уникальными метаболическими характеристиками. При обмене веществ в состоянии покоя 70% потребности сердечной мышцы в энергии поставляется из жирных кислот. Свободные жирные кислоты, также как продукты их превращения, такие как ацетоуксусная кислота и бета-гидроксимасляная кислота, которые в большом количестве выделяются из печени при голодании, очень подходящие для использования вещества. Однако существуют различия в удобстве потребления среди жирных кислот из-за, например, активности карнитинпальмитоилтрансферазы. Удобными веществами являются триацилглицерины, образованные в печени из липидов крови, также как цикломикроны, синтезированные в кишечной слизистой оболочке. Роль глюкозы как энергетического запаса небольшая, а большое количество циркулирующих жирных кислот замедляет метаболизм глюкозы в сердечной мышце. Инсулин и глюкоза стимулируют гликолиз и подавляют окисление жирных кислот. Однако в диабетическом состоянии наблюдается внезапный спад в окислении лактата, по крайней мере, у крыс. Замедление цикла трикарбоновых кислот приводит к быстрому окончанию сокращения, что и следовало ожидать. Митохондриальный переносчик аденина-один из регуляторных сайтов в дыхательном контроле сердечной мышцы.
Из-за того, что сердце - это полый орган, и для перекачивания необходимо, чтобы различные клетки взаимодействовали между собой (сеть кардиомиоцитов), кардиоциты связаны друг с другом мостиками с низким сопротивлением, которые позволяют продвигаться волне сокращения. Из-за непрекращающихся циклов сокращений периоды отдыха короткие. Наличие абсолютного рефракторного периода в каждом цикле защищает сердечную мышцу от истощения. В этот период сокращение не может быть остановлено. Перекачивание ионов кальция происходит по нескольким механизмам. Поскольку кальций необходим для сокращения, он проникает в клетки сердца как через плазматическую мембрану в цитоплазму, так и из саркоплазматического ретикулума. Было подсчитано, что более 10% энергии в нормально работающем левом желудочке потребляется во время работы Na+/K+ и Са++ АТФаз в процессах возбуждения и электромеханического сопряжения. Ионы кальция также стимулируют окислительное фосфорилирование помимо способности к сокращению. Нарушения в цитозольном транспорте кальция играют важную роль в опосредовании сократительной дисфункции при сердечном ударе.
Прямое влияние нервных стимулов но коронарные сосуды. Иннервация коронарной системы желудочков парасимпатическими (блуждающими) нервами не отличается высокой плотностью. Тем не менее, ацетилхолин, выделяющийся из окончаний блуждающих нервов, оказывает прямое сосудорасширяющее влияние на коронарные артерии.
Иннервация коронарных сосудов симпатическими нервами выражена гораздо сильнее. В главе 60 мы увидим, что симпатические медиаторы могут оказывать как сосудосуживающее, так и сосудорасширяющее влияние. Это зависит от наличия или отсутствия соответствующих адренорецепторов в стенке кровеносных сосудов. Суживающий эффект развивается при взаимодействии медиаторов с альфа-адренорецепторами; расширяющий эффект развивается при взаимодействии медиаторов с бета-адренорецепторами гладкомышечных клеток.
Оба типа адренорецепторов имеются в коронарных сосудах. Следует подчеркнуть, что в эпикардиальных сосудах преобладают альфа-адренорецепторы, в то время как во внутримышечных артериях, вероятно, преобладают бета-адренорецепторы. Таким образом, симпатическая стимуляция может вызывать (по меньшей мере, теоретически) умеренное сужение или расширение коронарной системы, но чаще — сужение. У некоторых людей альфа-сосудосуживающий механизм является непропорционально сильным.
Такие люди при возбуждении могут страдать ишемией миокарда спастического характера и испытывать стенокардитические боли в сердце. Метаболические факторы, особенно потребление кислорода миокардом, играют ведущую роль в регуляции коронарного кровотока. Если прямые влияния сердечных нервов меняют уровень коронарного кровотока в невыгодном для миокарда направлении, метаболический контроль в течение нескольких секунд перестраивает сосудистые реакции, адаптируя коронарный кровоток к потребностям сердечной мышцы.
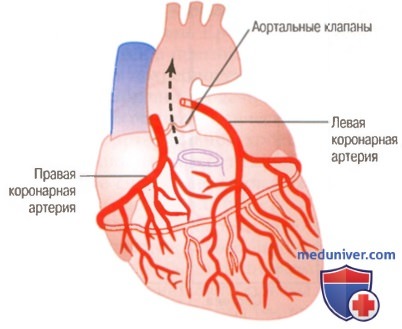
Коронарные артерии
Специфические особенности метаболизма сердечной мышцы
Основные принципы клеточного метаболизма изложены в отдельных статьях на сайте - просим вас пользоваться формой поиска выше. Они справедливы и для сердечной мышцы, и для других тканей, однако в сердце метаболические процессы имеют свои отличительные особенности. Наиболее важной особенностью является то, что в условиях покоя миокард использует главным образом жирные кислоты для получения энергии, а не углеводы, как другие ткани. Примерно 70% всей энергии в миокарде освобождается за счет окисления жирных кислот. Однако в условиях недостатка кислорода (в анаэробных или ишемических условиях) метаболизм в миокарде переходит на путь анаэробного гликолиза.
К сожалению, гликолиз требует большого количества глюкозы, транспортируемой кровью, и сопровождается накоплением большого количества молочной кислоты, что, вероятно, и провоцирует появление боли при ишемии миокарда.
Как и в других тканях, в миокарде более чем 95% метаболической энергии, высвобождаемой при окислении, используется для синтеза АТФ в митохондриях. АТФ, в свою очередь, является источником энергии для мышечного сокращения и других внутриклеточных процессов. При тяжелой коронарной ишемии АТФ расщепляется до АДФ, затем до АМФ и аденозина.
Поскольку мембрана кардиомиоцитов в некоторой степени проницаема для аденозина, он диффундирует из клеток в циркулирующую кровь.
Полагают, что выделение аденозина кардиомиоцитами приводит к расширению коронарных артериол во время коронарной гипоксии.
Однако потери аденозина имеют серьезные последствия для мышечных клеток. Примерно через 30 мин от начала тяжелой коронарной ишемии (например, в результате инфаркта миокарда) клетки теряют половину общего количества аденина через поврежденные клеточные мембраны. В нормальных клетках эти потери могли бы возмещаться вновь синтезированным аденином при скорости синтеза всего 2% в час (но не в ишеминизированных клетках). Таким образом, если приступ ишемии продолжается 30 мин и дольше, восстановление кровотока может оказаться слишком запоздавшим, чтобы сохранить жизнеспособность кардиомиоцитов. Это и является одной из основных причин гибели сердечных клеток при ишемии миокарда.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021

Сологуб Т. В., Романцова М. Г., Кремень Н. В., Александрова Л. М., Аникина О. В., Суханов Д. С., Коваленко А. Л., Петров А. Ю., Ледванов М. Ю., Стукова Н. Ю., Чеснокова Н. П., Бизенкова М. Н., Понукалина Е. В., Невважай Т. А.,
2.2.1. Сравнительная оценка энергообеспечения миокарда в норме и в динамике экспериментальной острой ишемии
Сократительная функция сердца требует постоянного энергообеспечения кардиомиоцита, которое реализуется в процессе сопряжения системы окислительного фосфорилирования и свободного дыхания, а также гликолиза.
Содержание свободного кислорода в миокарде составляет примерно 0.07 мл и связанного с миоглобином - 0.5 мл. Как известно, в условиях физической нагрузки минутный объем крови (МОК) может возрастать примерно в 10 раз, что требует увеличения энергообеспечения и возрастания доставки кислорода. Последнее достигается за счет интенсификации коронарного кровотока. Как известно, при отсутствии выраженных склеротических изменений в структуре коронарных сосудов соответствие коронарного кровотока энергетическим потребностям миокарда обеспечивается за счет адаптивной дилатации сосудов, исходно обладающих высоким базальным тонусом.
Установлено, что в состоянии относительного покоя через коронарные сосуды протекает 200-250 мл/мин крови, что составляет 4-6 % общего МОК. Во время физической нагрузки коронарный кровоток возрастает в 10-15 раз. Интенсификация коронарного кровотока при возросших энергетических потребностях регулируется на клеточном, органном и системном уровнях за счет усиления образования метаболитов изнашивания, в частности, аденозина, углекислого газа, водорода, а также гормональных и нервных влияний [53]. Мощным коронародилатирующим эффектом обладают биологически активные соединения, образующиеся при гипоксии миокарда, развитии в нем деструктивных изменений; к ним относятся: простациклин, простагландины А, Е, оксид азота (NO), вазоактивный интестинальный пептид (ВИП), ко-кальцигенин, предсердный натрийуретический фактор и др. [22].
Важную роль в адаптивных реакциях коронарного кровотока на повышенную нагрузку отводят вегетативным нервным влияниям. Так, активация холинэргических влияний на миокард приводит к дилатации коронарных сосудов за счет усиления продукции NO эндотелием [22, 23]. Нейрогенная симпатическая коронародилатация обеспечивается за счет функционального симпатолиза, когда вазоконстрикторным эффектам катехоламинов противодействует избыточное образование метаболитов изнашивания в процессе возрастания сократительной способности миокарда, реализующейся при участии β1 - адренорецепторов. Несмотря на довольно широкие адаптивные возможности коронарного кровотока, развитию реакций адаптации в условиях патологии препятствуют структурные нарушения коронарных сосудов. В то же время ряд анатомо-физиологических особенностей миокарда и коронарных сосудов, не проявляющихся развитием реакции дезадаптации в условиях нормы, могут быть отнесены к факторам риска трансформации реакций адаптации в реакции повреждения в условиях патологии [20, 36, 38]. Об этом свидетельствуют следующие факты:
Целью настоящих исследований явилось изучение характера нарушений энергообеспечения миокарда в условиях экспериментальной ишемии, в частности, установление патогенетической взаимосвязи изменений уровня макроэргов и активности дегидрогеназ (сукцинатдегидрогеназы (СДГ), лактатдегидрогеназы (ЛДГ) в динамике патологии, что позволит патогенетически обосновать новые способы медикаментозной коррекции метаболических расстройств в ишемизированном миокарде.
Как известно, источником образования АТФ в миокарде являются процессы окислительного фосфорилирования и свободного дыхания, сопряженные на внутренней мембране митохондрий. Установлено, что АТФ обладает низкой миграционной способностью к местам энергетических трат, в частности, к миозину, актину, цитоплазматической мембране, саркоплазматическому ретикулуму и др. Доставка макроэргических связей к указанным структурам обеспечивается в процессе перифосфорилирования АТФ с креатином с участием креатинфосфокиназы и за счет последующего транспорта креатинфосфата к местам энергетических трат. В связи с этим представляло интерес изучение соотношения АТФ и креатинфосфата в миокарде в динамике ишемии [38].
Эксперименты по изучению метаболических особенностей миокарда в норме и при патологии проведены на 80 беспородных белых крысах самцах массой 250-300 г.
Сравнительные серии экспериментов проведены в группе интактных животных, ложнооперированных животных и в группе животных с окклюзией коронарной артерии, достигаемой по методу H.Selye. в модификации Саидова А.Б. и соавторов [43].
Как оказалось, спустя 60 мин. с момента развития ишемии параллельно со снижением содержания в гомогенатах миокарда АТФ (р + ↔ Пируват + NADH + + Н +
В условиях адекватной оксигенации и при высокой скорости поглощения лактата равновесие смещается в сторону образования пирувата. При гипоксии, когда происходит накопление NAD + и Н + , пируват не может быть дегидрогенизирован и реакция сдвигается в сторону образования лактата [38].
Как показали результаты проведенных нами исследований, спустя 60 мин с момента развития ишемии, активность ЛДГ гомогенатов миокарда и сыворотки крови не отличалась от таковых показателей групп интактных и ложнооперированных животных. Резкое снижение активности ЛДГ гомогенатов миокарда отмечено лишь спустя 72 часа с момента развития острой ишемии миокарда ( р + до NADH ++ . Восстановленные эквиваленты NADH ++ поступают в цепь переноса электронов, где образуется АТФ и, наконец, электроны переносятся на атомы кислорода с образованием воды [38].
Одним из важнейших ферментов цикла Кребса является СДГ - флавопротеин, прочно связанный с внутренней митохондриальной мембраной, который катализирует дегидрирование сукцината с образованием фумарата.
Как показали результаты проведенных нами исследований, спустя 60 мин с момента развития острой ишемии миокарда, возникало выраженное снижение активности СДГ (р
В основных чертах процесс энергообразования в сердца не имеет принципиальных отличий от общей схемы энергетического обмена в организме. Источник энергии для сокращения сердца является АТФ, который образуется за счет:
1. Окислительное фосфорилирование. Для окислительного фосфорили-рования требуется много кислорода, поэтому мышцы обладают способностью резирвировать кислород в миоглобине. Субстратами для синтеза энергии могут использоваться жирные кислоты, углеводы и аминокислоты. Цикл Кребса в миокарде так же как и в других тканях является общим путем окисления белков, жиров и углеводов. Этот процесс является аэробным и не может протекать в других условиях. Энергия накапливается в виде макроэргических соединений, основными из которых являются АТФ и креатинфосфат (КФ). Однако энергетический процесс в миокарде имеет и отличительные особенности, которые обеспечивают специфику метаболизма миокарда, его высокую чувствительность к кислородному голоданию.
- Поскольку сердце не имеет запасов субстратов для образования энергии, поэтому надежность энергоснабжения сердца обеспечивается использованием миокардом широкого диапазона субстратов. В норме в аэробных условиях основными субстратами для синтеза АТФ в миокарде являются высшие жирные кислоты (ВЖК), они дают 67% энергии, 16,5% приходится на молочную кислоту, 8% АТФ образуется из глюкозы. Метаболизм аминокислот, ПВК и кетоновых тел в совокупности обеспечивает продукцию около 10% от общего пула АТФ. Они в различных метаболических путях трансформируются до ацетил-КоА, затем включаются в цикл Кребса и тканевое дыхание.
- Особое место в энергетики миокарда занимает молочная кислота, которая через образование ПВК поступает в цикл Кребса. Вспомним особенность лактатдегидрогеназы в сердце (изоформа ЛДГ-1,2). Этот изофермент в миокардиоцитах работает только в одном направлении: восстанавливает молочную кислоту в ПВК при участии НАДН, поэтому сердечная ЛДГ может работать только в аэробных условиях, так как уже малые концентрации пирувата ингибируют работу ЛДГ-1,2 , что препятствует образованию молочной кислоты в миокардиоцитах и способствует более полному окислению пирувата (через ацетил-КоА) в цикле Кребса (ЦТК). Этим объясняется высокая чувствительность миокарда к гипоксии. Поэтому поступающая из крови молочная кислота в миокарде быстро восстанавливается в ПВК, который является субстратом цикла Кребса и идет на образование энергии. Поэтому, лактат особенно важное место как субстрат для образования энергии в миокарде приобретает во время физической (мышечной) работы. Образующийся в процессе гликолиза в мышцах лактат поступает в миокард и его доля в энергетике миокарда возрастает до 65-90%.
- Специфической особенностью энергетического обмена миокарда является высокий уровень использования свободных жирных кислот, особенно натощак и в состоянии покоя. На окисление ВЖК может расходоваться 60-70% потребляемого сердцем кислорода. При физической нагрузке относительный вклад свободных ВЖК в энергетику уменьшается, а доля лактата возрастает. Однако на образование одного и того же количества АТФ в миокарде при использовании ВЖК требуется больше кислорода, чем при окислении глюкозы. Это особенно важно при ограничении доставки кислорода, когда использование глюкозы более выгодно.
Таким образом, процесс энергообеспечение миокарда наиболее эффективно может осуществляться в аэробных условиях. Высокая чувствительность миокарда к кислородному голоданию определяется следующими особенностями метаболизма:
1. Основным субстратом для образования АТФ в сердечной мышцы являются высшие жирные кислоты, окисление которых требует большого количества кислорода и может протекать только в аэробных условиях (бета-окисление, цикл Кребса),
2. В миокарде преобладают изоформы ЛДГ-1,2, которые ингибируются пируватом, поэтому анаэробный гликолиз в сердечной мышце является неэффективным и не может обеспечить энергией работу сердца.
2. Гликолиз. Гликолиз в миокарде не является основным поставщиком АТФ. На аэробном пути окисления углеводов энергии образуется в 18 раз больше по сравнению с анаэробным. Но хотя вклад гликолиза в энергообеспечение миокарда мал, ритмичное функционирование его чрезвычайно важно для клетки. Важность гликолиза для клеток сердца связана со следующими факторами:
А) Гексокиназа в миокардиоцитах связана с митохондриальной мембраной и это обстоятельство способствует тому, что она не ингибируется субстратом Гл-6-ф (работает как глюкокиназа печени). Миокардиальная гексокиназа осуществляет фосфорилирование глюкозы за счет митохондриальной АТФ и направляет ее в гликолиз, что сопровождается ее удвоением. Поэтому гликолитическую систему миокарда можно рассматривать как систему транспорта АТФ к местам ее использования в ионных насосах и сократительном аппарате. Благодаря этому гликолитический процесс в миокарде обеспечивает эффективную работу сердца.
Б) Гликолитический процесс и гликоген в миокардиоцитах тесно связан с мембранами, реализующими процесс возбуждения и сопряжения. Генерируемая гликолизом фракция АТФ используется в основном для энергетического обеспечения ионного транспорта, лежащего в основе процессов сопряжения и возбуждения. Поэтому, ритмическая генерация потенциалов действия водителями сердечного ритма мало меняется при ингибировании аэробного дыхания (например, при использовании цианида, при гипоксии или даже аноксии), но немедленно прекращается после выключения гликолиза. Это обеспечивает сохранение автоматизма изолированного сердца, в первый период клинической смерти и т.д. Таким образом, гликолиз играет решающее значение в обеспечение функций автоматизма и проводимости миокарда.
Креатинфасфат образуется из АТФ и креатина (который в свою очередь синтезируется из глицина, аргинина и метионина в печени и с током крови поступает в мышцы) в период расслабления мышцы, когда потребность в АТФ снижается. В образовании КФ участвует фермент креатинфосфокиназа (КФК) - специфический для мышц фермент, используется для диагностики мышечных нарушений. КФ предотвращает быстрое истощение запасов энергии, поставляет легко используемый макроэргический фосфат, необходимый для ресинтеза АТФ из АДФ (АТФ при мышечном сокращении быстро истощается, его хватает менее чем на 1 с сокращения).
Миоаденилаткиназная реакция. Миоаденилаткиназа - фермент мышц, катализирующий образование АТФ из 2-х молекул АДФ: АДФ + АДФ = АТФ + АМФ
Читайте также:

