Ишемический инсульт лечение на догоспитальном этапе реферат
Обновлено: 04.07.2024
Основными этапами медицинской помощи при остром нарушении мозгового кровообращения (ОНМК) являются следующие: догоспитальный, госпитальный, амбулаторно-поликлинический.
1. Догоспитальный этап
Он включает диагностику ОНМК, неотложные лечебные мероприятия, а также экстренную госпитализацию больного. Здесь необходим вызов врача скорой помощи, который должен прежде всего осмотреть больного, собрать анамнез, исключить другие причины ухудшения состояния (ими могут быть гипергликемия, гипогликемия, отравление, инфекция, черепно-мозговая травма, обмороки, мигрень, почечная или печеночная недостаточность), наконец, установить диагноз инсульта пока не уточненного характера.
Основную роль при этом играет анамнез, тщательно собранный со слов род-ственников, окружающих или самого больного, а также характеристика развития неврологических нарушений во времени. Внезапное и острое, в течение нескольких секунд или минут, развитие неврологического дефицита в виде слабости и/или онемения конечностей, лица и, нередко, нарушения речи у лиц, как правило, среднего или пожилого возраста на фоне значительного эмоционального, физического напряжения или сразу после сна, приема горячей ванны, при высоком или, наоборот, низком артериальном давлении позволяет достаточно точно поставить диагноз ОНМК.
Основные этапы медицинской помощи при остром нарушении мозгового кровообращения:
Наступление инсульта, как правило, сопровождается внезапным появлением у пациента следующих симптомов:
Однако надо помнить и о возможном развитии других симптомов и их комбинаций. Это, например, различные виды нарушений уровня бодрствования от оглушения до сопора и комы, глотания или координации движений; появление двоения в глазах, головокружения.
Неотложные лечебные мероприятия
Неотложные мероприятия бригады врачей скорой медицинской помощи по прибытии к больному инсультом должны включать в себя комплекс обязательных мер, которые проводятся сразу же после общего осмотра больного.
Оценка адекватности оксигенации и ее коррекция
О неадекватности оксигенации свидетельствуют:
увеличение частоты и аритмичность дыхательных движений;
цианоз видимых слизистых оболочек и ногтевых лож;
участие в акте дыхания вспомогательной мускулатуры;
набухание шейных вен.
Наиболее простым способом улучшения оксигенации является подача больному через носовые ходы кислорода со скоростью 2—4?л/мин. Обеспечение эффективной оксигенации при необходимости осуществляется постановкой воздуховода и очищением дыхательных путей. При нарушениях дыхания противопоказаны: лобелин гидрохлорид (угнетает дыхание, может спровоцировать тонико-клонические судороги, снижает артериальное давление (АД) и вызывает рвоту); цитизин (обладает очень кратковременным действием и не стабилизирует нормальное дыхание); камфора, прокаин с сульфокамфорной кислотой, никетамид (способствуют развитию судорожного синдрома и угнетают дыхание).
Коррекция нарушений кровообращения
Осуществляется путем стабилизации АД на уровне 180/100 мм рт. ст. у больных с артериальной гипертонией и на уровне 160/90?мм?рт.?ст. у нормотоников. Снижать АД в тех случаях, когда оно превышает указанные величины, не следует более чем на 15—20% от исходных. Наиболее часто применяют каптоприл 6,25—12,5 мг или эналаприл 5—10 мг. При недостаточной эффективности возможно введение в/в 1—2?мл 1%-ного раствора проксодолола в течение 1?минуты, повторно каждые 5 минут до достижения эффекта, но не более 10 мл 1%-ного раствора. Не рекомендуется назначать нифедипин из-за риска резкого снижения АД.
При артериальной гипотензии рекомендуется применение симпатомиметиков, препаратов, улучшающих сократимость миокарда (сердечные гликозиды), объемовосполняющих средств (низкомолекулярные декстраны, крахмалы и кристаллоидные растворы).
С этой целью используются бензодиазепины короткого действия, вводимые внутривенно: диазепам 0,2—0,4мг/кг, мидазолам 0,2—0,4 мг/кг. При неэффективности применяют вольпроат натрия (в/в 6 мг/кг в течение 3 минут с последующим переходом на 1—2 мг/кг/ч); тиопентал натрия (флакон растворяют 10 мл физиологического раствора натрия и вводят внутримышечно из расчета 1 мл на 10 кг веса больного).
Определение уровня глюкозы в крови
и его коррекция
Определение уровня глюкозы в крови проводится с помощью стандартного экспресс-теста. Коррекция при высоких значениях глюкозы осуществляется простым инсулином, при низком содержании — с помощью в/в водимого 40%-ного раствора глюкозы. При отсутствии возможности провести определение глюкозы в крови, но подозрении на нарушение углеводного обмена следует руководствоваться правилом: гипогликемия более опасна для жизни, чем гипергликемия. Исходя из этого, рекомендуется внутривенное введение 50—60 мл 40%-ной глюкозы. При наличии гипогликемии этим можно спасти больного, в то же время при гипергликемии дополнительное введение данного количества глюкозы не приведет к трагическим последствиям.
Первостепенные задачи оказания медицинской помощи больным с острым тяжелым инсультом на догоспитальном этапе — это поддержание жизненно важных функций и немедленная доставка пациента в соответствующий стационар. Противопоказанием для госпитализации больного с ОНМК является только его агональное состояние.
2. Госпитальный этап
При поступлении больного в стационар все последующие мероприятия должны проводиться в максимально сжатые сроки. Это, прежде всего, касается пациентов, у которых инсульт развился менее 3-х часов назад и еще есть возможность определения характера инсульта и проведения тромболизиса при его ишемическом генезе.
Тромболитическая терапия при ИИ должна проводиться в стационарах скорой медицинской помощи, в условиях отделения нейрореанимации или блока интенсивной терапии, при условии обязательного наличия в структуре стационара круглосуточных служб нейровизуализации с использованием компьютерной или магнитно-резонансной томографии и лабораторной диагностики.
Тромболизис может проводиться только после исключения геморрагического характера поражения мозга. Желательным также является первичное проведение и мониторирование ультразвуковой транскраниальной допплерографии для уточнения факта окклюзии артерии, верификации локализации окклюзии и контроля за постепенным открыванием сосуда.
Важнейшие задачи оказания медицинской помощи больным с острым тяжелым инсультом на догоспитальном этапе — это поддержание жизненно важных функций и немедленная доставка пациента в стационар. Противопоказанием для госпитализации больного с ОНМК является только его агональное состояние.
- Врач скорой помощи должен по телефону сообщить в блок интенсивной терапии неврологического отделения о том, что он транспортирует больного с ишемическим инсультом, которому показана тромболитическая терапия.
- Врач-невролог блока встречает больного в приемном отделении и транспортирует вместе с медперсоналом приемного отделения на компьютерную томографию. За время транспортировки и проведения этого обследования уточняет анамнез у родственников или самого больного.
- Осмотр и оценка неврологического статуса по шкале NIHSS.
- Измерение уровня АД на обеих руках.
- Установка кубитального периферического венозного катетера.
- Измерение уровня глюкозы в сыворотке крови.
- Забор крови и выполнение следующих лабораторных анализов:
- количество тромбоцитов;
- активированное частичное тромбопластиновое время;
- международное нормализованное отношение (МНО).
- В случае, если больной соответствует критериям включения его в тромболитическую терапию, после осмотра неврологом и выполнения компьютерной томографии головного мозга необходимо обеспечить мониторирование следующих жизненно важных функций в блоке в течение как минимум 48 часов:
- уровня АД;
- частоты сердечных сокращений (ЧСС);
- частоты дыхания (ЧД);
- температуры тела;
- сатурации кислородом (SaO2).
Подчеркну, что введение алтеплазы должно быть начато как можно раньше от начала заболевания. Рекомендуемая доза — 0,9 мг/кг массы тела (максимальная доза 90 мг). 10% всей дозы для пациента вводится в виде болюса внутривенно струйно в течение 1 минуты. Оставшаяся доза вводится внутривенно капельно в течение 1 часа.
Во время и после проведения тромболизиса чрезвычайно важен мониторинг основных жизненно важных функций: АД, ЧСС,ЧД, температуры тела, SaO2 .Во время процедуры тромболитической терапии необходимо контролировать динамику неврологического статуса, наиболее оптимальным является использование шкалы для оценки неврологического дефицита (шкала NIHSS).
Комплекс мероприятий, обязательных для проведения в стационаре:
- общие медицинские мероприятия—наблюдение и уход за больным;
- профилактика и лечение основных неврологических осложнений;
- специальные методы лечения инсульта;
- профилактика и лечение экстрацеребральных осложнений;
- реабилитационные мероприятия;
- мероприятия по ранней профилактике повторного инсульта.
Наблюдение за больным
Наблюдение за больным необходимо для выработки адекватной тактики по его ведению и включает в себя ряд мероприятий: мониторинг неврологического статуса, оксигенации крови, АД, ЭКГ, внутричерепного давления и церебрального перфузионного давления, центрального венозного давления; контроль основных параметров гомеостаза.
Уход за больным
Уход за больными в острой стадии инсульта, которые часто не только не могут самостоятельно повернуться в кровати, но и находятся в бессознательном состоянии, также является крайне ответственным мероприятием. Он должен включать в себя ежедневное выполнение следующих действий:
- повороты с боку на бок;
- протирание тела;
- регулярные клизмы и опорожнение мочевого пузыря;
- введение адекватного объема жидкости;
- туалет рото- и носоглотки;
- санация трахеобронхиального дерева (при проведении искусственной вентиляции легких);
- контроль за глотанием и питанием;
- профилактика стрессорных язв желудочно-кишечного тракта;
- антибактериальная терапия по показаниям;
- профилактика ДВС-синдрома и тромбоэмболии легочной артерии;
- проведение пассивной гимнастики и массажа.
Лечение основных неврологических осложнений
К основным патогенетическим изменениям мозга в процессе развития инфаркта мозга, сопровождающимся характерными неврологическими нарушениями, относятся следующие: отек мозга и острая обструктивная гидроцефалия.
Для лечения отека мозга необходима гипервентиляция в условиях искусственной вентиляции легких, снижение РаСО2 до уровня 30 мм рт. ст. Из осмотических диуретиков чаще всего используется маннитол внутривенно капельно в первоначальной дозе 0,5—2,0 г/кг массы тела в течение 20—25 минут, а затем в дозе, составляющей половину от первоначальной, каждые 4—6?часов, не более 3—4 суток. В случае отсутствия маннитола или при невосполненной гиповолемии внутривенно каждые 3—6?часов вводится по 100—150 мл 3%-ного раствора натрия хлорида в течение того же периода.
Оптимальной является следующая модель
этапной реабилитации после инсульта:
1-й этап – реабилитация начинается в неврологическом отделении больницы, куда доставлен больной бригадой скорой помощи;
2-й этап – по окончании острого периода с полным восстановлением нарушенных функций больной выписывается на амбулаторное долечивание или переводится в санаторий, а больной с выраженным двигательным дефицитом переводится в реабилитационное отделение.
3-й этап – амбулаторная реабилитация, реабилитация на дому.
Основными методами лечения острой обструктивной гидроцефалии являются дренаж боковых желудочков, декомпрессия задней черепной ямы и/или удаление некротизированной ткани при инфаркте мозжечка.
Нейропротекция — комплекс универсальных методов защиты мозга от структурных повреждений. Она должна начинаться уже на догоспитальном этапе лечения и продолжаться в стационаре.
С целью метаболической защиты мозга при любом типе инсульта используют препараты, корригирующие энергетический обмен, антиоксиданты и средства, обладающие нейротрансмиттерным и нейромодуляторным действием:
- пирацетам 12 г внутривенно;
- глицин сублингвально по 1—2?г в сутки;
- семакс 1% по 3 капли эндонозально;
- депротеинизированный гемодериват внутривенно 10—20%-ный инфузионный раствор по 250 мл;
- сернокислая магнезия 25%-ная 20,2?мл в 200 мл изотонического раствора натрия внутривенно капельно 2 раза в день;
- метилэтилпиридинол по 15 мл 1%-ного раствора внутривенно;
- церебролизин 10—30 мл внутривенно;
- кортексин 10 мг внутримышечно;
- этилметилгидроксипиридин сукцинат по 200—300 мг внутривенно капельно;
- холин альфосцерат по 1 г внутривенно капельно и др.
- ацетилсалициловая кислота 1 мг/кг массы тела;
- дипиридамол 25 мг 3 раза в день;
- клопидогрель 75 мг 1 раз в день;
- пентоксифиллин 200 мг внутривенно капельно и др.
- винпоцетин 10—20 мг внутривенно капельно;
- ницерголин 4 мг внутримышечно;
- аминофиллин 10 мл внутривенно и др.
Улучшение церебральной перфузии и улучшение реологических свойств крови
- реополиглюкин 200—400 мл внутривенно капельно;
- декстран 400 мл внутривенно капельно.
Антикоагулянты прямого действия — по показаниям
- гепарин 5000 ЕД 4—6 раз в сутки подкожно;
- фраксипарин 7500 ЕД подкожно 2 раза в сутки.
Антикоагулянты непрямого действия (оральные антикоагулянты)
- варфарин 2—5 мг в сутки под контролем МНО;
- фениндион 100 мг/сутки.
3. Амбулаторно-поликлинический этап
Реабилитация — комплекс мероприятий (медикаментозных, физических, педагогических, психологических, правовых), направленных на восстановление нарушенных в результате заболевания функций, социальной адаптации, качества жизни, а тогда, когда это возможно, и трудоспособности. Реабилитация также должна включать профилактику постинсультных осложнений и профилактику повторных инсультов. Длительность реабилитации определяется сроками восстановления нарушенных функций. Следует помнить, что максимальное улучшение двигательных функций отмечается в первые 6 месяцев, бытовых навыков и трудоспособности — в течение 1 года, речевых функций — на протяжении 2—3?лет с момента развития инсульта.
Оптимальной является следующая модель этапной реабилитации после инсульта:
Факторы риска, связанные с увеличением частоты ишемического инсульта. Кардиоэмболический-ишемический, атеротромботический-ишемический, лакунарно-ишемический инсульт. Основные этапы оказания медицинской помощи при остром нарушении мозгового кровообращения.
| Рубрика | Медицина |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 02.11.2021 |
| Размер файла | 18,0 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
1. Понятие ишемического инсульта
2. Классификация ишемического инсульта
3. Догоспитальный этап
Список использованной литературы
Ишемический инсульт - клинический синдром, развивающийся в результате критического снижения кровоснабжения части мозга в определенной артериальной лоханке, что приводит к ишемии с образованием очага острого некроза ткани головного мозга - церебрального инфаркт. Чаще всего ишемический инсульт развивается в результате тромбоза или эмболии при церебральном атеросклерозе или в результате кардиогенной эмболии.
За последние несколько десятилетий в нашем понимании возможностей терапии инсульта произошла революция. Свидетельства отсроченного необратимого повреждения головного мозга с момента развития укрепили отношение к инсульту как к экстренной ситуации, требующей скорейшей и наиболее патогенетически обоснованной медицинской помощи, предпочтительно в первые 3-6 часов после начала заболевания. Это станет возможным, если адекватную терапию инсульта начать уже на догоспитальном этапе - в условиях работы линейной или специализированной неврологической бригады.
Целью работы является определить рациональность лечебно-тактических мероприятий на догоспитальном этапе.
Для этого решались следующие задачи:
1. Рассмотреть понятие ишемического инсульта
2. Изучить классификацию ишемического инсульта
3. Рассмотреть лечебно-тактические мероприятия на догоспитальном этапе.
1. Понятие ишемического инсульта
Ишемический инсульт - это патологическое заболевание, которое не является отдельным или независимым заболеванием, а представляет собой эпизод, развивающийся как часть прогрессирующего общего или местного поражения сосудов при различных заболеваниях сердечно-сосудистой системы. Ишемический инсульт часто сопровождается следующими заболеваниями: артериальная гипертензия, атеросклероз, ревматическая болезнь сердца, ишемическая болезнь сердца, сахарный диабет и другие формы патологии с поражением сосудов. Клиника ишемического инсульта включает общемозговые и очаговые симптомы в зависимости от локализации сосудистых заболеваний. Наиболее важным методом инструментальной диагностики ишемического инсульта, а также дифференцировки от геморрагического инсульта, является КТ и МРТ головного мозга.
Поскольку ишемический инсульт сам по себе не считается заболеванием, невозможно определить какой-либо один этиологический фактор для него. Однако существуют факторы риска, связанные с увеличением частоты ишемического инсульта, которые можно разделить на две группы:
1. Поддается модификации.
- Бессимптомное поражение сонных артерий.
Кроме того, существуют факторы риска, связанные с образом жизни: низкая физическая активность, острый стресс или длительный психоэмоциональный стресс, избыточный вес, курение.
Комплекс клинических симптомов при ишемическом инсульте различен и зависит от локализации и объема поражения головного мозга. Наиболее распространенная локализация поражения в сонном бассейне (до 85%), реже-в вертебро-базилярном.
2. Классификация ишемического инсульта
Ишемический инсульт может быть следствием того или иного заболевания сердечно-сосудистой системы. Существует несколько патогенетических вариантов ишемического инсульта. В наиболее распространенной классификации ТОСТА выделяют следующие варианты ишемического инсульта:
1. Кардиоэмболический-ишемический инсульт, вызванный аритмией, клапанной болезнью сердца, инфарктом миокарда;
2. Атеротромботический-ишемический инсульт, вызванный атеросклерозом крупных артерий, что привело к артериальной эмболии;
3. Лакунарно-ишемический инсульт, вызванный окклюзией артерий малого калибра;
4. Ишемический инсульт, связанный с другими, более редкими причинами: гиперкоагуляция крови, рассечение артериальной стенки, неатеросклеротические васкулопатии;
5. Ишемический инсульт неизвестного происхождения - инсульт с неизвестной причиной или с наличием двух или более возможных причин, когда невозможно установить точный диагноз.
Кроме того, незначительный инсульт будет изолирован, если существующие симптомы исчезнут в течение первых трех недель заболевания. При ишемическом инсульте наблюдается ряд процессов, которые в совокупности приводят к гибели нейронов. Разрушение клеток происходит на фоне отека мозга. В этом случае объем мозга увеличивается, а внутричерепное давление повышается. Из-за отека клеток происходит смещение височной доли, а также травма среднего мозга.
При появлении первых признаков ишемического инсульта медицинская помощь должна быть оказана в течение первых трех часов, в противном случае прогноз неутешителен.
Существует несколько периодов ишемического инсульта:
- Ранний восстановительный период инсульта;
- Поздний период восстановления;
- Стадия остаточных явлений.
3. Догоспитальный этап
Догоспитальный этап включает в себя диагностику инсульта, неотложные медицинские меры, а также экстренную госпитализацию пациента. Здесь нужно вызвать врача скорой помощи, который должен предварительно осмотреть пациента, собрать анамнез, исключить другие причины ухудшения (это может быть гипергликемия, гипогликемия, отравление, инфекция, черепно-мозговая травма, обморок, мигрень, почечная или печеночная недостаточность) и, наконец, установить диагноз инсульта, который еще не выяснен.
Основную роль в этом играет анамнез, тщательно собранный со слов родственников, окружающих или самого пациента, а также особенности развития неврологических нарушений с течением времени. Внезапное и острое, в течение секунд или минут, развитие неврологического дефицита в виде слабости и / или онемения конечностей, лица и, часто, нарушения речи у людей, обычно среднего или пожилого возраста, в контексте значительных эмоциональных расстройств, физического напряжения или сразу после сна или принятия горячей ванны, при повышенном или, наоборот, пониженном артериальном давлении позволяет точно диагностировать инсульт.
Основные этапы оказания медицинской помощи при остром нарушении мозгового кровообращения:
Начало инсульта обычно сопровождается внезапным появлением следующих симптомов:
Однако следует также помнить о возможном развитии других симптомов и их сочетаний. Это, например, различные типы нарушений уровня бодрствования от оглушения до слабоумия и комы, глотания или координации движений; появление двоения в глазах, головокружения.
Неотложные действия бригады скорой помощи по прибытии к пациенту с инсультом должны включать в себя комплекс обязательных мероприятий, которые выполняются сразу после общего осмотра пациента.
При оценки на недостаточную оксигенацию указывают:
-Учащение и аритмия дыхательных движений;
-Цианоз видимых слизистых оболочек и ногтевого ложа;
-Участие в акте дыхания вспомогательных мышц;
-Набухание вен на шее.
Самый простой способ улучшить оксигенацию - обеспечить пациента кислородом через носовые ходы со скоростью 2-4 л / мин. Обеспечение эффективной оксигенации, при необходимости, достигается путем создания воздуховода и очистки дыхательных путей. При респираторных заболеваниях противопоказаны: лобелин гидрохлорид (угнетает дыхание, может вызывать тонико-клонические судороги, снижает артериальное давлениеи вызывает рвоту); цитизин (оказывает очень кратковременное действие и не стабилизирует нормальное дыхание); камфора, новокаин с сульфокамфорной кислотой, никетамид (способствуют развитию судорожного синдрома и угнетают дыхание).
Коррекция нарушений кровообращения осуществляется путем стабилизации артериального давления на уровне 180/100 мм рт. Изобразительное искусство. у пациентов с артериальной гипертензией и на уровне 160/90 мм рт. в нормотонике. Снижать артериальное давление в случаях, когда оно превышает указанные значения, оно не должно быть более 15-20% от исходного. Чаще всего используется каптоприл 6,25-12,5 мг или эналаприл 5-10 мг. При недостаточной эффективности можно вводить 1-2 мл 1% раствора проксодолола внутривенно в течение 1 минуты, повторно каждые 5 минут до достижения эффекта, но не более 10 мл универсального раствора. '1%. Не рекомендуется назначать нифедипин из-за риска резкого снижения артериального давления.
При артериальной гипотензии рекомендуется использовать симпатомиметики, препараты, улучшающие сократимость миокарда (сердечные гликозиды), средства, восполняющие объем (низкомолекулярные декстраны, крахмалы и растворы кристаллоидов).
Для купирования психомоторного возбуждения и судорог применяют бензодиазепины короткого действия, вводимые внутривенно: диазепам 0,2-0,4 мг / кг, мидазолам 0,2-0,4 мг / кг. При неэффективности применяют вольпроат натрия (внутривенно 6 мг / кг в течение 3 минут с последующим переходом на 1-2 мг / кг / ч); тиопентал натрия (флакон растворяют в 10 мл физиологического раствора натрия и вводят внутримышечно из расчета 1 мл на 10 кг веса пациента). Определение уровня глюкозы в крови производится с помощью стандартного экспресс-теста. Коррекция высоких значений глюкозы производится простым инсулином, при низких уровнях - с помощью 40% раствора глюкозы, вводимого внутривенно. Если невозможно определить уровень глюкозы в крови, но есть подозрение на нарушение углеводного обмена, необходимо руководствоваться правилом: гипогликемия более смертельна, чем гипергликемия. Исходя из этого рекомендуется внутривенное введение 50-60 мл 40% глюкозы. наличие гипогликемии, это может спасти пациента, при передозировке уровня глюкозы в крови дополнительное введение определенного количества глюкозы не приведет к трагическим последствиям.
Основными задачами оказания медицинской помощи пациентам с острым тяжелым инсультом на догоспитальном этапе являются поддержание жизненно важных функций и немедленная доставка пациента в соответствующую больницу. Противопоказанием к госпитализации больного, перенесшего инсульт, является только его агональное состояние.
ишемический инсульт кровообращение помощь
Принято считать, что здоровый образ жизни, нормализованная работа и своевременный отдых значительно снижают риск ишемического инсульта.
Основная задача врача на догоспитальном этапе - это правильная и своевременная диагностика инсульта, что возможно на основании уточнения жалоб, анамнеза и проведения соматического и неврологического обследования. Точное определение характера инсульта (геморрагический или ишемический) не обязательно, возможно только в условиях стационара после КТ или МРТ исследования головного мозга. Чтобы принять правильное тактическое решение о целевой госпитализации пациента в областной сосудистый центр или специализированную больницу, желательно определить вероятный тип инсульта уже на догоспитальном этапе.
Таким образом, разработка и внедрение единой политики догоспитального управления поможет оптимизировать систему здравоохранения для пациентов с инсультом, чтобы обеспечить наилучшие возможные исходы заболевания.
Список использованной литературы
1. Амосов, В.Н. Инсульт. Симптомы, первая помощь, методы восстановления / В.Н. Амосов. - М.: Вектор, 2013.
2. Фадеев, П.А. Инсульт. Доступно и достоверно / П.А. Фадеев. - М.: Мир и Образование, 2012.
3. Инсульт. Руководство для врачей. - М.: Медицинское информационное агентство, 2014.
5. Дифференциальная диагностика инсульта на догоспитальном этапе / М.А. Милосердов, Н.Н.Маслова, Ю. С. Корнева, О. О. Фролкова // Скорая мед. помощь. - 2015.
6. Багненко С.Ф., Верткин А.Л., Мирошниченко А.Г., Хубутия М.Ш. - Руководство по скорой медицинской помощи., 2007 г.
Подобные документы
Этиология острого нарушения мозгового кровообращения - патологического процесса в головном мозге, связаного с недостаточностью кровоснабжения мозга (ишемический инсульт) или внутричерепным кровоизлиянием. Догоспитальное оказание медицинской помощи.
реферат [640,2 K], добавлен 08.12.2011
Основные критерии постановки диагноза транзиторной ишемической атаки. Источники эмболии мозговых сосудов. Причины ишемического инсульта. Неврологический статус и топический диагноз больного. Основные принципы специального лечения ишемического инсульта.
история болезни [31,5 K], добавлен 12.03.2013
Ишемический инсульт - осложнение гипертонической болезни и атеросклероза - обусловлен болезнями клапанного аппарата сердца, инфарктом миокарда, врожденными аномалиями сосудов мозга, геморрагическими синдромами и артериитами. Симптоматическая терапия.
история болезни [35,1 K], добавлен 12.03.2009
Причины острого нарушения мозгового кровообращения. Симптомы ишемического и геморрагического инсульта. Неврологические расстройства при эмболиях. Мероприятия интенсивной терапии при внутримозговом кровоизлиянии. Комплексное лечение полирадикулоневритов.
реферат [18,8 K], добавлен 30.11.2009
Анализ жалоб пациента и сбор анамнеза, оценка текущего состояния и неврологического статуса. Данные дополнительных методов исследования, дифференциальный и синдромный диагноз. Обоснование клинического диагноза "ишемический инсульт", план лечения.
Ишемический инсульт — патологическое состояние, представляющее собой не отдельное или самостоятельное заболевание, а эпизод, развивающийся в рамках прогрессирующего общего или локального сосудистого поражения при различных заболеваниях сердечно-сосудистой системы. Зачастую ишемический инсульт сопутствует следующим заболеваниям: артериальная гипертензия, атеросклероз, ревматический порок сердца, ишемическая болезнь сердца, сахарный диабет и иные формы патологии с поражением сосудов. Клиника ишемического инсульта состоит из общемозговых и очаговых симптомов, зависящих от локализации сосудистых нарушений. Важнейший метод инструментальной диагностики ишемического инсульта, а также его дифференцировки от геморрагического инсульта, - это КТ и МРТ головного мозга.
МКБ-10


Общие сведения
Ишемическим инсультом называют мозговые нарушения кровообращения, характеризующиеся внезапным появлением очаговой неврологический или общемозговой симптоматики, сохраняющейся более 24 часов или вызывающая смерть пациента в более короткий срок.
Причины
Поскольку ишемический инсульт не рассматривается как отдельное заболевание, определение единого этиологического фактора для него невозможно. Однако существуют факторы риска, ассоциированные с повышенной частотой развития ишемического инсульта, которые можно разделить на две группы:
1. Модифицируемые.
2. Немодифицируемые.
- наследственная предрасположенность
- возраст
Кроме этого, существуют и факторы риска, связанные с образом жизни: низкий уровень физической активности, острый стресс или длительное психоэмоциональное напряжение, избыточная масса тела, табакокурение.
Патогенез
Определенная последовательность молекулярно-биохимических изменений в веществе мозга, вызываемая острой фокальной ишемией мозга, способна привести к тканевым нарушениям, в результате которых происходит гибель клеток (инфаркт мозга). Характер изменений зависит от уровня снижения мозгового кровотока, продолжительности такого снижения и чувствительности вещества мозга к ишемии. Степень обратимости тканевых изменений на каждом этапе патологического процесса определяется уровнем снижения мозгового кровотока и его продолжительностью в сочетании с факторами, определяющими чувствительность мозга к гипоксическому повреждению.
Классификация
Ишемический инсульт может быть последствием того или иного заболевания сердечно-сосудистой системы. Выделяют несколько патогенетических вариантов ишемического инсульта. В классификации TOAST (Trial of Org 10172 in Acute Stroke Treatment), получившей наибольшее распространение, выделяют следующие варианты ишемического инсульта:
- кардиоэмболический — ишемический инсульт, произошедший по причине аритмии, клапанного порока сердца, инфаркта миокарда;
- атеротромботический — ишемический инсульт, произошедший по причине атеросклероза крупных артерий, результатом которого стала артерио-артериальная эмболия;
- лакунарный — ишемический инсульт, произошедший по причине окклюзии артерий малого калибра;
- ишемический инсульт, связанный с иными, более редкими причинами: гиперкоагуляцией крови, расслоением стенки артерий, неатеросклеротическими васкулопатиями;
- ишемический инсульт неизвестного происхождения — инсульт с неустановленной причиной или с наличием двух и более возможных причин, когда установить точный диагноз не представляется возможным.
Кроме того, выделяют малый инсульт, когда имеющаяся симптоматика регрессирует в течение первых трех недель заболевания.
Различают также несколько периодов ишемического инсульта:
Симптомы ишемического инсульта
Клинический симптомокомплекс при ишемическом инсульте разнообразен и зависит от локализации и объема очага поражения головного мозга. Более других распространена локализация очага поражения в каротидном бассейне (до 85%), реже — в вертебрально-базилярном.
Инфаркт мозга в бассейне СМА
Особенностью инфаркта в бассейне кровоснабжения средней мозговой артерии является наличие выраженной системы коллатерального кровоснабжения. Окклюзия проксимального отдела средней мозговой артерии может вызывать субкортикальный инфаркт, при этом корковая область кровоснабжения остается непораженной. В отсутствии данных коллатералей возможно развитие обширного инфаркта в области кровоснабжения средней мозговой артерии.
Для инфаркта в области кровоснабжения поверхностных ветвей средней мозговой артерии типично возникновение девиации глазных яблок и головы в сторону пораженного полушария. При этом в случае поражения доминантного полушария развивается ипсилатеральная идеомоторная апраксия и тотальная афазия, а в случае поражения субдоминантного полушария — анозогнозия, дизартрия, апросодия и контралатеральное игнорирование пространства.
Основное клиническое проявление инфаркта головного мозга в области ветвей средней мозговой артерии — контралатеральный гемипарез и контралатеральная гемианестезия. В случае обширных очагов поражения возможно появление содружественного отведения глазных яблок и фиксации взора в сторону пораженного полушария. При инфарктах субдоминантного полушария развиваются эмоциональные нарушения и пространственное игнорирование.
Распространение пареза при инфаркте в бассейне кровоснабжения стриатокапсулярных артерий зависит от локализации и размеров поражения (верхняя конечность, лицо или вся контралатеральная часть тела). В случае обширного стриатокапсулярного инфаркта, как правило, развиваются типичные проявления окклюзии средней мозговой артерии (афазия, гомонимная латеральная гемианопсия). Лакунарный инфаркт клинически проявляется развитием лакунарных синдромов (изолированные гемипарез и гемигипестезия или их сочетание).
Инфаркт мозга в бассейне ПМА
Наиболее частым клиническим проявлением инфаркта в бассейне кровоснабжения передней мозговой артерии являются двигательные нарушения. В большинстве случаев окклюзии кортикальных ветвей развивается моторный дефицит в стопе и всей нижней конечности, а также слабо выраженный парез верхней конечности с обширным поражением языка и лица.
Инфаркт мозга в бассейне ЗМА
В результате окклюзии задней мозговой артерии развиваются инфаркты затылочной височной доли, а также медиобазальных отделов височной доли. В таких случаях клиническими проявлениями выступают дефекты полей зрения (контралатеральная гомонимная гемианопсия). Возможно также их сочетание со зрительными галлюцинациями и фотопсиями.
Инфаркт мозга в вертебробазилярном бассейне
Инсульт в вертебробазилярном бассейне кровоснабжения происходят в результате окклюзии единственной перфорирующей ветви базилярной артерии и сопровождаются, как правило, симптомами поражения черепных нервов на ипсилатеральной стороне. Окклюзия позвоночной артерии или ее основных пенетрирующих ветвей, отходящих от дистальных отделов, приводит к развитию синдрома Валленберга (латеральный медуллярный синдром).
Диагностика
При сборе анамнеза необходимо определиться с началом нарушений мозгового кровообращения, установить последовательность и скорость прогрессирования тех или иных симптомов. Для ишемического инсульта типично внезапное возникновение неврологических симптомов. Кроме того следует обратить внимание на возможные факторы риска возникновения ишемического инсульта (сахарный диабет, артериальная гипертензия, мерцательная аритмия, атеросклероз, гиперхолестеринемия и др.).
Инструментальная диагностика ишемического инсульта:
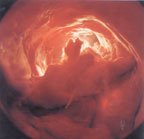
- МРТ головного мозга. Доказана эффективность нового режима МРТ-исследования, с помощью которого получают диффузионно-взвешенные изображения. В результате цитотоксического отека при ишемическом инсульте молекулы воды переходят из внеклеточного пространства внутриклеточное, это приводит к снижению скорости их диффузии. Эти изменения проявляются на диффузно-взвешенных МРТ-изображениях в виде повышения сигнала, что свидетельствует о развитии необратимых структурных повреждениях вещества мозга.

МРТ головного мозга. Участок ограничения диффузии в мозжечке и стволе мозга слева (острый ишемический инсульт)

Дифференциальный диагноз
МРТ и КТ головного мозга используют также и для дифференциации ишемического инсульта от иных форм внутричерепной патологии и динамического контроля над тканевыми изменениями во время лечения ишемического инсульта. Прежде всего, ишемический инсульт необходимо дифференцировать от геморрагического инсульта. Решающую роль в этом вопросе будут играть нейровизуализационные методы исследования. Кроме того, в некоторых случаях возникает необходимость дифференциации ишемического инсульта от острой гипертонической энцефалопатии, метаболической или токсической энцефалопатии, опухоли мозга, а также инфекционными поражениями мозга (абсцесс, энцефалит).
Лечение ишемического инсульта
При подозрении на ишемический инсульт пациента следует госпитализировать в специализированные отделения. В том случае, если давность заболевания составляет менее 6 часов — в блок интенсивной терапии тех же отделений. Транспортировка должна осуществляться только при приподнятом до 30 градусов положении головы пациента. Относительными ограничениями к госпитализации считают терминальную кому, терминальную стадию онкологических заболеваний, а также наличие в анамнезе деменции с выраженной инвалидизацией.
Немедикаментозное лечение ишемического инсульта должно включать в себя мероприятия по уходу за пациентом, коррекцию функции глотания, профилактику и терапию инфекционных осложнений (пневмония, инфекции мочевыводящих путей и др.). Координированный мультидисциплинарный подход к нему следует применять в условиях специализированного сосудистого отделения, располагающей блоком (палатой) интенсивной терапии с возможность круглосуточного выполнения ЭКГ, КТ, клинических и биохимических анализов крови, а также ультразвуковых исследований.
Терапия в острейшем периоде
Медикаментозное лечение ишемического инсульта наиболее эффективно в самом начале заболевания (3-6 часов после проявления первых признаков заболевания). При тромботической этиологии инсульта проводится селективный или системный тромболизис, при кардиоэмболическом генезе - антикоагулянтная терапия.
В первые 48 часов заболевания необходимо периодически определять насыщение гемоглобина кислородом артериальной крови. В случае если данный показатель достигает 92%, следует провести оксигенотерапию, начиная с 2-4 литров в минуту. Снижение уровня сознания пациента до 8 баллов и меньше (шкала комы Глазго) — абсолютный показатель к инкубации трахеи. Решение вопроса в пользу ИВЛ или против нее принимают, исходя из основных общих реанимационных положений.
При сниженном уровне бодрствования, при наличии клинических или нейровизуализационных признаков отека головного мозга или повышенного внутричерепного давления необходимо поддержание головы пациента в приподнятом на 30 градусов состоянии (без сгибания шеи!). Необходимо сводить к минимуму (а по возможности исключать) кашель, эпилептические припадки и двигательное возбуждение. Инфузии гипоосмоляльных растворов противопоказаны.
Плановая терапия
Важная составляющая терапии ишемического инсульта — коррекция жизненно важных функций и поддержание гомеостаза. Для этого необходим постоянный мониторинг основных физиологических показателей, коррекция и поддержание показателей гемодинамики, водно-электролитного баланса, дыхания, коррекция повышенного внутричерепного давления и отека мозга, профилактика и борьба с осложнениями.
- Инфузионная терапия. Рутинное использование глюкозосодержащий растворов нецелесообразно из-за риска развития гипергликемии, поэтом основным инфузионным раствором при лечении ишемического инсульта является раствор хлорида натрия (0,9%). При сопутствующем сахарном диабете пациентов переводят на подкожные инъекции инсулинов короткого действия за исключением тех случаев, когда проводится адекватный контроль гликемии, а пациент при этом находится в ясном сознании и без нарушения функции глотания.
- Обеспечение питания. В независимости от местонахождения пациента (блок интенсивной терапии, реанимация или неврологическое отделение) ежедневной задачей базисной терапии ишемического инсульта является адекватное питание пациента, а также контроль и восполнение водно-эликтролитных потерь. Показателем к проведению энтерального зондового питания считается прогрессирование тех или иных расстройств глотания. При этом расчет доз нутриентов следует проводить с учетом метаболических потребностей и физиологических потерь организма. При введении пищи перорально или через зонд пациент должен находиться в положении полусидя в течение 30 минут после кормления.
- Профилактика тромбозов. В целях профилактики тромбоза глубоких вен при ишемическом инсульте показано ношение компрессионных чулок или соответствующего бинтования. В тех целях, а также для предотвращения тромбоэмболии легочной артерии применяют прямые антикоагулянты (низкомолекулярные гепарины).
- Нейропротекция. Основное ее направление — применение препаратов с нейромодуляторными и нейротрофическими действиями. Самый известный в настоящее время препарат нейротрофического ряда — это гидрализат из мозга свиней. Головной и спинной мозг не имеют депонирующего свойства, и прекращение кровотока на 5-8 минут вызывает гибель нейронов. Поэтому введение нейропротекторных препаратов необходимо проводить уже в первые минуты ишемического инсульта.
Таким образом, ранняя реабилитация на фоне базисной терапии, а также сочетание реперфузии и нейропротекции позволяют достичь определенных успехов в медикаментозном лечении ишемического инсульта.
Хирургическое лечение
Хирургическое лечение ишемического инсульта подразумевает хирургическую декомпрессию — уменьшение внутричерепного давление, увеличение перфузионного давления, а также сохранение церебрального кровотока. Статистика указывает на снижение уровня летальности при ишемическом инсульте с 80 до 30%.
Реабилитация
В реабилитационном периоде после перенесенного ишемического инсульта все усилия неврологов направлены на восстановление утраченных двигательных и речевых функций пациента. Проводится электромиостимуляция и массаж паретичных конечностей, ЛФК, механотерапия. Для коррекции нарушений речи (афазии, дизартрии), а также нарушений глотания, необходима консультация логопеда.
Прогноз и профилактика
Прогноз при ишемическом инсульте зависит, прежде всего, от локализации и объема поражения головного мозга, возраста пациента, а также тяжести сопутствующих заболеваний. Наиболее тяжелое состояние пациента приходится на первые 3-5 дней заболевания, когда нарастает отек мозга в области очага поражения. Далее наступает период стабилизации или улучшения с возможным восстановлением нарушенных функций. В настоящее время процент летальных исходов при ишемическом инсульте составляет 15-20%.
Вторичная профилактика ишемического инсульта — комплексная программа, включающая в себя четыре направления: гипотензивную терапию (ингибиторы ангиотензин-превращающего фермента и диуретики); антитромботическую терапию (непрямые антикоагулянты и антиагреганты); гиполипидемическую терапию (статины); хирургическое лечение каротидных артерий (каротидная эндатерэктомия).
В России инсульт занимает 2-е место в структуре общей смертности населения и является основной причиной стойкой утраты трудоспособности: примерно 20% больных, перенесших инсульт, становятся тяжелыми инвалидами и нуждаются в посторонней помощи. Среди всех
В России инсульт занимает 2-е место в структуре общей смертности населения и является основной причиной стойкой утраты трудоспособности: примерно 20% больных, перенесших инсульт, становятся тяжелыми инвалидами и нуждаются в посторонней помощи. Среди всех видов инсульта преобладают ишемические поражения мозга.
Ишемический инсульт представляет собой гетерогенный клинический синдром. Согласно международным критериям TOAST, выделяют несколько патогенетических вариантов ишемического инсульта: инсульт, связанный с поражением артерий крупного калибра и развивающийся по типу атеротромбоза или артерио-артериальной эмболии; кардиоэмболический инсульт; микрососудистый (лакунарный) инсульт; редкие формы (синдром моя-моя, инсульт на фоне воспаления стенки сосуда (васкулит), расслоения (диссекция) стенки артерий и др.), а также недифференцированные формы. Лечение и вторичная профилактика ишемического инсульта должны проводиться с учетом его патогенетического варианта.
В начале 1990-х гг. было показано, что развитие инфаркта в первые минуты и часы заболевания происходит по быстрым механизмам некротической смерти клеток. Пусковым звеном является энергетический дефицит, который инициирует так называемый глутамат-кальциевый каскад, характеризующийся избыточным высвобождением возбуждающих аминацидергических нейротрансмиттеров — аспартата и глутамата — и чрезмерным внутриклеточным накоплением ионов Са2+ — основного триггера конечных механизмов каскада, приводящих к смерти клетки.
Поэтому при инсульте очень важно оказание быстрой и патогенетически обоснованной медицинской помощи, желательно в течение первых 2–3 ч с момента его развития.
Современные представления о механизмах развития ишемического инсульта позволили выделить два основных направления патогенетической терапии: улучшение перфузии ткани мозга (ранняя реканализация сосуда и реперфузия) и нейропротективная терапия.
При восстановлении адекватной перфузии ткани головного мозга клинического улучшения у больных можно ожидать даже в случае отсутствия у них при МРТ визуализируемой зоны диффузионно-перфузионного несоответствия.
Проведение терапевтической реперфузии целесообразно в пределах 3–6 ч, затем при ее применении значительно нарастает риск не только реперфузионного повреждения, но и геморрагических осложнений. Таким образом, реперфузия должна быть ранней, по возможности активной и кратковременной.
Установлено, что выраженность положительной клинической динамики зависит от скорости лизиса тромба: наилучшее восстановление неврологических функций происходит при быстром (почти мгновенном) лизисе тромба. При этом скорость лизиса тромба варьирует при разных патогенетических вариантах инсульта. Наиболее быстрый и полный лизис происходит при кардиоэмболическом инсульте, что сопровождается достоверным улучшением исхода инсульта и более полным функциональным восстановлением больного. Медленная реканализация чаще наблюдается при атеротромботическом поражении артерии и может не сопровождаться значимым улучшением клинической динамики.
Спонтанная реканализация окклюзированной артерии наблюдается примерно у 10% больных с ишемическим инсультом. Проведение раннего ультразвукового исследования (транскраниальной ультразвуковой допплерографии — аппараты Angiodin 3, Companion III, Sonovit SV-30, Биомед-2, Сономед-500) повышает частоту возможной реканализации до 20%.
При большинстве окклюзий артерий среднего и крупного калибра терапией выбора является тромболизис, обеспечивающий раннюю реканализацию в 30-40% случаев. В настоящее время разработаны пять поколений тромболитиков:
I поколение — системные тромболитики: природные активаторы плазминогена (стрептокиназа, урокиназа);
II поколение — фибриноселективные тромболитики: рекомбинантный тканевый активатор плазминогена (rt-PA, альтеплаза, актилиза), рекомбинантная проурокиназа;
IV поколение — усовершенствованные активаторы плазминогена III поколения (биосинтетические);
Тромболитики I поколения не применяются в клинических условиях из-за системного действия на гемостаз и высокой частоты геморрагических осложнений. Тромболитики III–V поколений проходят испытания пока еще в экспериментальных доклинических работах.
Основную роль в клинической практике играют тромболитики II поколения: rt-PA и рекомбинантная проурокиназа, обладающие малым системным тромболитическим эффектом, действующие преимущественно на свежий тромб и не активирующие факторы свертывания крови V и VII, что существенно снижает риск развития генерализованных геморрагических осложнений.
Рекомбинантный тканевый активатор плазминогена рекомендован к применению в первые 180 мин после развития ишемического инсульта, обусловленного окклюзией артерии среднего и крупного диаметра, при отсутствии геморрагического компонента в очаге ишемии и зоны обширной гиподенсивности на КТ/МРТ головного мозга, превышающей 1/3 области средней мозговой артерии, при значениях системного артериального давления не выше 180/110 мм рт. ст. Следует использовать дозу 0,9 мкг/кг, максимально — 90 мг/сут; 10 % дозы вводится внутривенно струйно, оставшиеся 90% — внутривенно капельно в течение 60 мин.
Одним из перспективных направлений реканализации является хирургическое удаление тромба — эндоваскулярная экстракция или иссечение. Результаты закончившегося исследования Merci Retriever Study, оценивающего эффективность эндоваскулярной экстракции тромба с помощью технологий Concentric Medical Inc., показали, что быстрая (мгновенная) реканализация окклюзированного сосуда наступает в 48% случаев, а реканализация в течение первых суток — в 81% случаев. Каких-либо осложнений, возникающих в результате манипуляции, не выявлено.
Теоретические данные позволяли полагать, что антикоагулянты, в частности гепарин, должны быть эффективными при ишемическом инсульте. Однако международные исследования (International Stroke Trial Collaborative Group) показали, что при лечении гепарином больных с ишемическим инсультом высокий риск развития раннего кровоизлияния превышает положительный эффект терапии. Лишь субгрупповой анализ post-hoc доказал целесообразность применения антикоагулянтной терапии гепарином в первые дни прогредиентного атеротромботического инсульта, а также при подтвержденной кардиогенной эмболии и проведении хирургических вмешательств на сосудах мозга. Гепарин назначают в течение первых 3–5 дней заболевания в суточной дозе до 10–15 тыс. ед. под контролем лабораторных показателей, прежде всего АЧТВ (которое не должно увеличиваться более чем в 2 раза). За 1–2 дня до окончания курса лечения гепарином целесообразно постепенное снижение его дозы с назначением антикоагулянтов непрямого действия (аценокумарол, варфарин, этил бискумацетат), прием которых продолжается в последующие 2–3 нед. Наиболее эффективно применение варфарина в дозе 2–5 мг/сут, особенно при длительной предшествующей терапии гепарином, при наличии мерцательной аритмии, после протезирования клапанов сердца или сопутствующем инфаркте миокарда. В случае отсутствия сопутствующей кардиальной патологии возможно назначение фенилина в суточной дозе 0,03–0,06 г. Следует помнить, что лечение антикоагулянтами непрямого действия также необходимо проводить под строгим лабораторным контролем показателей коагулограммы. Биологическая активность гепарина зависит от плазменного ингибитора протеаз — антитромбина-3. Поэтому при дефиците антитромбина-3 больным с нарастающим тромбозом основной или внутренней сонной артерии рекомендуется одновременно с гепарином вводить плазму крови (альбумин, декстран — 100 мл 1–2 раза в день).
Среди негеморрагических осложнений гепаринотерапии следует отметить преходящую тромбоцитопению (у 25% пациентов, причем у 5% — тяжелую), а также парадоксальную тромбоэмболию (Reilly et al., 2001), вследствие вызванной гепарином агрегации тромбоцитов. Тромбоэмболические осложнения, вызванные применением гепарина, лечатся прекращением его введения и назначением непрямых антикоагулянтов.
Гемодилюция и антиагрегантная терапия, не оказывая радикального реперфузионного действия, несколько улучшают микроциркуляцию в ткани мозга, что служит основанием для традиционного их применения в первые дни ишемического инсульта под контролем гемореологических и сердечно-сосудистых показателей.
Гемодилюцию проводят низкомолекулярными декстранами (реополиглюкин, реомакродекс, лонгастерил, реохем — по 250—500 мл внутривенно капельно). Основным ориентиром эффективности гемодилюции является снижение уровня гематокрита до 30—35%.
Сравнительное сопоставление влияния различных антитромбоцитарных препаратов показало высокую эффективность ацетилсалициловой кислоты (тромбо АСС, аспирин кардио) в дозе 1 мг/кг/сут при отсутствии достаточного антиагрегационного эффекта меньших доз препарата, что связано с недостаточным их влиянием на цАМФ и концентрацию простациклина. Установлена также эффективность пентоксифиллина (трентала, флекситала, пентилина), оказывающего комплексное реологическое действие, направленное не только на уменьшение агрегационной способности тромбоцитов, но и на улучшение деформируемости мембран эритроцитов и нормализацию микроциркуляции в целом. У больных молодого возраста с гиперкинетическим типом кровообращения (выраженная тахикардия, стойкое повышение систолического артериального давления) предпочтителен выбор малых доз β-адреноблокаторов (обзидан, анаприлин, индерал), обладающих антиагрегационными свойствами. У пожилых больных целесообразно назначение ангиопротекторов (ангинин, продектин, пармидин), также оказывающих антитромбоцитарное действие.
Позитивное влияние на состояние церебральной гемодинамики оказывают препараты комплексного сосудисто-метаболического действия, ярким представителем которых является кавинтон (винпоцетин). Анализ 25-летнего опыта применения препарата показал, что кавинтон улучшает мозговой кровоток и микроциркуляцию, оказывая избирательное вазодилатирующее и антивазоконстрикторное действие на церебральные сосуды, ингибируя агрегацию и адгезию форменных элементов крови, нормализуя деформируемость мембран эритроцитов. Наряду с этим препарат способствует улучшению энергетического метаболизма, оптимизируя окислительно-восстановительные процессы, активизируя транспорт кислорода и глюкозы, а также их утилизацию в ткани головного мозга. Кавинтон обладает антиоксидантными и антиэксайтотоксическими свойствами, нормализует ионный градиент клеточных мембран. При ишемическом инсульте в острой фазе эффективно назначение препарата в дозе 10–20 мг/сут внутривенно капельно (в разведении на 500 мл физиологического раствора) в течение 7–10 дней (в некоторых случаях до 21 дня) с дальнейшим переводом больного на прием таблетированных форм препарата: кавинтона форте — по 10 мг 3 раза в сутки в течение 3–4 нед, затем — кавинтона — по 5 мг 3 раза в сутки в течение 1–3 мес.
Проведение активной реперфузионной терапии возможно лишь в стационаре после нейровизуализирующего исследования (КТ/МРТ головного мозга), позволяющего исключить геморрагический компонент поражения, оценить размеры ишемизированной территории и патогенетический вариант инсульта. Это оттеняет преимущества другого направления терапии — нейропротекции (цитопротекции, метаболической защиты мозга), которая может использоваться на догоспитальном этапе при появлении первых симптомов инсульта даже при возможном геморрагическом его характере.
Следствием открытия феномена эксайтотоксичности явилось создание новых терапевтических стратегий — препаратов-антагонистов глутаматных NMDA- и AMPA-рецепторов и ингибиторов пресинаптического высвобождения глутамата. Несмотря на то что у препаратов этих групп в эксперименте были продемонстрированы выраженные нейропротективные эффекты, клинические испытания большинства из них были прекращены из-за широкого спектра серьезных побочных явлений (психических, локомоторных, общих токсических).
В настоящее время продолжаются исследования эффективности ремацемида — низкоаффинного неконкурентного антагониста NMDA-рецепторов, обладающего способностью ингибировать и потенциалзависимые кальциевые каналы. При клинических испытаниях внутривенных и оральных форм ремацемида в дозе до 400 мг каждые 12 ч значимых побочных эффектов не обнаружено.
Еще одним препаратом, блокирующим NMDA-зависимые каналы потенциалзависимым способом, является сульфат магния.
Внимание исследователей привлекает роль тормозного нейротрансмиттера глицина в механизмах острой церебральной ишемии. Была доказана роль глицина как тормозного нейротрансмиттера практически во всех отделах ЦНС. G. E. Fagg и A. C. Foster, F. Mayor и соавт. сделали вывод, что ГАМК и глицин являются равноценными нейротрансмиттерами, обеспечивающими защитное торможение в ЦНС, роль которого возрастает в условиях повышенного выброса глутамата. Ингибирующие свойства глицин проявляет посредством взаимодействия не только с собственными глициновыми рецепторами, но и с рецепторами ГАМК.
Вместе с тем J. W. Johnson и P. Ascher (1987) впервые экспериментально доказали, что глицин в субмикромолекулярных концентрациях необходим для нормального функционирования глутаматных NMDA-рецепторов. Потенцирующее действие глицина на NMDA-рецепторы проявляется в концентрациях ниже 0,1 мкмоль, а концентрации от 10 до 100 мкмоль полностью насыщают глициновый сайт. Введение высоких концентраций глицина (100 мкмоль и 1 млмоль) крысам в условиях недостатка кислорода не вызывало длительной модуляции активности NMDA-рецепторов в гиппокампе и не увеличивало эксайтотоксичность. Интересно, что введение животным высоких доз глицина или некоторых его агонистов (1-амино-1-карбоксициклопропана, являющегося почти полным агонистом, и D-циклосерина, обладающего 40–60% эффективности глицина) оказывает противосудорожное действие, а также усиливает эффекты противоэпилептических средств.
Наряду с нейротрансмиттерным глицин обладает также общеметаболическим действием, связывает низкомолекулярные токсичные продукты, в больших количествах образующиеся в процессе ишемии.
Являясь естественным метаболитом мозга, глицин не проявляет токсичности даже в дозах более 10 г/сут. Единственным побочным эффектом препарата может считаться легкая седация. Применение глицина в дозе 1–2 г/сут в течение 5 дней у пациентов с острым ишемическим инсультом (начиная с 6 ч после развития первых симптомов) позволяет обеспечить противоишемическую защиту мозга у больных с различной локализацией сосудистого поражения и разной тяжестью состояния — достоверно ускоряет регресс неврологической симптоматики (p 75; модифицированная шкала Рэнкина — 0–2) до 73,7 % от общего количества выживших больных.
Углубление знаний об ишемическом повреждении мозга и регенерации мозговой ткани позволяет нам все яснее представлять себе бесконечную сложность познания этих процессов. К счастью, работая в клинике, мы имеем возможность не отдаляться от реалий жизни и ежедневно оценивать применение научных гипотез на практике. Это помогает сохранять оптимизм и надежду.
В. И. Скворцова, доктор медицинских наук, профессор, член-корреспондент РАМН
РГМУ, Москва
Читайте также:

