Биотехнологические процессы получения органических кислот реферат
Обновлено: 02.07.2024
Органические кислоты — органические вещества, проявляющие кислотные свойства. К ним относятся карбоновые кислоты, содержащие карбоксильную группу -COOH, сульфоновые кислоты, содержащие сульфогруппу -SO3H и некоторые другие. В свободном состоянии кислоты находятся в плодах некоторых растений, крови, выделениях животных; они входят в состав жиров, эфирных и растительных масел, восков. Органические кислоты играют важную роль в некоторых процессах обмена веществ и функции желудочно-кишечного тракта. Полностью окисляясь в организме, они дают ему 10—15 кДж (2,4—3,6 ккал) и большое количество ценных щелочных компонентов, образуя углекислый газ (диоксид углерода) и воду.
Содержание
Введение
1. Биосинтез органических кислот …………………………………………. 4
2. Химический синтез органических кислот ……………………………….7
3. Этапы технологии получения, выделения
органических кислот ………………………………………………………….9
4. Производство готовой формы, и очистка
органических кислот …………………………………………………………11
5. Использование готовых форм в промышленности………………………15
Заключение
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
Прикрепленные файлы: 1 файл
биотехнология.docx
1. Биосинтез органических кислот …………………………………………. 4
2. Химический синтез органических кислот ……………………………….7
3. Этапы технологии получения, выделения
4. Производство готовой формы, и очистка
5. Использование готовых форм в промышленности………………………15
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
Органические кислоты — органические вещества, проявляющие кислотные свойства. К ним относятся карбоновые кислоты, содержащие карбоксильную группу -COOH, сульфоновые кислоты, содержащие сульфогруппу -SO3H и некоторые другие. В свободном состоянии кислоты находятся в плодах некоторых растений, крови, выделениях животных; они входят в состав жиров, эфирных и растительных масел, восков. Органические кислоты играют важную роль в некоторых процессах обмена веществ и функции желудочно-кишечного тракта. Полностью окисляясь в организме, они дают ему 10—15 кДж (2,4—3,6 ккал) и большое количество ценных щелочных компонентов, образуя углекислый газ (диоксид углерода) и воду. Эти продукты быстро выводятся из организма вместе со шлаками и излишней жидкостью, уменьшая отеки. При малоподвижном образе жизни, стрессовых ситуациях, загрязнении окружающей природной среды и воздействии других неблагоприятных факторов, приводящих к накоплению кислых продуктов неполного окисления, ощелачивающее действие органических кислот имеет важное значение в оздоровлении организма человека. Являясь сильными возбудителями секреции поджелудочной железы и моторной функции кишечника, органические кислоты оказывают влияние на процессы пищеварения.
Самыми известными органическими кислотами являются уксусная, м уравьиная, лимонная, щавелевая и молочная.
Органические кислоты используют в пищевой, химической, фармацевтической, легкой промышленности, в быту. В самых больших количествах производятся пищевые кислоты: лимонная, молочная, уксусная и винная.
Биосинтез органических кислот.
Несмотря на значительный прогресс в области органического синтеза многие кислоты (лимонная, молочная, итаконовая, уксусная и др.) получают в настоящее время микробиологическим синтезом.
Образование лимонной кислоты из глюкозы — сложный биохимический процесс. Вначале из глюкозы образуется пировиноградная кислота, но этот процесс чрезвычайно сложен.
Изучение анаэробного распада углеводов привело к установлению следующих промежуточных продуктов: углеводы + фосфорная кислота -> гексозофосфат -> триозофосфат + фосфо-глицериновая кислота -> фосфопировиноградная кислота. Дальнейшее превращение пировиноградной кислоты в зависимости от наличия ферментативных систем у дрожжей протекает различно.
Лимонная кислота встречается в плодах цитрусовых, ананасов, груш, брусники, клюквы. Лимоны и апельсины были главными источниками естественной (растительной) лимонной кислоты, которую производили преимущественно в Италии. Для получения лимонной кислоты путем микробного синтеза наиболее подходящим оказался плесневый гриб рода Aspergillus . В настоящее время селекционированно множество производственных штаммов Aspergillus niger для биосинтеза лимонной кислоты. Максимальный выход лимонной кислоты получается при биосинтезе из сахарозы, поэтому в качестве сырья используют мелассу. В последнее время успешно завершены эксперименты по биосинтезу лимонной кислоты дрожжами рода Candida из этанола. Общий выпуск лимонной кислоты в мире составляет 400 тыс.тонн в год.
Молочная кислота всегда присутствует в кислом молоке. Для промышленного получения этой кислоты используют глюкозу, мальтозу, сахарозу, лактозу, крахмал, т.к. молочнокислые бактерии трансформируют эти углеводы в молочную кислоту. Для сбраживания углеводов используют штаммы Lactobacillus delbruecki.
В большинстве производств молочную кислоту получают из мелассы ( 90 т в год).
Известно, что пировиноградная кислота является исходным продуктом для синтеза целого ряда важнейших веществ, определяющих направление обмена в живой клетке.
Дрожжи способны декарбоксилировать пировиноградную кислоту в уксусный альдегид, они также способны непосредственно превращать пировиноградную кислоту в уксусную посредством окислительного декарбоксилирования.
При спиртовом брожении пировиноградная кислота через уксусный альдегид образует этанол, а при гликолизе под действием лактикодегидрогеназы и НАД-Н2 она превращается в молочную. Пировиноградная кислота участвует в реакциях переаминирования, она легко аминируется в аланин.
Пировиноградная кислота участвует в синтезе кислот по циклу Кребса. Но прежде, чем она будет вовлечена в циклы ди- и трикарбоксильных кислот, она должна, с одной стороны, карбоксилироваться в щавелевоуксусную кислоту, а с другой — в присутствии коэнзима А превратиться в ацетил-КоА. Эти две реакции можно представить в следующем виде:
СН3—СО—СООН+С02+АТФ->НООС—СН2— СО—СООН+АДФ +Ф ,
Коэнзим А является переносчиком ацетильной группы, которая присоединяется к нему через эфирную микроэргическую связь. Поэтому в микроорганизмах широко распространены ацетилфосфаты, которые принимают участие в биохимических реакциях, связанных с выделением энергии. Роль коэнзима А в биологических окислениях и синтезах стала более интенсивно исследоваться после препаративного приготовления его, осуществленного Ф. Линеном и Е. Рейхертом. Была установлена взаимная связь между изменением содержания коэнзима А в дрожжевых клетках и скоростью окисления уксусной кислоты. Доказано, что при недостатке коэнзима А дрожжи слабо окисляют уксусную кислоту.
Ацетил-КоА образуется не только из пировиноградной кислоты, но и из уксусной кислоты и уксусного альдегида. Источником образования щавелевоуксусной кислоты являются яблочная и аспарагиновая кислоты, а также путь карбоксилирования пировиноградной кислоты.
Дрожжи обладают всеми ферментативными системами для образования щавелевоуксусной кислоты из указанных соединений, они содержат также коэнзим А и способны образовывать ацетил-КоА из пировиноградной и уксусной кислот.
С помощью изотопного углерода в виде NaHC1403 винные дрожжи способны карбоксилировать пировиноградную кислоту с образованием щавелевоуксусной кислоты. Последняя реагирует с ацетил-КоА и образует лимонную кислоту .
Методом бумажной хроматографии из культуральной жидкости дрожжей были выделены радиоактивная лимонная кислота, молочная, яблочная и янтарная.
Винные дрожжи способны превращать лимонную кислоту по циклу трикарбоксильных кислот и образовывать янтарную и глиоксалевую кислоты, последняя конденсируется с ацетил-КоА и образует яблочную кислоту по глиоксалатному циклу.
Кроме- того, винные дрожжи также способны синтезировать лимонную кислоту из глютаминовой кислоты и аланина путем дезаминирования их в соответствующие кетокислоты и в дальнейшем превращать их по циклу Кребса.
Во-первых, винные дрожжи способны карбоксилировать пировиноградную кислоту в щавелевоуксусную. Они также способны превращать пировиноградную кислоту в ацетил-КоА. Последний конденсируется с щавелевоуксусной кислотой и образует лимонную кислоту.
Во-вторых, дрожжи путем окислительного декарбоксилирования превращают пировиноградную кислоту в уксусную. Последнюю они способны конденсировать в янтарную кислоту через ацетил-КоА, янтарную кислоту они превращают в щавелевоуксусную через фумаровую и яблочную. Щавелевоуксусная кислота конденсируется с ацетил-КоА и образуется лимонная кислота.
Химический синтез органических кислот.
Цель синтетической химии — создание сложных веществ из элементов или простых химических соединений для применения их в практике (в том числе и в промышленности) и для теоретических исследований.
Впервые синтез органических соединений в лаборатории удалось осуществить Ф.Велеру (в период 1824–1828), при гидролизе дициана он получил щавелевую кислоту, выделяемую до этого из растений, а при нагревании циановокислого аммония за счет перестройки молекулы получил мочевину – продукт жизнедеятельности живых организмов .
В 1824 г. при действии циана на жидкий аммиак Вёлер синтезировал щавелевую кислоту. Щавелевую кислоту получают окислением углеводов, спиртов и гликолей смесью HNO3 и H2SO4 в присутствии V2O5, либо окислением этилена и ацетилена HNO3 в присутствии PdCl2 или Pd(NO3)2, а также окислением пропилена жидким NO2. Перспективен способ получения щавелевой кислоты из CO через формиат натрия:
Ранними промышленными методами получения уксусной кислоты были окисление ацетальдегида и бута на.
Ацетальдегид окислялся в присутствии ацетата марганца (II) при повышенной температуре и давлении. Выход уксусной кислоты составлял около 95 % при температуре 50-60 °С.
Окисление бутана проводилось при температуре 150—200 °C и давлении 150 атм. Катализатором этого процесса являлся ацетат кобальта.
Оба метода базировались на окислении продуктов крекинга нефти.
В результате повышения цен на нефть оба метода стали экономически невыгодными, и были вытеснены более совершенными каталитическими процессами карбонилирования метанола.
Муравьиная кислота. Как побочный продукт в производстве уксусной кислоты жидкофазным окислением бутана.
Реакцией монооксида углерода с гидроксидом натрия:
NaOH + CO → HCOONa → (+H2SO4, −Na2SO4) HCOOH
Это основной промышленный метод, который осуществляют в две стадии: на первой стадии монооксид углерода под давлением 0,6—0,8 МПа пропускают через нагретый до 120—130 °C гидроксид натрия; на второй стадии проводят обработку формиата натрия серной кислотой и вакуумную перегонку продукта.
Разложением глицериновых эфиров щавелевой кислоты. Для этого нагревают безводный глицерин со щавелевой кислотой, при этом отгоняется вода и образуются щавелевые эфиры. При дальнейшем нагревании эфиры разлагаются, выделяя углекислый газ, причём образуются муравьиные эфиры, которые после разложения водой дают муравьиную кислоту и глицерин.
Молочная кислота. В пищевой промышленности используется как консервант, пищевая добавка E270.
Получают молочную кислоту молочнокислым брожением глюкозы (ферментативная реакция):
Этапы технологии получения, выделения органических кислот.
К традиционным направлениям пищевой биотехнологии относится получение органических кислот – лимонной, молочной, яблочной, уксусной, янтарной, которые широко используются в пищевой промышленности в качестве регуляторов кислотности и консервантов.
Несмотря на значительный прогресс в области органического синтеза многие кислоты (лимонная, молочная, итаконовая, уксусная и др.) получают в настоящее время микробиологическим синтезом. Органические кислоты находят широкое применение в фармацевтической, химической, текстильной и других отраслях промышленности. Пищевая промышленность традиционно является основным потребителем лимонной, уксусной и молочной кислот, так как продукты естественного брожения более предпочтительны, чем синтетические кислоты в связи с безвредностью для организма человека содержащихся в них примесей.
С помощью микроорганизмов можно получить до 60 органических кислот. Многие из них получаются в промышленном масштабе - итаконовая, молочная, уксусная, лимонная, яблочная, янтарная. Эти пищевые кислоты используются как регуляторы кислотности и консерванты. Лимонную кислоту получают с помощью Yarrowia lipolytica, Aspergillus niger, молочную – Endomycopsis fibuligera, Rhisopus oryzae,
Lactobacillus casei, янтарную – Anaerobiospirillum succiniproducens. Уксусную кислоту получают путем микробиологической конверсии водорода и углекислого газа бактериями Acetobacterium woodi и Clostridium aceticum.
Этапы технологии получения и выделения; очистка и производство готовой формы органических кислот ( на примере лимонной кислоты)
Лимонная кислота (С6Н8О7) - трехосновная оксикислота, широко распространена в природе, относительно много ее содержится в некоторых ягодах, фруктах, особенно в цитрусовых (в лимоне 5-10 %), в листьях и стеблях некоторых растений.
Ранее лимонную кислоту выделяли в виде лимоннокислого кальция из продуктов переработки листьев хлопчатника, стеблей махорки, хвои ели и в значительных количествах из плодов лимонов. Однако это производство является крайне дорогим и небольшим по объему. Поэтому лимонная кислота была дефицитным и дорогим продуктом.
В настоящее время лимонная кислота по объему производства является одним из главных продуктов микробного синтеза, ее общий выпуск в разных странах достигает до 400 тыс. тонн в год.
В начале нашего столетия рядом исследователей было замечено, что некоторые плесневые грибы обладают способностью образовывать заметные количества органических кислот.
В дальнейшем путем отбора и направленной селекции были выделены активные продуценты органических кислот.
Для получения лимонной кислоты используют микроскопические грибы родов Aspergillus, Penicillium, Mucor, Ustina и др. В настоящее время основными продуцентами лимонной кислоты являются различные штаммы гриба Aspergillus niger, которые отличаются большой скоростью роста, легкостью культивирования и высоким выходом лимонной кислоты по отношению к массе окисляемого углевода. Они устойчивы к внешним воздействиям и имеют обильное конидиеношение. Споры грибов для получения лимонной кислоты хранят только в сухом виде.
Органические кислоты и их соли широко используются в пищевой, фармацевтической, кожевенной, текстильной, химической, металлургической и других отраслях промышленности. Большинство кислот, используемых для технических нужд, производится химическим путем на основе нефтехимического сырья и продуктов сухой перегонки древесины. В тех случаях, когда химический синтез кислот является сложным и экономически невыгодным, или если они имеют пищевое или медицинское назначение, кислоты производят микробиологическим путем. С помощью микроорганизмов может быть получено более 50 различных органических кислот, методы получения их разработаны достаточно подробно. В настоящее время только 6 органических кислот производится биотехнологическим путем в промышленном масштабе. Причем лимонную, глюконовую, кетоглюконовую и итаконовую кислоты производят только микробиологическим путем, а молочную и уксусную - как химическим, так и микробиологическим методами.
Уксусная кислота имеет наибольшее значение среди органических кислот. Ее используют при выработке многих химических веществ, включая каучук, пластмассы, волокна, инсектициды. Микробиологический способ производства уксусной кислоты состоит в превращении этанола в уксусную кислоту при участии бактерий Acetobacter иGluconobacter.Процесс идет в анаэробных условиях в режиме непрерывного культивирования продуцента.
Лимонную кислотушироко используют в пищевой (приготовление соков, кондитерских изделий), фармацевтической и косметической промышленности. Ею заменяют фосфаты в составе детергентов, так как она полностью метаболизируется живыми организмами и не загрязняет окружающую среду. Лимонная кислота образует хелаты с металлами, поэтому ее применяют для их очистки. Производят лимонную кислоту из сахара или из отходов его производства – мелассы, из содержащих глюкозу гидролизатов древесины и зерна. Мировое производство лимонной кислоты составляет более 300 тыс.т в год. Для промышленного производства лимонной кислоты используют, главным образом, культуру грибаAspergillus nigerиA. wentii.
Глюконовая, кетоглюконовая, итаконовая и молочная кислоты используются в пищевой промышленности в качестве подкислителей. Глюконат натрия, в виде которого обычно выделяют глюконовую кислоту, используют для извлечения металлов из руд, борьбы с коррозией, как моющее средство, в качестве медицинского препарата. Итаконовая кислота применяется при производстве пластмасс и красителей. Молочную кислоту используют при выделке кож и как сырье для производства биоразлагаемого полимера полилактата.
Получение продуктов брожения. Интенсивные технологии получения этанола.
Для производства спирта используют любое крахмалсодержащее сырье (все виды зерновых культур, картофель). Также используют сахаросодержащее сырье: свеклосахарную, тростниковую, сырцовую мелассу, сахар-сырец и др.
Технология производства этилового спирта состоит из ряда последовательных стадий: подготовка крахмалсодержащего сырья, разваривание крахмалсодержащего сырья, осахаривание разваренной массы, приготовление дрожжей, сбраживание осахаренного сусла, выделение спирта из бражки и его ректификация.
Подготовка крахмалсодержащего сырья включает его очистку от примесей, измельчение зерна на молотковых или вальцовых дробилках до частиц размером менее 3 мм. Очистка картофеля происходит на гидравлическом транспортере, затем его моют в картофелемоечных машинах и измельчают на молотковых дробилках или картофелетерках.
Измельченное сырье смешивается с теплой водой в соотношении 1 : 2,5–3,5. После перемешивания зерновой замес (или картофельная кашица) поступает в аппарат для разваривания, цель которого заключается в разрушении клеточной структуры сырья и растворении крахмала. Разваривание проводят в цилиндроконических аппаратах при нагревании острым паром под давлением не менее 0,4–0,6 МПа.
Процесс разваривания может проводиться периодическим, полунепрерывным или непрерывным способами. Наиболее распространено непрерывное разваривание. Измельченное сырье подогревается сначала вторичным, затем острым паром до температуры разваривания и выдерживается при этой температуре, продвигаясь по варочным аппаратам.
После 1 ч пропаривания при 90 °С в результате открытия нижнего клапана и резкого падения давления происходит как бы взрыв пропаренного сырья, и оно продавливается в аппарат (затиратель).
Разваренную массу охлаждают до температуры +57…61 °С (в зависимости от вида осахаривающего материала и способа осахаривания). Осахаривание охлажденной разваренной массы осахаривающими материалами (солодовым молоком или ферментными препаратами) проводят периодическим или непрерывным способом.
В результате получают продукт – сусло спиртового производства. Оно имеет массовую долю сухого вещества 16-18%, в том числе 13-15% сбраживаемых Сахаров. Оса харенное сусло (затор) охлаждают до температуры +18…22 °С в теплообменниках или с помощью вакуума.
В настоящее время биотехнологическими способами в промышленных масштабах синтезируют ряд органических кислот. Из них лимонную, глюконовую, кетоглюконовую и итаконовую кислоты получают лишь микробиологическим способом, молочную, салициловую и уксусную - как химическим, так и микробиологическим способами, а яблочную - химическим и энзиматическим путем.
ПОЛУЧЕНИЕ ОРГАНИЧЕСКИХ КИСЛОТ.
Получение уксусной кислоты. Уксусная кислота имеет наиболее важное значение среди всех органических кислот. Ее используют при выработке многих химических веществ, включая каучук, пластмассы, волокна, инсектициды. Микробиологический способ получения уксусной кислоты состоит в конверсии этанола в уксусную кислоту при участии бактерий штаммов Acetobacter и Gluconobacter:
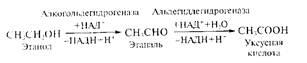
Процесс идет в анаэробных условиях в режиме непрерывного культивирования продуцента. Для роста бактерии Acetobacter aceti используют питательные среды, содержащие 6-12% этилового спирта, 1 % бактериального гидролизата, 0,05 % дигидрофосфата калия, 0,1% гидрофосфата аммония и 0,05% сульфата магния. Максимальная удельная активность непрерывной культуры Acetobacter aceti (количество микрограммов субстрата, подвергшегося окислению 1мкг биомассы за 1 мин) достигается к 20-м суткам культивирования при концентрации спирта 7 % и составляет 3,0 ед./мг.
Получение лимонной кислоты. Лимонную кислоту широко используют в пищевой, фармацевтической и косметической промышленности. Ею заменяют фосфаты в составе детергентов, так как она полностью метаболизируется живыми организмами. Лимонная кислота образует хелаты с металлами, поэтому ее применяют для их очистки. Объем мирового производства цитрата составляет 400 тыс. т/год. Самый крупный производитель лимонной кислоты США. Производство лимонной кислоты принадлежит к числу старейших промышленных микробиологических процессов: оно было организовано в 1893 г. С этого момента параллельно развитию фундаментальной микробиологии велись изыскания оптимальных продуцентов и технологических вариантов процесса ферментации.
Для промышленного производства лимонной кислоты используют главным образом культуру гриба Acetobacter niger, а также Acetobacter wentii.
Метаболическим источником лимонной кислоты в организме служит цикл трикарбоновых кислот — составная часть цикла Кребса. Суммарное уравнение химических процессов этого цикла следующее:
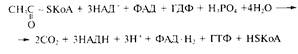
Реакция образования лимонной кислоты, катализируемая цитратсинтазой, открывает цикл Кребса, в котором цитрат постепенно окисляется до щавелево-уксусной кислоты (ЩУК). ЩУК снова конденсируется с ацетил-КоА, так что вновь образуется лимонная кислота (рис.1). Цитратсинтаза определяет скорость реакций, составляющих цикл Кребса. Активность фермента зависит от концентрации ЩУК, содержание которой может поддерживаться за счет функционирования конститутивной пируваткарбоксилазы, обеспечивающей переключение в аэробных условиях процессов гликолиза и глиоксилевого цикла.
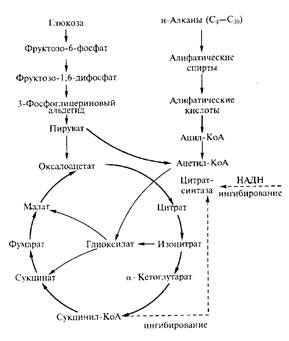
Рис. 1. Схема биосинтеза лимонной кислоты
синтазы тормозится НАДН и сукцинил - КоА. Скорость оборота цикла Кребса определяется поддержанием необходимого уровня окисленных форм коферментов дегидрогеназ (НАД + и ФАД; см. уравнение реакции), поэтому высокий выход цитрата получается лишь при условии хорошей аэрации. Накопление в культуральной среде существенных количеств цитрата - промежуточного соединения цикла Кребса - невыгодно для организма и является следствием дисбаланса метаболизма или нарушения его генетической природы. Рост культуры грибов обычно регулируют путем изменения содержания фосфата, ионов марганца, железа и цинка в среде. Дефицит фосфата ведет к сверхпродукции цитрата. Роль ионов металлов не до конца установлена. Считают, что дефицит ионов металлов влияет на свойства клеточных мембран и морфологию гиф.
Процесс ферментации, ведущий к образованию лимонной кислоты, проводят при низких значениях рН (3-4), что облегчает поддержание стерильных условий ферментации и уменьшает возможность образования побочных продуктов. В более щелочной среде происходит накопление щавелевой и глюконовой кислот. Предполагают, что в кислой среде стимулируется гликолиз, что обеспечивает направление потока углерода в цикл Кребса.
Питательные среды для культивирования продуцентов лимонной кислоты в качестве источника углерода содержат дешевое углеводное сырье: мелассу, крахмал и глюкозный сироп. Гриб Acetobacter niger чаще всего выращивают на мелассе. Гриб Trichoderma viride синтезирует значительные количества цитрата из глюкозы, что позволяет использовать для этого процесса целлюлозу. Предложены штаммы бактерий и дрожжей рода Candida, осуществляющие процесс на основе н-парафинов (С9-С30), которые пока широко не внедрены в промышленность.
Существует несколько технологических вариантов промышленного производства лимонной кислоты. Первоначально был разработан вариант процесса, основывающийся на поверхностной ферментации, позднее - на глубинном культивировании. Последнее ведется в две стадии: на первой стадии идет рост мицелия, а на второй, после выхода культуры в стационарную фазу - интенсивный синтез лимонной кислоты. В конце ферментации массу мицелия отделяют путем фильтрования и промывают. Затем при рН

Молочная кислота широко применяется в пищевой, текстильной и фармацевтической промышленности, в изготовлении растворителей и пластификаторов в лаках, олифах и т. п.
В промышленном производстве молочной кислоты обычно используют термофильные штаммы бактерий, синтезирующие целевой продукт при 50оС. Таким штаммом является Lactobacillus delbrueckii, отличающийся высокими стабильностью и активностью кислотообразования (выход молочной кислоты составляет 95-98 % от потребленной сахарозы).
Принципиальная технологическая схема получения L(+)-молочной кислоты состоит в следующем: мелассную среду, содержащую 5-20 % сахара, вытяжку солодовых ростков, дрожжевой экстракт, витамины, фосфат аммония, засевают L. delbrueckii. Брожение протекает при 49-50оС при исходном рН 6,3-6,5. По мере образования молочной кислоты ее нейтрализуют мелом.
Весь цикл ферментации завершается за 5-10 дней; при этом в культуральной жидкости содержатся 11-14 % лактата кальция и 0,1-0,5 % сахарозы. Клетки бактерий и мел отделяют фильтрованием, фильтрат упаривают до концентрации 3-0 %, охлаждают до 25оС и подают на кристаллизацию, которая длится 1,5-2 суток. Кристаллы лактата кальция обрабатывают серной кислотой при 60-70 С, гипс выпадает в осадок, а к надосадочной жидкости добавляют желтую кровяную соль при 65 С для удаления ионов железа, затем - сульфат натрия для освобождения от тяжелых металлов. Красящие вещества удаляют с помощью активированного угля.
После этого раствор молочной кислоты подвергают вакуум-упариванию до 50 или 80 %. Оставшийся не до конца очищенный раствор молочной кислоты используют для технических целей. Более очищенную кислоту можно получить при перегонке ее сложных метиловых эфиров, при экстракции простым изопропиловым эфиром в противоточных насадочных колоннах.
Получение пропионовой кислоты
Производство пропионовой кислоты осуществляется пропионовыми бактериями, представляющими собой грамположительные, бесспоровые, неподвижные палочки семейства Propionibacteriacae, культивируемые в средах, где источником углерода является глюкоза. Из трех молекул глюкозы образуется 4 молекулы пропионовой кислоты, 2 молекулы уксусной кислоты, 2 молекулы углекислого газа и 2 молекулы воды:
![]()
Перспективными для производства пропионовой кислоты оказались виды P. freudenreichii и P. acidipropionici.
Биосинтез кислоты проводят на достаточно простых средах, например такого состава (в %): углевод - 1-2; сульфат аммония - 0,3; гидолфосфат калия - 0,2; хлорид кобальта - 0,0001; биотин - 0,00001; пантоненат - 0,1; тиамин - 0,01.
Конечные продукты ферментации (пропионат и ацетат) можно не разделять, поскольку обе кислоты обладают консервирующими свойствами. Биосинтетическая пропионовая кислота применяется в пищевой и фармацевтической промышленности в качестве консерванта.
Окислительные процессы
Получение уксусной кислоты
Микробиологическое производство уксусной кислоты экономически выгодно лишь при получении пищевого уксуса, а не технической уксусной кислоты.
Исходная среда с 4 % этанола, 1,5 % уксусной кислоты и минеральными солями (моногидрофосфат аммония, дигидрофосфат калия, сульфат магния) непрерывно поступает в первый ферментатор, обогащается спиртом в последующих ферментаторах. Таким образом происходит обогащение среды уксусной кислотой при снижении концентрации этанола. Из последнего ферментатора непрерывно вытекает уксус. Выход уксусной кислоты достигает 30 кг/м /сут. и более.
Получение лимонной кислоты

Около 60 лет назад лимонную кислоту выделяли преимущественно из плодов цитрусовых растений. Теперь же основную массу ее производят с помощью определенных штаммов плесневого гриба Aspergillus niger.
Поскольку основным сырьем для получения лимонной кислоты является меласса, в которой содержится много железа, то на стадии пред-ферментации его осаждают при помощи желтой кровяной соли -K4[Fe(CN)6].
Известны два способа ферментации A. niger - поверхностный и глубинный. Первый из них реализуют на предприятиях малой и средней мощности в виде жидкофазной ферментации на жидкой среде (например, в ряде стран Европы и Америки) и в виде твердофазной ферментации (например, в Японии).
Технологическая схема жидкофазной ферментации представлена на рис. 4.3.

Рис. 4.3. Технологическая схема получения лимонной кислоты из мелассы поверхностным способом (жидкофазная ферментация): 1 - цистерна для мелассы; 4; 2 - центробежные насосы; 3 - реактор для разбавления мелассы; 4 - стерилизационная камера; 5 - бродильная камера; 6 - сборник сбраживаемых растворов; 7 - нейтрализатор; 8, 10 - нутч-фильтры; 9 - расщепитель; 11 -сборник-монтежю; 12 - вакуум-аппарат; 13 - дисолвер; 14 - фильтр-пресс; 15 - кристаллизатор; 16 - приемник; 17 - сушилка; 18 - готовая продукция; 19 - сборник фильтрата
Свободная лимонная кислота остается в растворе, а негидролизованный оксалат кальция и образовавшийся гипс СаS04 остаются в осадке. Раствор лимонной кислоты очищают, подвергают вакуум-упариванию и кристаллизуют. Кристаллы кислоты высушивают и фасуют. Мицелий продуцента либо используют для выделения фермента пектиназы, либо высушивают и поставляют на корм скоту и домашней птице.
Твердофазная ферментация на уплотненных средах для получения лимонной кислоты - наиболее простой способ из всех известных. Ферментацию определенного штамма A. niger проводят на увлажненных отрубях риса или пшеницы, находящихся в кюветах. Условия биосинтеза кислот при этом аналогичны условиям на агаризированных или в жидких питательных средах. После окончания процесса отруби экстрагируют водой, куда переходят кислоты, а затем выделяют цитрат кальция и чистую лимонную кислоту согласно схеме, изложенной выше.
Глубинный способ производства базируется на использовании специальных культур A. niger (В России применяют селекционированный штамм № 288/9). Инокулят подращивают сначала в инокуляторе, затем - в посевном аппарате (примерно в 1/10 объема основного ферментатора) на среде с 3-4 % сахара. Спустя 1-1,5 суток инокулят передают из посевного в основной ферментатор, где процесс ведут в течение 5-7-10 суток на аналогичной среде с трехразовым доливом 25-28 % (по сахару) раствора мелассы с целью доведения конечной концентрации сахара в культуральной жидкости до 12-15 %. После окончания ферментации (контроль - снижение кислотообразования) мицелий гриба отфильтровывают и культуральную жидкость подвергают обработке, как указано выше.
Общая технологическая схема получения лимонной кислоты при глубинной ферментации приведена на рис. 4.4.

Рис. 4.4. Технологическая схема получения лимонной кислоты при глубинной ферментации продуцента: 1 - емкость с мелассой; 2 - приемник мелассы; 3 - весы; 4 - варочный котел; 5 -центробежный насос; 6 - промежуточная емкость; 7 - стерилизующая колонка; 8 -выдерживатель; 9 - холодильник; 10 - посевной аппарат; 11 - головной ферментатор; 12 - стерилизующие фильтры; 13 - емкость для хранения мелассы; 14 - промежуточный сборник; 15 - барабанный вакуум-фильтр; 16 - приемник для мицелия; 17 - вакуум-сборник для мицелия; 18 - вакуум-сборник фильтрата культуральной жидкости
Лимонную кислоту широко используют в пищевой, медицинской, фармацевтической и лакокрасочной промышленности.
Читайте также:

