Аномальные свойства воды реферат
Обновлено: 05.07.2024
Аномалия точек кипения и замерзания воды. Исключительная способность воды растворять любые вещества, ее высокое поверхностное натяжение. Ключевая роль аномальных и специфически свойств воды в ее многообразном взаимодействии с живой и неживой природой.
| Рубрика | Биология и естествознание |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 17.10.2018 |
| Размер файла | 16,9 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Аномальные свойства воды
вода аномальное свойство
Первое аномальное свойство воды - аномалия точек кипения и замерзания: Если бы вода - гидрид кислорода - Н2О была бы нормальным мономолекулярным соединением, таким, например, как ее аналоги по шестой группе Периодической системы элементов Д.И. Менделеева гидрид серы Н2S, гидрид селена Н2Se, гидрид теллура Н2Те, то в жидком состоянии вода существовала бы в диапазоне от минус 90 o С до минус 70 o С. При таких свойствах воды жизни на Земле не существовало бы.
“Ненормальные” температуры плавления и кипения воды далеко не единственная аномальность воды. Для всей биосферы исключительно важной особенностью воды является ее способность при замерзании увеличивать, а не уменьшать свой объем, т.е. уменьшать плотность. Это вторая аномалия воды, которая именуется аномалией плотности. На это особое свойство воды впервые обратил внимание еще Г. Галилей. При переходе любой жидкости (кроме галлия и висмута) в твердое состояние молекулы располагаются теснее, а само вещество, уменьшаясь в объеме, становится плотнее. Любой жидкости, но не воды. Вода и здесь представляет собой исключение. При охлаждении вода сначала ведет себя как и другие жидкости: постепенно уплотняясь, она уменьшает свой объем. Такое явление можно наблюдать до +4°С (точнее до +3,98°С). Именно при температуре +3,98°С вода имеет наибольшую плотность и наименьший объем. Дальнейшее охлаждение воды постепенно приводит уже не к уменьшению, а к увеличению объема. Плавность этого процесса вдруг прерывается и при 0°С происходит резкий скачок увеличения объема почти на 10%! В это мгновение вода превращается в лед. Уникальная особенность поведения воды при охлаждении и образовании льда играет исключительно важную роль в природе и жизни. Именно эта особенность воды предохраняет от сплошного промерзания в зимний период все водоемы земли - реки, озера, моря и тем самым спасает жизнь.
Вода -- единственная жидкость на Земле, лед которой не тонет за счет того, что его объем на 1/11 больше объема воды.
Все термодинамические свойства воды заметно или резко отличаются от других веществ.
Наиболее важная из них - аномалия удельной теплоемкости. Аномально высокая теплоемкость воды делает моря и океаны гигантским регулятором температуры нашей планеты, в результате чего не происходит резкого перепада температур зимой и летом, днем и ночью. Континенты, расположенные вблизи морей и океанов, обладают мягким климатом, где перепады температуры в различные времена года бывают незначительными.
Мощные атмосферные потоки, содержащие огромное количество теплоты, поглощенное в процессе парообразования, гигантские океанические течения играют исключительную роль в создании погоды на нашей планете.
Ни одно вещества на Земле не обладает такой способностью поглощать тепло, как вода. Для превращения в пар 1г воды требуется 537 калории тепла. Конденсируясь, пар возвращает эти 537 калорий в окружающую среду.
Ни одно вещество в мире не поглощает и не отдает среде столько тепла, сколько вода. Теплоемкость воды в 10 раз больше теплоемкости стали и в 30 раз больше ртути. Вода сохраняет тепло на Земле.
С поверхности морей, океанов, суши испаряется за год 520000 кубических километров воды, которые, конденсируясь, отдают много тепла холодным и полярным регионам.
Не обладай вода такой уникальной способностью поглощать и отдавать тепло, климат Земли оказался бы непригодным для существования человека. В высоких широтах тогда царил бы нестерпимый холод, а в низких -- солнце испепелило бы все живое.
Благодаря наземному Мировому океану атмосфера представляет собой надежное теплое одеяло, укрывающее тело планеты и защищающее его от космического холода. Подземный океан снабжает Землю теплом из внутренних источников планеты.
Аномалия теплоёмкости заключается в следующем:
При нагревании любого вещества теплоемкость неизменно повышается. Да, любого вещества, но не воды. Вода - исключение, она и здесь не упускает возможности быть оригинальной: с повышением температуры изменение теплоемкости воды аномально; от 0 до 37°С она понижается и только от 37 до 100°С теплоемкость все время растет. В пределах температур, близких к 37°С, теплоемкость воды минимальна. Именно эти температуры - область температур человеческого тела, область нашей жизни. Физика воды в области температур 35-41°С (пределы возможных, нормально протекающих физиологических процессов в организме человека) констатирует вероятность достижения уникального состояния воды, когда массы кристаллической и объемной воды равны друг другу и способность одной структуры переходить в другую максимальная. Это замечательное свойство воды предопределяет равную вероятность течения обратимых и необратимых биохимических реакций в организме человека и обеспечивает “легкое управление” ими.
Общеизвестна исключительная способность воды растворять любые вещества. И здесь вода демонстрирует необычные для жидкости аномалии, и в первую очередь аномалии диэлектрической постоянной воды. Это связано с тем, что ее диэлектрическая постоянная (или диэлектрическая проницаемость) очень велика и составляет 81, в то время как для других жидкостей она не превышает 10. В соответствии с законом Кулона сила взаимодействия двух заряженных частиц в воде будет в 81 раз меньше, чем, например, в воздухе, где эта характеристика равна единице. В этом случае прочность внутримолекулярных связей уменьшается в 81 раз и под действием теплового движения молекулы диссоциируют с образованием ионов. Необходимо отметить, что из-за исключительной способности растворять другие вещества вода никогда не бывает идеально чистой.
Следует упомянуть еще об одном удивительной аномалии воды - исключительно высоком поверхностном натяжении. Из всех известных жидкостей только ртуть имеет более высокое поверхностное натяжение. Это свойство проявляется в том, что вода всегда стремится сократить свою поверхность. Некомпенсированные межмолекулярные силы наружного (поверхностного) слоя воды, вызванные квантовомеханическими причинами, создают внешнюю упругую пленку. Благодаря пленке многие предметы, будучи тяжелее воды, не погружаются в воду. Если, например, стальную иголку осторожно положить на поверхность воды, то иголка не тонет. А ведь удельный вес стали почти в восемь раз больше удельного веса воды. Всем известна форма капли воды. Высокое поверхностное натяжение позволяет воде иметь шарообразную форму при свободном падении.
Поверхностное натяжение и смачивание являются основой особых свойств воды и водных растворов, названого - капиллярностью. Капиллярность имеет огромное значение для жизни растительного, животного мира, формирования структур природных минералов и плодородия земли. В каналах, которые во много раз уже человеческого волоса, вода приобретает удивительные свойства. Она становится более вязкой, уплотняется в 1,5 раза, а замерзает при минус 80-70°С. Причиной сверханомальности капиллярной воды являются межмолекулярные взаимодействия, тайны которых еще далеко не раскрыты.
Ни одна жидкость не поглощает газы с такой жадностью, как вода. Но она их также легко отдает.
Дождь растворяет в себе все ядовитые газы атмосферы. Вода - ее мощный природный фильтр, очищающий атмосферу от всех вредных и ядовитых газов.
Ученым и специалистам известна так называемая поровая вода. В виде тончайшей пленки она устилает поверхность пор и микрополостей пород и минералов земной коры и других объектов живой и неживой природы. Связанная межмолекулярными силами с поверхностью других тел, эта вода, как и капиллярная вода, обладает особой структурой.
Таким образом, аномальные и специфические свойства воды играют ключевую роль в ее многообразном взаимодействии с живой и неживой природой. Все эти необычные особенности свойств воды настолько “удачны” для всего живого, что делает воду незаменимой основой существования жизни на Земле.
Подобные документы
Гигиеническое значение воды. Роль воды в передаче инфекционных заболеваний. Влияние химического состава воды на здоровье населения. Индифферентные химические вещества в воде. Классификация очистки воды. Организмы - индикаторы фекального загрязнения.
реферат [258,6 K], добавлен 09.12.2009
Основные физиологические функции воды. Обеспечение жизнедеятельности организма и соблюдение питьевого режима. Питьевые минеральные, столовые и лечебные воды. Гидрокарбонатные, хлоридные, сульфатные, смешанные, биологически активные и газированные воды.
контрольная работа [10,7 K], добавлен 11.05.2011
Изучение физико-химических, термических, оптических свойств воды и грунтов, их влияния на состав населения. Обзор явлений в водоёмах. Принципы восприятия света, звука, движения воды водными организмами. Анализ механико-динамических особенностей грунтов.
курсовая работа [38,7 K], добавлен 21.08.2011
Общая характеристика живой и неживой природы. Неорганические и органические вещества в клетке: макроэлементы, микроэлементы, ультрамикроэлементы, соли, вода, нуклеиновые кислоты, углеводы, белки, липиды. Понятие биогенных элементов. Свойства воды.
презентация [3,7 M], добавлен 26.04.2012
Характеристика зависимости биологических свойств активированной воды от вещества матрицы. Анализ долгосрочного сохранения памяти о проведенной активации водного вещества после ее кипячения. Факторы, определяющие макроструктурные преобразования кипятка.
Так что же особенного в этом веществе. Молекула воды является наиболее распространённым веществом на планете и, встречающимся на ней в твёрдом, жидком и газообразном состоянии. Вода – жидкость без запаха, вкуса и цвета, плотность составляет 1,0 г/ см3. Гидросфера занимает 71% поверхности земного шара. Рождается из элементов, занимающих первое и третье место по распространенности на земле, в объёмном соотношении 2:1. Это одна из самых маленьких известных молекул. Уже много веков учёные изучают воду. Времени прошло очень много, казалось бы о воде должно было быть всё известно, но не всё так просто.
Оглавление
Введение______________________________________________________ 2
1. Вода – одно из аномальных природных явлений___________________ 4
2. Магические свойства воды_____________________________________ 10
3. Три мифа о воде_____________________________________________ 12
4. Неразгаданные свойства воды_________________________________ 15
5. Вода с философской точки зрения______________________________ 18
Заключение__________________________________________________ 19
Список использованной литературы______________________________ 20
Файлы: 1 файл
Аномальные свойства воды.docx
Введение______________________ ______________________________ __ 2
1. Вода – одно из аномальных природных явлений__ _________________ 4
2. Магические свойства воды__________________________ ___________ 10
3. Три мифа о воде__________________________ ___________________ 12
4. Неразгаданные свойства воды__________________________ _______ 15
5. Вода с философской точки зрения__________________ ____________ 18
Заключение____________________ ______________________________ 19
Список использованной литературы____________________ __________ 20
До сегодняшнего дня казалось, что не может быть проще воды. Выученная всеми формула, температурный переход ото льда до пара, способность растворять некоторые вещества и участвовать в процессе конвекции – больше не надо ничего. На самом же деле, с обыкновенной водой оказалось не так уж все и просто.
На сегодняшний день общество находится на пороге совершенно другого понимания законов мироздания, открывающего новые перспективы: возможность программирования воды, лечение водой сложнейших заболеваний, управление погодой.
Огромная роль воды в жизни природы и человека послужила причиной того, что она была одним из первых веществ привлекло внимание ученых. Глубокие философские обобщения привели человечество к необходимости познания физической и химической природы воды. Тем не менее, изучение воды еще далеко не закончено.
Так что же особенного в этом веществе. Молекула воды является наиболее распространённым веществом на планете и, встречающимся на ней в твёрдом, жидком и газообразном состоянии. Вода – жидкость без запаха, вкуса и цвета, плотность составляет 1,0 г/ см3. Гидросфера занимает 71% поверхности земного шара. Рождается из элементов, занимающих первое и третье место по распространенности на земле, в объёмном соотношении 2:1. Это одна из самых маленьких известных молекул. Уже много веков учёные изучают воду. Времени прошло очень много, казалось бы о воде должно было быть всё известно, но не всё так просто.
Вода выступала катализаторам развития многих фундаментальных научных дисциплин. Вспомним также о ее причастности к ядерной физике в виде тяжелой и сверхтяжелой воды. В настоящее время наступила эра всеобщего изучения роли воды в патологических и нормальных процессах жизни, которую можно назвать эрой водной медицины и биологии.
Изо льда состоят огромные горные ледники, им покрыты и некоторые материки. Лёд хранит в себе большие запасы пресной воды. Лёд твёрдый, а течёт как жидкость. Образуя огромные реки, медленно стекающие с гор. Лёд необычайно долговечен и прочен. Он может десятки тысяч лет хранить в себе скелеты животных, погибших в ледниках. Улавливая солнечное излучение, вода помогает поддерживать температуру на земле в комфортном диапазоне. Мощные морские течения разносят огромные объёмы воды по всей планете, в частности не дают мерзнуть европейцам омывая Европу Гольфстримом. И, наконец, вода обеспечивает жизнедеятельность всех организмов: она переносит многие питательные вещества, выводит и собирает отходы.
Вода – одно из аномальных природных явлений
В первой половине XIX века учёные обнаружили, что некоторые характеристики воды нарушают общепринятые законы природы, что в этих несоответствиях присутствует Божественный замысел и что они являются доказательством того, что вода была сотворена ради существования жизни. Позже известным русским ученым Дмитрием Менделеевым была составлена периодическая таблица, на основании которой он предсказал существование еще не известных науке элементов, а также свойства этих элементов и их соединений. Так вот оказалось, что вода не признает никаких закономерностей этой периодической системы. Согласно логике этой системы, вода должна была бы замерзать при -90°С, а она замерзает при 0°С, кипеть при -70°С, а она кипит при 100°С. И это далеко не все, что делает воду уникальным веществом.
Несмотря на то, что вода принята за эталон меры плотности, объема и т.д. для других веществ, сама она, как это ни странно, является самым аномальным среди всех веществ.
Одним из таких аномальных свойств воды является ее способность расширяться при замерзании. Ведь все вещества при замерзании, то есть при переходе из жидкого состояния в твердое, сжимаются, а вода, наоборот, расширяется. Ее объем при этом увеличивается на 9 %.
Попробуем представить на мгновение, что бы случилось зимой в природе, если бы лед тонул. Реки, озера, моря и океаны промерзли бы до самого дна, и все живые организмы в них погибли бы. Но когда на поверхности воды образуется лед, то он, находясь между холодным воздухом и водой, препятствует дальнейшему охлаждению и промерзанию водоемов.
Это необычное свойство воды важно и для образования почвы в горах. Попадая в маленькие трещины, которые всегда найдутся в камнях, дождевая вода при замерзании расширяется и разрушает камень. Так постепенно каменная поверхность становится способной приютить растения, которые своими корнями довершают этот процесс разрушения камней и приводят к образованию на склонах гор почвы.
Еще одно странное свойство воды связано с ее особым состоянием при температуре +4°С. При этой температуре она обладает максимально возможной для себя плотностью, а значит — и тяжестью. Вода при этой температуре тяжелее, чем при какой-либо другой, и поэтому всегда будет опускаться в водоеме на дно. Но долго ли она там пробудет? Дело в том, что дно водоема, как правило, или теплее или холоднее этой воды, поэтому слои воды с температурой +4°С, достигнув дна, будут или нагреваться или охлаждаться, а после этого всегда всплывать на поверхность. Вследствие этих процессов в водоеме всегда будет происходить перемешивание слоев воды. А это очень важно для жизни, так как вода у дна какого-либо тихого пруда или озерца всегда бедна кислородом, и если бы не происходило перемешивания воды, обитатели водоема начали бы задыхаться от его нехватки.
Как известно, вода, испаряясь с поверхности тела человека, растений и животных, предохраняет их от перегрева. Способность отдавать тепло в окружающую среду при испарении присуща любой жидкости. Однако когда ученые сравнили эти способности у разных жидкостей, то оказалось, что вода является здесь своего рода чемпионкой. По сравнению с любой другой жидкостью она отдает при своем испарении в окружающую среду самое большое количество тепла, что, безусловно, делает ее самым лучшим регулятором температуры нашего тела.
Другое свойство воды, помогающее нам справляться как с перегревом нашего тела, так и с его переохлаждением, — это ее аномально высокая теплоемкость. Вода при нагревании на один градус поглощает в 5-30 раз больше тепла, чем какое-либо другое вещество. Поэтому и те процессы, которые происходят в нашем организме при интенсивной мышечной работе, вызывают не столь высокое поднятие температуры, как это было бы в случае других жидкостей. У соли, к примеру, такое же количество выделенного тепла вызвало бы поднятие температуры в 5 раз большее, чем у воды, у железа — в 10 раз, а у свинца — в 30 раз.
Еще одно свойство воды, помогающее бороться организму с перегревом, — высокая теплопроводность. Если бы эта физическая константа имела бы меньшее значение, то выделяемое в процессе интенсивной физической работы тепло не передавалось бы так хорошо из глубины тела на его поверхность и, соответственно, не удалялось бы из организма вместе с потом.
Такие аномальные свойства воды, помогающие нашему организму сохранять постоянную температуру, имеют значение и для жизни всей нашей планеты. Так, благодаря аномально высокой теплоемкости воды, на континентах не происходит резкого перепада температур зимой и летом, ночью и днем, поскольку они окружены своеобразным термостатом — водами Мирового океана. Летом он не дает Земле перегреваться, а зимой постоянно снабжает континенты теплом. Страны, расположенные вблизи океана, обладают мягким морским климатом. Напротив, безводные пустыни, находящиеся в глубине континентов, характеризуются резкими перепадами температуры, наблюдающимися даже в течение одних суток.
Еще одно аномальное свойство воды, имеющее значение для жизни всей планеты, связано с тем, что она обладает не только аномально высокой теплотой испарения, предохраняющей наш организм от перегрева, но и аномально высокой скрытой теплотой плавления. У стали эта величина почти вдвое ниже, у свинца — ниже почти в 15 раз. Это свойство воды спасает нас от катастрофических весенних наводнений. Из-за медленного таяния льда и снега почва вбирает в себя достаточное количество влаги и тем самым предотвращает в некоторых случаях гибель растений во время засухи.
Подобное же сочетание полезных свойств, имеющих значение как для внутренних процессов организма, так и для жизни всей планеты, мы можем обнаружить и в других аномальных свойствах воды. Возьмем, к примеру, вязкость. Эта величина у воды имеет идеальное значение для обеспечения жизненных процессов в организме. Будь вязкость воды несколько ниже, вода бы неслась по тончайшим сосудам нашего тела с такой скоростью и силой, что разрушала бы эти сосуды. А если бы вязкость была несколько большей — течение воды в этих сосудах затормозилось, и все жизненные процессы в тканях нашего организма прекратились. Однако вязкость воды оказалась идеальной как для нашей жизни, так и для жизни любых других организмов.
Значение вязкости воды идеально не только для внутренних процессов нашего тела, связанных с движением крови в кровеносных сосудах, но и для процессов, протекающих во внешней среде. И здесь мы опять сталкиваемся с чем-то аномальным: в отличие от вязкости других жидкостей, она снижается при повышении давления. Повышение температуры также понижает вязкость воды. Этот факт дает объяснение тому, почему подземные воды даже на больших глубинах при высоких давлениях и температурах довольно подвижны — они могут перемещаться, в том числе по направлению к поверхности земли, и могут быть, в конце концов, использованы растениями или человеком.
Возможность подобных перемещений обусловлена также необычными свойствами воды — сочетанием в ней высокого значения поверхностного натяжения и смачивания. Эта способность создает в почве и верхних слоях подпочвенного грунта так называемую подвешенную воду, которая, удерживаясь поверхностным натяжением, не стекает в более глубокие горизонты, обеспечивая растения влагой. Благодаря этому же явлению вода внутри деревьев поднимается с уровня почвы на высоту их кроны. Можно сказать, что одни и те же уникальные свойства воды в очередной раз оказываются необходимыми как для внутренней жизни организмов, так и для создания благоприятных условий их обитания.
Подобное же сочетание внешнего и внутреннего эффектов относится и к уникальной способности воды растворять в себе различные вещества, что определяется особенностью ее внутренней структуры. Без этого свойства процессы жизнедеятельности не могли бы протекать в живых организмах. Однако это же свойство воды необходимо не только здесь, но и для жизни водоемов, где растворенные вещества играют исключительную роль.
Еще в 1945 году бельгийский инженер запатентовал способ предохранения паровых котлов от пагубного воздействия накипи. Суть его изобретения заключалась в том, что воду, предназначенную для питания котлов, предварительно подвергали магнитной обработке, в результате чего накипь резко уменьшалась. Последующие исследования показали, что после обработки природной воды в магнитном поле изменяются многие ее физико-химические свойства. И аналогичные изменения в свойствах воды происходят не только при воздействии на нее магнитного поля, но и под влиянием ряда других физических факторов — звуковых сигналов, электрических полей, температурных изменений, радиации, турбулентности и т.д. Каков же может быть механизм подобных воздействий?





Аномальные свойства воды

Автор работы награжден дипломом победителя III степени
Текст работы размещён без изображений и формул.
Полная версия работы доступна во вкладке "Файлы работы" в формате PDF
Люди привыкли к воде, и считают ее обычным веществом. Многие не осознают, что структура воды и ее аномальные свойства обеспечивают существование жизни на Земле.
Обоснование выбора темы: с водой мы сталкиваемся ежедневно, и она занимает важнейшее место в нашей жизни. С одной стороны - нет ничего более простого и доступного на планете, как вода, с другой – более загадочного и уникального.
Цель исследования: выяснить причины уникальности воды; при проведении физико-химических опытов, доказать, что вода необычное вещество.
~ изучить и проанализировать литературу и информацию в Интернете по данной теме;
~ провести наблюдения за основными состояниями воды, её физическими свойствами;
~ определить и выделить удивительные свойства воды;
~ провести эксперименты и опыты, доказывающие уникальность воды;
~ понаблюдать, как человек использует необычные свойства воды;
Объект исследования: вода.
Предмет исследования: свойства воды, присущие только ей и неочевидные в природе.
Гипотеза: мы предположили, что аномальные свойства воды можно доказать в домашних условиях.
Методы исследования:
~ анализ литературы и других источников;
Актуальность заключается в практической значимости уникальности воды на современном этапе развития науки и техники. Проект реализуется в рамках химии и физики и может быть квалифицирован как экспериментально-информационный.
Глава № 1. ВОДА В ПРИРОДЕ
Вода входит в состав всех живых и растительных организмов. Вода присутствует не только в организме всех живых существ нашей планеты, но и во всех веществах на Земле – в минералах и горных породах.
Вода находится в постоянном и активном круговороте. Его движущей силой является Солнце, а основным источником воды - Мировой океан. Увлажняющая почву вода всасывается корнями растений. Вместе с водой растения получают растворенные питательные вещества. В растениях она поднимается по стеблям и возвращается в виде пара, в атмосферу через листья.
Вода в естественных природных условиях может существовать в трех агрегатных состояниях: твёрдое – лёд; жидкое – вода; газообразное - водяной пар. Один из ранних греческих философов, Фалес Милетский (640-546 гг. до нашей эры), исследовал универсальный характер воды. Он считал ее основным элементом, из которого рождается все. Обилие воды было очевидным, но Фалес заметил, что она является единственным веществом, естественным образом, присутствующим на Земле одновременно в трех разных состояниях: твердом, жидком и газообразном. В холодный зимний день снег и лед покрывают поля, рядом течет река, а над головой плывут облака.
Глава № 2. УДИВИТЕЛЬНЫЕ СВОЙСТВА ВОДЫ
§ 1. Химическая формула воды. Физические свойства воды
Вода - это простейшее химическое соединение двух атомов водорода и одного атома кислорода: H2O. Из химических свойств воды особенно важна способность воды растворять вещества разной химической природы. Она удивительно легко растворяет большое количество самых разнообразных веществ и газов и, что тоже весьма важно, так же легко их отдает.
Физические свойства воды – это свойства, которые проявляются вне химических реакций. Основными физическими свойствами воды являются – запах, цвет, прозрачность, вкус, плотность, температура, жесткость, вязкость, структура.
§ 2. АНОМАЛЬНЫЕ СВОЙСТВА ВОДЫ
Многие физические и химические свойства воды удивляют и выпадают из общих правил и закономерностей и являются аномальными. Отдельные свойства воды не соответствуют многим принципам физики и химии. Рассмотрим некоторые уникальные свойства воды.
Горячая вода застывает быстрее холодной
При замерзании вода увеличивается в объеме
В большинстве случаев при замерзании молекулы веществ располагаются ближе друг к другу, структура их становится компактнее и плотнее. Но с водой эта схема не работает. Плотность воды, при переходе ее из твердого состояния в жидкое, не уменьшается, как почти у всех других веществ, а возрастает. При замораживании объем воды увеличивается на 1%, но при этом становится не такой плотной, поэтому лед всегда легче воды, и находится на ее поверхности. Если бы озера замерзали снизу вверх, то водная жизнь вообще перестала бы существовать, а климатические и погодные условия резко изменились.
Вода – уникальный растворитель
К аномальным свойствам воды относят и ее самое высокое (после ртути) поверхностное натяжение по сравнению с любой другой жидкостью. Молекулы воды активно притягиваются друг к другу, в результате ее поверхность, стремится к минимуму. Именно поэтому естественной формой любой жидкости является шар. Объекты, более тяжелые, чем вода, могут удерживаться на ее поверхности. Насекомые способны ходить по ней, а лезвие бритвы или игла – плавать.
§ 3. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Те аномальные свойства воды, которые мы описали выше, попробуем проверить в домашних условиях.
Опыт № 1. Проведем эксперимент и понаблюдаем за горячей и холодной водой в морозильной камере.
Условия: В ячейки для льда я налила теплую воду 35 ° С и поставила в морозильную камеру, засекла время превращения воды в лёд. Тоже самое проделала с холодной водой – 0,5 ° С.
Результат: тёплая вода превратилась в лед через 20 минут; холодная вода превратилась в лед через 25 минут. Для опыта необходима вода определенной температуры.
Вывод: горячая вода замерзает быстрее, чем холодная при определенных условиях.
Опыт № 2. В ходе работы над проектом я обратила внимание, что вода может перемещаться самостоятельно.
Вывод: вода может подниматься вверх без посторонней помощи (приложение № 2) Это удивительное свойство помогает растениям получать влагу из почвы и перемещать от корней по стеблям к листьям.
Опыт № 3. Я задумалась, а какая вода быстрее будет подниматься вверх?
Условия: Я взяла 2 стакана: № 1 - с теплой водой и № 2 - с холодной водой; две полоски картона, один конец которых окрашен в разные цвета маркерами; опустила концы полосок картона в стаканы.
Результат: Краски маркера на полоске в тёплой воде поднялись вверх быстрее и выше, чем в холодной.
Вывод: теплая вода поднимается вверх быстрее холодной (приложение № 3). Теперь мне понятно, почему растения нужно поливать теплой водой, она доставит необходимые питательные вещества из почвы и живительную влагу быстрее.
Опыт № 4. Горку можно соорудить практически из чего угодно — и песка, соли, сахара. А можно ли сделать неподвижную горку из воды?
Условия: Я взяла хорошо вымытый сухой стакан, наполнила его водой до отказа, после чего аккуратно опускала в него по одной монете.
Результат: По мере опускания монет в стакан, вода из него не выливалась, а начала понемногу приподниматься, образуя горку. Это хорошо заметно, если посмотреть на стакан сбоку. По мере увеличения в стакане количества монет, горка становилась всё выше - поверхность воды надулась, словно воздушный шарик. Однако, в какой-то момент этот шарик лопнул, и вода струйками потекла по стенкам стакана. В этом опыте горка на поверхности воды образуется за счёт поверхностного натяжения.
Вывод: Взаимодействуя с твёрдой поверхностью, вода плохо к ней прилипает и плохо растекается. Именно поэтому она не стекает сразу же через край стакана при образовании горки (приложение № 4).
Опыт № 5. А можно ли управлять плавающими на поверхности предметами, при этом ничем их не касаясь.
Условия: В миску, наполненную водой, аккуратно положила 10-12 спичек. Расположила их в форме лучей звезды, по возможности равномерно. Взяла жидкое мыло и капнула в воду в центре спичечной звезды.
Результат: Спички тут же начали плыть от него к краям блюдца.
В другой миске вместо мыла опустила в центр спичечной звезды кончик кусочка сахара-рафинада.
Результат: Спички, наоборот, поплыли в обратном направлении и собрались возле погружённого в воду сахара.
Вывод: Такое поведение спичек обусловлено следующим: погружая в воду разные вещества (мыло и сахар), мы тем самым изменяем силу поверхностного натяжения. Когда капаешь мыло на поверхность жидкости, оно растворяется и смешивается с ней. Молекулы мыла проходят между молекулами воды и снижают их взаимное притяжение. Сахар действует противоположно мылу - он увеличивает поверхностное натяжение. (приложение № 5).
Опыт № 6. Следующий опыт показал, что поверхность воды может растягиваться. Как вы думаете, сколько капелек воды поместится на обычной монетке?
Условия: Я положила монетку на блюдце, а блюдце - на очень ровную поверхность. В пипетку набрала воды, капнула воду в центр монетки с очень близкого расстояния.
Результат: Опытным путем мной установлено, что на 2-х рублевой монетке помещается 20 капель воды, а на 5-ти рублевой - 28 капель. Вода на монете располагается не ровным тонким слоем, как это может показаться перед экспериментом, а образует горку. Поверхность воды растягивается и становится все более выпуклой с каждой новой каплей до тех пор, пока тонкая пленка, которую образует поверхность воды, не порвется. И тогда почти вся вода с монетки вытечет в блюдце
Вывод: Поверхность воды растягивается за счет поверхностного натяжения (приложение № 6).
Опыт № 7. В предыдущем опыте мы убедились, что поверхность воды похожа на тонкую пленку, которая может растягиваться. Теперь мы сможем рассмотреть эту пленку, и увидеть, что она может не только удерживать воду внутри, но и не дает утонуть относительно тяжелым предметам и прогибаться под их весом.
Условия: Я налила воду в стакан, взяла иголку и, держа ее горизонтально, поднесла максимально близко к поверхности воды и опустила.
Результат: Иголка плавает и можно будет рассмотреть, как поверхность воды прогибается под ее весом.
Вывод: Поверхностное натяжение воды позволяет удерживать на поверхности достаточно тяжелые предметы (приложение № 7).
Опыт № 8. В холодное время года наши квартиры теплые благодаря паровому отоплению. А почему в батареях именно вода?
Условия: Я поставила металлический ковш на плиту. Через 10 секунд его нельзя взять в руки - он раскален, так как металл нагрелся. В этот же ковш нальем стакан воды и поставим на плиту. Доводим до кипения, на это нужно уже больше времени. Переливаем горячую воду из ковша в стакан с ложкой.
Результат: Через десять минут металлический ковш остыл, а стакан стал очень горячим. Вода нагрела ложку и стенки стакана.
Вывод: У воды есть свойство долго удерживать тепло. Поэтому в батареях именно вода, ну и, конечно, вода самое доступное текучее вещество (приложение № 9).
Опыт № 9. Вода имеет свойство менять плотность при переходе в твердое состояние. Так ли это на самом деле?
Условия: Я взяла стеклянную бутылку, налила воду и поместила её в морозильную камеру холодильника.
Результат: вода замерзла и расширилась, её объём увеличился и бутылка растрескалась.
Вывод: Вода при низких температурах превращается в лед и при этом расширяется (приложение № 10).
Опыт № 10. Логично было бы предположить, что замерзая, вода, как и любое другое вещество становится тяжелее.
Условия: Кусочек льда я опустила в стакан с водой.
Результат: Лед плавает на поверхности и не тонет.
Вывод: Замерзая, вода увеличивается в объеме, но структура становится более рыхлой. Поэтому лед, легче самой воды, он плавает на поверхности и не тонет.
Опыт № 11. Приведем еще один интересный опыт, который продемонстрирует теплопроводность воды.
Условия: В воздушный шарик я налила холодную воду и немного надула. Поднесла шарик к горящей свече.
Результат: Воздушный шар не лопнул, так как в нем вода. Надуваем другой воздушный шарик и подносим к огню, он лопнул.
Вывод: Теплопроводность воды в 24 раза выше, чем у воздуха. Пока вода не испарится в шарике, он не лопнет (приложение № 12).
Опыт № 12. Жидкости, имеющие разную плотность – не смешиваются.
Условия: В стакан я поочерёдно налила жидкости разной плотности и цвета (растительное масло и воду).
Результат: они не смешиваются.
Вывод: Водородная связь определяет аномальное свойство воды смачивать большинство поверхностей. Такие вещества считаются гидрофильными. Другие вещества, такие как масла, жиры, воск и синтетика не намокают. Они являются гидрофобными. Разная плотность не дает смешиваться молекулам воды и масла (приложение № 13) .
Объект моего исследования – вода - кажется будничным и естественным, только на первый взгляд. Исследование позволило мне сделать вывод, что многие свойства воды, присущи только ей, они обязательно встречаются в природе, но они совсем не так очевидно представляются глазам наблюдателя, как в наших опытах. На основе опытов, мы доказали уникальность воды, как химического вещества, а физические свойства воды действительно обусловлены особенностями ее строения. Гипотеза, что аномальные свойства воды можно доказать в домашних условиях – подтвердилась.
В данной работе были рассмотрены такие уникальные свойства воды, как высокая теплоёмкость, плотность, теплопроводность, конвекция или перемешивание, поверхностное натяжение.
~ опытным путём рассмотрены различные свойства воды, являющиеся уникальными, как физико-химического вещества;
~ экспериментально установлено, что физические свойства воды действительно обусловлены особенностями ее строения. На основе это, было доказана уникальность воды, как химического вещества.
В ходе работы над проектом я научилась самостоятельности, у меня появился интерес к предметам физика и химия, которые мне еще только предстоит изучать, развились исследовательские умения и навыки, например, умение пользоваться дополнительной литературой, думать, рассуждать, делать выводы.
Список использованной литературы
1. Вода для жизни. Сбережем воду – сохраним жизнь. / авт.-сост. А. Н. Пахоменко и др. – Могилев: Могилев. обл. укруп. тип,
2. Врублевский А. И. Основы химии. Школьный курс. – 2-е изд. – Мн.: Юнипресс, 2010г. – 960 с.
3. Глинка Н. Л. Общая химия: учеб. пособие для вузов. – 23-е изд., испр. /Под ред. В. А. Рабиновича. – Л.: Химия, 1983г. – 704 с.
4. Энциклопедический словарь юного физика - М.: Педагогика, 1981
Справа – стакан с водой +35 °C, слева – стакан с водой - 0, 5 °C
Горячая вода начала превращаться в лед через 20 минут, холодная через 25 минут
средний стакан пустой, в двух крайних стаканах – вода
вода по бумажным мостикам перешла в средний стакан
картонную полоску с отметкой черного цвета опускаем в стакан с холодной водой, с отметкой коричневого цвета – в стакан с теплой водой

Вода является основой жизни на нашей планете. Эту субстанцию можно изучать до бесконечности. Нет, на Земле вещества более важного для нас, чем обыкновенная вода, и в то же время не существует другого такого вещества, в свойствах которого было бы столько аномалий.
Молекулярная формула воды указывает на то, что это вещество имеет простую структуру, однако до сих пор оно считается малоисследованным, поскольку существует еще много неизученных свойств данной субстанции, которые, возможно, и способствуют поддержанию жизни на Земле.
С водой мы сталкиваемся ежедневно, и она занимает важнейшее место
в жизни всего живого. С одной стороны нет ничего более простого и
доступного на планете, как вода, с другой – более загадочного и
уникального. Поэтому эта тема мне интересна, и я выбрал её для
исследования.
Цель проекта: доказать, что вода необычное вещество. Выяснить причины уникальных свойств воды при проведении физико-химических опытов.
I .1 Теоретическая часть
I .1.1 Вода в природе и жизни человека
Вода – весьма распространенное на Земле вещество. Почти ¾ поверхности земного шара покрыты водой, образующей океаны, моря, реки и озера. Много воды находится в газообразном состоянии в виде паров в атмосфере; в виде огромных масс снега и льда лежит она круглый год на вершинах высоких гор и в полярных странах. В недрах земли также находится вода, пропитывающая почву и горные породы
Вода находится в постоянном и активном круговороте. Его движущей силой является Солнце, а основным источником воды – Мировой океан. Почти четверть всей падающей на Землю солнечной энергии расходуется на испарение воды с поверхности водоемов. Если бы этого не происходило, средняя температура на нашей планете была бы значительно выше.
Примерно 2/3 атмосферной воды возвращается в виде осадков обратно в океан, а 1/3 выпадает на сушу. Эта вода пополняет ледники, реки и озера. В свою очередь поверхностные воды снова стекают в моря и океаны, растворяя встречающиеся им на пути породы.
Увлажняющая почву вода всасывается корнями растений. Вместе с водой растения получают растворенные питательные вещества. В растениях она поднимается по стеблям и возвращается в виде пара в атмосферу через листья.
Важным регулятором речного стока на суше являются горные ледники. Они отдают воду в основном в летние месяцы, а накапливают зимой.
С круговоротом воды происходит перемещение тепла, так, например, известно влияние близости побережья океана на климат.
Вода – универсальный растворитель. Двигаясь в круговороте, она растворяет в себе огромное количество веществ, которые лежали в почве или летали в воздухе. Это могут быть и питательные вещества, и ядовитые химикаты, и др.
Вода входит в состав всех живых и растительных организмов. Например, человек на 70% состоит из воды, рыба – на 80%. Вода – основа жизни, если человек теряет в виде воды 12% массы тела, то наступает смерть; человек не может жить без потребления воды более 3-4 суток. Большое дерево извлекает летом из почвы и испаряет в течение суток 500-700 дм 3 воды. Во всяком организме вода представляет собой среду, в которой протекают химические процессы, обеспечивающие жизнедеятельность организма, кроме того, она участвует в ряде биохимических реакций
Вода способна регулировать температуру нашего тела, выводить из
организма продукты жизнедеятельности и различные токсические
компоненты. С помощью воды наши мышцы выполняют свою основную
функцию – сократительную. Диета спортсменов всегда содержит повышенное количество жидкости. Ученые доказали, что для сохранения здоровья человек должен потреблять до 2,5 литров жидкости в сутки – это обеспечит ему хорошее самочувствие, активизирует умственную деятельность и придаст сил. Из воды состоят все ткани человеческого организма: мышцы, кости, легкие, сердце, почки, печень, кожа и жировая ткань. Больше всего жидкости, а именно 99%, содержит стекловидное глазное тело, а меньше всего, примерно 0,2%, зубная эмаль. Богат на содержание воды и головной мозг, поскольку без этой субстанции мы не сможем мыслить и формировать информацию. Любые биохимические реакции, происходящие в организме, могут оптимально протекать только при достаточном поступлении воды, в противном же случае в тканях и клетках будут скапливаться конечные продукты обмена веществ, которые приведут к развитию многих серьезных заболеваний. Чтобы этого избежать, необходимо соблюдать правильное потребление воды.
I .1.2 Строение воды
Физические и химические свойства воды определяются химическим, электронным и пространственным строением молекулы Н2О.
Химическая формула воды достаточно проста – это соединение атома кислорода с двумя атомами водорода. Но при этом в мире нет субстанции более загадочной. Вода, или оксид водорода, является химическим веществом. В нормальных условиях H 2 O (вода) сохраняется в
жидком агрегатном состоянии, в то время как аналогичные соединения
водорода являются газами. Все это можно объяснить особыми
характеристиками атомов, слагающих молекулы, и присутствием между ними связей.
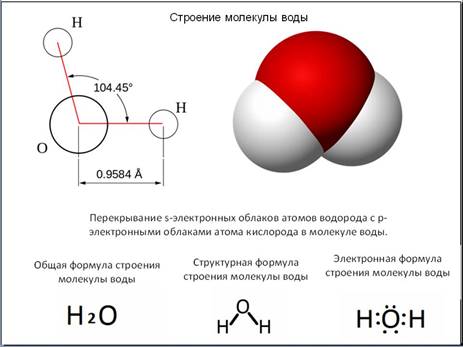
Молекула воды имеет угловое строение . Связи Н-О очень полярны. На атоме кислорода имеется избыточный отрицательный заряд, на атоме водорода – избыточные положительные заряды. В целом молекула воды является полярной, то есть диполем.
Этим объясняется тот факт, что вода является хорошим растворителем для ионных и полярных веществ.
Наличие избыточных зарядов на атомах Н и О, а также не поделенных электронных пар у атомов О ( кислорода) обуславливает образование между молекулами воды водородных связей, в следствии чего они объединяются в ассоциаты. Существование этих ассоциатов объясняют аномально высокие значения температуры плавления и температуры кипения воды.
Водородная связь между молекулами воды
Капля воды состоит из молекул, которые притягиваются
противоположными полюсами, образуя тем самым полярные связи, разорвать которые без усилий невозможно. Каждая молекула в своем составе содержит ион водорода, который настолько мал, что может проникать сквозь оболочку отрицательного атома кислорода, находящегося в соседней молекуле. В результате этого образуется водородная связь. Схема воды показывает, что каждая молекула имеет прочную связь с четырьмя соседними молекулами, две из которых образуются атомами кислорода, а другие две – атомами водорода.
I .1.3 Аномальные свойства воды или удивительное рядом
Академическая наука до сих пор не смогла дать рациональное объяснение
всем аномальным свойствам воды.
Вода – единственное вещество на Земле, которое существует в природе в трёх состояниях: жидком, твёрдом и газообразном (вода, лед и водяной пар). При обычных условиях вода – жидкость без вкуса и запаха; в тонком слое она бесцветна, однако при толщине более 2 метров она приобретает голубоватый оттенок.
Плотность воды. Плотность воды при переходе ее из твердого состояния в жидкое не уменьшается, как почти у всех других веществ, а возрастает. При нагревании воды от 0 до 4 0 С плотность ее также увеличивается. При 4 0 С вода имеет максимальную плотность, и лишь при дальнейшем нагревании ее плотность уменьшается.
Вода - единственное вещество, обладающее в жидком состоянии большей плотностью, чем в твёрдом, так как, структура льда более рыхлая, чем структура жидкой воды. Это - одно из аномальных свойств воды.
Теплоемкость. Удельной теплоёмкостью воды называют количество теплоты в джоулях, которое необходимо, чтобы поднять температуру 1 кг воды на 1° C . Вода обладает большой теплоёмкостью (4,184 Дж/г). Это значит, что существенное увеличение тепловой энергии вызывает лишь сравнительно небольшое повышение её температуры. Объясняется такое явление тем, что значительная часть этой энергии расходуется на разрыв водородных связей, ограничивающих подвижность молекул воды.
Большая теплоёмкость воды сводит к минимуму происходящие в ней температурные изменения. Благодаря этому биохимические процессы протекают в меньшем интервале температур, с более постоянной скоростью и опасность нарушения этих процессов от резких отклонений температуры грозит им не столь сильно. Вода служит для многих клеток и организмов средой обитания, для которой характерно довольно значительное постоянство условий.
Благодаря высокой теплоемкости в ночное время, а также при переходе от лета к зиме вода остывает медленно, а днем или при переходе от зимы к лету также медленно нагревается, являясь, таким образом, регулятором температуры на земном шаре.
Поглощая огромное количество теплоты, сама вода существенно не нагревается. Удельная теплоемкость воды в пять раз выше, чем у песка, и почти в десять раз выше, чем у железа.
Характерно, что явление прохождения удельной теплоемкости воды через минимум при температурном изменении обладает своеобразной симметрией: при отрицательных температурах также обнаружен минимум этой характеристики. Он приходится на – 20°С
Замерзание и кипение
Температуры замерзания и кипения воды не соответствуют общим закономерностям и законам химии. Так мы знаем, что вода в реальной жизни замерзает при 0° C , а кипит при 100° C , в то время как в соответствии с общими правилами химии эти процессы должны проходить при -90° C (минус девяносто) и -70° C (минус 70) соответственно.
Температурная яма
Как мы видим, температура человеческого тела 36,6 ° C близка к этому значению.
Эффект Мпембы – эффект горячей воды
Удивительно, но факт – горячая вода замерзает быстрее холодной, что противоречит логике и общему восприятию вещей.
Температура воды + 3,98 ° C
Как мы уже отметили выше, температура + 3,98 ° C , является для воды важным значением. При понижении температуры до этого уровня вода ведет себя в соответствии с общими законами и правилами этих наук. При дальнейшем понижении температуры у воды начинают проявляются ее аномальные свойства.
При температуре + 3,98 ° C у воды плотность имеет наибольшее значение, а объем наименьший.
Объем и плотность
Еще одним важным для всех нас является ее аномальное свойство при замерзании увеличиваться в объеме, тем самым уменьшая свою плотность. Уточним, что до + 3,98 ° C вода ведет в соответствии с общими законами химии и физики, а далее проявляются ее аномальные свойства.
Поверхностное натяжение
Еще одним удивительным и во многом аномальным свойством воды является ее поверхностное натяжение.
Хорошо всем известный пример демонстрирует, как аккуратно положенная на воду металлическая швейная игла плавает на ее поверхности, что во многом удивительно. Ведь плотность метала гораздо больше плотности воды.
Вся жизнь на Земле своим существованием во многом обязано именно этому свойству воды.
Вода — отличный растворитель
Вода является отличным растворителем, она удивительно легко растворяет большое количество самых разнообразных веществ и газов. И что тоже весьма важно, так же легко их отдает. Например, благодаря именно этому свойству после дождя мы чувствуем удивительную свежесть – дождь очищает воздух.
Вода и магнитное поле
Под воздействием магнитного поля у воды меняется ее способность к растворению веществ, изменяется скорость, проходящих в ней, химических реакций.
Аномальные свойства воды еще раз подтверждают общеизвестное высказывание — удивительное рядом.
II .Экспериментальная часть
Необычные свойства воды, обнаруживаемые в физико-химических экспериментах, и ее роль в биологических системах объясняют повышенный интерес к изучению структуры воды. Результаты исследований структуры воды, существенно дополняющие и развивающие принятые представления о структурном состоянии воды, позволяют подойти к расшифровке нового ранее неизведанного класса энергоинформационных явлений.
На этом этапе, на примере нескольких фокусов, которые являются ничем иным как нехитрыми, но очень занимательными опытами, продемонстрируем необычные свойства воды.
Мы знаем, что яйцо, как и другой тяжелый предмет, в банке с водой утонет. А если воду посолить?! Данное свойство мы продемонстрируем с помощью
Оборудование: три стакана с водой; три сырых яйца; соль.
Оборудование: воздушные шарики, свеча, спички, стакан холодной воды.
Проведение опыта. В воздушный шарик наливаем холодную воду и немного надуем. После этого необходимо зажечь свечу. Подносим шарик к свече (он не лопнул, так как в нем вода). Надуваем другой воздушный шарик и подносим к огню, он лопнул.
Оборудование: стакан, кусочек марли или ткани, вода, резинка для закрепления ткани.
Проведение опыта. В стакан наливаем холодную воду. Накрываем стакан марлей и закрепляем её резинкой. Быстро переворачиваем стакан с водой. Вода из стакана не выливается, т.к. атмосферное давление давит на перевернутый стакан, а между тканью и водой образовалась тонкая пленка, т.к. в нем ни осталось воздуха. Поэтому вода из перевернутого стакана не вытекает. Но стоит немного наклонить стакан, вода начинает вытекать.
Объяснение: этот опыт возможен из-за поверхностного натяжения воды. На предметы, находящиеся на поверхности, действуют силы со стороны жидкости (приложение).
На основе исследований и проведенных опытов можно сделать следующие выводы:
1. На нашей Земле нет вещества более важного для нас, чем обыкновенная вода, и в то же время не существует другого такого же вещества, в свойствах которого было бы столько противоречий и аномалий.
2. В данной работе были рассмотрены такие уникальные свойства воды, как плотность, атмосферное давление, теплопроводность, поведение воды при растворении в ней веществ.
3. Физические свойства воды действительно обусловлены особенностями ее строения. На основе отработанных опытов, мы доказали уникальность воды, как химического вещества.
4. Все эти свойства воды обязательно встречаются в природе, но они совсем не так очевидно представляются глазам наблюдателя, как в наших опытах.
Список источников
1. Энциклопедический словарь юного химика - М.: Педагогика, 1981
2. Егоров А.С., Аминова Т.Х. Химия: экспресс- репетитор для подготовки к ЕГЭ.- Ростов- на Дону: Феникс,2013.-279, [1] с.
3. Фрублевский А. И. Основы химии. Школьный курс. – 2-е изд. – Мн.: Юнипресс, 2010г. – 960 с.
4. Глинка Н. Л. Общая химия: учеб. пособие для вузов. – 23-е изд., испр. /Под ред. В. А. Рабиновича. – Л.: Химия, 1983г. – 704 с.
Интернет источники:
Читайте также:

