Трипаносома жизненный цикл кратко
Обновлено: 04.07.2024
К трансмиссивным заболеваниям с природной очаговостью относят трипаносомоз. Это тяжелое заболевание, называемое также сонной болезнью, встречается в странах Африки и Южной Америки. Болезнь у человека вызывают жгутиковые простейшие, называемые трипаносомами (Trypanosoma gambiense), паразитирующие в крови, лимфе, спинномозговой жидкости.
Жизненный цикл трипаносом проходит в двух хозяевах:
первом - позвоночное животное или человек,
втором - беспозвоночное животное (насекомое).
Заражение человека африканской сонной болезнью происходит при укусе и сосании крови кровососущей мухой це - це, в слюнных железах которой обитает инвазионная стадия трипаносомы.
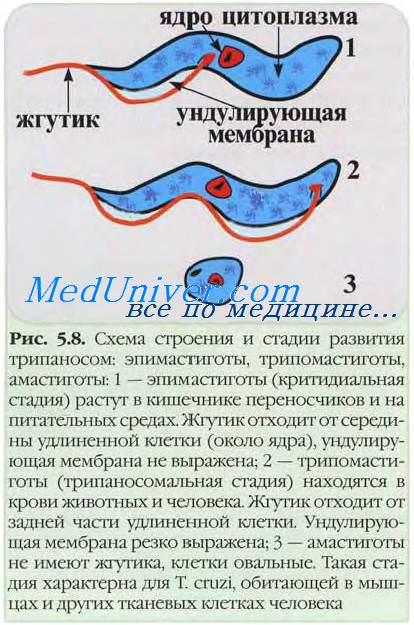
В организме человека паразит образует трипаносомную форму. Размеры от 13 до 39 мкм. Тело трипаносомы вытянутое, суженное в концах. Ядро находится в центре. На заднем теле расположен блефаропласт. От него отходит жгутик, тянущийся к переднему концу тела. Выйдя за пределы тела жгутик образует свободную часть. Между жгутиком и телом имеется ундулирующая мембрана. Передвижение трипаносом происходит за счет движения жгутика и ундулирующей мембраны. Питание осуществляется осмотически. Размножение бесполое, путем продольного деления.
Инкубационный период длится 2 - 3 недели, а болезнь протекает в течение 4 -7 недель. На ранних стадиях болезни трипаносомы размножаются в крови и лимфе, проникают в лимфатические узлы, которые увеличиваются.
На более поздних стадиях трипаносомы попадают в спинномозговую жидкость, спинной и головной мозг. Возникают тяжелые нарушения центральной нервной системы, развивается мышечная слабость, сонливость, депрессия и болезнь очень часто заканчивается смертью.
В организм мухи цеце трипаносомы попадают с кровью больного человека при сосании. Трипаносомы проникают в желудок насекомых. Там они размножаются, меняют форму, проходят часть цикла развития. Затем они оказываются в слюнных железах мухи цеце, где превращаются в инвазионную форму. Весь цикл развития в организме мухи цеце занимает около 20 дней. После этого муха це - це способна заражать человека и резервуарных хозяев (антилоп, коз, свиней, овец).
Для диагностики исследуют кровь, спинномозговую жидкость, пунктаты лимфатических узлов.
Профилактика связана с выявлением и лечением больных сонной болезнью, уничтожением переносчиков.
В Южной и Центральной Америке другой вид трипаносом (Trypanosoma cruzi) вызывает болезнь Чагаса. Размер трипаносом 20 мкм. Промежуточными хозяевами и переносчиками являются триатомовые клопы, называемые также "поцелуйными".
Резервуарными хозяевами служат броненосцы, муравьеды, белки, крысы, собаки, кошки.
Триатомовые клопы активны ночью. Они кусают человека в область губ и глаз. Во время сосания крови клопы оставляют фекалии и находящиеся на них трипаносомы попадают в ранку. Трипаносомы проникают с кровью в клетки различных органов. Там они превращаются в безжгутиковую лейшманиальную форму и интенсивно делятся. Затем они превращаются в критидиальную и трипаносомальную форму. Проникая в кровь, трипаносомы попадают в новые клетки. Часто поражается сердечная мышца, нервная система, поперечно - полосатые мышцы, эндокринная система.
Инкубационный период длится от 3 до 7 дней. Часто болеют дети. В некоторых случаях смерть наступает через 2 - 4 недели.
Иногда болезнь может протекать хронически, в зависимости от поражения систем органов. Такое течение болезни длится до 12 лет.
Диагноз на ранних стадиях ставят по нахождению трипаносом в крови. На более поздних - исследуют спинномозговую жидкость. Применяют эффективный метод ксенодиагностику - кормление незараженных клопов на больных. В кишечнике клопа трипаносомы размножаются, и на 10 - 20 - й день их можно обнаружить.
46.Токсоплазма.
К классу споровиков относят также токсоплазму (Toxoplasma gondii) -возбудитель токсоплазмоза. Токсоплазмоз - облигатный внутриклеточный паразит .
Окончательными хозяевами могут быть домашние кошки и другие представители семейства кошачьих. В их организме проходит кишечная фаза развития. Промежуточными хозяевами могут быть человек, многие виды млекопитающих, в том числе кошки и птицы. В организме промежуточных хозяев проходит внекишечная фаза развития. Полный цикл может осуществляться только в организме кошачьих .
Заражение человека (или других промежуточных хозяев) токсоплазмозом происходит при попадании в организм с пищей ооцист со спорозоитами, оказавшихся во внешней среде с фекалиями кошки, либо тканями других промежуточных хозяев (птиц, млекопитающих), содержащих цисты с цистозоитами или эндозоитами.
В процессе переваривания в тонком кишечнике под действием ферментов из ооцист выходят спорозоиты, а из цист - цистозоиты или эндозоиты, которые проникают в клетки слизистой оболочки кишечника и начинают размножаться бесполым способом (путем внутреннего почкования - эндодиогенией или эндополигенией). В результате образуются эндозоиты, способные вызвать некроз тканей кишечника. С током крови эндозоиты могут попадать в различные органы и ткани человека. Размножение осуществляется только в живых клетках. В цитоплазме этих клеток имеются большие скопления эндозоитов, напоминающие цисты. Оболочка вокруг эндоэоитов образована клеткой хозяина и такие цисты называют псевдоцистами. Это характерно для острого течения болезни.
Когда размножение эндозоитов перестает быть интенсивным, болезнь переходит в хроническую стадию. Вокруг эндозоитов образуется плотная оболочка цисты и сами эндозоиты превращаются в цистозоиты. Цисты обеспечивают выживание паразита, их оболочки непроницаемы для антител.
Токсоплазма похожа на дольки апельсина длиной 4 - 7 мкм, шириной 2 - 4 мкм. Передний конец тела сужен, задний расширен и закруглен. На переднем конце находится конусообразное образование - коноид - служащее для фиксации паразита на поверхности клетки (рис. 337).
Окончательные хозяева - кошки - заражаются, поедая промежуточных, инвазированных цистами токсоплазмы. Возможно заражение ооцистами. В кишечнике кошки оболочки цист растворяются, эндозоиты, цистозоиты попадают в клетки слизистой кишечника, где размножаются путем эндодиогении и шизогении. Из ооцист выходят спорозоиты, которые также проникают в клетки слизистой кишечника и размножаются шизогонией, в результате чего образуются мерозоиты. После нескольких шизогоний мерозоиты дают начало гаметоцитам (незрелым половым клеткам). Микрогаметоциты в результате деления ядра превращаются в микрогаметы, имеющие два жгутика, помогающие им двигаться в просвете кишечника. Образование макрогамет осуществляется без деления ядра.
Оплодотворение (слияние микро - и макрогамет) происходит в клетках эпителия кишечника. Образуется зигота, которая покрывается плотной оболочкой и превращается в ооцисту. Ооцисты выпадают в просвет кишечника и выделяются во внешнюю среду. Внутри ооцисты в результате спорогонии образуют спорозоиты.
Ооцисты со спорозоитами - инвазионная стадия, способная заражать промежуточных и окончательных хозяев. Ооцисты токсоплазмы устойчивы к внешним воздействиям и в почве сохраняются годами.
Человек может заражаться токсоплазмозом от животных, через загрязненную пищу, через шкурки. Мать способна передать возбудителя плоду через плаценту. При внутриутробном заражении может произойти гибель плода или родится ребенок с различными нарушениями ЦНС, сердечно - сосудистой системы и пороками развития. Симптомы токсоплазмоза разнообразны. Поражаются нервная, лимфатическая, половая, сердечно - сосудистая системы. Может быть бессимптомное носительство. Иногда болезнь может закончиться смертью.
Диагноз токсоплазмоза ставят, применяя иммунологические методы, исследуя сыворотку крови, делая биопсию лимфатических узлов.
Профилактика связана с выявлением и лечением носителей токсоплазмоза, соблюдением правил личной гигиены.
Малярийные плазмодии.
Паразиты человека относятся к отряду кровяных споровиков.. У человека вызывают заболевание 4 вида малярийных плазмодиев: возбудитель трехдневной малярии (Plasmodium vivax), возбудитель четырехдневной малярии (Plasmodium malariae), возбудитель тропической малярии (Plasmodium falciparum) и возбудитель малярии типа трехдневной (Plasmodium ouale).
Заболевание малярией выражается в повторяющихся с определенной частотой приступах лихорадки, сопровождающихся подъемом температуры,
Малярия распространена в странах с жарким и влажным климатом, расположенных в тропическом и субтропическом поясе, и там, где обитает малярийный комар. Это антропоноз, так как резервуаром может быть только человек. Малярия - облигатно-трансмиссивное заболевание, передается с помощью кровососущих насекомых, природно-эндемичная инфекция.
Заражение человека происходит при укусе самками малярийного комара, содержащими малярийный плазмодий на стадии спорозоита. Спорозоиты имеют размеры 5 - 8 мкм. Током крови они разносятся по телу и внедряются в клетки печени, где превращаются в шизонтов, размножающихся бесполым путем (шизогонией). В результате этого образуются мерозоиты, которые внедряются в эритроциты, где снова растут и делятся. Цикл развития мерозоитов в эритроцитах повторяется несколько раз.
Правильное чередование приступов при малярии связано с периодичностью шизогонии в эритроцитах. Начало приступа (озноб) совпадает с распадом эритроцитов и поступлением в плазму крови мерозоитов и продуктов их жизнедеятельности, вызывающих интоксикацию организм
После нескольких циклов бесполого размножения (шизогонии) начинается подготовка к половому процессу. При этом мерозоиты, находящиеся в эритроцитах, дают начало гамонтам (подготовительные стадии образования гамет).
Макрогамонты дадут впоследствии женские половые клетки - макрогаметы, микрогамонты - мужские микрогаметы. В крови человека образования половых клеток не происходит, так как человек - промежуточный хозяин в цикле развития малярийного плазмодия. Дальнейшее развитие плазмодия осуществляется, если гамонты с кровью попадают в желудок малярийного комара при сосании им крови больного человека. Малярийные комары - окончательные хозяева в цикле развития малярийного плазмодия. В желудке комара гамонты превращаются в крупные неподвижные макрогаметы и в мелкие подвижные микрогаметы. Происходит копуляция гамет, в результате чего образуется подвижная зигота (оокинета), которая внедряется в стенку желудка комара и инцистируются на стороне, обращенной в полость тела, превращаясь в ооцисту. Ядро зиготы многократно делится. Ооциста распадается на большое количество (до 10000) спорозоитов. Оболочка спороцисты разрушается и спорозоиты попадают в полость тела комара, а затем в слюнные железы насекомого. Малярийный комар снова может заражать человека. Ни на одной стадии паразит не находится во внешней среде.
Инкубационный период длится от 2 недель до 6 месяцев. Диагноз ставят при нахождении малярийных плазмодий в крови. Кровь берут непосредственно после приступа малярии.
Профилактика связана с уничтожением мест обитания малярийного комара.
Печеночный сосальщик.
Печеночный сосальщик (Fasciola hepatica) - гермафродит .
Мужская половая система состоит из пары семенников, семяпроводов, сливающихся в семяизвергательный канал, и заканчивается копулятивным органом. К женской половой системе относят: яичник, желточники, семяприемник, тельце Мелиса, которые открываются в оотип - камеру, где происходит оплодотворение и формирование оплодотворенных яиц. Из оотипа яйца поступают в матку и выводятся наружу через отверстие. Сосальщики очень плодовиты. В течение недели одна особь продуцирует до 1 миллиона яиц. Для дальнейшего развития яйца обязательно должны попасть в воду. В воде из яиц выходят личинки, покрытые ресничками, называемые мирацидиями. Эти личинки вбуравливаются в тело моллюска (малого прудовика). Так они теряют реснички и превращаются в следующие личиночные стадии - спороцисты. Спороцисты делятся партеногенетически и дают начало редиям, которые также в результате партеногенетического деления образуют личинки - церкарий, имеющие хвост. Они способны покинуть тело моллюска. Попав в воду эти личинки свободно плавают, и затем прикрепляются к растениям, теряют хвост, покрываются плотной оболочкой и превращаются в адолескарии (рис. 344).
Таким образом, в цикле развития печеночного сосальщика есть пять личиночных стадий. Для дальнейшего развития адолескарии должны быть съедены окончательным хозяином (коровой или человеком), в кишечнике которого оболочка цисты растворяется, личинка внедряется в печень, растет и превращается во взрослую особь.
Человек заражается печеночным сосальщиком при употреблении некипяченой прудовой воды или с грязными овощами. Диагноз ставят при нахождении яиц в фекалиях. Для предупреждения заболевания надо не пить сырую воду из зараженных водоемов, тщательно мыть овощи перед едой кипяченой водой.
Ланцетовидный сосальщик.
Иногда у человека в печени может паразитировать ланцетовидный сосальщик (Dicrocoelium lanceatum) и вызывать заболевание дикроцелиоз.
Ланцетовидный сосальщик имеет размеры 5 - 15 мм в длину и 1,5 - 2,5 мм в ширину. По строению похож на кошачьего сосальщика, но отличается тем, что семенники находятся в передней части тела сосальщика, а матка занимает заднюю часть тела гельминта .
В цикле развития происходит смена двух промежуточных хозяев: первый -наземный моллюск, второй - муравей. Окончательными хозяевами могут быть травоядные животные (овцы, крупный рогатый скот) и редко человек.
Во внешнюю среду выделяются яйца гельминтов, внутри которых развивается личинка - мирацидий. Яйца с мирацидиями попадают в первого промежуточного хозяина - наземного моллюска (рис. 350). В печени моллюска мирацидий превращаются в спороцисты первого порядка, затем второго порядка и в церкарии. В легких моллюска церкарии образуют сборные цисты, которые выделяются наружу. Эти сборные цисты могут быть проглочены вторым промежуточным хозяином -муравьем.
В муравьях из сборных цист выходят церкарии. Они превращаются в метацеркарии, являющиеся инвазионной стадией для окончательного хозяина.
Кошачий сосальщик.
Кошачий сосальщик (Opisthorchis felineiis) паразитирует в желчных протоках печени, желчном пузыре, поджелудочной железе у человека и многих млекопитающих (кошки, собаки, свиньи и др.) и вызывает заболевание - описторхоз.
Распространено это заболевание в бассейнах Оби, Иртыша, Камы, Днепра. Описторхоз - природно-очаговое заболевание. В природе очаги поддерживают животные, питающиеся рыбой.
Заражение описторхозом окончательных хозяев, в том числе и человека, происходит при употреблении в пищу сырой, малосоленой, вяленой рыбы из семейства карповых .
В мышцах рыб находятся инвазионные стадии паразита - метацеркарии. После попадания в кишечник окончательного хозяина метацеркарии проникают в печень, желчный пузырь, где превращаются во взрослых гельминтов.
Взрослый кошачий сосальщик имеет 8 - 12 мм в длину и 1,2 - 2 мм в ширину. Передний конец уже заднего. Есть ротовая и брюшная присоски. Имеются пищеварительная, выделительная, половая и нервная системы. Кишечник не разветвлен, слепо замкнут. Матка расположена в передней части тела, в задней - видны два семенника.
В цикле развития кошачьего сосальщика два промежуточных хозяина: первый - пресноводный моллюск; второй - рыбы из семейства карповых.
Яйца с фекалиями попадают в воду и заглатываются моллюсками. Из яиц выходят мирацидии, далее образуются спороцисты, редии и церкарий, которые выходят из моллюска и способны самостоятельно плавать. Церкарии проникают во второго промежуточного хозяина - рыбу - и превращаются в метацеркарии.
Диагноз описторхоза ставят при нахождении яиц в фекалиях. Профилактика связана с охраной водоемов от загрязнения сточными водами. Кроме того, необходимо обрабатывать термически рыбу перед употреблением.
Легочный сосальщик.
На Дальнем Востоке распространено
заболевание парагонимоз, вызываемое
легочной двуусткой (Paragonimus westermani), паразитирующей чаще всего в легких
человека. Иногда паразиты могут проникать
в печень, мышцы, мозг и вызывать тяжелое заболевание.
В цикле развития два промежуточных
хозяина: первый - моллюск, второй -
пресноводные раки и рыбы.
Заражение человека происходит при
употреблении в пищу сырых раков и крабов.
Кроме человека окончательными хозяевами
могут быть кошки, тигры, собаки, свиньи.
Диагноз парагонимоза ставят по нахождению яиц в фекалиях и мокроте больного.
Профилактика связана с термической обработкой ракообразных перед употреблением в пищу.
Кровяные сосальщики.
Род кровяные сосальщики(Schistosoma)
В кровеносной системе человека могут паразитировать сосальщики, вызывающие заболевания, именуемые шистосоматозами.
Эти заболевания распространены в странах Африки, Азии, Южной Америки. Болезнь протекает тяжело и без лечения заканчивается смертью.
В отличие от остальных сосальщиков, кровяные сосальщики раздельнополые. Самец крупнее самки, имеет желоб (гинекофорный канал), в котором находится самка.
Есть три вида кровяных сосальщиков, паразитирующих у человека (Schistosoma haematobium, Schistosoma mansoni, Schistosoma japonica) Промежуточными хозяевами для кровяных сосальщиков являются моллюски.
У человека половозрелые гельминты одного вида (Schistosoma haematobium) могут паразитировать в венах мочеполовой системы. Представители двух других видов способны обитать в венах кишечника, брыжейки, желудкам
Половозрелые особи выделяют яйца, имеющие острый шип. С помощью шипа яйца, продвигаясь по сосудам, прокалывают их стенки, выходят в ткани, затем оказываются в полости мочевого пузыря или в полости кишечника и выделяются наружу .
Для дальнейшего развития яйца попадают в воду и проникают в промежуточного хозяина - моллюска. В моллюске развиваются два поколения спороцист и церкарии. Церкарии имеют раздвоенный хвост и могут плавать в воде.
Заражение человека происходит через кожу при купании, при работе в водоемах, содержащих церкарии. После внедрения в организм человека личинки теряют хвост, растут и с током крови попадают в места окончательной локализации.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Трипаносомы являются одним из семейств протистов - одноклеточных организмов типа Euglenozoa (эвгленозои).
Трипаносомы относятся к патогенным микроорганизмам и представляют опасность для здоровья, вызывая тяжелые поражения систем и органов человека.
Строение трипаносомы
Строение трипаносомы, то есть ее морфологическая структура, имеет форму трипомастиготы в течение взрослой, трипаносомной стадии развития. Тело трипаносомы длиной от 12 до 40-70 мкм имеет продольную форму сильно вытянутого овала с заостренными концами (напоминающую веретено).
Оно состоит из одной клетки - митохондрии с цитоплазмой и единственным ядром; клетка имеет плотную гликопротеиновую оболочку (перипласт). Также в клетке трипаносомы имеется дисковидный органоид кинетонуклеус (или кинетопласт), содержащий ДНК, и меньшее по размеру тельце (кинетосома или блефаропласт), от которого начинается наружный вырост клетки трипаносомы флагеллоподий. Этот органоид движения паразита попросту именуется жгутиком. Он тянется вдоль тела клетки и приподнимает образованную перипластом пластинчатую перепонку, которая тоже расположена вдоль всей клетки (с одной стороны). Специалисты называют ее ундулирующей мембраной (от лат. undulatus - волнообразный), и ее функция – извиваясь, продвигать трипаносому в нужном направлении. Такое строение трипаносомы присуще паразиту, когда он находится в организме окончательного хозяина.
Кроме того, находясь там, трипаносома может быть и в форме амастиготы (овальной формы, меньшего размера и без жгутика). А вот на критидиальной стадии, пребывая в организме насекомого-переносчика, морфологическая структура клетки приобретает вид эпимастиготы: клетка удлиненная, но жгутик короткий и волнообразная мембрана сильно недоразвита.
Кстати, трипаносома крузи имеет C- или S-образную форму тела, а также более длинный жгутик и зауженную волнообразную мембрану.
Жизненный цикл и размножение трипаносомы
Трипаносомы – паразиты облигатные, то есть их существование за пределами чужого организма невозможно: хозяин обеспечивает питание и комфортную среду обитания паразита. Поэтому весь жизненный цикл трипаносомы проходит либо в теле насекомого, либо в теле человека (или животного). Так что жизненный цикл этого паразита двухэтапный.
Главным (окончательным) хозяином для трипаносом, по мнению большинства биологов, является человек, а насекомое-кровосос, переносящее паразита, получило статус промежуточного хозяина.
Африканская трипаносома развивается в передних отделах кишечника мухи цеце после того, как она насосалась крови зараженного позвоночного животного. В результате в ее организм попали трипомастиготы Trypanosoma brucei или Trypanosoma gambiense, которые начинают размножаться и переходят в форму эпимастигот. Добравшись до слюнных желез насекомого, эпимастиготы продолжают усиленно делиться. Жизненный цикл трипаносомы в теле мухи занимает примерно три недели. Непосредственно в слюну паразит проникает только когда разовьется до стадии метациклических трипомастигот, которые и попадают в хоботок. Теперь кровожадному насекомому остается только укусить жертву своего ненасытного аппетита, и готово – зрелые трипаносомы перекочевывают к новому хозяину.
Размножение трипаносомы бесполое, осуществляется путем продольного бинарного митоза, в ходе которого митохондрия и ядро разделяются на две части – реплицируя две копии каждой хроматиды.
Многократный процесс деления американской трипаносомы (с образованием эпимастиготы) протекает в кишечнике клопов. Когда клетка паразита становится трипомастиготой, то есть приобретает метациклическую форму, она готова к смене хозяина. Выход наружу из кишечника один – с экскрементами, которые животные слизывают с себя при укусе насекомого и заражаются. А люди чешут укушенное место, и заразные фекалии клопа попадают в клетки кожи через отверстие от укуса и микроскопические повреждения целостности кожного покрова при расчесывании.
Где обитает и чем питается трипаносома?
Итак, где обитает трипаносома? Средой своего обитания паразиты трипаносома бруцеи и трипаносома гамбиенсе избрали кровь, лимфу, лимфоузлы, цереброспинальный ликвор (спинномозговую жидкость), богатые белками серозные жидкости, а также ткани спинного и головного мозга. Американская трипаносома в человеческом организме чаще всего поселяется в клетках лимфатических узлов и сосудов, печени и селезенки, костного и головного мозга, а также мышечных тканей (в том числе миокарда).
Чем питаются трипаносомы? Тем, что им необходимо для поддержания своего существования и размножения – гликопротеинами и углеводами плазмы крови своего хозяина. Отверстия для попадания пищи внутрь (цитостома) у трипаносоматид нет, поэтому они утоляют голод с помощью эндосмоса – всасывания жидких питательных веществ всей оболочкой клетки. Следует отметить, что трипаносомы относятся к анаэробам, то есть для получения энергии они не нуждаются в кислороде и система дыхания у них цитохромная.
Виды трипаносом
Согласно паразитологической систематизации, класс трипаносом - гетеротрофные эукариотические патогенные эндопаразиты.
Трипаносома на латинском (заимствование из греческого): класс Mastigophora (жгутиконосцы, от греч. mastig - жгутик), подкласс животных жгутиконосцев (Zoomastigina), отряд Kinetoplastida (кинетопластиды). А по классификации протист, класс трипаносом - кинетопластида, семейство - трипаносоматиды, вид - трипаноплазма. Несколько разновидностей этого эндопаразита вызывают у человека очень опасные патологии.
Африканская трипаносома – причина развития у человека и животных африканского трипаносомоза (сонной болезни). Заболевание возникает после попадания в организм таких паразитов, как трипаносома бруцеи (Trypanosoma brucei) и трипаносома гамбиенсе или трипаносома гамбийская (Trypanosoma gambiense). В первом случае медики определяют возбудителя как Trypanosoma brucei gambiense (T.b.g.), который поражает население в странах Западной и Центральной Африки и вызывает длящуюся месяцами и годами хроническую инфекцию. Во втором случае тип возбудителя имеет уточненное название Trypanosoma brucei rhodesiense (T.b.r.), и он приводит к острой форме сонной болезни (с тяжелыми поражениями ЦНС) в основном среди сельского населения восточной и южной части африканского континента.
Способ заражения трипаносомами данных видов инокулятивный - через укус специфического насекомого-кровососа. Обитающая в несметных количествах тропическая муха цеце является переносчиком трипаносом бруцеи и гамбиенсе. К основным видам мухи цеце (Glossina), которые могут заражать людей африканским трипаносомозом, относятся G. palpalis, G. Tachinoides и G. morsitans.
Трипаносома конская (Trypanosoma eouipedum) вызывает так называемую случную болезнь лошадей, так как передача трипаносом данного вида происходит во время их спаривания. Нередко трипаносома бруцеи фигурирует как трипаносома конская, поскольку в центральных районах Африки ею заражаются лошади, причем развивающаяся смертельная болезнь нагана (нгана) поражает и многих других домашних животных.
Эпидемиология трипаносомозов. Жизненный цикл трипаносомозов. Клиника трипаносомозов.
Трипаносомозы регистрируют в странах Западного и Восточного побережья Африки. Резервуар возбудителя гамбийского трипаносомоза — больной человек; переносчики — мухи цеце (С. palpalis и G. tachinoides), обитающие около водоемов.
Основной природный резервуар возбудителя родезийского трипаносомоза — мелкие антилопы. Переносчики трипаносомозов — мухи цеце (G. tогsitans, G. pallipides и G swynnertoni), обитающие в саваннах Восточной Африки.
Жизненный цикл трипаносомозов
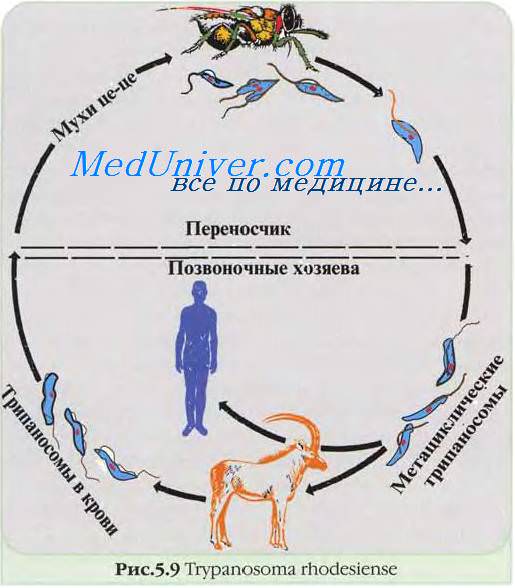
T. brucei подвид gambiense и Т. brucei подвид rhodesiense попадают в организм человека при укусе мухи цеце, а затем проникают в лимфатическую систему и далее в кровоток. Возбудители размножаются внеклеточно в кровяном русле и в тканях в виде трнпомастигот.
При сосании крови больного трипомастиготы проникают в организм мух цеце, превращаются в эпимастиготы и размножаются в кишечнике и слюнных железах. Через несколько недель в организме переносчика происходит скопление дочерних популяций трнпомастигот, в результате чего возбудители становятся способны заражать чувствительные организмы.
Клинические проявления трипаносомозов
Инкубационный период трипаносомозов продолжается 2-3 нед. Для заболеваний характерны паразитемия и диссеминированные поражения. Через 2-3 дня на месте укуса мухи цеце иногда образуется изъязвляющаяся папула (трипаносомидный шанкр). Паразиты бурно размножаются в месте проникновения и диссеминируют в кровоток. Возможно увеличение регионарных лимфатических узлов, где происходит скопление трипаносом. Циркуляция возбудителя в кровотоке достигает своего пика через 2-3 нед.
Пациенты испытывают приступы неправильно интермиттирующей лихорадки со стойкой тахикардией, болезненной лимфаденопатией, кожной сыпью и головной болью. Возможны психические расстройства. Проявления трипаносомозов носят цикличный характер: после удаления паразитов под действием иммунных механизмов, вызвавших приступ, наступает ремиссия. Рецидивы заболеваний вызваны выходом дочерних популяций, с абсолютно новым набором поверхностных Аг.
Установлено, что генетический аппарат трипаносом кодирует появление 22 вариантоспецифических поверхностных Аг у каждого штамма. Поражения, вызванные гамбийской трипаносомой, развиваются медленно, и вовлечение ЦНС наблюдают по истечении нескольких лет после начала заболевания. Родезийская трипаносома вызывает прогрессирующую болезнь с поражениями мозга и миокарда, развивающимися уже через 3-6 нед после начала заболевания.
Характерны кома, судороги, острая сердечная недостаточность и сильное истощение, приводящие к смерти больного в течение 6~9 мес. В динамике трипаносомозов развиваются сонливость, тремор конечностей, транзиторные параличи, речь становится невнятной и т.д.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Трипаносомоз – паразитарное протозойное заболевание, передающееся посредством вектора, переносчика и возбудителем которого являются простейшие рода Trypanosoma.
Трипаносомоз – важная причина развития тяжелых поражений жизненно важных органов, повышения смертности среди жителей в эндемичных районах. В основном случаи заболевания регистрируются среди бедных слоев населения.
Трипаносомозы распространены в Южной Америке (болезнь Шагаса, американский трипаносомоз) и странах Африки (авриканский трипаносомоз, или сонная болезнь).
Итак, трипаносомоз условно подразделяется на две основные группы:

Рисунок 1 – Трипаносома TRYPANOSOMA BRUCEI в периферической крови пациента (источник The scientist)
1. Сонная болезнь
1.1. Возбудитель
Причина африканского трипаносомоза (другое название "сонная болезнь") – простейшее Trypanosoma brucei. Переносчиком для трипаносом служит муха Цеце. Муха Цеце является биологическим и основным вектором (переносчиком) трипаносомоза.
Возможна механическая передача трипаносомоза посредством других кровососущих насекомых. Укусы мух приходятся на дневные часы. К переносу заболевания способны как мужские, так и женские особи мухи Цеце.
Муха Цеце относится к роду Glossinia, который насчитывает 3 подгруппы:
- 1 Glossinia (включает группу G. morsitans).
- 2 Nemorhina (включает группу G. palpalis).
- 3 Austenia (включает группу G. fusca).
Переносчики Trypanosoma brucei gambiense (T. b. gambiense) – G. palpalis и G. tachinoides. Для T. b. gambiense основной резервуар инфекции – люди, хотя регистрируют случаи инфекции у диких и домашних животных.
Переносчики Trypanosoma brucei rhodesiense (T. b. rhodesiense) – G. morsitans, G. swynnertoni, G. pallidipes. Резервуар для T. b. rhodesiense - крупный рогатый скот, иногда отмечают в качестве источника инфекции домашних животных (собаки, свиньи, овцы), диких животных (дикие кабаны, антилопы, львы, зебры, гиены).
Мухи Цеце способны служить переносчиком африканского трипаносомоза благодаря 2 основным факторам: способности инфицироваться при укусе позвоночных животных и поддерживать развитие и передачу инфекции другим позвоночным.
Африканский трипаносомоз – заболевание, распространенное в основном среди жителей деревень Африки (сельские жители наиболее подвержены укусам вектора инфекции). Переносчик африканского трипаносомоза – муха Цеце, tsetse fly.
Существует 2 формы сонной болезни: гамбийская (T. b. gambiense), регистрируется в Западной, Центральной Африке и вызывает 95% случаев заболевания; родезийская форма (T. b. rhodesiense), эндемична для Восточной и Южной Африки и вызывает 5% случаев сонной болезни.
Трипаносомоз сопровождается тяжелым поражением мозга с нарушением цикла сон-бодрствование, что и дало начало неофициальному названию болезни – сонная болезнь. При отсутствии лечения пациенты постепенно впадают в ступор и кому.
В настоящее время существуют эффективные схемы лечения, элиминирующие паразитов из кровеносной, лимфатической и нервной систем. Для подбора верной схемы терапии требуется проведение люмбарной пункции.
Несмотря на значительный прогресс в лечении трипаносомоза, современные лекарственные препараты не удовлетворяют всем потребностям врачей. Для назначения курса лечения необходима госпитализация пациента, нередко на прием препаратов развиваются побочные эффекты со стороны организма пациента.
В начале 60х годов 20 века, с началом использования эффективного лечения, ученым казалось, что африканский трипаносомоз взят под контроль и заболеваемость будет ежегодно снижаться. Так оно и было до начала 21 века. Контроль и профилактика были заброшены на несколько десятилетий.
Успех в лечении африканского трипаносомоза позволил ВОЗ включить данное заболевание в список болезней, подлежащих полной эрадикации (к 2020 году ВОЗ планирует свести заболеваемость африканским трипаносомозом к цифре 1:10 000 в 90% эндемичных районов Африки).
1.2. Факторы риска
Муха Цеце встречается лишь в Тропической Африке (sub-Saharan Africa). Существует большое количество факторов риска, делающих одну популяцию гораздо более восприимчивой к трипаносомозу по отношению к другой. Население, живущее в сельской местности, находится под наибольшим риском заражения.
К другим факторам риска относятся:
- 1 Социальные потрясения, гражданские войны.
- 2 Миграция крупного рогатого скота.
- 3 Миграция населения.
- 4 Снижение финансирования местных программ здравоохранения.
1.3. Эпидемиология
По оценкам ученых, в 1986 году приблизительно 70 миллионов людей жили в районах эндемичных по африканскому трипаносомозу. Случаи заражения регистрировались в 36 странах Тропической Африки. По данным ВОЗ смертность от африканского трипаносомоза составляла 40 тыс. случаев в год.
1.4. Жизненный цикл Trypanosoma brucei

Рисунок 2 – Жизненный цикл трипаносом Trypanosoma brucei (источник CDC)
Патогенез сонной болезни включает три основных звена:
- 1 Укус мухи приводит к местному формированию шанкра.
- 2 С кровью и лимфой происходит распространение паразита по организму, его проникновение в центральную нервную систему.
- 3 Благодаря антигенной вариации (существует большое количество вариантов поверхностного гликопротеина VSG), резистентности к трипанолитическим факторам происходит уклонение паразита от иммунной системы хозяина.
1.5. Симптомы инфекции
Отмечается различие в течении болезни не только между подвидами возбудителя африканского трипаносомоза, но и среди разных пациентов (различие реакции на трипаносомоз местных жителей и туристов, мигрантов в эндемичную зону).
Туристы, мигранты предрасположены к острому течению болезни. Среди данной группы выше риск смерти при отсутствии лечения. Инкубационный период составляет 1-4 недели.
В своем развитии заболевание проходит 3 клинические стадии:
- 1 Трипаносомозный шанкр. Шанкр развивается в месте укуса мухи и представляет собой болезненный плотный узел, окруженный отеком и гиперемией. Как правило, в течение 7-14 дней происходит самопроизвольное рассасывание шанкра.
- 2 Стадия гематогенной и лимфогенной диссеминации. Внедрение паразита в кровеносное русло происходит через 14-21 день от момента укуса. Начало данной стадии сопровождается повышением температуры, ознобами, лимфаденопатией (увеличением лимфатических узлов), головными болями, профузным потом. Нерегулярные эпизоды обострения данных симптомов в течение 7 дней. Наиболее частый симптом – шейная лимфаденопатия (увеличение лимфоузлов шеи). Вместе с лихорадкой, особенно у путешественников, появляется макулярная сыпь на туловище. В ОАК регистрируют анемию, лейкопению, моноцитоз.
- 3 Стадия менингоэнцефалита. Данная стадия сопровождается неспецифическими симптомами головной боли, сонливости (пациент спит днем, бессонница ночью). Со временем усиливается сонливость, повышается время сна. Прогрессия данных симптомов при T. b. rhodesiense занимает 3-6 недель, при T. b. gambiense – до двух лет. Нередко на данной стадии у пациента развивается пневмония. При отсутствии лечения происходит развитие комы и смерть пациента.
1.6. Диагностика африканского трипаносомоза
Характерная клиника (длительная лихорадка, воспаление лимфоузлов, неврологические симптомы) может вызвать у врача подозрение на трипаносомоз. Однако одной клиники недостаточно для назначения лечения. Классический алгоритм диагностики основывается на сочетании клиники и лабораторно-инструментальных исследований.
Клинические и серологические исследования не могут быть достоверными на 100%, поэтому предпочтительно подтверждать диагноз трипаносомоза определением возбудителя в биологических жидкостях пациента.
Процесс обследования пациента с трипаносомозом является пошаговой процедурой, каждый шаг в которой определяет ту или иную схему лечения. При определении паразита в биологических жидкостях необходимо провести оценку поражения ЦНС (берется на анализ спинномозговая жидкость). Поражение нервной системы определяет окончательную тактику лечения, вероятность рецидивов болезни.
1.6.1. Определение антител
Трипаносомы индуцируют продукцию в IgG и IgM в высоких концентрациях, что можно использовать для разработки анализов на определение паразита.
- 1 CATT (card agglutination test). Быстрый и простой анализ, хорошо подходит для скрининга, основан на определении специфических антител у больного африканским трипаносомозом.
- 2 Метод непрямой реакции иммунофлуоресценции.
- 3 Иммуно-ферментный анализ.
- 4 Метод иммунного лизиса трипаносом. Для исследования используют лабораторную культуру трипаносом. При добавлении плазмы пациента к трипаносомам происходит их лизис (антитела пациента крепятся к эпитопам на поверхности паразитов и активируют систему комплемента, приводя к лизису трипаносом).
1.6.2. Выявление трипаносом в средах организма
- 1 Исследование аспирата из пораженного лимфатического узла.
- 2 Исследование толстой капли крови. Является методом выбора при исследовании крови. Данный метод является простым и недорогим, позволяет диагностировать наличие других паразитов (микрофилярий, малярийного плазмодия).
- 3 Исследование мазков крови после предварительной окраски по Гимзе.
- 4 Метод центрифугирования крови, спинномозговой жидкости с последующим микроскопическим исследованием полученной взвеси.
- 5 Молекулярно-генетический анализ, основанный на определении нуклеиновых кислот паразита в биологических жидкостях (ПЦР, лигазная цепная реакция).
1.7. Медикаментозное лечение
| Заболевание и стадия | Первая линия терапии | Дозировка | Альтернативная схема лечения |
|---|---|---|---|
| Гамбийская форма африканского трипаносомоза | |||
| Первая стадия | Пентамидин изетионат | 4 мг/кг/день внутримышечно или внутривенно (разведенный в изотоническом растворе натрия хлорида, вводится в течение 2 часов) – 7 дней | -- |
| Вторая стадия | Нифуртимокс + эфлорнитин | Эфлорнитин: 400 мг/кг в день внутривенно (каждая доза препарата разводится в 250 мл физиологического раствора, вводится в течение 2 часов) – 7 дней. Нифуртимокс: 15 мг/кг в день перорально 3 р/д – 10 дней. | Эфлорнитин: 400 мг/кг в день внутривенно в 4х 2хчасовых инфузиях (каждая доза препарата разводится в 100 мл физиологического раствора) – 14 дней. Вторая линия терапии (напр. при рецидиве болезни): Меларсопрол 2.2 мг/кг в день внутривенно – 10 дней |
| Родезийская форма африканского трипаносомоза | |||
| Первая стадия | Сурамин | Начальная доза 4-5 мг/кг внутривенно (1ый день), в последующем введение препарата внутривенно в дозе 20 мг/кг в течение недели (максимальная доза 1г). | Пентамидин изетионат 4 мг/кг в день внутримышечно или внутривенно (препарат развести в физиологическом растворе, вводить в течение 2 часов) – 7 дней. |
| Вторая стадия | Меларсопрол | 2.2 мг/кг в день внутривенно – 10 дней. | -- |
1.8. Профилактические мероприятия
- 1 В настоящее время нет эффективной вакцины от африканского трипаносомоза.
- 2 Контроль за переносчиками инфекции (мухи Цеце): использование москитных сеток, инсектицидов, репеллентов.
- 3 Ношение одежды нейтрального цвета: яркая одежда может привлекать переносчиков болезни.
2. Американский трипаносомоз
Американский трипаносомоз – протозойное заболевание, вызванное Trypanosoma cruzi (T. cruzi). Переносчик американского трипаносомоза – кровососущий триатомовый клоп (reduviid bug).
Помимо трансмиссивного для болезни Шагаса существует вертикальный путь передачи инфекции. Клинические симптомы острой формы заболевания неспецифичны, при хроническом течении на первый план выходят симптомы кардиомиопатии и тяжелых желудочно-кишечных осложнений.

Рисунок 3 – Триатомовый клоп
Американский трипаносомоз является зоонозом, люди – случайные хозяева паразита. Инфицирование человека чаще всего происходит при посещении леса и контакте с вектором. Американский трипаносомоз характеризуется как болезнь бедности. Инфицирование человека происходит при дефекации клопа в первоначальное место укуса.
2.1. Эпидемиология и пути передачи
Важную роль в контроле за распространением инфекции сыграли скрининговые исследования крови людей, проживающих в эндемических районах, интенсивное лечение беременных пациенток.
Наиболее частый путь передачи – контакт с калом/мочой инфицированного кровососущего триатомового клопа. Как правило, триатомовые клопы обитают в стенах, на крышах плохо сконструированных, дешевых домов в сельской местности. Клопы прячутся в дневное время и активизируются ночью.
Чаще всего клопы кусают открытые участки тела человека - кожа лица, руки, ноги. При укусе жук откладывает зараженные фекалии в рану. Трипаносомы инфицируют макрофаг, на месте укуса клопа развивается местная реакция (инфильтрат). Далее макрофаг мигрирует в регионарный лимфоузел, где происходит дальнейшее размножение трипаносом.
Другие пути передачи T. cruzi
- 1 Употребление зараженной еды (фекалии/моча инфицированного триатомового клопа в еде).
- 2 Переливание крови от инфицированного донора.
- 3 Вертикальная передача от больной матери ребенку во время беременности/родов.
- 4 Пересадка органов от инфицированного донора.
- 5 Аварии в лаборатории.
2.2. Симптомы заболевания
Трипаносомы попадают в макрофаги посредством фагоцитоза. В последующем происходит выход паразита из фагосомы и его размножение в цитоплазме.
2.2.1. Острое течение болезни Шагаса
- 1 На месте укуса формируется инфильтрат, уплотнение темно-красного цвета, местная реакция тканей на антигены паразита (шагома).
- 2 Из места укуса происходит занос трипаносом в регионарные лимфатические узлы.
- 3 В последующем происходит попадание трипаносом в кровеносное русло.
- 4 Наиболее частый симптом – односторонний безболезненный отек тканей вокруг глаза (симптом Romana).
- 5 Конъюнктивит, лимфаденопатия околоушных лимфоузлов.
- 6 Общая слабость, головные боли.
- 7 Лихорадка в течение 4-5 недель.
- 8 Тяжелые системные проявления болезни: гепатоспленомегалия (увеличение печени и селезенки), менингоэнфефалит.
- 9 При тяжелом течении болезни ранним проявлением является кардит (воспаление тканей сердца).
Рисунок 4 – Симптом Romana при болезни Шагаса (источник Medical Pictures Info)
2.2.2. Хроническое течение болезни Шагаса
2.3. Методы диагностики
- 1 Мазок периферической крови, исследование толстой капли, окраска мазка по Гимзе. Для проведения данных исследований необходимо производить забор крови пациента в острую фазу болезни. При исследовании нефиксированного мазка крови можно выявить подвижные трипаносомы. При хроническом трипаносомозе данные методы обладают меньшей эффективностью.
- 2 При хроническом течении болезни на первый план выходят серологические методы диагностики. Для постановки диагноза требуется сочетание клиники с двумя положительными результатами разных серологических исследований (напр. ИФА и РИФ).
- 3 Определение антигенов паразита – Вестерн-блот анализ, используется для подтверждения положительных серологических тестов, не подходит для скрининга.
- 4 Ксенодиагностика. Пациенту подсаживают вектор, не несущий возбудителя болезни. При укусе происходит забор клопом трипаносом. Исследование срезов клопа.
- 5 Заражение мышей плазмой пациента с последующей аутопсией.
- 6 Молекулярно-генетический анализ. Наиболее применим при остром течении болезни.
2.4. Лечебная тактика
Цели при лечении американского трипаносомоза – элиминация паразита из организма хозяина и облегчение симптомов при необратимом повреждении органов. Для этиотропного лечения болезни доступно 2 препарата – бензимидазол и нифуртимокс. Эффект данных препаратов ограничен при терапии хронической формы болезни Шагаса.
Острая форма лечится с применением бензимидазола, либо нифуртимокса. Чем меньше времени прошло от момента инфицирования и чем моложе пациент, тем выше вероятность излечения. По данным литературы полное излечение пациентов на первом году жизни наблюдалось в 90% случаев, в целом излечение при остром течении регистрируется в 70% случаев.
При хроническом течении болезни и развитии симптомов со стороны сердца, желудочно-кишечного тракта антипаразитарное лечение не назначается. Хирургическое лечение применяется для коррекции осложнений со стороны сердца, пищевода, толстой кишки.
Читайте также:

