Теория резонанса в органической химии кратко
Обновлено: 04.07.2024
Основным является сессионный cookie, обычно называемый MoodleSession. Вы должны разрешить использование этого файла cookie в своем браузере, чтобы обеспечить непрерывность и оставаться в системе при просмотре сайта. Когда вы выходите из системы или закрываете браузер, этот файл cookie уничтожается (в вашем браузере и на сервере).
Другой файл cookie предназначен исключительно для удобства, его обычно называют MOODLEID или аналогичным. Он просто запоминает ваше имя пользователя в браузере. Это означает, что когда вы возвращаетесь на этот сайт, поле имени пользователя на странице входа в систему уже заполнено для вас. Отказ от этого файла cookie безопасен - вам нужно будет просто вводить свое имя пользователя при каждом входе в систему.
РЕЗОНАНСА ТЕОРИЯ, теория электронного строения хим. соединений, в основе к-рой лежит представление о том, что электронное распределение, геометрия и все др. физ. и хим. св-ва молекул должны быть описаны не одной возможной структурной ф-лой, а сочетанием (резонансом) всех альтернативных структур. Идея такого способа описания электронного строения принадлежит Л. Полингу (1928). Резонанса теория является развитием классич. теории хим. строения для молекул, ионов, радикалов, строение к-рых можно представить в виде неск. разл. структурных ф-л, отличающихся способом распределения электронных пар между атомными ядрами. Согласно резонанса теории, строение таких соед. является промежуточным между отдельными возможными классич. структурами, причем вклад каждой отдельной структуры можно учесть при помощи разл. модификаций квантовомех. метода валентных связей (см. Валентных связей метод).
Для соед. с сопряженными связями из всех возможных структур с разл. типами спаривания электронов кратных связей достаточно рассмотреть лишь структуры с неперекрещивающимися связями (канонич. структуры). Электронное строение бензола описывается резонансом пяти канонич. структур:
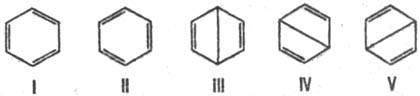
Волновая ф-ция молекулы бензола по Полингу представляет линейную комбинацию:
Y = 0,624( Y I + Y II ) + 0,271( Y III + Y IV + Y V ).
Откуда следует, что осн. вклад (примерно 80%) в волновую ф-цию вносят кекулевские структуры I и II. Их эквивалентность и эквивалентность структур III-V объясняют вырав-ненность всех углерод-углеродных связей в молекуле бензола и их промежут. (примерно полуторный) характер между простой и двойной связями углерод-углерод. Это предска зание находится в полном соответствии с экспериментально найденными длиной связи С—С в бензоле (0,1397 нм) и св-вами симметрии его молекулы (группа симметрии D 6h ).
Р езонанса теорию с успехом применяют для описания строения и св-в ионов и радикалов. Так, строение карбонат-иона представляют как резонанс (обозначается двусторонней стрелкой) трех структур, каждая из к-рых вносит одинаковый вклад в волновую ф-цию:
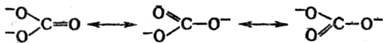
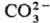
Поэтому ион обладает тригональной симметрией (группа симметрии V 3h ), и каждая связь С—О имеет на 1 / 3 характер двойной связи.
Строение аллильного радикала не соответствует ни одной из классич. структур VI и VII и должно описываться их резонансом:
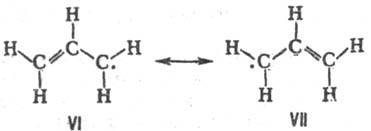
Спектр ЭПР аллильного радикала свидетельствует о том, что неспаренный электрон не локализован ни на одной из концевых метиленовых групп, а распределен между ними так, что радикал имеет группу симметрии С 2h , причем энергетич. барьер вращения концевых метиленовых групп (63 кДж/моль) имеет промежут. значение между величинами, характерными для барьеров вращения вокруг простой и двойной связи С—С.
В соед., включающих связи между атомами с существенно разл. электроотрицательностями, значит. вклад в волновую ф-цию вносят резонансные структуры ионного типа. Строение СО 2 в рамках резонанса теории описывается резонансом трех структур:
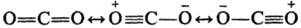
Длина связи между атомами С и О в этой молекуле меньше, чем длина двойной связи С=О.
Поляризация связей в молекуле формамида, приводящая к потере мн. св-в, характерных для карбонильной группы, объясняется резонансом:
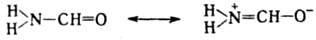
Резонанс структур ведет к стабилизации осн. состояния молекулы, иона или радикала. Мерой этой стабилизации служит энергия резонанса, к-рая тем больше, чем больше число возможных резонансных структур и чем больше число резонирующих низкоэнергетич. эквивалентных структур. Энергию резонанса можно рассчитать при помощи метода валентных связей или метода мол. орбиталей (см. Молекулярных орбиталей методы)как разность энергий осн. состояния молекулы и ее изолир. связей или осн. состояния молекулы и структуры, моделирующей одну из устойчивых резонансных форм.
По своей осн. идее резонанса теория очень близка к теории мезомерии (см. Мезомерия), однако носит более количеств. характер, ее символика вытекает непосредственно из классич. структурной теории, а квантовомех. метод валентных связей служит прямым продолжением резонанса теории. В силу этого резонанса теория продолжает сохранять определенное значение как удобная и наглядная система структурных представлений.
Лит.: Паулинг Л., Природа химической связи, пер. с англ., М.-Л., 1947; Уэланд Дж., Теория резонанса и ее применение в органической химии, пер. с англ., М., 1948; Полинг Л., "Ж. Весе. Хим. об-ва им. Д. И. Менделеева", 1962 т. 7, № 4, с. 462-67. В. И. Минкин.
Теория резонанса — теория электронного строения химических соединений, в соответствие с которой распределение электронов в молекулах (в том числе сложных ионах или радикалах), является комбинацией (резонансом) канонических структур с различной конфигурацией двухэлектронных ковалентных связей. Резонансная волновая функция, описывающая электронную структуру молекулы, является линейной комбинацией волновых функций канонических структур [1] .
Иными словами, молекулярная структура описывается не одной возможной структурной формулой, а сочетанием (резонансом) всех альтернативных структур.
Следствием резонанса канонических структур является стабилизация основного состояния молекулы, мерой такой резонансной стабилизации является энергия резонанса — разность между наблюдаемой энергией основного состояния молекулы и расчетной энергии основного состояния канонической структуры с минимальной энергией [2] .


Содержание
История
Идея резонанса был введена в квантовую механику Вернером Гейзенбергом в 1926 году при обсуждении квантовых состояний атома гелия. Он сравнил структуру атома гелия с классической системой резонирующего гармонического осциллятора.
Модель Гейзенберга была применена Лайнусом Полингом (1928 год) к описанию электронной структуры молекулярных структур. В рамках метода валентных схем Полинг успешно объяснил геометрию и физико-химические свойства целого ряда молекул через механизм делокализации электронной плотности π-связей.
СССР 40-50 гг.
В 1951 году на Всесоюзной конференция по состоянию теории химического состава органической химии под руководством академика А. Н. Несмеянова резонансная теория Полинга и теория мезомери Ингольда были объявлены буржуазными и лженаучными [4] .
Гонения на теорию резонанса получили негативную оценку в мировой научной среде. В одном из журналов Американского химического общества в обзоре, посвящённом положению в советской химической науке, в частности, отмечалось [5] :
В большинстве русских статей на эти темы (…), по-видимому, преобладает шовинистическая идея, что теория резонанса Лайнуса Полинга противоречит догмам диалектического материализма и поэтому должна быть отвергнута. Размах и резкость этого осуждения не имеет аналогов в истории химии
The large majority of Russian papers on these subjects (. ) apparently arising from the chauvinistic idea that the resonance theory of Linus Pauling opposes the tenets of dialectical materialism and therefore must be rejected. The intensity and crudeness of this invective appear to be without parallel in the annals of chemistry.
Читайте также:

