Супер бактерии это кратко
Обновлено: 07.07.2024
В 2017 году ВОЗ опубликовала список критической группы бактерий, представляющих собой повышенную опасность. В их числе – Acinetobacter baumannii, синегнойная палочка (Pseudomonas aeruginosa), энтеробактерии (Enterobacteriaceae), энтерококки фэциум (Enterococcus faecium), золотистый стафилококк (Staphylococcus aureus), хеликобактер пилори (Helicobacter pilori), кампилобактеры (Campylobacter), сальмонелла (Salmonella), гонококк (Neisseria gonorrhoeae), пневмококк (Streptococcus pneumonia), гемофильная палочка (Haemophilus influenza), шигелла (Shigella).
В числе устойчивых микроорганизмов оказались также бактерии Klebsiella pneumonia, Escherichia coli, MRSA (метициллин устойчивые бактерии Staphylococcus aureus) и другие, вызывающие серьезные заболевания: сепсис, гонорею, инфекции мочевыводящих путей, пневмонию.
Также, по оценкам ВОЗ, вероятность смерти людей инфицированных MRSA на 64% выше, если сравнивать с неустойчивой формой инфекции. Кроме того, по данным доклада центра RANDEurope и KMPG, от устойчивых к антибиотикам инфекций в мире ежегодно умирает по меньшей мере 700 тысяч человек. В США, по данным американского Центра по контролю и профилактике заболеваний, эта цифра ежегодно составляет 23 тысячи человек, в Евросоюзе показатель достигает 25 тысяч.
Для того чтобы понять, почему микроорганизмы становятся устойчивыми к лекарствам, важно знать их природу. Бактерии представляют собой одну из первых форм жизни на Земле. Ископаемые свидетельства датируются в ряде случаев началом периода архея – 3,5 миллиарда лет назад. Это обширная группа одноклеточных микроорганизмов.
Первый тип изменчивости имеет место, когда условия окружающей среды оказывают одинаковое влияние на всех особей одного вида. Примером такой изменчивости может послужить появление у зайцев белой шерсти, что ожидаемо в зимний период, поскольку это помогает быть более незаметными для хищников на снегу. Такой тип изменчивости затрагивает фенотипические особенности организма и не наследуется генетически.
Неопределенная изменчивость напрямую связана с изменениями генотипа организма, которые, как правило, нельзя предугадать. Пример – индивидуальные мутации, возникшие у отдельных особей одного вида. Подобная изменчивость может проявляться вне зависимости от текущих условий окружающей среды и способна устойчиво передаваться потомству.
Вспомним и о наследовании приобретенных признаков, открытом еще французским биологом Жаном Батистом Ламарком, основной тезис которого заключается в том, что в ответ на изменения окружающей среды организмы способны меняться, приспосабливаться и передавать приобретенные изменения своему потомству.
По форме бактерии можно разделить на палочковидные – бациллы, сферические – кокки – и спиралевидные – спириллы. По своему строению бактерии делятся на прокариот (доядерные), ДНК (дезоксирибонуклеиноваякислота) которых находится в определенной зоне клетки бактерии, и эукариот (ядерные) – их ДНК располагается в окруженном оболочкой ядре клетки.
Но, несмотря на разнообразие форм и строения, все бактерии объединяет одно важное свойство – способность передавать из поколения в поколение информацию с помощью своего генетического материала (ДНК), в том числе об устойчивости к лекарственным средствам. Причем передача информации и проявление новых признаков, включая резистентность, могут происходить достаточно быстро, учитывая скорость размножения бактерий.
Многие из них путем деления способны давать потомство в течение 30 минут, а за сутки всего одна клетка может образовать 72 новых поколения, каждое из которых получает определенную информацию об устойчивости к лекарственным препаратам, если, конечно, прародитель сталкивался с тем или иным антимикробным средством.
Наука и устойчивость
Сегодня в мире существует несколько тысяч натуральных и даже синтетических антибиотиков, объединенных в 16 классов. Например, пенициллин, относится к бета-лактамным препаратам. Но из всего множества созданных ранее антибиотиков в настоящее время используется не более пяти процентов. Это напрямую связано с тем, что бактерии со временем выработали устойчивость к основной массе таких препаратов.
Все это побудило ВОЗ после проведенных масштабных исследований с 2014 года рассматривать проблему антимикробной резистентности на глобальном уровне и рекомендовать мировому научному сообществу приступить к поиску путей ее решения.
Эту задачу, в частности, решают ученые Северо-Восточного университета в Бостоне (США). Им удалось найти ряд соединений, к одному из которых в лабораторных условиях ни одна из исследуемых бактерий не способна была выработать устойчивость.
И если речь идет, например, о создании принципиально нового вида антибиотиков, то необходимо понимать, что на их разработку, прохождение всех этапов исследований и внедрение в массовое производство, по данным экспертов, уходит в среднем 10 лет. В этой связи ученые также ищут способы решения глобальной проблемы на базе альтернативных антибиотикам противомикробных средств.
В частности, стратегия интегрирует в себя план действий по разработке и внедрению альтернативных методов, технологий, средств профилактики и лечения заболеваний, включая создание биологических лекарственных препаратов на основе бактериофагов.
В 1921 году Ричард Брайонг и Джозеф Мэйсин, последователи Феликса Д'Эрреля, французского микробиолога и первооткрывателя бактериофагов, сделали доклад об успешном лечении инфекций кожи стафилококковым бактериофагом, а в 1922 году Д'Эррель в своем фундаментальном труде изложил результаты начального этапа изучения бактериофагов. И только в 1929 году Александр Флеминг открыл пенициллин.
Что же такое бактериофаги? Они представляют собой внеклеточную форму жизни. Иными словами, это вирусы, размеры которых составляют в среднем от 20 до 200 нанометров (1 нанометр равен одной миллиардной части метра). Так же, как и бактерии, эти вирусы представляют собой еще одну наиболее распространенную форму жизни на нашей планете. Они присутствуют буквально везде: в океане, почве, глубоководных источниках, питьевой воде, пище.
Причем бактериофаги способны размножаться исключительно в клетке-хозяине. Они могут иметь кубическую, нитевидную или форму головастиков. Любая фаговая частица состоит из головки, содержащей нуклеиновую кислоту (ДНК или РНК), заключенную в белковую оболочку – капсид, – и хвостового отростка, состоящего из внутреннего стержня и сократительного чехла. Передвигается бактериофаг с помощью ножек-фибрилл, скрепленных в центре базальной пластиной.
Все бактериофаги имеют особенность, которой и пользуются ученые в ходе создания альтернативных антибактериальных препаратов – каждому типу бактерий свойственны собственные вирусы-фаги. При этом бактериофаги, как снайперы, избирательно поражают только бактериальные клетки, а не всю микрофлору организма, в отличие от антибиотиков.
Происходит этот процесс в несколько этапов. Сначала бактериофаг распознает бактериальную клетку и прикрепляется к ее оболочке. Затем вирус-бактериофаг производит инъекцию своей нуклеиновой кислоты (генома) внутрь бактерии. Далее происходит биосинтез белковых и нуклеиновых компонентов новых фаговых частиц на основе введенного генома. Еще один этап – соединение компонентов и формирование новых бактериофагов внутри бактерии. И, наконец, процесс лизиса – распад бактериальной клетки и выход зрелых фагов.
При неблагоприятных внешних условиях и малом количестве вредоносных клеток бактериофаги развиваются по лизогенному циклу: введенный геном существует внутри клетки пассивно – не размножаясь.
Кроме того, в отличие от антибиотиков, бактериофаги способны приобретать новые признаки естественным образом для борьбы с резистентными мутациями бактериальных клеток.
Отечественные разработки
Если говорить об успехах отечественных ученых в создании альтернативных антимикробных препаратов на основе бактериофагов, то еще благодаря сотрудничеству Феликса Д'Эрреля и грузинского микробиолога Георгия Элиавы в 1920-х годах в СССР был создан первый и единственный в мире научно-исследовательский центр бактериофагологии.
Во времена Великой Отечественной войны также применялась фаговая терапия. Особое внимание уделялось разработке и производству бактериофагов, подавляющих кишечные инфекции – холеру, брюшной тиф, дизентерию и сальмонеллез. Всего за годы войны для фронта было изготовлено более 200 тысяч литров бактериофагов.
В настоящий момент предприятие приступило к созданию всероссийской базы штаммовой коллекции бактериофагов для выпуска новых лекарственных противомикробных препаратов на их основе.
В перспективе – выпуск первого в мире лекарственного препарата, содержащего бактериофаги в капсулах для лечения и профилактики заболеваний, вызываемых бактериями рода стафилококков (лат. Staphylococcus), стрептококков (Streptococcus), протеи (Proteus – P. vulgaris, P. mirabilis), клебсиеллы (Klebsiella pneumoniae), синегнойной (Pseudomonas aeruginosa) и кишечной (Escherichia coli) палочек.
Супербактерии — это микроорганизмы, которые стали устойчивыми к лекарственным препаратам. Эти лекарственно устойчивые бактерии и грибки трудно контролировать и лечить, зачастую супербактерии устойчивы к антибиотикам.
Антибиотики являются жизненно важными препаратами, которые помогают спасти много жизней. Они лечат широкий спектр инфекций, от легких инфекций мочевыводящих путей до угрожающего жизни сепсиса. Однако рост супербактерий частично связан с чрезмерным использованием антибиотиков, что способствует устойчивости к ним. Невозможно полностью остановить устойчивость к антибиотикам, поскольку это является частью естественной эволюции микроорганизмов. Тем не менее, необходимо принимать меры, чтобы избежать устойчивости к антибиотикам.
Что такое супербактерии?
Любой микроорганизм может стать супербактерией, но бактериальные и грибковые штаммы, которые обычно заражают людей, животных и сельскохозяйственные культуры, становятся им. По мере того как эти бактерии и грибки приспосабливаются к действию препаратам, они начинают сопротивляться лечению. Устойчивые к антибиотикам инфекции могут привести к смертельным исходам.
Устойчивые к антибиотикам бактерии в большей степени присутствуют в учреждениях, требующих регулярной стерилизации, таких как больницы. Регулярная стерилизация является ключом к борьбе с инфекциями, но она также может сделать некоторые микроорганизмы сильнее. Кроме того, супербактерии могут присутствовать в некоторых продуктах питания, например, в продуктах животного происхождения, которые фермеры обработали антибиотиками.
К микроорганизмам самого высокого риска относятся:
- Клостридиум диффициле
- Ацинетобактерии, которые устойчивы к типу антибиотиков, называемых карбапенемами
- Candida auris
- Энтеробактерии
- Гонококк
Врачи традиционно используют карбапенемы для лечения тяжелых или других бактериальных инфекций высокого риска. Между тем, другие патогены могут представлять серьезную угрозу для здоровья, в том числе:
- метициллинрезистентный золотистый стафилококк, который вызывает стафилококковые инфекции
- некоторые виды кандиды
- пневмококк
- микобактерии туберкулеза
- некоторые виды сальмонелл
- ванкомицинрезистентные энтерококки
- синегнойная палочка
- Шигелла
- Кампилобактер
Патогены, которые могут стать устойчивыми и распространяться. К ним относятся:
- Аспергилл, которые устойчивы к противогрибковым обработкам
- Микоплазма гениталиум
- Бордетеллы коклюша
Больницы являются основными источниками лекарственно-устойчивых инфекций. Определенная группа бактерий вызывает большую часть антибиотикорезистентных инфекций в стационарных условиях. Эта группа включает в себя:
- Энтерококк
- Золотистый стафилококк
- Клебсиелла пневмонии
- Acinetobacter baumannii
- P. aeruginosa
- Вид энтеробактерий
Более сильные штаммы этих бактерий стали устойчивыми к антибиотикам и практически не реагируют на антибиотики. Некоторые даже выработали устойчивость к дезинфицирующим средствам, таким как дезинфицирующие средства на спиртовой основе, которые используют многие больницы.
Авторы научного доклада 2018 года отметили, что штаммы E. faecium были в 10 раз более толерантны к спиртовым дезинфицирующим средствам, чем более старые изоляты.
Приведенный перечень не дает полной картины всех потенциально устойчивых к лекарственным средствам патогенов. При регулярном воздействии антибиотиков или противогрибковых препаратов почти любые бактерии или грибки могут развить резистентность. Однако перечисленные выше патогенные микроорганизмы в настоящее время представляют наибольшую угрозу для здоровья.
Симптомы
Никакие особые симптомы не указывают на то, что у человека инфекция вызвана супербактерией. Человек будет испытывать те же симптомы, что и при обычной инфекции. Однако со временем инфекция не будет реагировать на лечение, и симптомы станут намного хуже. Если инфекция плохо поддается лечению, врач проводит диагностические тесты, чтобы определить, является ли патоген лекарственно устойчивым.
Эволюция
В конце концов, у человека может развится инфекция, которая плохо реагирует на первоначальный антибиотик. Врач может назначить другой антибиотик. Бактерии, которые переживут второе лечение, могут также развить устойчивость к нему. Поскольку этот цикл продолжается, способность патогена адаптироваться позволяет ему пережить множество различных антибиотиков, и он становится супербактерией. Кроме того, некоторые патогены обладают фенотипической устойчивостью, что означает, что они устойчивы к определенным антибиотикам без генетической мутации.
Предотвращение инфекции является одним из важных способов борьбы с супербактериями. Профилактика включает в себя:
- регулярное мытье рук теплой водой с мылом
- высушивание рук после мытья
- избегать кашля или чихания в руки
- мытье рук после обработки сырых продуктов животного происхождения
- мытье рук после общения с больным человеком или избегание контакта с ним, если это возможно
- не делиться личными вещами, такими как бритвы или полотенца
- при необходимости используйте только антибактериальное мыло или дезинфицирующие средства
- готовить пищу при безопасных температурах, которые могут убить микробы
Можно свести к минимуму риск заболевания, питаясь здоровой пищей, занимаясь спортом и получая достаточное количество сна.
Предотвращение устойчивости к антибиотикам
Устойчивость к антибиотикам — это естественный процесс, поэтому нет способа остановить его полностью. Однако можно замедлить развитие сопротивления. Можно предпринять шаги по сокращению использования антибиотиков.
- Принимайте антибиотики, когда это необходимо: большинство врачей назначают антибиотики только в том случае, если человек не может обойтись без них.
- Использование короткого курса лечения
- Не использовать антибиотики при вирусных инфекциях: антибиотики не влияют на болезни, вызванные вирусами, такими как грипп.
Исследователи работают над созданием новых и более эффективных антибиотиков и ищут пути борьбы с устойчивостью к антибиотикам. Например, исследование 2019 года показало, что антиоксидант из клюквы может предотвратить устойчивость к антибиотикам. Этот антиоксидант — проантоцианидин сделает некоторые антибиотики более эффективными, обходя естественное сопротивление бактерий. Новые исследования обещают улучшить лечение и снизить риск развития устойчивости к антибиотикам.
Заключение
Супербактерии стали серьезной проблемой. Эти микроорганизмы являются патогенами, которые стали устойчивыми к антибиотикам. Устойчивость к антибиотикам возникает естественным образом и это, как правило, очень медленный процесс. Однако чрезмерное использование антибиотиков привело к резкому увеличению резистентных бактерий, которые трудно устранить. В то время как различные препараты все еще могут устранить устойчивые бактерии или грибки, основное внимание следует уделять предотвращению развития инфекций.


Учредитель сетевого издания (Medical Insider), главный редактор, автор статей.
Врач ультразвуковой диагностики в СЗЦДМ, травматолог-ортопед, г. Санкт-Петербург

Вы могли никогда не слышать о таких микроорганизмах как акинетобактерия Баумана, синегнойная палочка, или энтеробактерии. Но эти три убийцы возглавили официальный список бактерий, для которых крайне необходимы новые лекарства. Он был составлен Всемирной организацией здравоохранения (ВОЗ) и содержит 12 бактерий и бактериальных семейств. Причем наименования из топ-3 входят в критически опасную категорию.
Рейтинг самых опасных супербактерий не предназначен для того, чтобы напугать людей. Это сигнал для исследователей и фармацевтических компаний о том, каковы должны быть их приоритеты.
Вот как выглядит полная подборка устойчивых к антибиотикам микроорганизмов, ранжированных по приоритету важности от среднего до критического.
12. Пневмококки
Устойчивость: к пенициллину
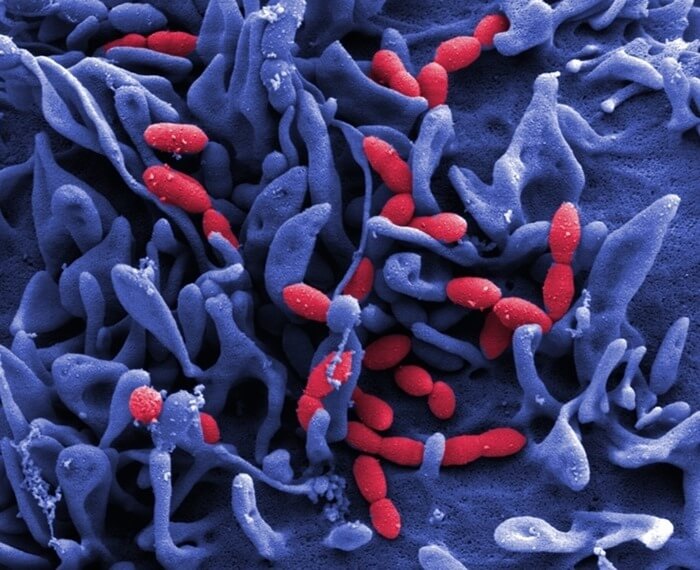
Эти бактерии могут стать причиной многих видов заболеваний, в том числе: пневмонии (воспаление легких), инфекций уха и пазух, менингита (инфекции оболочек головного и спинного мозга), и карбункула (заражение крови). Пневмококковые бактерии распространяются через кашель, чихание и тесный контакт с инфицированным человеком.
11. Гемофильная палочка
Устойчивость: к ампициллину
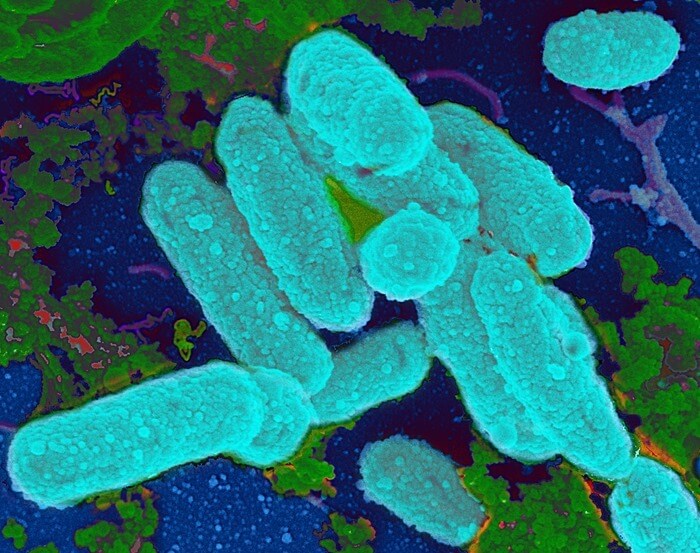
Эти микроорганизмы могут вызывать инфекции у людей всех возрастов, начиная от легких, таких как инфекции уха, до тяжелых, такие как инфекции кровотока.
10. Шигеллы
Устойчивость: к фторхинолону
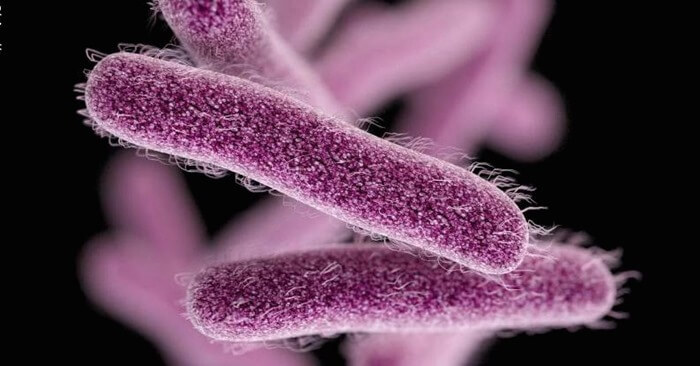
Эта группа бактерий вызывает заболевание под названием шигеллез. Большинство больных шигеллезом жалуются на понос, лихорадку и спазмы желудка. Дизентерия обычно длится от 5 до 7 дней. Избежать этого заболевания можно с помощью частого и тщательного мытья рук с мылом и соблюдения правил гигиены.
9. Энтерококки фэциум
Устойчивость: к ванкомицину
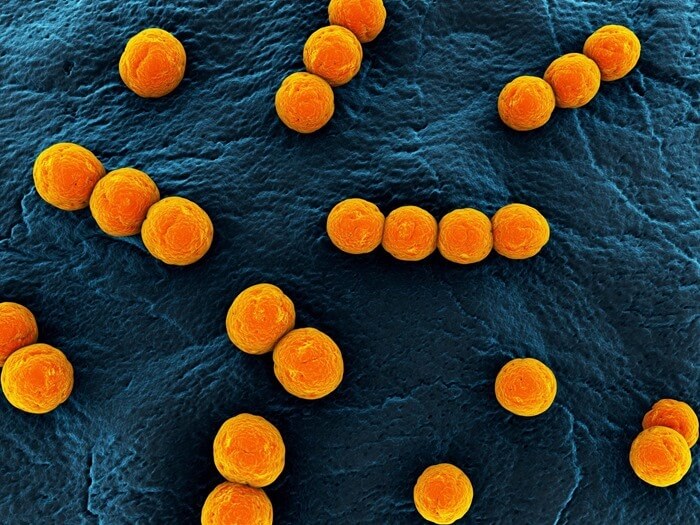
Энтерококки являются частью нормальной кишечной флоры у большого числа млекопитающих, и в настоящее время эти микробы используются в качестве индикаторов
загрязнения фекалиями воды и пищевых продуктов. Эти организмы считаются одной из основных причин внутрибольничных и инфекционных заболеваний из-за способности выжить в окружающей среде и их внутренней устойчивости к противомикробным препаратам. Часто вызывают инфекции мочеполовых органов.
8. Золотистый стафилококк
Устойчивость: к метициллину, нейтральный и устойчивый к ванкомицину
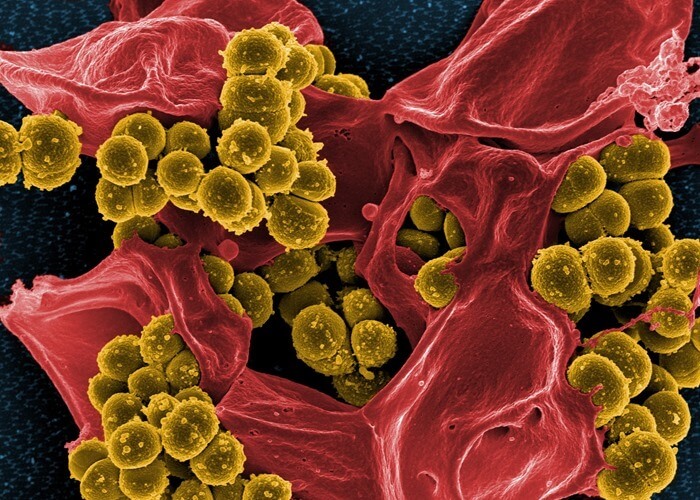
Этот патоген вызывает широкий спектр клинических инфекций. Это ведущая причина инфекционного эндокардита, а также кожных и плевролегочных инфекций.
7. Хеликобактер пилори
Устойчивость: к кларитромицину
6. Кампилобактеры
Устойчивость к фторхинолону
5. Сальмонелла
Устойчивость: к фторхинолону
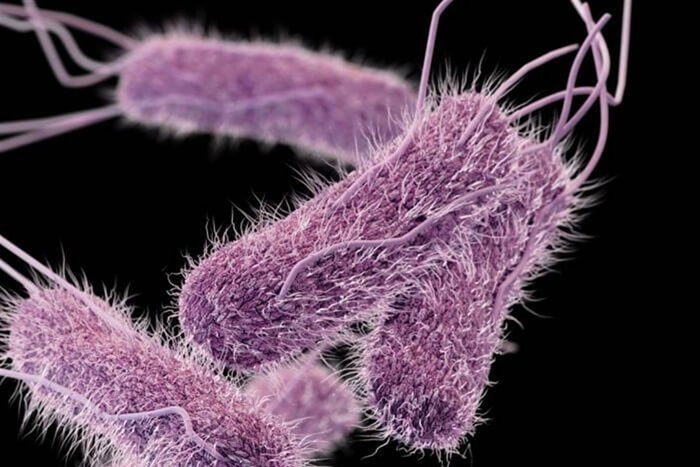
У людей, инфицированных сальмонеллой, развивается диарея, лихорадка, боль в животе спустя от 12 до 72 часов после заражения. Большинство людей выздоравливают без лечения через 4-7 дней. Тем не менее у некоторых больных диарея может быть настолько сильной, что их приходится госпитализировать.
4. Гонококки
Устойчивость: к фторхинолону и цефалоспорину
3. Акинетобактерия Баумана
Устойчивость: к карбапенемам
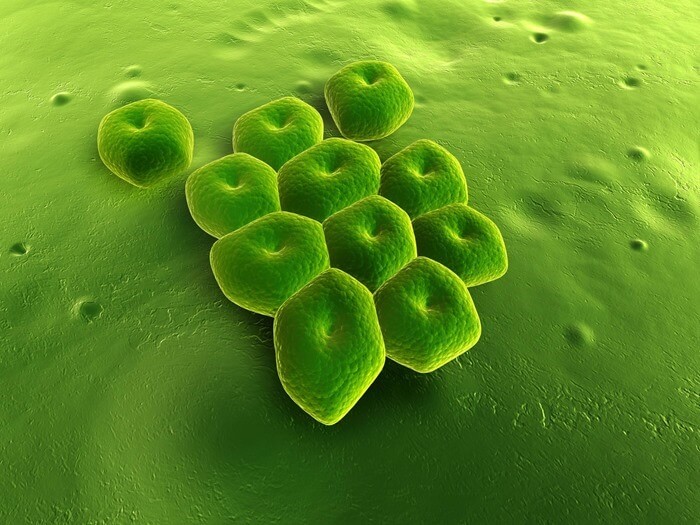
Acinetobacter baumannii - важнейший представитель рода Acinetobacter - является одним из наиболее опасных патогенов для учреждений здравоохранения во всем мире. Он обладает способностью быстро приобретать устойчивость к антибиотикам, что делает его одной из важнейших супербактерий, угрожающих нынешней антибиотической эре. Самой распространенной инфекцией, вызванной этим микробом, является госпитальная пневмония.
2. Синегнойная палочка
Устойчивость: к карбапенемам
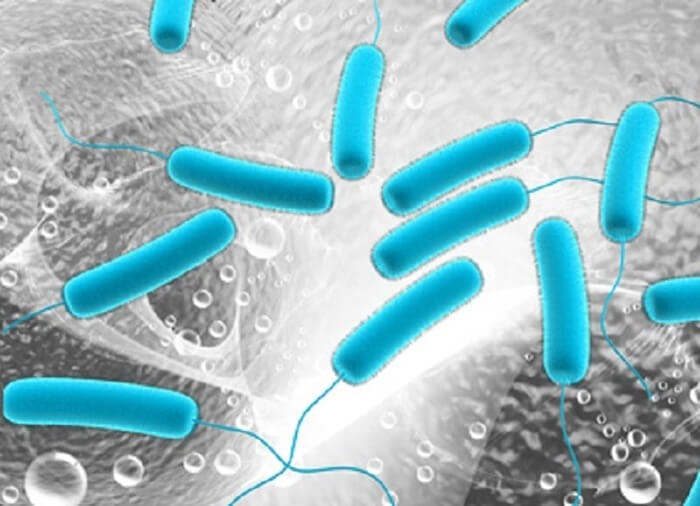
Патоген, поражающий пациентов со слабым иммунитетом. Синегнойная палочка известна как основная причина заболеваемости и смертности у пациентов с муковисцидозом и как одна из ведущих причин внутрибольничных инфекций
1. Энтеробактерии, в том числе клебсиелла, кишечная палочка, серрации и протеус
Устойчивость: к карбапенемам и штаммам, продуцирующим бета-лактамазы расширенного спектра действия
Один патоген, с устойчивостью к антибиотикам, не вошел в подборку ВОЗ. Речь идет о микобактерии туберкулеза. Проблема туберкулеза с лекарственной устойчивостью хорошо известна, а цель рейтинга ВОЗ заключалась в том, чтобы акцентировать внимание на угрозах, которые еще не получили широкого признания.
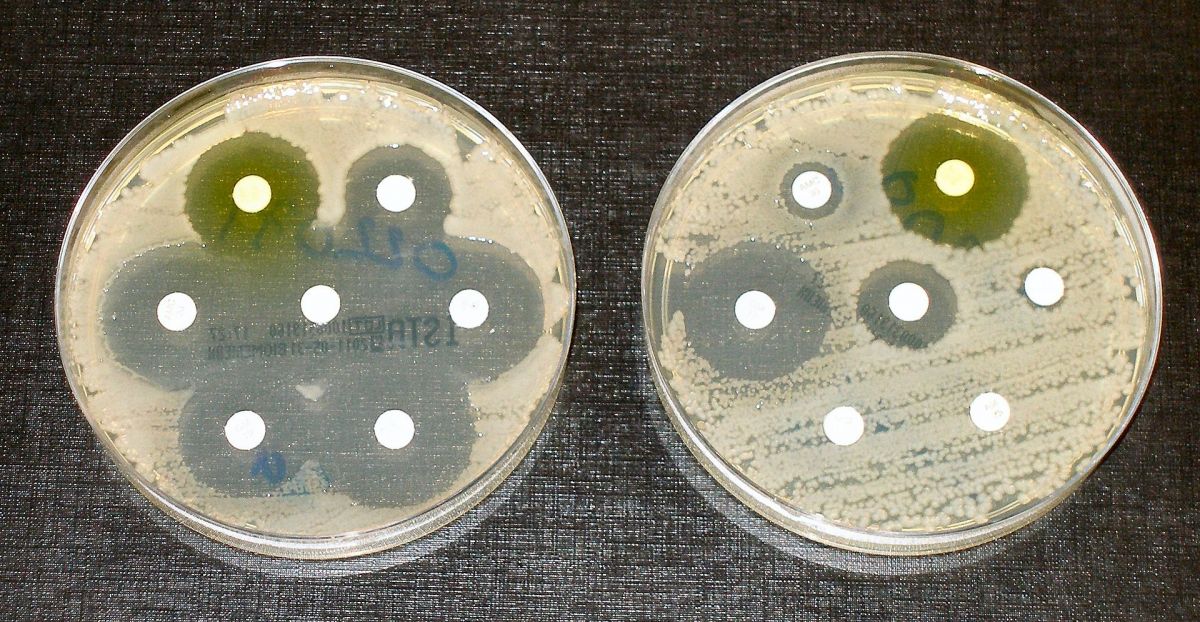
Тесты на устойчивость к антибиотикам. Бактерии высевают штрихами на чашках с белыми дисками, пропитанными антибиотиком. Чистые кольца, как на чашке слева, показывают, что бактерии не выросли — что свидетельствует об отсутствии устойчивости у этих бактерий. Бактерии на чашке справа полностью восприимчивы только к трем из семи протестированных антибиотиков / ©/ Dr Grahan Beards
Как известно, в 2014 году в Женеве Всемирная организация здравоохранения сделала доклад, содержащий полную картину влияния традиционных антимикробных препаратов на бактерии с учетом данных полученных из 114 стран.
В 2017 году ВОЗ опубликовала список критической группы бактерий, представляющих собой повышенную опасность.
В их числе —Acinetobacter baumannii, синегнойная палочка (Pseudomonas aeruginosa), энтеробактерии (Enterobacteriaceae), энтерококки фэциум (Enterococcus faecium), золотистый стафилококк (Staphylococcus aureus), хеликобактер пилори (Helicobacter pilori), кампилобактеры (Campylobacter), сальмонелла (Salmonella), гонококк (Neisseria gonorrhoeae), пневмококк (Streptococcus pneumonia), гемофильная палочка (Haemophilus influenza, шигелла (Shigella).
В числе устойчивых микроорганизмов оказались также бактерии Klebsiella pneumonia, Escherichia coli, MRSA (метициллин устойчивые бактерии Staphylococcus aureus) и другие, вызывающие серьезные заболевания: сепсис, гонорею, инфекции мочевыводящих путей, пневмонию.
Также, по оценкам ВОЗ, вероятность смерти людей инфицированных MRSA на 64% выше, если сравнивать с неустойчивой формой инфекции.
Кроме того, по данным доклада центра RANDEurope и KMPG, от устойчивых к антибиотикам инфекций в мире ежегодно умирает по меньшей мере 700 тысяч человек.
В США, по данным американского Центра по контролю и профилактике заболеваний, эта цифра ежегодно составляет 23 тысячи человек, в Евросоюзе показатель достигает 25 тысяч.
Зарождение “супербактерии”
Для того чтобы понять, почему микроорганизмы становятся устойчивыми к лекарствам, важно знать их природу. Бактерии представляют собой одну из первых форм жизни на Земле.
Ископаемые свидетельства датируются в ряде случаев началом периода архея — 3,5 миллиарда лет назад. Это обширная группа одноклеточных микроорганизмов.
Согласно теории, новые признаки в строении организмов и их функциональных особенностях возникают в связи с изменчивостью, которая, в свою очередь, может быть определенной и неопределенной.
Первый тип изменчивости имеет место, когда условия окружающей среды оказывают одинаковое влияние на всех особей одного вида.
Примером такой изменчивости может послужить появление у зайцев белой шерсти, что ожидаемо в зимний период, поскольку это помогает быть более незаметными для хищников на снегу. Такой тип изменчивости затрагивает фенотипические особенности организма и не наследуется генетически.
Неопределенная изменчивость напрямую связана с изменениями генотипа организма, которые, как правило, нельзя предугадать. Пример – индивидуальные мутации, возникшие у отдельных особей одного вида.
Подобная изменчивость может проявляться вне зависимости от текущих условий окружающей среды и способна устойчиво передаваться потомству.
Вспомним и о наследовании приобретенных признаков, открытом еще французским биологом Жаном Батистом Ламарком, основной тезис которого заключается в том, что в ответ на изменения окружающей среды организмы способны меняться, приспосабливаться и передавать приобретенные изменения своему потомству.
По форме бактерии можно разделить на палочковидные — бациллы, сферические –кокки — и спиралевидные — спириллы.

По своему строению бактерии делятся на прокариот (доядерные), ДНК (дезоксирибонуклеиноваякислота) которых находится в определенной зоне клетки бактерии, и эукариот (ядерные) — их ДНК располагается в окруженном оболочкой ядре клетки.
Но, несмотря на разнообразие форм и строения, все бактерии объединяет одно важное свойство — способность передавать из поколения в поколение информацию с помощью своего генетического материала (ДНК), в том числе об устойчивости к лекарственным средствам.
Причем передача информации и проявление новых признаков, включая резистентность, могут происходить достаточно быстро, учитывая скорость размножения бактерий.
Многие из них путем деления способны давать потомство в течение 30 минут, а за сутки всего одна клетка может образовать 72 новых поколения, каждое из которых получает определенную информацию об устойчивости к лекарственным препаратам, если, конечно, прародитель сталкивался с тем или иным антимикробным средством.
В 2017 году женщина скончалась из-за полной резистентности бактерии Klebsiella pneumoniae к 26 видам известных антибиотиков. Все они оказались полностью бесполезны в борьбе с инфекцией.
Наука и устойчивость
В настоящее время наиболее известными средствами для борьбы с бактериями являются антибиотики, появлению которых мировое сообщество обязано Александру Флемингу, обнаружившему в 1928 году в ходе исследования, что обыкновенная плесень Penicillium, которая произрастает на лежалом хлебе, вырабатывает вещество, убивающее бактерии семейства Staphylococcaceae.
Сегодня в мире существует несколько тысяч натуральных и даже синтетических антибиотиков, объединенных в 16 классов. Например, пенициллин, относится к бета-лактамным препаратам.
Но из всего множества созданных ранее антибиотиков в настоящее время используется не более пяти процентов. Это напрямую связано с тем, что бактерии со временем выработали устойчивость к основной массе таких препаратов.
Все это побудило ВОЗ после проведенных масштабных исследований с 2014 года рассматривать проблему антимикробной резистентности на глобальном уровне и рекомендовать мировому научному сообществу приступить к поиску путей ее решения.
Среди них есть и такой метод борьбы — научиться выращивать устойчивые виды бактерий и исследовать химические соединения, с помощью которых резистентность будет преодолена.
Эту задачу, в частности, решают ученые Северо-Восточного университета в Бостоне (США). Им удалось найти ряд соединений, к одному из которых в лабораторных условиях ни одна из исследуемых бактерий не способна была выработать устойчивость.
И если речь идет, например, о создании принципиально нового вида антибиотиков, то необходимо понимать, что на их разработку, прохождение всех этапов исследований и внедрение в массовое производство, по данным экспертов, уходит в среднем 10 лет.
В этой связи ученые также ищут способы решения глобальной проблемы на базе альтернативных антибиотикам противомикробных средств.
Она предусматривает меры по ограничению распространения устойчивости микроорганизмов к противомикробным препаратам, химическим и биологическим средствам.
В частности, стратегия интегрирует в себя план действий по разработке и внедрению альтернативных методов, технологий, средств профилактики и лечения заболеваний, включая создание биологических лекарственных препаратов на основе бактериофагов.
Вирусы против “супербактерий”
В 1921 году Ричард Брайонг и Джозеф Мэйсин, последователи Феликса Д’Эрреля, французского микробиолога и первооткрывателя бактериофагов, сделали доклад об успешном лечении инфекций кожи стафилококковым бактериофагом, а в 1922 году Д’Эррель в своем фундаментальном труде изложил результаты начального этапа изучения бактериофагов. И только в 1929 году Александр Флеминг открыл пенициллин.

Что же такое бактериофаги? Они представляют собой внеклеточную форму жизни. Иными словами, это вирусы, размеры которых составляют в среднем от 20 до 200 нанометров (1 нанометр равен одной миллиардной части метра).
Так же, как и бактерии, эти вирусы представляют собой еще одну наиболее распространенную форму жизни на нашей планете. Они присутствуют буквально везде: в океане, почве, глубоководных источниках, питьевой воде, пище.
Причем бактериофаги способны размножаться исключительно в клетке-хозяине. Они могут иметь кубическую, нитевидную или форму головастиков.
Любая фаговая частица состоит из головки, содержащей нуклеиновую кислоту (ДНК или РНК), заключенную в белковую оболочку — капсид, —и хвостового отростка, состоящего из внутреннего стержня и сократительного чехла. Передвигается бактериофаг с помощью ножек-фибрилл, скрепленных в центре базальной пластиной.
Все бактериофаги имеют особенность, которой и пользуются ученые в ходе создания альтернативных антибактериальных препаратов — каждому типу бактерий свойственны собственные вирусы-фаги.
При этом бактериофаги, как снайперы, избирательно поражают только бактериальные клетки, а не всю микрофлору организма, в отличие от антибиотиков.

Происходит этот процесс в несколько этапов. Сначала бактериофаг распознает бактериальную клетку и прикрепляется к ее оболочке. Затем вирус-бактериофаг производит инъекцию своей нуклеиновой кислоты (генома) внутрь бактерии.
Далее происходит биосинтез белковых и нуклеиновых компонентов новых фаговых частиц на основе введенного генома. Еще один этап — соединение компонентов и формирование новых бактериофагов внутри бактерии.
И, наконец, процесс лизиса — распад бактериальной клетки и выход зрелых фагов.
Иными словами, эти неклеточные формы жизни с генетической программой способны проникать практически в любую вредоносную бактериальную клетку, размножиться и разрушить ее, не причиняя вреда остальной микрофлоре организма.
При неблагоприятных внешних условиях и малом количестве вредоносных клеток бактериофаги развиваются по лизогенному циклу: введенный геном существует внутри клетки пассивно — не размножаясь.
Кроме того, в отличие от антибиотиков, бактериофаги способны приобретать новые признаки естественным образом для борьбы с резистентными мутациями бактериальных клеток.
Отечественные разработки
Если говорить об успехах отечественных ученых в создании альтернативных антимикробных препаратов на основе бактериофагов, то еще благодаря сотрудничеству Феликса Д’Эрреля и грузинского микробиолога Георгия Элиавы в 1920-х годах в СССР был создан первый и единственный в мире научно-исследовательский центр бактериофагологии.
Уже в 1930-х бактериофаги советского производства впервые были использованы в экстренных ситуациях. Например, в 1938 году в нескольких пограничных с СССР районах Афганистана для профилактики эпидемии холеры бактериофаги давали местному населению, добавляли в колодцы и водоемы.
Во времена Великой Отечественной войны также применялась фаговая терапия. Особое внимание уделялось разработке и производству бактериофагов, подавляющих кишечные инфекции — холеру, брюшной тиф, дизентерию и сальмонеллез. Всего за годы войны для фронта было изготовлено более 200 тысяч литров бактериофагов.
В настоящий момент предприятие приступило к созданию всероссийской базы штаммовой коллекции бактериофагов для выпуска новых лекарственных противомикробных препаратов на их основе.
В перспективе — выпуск первого в мире лекарственного препарата, содержащего бактериофаги в капсулах для лечения и профилактики заболеваний, вызываемых бактериями рода стафилококков (лат. Staphylococcus), стрептококков (Streptococcus), протеи (Proteus — P. vulgaris, P. mirabilis), клебсиеллы (Klebsiella pneumoniae), синегнойной (Pseudomonas aeruginosa) и кишечной (Escherichia coli) палочек.
Результаты наработок зарубежных и российских ученых по поиску новых антимикробных средств, безусловно, вселяют уверенность в том, что глобальная задача антимикробной резистентности в скором времени может быть решена.
Читайте также:

