Сепсис патогенез кратко и понятно
Обновлено: 05.07.2024
Сепсис – это неспецифическое инфекционное заболевание, характеризующееся развитием синдромного системного ответа на воспаление, возникающего при непрерывном или периодическом поступлении из очага инфекции в лимфо- и кровоток микроорганизмов, их токсинов, что становится причиной развития инфекционной полиорганной недостаточности вследствие утраты способности иммунных сил организма к ограничению инфекционного очага.
Сепсис – одна из наиболее трудно решаемых задач интенсивной терапии на современном этапе и является проблемой, прежде всего, макроорганизма. Помимо того, и свойства микробного фактора оказывают значительную роль в клинической симптоматике сепсиса.
Эпидемиология
Средняя частота сепсиса составляет 50–95 эпизодов на 100000 тыс. человек. Частота эпизодов сепсиса ежегодно увеличивается приблизительно на 9 %.
Этиология
Возбудителем сепсиса наиболее часто является нозокомиальная инфекция (Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter Baumannii, Pseudomonas aeruginosa, Escherichia coli, Clostridium difficile): 58 % составляет грамотрицательная микрофлора, 34 % – грамположительная, в 8 % случаев причиной сепсиса являются грибы.
Возбудители, обладающие потенциальной способностью спровоцировать сепсис, не имеют каких-либо отличий от возбудителей, выявленных при иных клинических формах болезни.
Патогенез
Факторы патогенеза сепсиса:
- Микробиологический: вид, вирулентность, количество и длительность воздействия попавших в организм микроорганизмов, что обуславливает бактериемию, микробную токсемию, эндо- и аутотоксикоз.
- Место проникновения инфекции: область, характер и объем повреждения тканей, состояние кровообращения в очаге, что может стать причиной возникновения системного деструктивного васкулита, гиперкоагуляции с последующей коагулопатией потребления – ДВС-синдрома.
- Реактивность организма: состояние иммунобиологических сил организма, его органов, систем, что приводит к дисбалансу иммунной системы – несостоятельности системы иммунореактивности.
Развитию сепсиса способствуют:
- неконтролируемая инфекция;
- массивная травма;
- геморрагический шок;
- некроз тканей;
- апоптоз;
- анафилаксия.
Пусковым агентом патологического процесса являются сигнальные молекулы PAMPs, которые различают антигенные структуры бактериальных клеток: липопротеины, пептидогликаны, бактериальные ДНК, липополисахариды и DAMPs, которые определяют антигенные структуры разрушенных клеток при различных воздействиях: белок теплового шока, ДНК, мочевую кислоту, HMGD-1.
В последующем происходи их соединение с Toll-подобными и Nod-подобными активационными рецепторами, которые активируют иммунологические механизмы врожденного иммунитета.
К сенсорам и эффекторам, воспринимающим и реализующим свой молекулярно-клеточный функциональный потенциал, относятся комплексные белковые системы (система комплемента, коагуляционно-литическая система), клетки сосудов и тканей (эндотелий, эпителий, жировые клетки), кровяные и лимфатические клетки (гранулоциты, моноциты, T- и B-лимфоциты). В результате активации этих систем и клеток происходит значительное поступление в кровоток биологически активных веществ (гуморальных и клеточных медиаторов), обладающих повреждающим действием и возникновение неконтролируемого небактериального воспалительного ответа, что и приводит к развитию прогрессирующей полиорганной недостаточности.
Клиническая картина
Патологические процессы, которые развиваются при сепсисе, затрагивают практически все органы и системы организма человека.
Выделяют следующие формы сепсиса:
- По темпу развития:
- молниеносный;
- острый;
- подострый;
- хронический;
- септический шок.
- По локализации очага инфекции:
- легочный;
- абдоминальный;
- акушерско-гинекологический;
- ангиогенный и т. д.
- В зависимости от разновидности возбудителя:
- грамположительный;
- грамотрицательный.
- По стадии компенсации:
- компенсированный;
- субкомпенсированный;
- декомпенсированный;
- рефрактерный.
Классификация сепсиса (Bone RC, Sprung Ch.L, Sibbald WJ (1992))
- Бактериемия.
- Синдром системной воспалительной реакции.
- Сепсис.
- Тяжелый сепсис.
- Септический шок.
- Синдром мультиорганной недостаточности.
В случае возникновения молниеносного сепсиса тяжелая клиническая картина развивается интенсивно в течение 1–3-х суток с момента проникновения или активизации инфекционного агента.
Острым считают сепсис продолжительностью не более 1–2 мес.
Если заболевание не регрессирует спустя 2–3 мес., то его расценивают как подострое течение сепсиса, если спустя 5–6 – как хроническое.
В преобладающем большинстве случаев сепсис характеризуется острым началом.
Приблизительно у четверти больных до возникновения типичной клинической симптоматики сепсиса выявляется состояние, обозначенное как предсепсис.
Оценку тяжести состояния пациента (при поступлении в лечебное учреждение) и прогнозирование исхода рекомендуется проводить при помощи модернизированной шкалы Sepsis Severity Score.
Общее состояние больного, как правило, тяжелое. Кратковременные периоды возбуждения сменяются заторможенностью, прогрессирует анемия, кожные покровы приобретают бледный субиктеричный цвет, пульс становится частым, лабильным и не имеет взаимосвязи с поражением бронхолегочной системы. На коже в результате тромбогеморрагического синдрома и септических заносов возникают экзантема в виде пустул, пузырьков, различные по площади кровоизлияния. Геморрагические очаги могут возникать в конъюнктиве склер и слизистых оболочках полости рта, носа.
Нарушение терморегуляции проявляется в виде гипертермии, гектической лихорадки, потрясающего озноба. В терминальную фазу довольно часто наблюдается снижение температуры тела ниже нормы.
Изменения со стороны центральной нервной системы – нарушение ментального статуса – проявляются в виде дезориентации, сонливости, спутанного сознания, возбуждения или заторможенности. Кома возможна, но не характерна.
Со стороны сердечно-сосудистой системы наблюдается тахикардия, вазодилатация в сочетании с вазоконстрикцией, падение сосудистого тонуса, снижение артериального давления, депрессия миокарда и уменьшение сердечного выброса.
Со стороны системы дыхания преобладают одышка, респираторный алкалоз, ослабление дыхательной мускулатуры, распространенные инфильтраты в легких, отек легких. При тяжелом сепсисе зачастую развивается дистресс-синдром взрослых в форме интерстициального отека межальвеолярных перегородок, усугубляющего газообмен в легких.
Изменения в почках проявляются в виде гипоперфузии, повреждения почечных канальцев, азотемии, олигурии. Патологические процессы в печени, селезенке манифестируются в виде желтухи, повышения уровня билирубина и трансаминаз. Объективно и при инструментальном исследовании наблюдаются гепатомегалия, спленомегалия.
Желудочно-кишечный тракт реагирует на сепсис тошнотой, рвотой, поносами, появляются или нарастают боли в животе.
Характерные изменения в крови: нейтрофильный лейкоцитоз и сдвиг лейкоцитарной формулы влево, вакуолизация и токсическая зернистость нейтрофилов, тромбоцитопения, эозинопения, снижение гемового железа, гипопротеинемия. Нарушение системной коагуляции развивается в виде активации коагуляционного каскада и угнетения фибринолиза, что усугубляет микроциркуляторные нарушения и снижение гемоциркуляции в органах.
Клиническая симптоматика сепсиса зависит от характера микробной флоры: грамположительная чаще вызывает нарушение функционирования сердечно-сосудистой системы (например – инфекционный эндокардит с поражением клапанов сердца), грамотрицательная – гектическую лихорадку, ознобы, вторичное поражение желудочно-кишечного тракта.
Метастатические гнойные очаги могут формироваться практически в любой области организма, в том числе в тканях мозга, мозговых оболочках, в легких и плевре, в суставах. Если абсцессы крупные, то развивается дополнительная симптоматика поражения соответствующего органа.
Септический шок является крайне тяжелым проявлением сепсиса и характеризуется прогрессирующей циркуляторной недостаточностью с персистирующей артериальной гипотензией даже при адекватном волемическом восполнении объема циркулирующей крови при отсутствии иных причин для критического снижения артериального давления.
Диагностика и дифференциальный диагноз
Основные сложности, возникающие при диагностике сепсиса:
- подобие клинических и лабораторных проявлений асептической системной воспалительной реакции и сепсиса;
- генетически детерминированные различия и особенности иммунного ответа на внедрение инфекционного агента;
- влияние проводимого лечения на динамику лабораторных показателей, отражающих активность воспалительного процесса;
- отсутствие достоверных лабораторных признаков сепсиса;
- отсутствие достаточного подтверждения значимости в отношении молекулярных маркеров сепсиса
При подходе к диагностическому алгоритму при сепсисе необходимо учитывать и распознавать:
- фазу и динамику септического процесса;
- ключевые звенья патогенеза сепсиса – сенсорные и эффекторные клетки;
- медиаторы и биомаркеры;
- органы, вовлеченные в процесс, нарушение их функций;
- исход септического процесса (ранний сепсис – возникает через несколько часов, молниеносное течение; поздний сепсис – возникает через несколько дней или месяцев, отличается хроническим медленным течением).
Сигнальные молекулы
В клинической практике наиболее часто определяется содержание прокальцитонина и IL-6 как биомаркеров сепсиса. При диагностическом уровне прокальцитонина в 1,1–1,4 нг/мл (Cut-off) в процессе дифференциальной диагностики сепсиса чувствительность составляет 97 %, а специфичность – 78 %. Диагностическое значение C-реактивного белка, как биомаркера инфекции составляет 79 мг/л. Чувствительность C-реактивного белка составляет 71,8 %, специфичность 66,6 %, наиболее часто определяется для оценки эффективности лечебных мероприятий.
Проводится лабораторное определение маркеров иммунной недостаточности, которые имеют прямую взаимосвязь между выраженностью эндо- и аутотоксикоза и общей иммунодепрессией (тесты для выявления несостоятельности иммунной системы). Кроме того, выполняются диагностические молекулярные методы, использующие грамположительные (грамотрицательные) культуры крови и цельную кровь.
Концепция PRIO
- Predisposition (предрасположенность): возраст, генетическая предрасположенность, преморбидный анамнез, иммуносупрессивная терапия и др.
- Infection (инфекция): расположение очага инфекции, агрессивность возбудителя инфекции.
- Response (реакция): клиническая симптоматика инфекционного процесса (температура тела, частота сердечных сокращений, уровень лейкоцитоза, концентрация прокальцитонина, C-реактивного белка и др.).
- Organ dysfunction (органная дисфункция): для оценки органной дисфункции применяется шкала SOFA.
Сепсис необходимо дифференцировать от генерализованной формы сальмонеллеза, бруцеллеза, лимфогранулематоза, иных заболеваний, сопровождающихся продолжительной лихорадкой неправильного или гектического характера.
Лечение
Общими принципами лечения сепсиса являются:
- Стабилизация гемодинамики: инфузионная терапия, вазоактивные фармсредства.
- Коррекция и протезирование органной дисфункции.
- Контроль инфекции: санация очага инфекции, антибактериальная фармакотерапия:
- Санация очага инфекции предусматривает оперативное выполнение манипуляции для непосредственного доступа к предполагаемым очагам инфекции. Получение биоматериала из возможного очага инфекции должно быть произведено сразу после его обнаружения.
- В случае прогрессирования органной дисфункции рекомендуется стандартное обследование пациентов с органной недостаточностью на присутствие инфекции для наиболее раннего выявления тяжелого сепсиса и соответствующей реализации своевременной интенсивной терапии.
- Расположение инфекционного очага должно быть определено в течение первых 12-ти часов, и при необходимости выполнена его хирургическая санация.
- Пациентам с подтвержденной инфекцией или получавшим антибиотикотерапию в течение 24-х часов до госпитализации в лечебное учреждение периоперационная профилактика не проводится (проводится терапия).
- Введение антибиотиков для профилактики проводится в течение 1-го часа до рассечения кожи.
- Антибиотики с целью профилактики отменяются в течение 24-х часов (48 часов – для кардиохирургических пациентов) после завершения оперативного вмешательства.
Первоначально проводится незамедлительная эмпирическая антибактериальная терапия, после получения микробиологического анализа переходят к целенаправленной антибактериальной терапии с учетом антибиотикорезистентности выявленного возбудителя. Антибиотикотерапия прекращается после эрадикации и снижения титра инфекционного агента и снижения уровня прокальцитонина.
При выявлении кандидозной инфекции проводится терапия кандидемии антимикотическими фармсредствами (эхинокандины, азолы, полиены).
Профилактика тромбоза глубоких вен при помощи гепаринотерапии существенно влияет на результаты лечения больных с сепсисом.
Для профилактики возникновения стресс-язв в желудочно-кишечном тракте назначаются блокаторы H2-рецепторов и ингибиторы протонной помпы. Помимо того, необходимо учитывать, что, кроме перечисленных фармсредств, важное значение в профилактике образования стресс-язв отводится полноценному энтеральному питанию.
При возникновении почечной недостаточности, которая приводит к быстрому прогрессированию полиорганной недостаточности, проводится гемодиализ, перитонеальный диализ.
Прогноз и исход
Сепсис – это одна из основных причин летальных исходов в отделениях реанимации и интенсивной терапии. Среди причин смерти сепсис занимает 13-е место. Ежедневно в Западной Европе от него погибает более 1400 человек.
Прогноз при сепсисе имеет прямую зависимость от вирулентности микроорганизмов, состояния иммунной системы, своевременности и адекватности комплексной терапии.
В случаях, когда эти факторы относительно благоприятны, прогноз может быть благоприятным.
Во всех остальных случаях прогноз сомнительный – главным образом у больных преклонного возраста и при наличии отягощенного преморбидного анамнеза.
Сепсис быстро переходит в тяжелую степень тяжести, летальность при котором достигает 30–60%.
Сепсис повышает риск смерти в течение 5-ти лет после перенесенного септического эпизода.
Профилактика включает мероприятия по строгому соблюдению правил асептики при различных хирургических манипуляциях, проведение иммунопрофилактики стафилококковым анатоксином, противопневмококковой вакциной.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
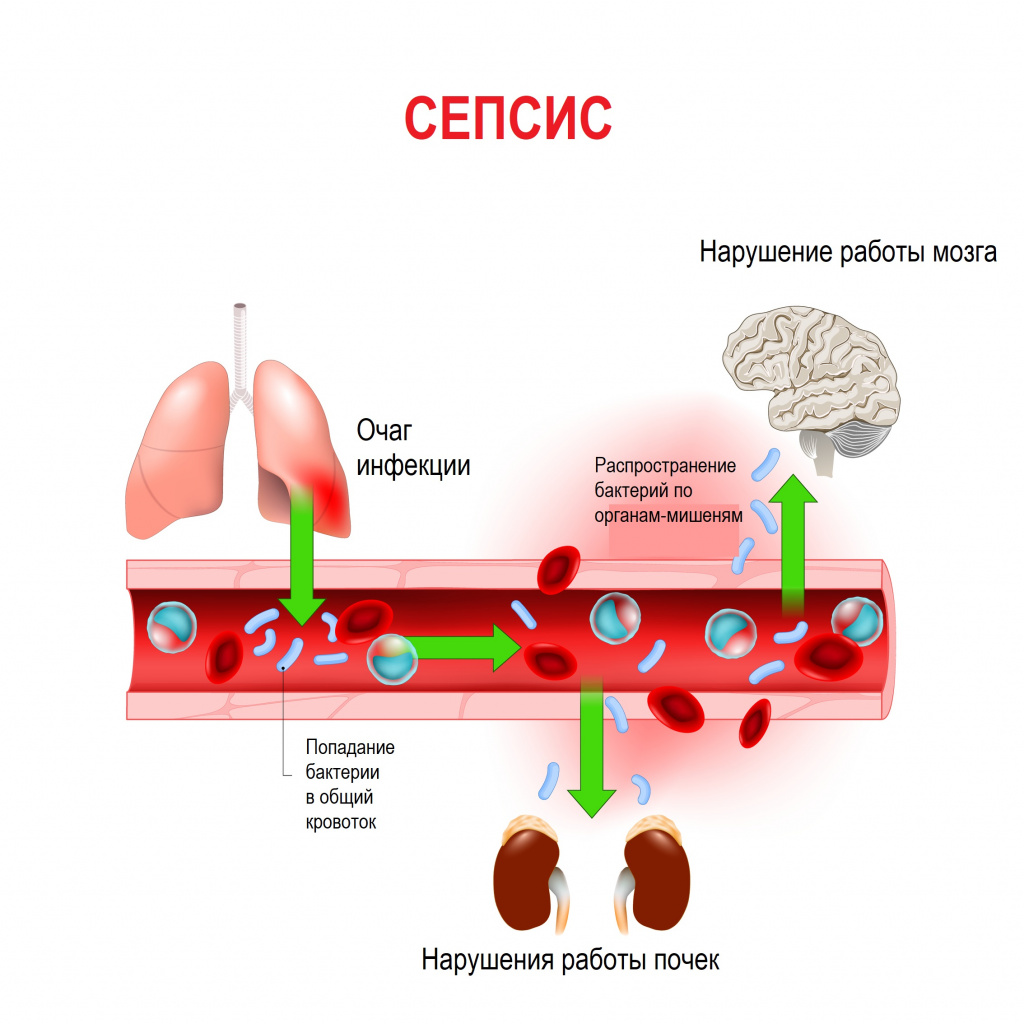
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
![Сепсис_дисфункция.jpg]()
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
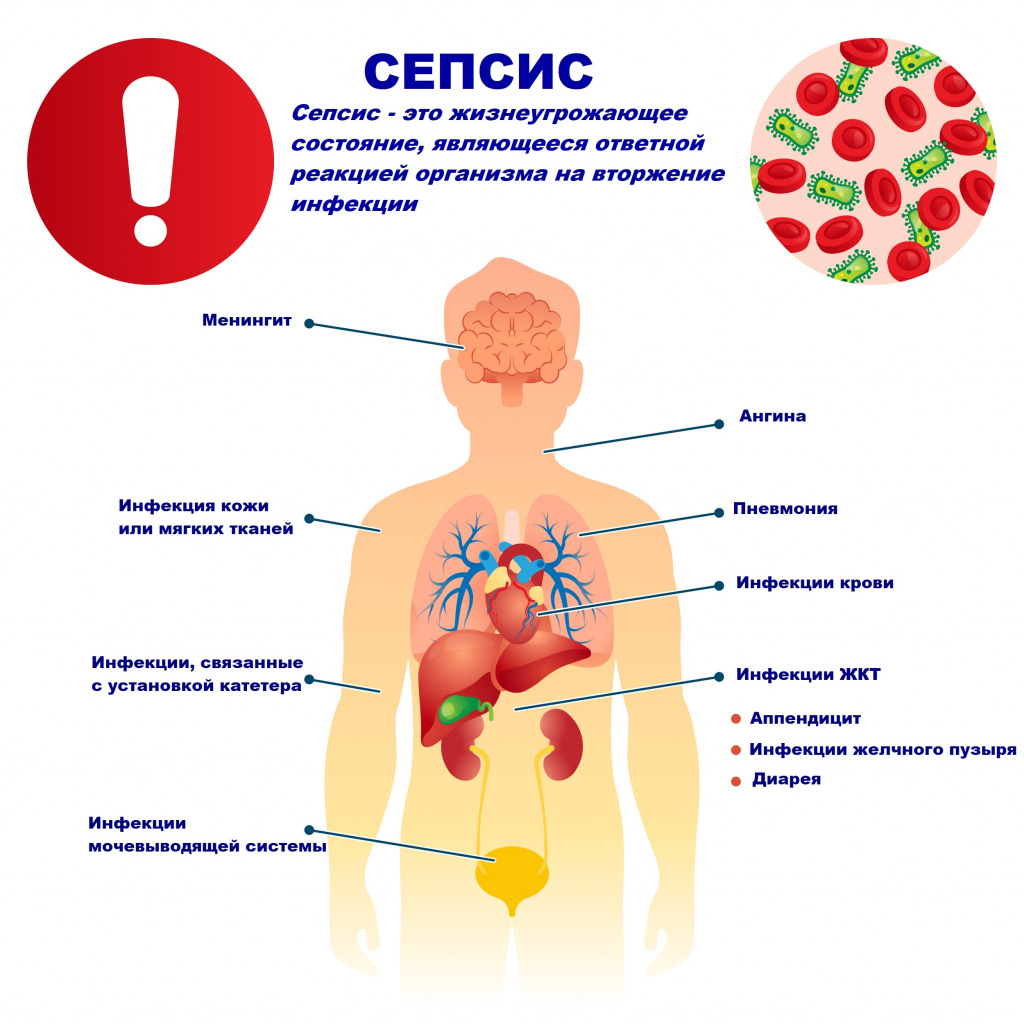
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
![Сепсис.jpg]()
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или 10%.
3. Тяжелый сепсис – сепсис, сочетающийся с полиорганной дисфункцией по двум и более органам, снижением артериального давления № 1700 Маркёры воспаления
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Читайте также: