Применение кислорода и озона кратко
Обновлено: 05.07.2024
Кислород – элемент VIA группы. Для него свойственны две аллотропные модификации с разными химическими формулами – кислород О2 и озон О3. Они отличаются не только составом молекул, но и различными характеристиками.
В конце XVIII века ученый Мартин Ван Марум провел эксперимент, в результате которого получил озон. Он через воздушное пространство пропускал электричество. Таким образом, образовался озон – это голубоватый газ с необычным запахом. Ученый предполагал, что полученный газ представляет собой электрическую материю.
Получение озона
Существует несколько способов получения молекул озона.
- Из кислорода воздуха при электрическом разряде
- 3О2 = 2О3 – 284 кДж
В промышленных условиях газ получают в озонаторах и отделяют фракционной перегонкой.
- 3О2 = 2О3 – 284 кДж
- Взаимодействие охлажденной концентрированной серной кислоты и пероксида бария
- 3H2SO4 + 3BaO2 = 3BaSO4 + O3 + 3H2O
Данной реакцией синтезируют озон в лабораториях.
- 3H2SO4 + 3BaO2 = 3BaSO4 + O3 + 3H2O
Физические свойства озона
Озон – бесцветный (в толстых слоях голубоватый) газ. Он почти в два раза тяжелее воздуха. Озон обладает специфическим запахом свежести.
- Температура сжижения -112˚С (газ приобретает оттенок индиго).
- Температура плавления -197˚С.
- Молярная масса озона – 48 г/моль.
Озон растворим в воде. Примеси позволяют растворяться еще быстрее. Если озон находится в состоянии газа, то он выступает в роли диамагнетика. Если озон – это жидкость, то проявляет свойства слабого парамагнетика.
Озон ядовит и губителен для бактерий. Его используют при обеззараживании воздуха и воды.
Химические свойства озона
Озон обладает сильными окислительными свойствами по сравнению с кислородом. Он реагирует с рядом веществ.
Если озон находится в состоянии газа, то реакция с сероводородом выглядит следующим образом:
H2S + O3 = SO2 + H2O
Озон способен взаимодействовать со ртутью при обычных условиях. В результате металл теряет блеск и способность липнуть к стеклу.
Токсичность озона
При умеренных концентрациях озон безвреден. Реакции с озоном характеризуются формированием свободных радикалов кислорода, которые губительны для организма при высоком содержании. Чрезмерное воздействие озона часто приводит к гибели. Озон особенно губителен для органов дыхания.
Озоновый слой в верхних слоях атмосферы
Озоновый слой – слой в верхней части атмосфера Земли, который состоит из бесцветного нестабильного газа. Он располагается на высоте 15-20 км над поверхностью планеты. Стратосфера – слой атмосферы, в котором содержится много озона.
Озон образуется в результате воздействия ультрафиолета на кислород. Слой газа задерживает все формы поступающей ультрафиолетовой коротковолновой радиации.
Озоновый экран защищает от вредного излучения, длина волн которого 290-320 нм. Это излучение может спровоцировать рак кожи. Озоновый слой появился на Земле около 600 млн лет назад в результате процесс фотосинтеза. Благодаря озоновому слою первые живые организмы смогли выйти из океана на сушу.
Дыры в озоновом слое
Озоновые дыры – локальное истощение озонового слоя. Самая большая озоновая дыра находится над Антарктидой. Если озоновый слой полностью исчезнет, то все живое на планете погибнет.
Озоновые дыры возникают по многим причинам, главная из которых – загрязнение окружающей среды. Озоновый слой разрушается под воздействием хлора, водорода, кислорода, брома и других продуктов сгорания. Выбросы фабрик, заводов и различных производств негативно влияют на выработку озона в верхних слоях атмосферы.
Озоновый слой может разрушить война. При испытании ядерного оружия выделяется огромное количество энергии и образуются окислы азота, которые разрушают озон. В период с 1952 по 1971 года при ядерных взрывах в атмосферу попало около 3 млн т окислов азота.
Реактивные самолеты выбрасывают окислы азота. Чем выше мощность турбореактивного двигателя, тем больше разрушающего вещества попадает в атмосферу. Ежегодно в воздух выбрасывается более 1 млн т соединений азота, из которых треть выбрасывают самолеты.
Защита озонового слоя
До 1989 года на производствах часто применялись галогенированные углеводороды, которые разрушают озоновый слой. Монреальская конвенция разработала программу по сокращению использования хлорфторуглеродов, которые быстро испарялись и достигали стратосферы. Они разлагаются на компоненты и разрушают озоновый слой. Из этих соединений раньше изготавливали аэрозоли, растворители и др.
Озоновые дыры произвольно создаются и исчезают. Это связано с некоторыми природными явлениями и даже климатическими особенностями. Газ озон образуется в результате воздействия ультрафиолета на кислород. Во время полярной ночи дыры образуются из-за того, что солнце не заходит несколько недель и ультрафиолет постоянно влияет на кислород. Во время полярного дня озоновый слой восстанавливается и воздействие ультрафиолета на живые организмы снижается.
Дыры могут формироваться в период активности Солнца. В результате этого они появляются и пропадают. Иногда это занимает несколько дней, реже растягивается на несколько месяцев.

Исторически так сложилось, что химический элемент и одно из простых веществ, образованных атомами этого элемента, имеют общее название — кислород. Поскольку между этими понятиями существует принципиальная разница, следует четко различать, о чем идет речь — о кислороде как о химическом элементе или о простом веществе.
Кислород как химический элемент
Самым первым химическим элементом, к изучению которого мы приступаем, является кислород. Как вы уже знаете, химический знак кислорода — О. Относительная атомная масса кислорода равна 16:
Позднее вы узнаете, какое строение имеет атом кислорода и чем он отличается от атомов других химических элементов.
Кислород как простое вещество
Простое вещество кислород существует в виде молекул. Молекула кислорода состоит из двух атомов химического элемента кислорода (рис. 73), поэтому химическая формула кислорода как простого вещества — O2.
Поскольку относительная атомная масса кислорода равна 16, то относительная молекулярная масса простого вещества кислорода равна:
![]()
Следовательно, молярная масса кислорода равна:
![]()
Как у всех газов, молярный объем кислорода при нормальных условиях равен:
![]()
История открытия кислорода
Кроме кислорода, существует еще одно простое вещество, молекулы которого состоят только из атомов кислорода. Это озон, молекула которого содержит три атома кислорода (рис. 74), его формула — О3.
При нормальных условиях озон представляет собой газ с резким раздражающим запахом. Он очень токсичен для всех живых организмов и поэтому используется вместо хлора для обеззараживания воды.
Небольшие количества озона образуются в воздухе во время грозы, а также в результате взаимодействия смолы хвойных деревьев с кислородом. Озон оказывает губительное действие на бактерии, поэтому лесной воздух (особенно в хвойных лесах) обладает целебным действием.
В небольших количествах озон образуется также при работе копировальных аппаратов и лазерных принтеров. Использовать такие приборы следует только в хорошо проветриваемых помещениях.
В верхних слоях атмосферы Земли (на высоте примерно 30—40 км) существует озоновый слой. Содержащийся в нем озон образуется из кислорода под воздействием солнечного излучения. Некоторые компоненты этого излучения губительны для живых организмов и растений на нашей планете, а озоновый слой поглощает их. Если бы не было озонового слоя, то жизнь на Земле постепенно бы прекратилась.
Многие ученые считают, что вещества, образующиеся в процессе производственной деятельности человека, разрушают озоновый слой. Это прежде всего фреоны — соединения, использующиеся в холодильных установках и дезодорантах, выбросы реактивных самолетов и ракет. Попадая в озоновый слой, эти вещества приводят к уменьшению его толщины или даже разрыву этого слоя — образованию так называемых озоновых дыр. В результате образования и увеличения размеров озоновых дыр могут наступить серьезные экологические катастрофы.
Применение кислорода
Кислород очень широко применяется в народном хозяйстве. На рисунке 75 приведены основные области применения кислорода. Главными потребителями кислорода являются металлургическая промышленность (выплавка стали), космическая техника (окислитель ракетного топлива), процессы обработки металлов (сварка и резка металлов).
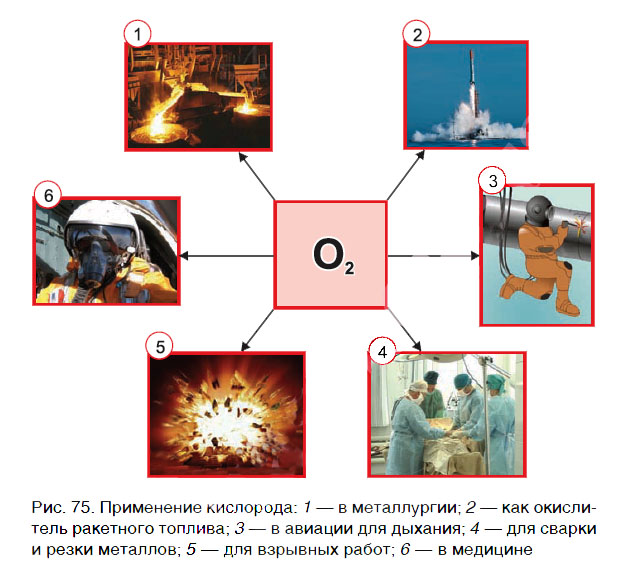
Краткие выводы урока:
- Химический элемент кислород образует два простых вещества — кислород О2 и озон О3.
- Когда говорят о кислороде как о химическом элементе, подразумевают атомы кислорода О.
- Когда говорят о кислороде как о простом веществе, подразумевают вещество, состоящее из молекул и имеющее формулу О2.

Средняя оценка: 4.5
Всего получено оценок: 268.
Средняя оценка: 4.5
Всего получено оценок: 268.
Озон – химическое газообразное вещество, которое является сильным окислителем. Какими свойствами обладает газ, и для каких целей его получают?
Общая информация

Рис. 1. Х. Ф. Шенбейн.
Формула озона – О3, то есть озон состоит из трех молекул кислорода. Озон – это аллотропное видоизменение кислорода. О3 – газ светло-синего цвета, с характерным запахом, нестойкий, токсичный. При температуре -111,9 градусов этот газ сжижается. Растворимость озона в воде больше, чем у кислорода: 100 объемов воды растворяют 49 объемов озона.

Рис. 2. Формула озона.
Это вещество образуется в атмосфере при электрических разрядах. Озоновый слой в стратосфере (25 км. от поверхности) поглощает ультрафиолетовое излучение, опасное для всех живых организмов.
Озон – сильный окислитель, даже более сильный, чем кислород. Он способен окислять такие металлы, как золото и платина.
Особая химическая активность озона объясняется тем, что его молекула легко распадается на молекулу кислорода и атомарный кислород. Образовавшийся атомарный кислород более активно реагирует с веществами, чем молекулярный.
Озон способен из раствора йодистого калия выделять йод:
Бумага, смоченная йодистым калием и крахмалом в воздухе, содержащем озон, синеет. Эта реакция используется для обнаружения озона.
В 1860 году ученые Эндрюс и Тэт экспериментально доказали при помощи стеклянной трубки с манометром, наполненной чистым кислородом, что при превращении кислорода в озон происходит уменьшение объема газа
Получение и применение озона
Получают озон при действии электрических разрядов на кислород в озонаторах.
Озон применяют для обеззараживания питьевой воды, для обезвреживания промышленных сточных вод, в медицине – в качестве дезинфицирующего средства. Также как и хлорирование, озонирование обладает обеззараживающим эффектом, но его плюсом является то, что при использовании озона в обработанной воде не образуется токсинов. Озон также эффективно борется с плесенью и бактериями.

Рис. 3. Озонирование.
При остром отравлении озон поражает органы дыхания, раздражает слизистые глаз, вызывает головную боль. Токсичность озона резко возрастает при одновременном воздействии оксидов азота.
Что мы узнали?
Озон – газ, который был обнаружен в конце XVIII века, а свое современное название получил только в середине XIX века. В отличие от кислорода этот газ имеет характерный запах и отличается светло-синим цветом.
Кислород может существовать в виде двух аллотропных видоизменений: кислород О2 и озон О3.
При сравнении физических свойств кислорода и озона целесообразно вспомнить, что это газообразные вещества, различающиеся по плотности (озон в 1,5 раза тяжелее кислорода) , температурам плавления и кипения. Озон лучше растворяется в воде.
Кислород в нормальных условиях — газ, без цвета и запаха, озон — газ голубого цвета с характерным резким, но приятным запахом.
Есть отличия и в химических свойствах.
Озон химически активнее кислорода. Активность озона объясняется тем, что при его разложении образуется молекула кислорода и атомарный кислород, который активно реагирует с другими веществами. Например, озон легко реагирует с серебром, тогда как кислород не соединяется с ним даже при нагревании:
6Ag+O3=3Ag2O
Но в то же время и озон и кислород реагируют с активными металлами, например с калием К.
Получение озона происходит по следующему уравнению:
3O2=2O3- теплота
Реакция идет с поглощением энергии при прохождении электрического разряда через кислород, например во время грозы, при сверкании молнии. Обратная реакция происходит при обычных условиях, так как озон — неустойчивое вещество. В природе озон разрушается под действием газов, выбрасываемых в атмосферу, например фреонов, в процессе техногенной деятельности человека.
Результатом является образование так называемых озоновых дыр, т. е. разрывов в тончайшем слое, состоящем из молекул озона.
Кислод использут всюду - в промышленности ( полддувка в домны, выжигание серы в цветной металлургии) . Для медицинских целей - некоторым людям тяжело дышать без баллона кислорода.
Озон - сильнейший окислитель. Применяется для обеззараживания воды ( в развитых странах ), для аналитического органического анализа и еще 1000 применений! ! !
Озоном, отбеливают доски для мебели и очищают от запахов помещения, обезвреживают питьевую воду и сточные воды, озон одно из составляющих благотворного воздействия на людей когда они находятся в сосновом лесу
Как бы всё!
Озон — аллотропное состояние кислорода состоящий из трёхатомных молекул О3, на цвет голубоватый, образуется в атмосфере при электрических разрядах, в лабораторных условиях может быть получен пропусканием т ихих электрических разрядов на кислород.
Основное применение в органическом синтезе других веществ, а также рассматривается как вариант использования жидкого озона для окисления топлива в космических ракетах.

Что такое озон
Это аллотропное состояние кислорода, образование озона наблюдается во всех химических процессах, в результате которого выделяется атомарный кислород.
В лабораторных условиях озон можно получить не только пропусканием разрядов через кислород, но действием быстрых электронов и протонов, рентгеновских и ультрафиолетовых лучей.
При пропускании электрических искр через кислород или воздух появляется характерный запах, знакомый каждому, кто имел дело с электростатической машиной или индукционной катушкой. Причиной этого запаха является образование нового газообразного вещества — озона.
Так как озон может быть получен из совершенно чистого сухого кислорода при действии электрических искр, то отсюда следует, что озон состоит только и кислорода и представляет собой особое видоизменение этого элемента.
Физические свойства, получение озона

Молекулярный вес озона равен 48, в то время как молекулярный вес кислорода 32. Атомный вес кислорода равен 16; следовательно, молекула озона состоит из трех атомов кислорода, а молекула кислорода только из двух таких же атомов.
Таким образом, кислород в свободном состоянии может существовать в виде двух аллотропических видоизменений: обыкновенного кислорода О2 и озона.
Для получения озона пользуются действием тихих электрических разрядов на кислород. Приборы, служащие для этой цели,, носят название озонаторов. На рис. 2 изображен озонатор состоящий в основном из двух стеклянных трубок, вставленных одна в другую.
Кислород медленно просасывается между трубками. Во внутреннюю трубку наливают разбавленный раствор серной кислоты, и весь прибор помещают в стакан с тем же раствором. В растворы погружают провода от индукционной катушки.
Таким образом, растворы являются электродами и в тоже время служат для охлаждения газа. При работе катушки в пространстве между стенками трубок происходит тихий электрический разряд. Выходящий из прибора кислород содержит несколько процентов озона. Чем ниже температура, тем больше получается озона.
Озон что это
Озон можно отделить от кислорода сильным охлаждением, причем озон сгущается в синюю жидкость, кипящую при —112°. Жидкий озон легко взрывается.
Растворимость озона в воде значительно больше, чем растворимость кислорода: 100 объемов воды при 0° растворяют 49 объемов озона.
При обыкновенной температуре озон довольно устойчив, но. при нагревании легко разлагается, снова превращаясь в кислород. Распад озона сопровождается выделением тепла и увеличением объема в полтора раза, так как из каждых двух молекул озона получаются три молекулы кислорода:
В химическом отношении озон отличается от кислорода более сильной окислительной способностью: при действии озона блестящая серебряная пластинка быстро чернеет, покрываясь слоем перекиси серебра Ag2O2, сернистые соединения металлов окисляются в соли серной кислоты.
Бумага, смоченная скипидаром, воспламеняется; многие красящие вещества обесцвечиваются. При этом молекула озона теряет один атом кислорода и озон переходит в обыкновенный кислород.
Из раствора йодистого калия озон выделяет иод:
Если поместить в воздух, содержащий озон, бумажку, смоченную раствором йодистого калия и крахмальным клейстером, то она тотчас же синеет. Этой реакцией пользуются для открытия озона.
Как сильный окислитель, озон убивает бактерии и потому применяется для обеззараживания воды и для дезинфекции воздуха.
Озон постоянно образуется в небольших количествах при электрических разрядах в атмосфере. Образование озона может происходить также при различных процессах окисления, например при окислении влажного фосфора, скипидара, смолистых веществ и т. п.
Последним обстоятельством объясняется присутствие озона в воздухе хвойных лесов; этот воздух является особенно полезным для здоровья, так как не содержит бактерий.
Открытие озона
В 1850 г. параллельно основной работе, он выяснил, что озон может реагировать с органическими веществами проявляя себя как окислитель.
Благодаря своим дезинфицирующим свойства был применен в 1898 году в Франции. В небольшом на то время городке Бон Вояж был построен завод для дезинфекции воды реки Вазюби.
На территории России завод по озонированию был запущен в Санкт-Петербурге в 1911 году.
Большое применение озона получил в годы Первой мировой войны как антисептическое средство.
В настоящее время с появлением надежных энергосберегающих генераторов озона возросло применение для очистки воды, что хорошо применяется на территории США и по всей Европе.
Химические свойства озона
Образование озона проходит по обратимой реакции:
3O2 + 68kcal/mol(285kJ/mol) → 2О3
Молекула О3 неустойчива и при достаточных концентрациях в воздухе при нормальных условиях самопроизвольно за несколько десятков минут превращается в O2 с выделением тепла.
Повышение температуры и понижение давления увеличивают скорость перехода в двухатомное состояние. При больших концентрациях переход может носить взрывной характер.
Контакт озона даже с малыми количествами органических веществ, некоторых металлов или их окислов резко ускоряет превращение.
В присутствии небольших количеств азотной кислоты озон стабилизируется, а в герметичных сосудах из стекла, некоторых пластмасс или чистых металлов озон при низких температурах (−78 °С) практически не разлагается.
Озон — очень сильный окислитель, намного более реакционноспособный, чем двухатомный кислород. Окисляет почти все металлы (за исключением золота, платины и иридия) до их высших степеней окисления (после некоторого поверхностного окисления довольно хорошо противостоят действию озона Ni, Cu, Sn). Озон окисляет многие неметаллы. Продуктом реакции в основном является кислород.
Озон повышает степень окисления оксидов:
Эта реакция сопровождается хемилюминесценцией. Диоксид азота может быть окислен до азотного ангидрида:
Не реагирует с молекулярным азотом при комнатной температуре, но при 295°С озон вступает с ним в реакцию:
Озон реагирует с углеродом при нормальной температуре с образованием диоксида углерода:
Озон не реагирует с аммониевыми солями, но реагирует с аммиаком с образованием нитрата аммония:
Озон реагирует с водородом с образованием воды и кислорода:
Озон реагирует с сульфидами с образованием сульфатов:
С помощью озона можно получить серную кислоту как из элементарной серы, так и из диоксида серы и сероводорода:
В газовой фазе озон взаимодействует с сероводородом с образованием диоксида серы:
В водном растворе проходят две конкурирующие реакции с сероводородом, одна с образованием элементарной серы, другая с образованием серной кислоты:
Все три атома кислорода в озоне могут реагировать по отдельности в реакции хлорида олова с соляной кислотой и озоном:
Обработкой озоном раствора иода в холодной безводной хлорной кислоте может быть получен перхлорат иода(III):
Твёрдый перхлорат нитрония может быть получен реакцией газообразных NO2, ClO2 и O3:
Озон может участвовать в реакциях горения, при этом температуры горения выше, чем с двухатомным кислородом:
Озон может вступать в химические реакции и при низких температурах. При 77 K (−196 °C, температура кипения жидкого азота), атомарный водород взаимодействует с озоном с образованием гидропероксидного радикала с димеризацией последнего:
Озон может образовывать неорганические озониды, содержащие анион O3 − . Эти соединения взрывоопасны и могут храниться только при низких температурах. Известны озониды всех щелочных металлов (кроме франция). KO3, RbO3 и CsO3 могут быть получены из соответствующих супероксидов:
Озонид калия может быть получен и другим путём из гидроксида калия[13]:
NaO3 и LiO3 могут быть получены действием CsO3 в жидком аммиаке NH3 на ионообменные смолы, содержащие ионы Na + или Li + :
Обработка озоном раствора кальция в аммиаке приводит к образованию озонида аммония, а не кальция:
Озон может быть использован для удаления железа и марганца из воды с образованием осадка (соответственно гидроксида железа(III) и диоксигидрата марганца), который может быть отделён фильтрованием:
В кислых средах окисление марганца может идти до перманганата.
Озон превращает токсичные цианиды в менее опасные цианаты:
Озон может полностью разлагать мочевину:
Взаимодействие озона с органическими соединениями с активированным или третичным атомом углерода при низких температурах приводит к соответствующим гидротриоксидам.
Реакция озона с непредельными соединениями с образованием органических озонидов находит применение в анализе органических веществ.
Реакции озона с другими веществами
Озон реагирует в водном растворе с сероводородом образуя серную кислоту
и элементарной серы
Реагирует с углеродом при нормальных условиях
Озон применение для чего нужен
Давно рассматривается применение озона в качестве высокоэнергетического и вместе с тем экологически чистого окислителя в ракетной технике. Общая химическая энергия, освобождающаяся при реакции сгорания с участием озона, больше, чем для простого кислорода, примерно на одну четверть 719 ккал/кг).
Больше будет, соответственно, и удельный импульс. У жидкого озона большая плотность, чем у жидкого кислорода (1,35 и 1,14 г/см³ соответственно), а его температура кипения выше (−112 °C и −183 °C соответственно), поэтому в этом отношении преимущество в качестве окислителя в ракетной технике больше у жидкого озона.
Однако препятствием является химическая неустойчивость и взрывоопасность жидкого озона с разложением его на O и O2, при котором возникает движущаяся со скоростью около 2 км/с детонационная волна и развивается разрушающее детонационное давление более 3·10 7 дин/см² (3 МПа), что делает применение жидкого озона невозможным при нынешнем уровне техники, за исключением использования устойчивых кислород-озоновых смесей (до 24 % озона).
Преимуществом подобной смеси также является больший удельный импульс для водородных двигателей, по сравнению с озон-водородными. На сегодняшний день такие высокоэффективные двигатели, как РД-170, РД-180, РД-191.
Также разгонные вакуумные двигатели вышли по УИ на близкие к предельным параметры, и для повышения удельного импульса необходимо найти возможность перейти на новые виды топлива.
Жидкий озон при низких температурах (в жидком азоте) также иногда применяется в органическом синтезе для мягкого разрыва двойной углерод-углеродной связи.
Что мы узнали о озоне?
Как пахнет озон?
Как образуется озон?
Озон образуется во многих процессах, сопровождающихся выделением атомарного кислорода, например при разложении перекисей, окислении фосфора и т. п.
Какая плотность озона?
Сколько атомов кислорода содержится в молекуле озона?
В молекуле озона — три атома кислорода, а в молекуле кислорода — два атома кислорода.
Вы читаете, статья на тему Озон
Похожие страницы:
КИСЛОРОД анализ О, Качественная реакция на Кислород Индигокармин Индиго-5,5′-дисульфокйслоты динатриевая соль C16H8O8N2Na2S2, ММ 466,36 Синие кристаллы (порошок); малорастворим в воде. Легко.
КИСЛОРОД ОБЩЕЕ Этого мнения, при всем уважении к кислороду, автор не разделяет. Не надо приписывать кислороду того, что он дать.
Кислород (Oxygenium) Ат. вес 16. Из всех элементов, встречающихся на земле, кислород является наиболее распространенным. В свободном состоянии он находится.
Азотистая кислота HNO2 Если нагревать калиевую или натриевую селитру, то они теряют часть своего кислорода и переходят в соли азотистой.
Общая характеристика группы кислорода Элемент Символ Атомный вес Порядковый номер Распределение электронов По слоям Кислород . . О 16 8.
Простые эфиры Простыми эфирами называются органические соединения, молекулы которых состоят из двух углеводородных радикалов, связанных с атомом кислорода. Примером может.
Читайте также:

