Оксигемоглобин это в биологии 8 класс кратко
Обновлено: 04.07.2024
Смотреть что такое ОКСИГЕМОГЛОБИН в других словарях:
ОКСИГЕМОГЛОБИН
см. Гемоглобин, Кровь, Дыхание.
ОКСИГЕМОГЛОБИН
ОКСИГЕМОГЛОБИН
оксигемоглобин сущ., кол-во синонимов: 2 • гематоглобулин (1) • гемоглобин (6) Словарь синонимов ASIS.В.Н. Тришин.2013. . Синонимы: гематоглобулин, гемоглобин. смотреть
ОКСИГЕМОГЛОБИН
ОКСИГЕМОГЛОБИН, о к с и г е н и р о в а н н ы й гемоглобин, НbО2, продукт обратимого присоединения кислорода к "восстановленному" гемоглобину (НЬ); п. смотреть
ОКСИГЕМОГЛОБИН
Оксигемоглобин — см. Гемоглобин, Кровь, Дыхание.
ОКСИГЕМОГЛОБИН
Облог Облик Облиго Обл Обкос Обком Обилие Обелиск Обгон Носилки Носик Нос Ном Нолик Нок Нло Нимб Нил Никс Николо Нии Неолог Неоком Немо Негибко Небо Мосол Моск Моос Монолог Моноблок Моно Монгол Монго Молоко Молескин Моки Могол Много Млеко Мкс Мис Миолог Миоглобин Мио Минск Минос Милон Мило Милин Миленок Миколог Мик Миелин Миг Мес Менсол Мениск Мелос Мелон Мелок Мелко Мелис Мел Меконг Мег Лоск Лосенок Лоно Лонг Ломонос Ломик Лом Локон Локо Лок Логос Логин Логико Логик Лог Лобок Лобио Лобик Лобие Лоб Лисенок Лис Лион Линкос Линк Лимон Лиминг Лимб Лик Лиго Лесогон Лесник Лесин Лесик Леон Ленск Леникс Лен Лек Легко Легион Кси Косо Косно Космолог Кос Консоме Конго Кон Комс Комингс Коми Комби Ком Колос Колон Коломбо Колоб Коло Колесо Колено Кол Кобол Кобе Клон Клион Клио Клин Клим Клеом Клен Кисло Кислин Кинолог Кино Кинг Кимоно Ким Килоом Кило Килим Кил Кен Кеб Кгб Искони Иск Ионол Ион Иомен Иол Инок Инко Инк Илим Икс Икос Иго Игил Игемон Ибсен Иблис Ибис Ибикон Енол Емко Елкин Елико Госкино Гос Гонг Гон Гомон Гомолог Гомик Голосок Голосник Голос Голо Голик Гол Гоблин Гоби Гномик Гном Глог Глобин Гликоген Глеб Гко Гинкго Гинеколог Гимн Гик Гибко Геолого Геолог Геобиолог Ген Гемоглобин Гемин Гемблинг Гем Гелиос Гелио Геликон Гекс Геб Босиком Бонмо Бон Бологое Бокс Боком Бок Боинг Боек Богомол Богомил Бог Блокинг Блок Блогинг Блог Блинок Блин Блик Блеск Бис Биос Биом Биолого Биолог Биокол Био Облом Обломок Обмен Обмин Обмол Обнос Обносок Обои Обок Обол Обсе Огиенко Огон Огонек Бином Окб Окисел Окно Око Бинго Бимс Оксим Олег Биг Бен Белоног Бегом Бегло Бег Олеин Бек Бекон Белг Бес Бигос Бикс Билон Оксиген Оксигемоглобин Бинк Около Окоем. смотреть
ОКСИГЕМОГЛОБИН
оксигемоглоби́н (см. окси. ) соединение гемоглобина с кислородом, образующееся при прохождении крови по капиллярам органов дыхания и легко распадающе. смотреть
ОКСИГЕМОГЛОБИН
1) Орфографическая запись слова: оксигемоглобин2) Ударение в слове: оксигемоглоб`ин3) Деление слова на слоги (перенос слова): оксигемоглобин4) Фонетиче. смотреть
ОКСИГЕМОГЛОБИН
(оксигенированный гемоглобин HbO2) соединение гемоглобина с кислородом. Переносит о2 от органов дыхания к тканям, определяет ярко-красный цвет артериальной крови. относительное содержание о. в крови зависит от парциального давления кислорода. При высоком парциальном давлении о2 (в капиллярах легких) гемоглобин (Hb) на 95 % находится в форме Hbо2. При прохождении крови по капиллярам тканей о. распадается с выделением кислорода. Гемоглобин отдает тканям свой кислород и затем забирает углекислый газ (Со2), выделяющийся в процессе жизнедеятельности тканей. Соединение гемоглобина с углекислым газом называется карбгемоглобином (HbСо2). в капиллярах легких карбгемоглобин легко распадается на Hb и Со2. См. также Карбоксигемоглобин, Оксид углерода. смотреть
ОКСИГЕМОГЛОБИН
oxyhemoglobin - оксигемоглобин.Форма гемоглобина , образующаяся при оксигенации, т.е. присоединение к одному из гемов молекулы кислорода; т. смотреть
ОКСИГЕМОГЛОБИН
ОКСИГЕМОГЛОБИН, соединение ГЕМОГЛОБИНА из ЭРИТРОЦИТОВ (красных кровяных клеток) с кислородом, поступающим из легких. В этой форме кислород в крови пере. смотреть
ОКСИГЕМОГЛОБИН
Ударение в слове: оксигемоглоб`инУдарение падает на букву: иБезударные гласные в слове: оксигемоглоб`ин
ОКСИГЕМОГЛОБИН
(oxyhaemoglobin) ярко-красное вещество, образующееся благодаря обратимому соединению содержащегося в эритроцитах пигмента гемоглобина с кислородом. Оксигемоглобин является той формой, в которой кислород переносится из легких в различные ткани организма, где затем происходит его освобождение. Для сравнения: Метгемоглобин. смотреть
ОКСИГЕМОГЛОБИН
оксигемоглобин [см. окси. ] - соединение гемоглобина с кислородом, образующееся при прохождении крови по капиллярам органов дыхания и легко распадающееся в тканях тела, благодаря чему осуществляется перенос кислорода из органов дыхания к тканям.
ОКСИГЕМОГЛОБИН
оксигемоглоби/н, -а Синонимы: гематоглобулин, гемоглобин
ОКСИГЕМОГЛОБИН
(Окси- + Гемоглобин;. син. гемоглобин оксигенированный)форма гемоглобина, в которой он обратимо соединен с кислородом и обеспечивает перенос последнего. смотреть
ОКСИГЕМОГЛОБИН
гемоглобин, связанный с кислородом; переносит кислород от органов дыхания к тканям, определяет ярко-красный цвет артериальной крови. Синонимы: гематог. смотреть
ОКСИГЕМОГЛОБИН
оксигемоглобин (окси- + гемоглобин; син. гемоглобин оксигенированный) — форма гемоглобина, в которой он обратимо соединен с кислородом и обеспечивает п. смотреть
ОКСИГЕМОГЛОБИН
(окси- + гемоглобин; син. гемоглобин оксигенированный) форма гемоглобина, в которой он обратимо соединен с кислородом и обеспечивает перенос последнего кровью от легких к тканям. смотреть
ОКСИГЕМОГЛОБИН
ОКСИГЕМОГЛОБИН, гемоглобин, соединенный с кислородом; переносит кислород от органов дыхания к тканям, определяет ярко-красный цвет артериальной крови. смотреть
ОКСИГЕМОГЛОБИН
ОКСИГЕМОГЛОБИН - гемоглобин, соединенный с кислородом; переносит кислород от органов дыхания к тканям, определяет ярко-красный цвет артериальной крови.
. смотреть
ОКСИГЕМОГЛОБИН
ОКСИГЕМОГЛОБИН , гемоглобин, соединенный с кислородом; переносит кислород от органов дыхания к тканям, определяет ярко-красный цвет артериальной крови. смотреть
ОКСИГЕМОГЛОБИН
ОКСИГЕМОГЛОБИН, гемоглобин, соединенный с кислородом; переносит кислород от органов дыхания к тканям, определяет ярко-красный цвет артериальной крови. смотреть
ОКСИГЕМОГЛОБИН
сущ. муж. родаоксигемоглобін -у
ОКСИГЕМОГЛОБИН
оксигемоглоб'ин, -аСинонимы: гематоглобулин, гемоглобин
ОКСИГЕМОГЛОБИН
- гемоглобин, соединенный с кислородом; переносит кислородот органов дыхания к тканям, определяет ярко-красный цвет артериальнойкрови.
ОКСИГЕМОГЛОБИН
(2 м)Синонимы: гематоглобулин, гемоглобин
ОКСИГЕМОГЛОБИН
оксигемоглобинСинонимы: гематоглобулин, гемоглобин
ОКСИГЕМОГЛОБИН
氧络血红朊Синонимы: гематоглобулин, гемоглобин
ОКСИГЕМОГЛОБИН
Начальная форма - Оксигемоглобин, винительный падеж, единственное число, мужской род, неодушевленное
Красный пигмент крови человека, сложный железосодержащий белок (хромопротеин, состоящий из глобина и четырех гемов с двухвалентным железом в центре каждого) – гемоглобин (Hb), соединяясь с молекулярным кислородом (O2) в легких, образует оксигенированную форму – оксигемоглобин (HHbO2). Оксигемоглобин, приобретая уникальные свойства и обеспечивая дыхание, как одно из элементарных проявлений жизни, продолжает саму жизнь организма. Например, достаточно ввести окись углерода вместо кислорода или нарушить потребление О2 клетками при попадании цианидов (солей синильной кислоты), которые ингибируют ферментные системы тканевого дыхания, как тут же наступает гибель организма.

Дыхание, на первый взгляд, кажется совсем простым процессом. Между тем, оно основано на взаимодействии многих компонентов, составляющих гигантскую молекулу красного пигмента крови – хромопротеина гемоглобина, который, в свою очередь, отличается многообразием производных, где из их числа несомненный интерес вызывает оксигемоглобин. Итак, оксигемоглобин образуется в легких путем соединения сложного железосодержащего белка гемоглобина с кислородом, поступающим с вдыхаемым воздухом.
Образование и распад оксигемоглобина
В спокойном состоянии тканям человеческого тела достаточно около 0,2 л кислорода в одну минуту, но все меняется при физической нагрузке и чем она интенсивнее, тем больше необходимого для дыхания газа запрашивают ткани. Для удовлетворения их нужд потребность в кислороде может увеличиваться в 10 – 15 раз и составлять до 2, а то и 3 литров О2 в одну минуту. Однако газообразный кислород в данном количестве никак не сможет пробраться в ткани, поскольку он почти не растворим и в воде, и в плазме, то есть, этот элемент в ткани должен доставить какой-то белок, способный соединиться с ним и решить задачу транспорта.

Кровь, как биологическая среда, реализует свои функциональные обязанности по обеспечению дыхания за счет присутствия в ней сложного содержащего железо протеина – гемоглобина, физиологическая роль которого, как транспортного средства кислорода, базируется на способности Hb связывать и отдавать О2 в корреляции с концентрацией (парциальным давлением – P) данного газа в крови. Образование оксигемоглобина осуществляется в паренхиме легких, куда кислород прибывает при дыхании из воздуха окружающей среды.
Процесс образования HHbO2 происходит в доли секунды (0,01 с), поскольку кровь в легких задерживается всего-то на полсекунды. Схематично и коротко образование оксигемоглобина можно представить в следующем виде:
- Попадая в капиллярные сосуды легких, кровь обогащается кислородом, то есть, красный кровяной пигмент к своим 4 гемам присоединяет кислород – идет реакция окисления (оксигенации);
- Кислород связывается с гемами хромопротеина при помощи координационных связей феррума (железо – Fe) и, не изменяя в данном случае валентности последнего (в геме валентность железа всегда – II), переводит его (Hb) в несколько иное состояние;
- Гем железосодержащего протеина представляет собой активный центр, с его помощью хромопротеин в результате вышеуказанной реакции переходит в непрочный комплекс – оксигенированный гемоглобин (HHbO2), который, находясь в красных кровяных тельцах – эритроцитах, с током крови доставляется к клеткам тканей, чтобы через распад оксигемоглобина и выделения в процессе диссоциации кислорода, обеспечить их дыхание.
Таким образом, результатом реакции оксигенации становится образование оксигемоглобина, подкисление биологической жидкости, снижение ее щелочного резерва, то есть, ее умения связывать углекислоту (СО2), которое, разумеется, на тот момент снижается.
Железосодержащий протеин, насытившись в легочной паренхиме кислородом и приобретя оксигенированную форму, уносит О2 к тканям, в капиллярных сосудах которых его концентрация в крови резко понижена. Там происходит распад оксигемоглобина (диссоциация), кислород уходит на тканевое дыхание, гемоглобин забирает отработанный углекислый газ, превращаясь в другую физиологическую модель – карбогемоглобин (HHbCO2), и в этом качестве отправляется в главный орган дыхания, чтобы обменять CO2 на очередную порцию необходимого организму газа.

Кривая образования и распада (диссоциации) оксигемоглобина
Агентом, гарантирующим быстрое насыщение железосодержащего белка кислородом (образование оксигемоглобина), выступает высокое напряжение (парциальное давление) О2 в легочных альвеолах (порядка 100 мм рт. ст.).
Корреляцию между степенью насыщения красного кровяного пигмента кислородом и парциальным давлением O2 (PO 2) выражают в виде S-образной кривой (сигмоиды), которую называют кривой диссоциации оксигемоглобина.

Свойственная красному кровяному пигменту S-образная (сигмоида) кривая диссоциации оксигемоглобина свидетельствует о том, что контактирование первой молекулы О2 с одним из гемов Hb открывает путь присоединению других молекул элемента остальными тремя гемами. Кривой насыщения железосодержащего белка кислородом принадлежит немалая физиологическая значимость – S-образная конфигурация позволяет крови обогатиться данным газом при изменениях концентрации кислорода в биологической жидкости в довольно обширных интервалах. К примеру, не следует ожидать таких особенных расстройств дыхательной функции крови, как выраженное кислородное голодание (гипоксия), при подъеме на высоту до 3,5 км над уровнем моря или во время перелета на самолете. Хотя PO 2 во вдыхаемом воздухе сильно понизится, концентрация кислорода в крови будет находиться на достаточно высоком уровне, чтобы обеспечить насыщение Hb данным газом. На это указывает и отлогий график формирования и распада оксигемоглобина на верхнем его отрезке (верхний отрезок кривой свидетельствует о течении процесса насыщения О2 красного пигмента крови в легочной паренхиме и находится в пределах 75 – 98%).
Кривая диссоциации оксигемоглобина может быть разделена на 4 отрезка, каждому их которых соответствует определенный период образования оксигемоглобина (зависимость скорости насыщения хромопротеина кислородом от парциального давления газа в крови):
- 0 – 10 мм рт. ст. – гемоглобин не спешит насыщаться;
- 10 – 40 мм рт. ст. – оксигенация резко ускоряется (стремительный подъем кривой), доходя до 75%;
- 40 – 60 мм рт. ст. – оксигенация заметно замедляется, потихоньку добираясь до 90%;
- Значения PO2 пересекают отметку 60 мм рт. ст. – насыщение идет слабо (линия лениво ползет вверх). Однако кривая медленно продолжает стремиться к отметке 100%, но, так и не достигнув ее, останавливается на уровне 96 – 98%. Кстати, и такие показатели насыщения Hb кислородом отмечаются только у молодых и здоровых людей (PO2 артериальной крови ≈ 95 мм рт. ст., легочных капилляров – ≈ 100 мм рт. ст.). С возрастом дыхательные способности крови снижаются.
Несовпадение парциального давления кислорода артериальной крови и смеси газов в альвеолах легких трактуется:
- Некоторыми разногласиями между интенсивностью тока крови и вентилированием разных отделов главного органа дыхания – легких;
- Притоком незначительного объема крови из бронхиальных вен в венозные сосуды легких (шунтирование), где, как известно, течет артериальная кровь;
- Прибытием доли крови из коронарных вен в левый желудочек сердца посредством тебезиевых вен (вены Тебезия-Вьессена), в которых проходимость возможна в обоих направлениях.
Между тем, причины, вследствие которых кривая образования и диссоциации оксигемоглобина приобрела сигмоидную форму, пока остаются не до конца выясненными.
Смещение кривой диссоциации оксигемоглобина
Но кривая диссоциации оксигемоглобина, о которой идет речь выше, справедлива, если в организме все нормально. В других ситуациях график может сдвигаться в ту или иную сторону.
В числовом выражении сродство гемоглобина к кислороду обозначается величиной P50 – напряжение полунасыщения красного пигмента крови кислородом или иными словами: парциальное напряжение О2, при котором 50% Hb пребывает в форме оксигемоглобина (оптимальные условия: рН – 7,4, tº – 37ºC). Нормальные значения этого показателя в артериальной крови приближаются к величине 34,67 гПа (26 мм рт. ст.). Смещение графика вправо указывает на то, что способность красного кровяного пигмента соединяться с кислородом снижается, что, естественно, увеличивает значения P50. И, наоборот – смещение кривой влево говорит об увеличении сродства этого хромопротеина к кислороду (↓P50.).

Ходу сигмоиды помогают некоторые факторы, повышающие обогащение крови кислородом и таким образом участвующие в тканевом дыхании, поэтому названные вспомогательными:
- Повышение водородного показателя (pH) крови (эффект Бора), поскольку способность гемоглобина присоединять кислород связана с водородным показателем (pH) данной биологической среды (гемоглобин представляет одну из четырех буферных систем и влияет на регуляцию кислотно-основного баланса, поддерживая pH на нужном уровне: 7,36 – 7,4). Следовательно, чем выше водородный показатель, тем активнее ведет себя гемоглобин в отношении кислорода и наоборот – снижение pH отнимает возможности хромопротеина присоединять кислород, например: ↓pH до 7,2 заставит график отклоняться вправо (≈ на 15%), ↑pH до 7,6 передвинет кривую диссоциации оксигемоглобина влево (≈ на 15%);
- Отделение углекислого газа от карбогемоглобина в легких и выход СО2 с выдыхаемым воздухом (эффект Бора-Вериго) на фоне повышения водородного показателя создает условия для жадного насыщения гемоглобина кислородом (образование оксигемоглобина в легких);
- Возрастание уровня значимого для обмена фосфата – 2,3-дифосфоглицерата (2,3-ДФГ), содержание которого в крови меняется в зависимости от условий протекания обменных процессов;
- Снижение температуры в легких (в тканях она выше, нежели в легких) и чем ниже упадет tº, тем больше способностей присоединять кислород появляется у железосодержащего белка (при повышении температуры идет обратный эффект).
Уровень красного пигмента в крови, а также его способность присоединять кислород (кривая диссоциации оксигемоглобина) в некоторой степени подвержены возрастным колебаниям. Так, у младенцев, только-только известившим мир о своем появлении первым криком, количество гемоглобина заметно выше, что объясняется присутствием фетального гемоглобина, который, как известно, обладает повышенным сродством к кислороду. Красный пигмент крови стариков, напротив, постепенно снижает способности связывать кислород.
В заключение хочется заметить, что гемоглобин не только имеет сродство к кислороду и довольно легко соединяется с углекислым газом. Кроме физиологических соединений красного кровяного пигмента при определенных условиях возникают связи с другими газами, в частности – с угарным газом (CO) и оксидом азота (NO), причем соединение происходит также непринужденно
Высокое сродство Hb к угарному газу влечет образование карбоксигемоглобина (HHbCO), который препятствует соединению хромопротеина с кислородом, а в результате этого ткани остаются без O2. К чему это может привести – всем известно: при отравлении угарным газом высок риск смертельного исхода, если вовремя не помочь человеку.
При отравлении оксидом азота или парами нитробензола гемоглобин переходит в метгемоглобин (HHbOH) с изменением валентности железа (II → III). Метгемоглобин также не позволяет кислороду соединиться с гемоглобином, в итоге – наступает кислородное голодание тканей, создается угроза жизни организма.
Гемоглобин (от др.-греч. Гемо — кровь и лат. globus — шар) – это сложная белковая молекула внутри красных клеток крови – эритроцитов (у человека и позвоночных животных). Гемоглобин составляет примерно 98% массы всех белков эритроцита.
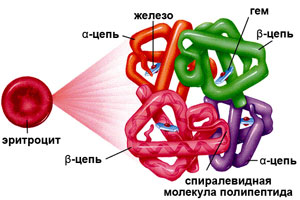
Гемоглобин (от др.-греч. Гемо — кровь и лат. globus — шар) – это сложная белковая молекула внутри красных клеток крови – эритроцитов (у человека и позвоночных животных). Гемоглобин составляет примерно 98% массы всех белков эритроцита. За счет своей структуры гемоглобин участвует в переносе кислорода от легких к тканям, и оксида углерода обратно.
Строение гемоглобина
Гемоглобин состоит из двух цепей глобина типа альфа и двух цепей другого типа (бета, гамма или сигма), соединенными с четырьмя молекулами гемма, содержащего железо. Структура гемоглобина записывается буквами греческого алфавита: α2γ2.
Обмен гемоглобина
Гемоглобин образуется эритроцитами в красном костном мозге и циркулирует с клетками в течение всей их жизни – 120 дней. Когда селезенкой удаляются старые клетки, компоненты гемоглобина удаляются из организма или поступают обратно в кровоток, чтобы включиться в новые клетки.
Типы гемоглобина
К нормальным типам гемоглобина относится гемоглобин А или HbA (от adult — взрослый), имеющий структуру α2β2, HbA2 (минорный гемоглобин взрослого, имеющий структуру α2σ2 и фетальный гемоглобин (HbF, α2γ2. Гемоглобин F – гемоглобин плода. Замена на гемоглобин взрослого полностью происходит к 4-6 месяцам (уровень фетального гемоглобина в этом возрасте менее 1%). Эмбриональный гемоглобин образовывается через 2 недели после оплодотворения, в дальнейшем, после образования печени у плода, замещается фетальным гемоглобином.
| Тип гемоглобина | Процент содержания у взрослого человека |
| HbA - взрослый гемоглобин | 98% |
| HbA2 – взрослый гемоглобин минорный | Около 2% |
| HbFi – фетальный гемоглобин | 0,5-1% |
| Эмбриональный гемоглобин | нет |
| HbA1C – гликированный гемоглобин | |
Аномальных гемоглобинов более 300, их называют по месту открытия.
Функция гемоглобина
Основная функция гемоглобина – доставка кислорода от легких к тканям и углекислого газа обратно.
Формы гемоглобина
- Оксигемоглобин – соединение гемоглобина с кислородом. Оксигемоглобин преобладает в артериальной крови, идущей от легких к тканям. Из-за содержания оксигемоглобина артериальная кровь имеет алый цвет.
- Восстановленный гемоглобин или дезоксигемоглобин (HbH) - гемоглобин, отдавший кислород тканям
- Карбоксигемоглобин – соединение гемоглобина с углекислым газом. Находится в венозной крови и придает ей темный вишневый цвет.
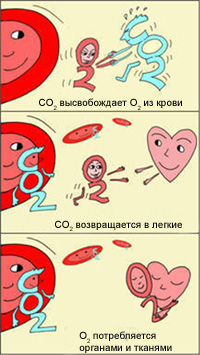
Эффект Бора
В легких, в условиях избытка кислорода, он соединяется с гемоглобином эритроцитов. Эритроциты с током крови доставляют кислород ко всем органам и тканям. В тканях организма с участием поступающего кислорода проходят реакции окисления. В результате этих реакций образуются продукты распада, в том числе, углекислый газ. Углекислый газ из тканей переносится в эритроциты, из-за чего уменьшается сродство к кислороду, кислород выделяется в ткани.

Какой уровень гемоглобина в норме?
В каждом миллилитре крови содержится около 150 мг гемоглобина! Уровень гемоглобина меняется с возрастом и зависит от пола. Так, у новорожденных гемоглобин значительно выше, чем у взрослых, а у мужчин выше, чем у женщин.
Что еще влияет на уровень гемоглобина?
Некоторые другие состояния также влияют на уровень гемоглобина, например, пребывание на высоте, курение, беременность.

- У беспозвоночных животных гемоглобин растворен в плазме крови.
- В сутки из легких в ткани переносится около 600 литров кислорода!
- Красный цвет крови придает гемоглобин, входящий в состав эритроцитов. У некоторых червей вместо гемоглобина хлорокруорин и кровь зеленая. А у каракатиц, скорпионов и пауков голубая, так как вместо гемоглобина – содержащий медь гемоцианин.

Структура гемоглобина человека. Железосодержащие гем-группы показаны зелёным. Красным и синим показаны альфа- и бета- субъединицы.
Гемоглобин появился более чем 400 миллионов лет назад у последнего общего предка человека и акул в результате 2 мутаций, приведших к формированию четырёхкомпонентного комплекса гемоглобина, сродство которого к кислороду достаточно для связывания кислорода в насыщенной им среде, но недостаточно, чтобы удерживать его в других тканях организма. [2] [3]
Большой вклад в исследование структуры и функционирования гемоглобина внёс Макс Фердинанд Перуц, получивший за это в 1962 году Нобелевскую премию [4] .
Нормальным содержанием гемоглобина в крови человека считается: у мужчин — 130 — 160 г/л (нижний предел — 120 , верхний предел — 180 г/л ), у женщин — 120 — 160 г/л ; у детей нормальный уровень гемоглобина зависит от возраста и подвержен значительным колебаниям. Так, у детей через 1 — 3 дня после рождения нормальный уровень гемоглобина максимален и составляет 145 — 225 г/л , а к 3 — 6 месяцам снижается до минимального уровня — 95 — 135 г/л , затем с 1 года до 18 лет отмечается постепенное увеличение нормального уровня гемоглобина в крови [5] .
Во время беременности в организме женщины происходит задержка и накопление жидкости, что является причиной гемоделюции — физиологического разведения крови. В результате наблюдается относительное снижение концентрации гемоглобина (при беременности уровень гемоглобина в норме составляет 110 — 155 г/л ). Кроме этого, в связи с внутриутробным ростом ребёнка происходит быстрое расходование запасов железа и фолиевой кислоты. Если до беременности у женщины был дефицит этих веществ, проблемы, связанные со снижением гемоглобина, могут возникнуть уже на ранних сроках беременности [6] .
Главные функции гемоглобина: перенос кислорода и буферная функция. У человека в капиллярах лёгких в условиях избытка кислорода последний соединяется с гемоглобином образуя оксигемоглобин. Потоком крови эритроциты, содержащие молекулы гемоглобина со связанным кислородом, доставляются к органам и тканям, где кислорода мало; здесь необходимый для протекания окислительных процессов кислород освобождается от связи с гемоглобином. Кроме того, гемоглобин способен связывать в тканях небольшое количество (около 1/3) диоксида углерода (CO2) образуя карбгемоглобин [en] и освобождать его в лёгких (2/3 углекислого газа переносится в растворённом виде или в виде солей плазмой крови и цитоплазмой эритроцитов) [7] .
Гемоглобин является сложным белком класса гемопротеинов, то есть в качестве простетической группы здесь выступает гем — порфириновое ядро, содержащее железо. Гемоглобин человека является тетрамером, то есть состоит из 4 протомеров. У взрослого человека они представлены полипептидными цепями α1, α2, β1 и β2. Субъединицы соединены друг с другом по принципу изологического тетраэдра. Основной вклад во взаимодействие субъединиц вносят гидрофобные взаимодействия. И α-, и β-цепи относятся к α-спиральному структурному классу, так как содержат исключительно α-спирали. Каждая цепь содержит восемь спиральных участков, обозначаемых буквами от A до H (от N-конца к C-концу).
Гем представляет собой комплекс протопорфирина IX, относящегося к классу порфириновых соединений, с атомом железа(II). Этот кофактор нековалентно связан с гидрофобной впадиной молекул гемоглобина и миоглобина.
Железо(II) характеризуется октаэдрической координацией, то есть связывается с шестью лигандами. Четыре из них представлены атомами азота порфиринового кольца, лежащими в одной плоскости. Две другие координационные позиции лежат на оси, перпендикулярной плоскости порфирина. Одна из них занята азотом остатка гистидина в 93-м положении полипептидной цепи (участок F). Связываемая гемоглобином молекула кислорода координируется к железу с обратной стороны и оказывается заключённой между атомом железа и азотом ещё одного остатка гистидина, располагающегося в 64-м положении цепи (участок E).
Связь гемоглобина с монооксидом углерода более прочная, чем с кислородом. Поэтому часть гемоглобина, образующая комплекс с монооксидом углерода, не участвует в транспорте кислорода. В норме у человека образуется 1,2 % карбоксигемоглобина. Повышение его уровня характерно для гемолитических процессов, в связи с этим уровень карбоксигемоглобина является показателем гемолиза.
В отличие от миоглобина гемоглобин имеет четвертичную структуру, которая придаёт ему способность регулировать присоединение и отщепление кислорода и характерную кооперативность: после присоединения первой молекулы кислорода связывание последующих облегчается. Структура может находиться в двух устойчивых состояниях (конформациях): оксигемоглобин (содержит 4 молекулы кислорода; напряжённая конформация) и дезоксигемоглобин (кислорода не содержит; расслабленная конформация).
Устойчивое состояние структуры дезоксигемоглобина усложняет присоединение к нему кислорода. Поэтому для начала реакции необходимо достаточное парциальное давление кислорода, что возможно в альвеолах лёгких. Изменения в одной из 4 субъединиц влияют на оставшиеся, и после присоединения первой молекулы кислорода связывание последующих облегчается.
Отдав кислород тканям, гемоглобин присоединяет к себе ионы водорода и углекислый газ, перенося их в лёгкие [9] .
Гемоглобин является одним из основных белков, которыми питаются малярийные плазмодии — возбудители малярии, и в эндемичных по малярии районах земного шара весьма распространены наследственные аномалии строения гемоглобина, затрудняющие малярийным плазмодиям питание этим белком и проникновение в эритроцит. В частности, к таким имеющим эволюционно-приспособительное значение мутациям относится аномалия гемоглобина, приводящая к серповидноклеточной анемии. Однако, к несчастью, эти аномалии (как и аномалии строения гемоглобина, не имеющие явно приспособительного значения) сопровождаются нарушением кислород-транспортирующей функции гемоглобина, снижением устойчивости эритроцитов к разрушению, анемией и другими негативными последствиями. Аномалии строения гемоглобина называются гемоглобинопатиями.
Гемоглобин высокотоксичен при попадании значительного его количества из эритроцитов в плазму крови (что происходит при массивном внутрисосудистом гемолизе, геморрагическом шоке, гемолитических анемиях, переливании несовместимой крови и других патологических состояниях). Токсичность гемоглобина, находящегося вне эритроцитов, в свободном состоянии в плазме крови, проявляется тканевой гипоксией — ухудшением кислородного снабжения тканей, перегрузкой организма продуктами разрушения гемоглобина — железом, билирубином, порфиринами с развитием желтухи или острой порфирии, закупоркой почечных канальцев крупными молекулами гемоглобина с развитием некроза почечных канальцев и острой почечной недостаточности.
Ввиду высокой токсичности свободного гемоглобина в организме существуют специальные системы для его связывания и обезвреживания. В частности, одним из компонентов системы обезвреживания гемоглобина является особый плазменный белок гаптоглобин, специфически связывающий свободный глобин и глобин в составе гемоглобина. Комплекс гаптоглобина и глобина (или гемоглобина) затем захватывается селезёнкой и макрофагами тканевой ретикуло-эндотелиальной системы и обезвреживается.
Другой частью гемоглобинообезвреживающей системы является белок гемопексин [en] , специфически связывающий свободный гем и гем в составе гемоглобина. Комплекс гема (или гемоглобина) и гемопексина затем захватывается печенью, гем отщепляется и используется для синтеза билирубина и других жёлчных пигментов или выпускается в рециркуляцию в комплексе с трансферринами для повторного использования костным мозгом в процессе эритропоэза.
Экспрессия генов гемоглобина до и после рождения.
Также указаны типы клеток и органы, в которых происходит экспрессия гена (данные по Wood W. G., (1976). Br. Med. Bull. 32, 282.). [10]
Дефицит гемоглобина может быть вызван, во-первых, уменьшением количества молекул самого гемоглобина (см. анемия), во-вторых, из-за уменьшенной способности каждой молекулы связать кислород при том же самом парциальном давлении кислорода.
Гипоксемия — это уменьшение парциального давления кислорода в крови, её следует отличать от дефицита гемоглобина. Хотя и гипоксемия, и дефицит гемоглобина являются причинами гипоксии. Если дефицит кислорода в организме в общем называют гипоксией, то местные нарушения кислородоснабжения называют ишемией.
Прочие причины низкого гемоглобина разнообразны: кровопотеря, пищевой дефицит, болезни костного мозга, химиотерапия, отказ почек, атипичный гемоглобин.
Повышенное содержание гемоглобина в крови связано с увеличением количества или размеров эритроцитов, что наблюдается также при истинной полицитемии. Это повышение может быть вызвано: врождённой болезнью сердца, лёгочным фиброзом, слишком большим количеством эритропоэтина.
Читайте также:

