Нахождение алканов в природе кратко
Обновлено: 04.07.2024
Алканы — предельные (насыщенные, парафиновые) углеводороды, то есть органические соединения, состоящие из углерода и водорода, не имеющие двойных, тройных связей. Основополагающий вывод теории химического строения А. М. Бутлерова о связи между строением и свойствами лежит в основе нашего рассмотрения отдельных классов органических соединений. С той или иной степенью полноты такая взаимосвязь прослеживается в рамках матрицы свойств-признаков, которая может иметь вид, представленный в табл. 9-1.
Практическое значение алканов
Понятны в этой связи две основные области применения алканов — в качестве высококалорийного топлива, прежде всего моторного, потребность в котором постоянно растет в мире, и как важнейшее промышленное сырье для получения самых разнообразных химических продуктов.
В обоих качествах алканам в ближайшее время приемлемой альтернативы нет. В ряду углеродсодержащих органических природных продуктов (уголь, торф, древесина, нефть, газ) последние два наиболее насыщены водородом и являются по этой причине наиболее удобным и дешевым сырьем в органическом синтезе. Переход промышленности органического синтеза на это сырье в первой половине XX века позволил качественно обновить и расширить ассортимент химической продукции, значительно снизив ее себестоимость.
Нахождение алканов в природе
Основными источниками алканов в природе являются нефть и природный газ. Нефть представляет собой сложную смесь органических соединений, состоящую в основном из алканов, циклоалканов, ароматических углеводородов; алкены в нефти почти никогда не содержатся. Ее состав сильно варьирует в зависимости от месторождения. Например, алканы в очень большом количестве содержатся в пенсильванской (США), татаро-башкирской, грозненской (Россия) нефти, циклоалканы — в бакинской, в уральской нефти много ароматических углеводородов. Природный газ содержит главным образом метан, а попутный нефтяной газ — в основном метан, а также другие летучие алканы — этан, пропан, бутан, изобутан.
Строение алканов
Алканы содержат химические связи двух типов: С-С и С-Н . Это типичные ковалентные двухцентровые, двухэлектронные, неполярные химические связи. Прочность связей С-С и С-Н (табл. 9-3) зависит от типа атома углерода, у которого происходит разрыв связи.
Наименее прочной она является у третичного атома углерода, что делает такую связь наиболее уязвимой при химических реакциях. Дипольный момент алканов равен нулю, что свидетельствует о неполярном характере связей С-Н и С-С . Межмолекулярные взаимодействия алканов включают главным образом дисперсионную составляющую и являются очень слабыми. Это предопределяет для алканов в твердом состоянии молекулярный тип кристаллической решетки и легкость ее разрушения.
Пространственные конформационные изомеры алканов (см. раздел 3.2.3) имеют малый энергетический барьер и в нормальных условиях не могут быть выделены в индивидуальном виде, так как они быстро переходят друг в друга. Однако, поскольку конформационная изомерия проявляется относительно каждой С-С связи, ее суммарное влияние становится заметным.
Физические свойства алканов
Слабостью межмолекулярных взаимодействий обусловлены высокая летучесть и испаряемость низших алканов, очень низкая температура плавления (табл. 9-5). Очевидно закономерное влияние молекулярной массы алканов на температуры плавления и кипения, на плотность, которая даже у полиэтилена и полипропилена, тем не менее, остается меньше единицы. Разветвления цепи, уменьшая межмолекулярные взаимодействия и делая более рыхлой упаковку молекулярной кристаллической решетки, закономерно снижают по сравнению с нормальными (неразветвленными) изомерами температуры кипения, плавления и плотность. Первые четыре члена гомологического ряда алканов в нормальных условиях являются газами, от пентана до пентадекана — жидкостями, начиная с гексадекана — твердые вещества. Для бытовых целей обычно используют пропан-бутановую смесь, которая легко сжижается при небольших давлениях.
Химические свойства алканов
Неполярность связей С-С и С-Н предопределяет в основном гомолитический тип разрыва связей и радикальный характер химических реакций. Вследствие высокой прочности связей С-С и С-Н следует ожидать от алканов химической инертности. В каких же условиях и с какими реагентами алканы способны вступать в химические реакции? Проведем анализ простейшей реакции хлорирования метана:
Принципиальная возможность протекания данной реакции может быть установлена, согласно уравнению (53), для реакции, протекающей в изобарно-изотермических условиях:
ΔG = ΔН – TΔS
Поскольку в результате реакции число частиц не меняется, изменением энтропии ( ΔS ) можно пренебречь, тогда ΔG ≈ ΔН .
Таким образом, для реакции хлорирования метана, согласно (58),
получим уравнение изотермы Вант-Гоффа:
ΔG ~ ΔH = -2,3RTlgK. (87)
Оценим теперь глубину протекания реакции, возможный максимальный выход продуктов реакции. Примем Т= 300 К, R = 8,314 Дж/(К·моль). Тогда согласно (80) имеем:
Очевидно, что реакция практически нацело сдвинута вправо. Известно эмпирическое правило для реакций, в которых изменение энтропии незначительно: если ΔН 1, если ΔН>+63 кДж, то К 6С (тв.) + 7Н2 (газ) С6Н14 (газ)
тепловой эффект ΔН = -167,4 кДж/моль, но К ~ 1.
Хотя реакция хлорирования метана принципиально возможна, тем не менее смесь метана и хлора в темноте в нормальных условиях не реагирует! Такая ситуация объясняется только тем, что велика энергия активации данной реакции. Последнее обстоятельство не позволяет преодолеть энергетический барьер заметному числу исходных молекул.
Любая многостадийная химическая реакция включает медленную, лимитирующую стадию, определяющую скорость реакции. Выявление и изучение такой стадии, анализ факторов, влияющих на ее ход, и являются центральной проблемой для асинхронных процессов. В газовой фазе, где решающим при беспорядочном броуновском движении будет столкновение частиц, более вероятно реализуется асинхронный процесс. Реакция хлорирования метана может начаться с двух реакций, других типов связей нет:
а) Cl2 → Cl • + Сl • ΔHa = +242,7 кДж/моль
При отсутствии внешних воздействий (сольватация и др.) тепловое движение при температурах ниже 100 °С может разрушить связь не прочнее 130 кДж/моль в очень незначительном числе молекул. Вот почему в обычных условиях реакция хлорирования метана не идет! Квант близкого к УФ света имеет энергию порядка 293 кДж/моль. Этой энергии достаточно только для разрыва связи Сl-Сl . Гетеролиз Сl-Сl → Cl + + Cl – невозможен, так как на это требуется 1129,7 кДж/моль в очень незначительном числе молекул. Далее радикал Сl • может реагировать двояким образом:
Очевидна предпочтительность реакции в). Атака радикала хлора на водород метана не требует строгой ориентации. Далее возможен только один вариант взаимодействия:
д) СН • 3 + Сl2 →СН3Сl + Сl • ΔHд = -338,9 + 242,7 = -96,2 кДж/моль
Важной особенностью этого механизма является то, что вместо радикала хлора, расходуемого в реакции в ), появляется другой радикал хлора в реакции д ). Такие процессы называются цепными и имеют три фазы: инициирование, рост цепи и обрыв цепи.
Инициирование обычно осуществляется УФ-, γ-, рентгенол ским облучением, воздействием высоких температур, добавлением активных радикалов, получаемых разложением перекисей или других легко разлагаемых до радикалов соединений.
RO—OR →RO • + RO • ΔН =+146,4 кДж/моль
Обрыв цепи, кроме указанных реакций, возможен на стенках сосуда, при взаимодействии с примесями и т. д. Теоретически одного акта разрыва связи Сl-Сl достаточно для завершения реакции во всем объеме. Однако на самом деле число циклов обычно не превышает 100-10000. Это обусловлено тем, что реакции обрыва цепи идут исключительно быстро, поскольку при этом происходит образование устойчивых молекул из нестабильных радикалов.
Рост цепи доминирует над обрывом в условиях, когда концентрация радикалов мала, то есть вероятность встречи двух радикалов меньше, чем радикала и молекулы (в данном случае — метана). Поэтому необходимо постоянное инициирование. За цикл работ по разработке теории цепных реакций в 1956 году удостоены Нобелевской премии Н. Н. Семенов (Россия) [60] и С.-Н. Хиншелвуд (Англия). Теория цепных реакций оказалась хорошо приложимой к процессам горения, окисления органических соединений, старения полимеров, горения, детонации порохов и взрывчатых веществ, гетерогенного катализа, полимеризации, деления трансурановых элементов и др.
Алканы реагируют при освещении с галогенами (хлором и бромом). При этом постепенно происходит замещение атомов водорода в молекуле алкана на атомы галогена:




Газообразные алканы (метан — бутан) входят в состав природного газа . Жидкие и твёрдые алканы содержатся в нефти .
Выделение большого количества теплоты позволяет использовать насыщенные углеводороды в качестве топлива .
Способность вступать в химические реакции даёт возможность применять алканы в качестве сырья для производства разнообразных органических веществ.
Мы приступаем к новому разделу - органической химии. Совершенно необязательно (и даже преступно по отношению к собственному времени!) знать наизусть, зубрить свойства органических веществ.
По мере изучения вы поймете, что свойства вещества определяются его строением, и научитесь легко предсказывать ход реакций ;)
- Атомы в молекуле соединены в определенной последовательности, в соответствии с их валентностью. Порядок связи атомов отражает химическое строение.
- Зная свойства веществ, можно установить их химическое строение, и наоборот, зная строение вещества можно сделать вывод о его свойствах.
- Атомы или группы атомов оказывают взаимное влияние друг на друга непосредственно или через другие атомы
- Свойства вещества зависят от количественного и качественного состава, а также от химического строения молекулы

Алканы (парафины) - насыщенные углеводороды, имеющие линейное или разветвленное строение, содержащие только простые связи. Относятся к алифатическим углеводородам, так как не содержат ароматических связей.
Алканы являются насыщенными соединениями - содержат максимально возможное число атомов водорода. Общая формула их гомологического ряда - CnH2n+2.
Номенклатура алканов
Номенклатура (от лат. nomen - имя + calare - созывать) - совокупность названий индивидуальных химических веществ, а также правила составления этих названий. Названия у алканов формируются путем добавления суффикса "ан": метан, этан, пропан, бутан и т.д.
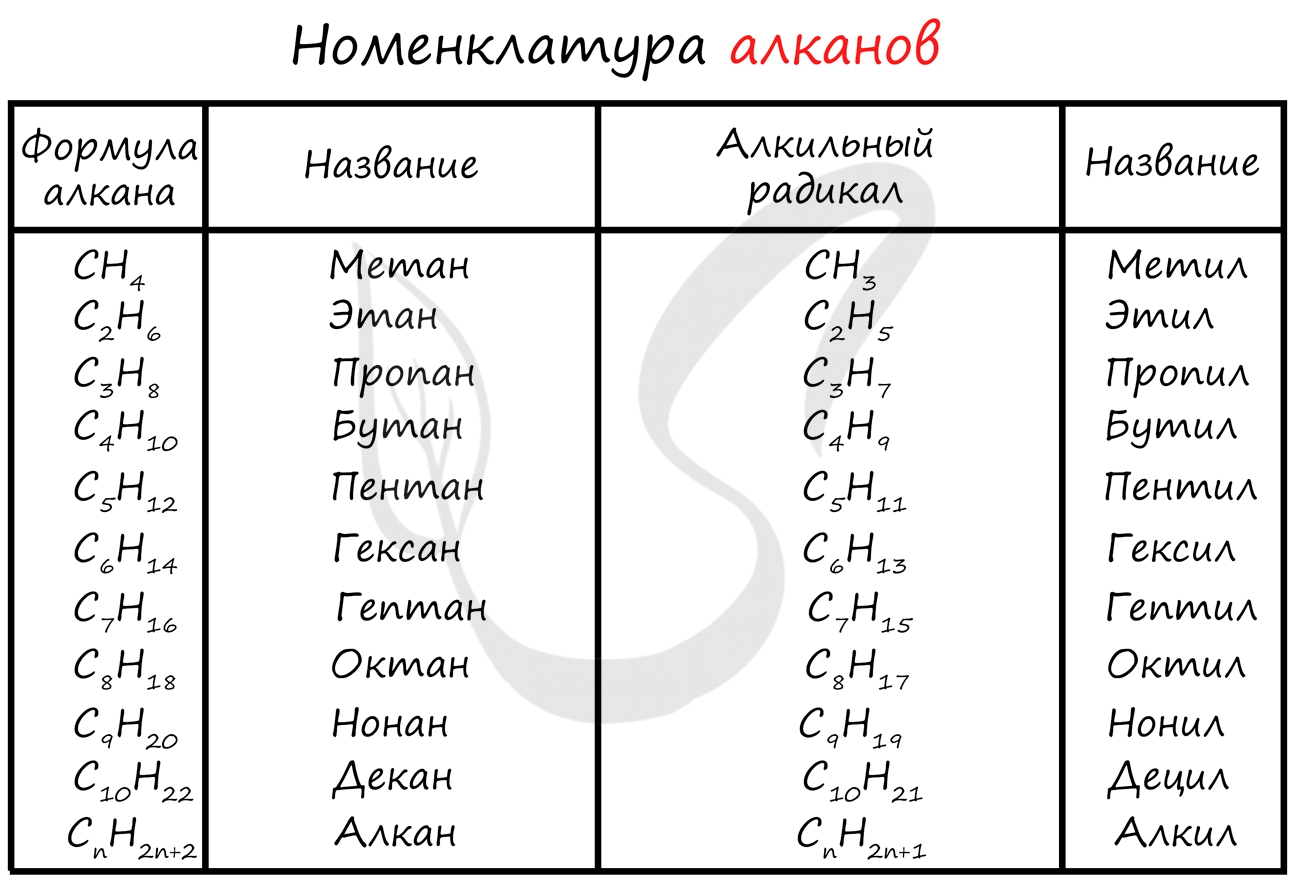
Гомологами называют вещества, сходные по строению и свойствам, отличающиеся на одну или более групп CH2
Перечисленные выше алканы, являются по отношению друг к другу гомологами, то есть составляют один гомологический ряд (греч. homólogos - соответственный).
Названия алканов формируются по нескольким правилам. Если вы знаете их, можете пропустить этот пункт, однако я должен познакомить читателя с ними. Итак, алгоритм составления названий следующий:
- В структурной формуле вещества необходимо выбрать самую длинную (пусть и изогнутую на рисунке!) цепь атомов углерода
- Атомы выбранной цепи нумеруют, начиная с того конца, к которому ближе разветвление (радикал)
- В начале название перечисляют радикалы и другие заместители с указанием номеров атомов углерода, с которыми они связаны. Если в молекуле имеется несколько одинаковых радикалов, то цифрой указывают нахождение каждого из них в главной цепи и перед их названием соответственно ставят частицы ди-, три-, тетра- и т.д.
- Основой названия служит наименование предельного углеводорода с тем же количеством атомов углерода, что и в главной цепи
Внимательно изучите составленные для различных веществ названия ниже.
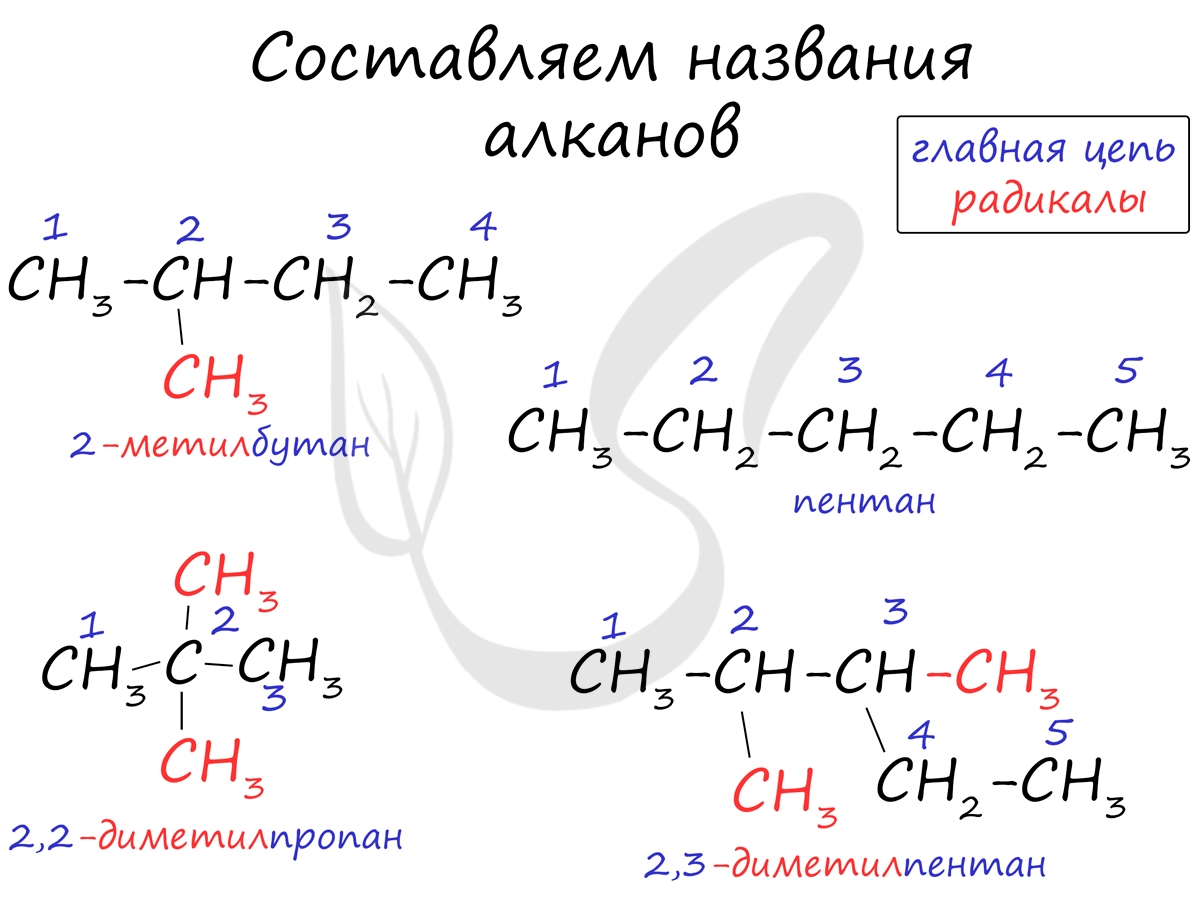
В углеводородной цепочке различают несколько типов атомов углерода, в зависимости от того, с каким числом других атомов углерода соединен данный атом. Различают первичные, вторичные, третичные и четвертичные атомы углерода.

Изомерами (греч. isomeros - составленный из равных частей) называют вещества, имеющие одну молекулярную формулу, но отличающиеся по строению (структурная изомерия) или расположению атомов в пространстве (пространственная изомерия).
Изомерия бывает структурной (межклассовая, углеродного скелета, положения функциональной группы или связи) и пространственной (геометрической, оптической). По мере изучения классов органических веществ вы узнаете о всех этих видах.
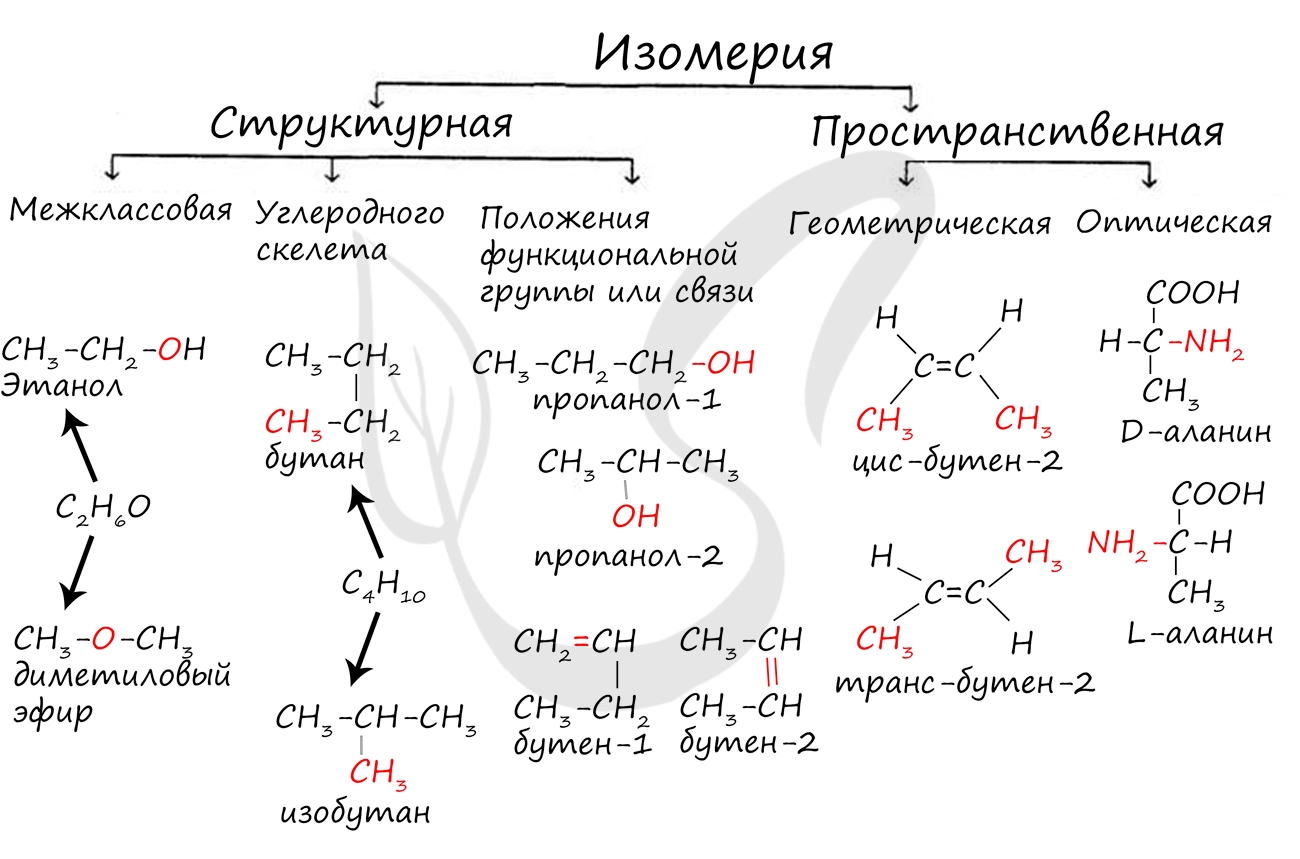
В молекулах алканов отсутствуют функциональные группы, кратные связи. Для алканов возможна изомерия только углеродного скелета. Так у пентана C5H12 существует 3 структурных изомера.

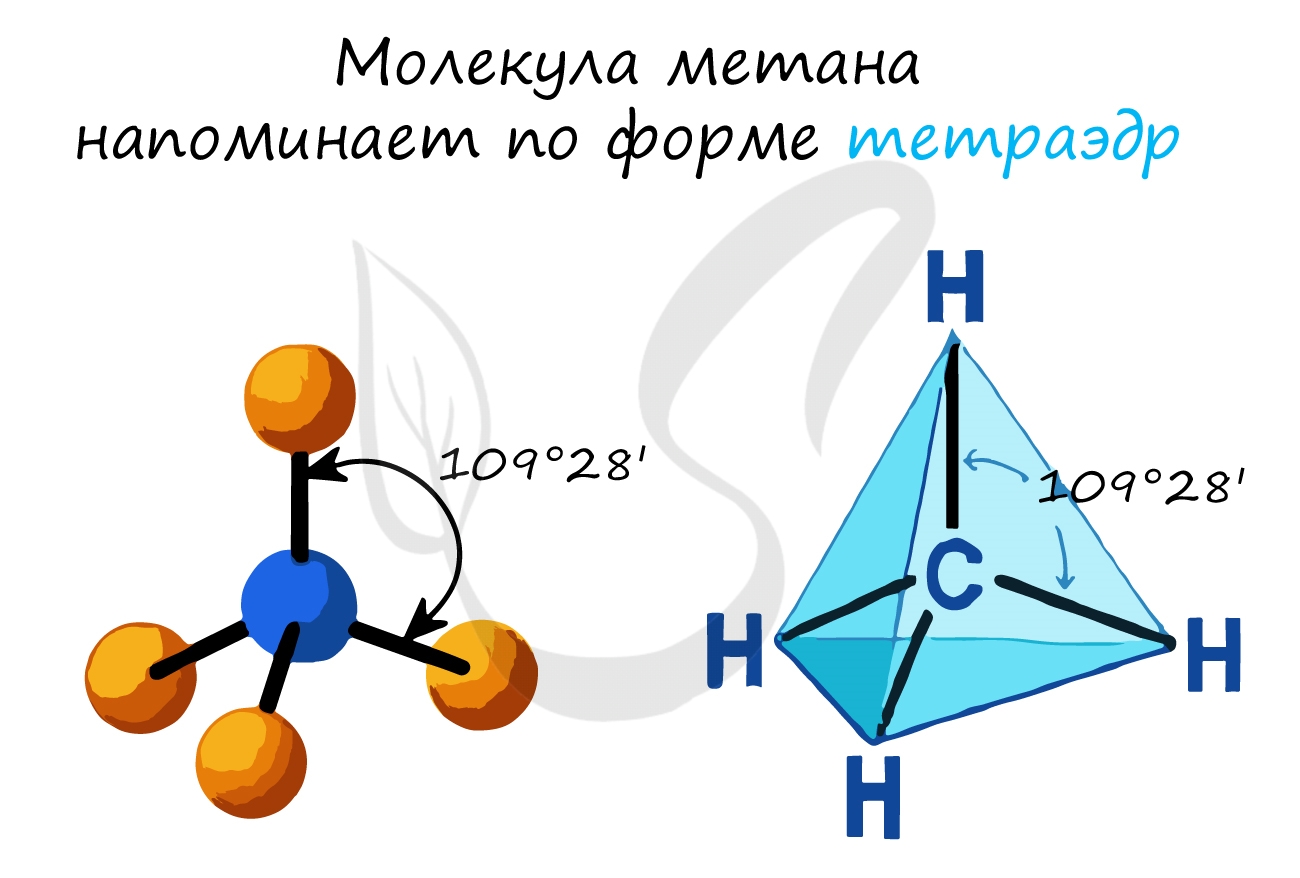
- В молекулах алканов присутствуют одиночные сигма-связи (σ-связи), длина которых составляет 0,154 нм
- Тип гибридизации атомов углерода - sp 3
- Валентный угол (между химическими связями) составляет 109°28'
Природный газ и нефть
Алканы входят в состав природного газа: метан 80-97%, этан 0.5-4%, пропан 0.2-1.5% , бутан 0.1-1%, пентан 0-1%. Состав нефти нельзя выразить одной формулой, он непостоянен и зависит от месторождения.
В состав нефти входят алканы с длинными углеродными цепочками, например: C8H18, C12H26. Путем крекинга из нефти получают алканы.

Получение алканов
В ходе крекинга нефти получается один алкан и один алкен.
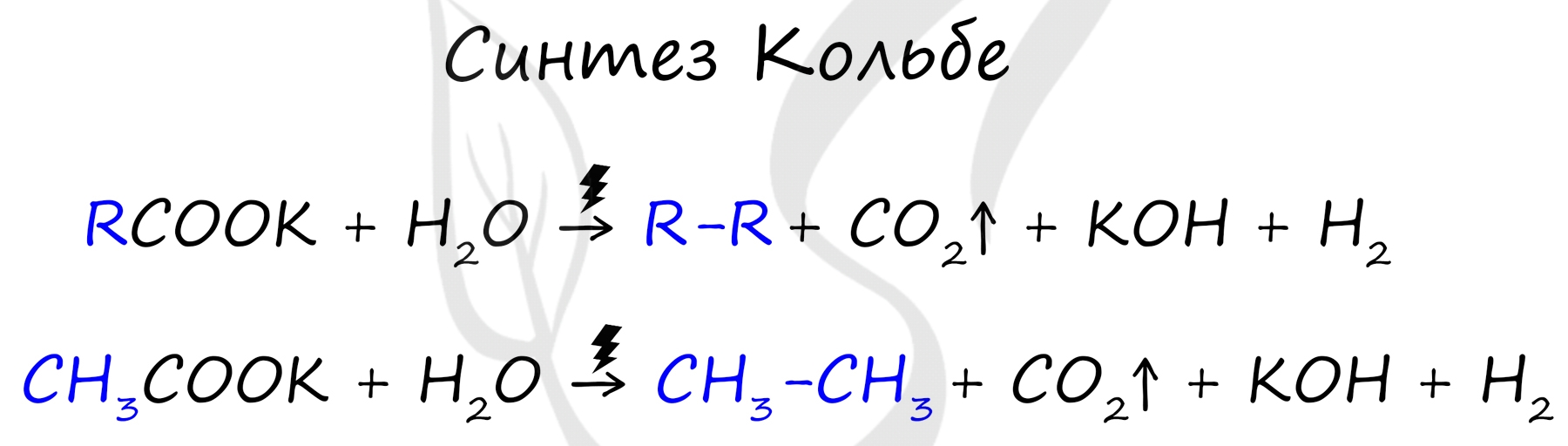
Данный синтез заключается в сплавлении соли карбоновой кислоты с щелочью, в результате образуется алкан.

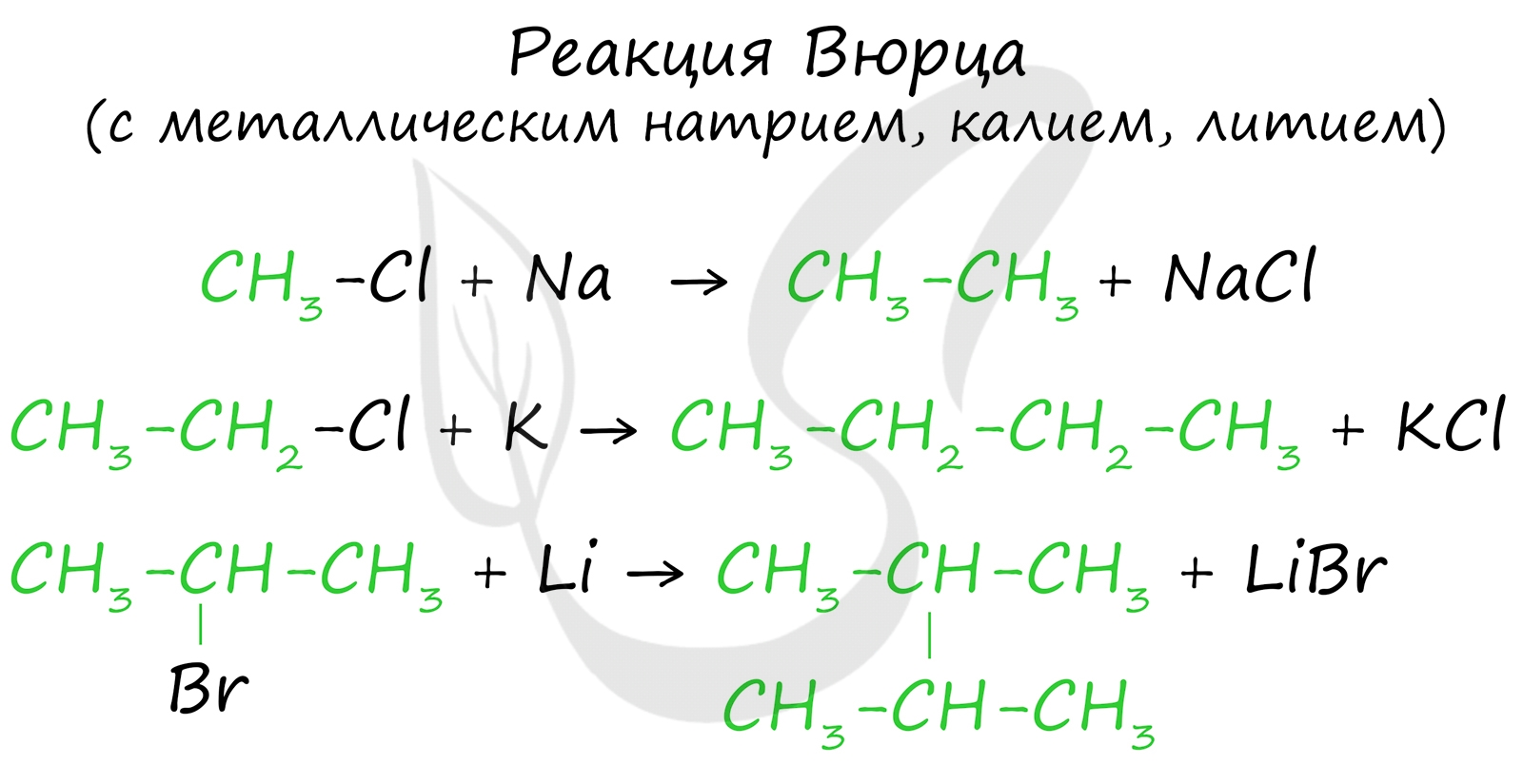
Эта реакция заключается во взаимодействии галогеналкана с металлическим натрием, калием или литием. В результате происходит удвоение углеводородного радикала, рост цепи осуществляется зеркально: в том месте, где находился атом галогена.
В ходе синтеза Гриньяра с помощью реактива Гриньяра (алкилмагнийгалогенида) получают различные органические соединения, в том числе несимметричные (в отличие от реакции Вюрца).
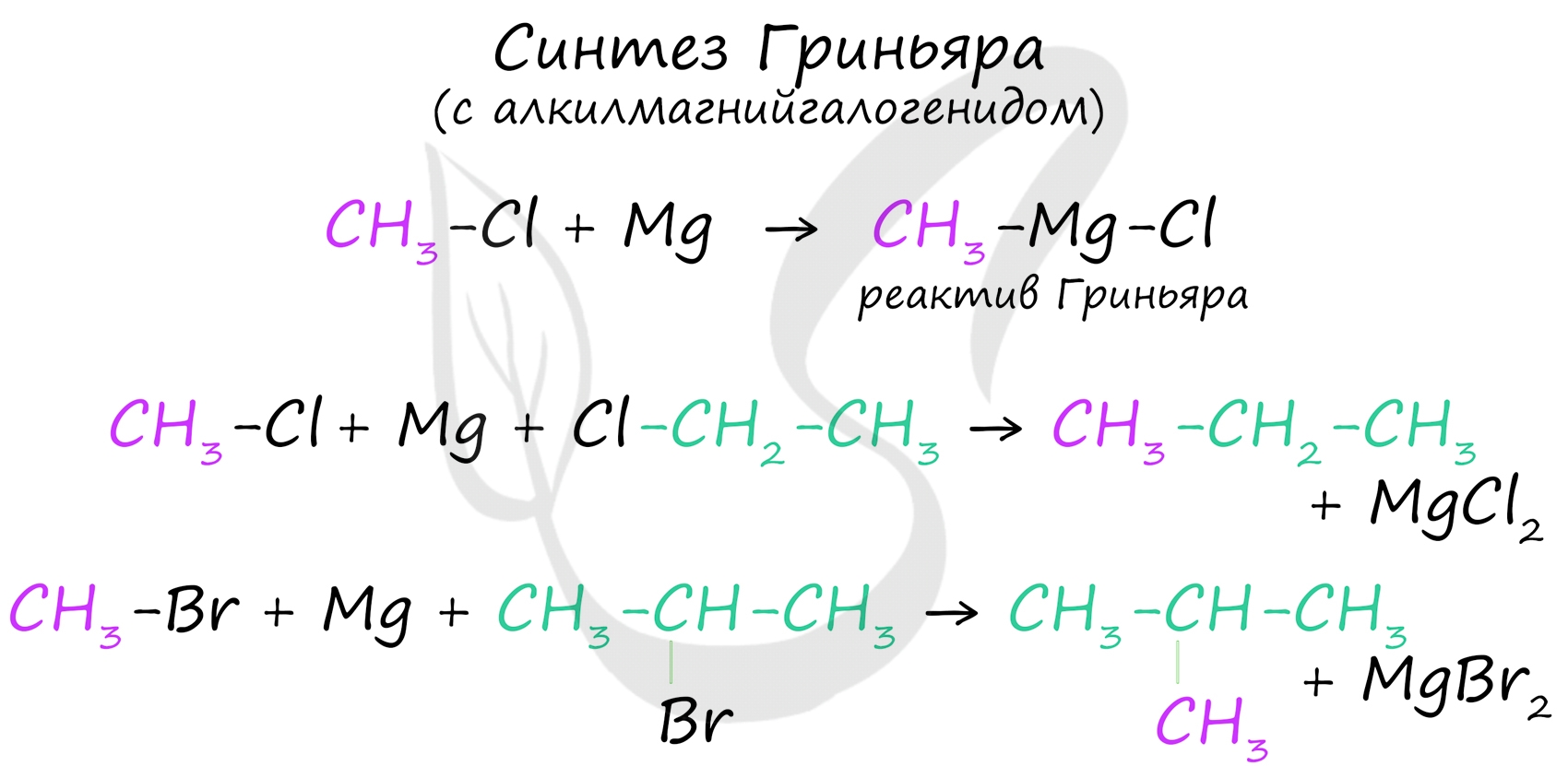
На схеме выше мы сначала получили реактив Гриньяра, а потом использовали его для синтеза. Однако можно записать получение реактива Гриньяра и сам синтез в одну реакцию, как показано на примерах ниже.

В результате электролиза солей карбоновых кислот может происходить образование алканов.
В результате разложения карбида алюминия образуется метан и гидроксид алюминия.
Химические свойства алканов
Атом галогена замещает атом водорода в молекуле алкана. Запомните, что легче всего идет замещение у третичного атома углерода, чуть труднее - у вторичного и значительно труднее - у первичного.

Реакции с хлором на свету происходят по свободнорадикальному механизму. На свету молекула хлора распадается на свободные радикалы, которые и осуществляют атаку на молекулу углеводорода.

Реакция Коновалова заключается в нитровании алифатических (а также ароматических) соединений разбавленной азотной кислотой. Реакция идет при повышенном давлении, по свободнорадикальному механизму.
Для удобства и более глубокого понимания, азотную кислоту - HNO3 - можно представить как HO-NO2.

Все органические вещества, в их числе алканы, сгорают с образованием углекислого газа и воды.
В ходе каталитического, управляемого окисления, возможна остановка на стадии спирта, альдегида, кислоты.
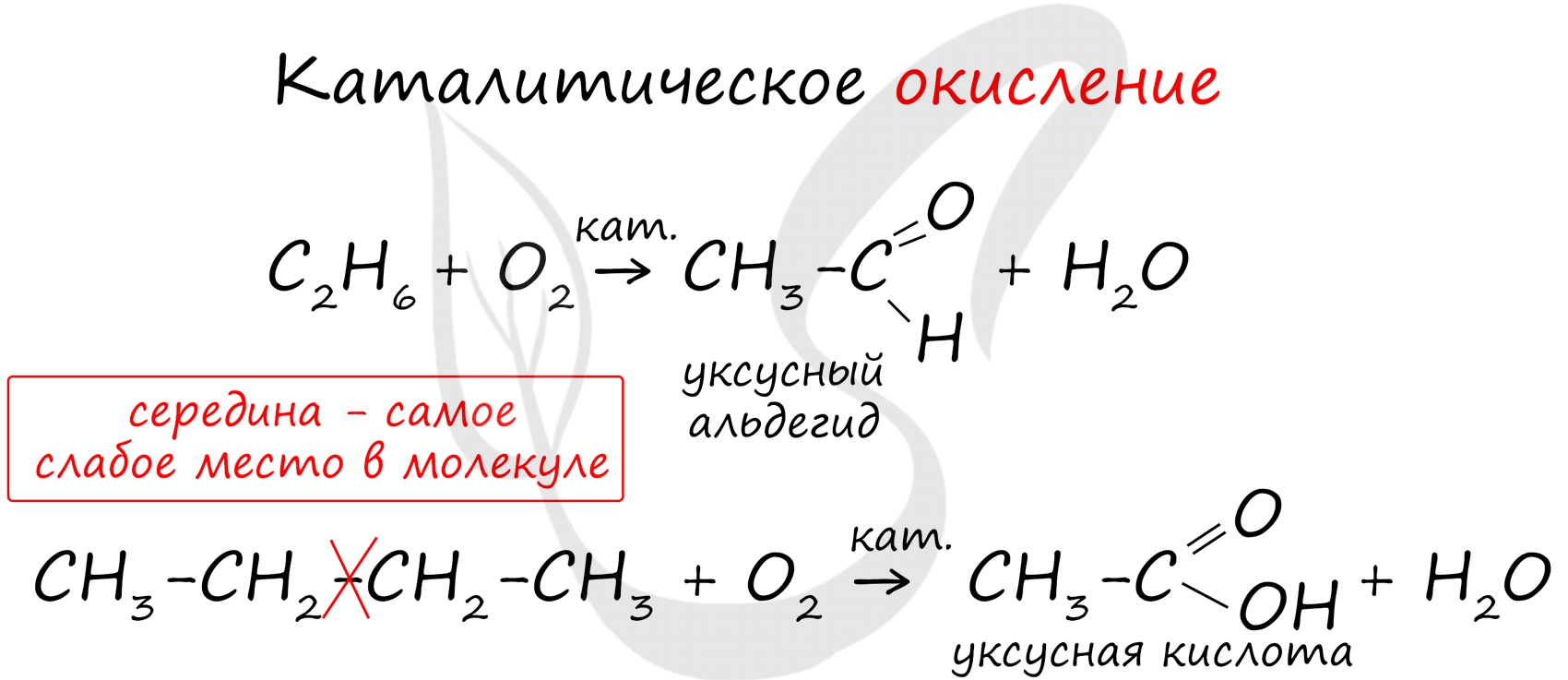
Пиролиз (греч. πῦρ - огонь + λύσις - разложение) - термическое разложение неорганических и органических соединений. Принципиальное отличие пиролиза от горения - в отсутствии кислорода.
В реакциях, по итогам которых образуются изомеры, используется характерный катализатор AlCl3.

Вам уже известно, что в результате крекинга образуется один алкан и один алкен. Это не только способ получения алканов, но и их химическое свойство.
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
II. Химические свойства алканов
1. Реакции замещения
а) Галогенирование
При действии света - hν или нагревании (стадийно – замещение атомов водорода на галоген носит последовательный цепной характер. Большой вклад в разработку цепных реакций внёс физик, академик, лауреат Нобелевской премии Н. Н. Семёнов )
В реакции образуются вещества галогеналканы RГ или С n H 2n+1 Г
(Г - это галогены F, Cl, Br, I)
CH 4 + Cl 2 hν → CH 3 Cl + HCl (1 стадия)
CH 3 Cl + Cl 2 hν → CH 2 Cl 2 + HCl (2 стадия)
Скорость реакции замещения водорода на атом галогена у галогеналканов выше, чем у соответствующего алкана, это связано с взаимным влиянием атомов в молекуле:
Электронная плотность связи С – Cl смещена к более электроотрицательному хлору, в результате на нём скапливается частичный отрицательный заряд, а на атоме углерода – частичный положительный заряд.
На атом углерода в метильной группе ( - СН3) создаётся дефицит электронной плотности, поэтому он компенсирует свой заряд за счёт соседних атомов водорода, в результате связь С – Н становится менее прочной и атомы водорода легче замещаются на атомы хлора. При увеличении углеводородного радикала наиболее подвижными остаются атомы водорода у атома углерода ближайщего к заместителю:
Со фтором реакция идёт со взрывом.
С хлором и бромом требуется инициатор.
Иодирование происходит обратимо, поэтому требуется окислитель для удаления HI из рекции.
Внимание!
В реакциях замещения алканов легче всего замещаются атомы водорода у третичных атомов углерода, затем у вторичных и, в последнюю очередь, у первичных. Для хлорирования эта закономерность не соблюдается при T>400˚C.
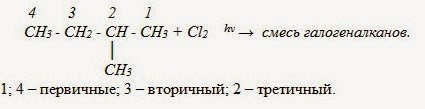
б) Нитрование (реакция М.И. Коновалова , он провёл её впервые в 1888 г)
2. Реакции отщепления (дегидрирование)
б) При нагревании до 1500 С происходит образование ацетилена и водорода:
3. Реакции перегруппировки (изомеризация)
4. Реакции горения (горят светлым не коптящим пламенем)
Помните! Смесь метана с воздухом и кислородом взрывоопасна
5. Реакции разложения
а) Крекинг при температуре 700-1000°С разрываются (-С-С-) связи:
б) Пиролиз при температуре 1000°С разрываются все связи,
продукты – С и Н2:
в) Конверсия метана с образованием синтез – газа (СО + Н2)
III. Получение алканов
1. Получение в лаборатории
1. Гидролиз карбида алюминия (получение метана):
2. Реакция Вюрца (взаимодействие натрия с галогенпроизводными алканов):
(R- это радикал; Г- это галоген)
3. Термическое декарбоксилирование солей карбоновых кислот в присутствии щелочей:
(ацетат натрия+ едкий натр=(метан+карбонат натрия)
этилат натрия этан
4. Каталитическое гидрирование алкенов и алкинов:
5. Электролиз растворов солей карбоновых кислот - реакция КОЛЬБЕ
Пример. Электролиз водного раствора ацетата натрия
Катод (-): H2O , Na + - Процесс восстановления: 2H 2 O + 2ē → H 2 ↑ + 2OH -
Анод (+): H 2 O, CH3COO - (анионы органических кислот активнее воды) – Процесс окисления:
2H2O + 2CH3COONa эл . ток = H2 + 2NaHCO3 + C2H6
2. Получение в промышленности
1. Из природного и попутного нефтяного газа
Важнейшим источником алканов в природе является природный газ, минеральное углеводородное сырье - нефть и сопутствующие ей нефтяные газы. Природный газ на 95 процентов состоит из метана. Такой же состав имеет болотный газ, образующийся в результате переработки бактериями (гниения) углеводов.
Метан называют ещё и болотным; рудничным газом.
Попутные нефтяные газы состоят в основном из этана, пропана, бутана и частично пентана. Их отделяют от нефти на специальных установках по подготовке нефти. При отсутствии газоконденсатных станций попутные нефтяные газы сжигают в факелах, что является крайне неразумной и разорительной практикой в нефтедобыче. Одновременно с газами нефть очищается от воды, грязи и песка, после чего поступает в трубу для транспортировки. Из нефти при ее разгонке (перегонке, дистилляции) отбирая последовательно все более и более высококипящие фракции получают:
бензины - т. кип. от 40 до 180 С, (содержит углеводороды С5-С10), состоит более, чем из 100 индивидуальных соединений, нормальных и разветвленных алканов, циклоалканов, алкенов и ароматических углеводородов;
легкий газойль (дизельное топливо) 230-305 С (С13-С17);
тяжелый газойль и легкий дистиллят смазочного масла 305-405 С (С18-С25);
смазочные масла 405-515 С (С26-С38).
Остаток после перегонки нефти называется асфальтом или битумом.
2. Синтезом из водяного газа:
3. Синтезом из простых веществ:
IV. Применение
1. Предельные углеводороды находят широкое применение в самых разнообразных сферах жизни и деятельности человека.
2. Использование в качестве топлива – в котельных установках, бензин, дизельное топливо, авиационное топливо, баллоны с пропан-бутановой смесью для бытовых плит.
3. Вазелин используется в медицине, парфюмерии, косметике, высшие алканы входят в состав смазочных масел, соединения алканов применяются в качестве хладагентов в домашних холодильниках.
4. Смесь изомерных пентанов и гексанов называется петролейным эфиром и применяется в качестве растворителя. Циклогексан также широко применяется в качестве растворителя и для синтеза полимеров.
5. Метан используется для производства шин и краски.
6. Значение алканов в современном мире огромно. В нефтехимической промышленности предельные улеводороды являются базой для получения разнообразных органических соединений, важным сырьем в процессах получения полупродуктов для производства пластмасс, каучуков, синтетических волокон, моющих средств и многих других веществ. Велико значение в медицине, парфюмерии и косметике.
Читайте также:

