Миостатин и его влияние на организм кратко
Обновлено: 08.07.2024
Спортивное питание: да или нет
В этом пункте разберем, кому все – таки стоит начинать прием добавок, а кому лучше подождать, или же вообще не тратить деньги.
Следующим критерием будет наличие стресса и занятость в течение дня. Как мы знаем, добавки – это хороший способ наполнить наше тело питательными веществами, чтобы поддержать здоровье и питание мышц в стрессовое время, когда на обычное качественное питание у нас просто не хватает время. Если вы не хотите жертвовать своим питанием, и все еще хотите тренироваться, то вы подвергаете ваш организм стрессу, и в этом случае, добавки будут вашим отличным помощником.
Теперь, если вы приобрели спортивное питание, то это не значит, что оно все сделает за вас и можно расслабляться. Если вы считаете, что закрыли свою дневную норму белка шейкером с протеином и можно наедаться в течение оставшегося дня, чем попало, тогда добавки не для вас. Спортивное питание является отличным помощником в вашем рационе, но никак не заменяет его, поэтому в нем должно быть место, как качественной белковой еде, так и добавкам, и вы должны понимать это.
Далее поговорим о людях, которые считают, что можно получить хорошую спортивную форму без применения спортивных добавок. Да, это так, но вы будете отставать. Научно доказано, что, если вы хотите выйти на новый уровень, иметь более атлетическую форму, тренироваться усерднее и, возможно, принимать участие в соревнованиях, то добавки сделают этот процесс более гибким и позволят добиться результатов в кратчайшие сроки.
Для того чтобы понять пользу и необходимость применения данного вида спортивного питания, разберем его технологию производства. Не сложно догадаться, что основным сырьем для производства протеиновых смесей является – молоко. Молоко находится в жидкой форме, но не потому, что в нем много воды, а потому что вещества в молоке растворены друг в друге. Сухая масса веществ в молоке составляет 12%-13%, от общей массы продукта или от объема. Первым шагом на пути производства высокобелковой смеси является выделение сыворотки из молока. Для того, что бы отделить сыворотку из молока, молоко проходит несколько стадий. Самый простой путь получения сыворотки – выделить творог из молока. Творог – кисломолочный продукт, получается он путем сквашивания молока и отделением от него сыворотки. При сквашивании молока, большая часть молочного белка (или казеина) а так же жиров отсеется в нем, а отделившаяся жидкость и есть – сыворотка. Около 6% сухого вещества остается в сыворотке, то есть примерно половина всех молочных элементов остается в сыворотке. Интересный факт, что количество жиров в сыворотке – незначительное, а вот несмотря на то, что казеин (основной молочный белок) остался в твороге, в сыворотке остаются другие, не менее ценные белки – сывороточные протеины. Теперь мы знаем, что при производстве творога и сыра, остается сыворотка, как побочный продукт. В твороге основную часть белков составляют казеин, а в сыворотке – сывороточный протеин
Для того, что бы получить так называемый сывороточный протеин (высококонцентрированный продукт), сыворотку необходимо разделить на отдельные компоненты и выделить сывороточный концентрат (Whey Protein). Концентрат сывороточного протеина – питательный и крайне полезный продукт. Его уже можно употреблять в пищу. При производстве протеина используется так называемый метод мембранной фильтрации. Суть его заключается в том, что мембрана служит как фильтр и задерживает молекулы. Существую различные по величине сетки мембраны, которые задерживают соответственно различные молекулы. Все выделяют четыре вида мембран: микрофильтрафия, ультрафильтрация, нанофильтрация и обратный осмос. Для того, что бы лучше понять то, как делают протеин, давайте посмотрим на схему его производства:
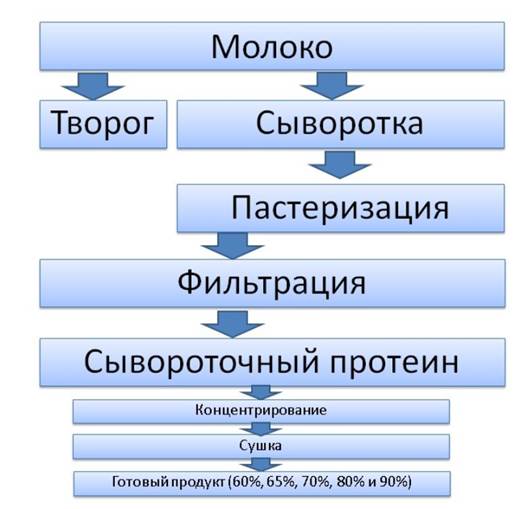
Рисунок 1 - Схема производства протеина
Итак, что же это получается, что такой популярный и разрекламированный в сфере фитнеса протеин – это всего лишь обычное переработанное молоко?
Отсюда можно сделать вывод, что ничего сверхъестественного от протеина ждать не стоит, поскольку это обычный продукт, только в более удобной форме для употребления. Но все же не зря он занимает такое почетное место в построении тела? Не зря, ведь главная основа для построения мышц – это белок, чем и является протеиновая смесь. Так как норма белка для тренирующихся людей колеблется от 1.5 до 2 грамм на вес тела, то если взять вес среднестатистического человека, то получим 65 * 1.8 = 117 грамм белка в день. То есть, нам нужно сделать около четырех белковых приемов пищи, для того чтобы закрыть этот объем. Учитывая нашу постоянную занятость в течение дня, это будет довольно проблематично, поэтому протеиновый шейк с радостью решает эту проблему. К тому же по соотношению цена на грамм белка с той же самой куриной грудкой протеин приятно удивит вас.
BCAA – незаменимые аминокислоты
Здесь все немного сложнее, нежели с протеином. Спортивные добавки BCAA состоят из лейцина, изолейцина и валина. Они ускоряют рост мышц и предотвращают их разрушение, как нам заявляют производители. Помимо этого, также выделяют следующие полезные свойства:
- Набор сухой мышечную массу.
- Уменьшение жировой прослойки.
- Повышение силовых показателей.
- Повышение действия других спортивных добавок.
- Синтезируют мышечный протеин.
- Стимулируют выделение инсулина.
Казалось бы, покупай, пей и расти, все просто. На самом деле отношение к этой добавке может измениться, если посмотреть на таблицу ниже
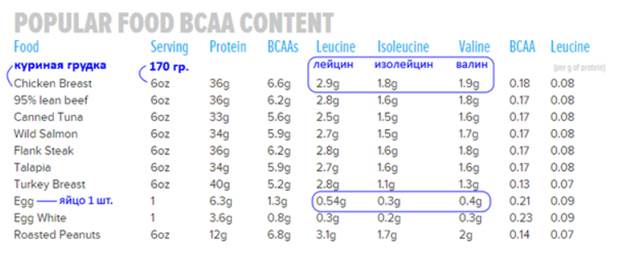
Рисунок 2 - Содержание BCAA в обычных продуктах
Для прояснения картины, приведем пример, что для человека с нормой белка 120 грамм в день, дневная норма BCAA составляет:
- изолейцин – 4,8 г;
То есть, получается ситуация схожая с протеином, к тому же, если сделать некоторые подсчеты, то можно заметить, что норму BCAA закрыть даже легче. Получается опять развод? Не совсем. При интенсивных тренировках потребность в аминокислотах намного возрастает, поэтому с пищей их может не хватит, если вы, конечно, не будете пихать в себя яйца и куриные грудки. Как известно, мышцам для восстановления требуется до 48 часов. Поэтому, если ваш тренировочный процесс построен таким образом, что вы, скажем, тренируетесь ежедневно, тогда прием BСAA позволит вам это делать комфортно и без лишней мышечной боли.
К тому же можно выделить еще один волшебный эффект от данной спортивной добавки. После пробуждения, у нас сразу запускаются катаболические процессы, вызванные ночным голоданием. В связи с недостатком питания, мышцы так же подвергаются катаболизму, а поскольку BCAA являются основным питанием для мышечной массы, то это то, что нам нужно. К тому же выпить натощак бокал с водой с растворенным вкусным порошком не составит труда.
Почти любой сайт в интернете скажет вам, что креатин – это, пожалуй, единственная по – настоящему рабочая добавка. Да, действительно, это так. К тому же мы, в принципе, не можем получить дневную норму креатина с едой, как это работает на вышеперечисленном спортивном питании. Чтобы убедиться в этом, возьмем в пример говядину - довольно дешевый и богатый источник креатина. В килограмме этого мяса содержится всего лишь 5 грамм креатина. Не трудно догадаться, что такой объем пищи не под силу нашему организму.
Креатин – хоть и рабочая добавка, но действует она не на всех. Чтобы извлечь максимальную для себя выгоду при приеме креатина, нужно соблюдать несколько правил. Для начала разберем принцип работы креатина, он прозрачно прост:
Основная энергия нашего организма сосредоточена в молекулах АТФ. Однако есть проблема – их запас настолько мал, что его хватит только на 2-3 секунды активности. Из-за этого в мышцах постоянно синтезируются новые молекулы, и происходит это при помощи:
- гликогена и молочной кислоты;
Креатин активно участвует в процессах фосфагенной системы, что дает энергию на короткие интенсивные активности. Уровень кислоты резко падает после первых 10 секунд занятий, из-за чего медленно образуется фосфат креатина – именно он и синтезирует АТФ. Получается, что основная функция креатина – ускоренное образование молекул АТФ, благодаря которым в мышцы поступает больше энергии, а усталость наступает позже.
Итак, первое правило креатина – это, конечно же, повышение уровня тренировочной активности. Креатин дает вашим мышцам больше энергии, поэтому, почему бы не увеличить рабочие веса, интенсивность тренировок, ведь все это, в конечном итоге, скажется на вашем росте.
Второе правило заключается в способе приема креатина. Обычно, это 10 грамм в тренировочный день (5 грамм с утра, 5 грамм после тренировки), и 5 грамм в день отдыха. Людям с весом более 90 килограмм следует увеличивать норму в индивидуальном порядке. Помимо обычного приема, существует, так называемая, фаза загрузки. То есть, в первые дни приема увеличивать норму до 20 грамм в день. Относительно нее бытуют разные мнения, остановимся на том, что 20 грамм слишком тяжело для нашего организма, особенно почек, и мы не слишком торопимся за получением эффекта, так как спустя неделю обычного приема креатина он не заставит себя ждать. Важно отметить, что креатин хорошо сочетается со сладкими продуктами, поскольку главный доставщик креатина к мышцам, это инсулин. Длительность приема креатина обычно длится от одного до двух месяцев, в зависимости от степени тренированности спортсмена. Далее делается пауза – от двух до четырех недель, и по желанию продолжается или не продолжается прием.
Таким образом, изучив необходимую информацию, и купив за небольшие деньги баночку креатина, можно получить следующие положительные эффекты:
1) Увеличение силы. Этот эффект подтвержден опытами, результаты которых гласят – креатин моногидрат может увеличить максимальный вес при повторных подходах в жиме лежа на 10 кг всего за неделю. Помимо этого возрастают и спринтерские способности.
2) Увеличение массы и проявление рельефа мышц. Креатин всасывается в мышечные клетки – благодаря этому мышцы выглядят больше и рельефнее.
3) Увеличение времени тренировки. Креатин сдерживает образование молочной кислоты, что отодвигает эффект мышечного отказа. Помимо этого сокращается время восстановления после тренировки.
4) Влияние на образование анаболических гормонов. Анаболизм – это формирование новых клеток. Креатин повышает выработку соматотропина и тестостерона: первый называют гормоном роста из-за эффективного влияния на рельефность мышц, а второй наращивает мышцы и ускоряет синтез белка. Помимо этого креатин подавляет образование миостатина – гормона, который мешает мышцам расти.
Омега 3 и витаминно – минеральные комплексы
Омега 3, наряду с креатином, является по – настоящему важным элементом не только для спортсменов, но и для не тренирующихся людей. Наш организм сам не способен вырабатывать Омега-3, а воздействие Омега-3 на организм человека по-настоящему ошеломляюще! Попадая в организм с продуктами питания, жирные кислоты Омега-3 встраиваются в структуру клеточных мембран. Это очень улучшает структуру мембран: происходит активизация работы клеток, улучшается их питание и обменные процессы. Особенно это важно для работы клеток сердца и мозга, которые всегда находятся под нагрузкой. Поскольку продукты с богатым содержанием этого жира проблематично употреблять в ежедневной форме, то капсулы будут отлично справляться с этой работой.
Что насчёт различных комплексов мультивитаминов, то здесь ходят разные мнения. Если у человека довольно богатый и сбалансированный рацион, то нужды в их приеме нет. Единственное, что можно выделить, это Цинк, так как продукты, содержащие это вещество, редко встречаются в нашем рационе.
Менее популярное спортивное питание
В этот список отнесем: гейнер, L – карнитин, цитруллин, тестобустеры, глютамин. Теперь немного поговорим про них:
Гейнер - Это смесь протеина (чаще всего используется тот же самый сывороточный) с комплексом углеводов. Данный вид добавки подойдет в основном для эктоморфов, для того, чтобы сдвинуть с места их упрямый метаболизм. Плюс: быстрый рост массы (не мышечной, а именно общей, то есть включая и жир). Минусы: 1) гейнер выгоднее заменить различными крупами и макаронными изделиями, но, если вы не любите готовить, тогда он вам подойдет; 2) вырастут ваши расходы на туалетную бумагу.
L – карнитин - заменимая аминокислота, в организме она содержится преимущественно в печени и мышечной ткани. Карнитин имеет целый ряд полезных свойств, но спортсмены принимают его прежде всего для ускорения сжигания жира (он транспортирует жирные кислоты к клеточным митохондриям) и для получения дополнительной энергии для тренировок в результате этого процесса. Итак, если вы готовы заплатить за более эффективное сжигание жира, тогда эта добавка для вас.
Цитруллин - это заменимая аминокислота, которая не закодирована в ДНК человека, но всё же присутствующая в некоторых видах белка. Цитруллин, по многим наблюдениям, обладает множеством синергетических эффектов с другими популярными добавками, особенно с BCAA (аминокислоты с разветвлёнными боковыми цепями). Многие исследования показали, что цитруллин-малат обладает множеством полезных свойств, повышающих работоспособность спортсменов. Помимо того, что цитруллин играет важную роль в цикле мочевины, он также улучшает здоровье и физическую производительность:
1) Увеличение внутриклеточного производства NO (оксида азота), который оказывает положительный эффект на процесс вазодилатации (релаксации гладкой мускулатуры в стенках кровеносных сосудов) и кровотока в мышцах
2) Повышает эффективность использования незаменимых аминокислот (в первую очередь BCAA) во время тренировки
3) Уменьшение времени восстановления после тренировки за счёт снижения мышечной боли
4) Усиление элиминации (устранения) токсических метаболитов азота
5) Повышение уровня гормона роста после тренировки в более высокой степени, нежели у тех людей, которые не принимают цитруллин-малат (исследование сравнивало группу принимающих цитруллин и группу, принимающих плацебо)
6) Снижение (ингибирование) увеличения уровня инсулина в плазме, которое обычно возникает после интенсивной тренировки
Так нам расписывают волшебные свойства цитруллина производители. К сожалению, действие этой добавки очень сложно отследить, и польза приема определяется в индивидуальном порядке. Но, цитруллин – это одна из самых безопасных спортивных добавок, поэтому, купив и попробовав, вы ничего не потеряете.
Тестобустеры - В эту группу входит довольно большое число добавок с разными составами, такие как Трибулус, ZMA. Принимают их для повышения секреции уровня тестостерона. Данный вид спортивного питания рекомендуется применять мужчинам, старше 30 лет, когда собственная выработка тестостерона замедляется. В остальных случаях, покупка этой добавки - скорее всего выбрасывание денег на ветер.
Глютамин - условно незаменимая аминокислота. Мышечная ткань человека состоит из неё примерно на 60%. Смысла в ее дополнительном приеме нет, особенно, если вы пьете протеин или BCAA, так как в них, как и во многих других источниках белка глютамина содержится в достатке.
Рынок спортивного питания с каждым годом растет с завидным масштабом. Так его прирост составляет около 15% в год в регионах и 10% в Москве. Поэтому, если вы тренируетесь, важно быть компетентным в этой сфере. Данная статья позволит вам полностью разобраться и определить для себя оптимальный набор спортивного питания для вашего тренировочного процесса. Добавки могут стать отличным помощником в построении спортивной формы, но не стоит забывать про три важнейших критерия для роста мышц: тренировки, питание, сон.

Читательской аудитории этого журнала хорошо известно значение поддержания нормального функционального состояния скелетной мускулатуры для здоровья и долголетия. Известны им и различные состояния, сопровождающиеся потерей или риском потери мышечной массы, такие, как:
- продолжительные периоды отсутствия нормальной физической активности (длительный постельный режим, пребывание в невесомости),
- травмы, приводящие к длительной иммобилизации групп мышц,
- онкологические заболевания,
- ряд осложнений химиотерапии,
- сепсис, некоторые острые и хронические инфекции, включая СПИД,
- старческая саркопения (потеря мышечной массы), начинающаяся фактически после 40 лет.
Очевидно, что знание способов регуляции величины мышечной массы имело бы огромное терапевтическое значение и означало бы значительное снижение риска осложнении и даже летальных исходов.

Рис. 1. Бык породы Belgian Blue (Бельгийская голубая).
Так, например, установлено, что у пациентов с хроническими обструктивными легочными заболеваниями именно уменьшение индекса мышечной массы ниже определенной величины, а не индекса массы тела в целом, наиболее точно коррелирует со смертностью (Marquis К., et al., 2002).
Наряду со значительным увеличением всех мышечных групп видно практически полное отсутствие подкожной жировой ткани.
В результате этих экспериментов было доказано, что белок GDF-8 является отрицательным регулятором роста скелетных мышц и поэтому он получил название миостатин, а животные с таким дефектом - миостатин ноль мышей.
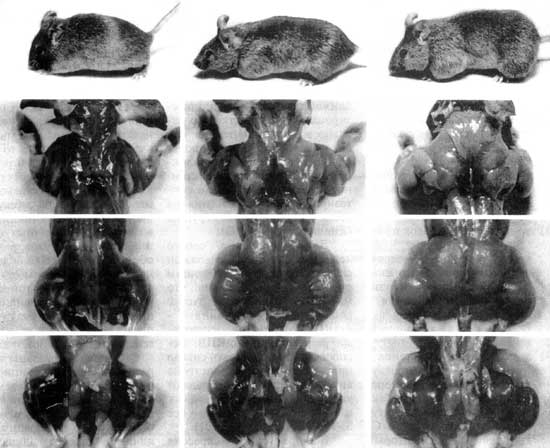
Способность миостатина ограничивать рост мышечной массы сразу привлекла к нему внимание как к потенциальной мишени для терапевтического вмешательства при дегенеративных заболеваниях, травмах и других патологиях мышечной системы, а также - для применения в спортивной медицине и спорте.
Было установлено, что миостатин по своей структуре относится к белкам типа TGF-β (Transforming Growth Factor-beta, трансформирующий фактор роста-бета), которые представляют собой секретируемые факторы, необходимые как в ходе эмбриогенеза, так и во взрослом состоянии для тканевого гомеостаза.
Миостатин имеет общие структурные свойства с другими белками семейства TGF-β:
- гидрофобное ядро в районе N-концевой части молекулы, которое служит как секреторный сигнал;
- консервативный блок из четырех аминокислот в С-концевой половине молекулы, являющийся сигналом для процессинга (протеолитического расщепления в процессе образования активного белка из предшественника большей длины);
- девять остатков цистеина в С-концевой части молекулы, необходимых для образования функционально активной вторичной структуры. После процессинга С-концевой домен, который становится функционально активным миостатином, остается нековалентно связанным с N-концевой частью молекулы, которую в данном случае называют пропептидом;
- Миостатин, как и другие белки типа TGF-β , секре-тируется в виде неактивного комплекса с пропептидом.
Процесс экспрессии миостатина, возможно, регулируется белком Titin-cap (Nicholas G. et al., 2002), так как установлено, что синтез этого белка уменьшает выход миостатина из клеток. Секретированный в виде комплекса с пропептидом миостатин неактивен, так как не может связываться со своим рецептором. Для проявления активности миостатин должен быть отделен от пропептида. Активация миостатина осуществляется в результате расщепления пропептида протеазами типа катепсина D.
Считается, что основная масса синтезированного миостатина проявляет свое действие аутокринным и паракринным образом, т.е. миостатин действует внутри и в районе ближайшего окружения синтезировавшей его клетки, но недавно в экспериментах in vivo доказана возможность проявления его активности эндокринным образом, т.е. системное воздействие локально синтезированного миостатина на все мышечные группы (Zimmers Т. et al, 2002).
Для проявления своего действия миостатин должен связаться с соответствующим ему рецептором. Показано, что миостатин взаимодействует с рецепторами активина ActRIIB. Мыши с измененными рецепторами ActRIIB, неспособными передавать сигнал при связывании миостатина внутрь клетки, также обладают увеличенной мускулатурой, как и миостатин-ноль мыши (Lee S.-J. & McPherron A., 2001).
В эмбриогенезе экспрессия гена миостатина начинается в прогениторных клетках мио-генной линии и продолжается во взрослых аксиальных и параксиальных мышцах (McPherron A. et al., 1997). При этом уровень синтеза миостатина различен в разных скелетных мышцах (Kambadur R. et al., 1997).
Последующие исследования обнаружили экспрессию гена миостатина в ряде других тканей. Показано, что миостатин присутствует в кардиомио-цитах и волокнах Пуркинье в сердце (Sharma M., et al., 1999), синтез мРНК миостатина обнаружен в молочных железах (Ji S, et al., 1998) и в адипоцитах (Kim HS, etal, 2001).
Можно предполагать, что половые различия в количестве секретируемого миостатина, наряду с другими факторами, влияют на половой диморфизм в развитии скелетной мускулатуры. При одинаковом уровне
Синтеза мРНК миостатина, т.е. уровне экспрессии гена миостатина, уровень секретированного миостатина выше у женщин, чем у мужчин (McMahon et al., 2002).
Поскольку экспрессия гена миостатина начавшаяся в эмбриогенезе продолжается в постнатальных мышцах и мышцах взрослого организма, то миостатин, по-видимому, играет существенную роль на всех стадиях миогенеза и в тканевом гомеостазе скелетной мускулатуры во взрослом состоянии при воздействии различных функциональных стимулов, включая обездвиживание. Для более ясного представления места миостатина в мышечном гомеостазе на рис. 3 и 4 приведена общая информация схематически представляющая миогенез и регенерацию мышечной ткани.
Рис. 3. Схематическое представление этапов развития и дифференцировки мышечной ткани.
Активация генов MyoD и Myf5 дает начало миогенной линии клеток, прогениторные клетки (клетки-предшественники) дают начало миобластам. Активация гена миогенина коммитирует миобласты к последующей дифференцировке и пролиферации. Миостатин, активируя ген р21 и синтез Smad-белков, ограничивает (или останавливает) пролиферацию миобластов. Миобласты, прекратившие деление, переходят к стадии морфогенеза, то есть к закладке предшественников мышечных волокон - myotubes. Взаимодействуя друг с другом, они выстраиваются в цепочки и сливаются в вытянутые многоядерные клетки (синцитии). После слияния начинаются дифференцировка мембран, биохимическая и цитоплазматическая дифференцировка, в результате чего возникают окончательно сформированные зрелые мышечные волокна.
На рис. 3 показаны этапы развития и дифференцировки мышечной ткани. Эта схема составлена для отображения процессов происходящих в эмбриогенезе, но с небольшими отличиями она справедлива и для мышц взрослого организма.
Зрелые мышечные волокна - продукт конечной дифференцировки и неспособны к какому-либо делению, т.е., ни они сами, как структура в целом, ни клеточные ядра внутри волокон не могут делиться и рост мышц и регенерация осуществляются благодаря пролиферации сателлитных клеток, которые были открыты в 1961г., благодаря использованию электронной микроскопии (Mauro А.). Сателлитные клетки имеют размеры близкие к размерам клеточных ядер мышечных волокон и, как и эти ядра, находятся на периферии мышечных волокон, и только электронная микроскопия позволила установить, что они физически отделены от зрелых мышечных волокон и находятся между сарколеммой и базальной ламиной (Muir, A.R. et al., 1965).
В мышечных волокнах количество цитоплазмы, приходящееся на одно ядро, находится в определенных достаточно узких пределах (мионуклеарный домен). Увеличение размеров волокна (гипертрофия) достигается благодаря слиянию пролиферирующих сателлитных клеток с волокном, так что размеры мионуклеарного домена остаются в тех же пределах, что и до гипертрофии. Стимулом для деления (пролиферации) сателлитных клеток у взрослых организмов является, в первую очередь, миотравма, в том числе на уровне отдельного мышечного волокна. Участие сателлитных клеток в ответе на миотравму представлено на рис. 4. Выходя из состояния покоя, сателлитные клетки начинают экспрессировать миоген-ные маркеры, т.е., активируются гены характерные для миобластов. В процессе регенерации поврежденных скелетных мышц сателлитные клетки сливаются с существующими мышечными волокнами (гипертрофия) или между собой, создавая новые волокна (гиперплазия).
Определяя долю сателлитных клеток в мышечной ткани удобнее сопоставлять миофиб-риллы и сателлитные клетки по числу ядер, поскольку мышечные волокна многоядерны. Во взрослом состоянии ядра сателлитных клеток составляют 2-7% от общего числа ядер в различных мышцах. При рождении р ядра сателлитных клеток составляют около 30% от общего числа ядер в мышцах нижних конечностей (Schultz E. & McCormick K.M., 1994). Эти неонатальные сателлитные клетки пролиферируют и сливаются с растущими мышечными волокнами, привнося в них дополнительные ядра в ходе постнатального роста скелетных мышц.
Рис.4. Схематическое представление участия сателлитных клеток в регенерации мышечных волокон.
В ответ на миотравму сателлитные клетки активируются и пролиферируют. Часть клеток после деления возвращается в состояние покоя (для восстановления пула сателлитных клеток). Основная часть клеток в результате хемотаксиса мигрирует к поврежденным участкам и, в зависимости от степени повреждения, или сливается с поврежденным мышечным волокном или сателлитные клетки сливаются друг с другом, образуя новые волокна. Ядра недавно слившихся сателлитных клеток находятся в центре волокон, затем, по мере восстановления внутриклеточных структур волокна, мигрируют к периферии.
Таким образом, сателлитные клетки обеспечивают поддержание функционального состояния скелетных мышц взрослого организма, необходимы для восстановления поврежденных мышечных волокон и являются источником дополнительных ядер при гипертрофии мышц в результате тренировок. Гипертрофия и/или гиперплазия скелетных мышц у животных с отсутствием функционально активного миостатина доказывает, что миостатин влияет на пролиферацию сателлитных клеток, поскольку постнатальный рост мышц и увеличение числа ядер в мышечных волокнах в процессе развития до взрослого состояния происходит благодаря пролиферации сателлитных клеток.
При активации сателлитных клеток (выходе из состояния покоя) в них начинают работать гены характерные для миобластов и, таким образом, сателлитные клетки становятся, по сути, миобластами. Это означает, что степень пролиферации сателлитных клеток во взрослых мышцах также ограничивается миостатином, как и пролиферация миобластов в эмбриогенезе. Показано, что и белок TGF-β ингибирует пролиферацию сателлитных клеток в культуре (Allen R.E. & Boxhorn L.K., 1987).
Роль миостатина в гомеостазе зрелых мышечных волокон в полной мере пока не выяснена, но имеется ряд работ по исследованию уровня синтеза как мРНК миостатина, так и самого миостатина в мышцах во взрослом состоянии на животных моделях и у человека при различных физиологических состояниях.
Так системная сверхэкспрессия миостатина у мышей в течение двух недель приводит к потере свыше 30% общей массы тела и 50% по мышечной массе, то есть картина практически идентичная синдрому кахексии у человека. Эта работа доказала, что миостатин может действовать эндокринным образом. Введение ингибиторов миостатина пропептида или фоллистатина значительно замедляет потерю мышечной массы при повышенном уровне миостатина. Также важно отметить, что наряду с потерей мышечной массы происходит практически полная потеря подкожного жира, что также согласуется с данными о влиянии миостатина на дифференцировку адипоцитов (Zimmers Т.А. et al., 2002).
У людей разных возрастных категорий уровень миостатина в сыворотке крови наиболее высок у мужчин и женщин старше 72 лет и коррелирует со степенью саркопении. У мужчин и женщин среднего возраста уровень миостатина в сыворотке в свою очередь выше по сравнению с молодыми людьми. Индексы нежировой массы тела и мышечной массы тела обратно пропорционально коррелируют с сывороточным миостатином во всех возрастных категориях. Эти данные позволяют рассматривать миостатин не просто как биомаркер возрастной саркопении, но как супрессор мышечной массы. (Yarasheski K.E., et al., 2002).
Внутримышечная и сывороточная концентрации миостатина увеличены у больных СПИДом в стадии, когда наблюдается потеря мышечной массы, при этом концентрация миостатина обратно пропорционально коррелирует с индексом нежировой массы тела. Эти результаты показывают, что миостатин вносит вклад в потерю мышечной массы при СПИДе. (Gonzalez-CadavidN.E.et al., 1998).
В прямых экспериментах на крысах выявлено, что потеря мышечной массы, происходящая при космическом полете, связана с увеличением уровня миостатина в скелетных мышцах (2-5 кратное в различных мышцах к 17-му дню полета). Эти результаты показывают, что миостатин один из основных элементов в многофакторной патофизиологии мышечной атрофии происходящей при космическом полете (Lalani R., et al., 2000).
В наземных экспериментах на людях установлено, что к 25-му дню неподвижного режима (в качестве модели космического полета) уровень миостатина повышается на 12% (ZachwiejaJ. J. etal., 1999).
Иммобилизация мышц у мышей приводит к увеличению концентрации мРНК миостатина (экспрессии гена миостатина) в обездвиженных мускулах уже через 24 часа эксперимента, хотя потеря мышечной массы начинается лишь после третьего дня. Наиболее неожиданный результат, полученный в этих экспериментах, состоял в том, что синтез миостатина значительно различался в мышцах содержащих различные изоформы (варианты) тяжелой цепи миозина. При иммобилизации синтез миостатина значительно возрастал в быстрых мышцах, которые атрофировались к седьмому дню на 17%, в то время как m. soleus, в которой синтез миостатина не обнаруживался, атрофировалась к тому же дню на 42%. M. soleus состоит только из волокон типов I и IIа, тогда как m. gastrocne-mius и т. plantaris представляют собой типы IId/x и IIb, хотя и содержат типы I и IIа. (Carlson С. et al., 1999). Единственно приемлемое объяснение этого феномена - воздействие миостатина синтезированного m. gastrocnemius и т. plantaris на т. soleus, т.е. эндокринное воздействие.
Другое заключение состоит в том, что синтез миостатина коррелирует с типом волокон, т.е. синтез миостатина при иммобилизации мышц у мышей коррелирует с изоформой тяжелой цепи миозина IIb.
На мышиной модели мышечной дистрофии Дюшена (мыши линии mdx) показано, что блокада эндогенного миостатина путем внутрибрюшинных инъекций антител к миостатину в течение трех месяцев приводит к увеличению мышечной массы, размеров и силы мышц (Bogdanovich S., et al., 2002). Гибриды mdx-мышей с миостатин-ноль мышами имеют значительно лучшее состояние мускулатуры, чем исходные mdx-мыши (Wagner K.R. et al., 2002). Нормализация состояния мышц у mdx-мышей путем блокады миостатина или скрещивания с миостатин-ноль мышами открывает новые возможности для лечения патологий сопровождающихся потерей мышечной массы.
Баллу (Ballough W.S., 1962,1965) свыше тридцати лет назад высказал предположение о существовании тканеспецифических ингибиторов - кейлонов (chalones), которые, синтезируясь данной тканью, ингибирует ее рост и, таким образом, поддерживает адекватную массу этой ткани. Это предположение вполне подтвердилось в случае скелетной мускулатуры (Zimmers T.A. et al., 2002).
Очевидно, что искусственное ингибирование активности миостатина повлечет за собой революционные изменения в медицине и спорте и, возможно, будет использоваться в широких терапевтических целях (Lee S. J., McPherron А.С., 2001).
Так получилось, что мне посчастливилось довольно длительный период работать с гормоном миостатином (к сожалению, только теоритически, в лаборатории не получилось), о котором многие здесь уже слышали, поэтому я хочу немного рассказать о том, что это такое и для чего он нужен, но немного с другой стороны.
Начать, пожалуй, надо с того, что компетентных русских источников по этому гормону нет. Начиная свою работу по эндокринологии, я нашел что-то вменяемое только на sportwiki, но там информации крайне мало, а ее качество оставляет желать лучшего. Данные пришлось собирать по крупицам, отсеивая шелуху.
Дублировать информацию из Википедии, думаю, нет смысла, а всякие структурные и классификационные вещи не интересны, поэтому перейдем сразу к самому интересному — зачем же нам такой гормон, который разрушает мышцы.
Однако на этом функции миостатина в организме не заканчиваются, но, к сожалению, все далее перечисленные будут играть роль в патофизиологии.
И напоследок, наверное, надо все-таки написать, что просто блокировка проведения сигнала миостатина хоть и позволит увеличить мышцы в объеме, сила и скорость сокращения значительно уменьшаются, что делает такю манипуляцию бессмысленной для спортсменов.
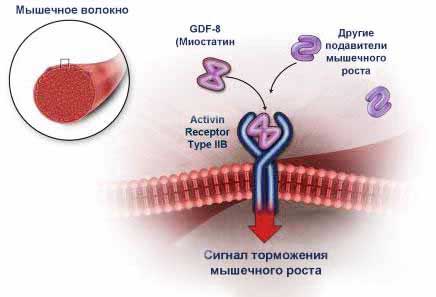
Миостатин (также известен как фактор дифференциации роста 8 или GDF-8) - синтезируемый внутри организма пептид, который подавляет рост и дифференцировку мышечной ткани. Миостатин образуется в мышцах и затем выделяется в кровь, оказывая свое действие на мышцы за счет связывания с рецепторами ACVR2B (activin type II receptor). [1] У человека миостатин закодирован в гене MSTN. [2]
Исследования на животных показывают, что блокирование действия миостатина приводит к значительному увеличению сухой мышечной массы с практически полным отсутствием жировой прослойки. [3]

Бельгийская голубая - порода с мутацией гена миостатина

Борзая с мутацией гена миостатина

Знаменитый бодибилдер Flex Wheeler с врожденной мутацией гена миостатина

Мальчик 12 лет, как утверждалось с мутацией гена миостатина

Слева Ричард Сандрак в 12 лет, справа в 24 года: мышцы исчезли, когда он перестал тренироваться

В настоящее время ведется разработка целого ряда блокаторов действия миостатина, однако на настоящий момент нет ни одного препарата одобренного к применению на людях.
Wyeth Pharmaceuticals в 2002 году начала разработку препарата MYO-029 (Stamulumab) - рекомбинантные антитела, которые связываются с миостатином и блокируют его эффекты.
В начале 2005 года Wyeth Pharmaceuticals при дополнительном финансировании MDA начала фазу 1-2 клинических исследований безопасности и переносимости MYO-029 (Stamulumab) на 116 испытуемых. Данные клинических испытаний были опубликованы только в январе 2008 года.
Препарат показал себя безопасным и хорошо переносимым в трех различных дозировках, о чем сообщено в отчете, опубликованном Kathryn Wagner с коллегами из Johns Hopkins University School of Medicine в Baltimore в журнале Annals of Neurology [4]
Однако в марте 2008 года, после окончания клинических испытаний компания объявила о приостановке развития проекта MYO-029 (Stamulumab), так как ни у кого из участвующих в исследовании не было статистически значимого улучшения силы или роста мышц.

Большой потенциал имеет новый препарат ACVR2B, который представляет собой раствор элементов рецепторов к миостатину. Молекулярные элементы ACVR2B имеют участок, схожий с активным центром рецептора и связываются со свободным миостатином, блокируя его способность активировать рецепторы. Данный препарат был создан в 2005 году, под руководством все того же доктора Se-Jin Lee, Johns Hopkins University School of Medicine в Baltimore. Se-Jin Lee надеется, что ACVR2B может использоваться в ближайшем будущем и на людях, тогда как по состоянию на 2005 год он уже доказал высокую эффективность на лабораторных мышах. Команда доктора Se-Jin Lee апробировала различные дозы ACVR2B на 49 мышах и зафиксировала мышечный прирост после четырех недель применения препарата. Максимальные показатели мышечного прироста были достигнуты при двух инъекциях в неделю, в дозировке 50 мкг на килограмм массы тела. Мышечная масса этих мышей увеличилась на 61% по сравнению с исходной. [5]
ACE-031 еще один перспективный препарат класса блокаторов миостатина, он представляет собой раствор экстрацеллюлярных частей рецепторов ActRIIB соединенных с Fc фрагментом иммуноглобулина G. Путем блокирования сигнала через рецептор ActRIIB, препарат увеличивает мышечную массу и силу. Предварительные испытания ACE-031 продемонстрировали высокую эффективность на экспериментальных моделях с животными.
Клинические испытания ACE-031 для лечения миодистрофии были прекращены в мае 2013 года в связи с развитием побочных эффектов (дилатация сосудов кожи, кровотечения из носа и десен). [6] В продаже доступны кустарные препараты от китайского производителя.
В качестве еще одного блокатора миостатина предложены модифицированные пропептиды миостатина , в частности мутированный пропептид миостатина D76A. Механизм действия препаратов весьма интересен. До тех пор, пока незрелый миостатин (предшественник миостатина) не подвергнется модификации под влиянием металлопротеиназы, он не будет оказывать свое действие. Применяя мутированные пропептиды миостатина, типа D76A происходит необратимое или частично-необратимое связывание с металлопротеиназой, после чего посттрансляционный процессинг промиостатина прекращается, а проще говоря, не образуется зрелый миостатин.
Пробы проводились только на животных, и данных о применении препаратов данной группы на людях пока нет.

В настоящее время нет возможности полноценного применения препаратов или добавок действующих, как антагонисты миостатина поскольку:
1. Недостаточная доказательная база. Многие исследования дают диаметрально противоположные выводы, поэтому пока достоверных данных в этой области очень мало.
2. Побочные эффекты. Сейчас еще рано судить о безопасности выключения действия миостатина. Возможно, это может приводить к отсроченным осложнениям различного рода, к примеру, гипертрофия миокарда. Так же последние работы показали, что интенсивный мышечный рост приводит к увеличению частоты травм связочного аппарата, который остается на таком же уровне развития и рассчитан на относительно меньшие нагрузки.
3. Низкая селективность. Как уже было замечено, миостатин является частью очень обширной метаболической системы, где многие элементы имеют схожее строение и дублируют функцию других. Применяя препараты, ингибирующие действие миостатина, можно получить сбой в работе других элементов метаболической системы. Иными словами, учитывая довольно широкий диапазон компетенции данной метаболической системы, помимо мышечного роста существует вероятность многочисленных серьезных побочных эффектов со стороны всех систем органов и тканей.

В то время, как в научном мире идут ярые споры и активно ведутся испытательные работы, мир спортивной индустрии активно производит абсолютно безопасные и "эффективные" блокаторы миостатина.
Myo-Blast, по заявлению производителя, содержит самую высокую дозу наиболее мощного средства миостатин-нейтрализующего средства, известного как — Myozap CSP3.
Выдержка из описания:
Myozap CSP3 - торговое название патентованной состава для нейтрализации миостатин-белка. Этот экстракт получен из экзотического морского растения (Cystoseira canariensis) и был сначала обнаружен в течение научных исследований, проводимых исследователями биохимии в Las Palmas Университет в Испании. Как только Вы начинаете нейтрализовать миостатин, начинается рост новых мышечных клеток. С помощью этого спортивного питания, новые клетки мышцы увеличиваются в размере и образуют новые волокна мышечной ткани. Каждое новое волокно, фактически представляет потенциал для дополнительной новой мышцы, сверх тех, что Вы уже имеете. И эти многие новые мышечные волокна в конечном счете формируются в вашем теле, давая Вам возможность преодолеть генетический порог, заданный миостатином.
Myostat, Myo-T12 и пр. имеют похожее описание и то же самое действующее вещество - Cystoseira canariensis.

Несмотря на эти громкие слова, данные добавки абсолютно неэффективны. В настоящее время нет ни одной добавки, которая бы влияла на обмен миостатина.
1. Исследования, проведенные Джорджеи Ниффисом, профессором из Института Национального Здоровья (США, штат Огайо), выявили, что все качества, приписываемые спортивному питанию на основе Cystoseira canariensis - не более, чем рекламный ход. В процессе эксперимента выяснилось, что даже в количестве в 50 раз больше рекомендуемого эти добавки не оказали никакого существенного влияния на рост мышечной массы.
2. Все современные антагонисты миостатина белковой природы, поэтому они не принимаются внутрь, так как в этом случае активное вещество было бы неминуемо разрушено пищеварительными ферментами.
В 2009 году было опубликовано исследование, проведенное иранскими учеными. Они выявили, что миостатин в значительной степени подавляется при дополнительном приеме креатина. [7]
Hulmi JJ и Tannerstedt J доказали, что протеин блокирует синтез миостатина при систематическом употреблении тренирующимися людьми. [8]

Исследованием, проведенном учеными Ноттингемского университета, установлено, что активность синтеза мышечных белков у курильщиков оказалась значительно ниже, чем у некурящих. Кроме того, в организме любителей никотина гораздо выше уровень белка миостатина и фермента MAFbx. Первый из них просто задерживает мышечный рост, а второй – расщепляет белки мышц. [9]

Анаболические препараты могут применяться только по назначению врача и противопоказаны детям. Представленная информация не призывает к применению или распространению сильнодействующих веществ и нацелена исключительно на снижение риска осложнений и побочных эффектов.
Читайте также:

