Классификация химических реакций кратко
Обновлено: 30.06.2024
Химическая реакция — это превращение одних веществ (реагентов) в другие, отличающиеся по химическому составу или строению (продукты реакции).
ПРИЗНАКИ ХИМИЧЕСКИХ РЕАКЦИЙ
Химическое превращение от физического всегда можно отличить по наличию одного или нескольких признаков:
· образование слабодиссоциированных веществ (например, воды);
· выделение энергии (тепловой или световой).
ТИПЫ КЛАССИФИКАЦИЙ ХИМИЧЕСКИХ РЕАКЦИЙ
Существует несколько подходов к классификации химических реакций, основные из них представлены на схеме ниже.
Рассмотрим их подробнее.
КЛАССИФИКАЦИЯ ПО ЧИСЛУ И СОСТАВУ РЕАГИРУЮЩИХ И ОБРАЗУЮЩИХСЯ ВЕЩЕСТВ
Первая реакция является реакцией соединения (иногда говорят присоединения), поскольку из двух веществ получается одно. Во второй реакции, наоборот, из одного вещества получается два и это реакция разложения.
В реакциях замещения простое вещество замещает один из элементов в сложном веществе, в результате чего получается новое просто вещество и новое сложное вещество. Например:
В реакциях обмена два сложных вещества обмениваются своими составными частями и образуется два новых сложных вещества:
КЛАССИФИКАЦИЯ ПО ИЗМЕНЕНИЮ СТЕПЕНИ ОКИСЛЕНИЯ
Окислительно-восстановительные реакции (ОВР) — реакции, протекающие с изменением степеней окисления элемента(ов).
В любой окислительно-восстановительной реакции (ОВР) всегда должен быть как минимум один элемент, повышающий степень окисления ( восстановитель ), и другой — понижающий степень окисления ( окислитель ).
Если элемент-окислитель и элемент-восстановитель входят в состав разных молекул, то такая ОВР называется межмолекулярной .
Если же эти элементы входят в состав одной молекулы, такие реакции называются внутримолекулярными ОВР.
6KOH(конц.)+3Cl 2 =KClO 3 +5KCl+3H 2 O
Cl 0 2+1⋅2e¯→2Cl − | 5 окислитель, процесс восстановление
Cl 0 2−5⋅2e¯→2Cl +5 | 1 восстановитель, процесс окисление
В этой реакции хлор простое вещество одновременно и окислился (до KClO3) и восстановился (до KCl). Такие реакции называются реакциями диспропорционирования.
Окислительно-восстановительные реакции, в которых один и тот же элемент одновременно и повышает, и понижает степень окисления, называются реакции диспропорционирования .
Противоположны этим реакциям реакции - реакции конпропорционирования:
S +4 +4e¯→S 0 | 1 окислитель, процесс восстановление
S −2 −2e¯→S 0 | 2 восстановитель, процесс окисление
Окислительно-восстановительные реакции, в которых один и тот же элемент одновременно и окисляется, и восстанавливается до одной степени окисления, называются реакции конпропорционирования .
Более подробно тема ОВР рассмотрена в темах "ОВР в органической химии" . "Окислительно-восстановительные реакции"
КЛАССИФИКАЦИЯ ПО ТЕПЛОВОМУ ЭФФЕКТУ
Тепловой эффект реакции — ΔH — теплота, поглощаемая или выделяемая системой в ходе химической реакции.
Вспомним, что любая химическая реакция протекает с разрывом старых химических связей и образованием новых. При этом изменяется электронное состояние атомов, их взаиморасположение, а потому и внутренняя энергия продуктов реакции отличается от внутренней энергии реагентов. Как вы знаете, в образовании связи участвуют атомные орбитали. Для молекул с ковалентной связью механизм образования химической связи объясняет метод валентных связей (ВС). Основные принципы метода ВС рассматриваются в теме "Виды, характеристики и механизмы образования химической связи". Наиболее полно особенности образования связывающих и разрыхляющих орбиталей объясняет метод молекулярных орбиталей, как линейной комбинации атомных орбиталей (МОЛКАО), изучающийся в специальном разделе химической термодинамики и в квантовой химии. Рассмотрим два принципиально возможных варианта перераспределения энергии при протекании химической реакции:
1. Е реагентов > Е продуктов . Благодаря "выигрышу" в энергии атомы соединяются и образуют молекулы. Исходя из закона сохранения энергии, в результате такой реакции избыточная энергия выделяется в окружающую среду, чаще всего в виде тепла или света.
2. Е реагентов В этом случае для протекания реакции необходима дополнительная энергия, которая может быть получена извне в виде дополнительного нагревания, УФ-облучения или в других формах. При этом температура реагирующей системы должна понижаться за счет поглощения энергии.
Экзотермические реакции — реакции, протекающие с выделением тепла (+Q)
Самые типичные экзотермические реакции — это реакции горения. Иногда энергетический "выигрыш" настолько велик, что происходит выделение и тепловой и световой энергии, что чаще всего принято называть взрывом. Например, горение метана в атмосфере воздуха.
В случае, если на образование новых химических связей требуется энергия большая, чем выделилась при разрыве старых связей, то системе требуется дополнительная подача тепла.
Эндотермические реакции — реакции, протекающие с поглощением тепла (-Q)
Существует несколько классификаций реакций, протекающих в неорганической и органической химии.
По характеру процесса
Так называют химические реакции, где из нескольких простых или сложных веществ получается одно сложное вещество. Примеры:
В результате реакции разложения сложное вещество распадается на несколько сложных или простых веществ. Примеры:
В ходе реакций замещения атом или группа атомов в молекуле замещаются на другой атом или группу атомов. Примеры:
К реакциям обмена относятся те, которые протекают без изменения степеней окисления и выражаются в обмене компонентов между веществами. Часто обмен происходит анионами/катионами:
AgF + NaCl = AgCl↓ + NaF

Окислительно-восстановительные реакции (ОВР)
-
Межмолекулярные - атомы окислителя и восстановителя входят в состав разных молекул. Примеры:

Замечу, что окислителем и восстановителем могут являться только исходные вещества (а не продукты!) Окислитель всегда понижает свою СО, принимая электроны в процессе восстановления. Восстановитель всегда повышает свою СО, отдавая электроны в процессе окисления.
От обилия информации можно запутаться. Я рекомендую сформулировать четко: "Окислитель - понижает СО, восстановитель - повышает СО". Запомнив эту информацию таким образом, вы не будете путаться.

ОВР уравнивают методом электронного баланса, с которым мы подробно познакомимся в разделе "Решения задач".
Обратимые и необратимые реакции
Обратимые реакции - такие химические реакции, которые протекают одновременно в двух противоположных направлениях: прямом и обратном. При записи реакции в таких случаях вместо знака "=" ставят знак обратимости "⇆".
Классическим примером обратимой реакции является синтез аммиака и реакция этерификации (из органической химии):
Необратимые реакции протекают только в одном направлении, до полного расходования одного из исходных веществ. Главное отличие их от обратимых реакций в том, что образовавшиеся продукты реакции не взаимодействуют между собой с образованием исходных веществ.
- Образуются малодиссоциирующие вещества (например - вода, однако есть исключения - реакция этерификации)
- Реакция сопровождается выделение большого количества тепла
- В ходе реакции образуется газ или выпадает осадок
Примеры необратимых реакций:
NaOH + HCl = NaCl + H2O (образуется вода)
2Na + 2H2O = 2NaOH + H2 (сопровождается выделением большого количества тепла)

Реакции и агрегатное состояние фаз
Фазой в химии называют часть объема равновесной системы, однородную во всех своих точках по химическому составу и физическим свойствам и отделенную от других частей того же объема поверхностью раздела. Фаза бывает жидкой, твердой и газообразной.
Все реакции можно разделить на гетеро- и гомогенные. Гетерогенные реакции (греч. heterogenes - разнородный) - реакции, протекающие на границе раздела фаз, в неоднородной среде. Скорость таких реакций зависит от площади соприкосновения реагирующих веществ.
К гетерогенным реакциям относятся следующие реакции (примеры): жидкость + газ, газ + твердое вещество, твердое вещество + жидкость. Примером такой реакции может послужить взаимодействие твердого цинка и раствора соляной кислоты:

Гомогенные реакции (греч. homogenes - однородный) - реакции, протекающие между веществами, находящимися в одной фазе.
К гомогенным реакциям относятся (примеры): жидкость + жидкость, газ + газ. Примером такой реакции может служить взаимодействие между растворами уксусной кислоты и едкого натра.

Реакции и их тепловой эффект
Все реакции можно разделить на те, в ходе которых тепло поглощается, или, наоборот, тепло выделяется. Представьте пробирку, охлаждающуюся или нагревающуюся в вашей руке - это и есть тот самый тепловой эффект. Иногда тепла выделяется так много, что реакции сопровождаются воспламенением или взрывом (натрий с водой).
Экзотермические реакции (греч. exo - вне) - химические реакции, сопровождающиеся потерей энергии системой и выделением тепла (той самой энергии) во внешнюю среду. При написании химических реакций в конце экзотермических ставят "+ Q" (Q - тепло), иногда бывает указано точное количество выделяющегося тепла. Например:
2Mg + O2 = 2MgO + Q
NaOH + HCl = NaCl + H2O + 56 кДж

К экзотермическим реакциям часто относятся реакции горения, соединения.
Исключением является взаимодействие азота и кислорода, при котором тепло поглощается:
Как уже было отмечено выше, если тепло выделяется во внешнюю среду, значит, система реагирующих веществ потеряло это тепло. Поэтому не должно казаться противоречием, что внутренняя энергия веществ в результате экзотермической реакции уменьшается.
Энтальпией называют (обозначение Н), количество термодинамической (тепловой) энергии, содержащееся в веществе. Иногда с целью "запутывания" в реакции вместо явного +Q при экзотермической реакции могут написать ΔH 0, так как внутренняя энергия веществ увеличивается. Например:
CaCO3 = CaO + CO2↑ ; ΔH > 0 (значит реакция эндотермическая, так как внутренняя энергия увеличивается)

Замечу, что не все реакции разложения являются эндотермическими. Широко известная реакция разложения дихромата аммония ("вулканчик") является примером экзотермического разложения, при котором тепло выделяется.

Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Классификация реакций
Эндотермической, обратимой Эндотермической, необратимой Экзотермической, обратимой Экзотермической, необратимой
Реакция углерода с кислородом является необратимой, сопровождается выделением тепла (процесс горения) - экзотермическая.
Горение азота в кислороде, как это ни удивительно, относится к реакции эндотермической. Это связано с наличием в азоте очень прочной тройной связи, для разрыва которой нужно приложить много усилий.
Цинк вытесняет атомы водорода из кислоты, такая реакция относится к реакциям замещения.
Обратимой, экзотермической Обратимой, эндотермической Необратимой, экзотермической Необратимой, эндотермической

Темы кодификатора ЕГЭ: Классификация химических реакций в органической и неорганической химии.
Химические реакции — это такой вид взаимодействия частиц, когда из одних химических веществ получаются другие, отличающиеся от них по свойствам и строению. Вещества, которые вступают в реакцию — реагенты . Вещества, которые образуются в ходе химической реакции — продукты .
В ходе химической реакции разрушаются химические связи, и образуются новые.
В ходе химических реакций не меняются атомы, участвующие в реакции. Меняется только порядок соединения атомов в молекулах. Таким образов, число атомов одного и того же вещества в ходе химической реакции не меняется .
Химические реакции классифицируют по разным признакам. Рассмотрим основные виды классификации химических реакций.
Классификация по числу и составу реагирующих веществ
По составу и числу реагирующих веществ разделяют реакции, протекающие без изменения состава веществ, и реакции, протекающие с изменением состава веществ:
1. Реакции, протекающие без изменения состава веществ (A → B)
К таким реакциям в неорганической химии можно отнести аллотропные переходы простых веществ из одной модификации в другую:
Sромбическая → Sмоноклинная.
В органической химии к таким реакциям относятся реакции изомериза-ции , когда из одного изомера под действием катализатора и внешних факторов получается другой (как правило, структурный изомер).
Например , изомеризация бутана в 2-метилпропан (изобутан):
2. Реакции, протекающие с изменением состава
- Реакции соединения (A + B + …→ D) — это такие реакции, в которых из двух и более веществ образуется одно новое сложное вещество. Внеорганической химии к реакция соединения относятся реакции горения простых веществ, взаимодействие основных оксидов с кислотными и др. В органической химии такие реакции называются реакциями присоединения . Реакции присоединения — это такие реакции, в ходе которых к рассматриваемой органической молекуле присоединяется другая молекула. К реакциям присоединения относятся реакции гидрирования (взаимодействие с водородом), гидратации (присоединение воды), гидрогалогенирования (присоединение галогеноводорода), полимеризация (присоединение молекул друг к другу с образованием длинной цепочки) и др.

Например , гидратация :
- Реакции разложения ( A → B + C + …) — это такие реакции, в ходе которых из одной сложной молекулы образуется несколько менее сложных или простых веществ. При этом могут образовываться как простые, так и сложные вещества.

Например , при разложении пероксида водорода:
В органической химии разделяют собственно реакции разложения и реакции отщепления . Реакции отщепления (элиминирования) — это такие реакции, в ходе которых происходит отрыв атомов или атомных групп от исходной молекулы при сохранении ее углеродного скелета.
Например , реакция отщепления водорода (дегидрирование) от пропана:
Например , реакция крекинга бутана (расщепление на более простые молекулы при нагревании или под действием катализатора):
- Реакции замещения — это такие реакции, в ходе которых атомы или группы атомов одного вещества замещаются на атомы или группы атомов другого вещества. В неорганической химии эти реакции происходят по схеме:
AB + C = AC + B .

Например , более активные галогены вытесняют менее активные из соединений. Взаимодействие йодида калия с хлором:
2KI + Cl2 → 2KCl + I2.
Замещаться могут как отдельные атомы, так и молекулы.
Например , при сплавлении менее летучие оксиды вытесняют более летучие из солей. Так, нелетучий оксид кремния вытесняет оксид углерода из карбоната натрия при сплавлении:
В органической химии реакции замещения — это такие реакции, в ходе которых часть органической молекулы замещается на другие частицы. При этом замещенная частица, как правило, соединяется с частью молекулы-заместителя.
Например , реакция хлорирования метана:
По числу частиц и составу продуктов взаимодействия эта реакция больше похожа на реакцию обмена. Тем не менее, по механизму такая реакция является реакцией замещения.
- Реакции обмена — это такие реакции, в ходе которых два сложных вещества обмениваются своими составными частями:
AB + CD = AC + BD

К реакциям обмена относятся реакции ионного обмена, протекающие в растворах; реакции, иллюстрирующие кислотно-основные свойства веществ и другие.
Пример реакции обмена в неорганической химии — нейтрализация соляной кислоты щелочью:
NaOH + HCl = NaCl + H2O
Пример реакции обмена в органической химии — щелочной гидролиз хлорэтана:
Классификация химических реакций по изменению степени окисления элементов, образующих вещества
По изменению степени окисления элементов химические реакции делят на окислительно-восстановительные реакции, и реакции, идущие без изменения степеней окисления химических элементов.
- Окислительно-восстановительные реакции (ОВР) — это реакции, в ходе которых степени окисления веществ изменяются. При этом происходит обмен электронами.
В неорганической химии к таким реакциям относятся, как правило, реакции разложения, замещения, соединения, и все реакции, идущие с участием простых веществ. Для уравнивания ОВР используют метод электронного баланса (количество отданных электронов должно быть равно количеству полученных) или метод электронно-ионного баланса.
В органической химии разделяют реакции окисления и восстановления, в зависимости от того, что происходит с органической молекулой.
Реакции окисления в органической химии — это реакции, в ходе которых уменьшается число атомов водорода или увеличивается число атомов кислорода в исходной органической молекуле.
Например , окисление этанола под действием оксида меди:
Реакции восстановления в органической химии — это реакции, в ходе которых увеличивается число атомов водорода или уменьшается число атомов кислорода в органической молекуле.
Например , восстановление уксусного альдегида водородом:
- Протолитические реакции и реакции обмена — это такие реакции, в ходе которые степени окисления атомов не изменяются.
Например , нейтрализация едкого натра азотной кислотой:
Классификация реакций по тепловому эффекту
По тепловому эффекту реакции разделяют на экзотермические и эндотермические.
Экзотермические реакции — это реакции, сопровождающиеся выделением энергии в форме теплоты (+Q). К таким реакциям относятся почти все реакции соединения.
Исключения — реакция азота с кислородом с образованием оксида азота (II) — эндотермическая:
Реакция газообразного водорода с твердым йодом также эндотермическая:
Экзотермические реакции, в ходе которых выделяется свет, называют реакциями горения.
Например , горение метана:

Также экзотермическими являются:
Эндотермические реакции — это реакции, сопровождающиеся поглощением энергии в форме теплоты (— Q). Как правило, с поглощением теплоты идет большинство реакций разложения (реакции, требующие длительного нагревания).
Например , разложение известняка:
Также эндотермическими являются:
- реакции гидролиза;
- реакции, идущие только при нагревании ;
- реакции, протекающие только при очень высоких температурах или под действием электрического разряда.
Например , превращение кислорода в озон:
В органической химии с поглощением теплоты идут реакции разложения. Например , крекинг пентана:
Классификация химических реакций по агрегатному состоянию реагирующих веществ (по фазовому составу)
Вещества могут существовать в трех основных агрегатных состояниях — твердом, жидком и газообразном. По фазовому состоянию разделяют реакции гомогенные и гетерогенные .
- Гомогенные реакции — это такие реакции, в которых реагирующие вещества и продукты находятся в одной фазе, и столкновение реагирующих частиц происходит во всем объеме реакционной смеси. К гомогенным реакциям относят взаимодействия жидкость-жидкость и газ-газ.
Например , окисление сернистого газа:
- Гетерогенные реакции — это реакции, в которых реагирующие вещества и продукты находятся в разных фазах. При этом столкновение реагирующих частиц происходит только на границе соприкосновения фаз. К таким реакциям относятся взаимодействия газ-жидкость, газ-твердая фаза, твердая-твердая, и твердая фаза — жидкость.
Например , взаимодействие углекислого газа и гидроксида кальция:
Для классификации реакций по фазовому состоянию полезно уметь определять фазовые состояния веществ. Это достаточно легко сделать, используя знания о строении вещества, в частности, о типах кристаллической решетки.
Вещества с ионной, атомной или металлической кристаллической решеткой, как правило твердые при обычных условиях; вещества с молекулярной решеткой, как правило, жидкости или газы при обычных условиях.
Обратите внимание, что при нагревании или охлаждении вещества могут переходить из одного фазового состояния в другое. В таком случае необходимо ориентироваться на условия проведения конкретной реакции и физические свойства вещества.
Например , получение синтез-газа происходит при очень высоких температурах, при которых вода — пар:
Таким образом, паровая конверсия метана — гомогенная реакция.
Классификация химических реакций по участию катализатора
Катализатор — это такое вещество, которое ускоряет реакцию, но не входит в состав продуктов реакции. Катализатор участвует в реакции, но практически не расходуется в ходе реакции. Условно схему действия катализатора К при взаимодействии веществ A + B можно изобразить так:
В зависимости от наличия катализатора различают каталитические и некаталитические реакции.
- Каталитические реакции — это реакции, которые идут с участием катализаторов. Например, разложение бертолетовой соли: 2KClO3 → 2KCl + 3O2.
- Некаталитические реакции — это реакции, которые идут без участия катализатора. Например, горение этана: 2C2H6 + 5O2 = 2CO2 + 6H2O.
Все реакции, протекающие с участием в клетках живых организмов, протекают с участием особых белковых катализаторов — ферментов. Такие реакции называют ферментативными.
Более подробно механизм действия и функции катализаторов рассматриваются в отдельной статье.
Классификация реакций по способности протекать в обратном направлении
Обратимые реакции — это реакции, которые могут протекать и в прямом, и в и обратном направлении, т.е. когда при данных условиях продукты реакции могут взаимодействовать друг с другом. К обратимым реакциям относятся большинство гомогенных реакций, этерификация; реакции гидролиза; гидрирование-дегидрирование, гидратация-дегидратация; получение аммиака из простых веществ, окисление сернистого газа, получение галогеноводородов (кроме фтороводорода) и сероводорода; синтез метанола; получение и разложение карбонатов и гидрокарбонатов, и т.д.
Необратимые реакции — это реакции, которые протекают преимущественно в одном направлении, т.е. продукты реакции не могут взаимодействовать друг с другом при данных условиях. Примеры необратимых реакций: горение; реакции, идущие со взрывом; реакции, идущие с образованием газа, осадка или воды в растворах; растворение щелочных металлов в воде; и др.
Вспомните, чем отличаются химические явления или химические реакции от физических (Конспект).

Химические реакции, протекающие
без изменения состава веществ.
Одно из положений теории химического строения утверждает, что свойства веществ зависят не только от их качественного и количественного состава, но и от строения. Следовательно, можно сделать вывод, что некоторые химические реакции могут сопровождаться изменением только качественного или только количественного состава исходных и образующихся веществ или же изменением их строения.
На примере кислорода и озона можно проиллюстрировать философский закон о переходе количественных отношений в качественные. Вспомните и сравните физические, химические и физиологические свойства кислорода и озона.
Влияние строения простых веществ, образованных одним химическим элементом на их свойства, иллюстрируют аллотропные модификации углерода.
Процесс получения искусственных алмазов моделирует природные экстремальные явления: проводится при очень высоких давлениях и температурах.
Первые сведения об аллотропии и аллотропных модификациях связаны с фосфором. В 1669 г. алхимик Хеннинг Брант, прокаливая сухой остаток мочи в попытке получить философский камень, получил белый фосфор (от греч. phos — свет и phoros — несущий), который затем превратился в красный.
Химические реакции, протекающие
с изменением состава веществ
(по признаку числа и состава реагентов и продуктов реакции).
Из курса химии основной школы вы знаете четыре типа реакций по этому признаку: соединения, разложения, замещения и обмена.
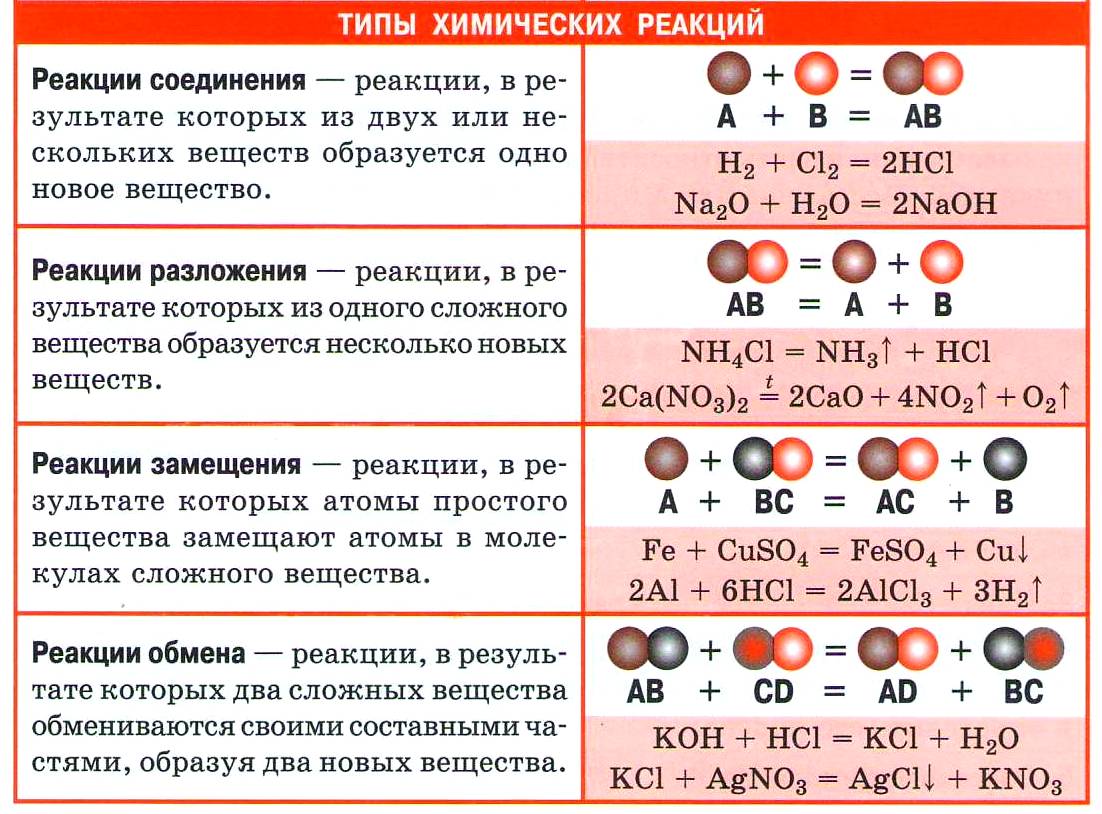
1. Реакции соединения (присоединения)
В неорганической химии весь спектр разнообразных реакций можно проиллюстрировать примерами промышленных процессов:
- Реакция горения фосфора — первая стадия получения чистой фосфорной кислоты: 4Р + 5O2 = 2Р2O5
В этом процессе участвуют два простых вещества и получается одно сложное.
- Заключительная стадия получения фосфорной кислоты описывается уравнением Р2O5 + 3Н2O = 2Н3РO4(сложное вещество образуется в результате взаимодействия двух сложных веществ).
- На заключительной стадии получения азотной кислоты в реакцию вступают три вещества (одно простое и два сложных): 4NO2 +O2 + 2Н2O = 4HNO3
В органической химии реакции соединения называются реакциями присоединения, так как к основному веществу (субстрату) присоединяется дополнительное вещество (реагент). Такие реакции характерны для непредельных углеводородов и в зависимости от реагента носят видовые названия:
- гидрирование — присоединение водорода;
- галогенирование — присоединение галогенов;
- гидрогалогенирование — присоединение галогеноводородов;
- гидратация — присоединение воды.
Частным случаем реакции присоединения является реакция полимеризации — соединение множества одинаковых молекул мономера в макромолекулу полимера.
2. Реакции разложения (отщепления)
Рассмотрим реакции разложения на примере реакций получения кислорода лабораторными способами.
Последняя реакция используется не для получения кислорода, а в медицинских целях. Полученное при разложении серебро прижигает ранки или удаляет бородавки, если используется особый ляписный (от лат. lapis infernalis — адский камень) карандаш.
В органической химии реакции разложения называют реакциями отщепления. Так, для получения этилена используются реакции дегидратации этанола, деполимеризации полиэтилена, дегидрирования этана (запишите уравнения реакций).
3. Реакции замещения
Как видно из определения, эти реакции характеризуют свойства классов простых веществ. Например, такое важное свойство галогенов, как их способность вытеснять менее активные галогены из растворов галогеноводородных кислот или их солей: Сl2 > Вг2 > I2.
Аналогично, этот тип реакций характеризует химические свойства металлов:
- Щелочные и щёлочноземельные металлы активно взаимодействуют с водой: 2Na + 2Н2O = 2NaOH + Н2↑
- С растворами кислот взаимодействуют металлы, стоящие в ряду напряжений до водорода: Zn + 2НСl = ZnCl2 + H2↑
- Металлы, стоящие в ряду напряжений до металла соли, вытесняют его из раствора соли: Fe +CuSO4 = Сu +FeSO4
- Более активные металлы вытесняют менее активные из их оксидов с выделением большого количества теплоты — металлотермия: 2Аl +Fe2O3 = Аl2O3 + 2Fe
Реакции замещения характерны для предельных соединений, например галогенирование метана, согласно цепочке переходов: СН4 –> СН3Сl –> СН2Сl2 –> СНСl3 –> ССl4.
Нитрование бензола относится к реакциям замещения, но протекает между двумя сложными веществами: С6Н6 + HNO3 —> C6H5NO2 + Н2O
В органической химии продуктами реакций этого типа являются не простое и сложное вещества, а два сложных. Кроме этого, в реакцию замещения могут вступать и сложные вещества.
4. Реакции обмена
Для растворов электролитов такие реакции протекают в соответствии с правилом Бертолле (названным по имени предложившего его французского химика Клода Бертолле) и возможны в том случае, если образуется осадок, газ или малодиссоциирующее вещество (например, вода).
- Золотисто–жёлтый осадок иодида свинца выпадает при взаимодействии растворов иодида натрия и нитрата свинца:
2NH4Cl + Са(ОН)2 = СаСl2 + 2NH3↑ + 2Н2O
NH4 + + ОН – = NH3↑ + Н2O
- Частным случаем реакции обмена является реакция нейтрализации — она протекает между растворами кислот и щелочей:
NaOH + НСl = NaCl + Н2O
OH – + H + = H2O
Химические реакции, протекающие
с тепловым эффектом.
Важный классификационный признак реакций — выделение или поглощение теплоты. Как правило, реакции соединения сопровождаются выделением теплоты. Такие реакции называются экзотермическими.
Если экзотермическая реакция сопровождается выделением света, то она называется реакцией горения: 2Mg + О2 = 2MgO + Q
Важным источником теплоты и энергии является горение углеводородов: СН4 + 2О2 –> СО2↑ + 2Н2О + Q
Но нет правил без исключения: реакция взаимодействия азота с кислородом сопровождается поглощением теплоты: N2 + О2 2NO – Q
Схематично экзо- и эндотермические реакции отражает рисунок.
Если в уравнении реакции указывается тепловой эффект, то уравнение называется термохимическим.
Например:
СН4 + 2О2 —> СO2 + 2Н2O + 800 кДж — реакция экзотермическая;
СаСO3 = СаО + СO2 – 187 кДж — реакция эндотермическая.
Классификация реакций по другим критериям
Классификация реакций — многоплановый процесс. Их можно классифицировать также:
- по направлению (обратимые и необратимые реакции);
- по использованию катализатора (каталитические и некаталитические реакции);
- по агрегатному состоянию реагентов и продуктов реакции (гомогенные и гетерогенные реакции);
- по изменению степеней окисления элементов, образующих реагенты и продукты реакции (окислительно–восстановительные и реакции, протекающие без изменения степеней окисления).

Химическая реакция — это превращение одного или нескольких исходных веществ (реагентов) в другие вещества, при этом ядра атомов не меняются, происходит только перераспределение электронов и ядер, и образуются новые химические вещества. При химических реакциях не изменяется общее число ядер атомов и изотопный состав химических элементов (в отличие от ядерных реакций).
Классификация химических реакций схема
Химические реакции классифицируются по тепловому эффекту, по изменению степени окисления атомов в реагирующих веществах, по числу и составу исходных и образующихся веществ, и по признаку обратимости.

Классификация химических реакций по числу и составу исходных и образующихся веществ
Реакция, в которой из одного исходного вещества образуется несколько новых веществ
2HgO → t → 2Hg + O2
Реакция между простым и сложным веществами, в результате которой атомы простого вещества замещают атомы одного из элементов сложного вещества
Реакция, в результате которой два вещества обмениваются своими составными частями, образуя два новых вещества
NaOH + HCl → NaCl + H2O
Реакция, в результате которой из двух или нескольких веществ образуется одно новое
Классификация химических реакций по тепловому эффекту
Тепловой эффект химической реакции — это количество теплоты (Q), которое выделяется или поглощается в химической реакции.
Реакция, проходящая с поглощением теплоты
Реакция, проходящая с выделением теплоты
Термохимическое уравнение — уравнение химической реакции, в котором указан тепловой эффект реакции:
Термохимические расчеты основаны на законе Гесса:
- тепловой эффект химической реакции зависит от состояний исходных веществ и продуктов реакций, но не зависит от промежуточных стадий процесса
- тепловой эффект химической реакции равен сумме теплот образования продуктов реакции эа вычетом суммы теплот образования исходных веществ
Классификация химических реакций по признаку обратимости
Такая реакция, которая в данных условиях протекает одновременно в двух взаимно противоположных направлениях
Такая реакция, которая в данных условиях протекает до конца, т. е. до полного превращения исходных реагирующих веществ в конечные продукты реакции
Таблица признаки необратимости реакций
Реакция идет с выделением большого количества теплоты
2Mg + O2 → 2MgO + Q
Хотя бы один продукт реакции покидает сферу реакции (выпадает в осадок или выделяется в виде газа)
В результате реакции образуются малодиссоциируе-мые вещества
HCl + NaOH → NaCl + H2O
Классификация химических реакций по изменению степени окисления
Проходящая с изменением степени окисления атомов (окислительно-восстановительная)
реакция, при которой происходит переход электронов от одних атомов, молекул или ионов к другим
- 2KI -1 + Сl 2 0 → 2КСl -1 + I 2 0
Проходящая без изменения степени окисления
Реакция, в которой степень окисления каждого атома после реакции остается неизменной
Влияние изменения условий на положение химического равновесия
Изменение условий, при которых система находится в состоянии химического равновесия
Изменение скоростей прямой и обратной реакции в начальный момент
Направление смешения положения равновесия
В большей степени возрастает скорость эндотермической реакции
В сторону эндотермической реакции
В большей степени понижается скорость эндотермической реакции
В сторону экзотермической реакции
В большей степени возрастает скорость реакции, протекающей с уменьшением числа молей газообразных веществ
В сторону уменьшения числа молей газообразных веществ в системе
В большей степени понижается скорость реакции протекающей с уменьшением числа молей газообразных веществ
В сторону увеличения числа молей газообразных веществ в системе
Возрастает скорость реакции, по которой вводимое вещество расходуется
В сторону реакции, по которой вводимое вещество расходуется
Уменьшается скорость реакции, где реагентом является вещество, концентрация которого уменьшается
В сторону реакции, по которой образуется вещество, концентрация которого уменьшается
Читайте также:

