Классификация белков биохимия кратко
Обновлено: 02.07.2024
В настоящее время еще не разработана стройная система номенклатуры и классификации белков. Традиционная классификация белков по группам, основанная, скорее, на случайных показателях (физико-химические свойства, форма молекул, локализация и происхождение, аминокислотный состав), уже не отвечает полностью возросшему уровню знаний о их структуре и функциях. Из огромного количества природных белков структура и функции расшифрованы для относительно небольшого числа (не более нескольких сотен), и поэтому структура и функции белков пока не могут служить основой для их рациональной классификации. Пожалуй, только для одной группы белков, обладающих способностью катализировать химические реакции, т.е. ферментов, разработана стройная система номенклатуры и классификации, в основу которой положены типы катализируемых химических реакций и химическая природа реагирующих веществ. Однако полностью идентифицированные до сих пор ферменты также составляют незначительную долю белков (ферментов описано более 3000). Тем не менее функциональный принцип, рекомендуемый некоторыми авторами, хотя и не может служить универсальной основой для классификации всех белков, представляет определенный интерес. В соответствии с функциональным принципом различают 12 главных классов белков: 1) каталитически активные белки (ферменты); 2) белки-гормоны (хотя есть и стероидные гормоны); 3) белки-регуляторы активности генома; 4) защитные белки (антитела, белки свертывающей и антисвертывающей систем крови); 5) токсические белки; 6) транспортные белки; 7) мембранные белки; 8) сократительные белки; 9) рецепторные белки; 10) белки-ингибиторы ферментов; 11) белки вирусной оболочки; 12) белки с иными функциями.
Были предприняты также попытки классифицировать белки, исходя из особенностей вторичной и третичной структуры. В соответствии с этим различают α-, β-, α+β- и α/β-белки. α-Белки содержат только α-спирали (не менее 60%), β-белки – только β-структуры (не менее двух антипараллельных цепей), α+β-белки – те и другие структуры в пределах одной полипептидной цепи (пример – молекулы лизоцима), а класс α/β-белков содержит множество α- и β-структур, чередующихся вдоль полипептидной цепи или домена (см. рис. 1.19). Домены создаются объединением и чередованием α-спиралей и β-слоев, между которыми открываются более рыхлые структуры.
Учитывая необходимость для студента-медика основательного знакомства с отдельными группами белков, которые могут служить предметом изучения в его будущей профессиональной деятельности (например, белки крови), приводим старую классификацию белков с краткой характеристикой новых данных о структуре, составе и свойствах отдельных представителей. Согласно этой классификации, обширный класс белковых веществ в зависимости от химического состава делят на простые и сложные белки.
Простые белки построены из остатков аминокислот и при гидролизе распадаются соответственно только на свободные аминокислоты.
Сложные белки – это двухкомпонентные белки, которые состоят из какого-либо простого белка и небелкового компонента, называемого про-стетической группой. При гидролизе сложных белков, помимо свободных аминокислот, освобождается небелковая часть или продукты ее распада.
Простые белки в свою очередь делятся на основании некоторых условно выбранных критериев на ряд подгрупп: протамины, гистоны, альбумины, глобулины, проламины, глютелины и др. Классификация сложных белков (см. главу 2) основана на химической природе входящего в их состав небелкового компонента. В соответствии с этим различают фосфопротеины (содержат фосфорную кислоту), хромопротеины (в состав их входят пигменты), нуклеопротеины (содержат нуклеиновые кислоты), гликопротеины (содержат углеводы), липопротеины (содержат липиды) и металлопротеины (содержат металлы).
Белки — природные высокомолекулярные органические соединения, построенные из остатков 20 аминокислот, которые соединены пептидными связями в полипептидные цепи. В процессах жизнедеятельности всех организмов белки выполняют структурную, регуляторную, каталитическую, защитную, транспортную, энергетическую и другие функции. Белки — основа кожи, шерсти, шелка и других натуральных материалов, важнейшие компоненты пищи человека и корма животных. Названию белки, наиболее принятому в отечественной литературе, соответствует термин протеины (от греч. proteios — первый).
Классификация белков
Белки разделяются на протеины (простые белки), состоящие только из аминокислот и при гидролизе почти не образующие других продуктов, и протеиды (сложные белки), состоящие из собственно белковой части, построенной из α-аминокислот, и из соединенной с ней небелковой части, иначе называемой простетической группой. При гидролизе протеиды кроме α-аминокислот образуют и другие вещества, например, фосфорную кислоту, глюкозу, гетероциклические соединения и т. д.
1. Протеины разделяются на группы в зависимости от их растворимости и положения изоэлектрической точки:
5) Гистоны. Менее сильные основания. Содержат значительное количество диаминокислот со свободными аминогруппами. Растворимы в воде и в разбавленных кислотах, но нерастворимы в разбавленных щелочах. Обычно представляют собой собственно белковые части сложных белков. В качестве примера можно назвать глобин – белок, входящий в состав сложного белка крови – гемоглобина.
6) Склеропротеины. Нерастворимы в воде, растворах солей, кислот и щелочей (они растворяются лишь при длительной обработке концентрированными кислотами и щелочами, причем с расщеплением молекул). Устойчивы к гидролизу. Характеризуются высоким содержанием серы. В животных организмах выполняют опорные и покровные функции; в растениях не встречаются. Представители: коллаген – белковое вещество костей, кожи, хрящей, соединительных тканей; эластин – белок стенок кровеносных сосудов, сухожилий; кератин — белок шерсти, волос, рогового вещества, ногтей, эпидермиса кожи; фиброин – белок шелка.
2. Протеиды разделяются на группы в зависимости от состава небелковой части:
2) Фосфопротеиды. Гидролизуются на простой белок и фосфорную кислоту. Слабые кислоты. Свертываются не при нагревании, а от действия кислот. К ним относятся казеин коровьего молока и вителлин – белок, входящий в состав желтка куриного яйца.
4) Хромопротеиды. Распадаются при гидролизе на простой белок и красящее вещество. Примером является гемоглобин крови; при гидролизе он расщепляется, образуя белок глобин и красящее вещество гем красного цвета.
5) Липопротеиды. Это соединения белка с липидами. Содержатся в протоплазме клеток, в сыворотке крови, в яичном желтке.
Белки классифицируются также по форме их молекул:
1) фибриллярные (волокнистые) белки, молекулы которых имеют нитевидную форму; к ним относят фиброин шелка, кератин шерсти;
2) глобулярные белки, молекулы которых имеют округлую форму; к ним относятся, например, альбумины, глобулины и ряд других, в том числе и сложные белки.

Классификация белков
Всё|Все природные белки|белки (протеины) подразделяют на два больших|больших класса:
Простые белки|белки гидролизуются кислотами или щелочами до аминокислот и не дают при гидролизе других органических и неорганических соединений. Они состоят только из остатков α-аминокислот.Классификация простых белков основана на раство-римости.
Сложные белки|белки кроме аминокислотных остатков белковой части молекулы содержат также небелковую, или простетическую группу. Простетическая группа может быть представлена химическими веществами различной природы. Сложные белки|белки подразделяются по небелковому компоненту. Полноценными называют белки|белки, содер-жащие всё|все незаменимые аминокислоты|аминокислоты. Белки|Белки, не содержащие хотя бы одну незаменимую аминокислоту, называют н е п о л н о ц е н н ы м и.
Каталитическая. Наиболее многочисленная группа белков – это белки|белки-ферменты, катализирующие биохимические реакции. С помощью белков-ферментов в живой клетке достигается законо-мерная последовательность химических превращений веществ, обеспечивающая жизнедеятельность организмов.
Запасные|Запасные белки|белки в больших|больших количествах накапливаются в клетках зерна|зёрна и семян при созревании на растении, а затем при прораста-нии зерна|зёрна и семян гидролизуются до аминокислот или молекуляр-ных пептидов, используемых затем клеткой для формирования нового растения на ранних стадиях развития. В животном орга-низме белки|белки в запас не откладываются поэтому должны поступать вместе с пищей ежедневно в необходимых количествах.
Защитные белки|белки предохраняют живой организм от разрушения или способствуют его выживанию при повреждении. Защитная функция белков – токсинов, вырабатываемых растениями, заключается в том, что они за-щищают растения от поедания их животными, а также ингибируют протеолитические ферменты насекомых-вредителей, повреждающих семена|семёна многих растений.
Структурные белки|белки входят в состав покровных тканей растений,Они составляют также структурную основу биомембран клеток, обеспечивая сохранение органеллами клетки необходимой последовательности биохимических реакций.
Сократительная и двигательная. К этим белкам|белкам относится миозин мышц.
Эти белки|белки участвуют в регуляции обменных реакций. К ним относятся многие гормоны, например инсулин, регулирующий обмен глюкозы.
Транспортные белки|белки переносят специфические молекулы или ионы. Например, гемоглобин. Свя-зывают кислород и переносят его к периферическим тканям.
Видео по теме : Классификация белков биохимия
Классификация белков биохимия

В организме человека содержится свыше 50 000 индивидуальных белков, отличающихся первичной структурой, конформацией, строением активного центра и функциями. Белки|Белки построены из 20 химически различных аминокислот, каждая из которых может занимать любое положение в полипептидной цепи. Кроме того, белки|белки различаются количеством аминокислот, из которых они построены.
Однако большинство таких белков в среде должны принимать множество конформаций с приблизительно одинаковой энергией, но разными химическими свойствами и функциями. Поэтому в эволюции, по-видимому, была отобрана лишь небольшая часть возможных вариантов белков, которые способны принимать единственную стабильную конформацию.
Таким образом, первичная структура известных белков, отобранных эволюцией, обеспечивает исключительную стабильность одной из возможных конформаций, которая и определяет особенности функционирования данного белка|белка.
Возникновение новых белков часто связано с незначительными изменениями в структуре уже имеющихся белков. Кроме того, благодаря генетическим механизмам, о которых будет сказано в разделе 4, белок|белок с полезными свойствами или основная структурная часть этого белка|белка могут входить в состав других белков. Такие белки|белки, имеющие схожую последовательность аминокислот и родственные функции, объединяют в семейства родственных белков.
А. Классификация белков
До настоящего времён нет единой и стройной классификации, учитывающей различные параметры белков. В основе имеющихся классификаций обычно лежит один признак. Так, белки|белки можно классифицировать:
- по форме молекул (глобулярные или фибриллярные);
- по молекулярной массе (низкомолекулярные, высокомолекулярные и др.);
- по химическому строению (наличие или отсутствие небелковой части);
- по выполняемым функциям (транспортные, защитные, структурные белки|белки и др.);
- по локализации в клетке (ядерные, цито-плазматические, лизосомальные и др.);
- по локализации в организме (белки|белки крови, печени, сердца|сердца и др.);
- по возможности адаптивно регулировать количество данных белков: белки|белки, синтезирующиеся с постоянной скоростью (конститутивные), и белки|белки, синтез которых может усиливаться при воздействии факторов среды|среды (индуцибельные);
- по продолжительности жизни в клетке (от очень быстро обновляющихся белков, с Т1/2 менее 1 ч, до очень медленно обновляющихся белков, Т1/2 которых исчисляют неделями и месяцами|месяцами);
- по схожим участкам первичной структуры и родственным функциям (семейства белков).
Б. Классификация белков по форме молекул
Это одна из самых старых классификаций, которая делит белки|белки на 2 группы: глобулярные и фибриллярные. К глобулярным относят белки|белки, соотношение продольной и поперечной осей которых не превышает 1:10, а чаще составляет 1:3 или 1:4, т.е. белковая молекула имеет форму эллипса. Большинство индивидуальных белков человека относят к глобулярным белкам|белкам. Они имеют компактную структуру и многие из них, за счёт удаления гидрофобных радикалов внутрь молекулы, хорошо растворимы в воде. Наглядные примеры строения и функционирования глобулярных белков — рассмотренные выше миоглобин и гемоглобины.
Фибриллярные белки|белки имеют вытянутую, нитевидную структуру, в которой соотношение продольной и поперечной осей составляет более 1:10. К фибриллярным белкам|белкам относят коллагены, эластин, кератин, выполняющие в организме человека структурную функцию, а также миозин, участвующий в мышечном сокращении, и фибрин — белок|белок свёртывающей системы крови. На примере коллагенов и эластина рассмотрим особенности строения этих белков и связь их строения с функцией.
Благодаря необъятному количеству возможных комбинаций при синтезе белка из 20 аминокислот существует множество разнообразных аминокислотных последовательностей, каждая из которых потенциально соответствует определенному белку. Все эти белки легко сгруппировать по отдельным классам, выделяя определенный признак – функцию или особенности строения.
Классификация по функции
В соответствии с биологическими функциями выделяют:
- структурные белки (коллаген, кератин),
- ферментативные (пепсин, амилаза),
- транспортные (трансферрин, альбумин, гемоглобин),
- резервно-пищевые (белки яиц и злаков),
- сократительные и двигательные (актин, миозин, тубулин),
- защитные (иммуноглобулины, тромбин, фибриноген),
- регуляторные (соматотропный гормон, адренокортикотропный гормон, инсулин).
Классификация по строению
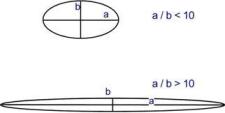
В зависимости от формы молекулы выделяют глобулярные и фибриллярные белки. В глобулярных белках соотношение продольной и поперечной осей составляет менее 10 и в большинстве случаев не более 3-4. Эти белки характеризуются компактной трехмерной укладкой полипептидных цепей. Например: инсулин, альбумин, глобулины плазмы крови.
Фибриллярные белки имеют соотношение осей более 10. Они состоят из пучков полипептидных цепей, спиралью навитых друг на друга и связанные между собой поперечными ковалентными и водородными связями. Выполняют защитную и структурную функции. Например: кератин, миозин, коллаген.
По количеству белковых цепей в одной молекуле выделяют мономерные белки, которые имеют одну субъединицу (протомер) и полимерные белки, имеющие несколько субъединиц. Например, к мономерным белкам относятся альбумины, миоглобин, к полимерным - гемоглобин (4 субъединицы), ферменты лактатдегидрогеназа и креатинкиназа (4 и 2 субъединицы, соответственно), гексокиназа (2 субъединицы). Субъединицы в белке могут быть как одинакового, так и различного строения.
Есть и более крупные белки. К ним относятся РНК-полимераза E.coli – 5 цепей, аспартаткарбамоилтрансфераза – 12 протомеров, глутаминсинтетаза – 12 протомеров, пируватдегидрогеназа – 72 белковых цепи.
По химическому составу все белки подразделяют на простые и сложные. Простые белки содержат в структуре только аминокислоты (альбумины, глобулины, гистоны, протамины). Сложные белки, кроме аминокислот, имеют небелковые компоненты:
Читайте также:

