Интенсивная терапия при чмт кратко
Обновлено: 04.07.2024
Принципы ведения пациентов с черепно-мозговой травмой. Где должны лечиться пациенты с ЧМТ?
Целью интенсивной терапии при острой травме мозга является минимизация возможных вторичных повреждений путем оптимизации мозговой перфузии и оксигенации. Несмотря на то, что большинство пациентов с острым повреждением мозга составляют пациенты с сосудистыми катастрофами, пациентами отделений реанимации чаще становятся пациенты с ЧМТ. Принципы лечения в целом одни и те же.
Несмотря на относительно высокую распространенность, неблагоприятные исходы и высокую стоимость лечения ЧМТ, надежно подтверждено лишь ограниченное число методов ведения. Исследования в этой области затрудняются разнообразием вариантов травмы, динамичностью ее развития и дефицитом совместных исследований. Поэтому подходы к лечению ЧМТ во всем мире очень разные и чаще основаны на мнении отдельных специалистов, чем на достоверных данных. Наиболее широко используемым руководством по лечению ЧМТ является серия периодических изданий фонда Brain Trauma Foundation,
Где пациенты с черепно-мозговой травмой (ЧМТ) должны проходить лечение?
Около 40% пациентов с тяжелой травмой мозга в Великобритании лечатся не в нейрохирургических центрах либо из-за трудно прогнозируемого исхода заболевания, либо в результате того, что специализированные центры не в состоянии взять на себя лечение пациентов, которые не нуждаются в нейрохирургическом вмешательстве. До сих пор ведутся споры о более неблагоприятном исходе у пациентов, проходящих лечение ЧМТ вне специализированных центров. При ЧМТ перевод в нейрохирургический центр осуществляется при наличии следующих критериев:
• Тяжелая ЧМТ (ШКГ 120 мм рт. ст., САД 70-90 мм рт.ст., ЦВД 5-10 мм рт.ст. осуществляется комбинацией внутривенного введения жидкостей и вазопрессоров (норадреналина).
• Гипертензия может усугубить вазогенный отек.
- b-блокаторы являются препаратами выбора для лечения, так как не вызывают церебральную вазодилатацию.
Нормоксия при черепно-мозговой травме (ЧМТ):
• Поддерживайте SaО2 >95%, РаО2 >13 кПа.
• Гипоксемия (SaО2
Нормогликемия при черепно-мозговой травме (ЧМТ):
• Поддерживайте сахар крови на уровне 4-8 ммоль/л путем инфузии инсулина, избегая введения растворов для инфузии, содержащих декстрозу.
• В условиях сниженного мозгового кровотока гипергликемия приводит к усилению анаэробного метаболизма и усугубляет внутриклеточный церебральный ацидоз.
Общие принципы ведения пациентов с черепно-мозговой травмой:
• Положение пациента: с приподнятым на 15-20° головным концом.
- улучшается церебральный венозный возврат без нарушения церебрального перфузионного давления.
- помогает снизить риск пневмонии связанной с ИВЛ.
• У пациентов без сознания достаточно сложно выявить повреждения шейного отдела, в этом случае следуют местным протоколам. Позвоночник должен быть обследован как можно раньше, потому что иммобилизация затрудняет уход.
• Поддержание водного баланса: изотонический раствор хлорида натрия или раствор Хартмана. Целевой показатель концентрации натрия п плазме 145-155 ммоль/л, осмолярность сыворотки крови 320 мосмоль/л. Гипернатриемия корректируется введением воды в назогастральный зонд или per rectum.
• Питание: раннее начало, предпочтительно энтеральное питание. Начинают в течение 72 часов, чтобы на 7 день перейти к полноценному питанию.
• Антибиотикопрофилактика не рекомендуется. Риск пневмонии, связанной с аспирацией, ИВЛ, травмой грудной клетки при ЧМТ высокий (70%).
• Профилактика тромбоза глубоких вен:
- Риск тромбоза глубоких вен у пациентов с ЧМТ 15-20%. Существует также риск увеличения размеров гематомы/ушиба в первые дни после травмы.
- Первые 72 часа проводится механическая профилактика (компрессионные чулки разной степени плотности, или прерывистая пневмокомпрессия), позднее—низкомолекулярный гепарин.
• Профилактика стрессовых язв:
- Риск возникновения стрессовых язв примерно 10% (язва Кушинга).
- Рекомендовано проведение стандартной профилактики (например, ранитидин, сукралфат).
• Физиотерапия, повороты пациента, уход за глазами, назначение слабительных и т.д. должны осуществляться как у всех пациентов в интенсивной терапии.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Медицинское компьютерное оборудование для диагностики функционального состояния организма у больных, здоровых и спортсменов.
Основные принципы интенсивной терапии тяжелой черепно-мозговой травмы
Лечебные мероприятия при поступлении пострадавшего в стационар.
Лечебные мероприятия при поступлении пострадавшего в стационар, заключаются в максимально полном и быстром восстановлении основных жизненно важных функций. Это прежде всего нормализация артериального давления (АД) и объема циркулирующей крови (ОЦК), показателей внешнего дыхания и газообмена, так как артериальная гипотония, гипоксия, гиперкапния относятся к вторичным повреждающим факторам усугубляющим первичное травматическое повреждение головного мозга [2;14;26;30;48;65;66]. Устранение психомоторного возбуждения, судорожных, ноцицептивных и болевых реакций оптимизируют темп и полноценность восстановления физиологических параметров.
Диагностика.
С момента поступления больного в стационар и по мере стабилизации жизненно — важных функций проводится весь необходимый комплекс диагностических мероприятий: оценка неврологического статуса, рентгенологические исследования, включая компьютерную томографию (КТ), а при ее отсутствии ЭХО-энцефалографию, наложение диагностических фрезевых отверстий, церебральную ангиографию. Реальная оценка неврологического статуса, отражающего тяжесть повреждения мозга, может быть достигнута только после восстановления жизненно — важных функций.
Наиболее важным методом диагностики при ЧМТ, является КТ, которая помимо выявления внутричерепных гематом и очагов ушибов позволяет визуализировать локализацию, распространенность и выраженность отека и набухания мозга, его дислокацию, а также оценивать эффект лечебных мероприятий при повторных исследованиях. Магнитно – резонансная томография (МРТ) дополняет КТ, в частности, в визуализации мелких структурных изменений при диффузном аксональном повреждении. МРТ также выявляет изоплотностные гематомы, позволяет дифференцировать различные виды отека мозга, а следовательно и более адекватно строить лечебную тактику [31].
В зависимости от полученных результатов обследования, больной либо может потребовать срочного хирургического вмешательства, либо продолжения интенсивной терапии. Если в течение первых суток после травмы состояние больного остается тяжелым или тяжесть его состояния нарастает, необходима повторная КТ, так как возможно отсроченное формирование внутричерепных гематом или увеличение очагов кровоизлияний, выявленных при первичной КТ. Известно, что только 84% из числа выявляемых внутримозговых гематом образуются в течение первых 12 часов после травмы [2].
Хирургическое лечение.
Показаниями к срочному нейрохирургическому вмешательству являются наличие факторов, вызывающих острое сдавление мозга, смещение срединных структур мозга с компрессией цистерн основания, проявляющееся нарастанием общемозговой и очаговой неврологической симптоматики. Это могут быть эпидуральные, внутримозговые или субдуральные гематомы, острая пневмо- и гидроцефалия, наличие вдавленного перелома и проникающего черепно-мозгового ранения [11].
При отсутствии показаний к нейрохирургическому вмешательству, и после него всем больным проводятся интенсивно-терапевтические мероприятия.
Интенсивная терапия.
Основная цель интенсивной терапии при ЧМТ заключается в поддержании нарушенных жизненно — важных функций и основных механизмов гомеостаза, создании условий для максимально полного восстановления функции мозга.
Артериальное давление и дыхание.
Одним из основных элементов интенсивной терапии является поддержание центральной гемодинамики и обеспечение адекватной вентиляции. Известно, что у больных с тяжелой ЧМТ возникновение эпизодов артериальной гипотонии (систолическое артериальное давление менее 90 mmHg) и артериальной гипоксемии (рО2 в артериальной крови менее 60 mmHg) как в ближайшие часы, так и в ближайшие сутки и даже недели после тяжелой ЧМТ, являются прогностически неблагоприятными признаками. Особенно опасны эти изменения у больных с внутричерепной гипертензией [5;33;69].
Искусственная вентиляция легких (ИВЛ) показана всем больным с тяжелой ЧМТ находящимся в коматозном состоянии (8 и менее баллов по шкале комы Глазго (ШКГ)). ИВЛ направлена на поддержание адекватного газообмена (рО2 не ниже 75 mmHg; при нормокапнии — pCO2 35 ± 2 mmHg (4-5 kPa)) [54]. Хорошо известно, что гиперкапния приводит к церебральной вазодилятации, увеличению объемного МК и повышению ВЧД. Однако, за последние годы было убедительно показано, что длительное профилактическое использование гипервентиляции с формированием выраженной гипокапнии (рСО2 менее 25 ммHg) ухудшает исходы ЧМТ [59]. Длительная (более 1 часа) гипокапния особенно опасна в первые 24 часа после травмы, так как значительно уменьшая церебральную перфузию (уменьшение объемного МК) приводит к формированию вторичного ишемического повреждения мозга [17].
Внутричерепное давление и церебральное перфузионное давление.
До настоящего времени основные методы контроля ВЧД являются инвазивными, что ограничивает их использование специальными показаниями. Ими являются наличие тяжелой ЧМТ, коматозное состояние больного (менее 8 баллов по ШКГ), патологические изменения при КТГ (контузионные очаги, гематомы, отек мозга, признаки смещения срединных структур, компрессия базальных цистерн) [3;60].
У больных в коме при нормальной КТ картине мониторинг ВЧД показан, при сочетании каких — либо двух из ниже перечисленных факторов: возраст свыше 40 лет; наличие односторонних или двухсторонних постуральных двигательных реакций; снижение систолического АД ниже 90 mmHg [61].
В настоящее время технические возможности позволяют измерять как внутрижелудочковое, так субдуральное, эпидуральное и внутритканевое давление. Наиболее часто используется внутрижелудочковый метод контроля ВЧД, поскольку это позволяет одновременно его снижать путем выведения ликвора из желудочков мозга. Однако при диффузном отеке — набухании мозга, резкое сужение боковых желудочков не позволяет использовать этот метод. В этих ситуациях контроль ВЧД может осуществляться с использованием субдуральных, эпидуральных или внутритканевых датчиков [27].
Имеются данные о том, что подержание ВЧД в пределах до 20 мм Нg достоверно улучшают исходы тяжелой ЧМТ. В связи с чем целесообразно использовать все методы интенсивной терапии для поддержания ВЧД ниже этого уровня [23;55].
Вполне очевидно, что показатель церебрального перфузионного давления (разница между средним АД и средним ВЧД) является не менее важным с точки зрения обеспечивания адекватного МК [74]. При этом полагают, что его уровень следует подерживать не ниже 70 ммНg. Так, например поддержание ВЧД в пределах до 20 mmHg, а системного АД свыше 90 mmHg не допускает снижения церебрального перфузионного давления ниже критического уровня [13;24;28;41;45;71;76].
Парентеральное и энтеральное питание при тяжелой ЧМТ.
В настоящее время доказана необходимость раннего полноценного замещения белковых и энергетических потребностей у пострадавших не позднее 72 часов после тяжелой ЧМТ [15;88]. С этой целью применяют современные средства парентерального питания, включающие полноценные растворы аминокислот и жировые эмульсии, преимуществом среди которых обладают содержащие смесь триглицеридов с длинной и средней цепями [12]. Переход на энтеральный путь введения сбалансированных пищевых продуктов ( типа Enshure, Ovolact и др.) осуществляется, по возможности, в течение первой недели после травмы, преимуществом обладает тонкокишечное питание через гастротонкокишечную стому, по сравнению с назогастральным питанием [34;39;64].
Мероприятия по лечению отека мозга и внутричерепной гипертензии.
Все мероприятия и средства реанимации и интенсивной терапии, которые используются для борьбы с внутричерепной гипертензией и отеком-набуханием мозга можно условно разделить на четыре группы [78]:
Первая группа — общереанимационые мероприятия и средства, используемые в критических ситуациях различного происхождения. Это поддержание адекватной ИВЛ и оксигенации (рО2 > 70 mmHg), поддержание системного АД, поддержание ОЦК, устранение двигательного возбуждения, судорог, предупреждение и устранение болевых и ноцицептивных реакций, поддержание нормальной температуры тела [22;82;83;86].
Вторая группа это мероприятия, которые являются специфическими для больных с тяжелой ЧМТ и включают в себя: возвышенное положение (? 30° ) головы и туловища (только при стабильном АД и нормальном ОЦК), использование умеренной гипервентиляции, применение осмотических и неосмотических диуретиков.
Необходимо восстановление и поддержание жизненно важных функций: дыхания (восстановление проходимости дыхательных путей, устранение гиповентиляционных нарушений - гипоксемии, гиперкапнии) и кровообращения (устранение гиповолемии, артериальной гипотензии и анемии (стандарт).
3.1. Мониторинг (рекомендации)
Проведение рациональной интенсивной терапии должно основываться на мониторинге жизненно важных функций. У пострадавших с угнетением бодрствования по ШКГ до 8 баллов и менее следует стремиться к осуществлению нейромониторинга, мониторинга кровообращения, дыхания и оксигенации артериальной крови и головного мозга. Оптимальными являются непрерывное измерение внутричерепного давления (ВЧД) и определение церебрального перфузионного давления (ЦПД), контроль оксигенации мозга тем или иным способом (измерение напряжения кислорода в веществе головного мозга, параинфракрасная церебральная оксиметрия или измерение насыщения гемоглобина кислородом в луковице яремной вены через ретроградно введенный катетер), мониторинг артериального давления (лучше инвазивным способом), пульсоксиметрия, мониторинг содержания углекислого газа в конечно-выдыхаемых порциях воздуха и сердечного ритма.
По возможности данный диагностический комплекс может быть расширен за счет ультразвукового исследования сосудов мозга, мониторинга центрального венозного давления, системной гемодинамики, определения кислотно-основного состояния артериальной и венозной крови, проведения тканевого микродиализа 7.
3.2. Респираторная поддержка
У пострадавшего с нарушениями бодрствования по ШКГ до 10 баллов и менее (сопор и кома) следует выполнять интубацию трахеи, проводить респираторную поддержку с целью профилактики аспирационных осложнений и обеспечения нормальной оксигенации артериальной крови и ликвидации гиперкапнии (стандарт).
Интубацию трахеи необходимо выполнять без разгибания шейного отдела позвоночника: или назотрахеальным способом, или оротрахеальным с сохранением оси позвоночника. При снижении бодрствования до сопора и комы проводят вспомогательную или контролируемую искусственную вентиляцию легких (ИВЛ) кислородно-воздушной смесью с содержанием кислорода не менее 40-50%. Для предупреждения эпизодов несинхронности респиратором с дыхательными попытками пострадавшего при проведении ИВЛ, вызывающих резкое повышение внутригрудного давления и ВЧД, необходим подбор режимов вентиляции или введение короткодействующих миорелаксантов и седативных средств. Необходимо поддерживать РаСО2 в пределах 36-40 мм рт.ст. и насыщение гемоглобина кислородом в оттекающей от мозга крови не менее 60%. Для предотвращения церебральной гипоксии все манипуляции, связанные с размыканием контура аппарата ИВЛ, должны сопровождаться пре- и постоксигенацией 100% кислородом. При проведении ИВЛ следует предупреждать гипервентиляцию и связанную с ней гипокапнию. При отсутствии признаков внутричерепной гипертензии у больных с тяжелой ЧМТ следует избегать длительной гипервентиляции (РаСО2 10 мкг/кг/мин - имеет дополнительный эффект на а1 рецепторы, вызывая вазоконстрикцию), Мезатона (0,4-5 мкг/кг/мин) и в редких случаях - Добутамина (0,5-20 мкг/кг/мин). При гиповолемии следует применять инфузию коллоидных и кристаллоидных растворов. Необходимо контролировать осмолярность и концентрацию натрия в плазме крови. Низкие значения осмолярности ( °С).
3.8.2.6. Применение гипервентиляции в лечении внутричерепной гипертензии
Гипервентиляция является временной мерой для снижения повышенного внутричерепного давления, например при транспортировке больного в операционную при неэффективности всех консервативных мер коррекции внутричерепной гипертензии. При использовании гипервентиляции следует контролировать достаточность снабжения мозга кислородом, определяя насыщение кислорода в крови в яремной вене. Нормальными считают показатели SvjO2, находящиеся в пределах 55-75%, при условии достаточной оксигенации артериальной крови. Норма PbrO2 составляет 25-35 мм рт.ст. при напряжении кислорода в артериальной крови 80-100 мм рт.ст. [1, 6, 7] (рекомендации). Гипервентиляция может быть эффективным методом коррекции ВЧГ, обусловленной гиперемией мозга [18, 32].
3.9. Роль глюкокортикоидов в остром периоде тяжелой ЧМТ
С 2000 г. до настоящего времени использование глюкокортикоидов не рекомендуется для лечения острого периода тяжелой ЧМТ, поскольку, согласно результатам ряда исследований I и II класса, они не снижают ВЧД и не улучшают исход у больных с тяжелой ЧМТ (стандарт). Рандомизированное исследование, проведенное в 2004 г. у пациентов с тяжелой ЧМТ (CRASH), выявило большую летальность в группе, получавшей высокие дозы метилпреднизолона по сравнению с плацебо. Метаанализ, опубликованный сообществом Кокрейна, указывает на наличие повышенного риска желудочно-кишечных кровотечений, гипергликемии и смертности у пациентов, получавших глюкокортикоиды.
Применение глюкокортикоидов оправдано при повреждении диэнцефальной области и связанной с этим гормональной недостаточностью.
3.10. Инфекционные осложнения у пострадавших с тяжелой ЧМТ
3.10.1. Профилактика и лечение легочных осложнений
3.10.1.1. Предотвращение аспирации содержимого ротоглотки и желудка
Необходимо проведение ранней интубации трахеи и поддержание необходимого давления в манжетах эндотрахеальных трубок (20-25 см вод.ст.). Для предотвращения аспирации используют метод постоянной надманжеточной аспирации. При продолжительности ИВЛ более 5 сут необходимо выполнение трахеостомии [10] (стандарт).
Для профилактики гастроэзофагеального рефлюкса пострадавшим необходимо придавать положение на боку с возвышенным головным концом кровати и осуществлять энтеральное питание через назоеюнальный зонд (стандарт). На поздних сроках лечения тяжелых поражений головного мозга при наличии у больного признаков дисфагии возможно осуществление чрескожной эндоскопической гастростомии (рекомендации).
3.10.1.2. Предотвращение кросс-контаминации и колонизации через руки персонала (рекомендации)
Необходимо осуществлять тщательную обработку аппаратуры для ИВЛ, фибробронхоскопов и проводить регулярный мониторинг бактериологической загрязненности аппаратов ИВЛ после стерилизации. Следует поддерживать порядок индивидуального применения аспирационных аппаратов и исключать повторное употребление санационных катетеров. По возможности следует применять специальные закрытые системы для санации трахеобронхиального дерева и комбинированные дыхательные фильтры. Санацию трахеобронхиального дерева необходимо осуществлять в стерильных перчатках. После любых манипуляций с больным следует обрабатывать руки и перчатки специальными спиртовыми дезинфицирующими растворами. Для вытирания рук после мытья проточной водой следует использовать одноразовые бумажные полотенца или салфетки.
При назначении антибактериальной терапии следует учитывать фармакокинетические свойства антибиотиков, подбирать дозы препаратов с учетом их минимально подавляющих концентраций и проводить плановую ротацию препаратов [1].
3.10.2. Профилактика и лечение внутричерепных гнойных осложнений
При плановых и экстренных нейрохирургических вмешательствах показана антибактериальная профилактика с учетом микробиологической обстановки стационара.
Нарушение правил асептики/антисептики при манипуляциях с наружным вентрикулярным дренажем является наиболее частым источником внутричерепной инфекции. Риск развития внутричерепных гнойно-воспалительных осложнений увеличивается при длительном наружном дренировании ЦСЖ [20] (рекомендации). Длительность дренирования ликвора более 14 сут сопряжена с высоким риском развития интракраниальной инфекции.
Для снижения риска развития внутричерепных гнойно-воспалительных осложнений при наружном дренировании ЦСЖ необходимо обучать персонал правилам обращения с дренирующей системой и забора анализов. Не рекомендуется рутинная замена любых элементов дренирующей системы без необходимости. Требуется строгое соблюдение замкнутости и герметичности системы на протяжении всего периода дренирования ЦСЖ. Забор анализов ЦСЖ допускается только через специальный порт, исключающий разгерметизацию и разъединение системы. При случайном разъединении любых элементов системы необходимо произвести замену всех элементов, подключаемых к наружному вентрикулярному дренажу. Забор анализов из дренажа необходимо производить с соблюдением принципов асептики и антисептики, принятых для операционных. Перед забором анализов порт забора рекомендуется в течение 3 мин обрабатывать растворами одно/многоосновных спиртов (например 70% раствор этилового спирта, раствор хлоргексидина и этилового спирта), допущенных к обработке операционного поля, или поливидин-йодином в течение 30 с [20] (опции).
В течение всего периода дренирования ЦСЖ необходимо поддерживать его ток по дренажу в направлении ликвороприемника, что снижает риск восходящей инфекции по дренажу [20] (рекомендации).
Следует избегать ретроградного тока ЦСЖ из ликвороприемника из-за повышения риска восходящей инфекции [20] (опции).
Следует избегать рутинной замены ликвороприемника, связанной с разгерметизацией всей системы дренирования. Замену ликвороприемника необходимо осуществлять при его заполнении не менее чем на ¾ объема [20] (рекомендации).
Туалет раны, включающий удаление волос и обработку растворами асептиков и антисептиков, в месте установки наружного вентрикулярного дренажа и контрапертуры должен выполняться не реже чем каждые 48 ч. Рекомендуется повязка, включающая адгезивные герметичные наклейки на обе раны [20] (опции).
Клинические признаки менингита (ригидность затылочных мышц, снижение уровня сознания, появление дисфункции черепных нервов, повышение температуры тела, в том числе периодическое) у пациентов с наружным вентрикулярным дренажем являются абсолютным показанием к исследованию ЦСЖ, включающему в себя исследование на наличие бактериальных агентов, помимо общего анализа [27] (рекомендации).
Данные лабораторных исследований, свидетельствующие о высокой вероятности интракраниальных гнойно-воспалительных осложнений: цитоз более 500/3 с количеством нейтрофилов разной степени распада более 80%; снижение соотношения глюкоза ЦСЖ/глюкоза плазмы крови менее 0,4; повышение белка ЦСЖ более 0,6‰ в сочетании с повышением лактата ликвора более 4,0 ммоль/л. Дополнительно рекомендуется принимать во внимание повышение маркеров воспалительной реакции - прокальцитонина более 2,0 мкг/л. В сложных диагностических случаях возможно исследование ЦСЖ ПЦР на ДНК наиболее вероятных возбудителей с учетом микробиологической обстановки стационара.
Анализ ЦСЖ должен быть выполнен в максимально короткие сроки после его забора, в связи с ее гипоосмолярностью и уменьшением количества клеток на 35% в течение 1-го часа и до 50% в течение 2-го часа. Рекомендуется выполнять анализ ЦСЖ с подсчетом и морфологической классификацией клеточного состава, определением уровня белка, глюкозы, лактата. В случаях инфицирования наружного вентрикулярного дренажа необходимо его удаление [20, 33]. В случаях шунтозависимого состояния необходима повторная установка дренажа через неинфицированные ткани через подкожный туннель длиной не менее 5 см. При гнойно-воспалительных осложнениях, вызванных полирезистентной Аcinetobacter, отказ от смены дренажа ассоциирован с повышением летальности [20, 33] (опции).
Получение результатов посевов ЦСЖ с определением чувствительности к антибиотикам является обязательным в лечении интракраниальных гнойно-воспалительных осложнений. В случаях невозможности проведения поясничной пункции или забора ЦСЖ из вентрикулярного дренажа, а также до получения результатов посевов ЦСЖ необходимо проведение эмпирической антибиотикотерапии. Предпочтительной эмпирической терапией является терапия с парентеральным введением цефтриаксона (2 г каждые 12 ч) или цефотаксима (2 г каждые 6 ч). Альтернативной схемой эмпирической терапии является меропенем (2 г каждые 8 ч) в сочетании с ванкомицином (60 мг на 1 кг массы тела в сутки - длительная инфузия). Данная схема эмпирической терапии является предпочтительной в стационарах с высокой частотой встречаемости пенициллин-резистентной и/или цефалоспорин-резистентной внутрибольничной инфекции [26]. В особых случаях при тяжелом течении менингита и отсутствии противопоказаний возможно интратекальное введение антибактериальных препаратов. Возможно интратекальное введение специально адаптированных к интратекальному введению солей антибиотиков: ванкомицин (10-20 мг/сут), гентамицин (4-8 мг/сут), тобрамицин (5-20 мг/сут), амикацин (5-30 мг/сут), поимиксин В (5 мг/сут), колистин (10 мг/сут) [33]. После интратекального введения антибиотиков наружный дренаж следует держать закрытым в течение не менее 1 ч [20]. Пациенты, которым антибактериальная терапия проводится интратекально, должны быть под постоянным наблюдением на предмет развития нейротоксичности: усугубление менингеальных симптомов, угнетение уровня сознания, фокальные или генерализованные судорожные приступы [20, 33] (опции).
3.11. Питание пострадавших с тяжелой ЧМТ
Необходимо раннее проведение соответствующей потребностям больного в белке и энергии нутритивной поддержки пострадавших с ЧМТ, находящихся в критическом состоянии. Базовый энергообмен у пострадавших с тяжелой ЧМТ соответствует 20-25 ккал/кг в сутки. Для точной оценки энергопотребности больных необходимо использовать метод непрямой калориметрии. При отсутствии метаболографа энергетические потребности пациентов рассчитывают по формулам. Питание можно осуществлять как энтерально, так и парентерально. Преимуществами энтерального питания перед парентеральным являются меньший риск развития гипергликемии и инфекционных осложнений. Для проведения энтерального питания устанавливают назо- или орогастральный зонд. При неэффективности гастрального варианта питания более 2 сут проводят установку тонкокишечного зонда. В таком случае для питания больных следует использовать специальные полуэлементные смеси. При необходимости длительного энтерального зондового питания более 4 нед возможно наложение гастростомы [1, 26, 34-36] (рекомендции).
3.12. Противосудорожная терапия
ЧМТ является основной причиной развития эпилепсии среди пациентов среднего возраста. К посттравматическим судорогам относят однократные или повторные судороги, впервые развившиеся после ЧМТ. Различают судороги острейшего периода (в первые 12 ч), раннюю (первые 7 сут) и позднюю (более 1 нед) посттравматическую эпилепсию. При этом, особенно в остром периоде травмы, должны быть исключены другие потенциальные причины развития судорожного синдрома, такие как электролитные нарушения, алкогольная интоксикация, наличие эпилепсии в анамнезе и др. Диагноз эпилепсии может быть установлен на основании клинической картины приступа (согласно описанию очевидцев или видео приступа), подтвержденной данными рутинной ЭЭГ, видео-ЭЭГ мониторинга в течение 24-72 ч, а также измерения уровня пролактина в плазме крови в первый час после приступа.
Эпилептический статус - генерализованный судорожный приступ длительностью более 5 мин или серия приступов, между которыми пациент не приходит в сознание. Эпи-статус требует немедленного купирования путем введения противоэпилептических препаратов. Купирование судорог следует начинать с препаратов для внутривенного введения. При отсутствии внутривенной формы препарата его вводят через желудочный зонд. При неэффективности монотерапии необходимо использовать комбинацию антиконвульсантов. Миорелаксанты не являются противосудорожными препаратами и купируют только мышечный компонент судорог и применяются временно в случае необходимости синхронизации больного с аппаратом ИВЛ.
Результатами исследований I класса доказано, что профилактическое использование фенитоина, карбамазепина, фенобарбитала или вальпроатов неэффективно для предупреждения поздней посттравматической эпилепсии (стандарт). В остром периоде ЧМТ рекомендуется назначать противосудорожные препараты (фенитоин и карбамазепин) у пострадавших с высоким риском развития ранних судорожных припадков. К факторам риска относятся наличие корковых контузионных очагов, вдавленных переломов черепа, внутричерепных гематом, проникающая ЧМТ, развитие судорожного припадка в первые 24 ч после травмы (опции). При постановке диагноза посттравматическая эпилепсия назначается противоэпилептическая терапия, отмена которой может быть произведена постепенно при условии отсутствия приступа на протяжении двух лет (опция).
3.13. Нейропротективная терапия в остром периоде тяжелой ЧМТ
В отличие от экспериментальных исследований, доказательства эффективности нейропротективных препаратов к клинической практике крайне ограничены. Среди возможных нейропротективных агентов рассматривались молекулы с различной биохимической направленностью: инактиваторы свободнорадикальных механизмов (полиэтиленгликоль супероксиддесмутаза - ПЭГ СОД, альфа-токоферол, мелатонин и др.), инактиваторы карбоксильных групп (Д-пеницилламин, карнозин, аминогуанидин), активаторы синтеза глутатиона (N-ацетилцистеин, гамма-глутамилцистеина этиловый эфир), стероиды (прогестерон, метилпреднизолон), блокаторы кальциевых каналов (нимодипин), иммуносупрессоры (циклоспорин А), модуляторы эксайтотоксичности.
Лишь некоторые из вышеперечисленных молекулярных агентов были апробированы в клинических исследованиях у пациентов с тяжелой ЧМТ. Одним из первых была исследована ПЭГ-СОД, причем вторая фаза испытаний показала ее положительный эффект на снижение частоты развития неблагоприятных исходов (персистирующего вегетативного состояния и смерти) по сравнению с плацебо, однако это не получило подтверждения в третьей фазе. Во второй фазе испытаний (SYNAPSE) прогестерон показал хорошую эффективность в отношении снижения смертности и улучшения исходов по ШИГ на 3-й и 6-й месяц после травмы по сравнению с плацебо, однако результаты третьей фазы (PROTECT III) не выявили различий между группами. Аналогично многообещающие результаты показало исследование второй фазы циклоспорина А, однако третья фаза завершится только в 2018 г. Метаанализ, проведенный сообществом Кокрейна в отношении нимодипина, установил возможность его использования для уменьшения риска летального исхода только для группы пациентов с субарахноидальным кровоизлиянием. Эффективность антагонистов брадикинина (Делтибанта), модуляторов эксайтотоксичности (Дексанабинола), сульфата магния и его аналога селфотеля была опровергнута проведенными клиническими исследованиями.
Таким образом, из всех немногих исследованных нейропротективных агентов, дошедших до третьей фазы испытаний в реальной клинической практике, эффективность не показал ни один. Однако оставшиеся агенты требуют планирования и проведения новых мультицентровых рандомизированных плацебо-контролируемых исследований. Однако существенным и трудно преодолимым ограничением для их использования является чрезвычайно узкое терапевтическое окно.
Закрытая черепно-мозговая травма (ЗЧМТ) - повреждение черепа и мозга, которое не сопровождается нарушением целостности мягких тканей головы и/или апоневротическим растяжением черепа.
К открытой ЧМТ относятся повреждения, которые сопровождаются нарушением целостности мягких тканей головы и апоневротического шлема черепа и/или
соответствуют зоне перелома.
К проникающим повреждениям относят такую ЧМТ, которая сопровождается переломами костей черепа и повреждением твердой мозговой оболочки мозга с возникновением ликворных свищей (ликвореей).
Код протокола: E-008 "Закрытая черепно-мозговая травма (сотрясение головного мозга, ушиб головного мозга, внутричерепные гематомы и т.д.)"
Профиль: скорая медицинская помощь
Классификация
1. Первичные – повреждения обусловлены непосредственным воздействием травмирующих сил на кости черепа, мозговые оболочки и мозговую ткань, сосуды мозга и ликворную систему.
2. Вторичные – повреждения не связаны с непосредственным повреждением мозга, но обусловлены последствиями первичного повреждения мозга и развиваются в основном по типу вторичных ишемических изменений мозговой ткани (внутричерепные и системные).
Внутричерепные – цереброваскулярные изменения, нарушения ликвороциркуляции, отек мозга, изменения внутричерепного давления, дислокационный синдром.
Системные – артериальная гипотензия, гипоксия, гипер- и гипокапния, гипер- и гипонатриемия, гипертермия, нарушение углеводного обмена, ДВС-синдром.
По тяжести состояния больных с ЧМТ – основывается на оценке степени угнетения сознания пострадавшего, наличии и выраженности неврологических симптомов, наличии или отсутствии повреждения других органов. Наибольшее распространение получила шкала комы Глазго (предложенная G. Teasdale и B. Jennet 1974г.). Состояние пострадавших оценивают при первом контакте с больным, через 12 и 24 часа по трем параметрам: открыванию глаз, речевому ответу и двигательной реакции в ответ на внешнее раздражение.
Выделяют классификацию нарушений сознания при ЧМТ, основанную на качественной оценке степени угнетения сознания, где существуют следующие градации состояния сознания:
К легким ЗЧМТ относят сотрясение головного мозга и ушиб головного мозга легкой степени.
ЗЧМТ средней степени тяжести – ушиб головного мозга средней тяжести.
К тяжелой ЗЧМТ относят ушиб головного мозга тяжелой степени и все виды сдавления головного мозга.
- отсутствие вторичной (дислокационной) неврологической симптоматики, отсутствие или нерезкая выраженность первичных полушарных и краниобазальных симптомов. Угроза для жизни отсутствует, прогноз восстановления трудоспособности обычно хороший.
- очаговые симптомы – могут быть выражены те или иные полушарные и краниобазальные симптомы. Иногда наблюдаются единичные, мягко выраженные стволовые симптомы (спонтанный нистагм и др.).
Для констатации состояния средней степени тяжести достаточно иметь один из указанных параметров. Угроза для жизни незначительная, прогноз восстановления трудоспособности чаще благоприятный.
- очаговые симптомы – стволовые умеренно выражены (анизокория, легкое ограничение взора вверх, спонтанный нистагм, контралатеральная пирамидная недостаточность, диссоциация менингеальных симптомов по оси тела и др.); могут быть резко выражены полушарные и краниобазальные симптомы, в том числе эпилептические припадки, парезы и параличи.
Для констатации тяжелого состояния допустимо иметь указанные нарушения хотя бы по одному из параметров. Угроза для жизни значительная, во многом зависит от длительности тяжелого состояния, прогноз восстановления трудоспособности чаще неблагоприятный.
- очаговые симптомы – стволовые выражены четко (парез взора вверх, выраженная анизокория, дивергенция глаз по вертикали или горизонтали, тонический спонтанный нистагм, ослабление реакции зрачков на свет, двусторонние патологические рефлексы, децеребрационная ригидность и др.); полушарные и краниобазальные симптомы резко выражены (вплоть до двусторонних и множественных парезов).
При констатации крайне тяжелого состояния необходимо иметь выраженные нарушения по всем параметрам, причем по одному из них обязательно предельное, угроза для жизни максимальная. Прогноз восстановления трудоспособности чаще неблагоприятный.
- очаговые симптомы – стволовые в виде предельного двустороннего мидриаза, отсутствие роговичных и зрачковых реакций; полушарные и краниобазальные обычно перекрыты общемозговыми и стволовыми нарушениями. Прогноз выживания больного неблагоприятный.
1. Сотрясение головного мозга – состояние, возникающее чаще вследствие воздействия небольшой травмирующей силы. Встречается почти у 70% пострадавших с ЧМТ. Сотрясение характеризуется отсутствием утраты сознания или кратковременной утратой сознания после травмы: от 1-2 до 10-15 минут. Больные жалуются на головные боли, тошноту, реже - рвоту, головокружение, слабость, болезненность при движении глазных яблок.
Может быть легкая асимметрия сухожильных рефлексов. Ретроградная амнезия (если она возникает) кратковременна. Антероретроградной амнезии не бывает. При сотрясении мозга указанные явления вызваны функциональным поражением головного мозга и по прошествии 5-8 дней проходят. Для установления диагноза необязательно наличие всех указанных симптомов. Сотрясение головного мозга является единой формой и не подразделяется на степени тяжести.
2. Ушиб головного мозга – это повреждение в виде макроструктурной деструкции вещества мозга, чаще с геморрагическим компонентом, возникшим в момент приложения травмирующей силы. По клиническому течению и выраженности повреждения мозговой ткани, ушибы мозга разделяют на ушибы легкой, средней и тяжелой степени.
3. Ушиб мозга легкой степени (10-15% пострадавших). После травмы отмечается утрата сознания от нескольких минут до 40 мин. У большинства имеется ретроградная амнезия на период до 30 мин. Если возникает антероретроградная амнезия, то она непродолжительна. После восстановления сознания пострадавший жалуется на головную боль, тошноту, рвоту (часто повторную), головокружение, ослабление внимания, памяти.
Могут выявляться - нистагм (чаще горизонтальный), анизорефлексия, иногда легкий гемипарез. Иногда появляются патологические рефлексы. Вследствие субарахноидального кровоизлияния может выявляться легко выраженный менингеальный синдром. Может наблюдаться бради- и тахикардия, транзиторное увеличение артериального давления на 10-15 мм рт. ст. Симптоматика регрессирует обычно в течение 1-3 недель после травмы. Ушиб головного мозга легкой степени тяжести может сопровождаться переломами костей черепа.
4. Ушиб головного мозга средней степени тяжести. Утрата сознания длится от нескольких десятков минут до 2-4 часов. Угнетение сознания до уровня умеренного или глубокого оглушения может сохраняться в течение нескольких часов или суток. Наблюдается выраженная головная боль, часто повторная рвота. Горизонтальный нистагм, ослабление реакции зрачков на свет, возможно нарушение конвергенции.
Отмечаются диссоциация сухожильных рефлексов, иногда умеренно выраженный гемипарез и патологические рефлексы. Могут быть нарушения чувствительности, речевые расстройства. Менингеальный синдром умеренно выражен, а ликворное давление умеренно повышено (за исключением пострадавших, у которых имеется ликворея).
Имеется тахи- или брадикардия. Нарушения дыхания в виде умеренного тахипноэ без нарушения ритма и не требует аппаратной коррекции. Температура субфебрильная. В 1-е сутки могут быть - психомоторное возбуждение, иногда судорожные припадки. Имеется ретро- и антероретроградная амнезия.
5. Ушиб мозга тяжелой степени. Утрата сознания длится от нескольких часов до нескольких суток (у части больных с переходом в апаллический синдром или акинетический мутизм). Угнетение сознания до сопора или комы. Может быть выраженное психомоторное возбуждение, сменяющееся атонией.
Выражены стволовые симптомы – плавающие движения глазных яблок, разностояние глазных яблок по вертикальной оси, фиксация взора вниз, анизокория. Реакция зрачков на свет и роговичные рефлексы угнетены. Глотание нарушено. Иногда развивается горметония на болевые раздражения или спонтанно. Двусторонние патологические стопные рефлексы. Имеются изменения мышечного тонуса, часто – гемипарез, анизорефлексия. Могут быть судорожные припадки.
Нарушение дыхания – по центральному или периферическому типу (тахи- или брадипноэ). Артериальное давление или повышено, или снижено (может быть нормальным), а при атонической коме нестабильно и требует постоянной медикаментозной поддержки. Выражен менингеальный синдром.
К особой форме ушибов мозга относится диффузное аксональное повреждение мозга. Его клинические признаки включают нарушение функции мозгового ствола – угнетение сознания до глубокой комы, резко выраженное нарушение витальных функций, которые требуют обязательной медикаментозной и аппаратной коррекции.
Летальность при диффузном аксональном повреждении мозга очень высока и достигает 80-90%, а у выживших развивается апаллический синдром. Диффузно аксональное повреждение может сопровождаться образованием внутричерепных гематом.
В генезе сдавления мозга ведущую роль играют вторичные внутричерепные механизмы. К нарастающим сдавлениям относятся все виды внутричерепных гематом и ушибы мозга, сопровождающиеся масс-эффектом.
Гематомы могут быть: острыми (первые 3 суток), подострыми (4 сут.-3 недель) и хроническими (позже 3 недель).
Классическая клиническая картина внутричерепных гематом включает наличие светлого промежутка, анизокорию, гемипарез, брадикардию, которая встречается реже. Классическая клиника характерна для гематом без сопутствующего ушиба мозга. У пострадавших с гематомами в сочетании с ушибом головного мозга уже с первых часов ЧМТ имеются признаки первичного повреждения мозга и симптомы сдавления и дислокации мозга, обусловленные ушибом мозговой ткани.
Факторы и группы риска
Диагностика
Диагностические критерии
Несомненно, обязательным является оценка уровня сознания, наличия менингеальных симптомов, состояния зрачков и их реакция на свет, функции черепных нервов и двигательных функций, неврологических симптомов, повышение внутричерепного давления, дислокация мозга, развитие острой ликворной окклюзии.
Лечение
Выбор тактики лечения пострадавших определяют характером повреждения головного мозга, костей свода и основания черепа, сопутствующей внечерепной травмой и развитием осложнений вследствие травмы.
Основная задача при оказании первой помощи пострадавшим с ЧМТ – не допустить развития артериальной гипотензии, гиповентиляции, гипоксии, гиперкапнии, так как эти осложнения приводят к тяжелым ишемическим поражениям мозга и сопровождаются высокой летальностью.
В (breathing) – восстановление адекватного дыхания: устранение обструкции дыхательных путей, дренирование плевральной полости при пневмо-, гемотораксе, ИВЛ (по показаниям).
С (circulation) – контроль за деятельностью сердечно-сосудистой системы: быстрое восстановление ОЦК (переливание растворов кристаллоидов и коллоидов), при недостаточности миокарда – введение инотропных препаратов (допамин, добутамин) или вазопрессоров (адреналин, норадреналин, мезатон). Необходимо помнить, что без нормализации массы циркулирующей крови введение вазопрессоров опасно.
Показанием к интубации трахеи и проведению ИВЛ являются апноэ и гипоапноэ, наличие цианоза кожи и слизистых оболочек. Интубация через нос имеет ряд преимуществ, т.к. при ЧМТ не исключается вероятность шейно-спинальной травмы (и поэтому же всем пострадавшим до уточнения характера травмы на догоспитальном этапе необходимо фиксировать шейный отдел позвоночника, накладывая специальные шейные воротники). Для нормализации артериовенозной разницы по кислороду у пострадавших с ЧМТ целесообразно применение кислородно-воздушной смеси с содержанием кислорода до 35-50%.
Обязательным компонентом лечения тяжелой ЧМТ является устранение гиповолемии, и с этой целью обычно жидкость вводят в объеме 30-35 мл/кг в сутки. Исключением являются больные с острым окклюзионным синдромом, у которых темп продукции ЦСЖ напрямую зависит от водного баланса, поэтому у них оправдана дегидратация, позволяющая снижать ВЧД.
Для профилактики внутричерепной гипертензии и ее повреждающих головной мозг последствий на догоспитальном этапе применяют глюкокортикоидные гормоны и салуретики.
Глюкокортикоидные гормоны предупреждают развитие внутричерепной гипертензии за счет стабилизации проницаемости гематоэнцефалического барьера и уменьшения транссудации жидкости в ткань мозга.
На догоспитальном этапе целесообразно внутривенное или внутримышечное введение преднизолона в дозе 30 мг.
Однако следует иметь в виду, что из-за сопутствующего минералокортикоидного эффекта преднизолон способен задерживать в организме натрий и усиливать элиминацию калия, что неблагоприятно сказывается на общем состоянии больных с ЧМТ.
Поэтому предпочтительнее использование дексаметазона в дозе 4-8 мг который практически не обладает минералокортикоидными свойствами.
При отсутствии нарушений кровообращения одновременно с глюкокортикоидными гормонами для дегидратации мозга возможно назначение быстродействующих салуретиков, например, лазикса в дозе 20-40 мг (2-4 мл 1% раствора).
Ганглиоблокирующие препараты при высокой степени внутричерепной гипертензии противопоказаны, так как при снижении системного кровяного давления может развиться полная блокада мозгового кровотока за счет сдавления капилляров мозга отечной мозговой тканью.
Для снижения внутричерепного давления - как на догоспитальном этапе, так и в стационаре - не следует пользоваться осмотически активными веществами (маннит), ибо при поврежденном гематоэнцефалическом барьере создать градиент их концентрации между веществом мозга и сосудистым руслом не удается и вероятно ухудшение состояния больного из-за быстрого вторичного повышения внутричерепного давления.
Исключение - угроза дислокации головного мозга, сопровождающаяся тяжелыми нарушениями дыхания и кровообращения.
В этом случае целесообразно внутривенное введение маннита (маннитола) из расчета 0,5 г/кг массы тела в виде 20% раствора.
Черепно-мозговая травма – наиболее частая причина смерти у лиц молодого возраста. Летальность при тяжелой ЧМТ (3-8 баллов ШГ) остается на очень высоком уровне – 30-50%.
Таблица 1. Шкала Глазго
на словесную ко-манду
выполнение сло-весной команды
сгибание конеч-ности на боль
разгибание ко-нечности на боль
Всего 3-15 баллов.
Соответствие характеристик по шкале Глазго с традиционными методами.
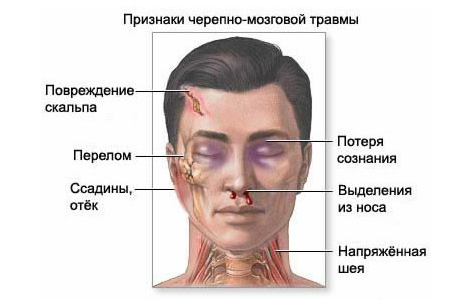
Ведение больных с ЧМТ
При нарушении функций жизненно важных органов обследованию должны предшествовать неотложные мероприятия – интубация трахеи, проведение ИВЛ, введение вазопрессоров. Сбор информации врачи проводят по схеме: Кто? Где? Когда? Что произошло? Из-за чего, после чего? Что было раньше?
Далее нужно определить глубину нарушения сознания по шкале Глазго.
Клинические проявления (симптомы) ЧМТ тяжелой степени в остром периоде
(первый период)
Критерии: 3-8 баллов по шкале Глазго. Поражаются верхние и нижние отделы головного мозга, продолговатый мозг.
Клиника: кома, реже глубокий сопор, нормотермия или гипертермия, снижение или повышение АД и ЧСС, нарушение ритма дыхания. Нейродистрофические изменения внутренних органов, кожных покровов, асимметрия АД.
Ориентировочная продолжительность этого периода 7-14 дней.
Клинические проявления ЧМТ средней степени тяжести в остром периоде (первый период)
Критерии: 9-12 баллов по шкале Глазго. Поражаются большие полушария, экстрапирамидная система.
Клиника: сопор, гипокинезия, гипомимия, каталептическое состояние, повышение тонуса мышц конечностей, гипертермия от 37°С до 38,5°С, артериальное давление, ЧСС нормальные или умеренно повышены, наблюдается асимметрия рефлексов.
Обследование
Больные должны подвергаться динамическому неврологическому наблюдению и инструментальным методам обследования:
- сразу при поступлении в отделение;
- повторно через 3 часа;
- затем ежесуточно;
- в случае ухудшения состояния – незамедлительно;
- неврологическое обследование (невропатолог);
- компьютерная томография головы – если такая возможность имеется;
- рентгенография грудной клетки, черепа в двух проекциях, шейного отдела позвоночника;
- эхоэнцефалоскопия (если КТ не выполнена);
- люмбальная пункция, если другие методы не дают достаточной информации или подозревается менингит.
Внимание! Почти каждый десятый пациент с тяжелой черепно-мозговой травмой, одновременно имеет и повреждение шейного отдела позвоночника. Пока повреждение позвоночника не будет исключено, следует вести как больного, имеющего травму позвоночника.
Соответственно, все больные с ЧМТ должны быть в воротниках-фиксаторах шейного отдела до момента исключения повреждения шейного отдела позвоночника.
Лабораторное обследование:
- общий анализ крови и мочи,
- гематокрит,
- глюкоза,
- мочевина,
- креатинин крови,
- газы крови и КОС,
- электролиты крови (натрий, калий, магний),
- осмолярность крови.
- кровь и моча на содержание алкоголя, токсических веществ.
Мониторинг
Наряду со стандартным мониторингом (неинвазивное АД, ЧСС, ЧД, сатурация крови, ЭКГ и т.д.), у пациентов с поражениями мозга должен проводиться нейро-мониторинг. Во всех развитых странах общепризнанными методами мониторинга являются: непрерывное измерение внутричерепного давления, контроль оксигенации мозга, тканевой микродиализ, измерение мозгового кровотока и многие другие.
Именно на основе этих данных и строится лечение больных с черепно-мозговой травмой. И, в первую очередь, благодаря внедрению современного нейромониторинга, была снижена смертность и инвалидность в этой группе больных. Но в маленьких городах и, тем более селах, использовать эти методы нет никакой возможности.
Анестезиологическое пособие
- Гиперкапнии следует избегать. Лучше использовать полуоткрытый контур, большую скорость подачи газовой смеси (>6 л/мин), если нет капнографического контроля;
- Режим нормовентиляции, при необходимости, умеренной гипервентиляции (РаСO2, PetCO2 32-40 мм рт. ст.);
- Тотальная внутривенная анестезия на основе пропофола – анестезия выбора, если нет грубых гемодинамических нарушений. Также используют тиопентал натрия, наркотические анальгетики, бензодиазепины, изофлуран, севофлуран, оксибутират натрия. Натрия хлорид 0,9% – в качестве основного препарата для инфузии;
- 3-7,5% раствор натрия хлорида (HS) при признаках внутричерепной гипертензии.
Нельзя использовать:
- фторотан,
- закись азота,
- р-ры глюкозы,
- кетамин,
- растворы альбумина и ГЭК,
- декстраны.
Доказано, что систематическое применение растворов альбумина при ЧМТ может увеличивать ранние смертельные исходы.
Особенности лечения при сочетанной травме
При сочетанной травме, наряду с традиционными мероприятиями (инфузионная терапия, восполнение кровопотери) использовать раннее назначение ингибиторов фибринолиза: болюс транексамовой кислоты 10-15 мг/кг за 10 минут, затем инфузия 1 г в течение 8 часов. Это позволяет уменьшить кровопотерю, и, возможно, и объем внутричерепного кровотечения. Избегать даже кратковременных эпизодов гипотонии. При необходимости, наряду с инфузионной терапией, ис-пользовать введение вазопрессоров.
Среднее артериальное давление нужно поддерживать чуть выше 90 мм рт. ст.
После окончания хирургического вмешательства осуществляют перевод пацинта в палату интенсивной терапии на управляемом дыхании.
Острый период ТЧМТ. Лечение
Первичное повреждение мозга, которое произошло в момент травмы, уменьшить врачи не могут. Лечение должно быть направлено на предотвращение вторичных повреждений мозга, которые развиваются уже после получения человеком травмы. Многие факторы могут способствовать возникновению их. В первую очередь это гипотензия, гипоксия, повышенное внутричерепное давление. Начать терапию нужно именно с их коррекции.
Первоочередные мероприятия
Больному нужно придать полусидячее положение с приподнятым головным концом кровати на 25-45 градусов. При наличии у пацинта проявлений аспирационного синдрома и нарушенного сознания (кома, глубокий сопор) — рекомендуется срочная интубация трахеи и проведение санации трахеобронхиального дерева. При наличии в аспирируемой жидкости твердых частиц пищи, прогрессировании острой дыхательной недостаточности, необходима экстренная лечебно-диагностическая бронхоскопия.
Следующие параметры гомеостаза нужно контролировать и поддерживать до выхода больного из тяжелого состояния:
- РаO2 не ниже 70 мм рт. ст;
- РаСO2 в пределах 36-40 мм рт. ст;
- petCO2 35-40 мм рт. ст;
- SpO2 90-98 %;
- систолическое АД в пределах 100-160 мм рт. ст;
- среднее артериальное давление 85-95 мм рт. ст;
- водный баланс ±500 мл;
- натрий крови 140-155 ммоль/л;
- pH 7,35-7,45;
- магний крови 0.75-1.0 ммоль/л;
- глюкоза крови 4,6-10 ммоль/л;
- осмолярность крови 290-300 мосм/л;
- гематокрит 30-35 процентов;
- Нb не ниже 90-100 г/л;
- температура тела не выше 37,5°С;
- внутричерепное давление 1
Читайте также:

