Химические свойства газов кратко
Обновлено: 05.07.2024
Любое газовое топливо представляет собой смесь различных простых горючих и балластных газов. Химические свойства газа определяют свойства смеси, т. е. газового топлива.
Алканы, т. е. углеводороды предельного ряда, являются основными составляющими горючей части природных и попутных газов. Алканы нередко называют парафинами или углеводородами метанового ряда. Общая химическая формула алканов - СnН2n+2. Родоначальником ряда алканов является метан - СН4, далее, по мере увеличения числа атомов углерода в молекуле, следуют: этан - С2Н6, пропан - С3Н8, бутан - С4Н10, пентан - C5H12, гексан - С6Н14 и т. д.
Физические и химические свойства газа предельных углеводородов закономерно изменяются по мере увеличения их молекулярного веса.
В нормальных условиях, т. е. при температуре 0° С и давлении 760 мм рт. ст., первые члены ряда до бутана включительно - газы, не имеющие цвета и запаха, последующие - жидкости. Все алканы, кроме метана, имеют плотность выше плотности воздуха.
Под действием высокой температуры алканы расщепляются, переходят в более простые и стойкие соединения (например, метан, а также алкены), выделяя сажистый углерод и водород. Стойкость алканов против воздействия температуры снижается с увеличением молекулярной массы.
Содержание углеводородов тяжелее бутана - пентана даже в "сыром" природном газе (т. е. не подвергавшемся обработке) незначительно, поэтому при расчетах химические свойства газа ограничиваются пентаном, суммируя с ним все последующие углеводороды.
Алканы, как и продукты их полного сгорания, не являются ядовитыми. Имеются данные, что высокомолекулярные предельные углеводороды при больших концентрациях в воздухе обладают слабым наркотическим действием.
Алкены, или олефины, входят в заметных количествах в состав искусственных газов, особенно газов крекинга жидкого топлива. Родоначальником ряда алкенов является этилен. Общая химическая формула алкенов - СnН2n- Первые три члена этого ряда - этилен (этен) - С2Н4, пропилен (пропен) - С3Н6 и бутилен (бутен) - С4Н8.
Алкены, являющиеся непредельными углеводородами, представляют собой ценное сырье для химической промышленности.
Токсическое действие алкенов сходно с действием алканов, т. е. при высоких концентрациях они обладают наркотическими свойствами.
Водород Н2 имеется во всех искусственных газах. Это горючий газ, не имеющий запаха и цвета, не токсичен. Водород является самым легким из газов, он в 14,5 раз легче воздуха, поэтому низшая объемная теплота его сгорания меньше, чем у других компонентов газового топлива.
Сероводород H2S содержится в большинстве искусственных и некоторых природных газах. Это бесцветный горючий газ тяжелее воздуха (плотность - 1,54 кг/м 3 ), с сильным запахом, напоминающим запах тухлых яиц. Вызывает сильную коррозию металлов.
Сероводород ядовит. Он действует на нервную систему, а также на дыхательные пути и глаза. При концентрациях сероводорода выше 1 мг/л смертельное отравление может произойти почти мгновенно от паралича дыхательных центров. Допустимая концентрация его в воздухе помещений установлена не более 0,01 мг/л, а в газе, поступающем в городские сети, - не болев 2 г на 100 м 3 . Высокая токсичность сероводорода и строгие требования к его содержанию вызывают необходимость очистки газового топлива перед подачей его потребителям.
Окись углерода СО в большом количестве содержится в генераторных газах, являясь наряду с водородом основным горючим компонентом.
Окись углерода - химически стойкий горючий газ, не имеющий цвета. Плотность СО (1,25 кг/м 3 ) незначительно ниже плотности воздуха.
Окись углерода является сильным ядом; концентрация его в воздухе в 1% приводит через 1-2 мин к сильному отравлению и смерти. Предельная концентрация СО в воздухе рабочей зоны цехов по существующим нормам не более 0,03 мг/л при длительной работе и не более 0,05 мг/л при пребывании в загазованной атмосфере до 1 ч.
Окись углерода является продуктом неполного сгорания углерода и может находиться в продуктах сгорания любого топлива, содержащего углерод или углеродные соединения.
Сероуглерод CS2 в небольших количествах входит в состав газов, получаемых при сухой перегонке топлив, содержащих серу. Температура кипения сероуглерода +46° С, т. е. при обычных условиях он является жидкостью. Пары сероуглерода в 2,6 раза тяжелее воздуха. Высокие концентрации паров сероуглерода в воздухе приводят к отравлению. Предельно допустимая концентрация в рабочей зоне 0,01 мг/л.
Цианистый водород HCN - сильнейший яд, содержащийся в небольших количествах в газах сухой перегонки топлива. Предельное содержание HCN в газах, применяемых для городского газоснабжения, Пе выше 0,05 мг/л, предельно допустимая концентрация в воздухе промышленных предприятий - 0,0003 мг/л.
Кроме перечисленных выше горючих газов и паров искусственные газы содержат некоторое количество смол, аммиака, нафталина. Эти соединения, представляющие большую ценность для химической промышленности, извлекаются из газового топлива в установках улавливания или очистки газа.
В качестве балластных примесей во всех газах, как природных, так и искусственных, имеются азот N2, водяные пары Н2О и двуокись углерода СО2. Азот и двуокись углерода не токсичны и не агрессивны, т. е. не обладают коррозионными свойствами. Наличие водяных паров может привести к образованию конденсата, усиленной коррозии трубопроводов и образованию гидратных пробок при дальнем транспорте природного газа. Во избежание этого природные и попутные газы перед подачей в магистральные трубопроводы подвергают осушке, при которой одновременно удаляется и двуокись углерода.
div' data-cycle-timeout='0' data-cycle-fx='carousel' data-cycle-carousel-visible='8' data-cycle-carousel-fluid=true data-allow-wrap='false' data-cycle-log='false' >












Газообразные вещества – вещества со слабыми связями между частицами. Главные свойства газов – это подвижность и хаотичное движение частиц, направление которых меняется при столкновении. Газ – одно из 4 агрегатных состояний веществ, которые на сегодняшний день известны науке.
Четыре агрегатных состояния вещества

Краткая история открытия газов
На июль 2017 года открыто 826 газов, а в будущем, возможно, к газообразному агрегатному состоянию припишут еще 90 веществ. Многие открытые газы не природные, они получены в лабораторных условиях.
Свойства газообразных веществ
Выделяется целый ряд физических и химических свойств газов. Основные физические свойства:
- Газы способны занимать все отведенное им пространство, независимо от объема вещества. Это отличает их от жидкостей и твердых тел: и первые, и вторые занимают ограниченный объем. Простой пример данного свойства: если во время готовки закрыть кухню, запах останется только на ней. Если открыть дверь, он распространится по всей квартире. И в том, и в другом случае объем газа одинаковый.
- Газообразные вещества легко соединяются между собой. В полученных смесях нет четких границ: молекулы хаотично перемешиваются.
- Связи между частицами вещества очень слабые. Пространство между частицами в разы больше, чем размер самих частиц. Именно поэтому газы способны заполнять произвольные объемы.
- Объем газов может многократно сжиматься. Например, кислород можно сжать до 200 раз по сравнению с первоначальным объемом.
- Газы способны к диффузии, то есть к проникновению в другие вещества и перемешиванию. Это касается не только других газов, упомянутых выше. Например, частицы кислорода проникают в воду.
- Газы отличаются по тяжести молекул. В связи с этим, несмотря на диффузию, два газа с заметными различиями в массе постепенно разделятся.
- Газообразные вещества могут появляться путем межфазного перехода, то есть из других агрегатных состояний. Первый вариант межфазного перехода – испарение при нагреве жидкого вещества, второй – сублимация, при которой твердое вещество, минуя стадию жидкости, сразу становится газом.
- Газы не проводят электрический ток. Исключение составляют ионизированные вещества.
- У газов низкая теплопроводность и теплоемкость. Конкретные показатели зависят от типа молекул.
- Если газ находится под высоким давлением, он способен повредить стенки сосуда, если те недостаточно прочны. Объясняется это просто: чем больше давление, тем сильнее отталкиваются друг от друга частицы вещества. Потенциальная энергия газа увеличивается и вызывает взрывное расширение.
Если же газ подвергнуть высоким температурам, сначала он станет разреженным. Увеличится скорость теплового движения частиц. При достижении определенного температурного показателя произойдет тепловая ионизация, вещество перейдет в следующее агрегатное состояние – плазму.
Некоторые газы не имеют цвета, другие же заметны человеческому глазу. Например, I2, йод. Это вещество получают путем сублимации кристаллов йода, и его клубы имеют ярко выраженный фиолетовый оттенок. Но большинство соединений все же бесцветные, прозрачные и легкие, поэтому долгое время их не могли открыть и изучить.
Классификация газов

Вещества в газообразном состоянии принято делить на несколько категорий. Классификацию часто просят отразить в конспектах во время школьных занятий. Рассмотрим самые распространенные ее типы.
Органические и не органические
Органическими газами являются те вещества, которые содержат углерод. Примеры:
- этилен (С2Н4);
- метиламин (CH3NH2);
- ацетилен (C2H2).
Также к этой категории относятся метан, пропан, этан. Логично, что к неорганическим соединениям относятся те, в которых C отсутствует. Это аммиак, хлор и фтор, силан, гелий, неон, аргон и так далее. Инертные и благородные газы – не органические.
Простые и сложные
Органические и не органические газы, в свою очередь, делятся на простые и сложные. Перечисленные выше органические соединения – сложные. В них содержатся разные атомы: ацетилен (C2H2) – 2 атома углерода и 2 атома водорода, этилен (С2Н4) – 2 атома углерода и 4 водорода. Если же газ получается из одного или нескольких атомов одного и того же элемента таблицы Менделеева, его называют простым.
Простые газы: кислород O2, азот O3, водород H2, хлор Cl2. Перечислять можно и дальше.
Газообразные вещества в химии
Газы в химии начинают изучать в 8 классе. Рассмотрим основные свойства, которые принято включать в учебники по предмету.
Атомы или молекулы газов соединяются между собой ковалентными связями. Они очень слабые и часто рвутся, именно поэтому вещества в газообразном агрегатном состоянии способны заполнять произвольные объемы и емкости разных форм. Бывают два вида строения решеток у газов:
На уроках химии газообразные вещества часто получают в лабораторных условиях. Для этого могут пользоваться разными методами: нагревать жидкость, твердые вещества, добиваться реакции между сложными соединениями. Некоторые формулы реакций:
Zn + 2HCl = ZnCl2 + H2 – водород.
NH4Cl + NaOH = NaCl + H2O + NH3 – аммиак
CaCO3 + 2HCl = CaCl2 + H2O + CO2 – углекислый газ.
Так как многие газы прозрачны и не имеют запаха, используются дополнительные методы их обнаружения. Одни соединения усиливают пламя, другие останавливают горения. Ряд газообразных веществ может менять цвет взвешенной в воде извести, делать жидкость мутнее.
Примеры газов

В списке газов свыше 800 наименований. Стоит рассмотреть самые распространенные:
Природный газ — это полезное ископаемое, представляющее собой углеводороды в газообразном состоянии. Образуются они в недрах земли. Составляющие применяются как топливный ресурс. Газ взрывоопасен и горюч. Запаха и какого-либо оттенка он не имеет, легче воздуха примерно в 1,8 раза. В пластах он залегает в виде шапки из газа нефтегазовых месторождений либо же в качестве отдельных скоплений, может иметь кристаллическое состояние.

Классификация и свойства
Природный газ подразделён на 3 основные категории. Они описываются следующими характеристиками:
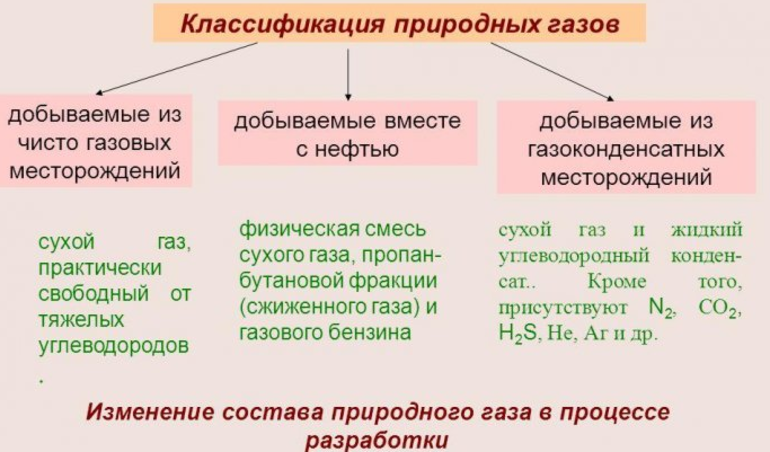
- Исключает присутствие углеводородов, в которых более 2 углеродных соединений. Их называют сухими и получают только в тех местах, которые предназначаются для добычи.
- Добывается наряду с первичным сырьём сжиженный и сухой газ и газообразный бензин, смешанные между собой.
- Присутствует в составе большое количество тяжёлых углеводородов и сухой газ. Имеется и незначительный процент примесей. Добывают из месторождений газоконденсатного типа.
Природный газ считается смешанным составом, в котором присутствуют несколько подвидов вещества. Именно по этой причине нет точной формулы компонента. Главным является метан, которого содержится более 90%. Он наиболее устойчив к температуре. Легче воздуха и малорастворим в воде. При горении на открытом воздухе образуется пламя голубого цвета. Мощнейший взрыв происходит в том случае, если соединить метан с воздухом в пропорции 1:10. Если человек вдыхает большую концентрацию этого элемента, то его здоровью может быть нанесён вред.
Применяют его как сырьё и промышленное топливо. Также его активно используют, чтобы получить нитрометан, муравьиную кислоту, фреоны и водород. При распаде углеводородных связей под влиянием тока и температур получается применяемый в промышленности ацетилен. При окислении аммиака с метаном образуется синильная кислота.
В составе природного газа имеет такой список компонентов:
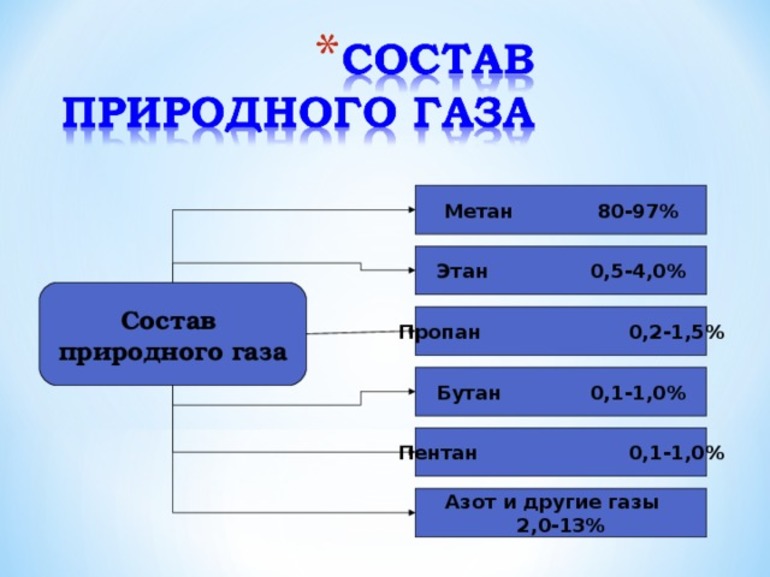

- Этан — газообразное вещество, не имеющее цвета. При горении освещает слабо. В воде практически не растворяется, а в спирте может при соотношении 3:2. В качестве топлива его не нашёл применения. Основной целью использования считается производство этилена.
- Пропан — хорошо применяемый тип топлива, который в воде не растворяется. При сгорании выделяется большое количество тепла.
- Бутан — со специфическим запахом, небольшую токсичность. Отрицательно воздействует на здоровье человека: может поражать нервную систему, вызывает аритмию и асфиксию.
- Азот может использоваться для того, чтобы в буровых скважинах поддерживать соответствующее давление. Чтобы получить этот элемент, необходимо сжижать воздух и разделить его путём разгонки. Применяется для изготовления аммиака.
- Диоксид углерода — соединение может переходить в газообразное из твёрдого состояния при атмосферном давлении. Находится в воздухе и в минеральных источниках, а также выделяется при дыхании существ. Является пищевой добавкой. является довольно токсичным элементом. Он может негативно отразиться на работе нервной системы человека. Имеет запах протухших яиц, сладковатый привкус и является бесцветным. Отлично растворяется в этаноле. С водой не реагирует. Необходим для получения сульфитов, серной кислоты и серы.
- Гелий считается уникальным веществом. Он может скапливаться в земной коре. Получают его путём заморозки газов, в состав которых он входит. При нахождении в газообразном состоянии никак себя внешне не проявляет, в жидком — может поражать живые ткани. Он не способен взрываться и воспламеняться. Но если в воздухе будет присутствовать большая его концентрация, то это может привести к удушью. Применяют для заполнения дирижаблей и воздушных шаров, при работе с металлическими поверхностями.
- Аргон — это не имеющий внешних характеристик газ. Его применяют при резке и сварке металлических деталей, а также для того чтобы увеличить срок хранения пищевых продуктов (благодаря этому веществу вытесняется вода и воздух).
Физические свойства природного ископаемого следующие: температура самовозгорания составляет 650 градусов по шкале Цельсия, плотность природного газа — 0,68−0,85 (в газообразном состоянии) и 400 кг/м3 (жидкий). При смешении с воздухом взрывоопасными считаются концентрации 4,4−17%. Октановое число ископаемого составляет 120−130. Рассчитывают его исходя из соотношения легковоспламеняющихся компонентов к трудно окисляющимся при сжатии. Теплотворность приблизительно равна 12 тысячам калорий на 1 метр кубический. Теплопроводность газа и нефти одинаковая.
При добавлении воздуха природный источник может быстро воспламеняться. В бытовых условиях он поднимается к потолку. Именно оттуда и начинается возгорание. Связано это с лёгкостью метана. А вот воздух примерно в 2 раза тяжелее этого элемента.
В соответствии с химическими характеристиками, ресурс может вступать в реакции дегидрирования, пиролиза и замещения. Когда в составе будет присутствовать более 4% тяжёлых углеводородов, свойства начнут меняться.
Месторождение и добыча

Газ сжижают уже после его добычи. Именно по этой причине мировые запасы считают в кубических метрах. В год может достигаться до 3,6 миллиарда кубометров. Основными странами поставщиками являются Россия, Аравия, Иран, Туркмения, Катар, США, Венесуэла и Объединённые Эмираты.
Мировым лидером по добыче считается Российская Федерация. Основная часть залежь приходится на Уренгой. Там находится приблизительно 16 триллионов кубических метров газа. Также гигантским является и Ямбургское месторождение, где насчитывается 8,2 триллиона газа.
На важность природного ископаемого указывает расход. Скважины бурят по вечной мерзлоте. Для добычи ямбургского топлива необходимо преодолеть 1−3 километра. Из них примерно 50 метров приходится на мерзлоту.
Имеется ещё и Бованенковское месторождение, запасы которого составляют 4,9 триллиона кубических метров. Для местного населения предприятие по добыче и переработке считается местом занятости и дохода.

На днище Баренцева моря были обнаружены залежи ископаемого. Глубина его зарождений — не более 400 метров. На этой местности добыча в полном объёме не разрабатывается. Примерный объём залежей составляет 4 триллиона.
На юге Карского моря тоже имеются источники газа. Там было открыто Ленинградское (примерно 3 триллиона кубометров) и Русановское (779 миллиардов кубов топлива) месторождения.
Транспортировка топлива

Природный газ из недр в скважины поставляется обычным путём. Лёгкая субстанция имеет свойство просачиваться через имеющиеся в породе поры. Область низкого давления создают в скважине. В местах скопления ресурса оно высокое. На крупные залежи бурят несколько скважин, которые располагаются на равном друг от друга расстоянии.
К окончательной транспортировке топливо следует хорошо подготовить. Это обусловлено наличием примесей, которые могут вызывать осложнения с перемещением или же последующим применением. К примеру, из-за водяных паров при определённых условиях могут получаться гидраты, которые будут оседать в различных местах. Это вызовет затруднительное передвижение. Из-за сероводорода на оборудовании может возникать коррозия.
Кроме того, следует произвести тщательную подготовку трубопровода. Широкое применение получили азотные установки, благодаря которой получается инертная среда.

Трубопроводный способ на сегодняшний день обладает большой популярностью. Обслуживание и монтаж труб является довольно дорогой процедурой. Но несмотря на высокую стоимость, такой метод является наиболее выгодным для транспортировки на ближние и средние дистанции.
Помимо трубопровода, газ могут перевозить в специальных газовозах. Это суда со специальными изотермическими ёмкостями, температурный показатель в которых может составлять -160 градусов. Этот способ на расстояния более 2 тысяч километров считается экономически выгодным.
Применение в различных сферах деятельности
Топливо является основной областью применения. Для транспортировки источника по трубопроводу, необходимо ресурс осушить, в противном случае он может вызвать коррозию на поверхности. Также следует из состава убрать углекислый газ и сероводород.
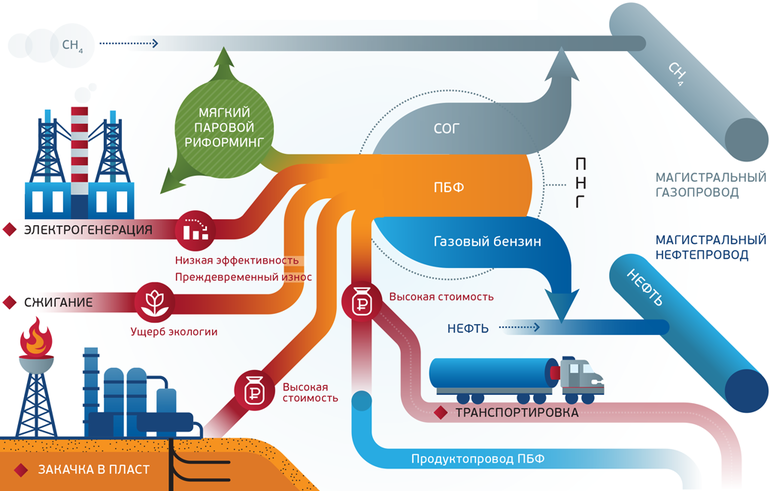
Чтобы избежать неприятных ситуаций, ископаемое одоризируют — добавляют пахучие элементы, которые будут свидетельствовать про утечку. Без обработки могут быть большие потери топлива, так как, с точки зрения химии, запаха оно не имеет.
Помимо этого, газ является горючим веществом для работы кухонных плит и отопительных котлов. Уже появились и газовые лампы для освещения улиц и помещений.
Из метана в химической промышленности добывают аммиак и некоторые пластификаторы. Из него синтезируются цианистый водород, ацетилен и метанол. Из метана производят и синтетический каучук. Происхождение полиэтилена было открыто при работе с природным газом.
Газообразное состояние вещества - самое распространенное по сравнению с другими агрегатными параметрами соединений. Ведь в этом состоянии находятся:
- звезды;
- межзвездное пространство;
- планеты;
- атмосфера;
- космос в целом.

Главные отличительные свойства газов - это слабые межмолекулярные взаимодействия в кристаллической решетке, из-за которых и проявляются все основные характеристики этих веществ. Газов, безусловно, очень много. Однако мы рассмотрим самый важный и третий по распространенности на нашей планете - природный.
Природный газ: состав
Если характеризовать качественный состав природного газа, то сразу нужно выделить компоненты двух групп: органические и неорганические. Поскольку хоть и принято считать, что он состоит из метана, однако это не совсем так.
К органическим составляющим относятся:
- метан - СН4;
- пропан - С3Н8;
- бутан - С4Н10;
- этан - С2Н4;
- более тяжелые углеводороды с количеством атомов углерода больше пяти.
Неорганические компоненты включают в себя следующие соединения:
- водород (в небольших количествах) - Н2;
- углекислый газ - СО2;
- гелий - Не;
- азот - N2;
- сероводород - H2S.
Каким именно будет состав той или иной смеси, зависит от источника, то есть месторождения. Этими же причинами объясняются и различные физико-химические свойства природного газа. Однако добывается любой из них, и ценность также имеет каждый. Просто какой-то вид применяется как топливо, а насыщенный посторонними примесями слишком жирно используется в химической отрасли для синтезов соединений.
Физико-химические свойства природного газа
Чтобы указать подобные параметры в точности, следует знать, каков именно состав газовой смеси. Ведь если в ней преобладает в основном метан (до 97%), то характеристики можно приводить, ориентируясь именно на него.
Если же неорганических компонентов или тяжелых углеводородов в избытке (до нескольких процентов), тогда физико-химические свойства природного газа резко меняются.
Поэтому можно указать лишь приблизительные граничные показатели по физическим характеристикам.
Кроме этого, следует отметить и химическую сторону параметров природного газа.
- Является сильно горючим веществом, способен самовоспламеняться при подаче искры и без нее при определенной температуре.
- Так как основной компонент - метан, то обладает всеми его химическими свойствами.
- Вступает в реакции замещения, дегидрирования, пиролиза, подвергается рефракции.
- Сжимается и сжижается при низких температурах и повышенном давлении.

Очевидно, что подобные физико-химические свойства природного газа определяют широкий спектр его использования в промышленности.
Особое свойство природного газа
Особое свойство рассматриваемого соединения - это способность образовывать газогидратные залежи, то есть находиться в твердом состоянии. Данные структуры представляют собой поглощенные молекулами пластовой воды объемы природного газа в соотношении 1/220. Поэтому подобные залежи являются чрезвычайно богатыми породами. Места их сосредоточения в природе:
- глубинные поддонные слои Мирового океана;
- скопления вечной мерзлоты.
Условия существования - гидродинамическое давление и низкие температуры.
Природные месторождения газа
Если говорить о содержании природного газа в природе, то можно выделить основные места концентрации:
Если же обозначать распространение месторождений газа территориально, то лидерами являются следующие страны:
- Россия.
- Страны Персидского залива.
- США.
- Канада.
- Иран.
- Казахстан.
- Азербайджан.
- Узбекистан.
- Норвегия.
- Туркмения.
- Нидерланды.
Добыча в мире составляет ежегодно примерно 3643 млрд м 3 в год. Из них только на Россию приходится 673,46 млрд м 3 .
Температура природного газа, при которой он сгорает, равна 650 0 С. То есть это тот показатель, при котором он способен самовоспламеняться. При этом выделяется большее количество тепловой энергии, чем при горении любого другого вида топлива. Естественно, это не могло не отразиться на областях использования данного вещества.
Именно поэтому многие страны, не имеющие природных запасов газа, вынуждены импортировать его из других государств. Транспортировка осуществляется несколькими способами:
- по трубопроводу в газообразном состоянии;
- в цистернах по морскому пути - в жидком виде;
- в железнодорожных вагонах-цистернах - сжиженный.

Каждый из путей имеет свои преимущества и недостатки. В частности, морской и железнодорожный варианты более безопасные, так как химическая активность сжиженного газа в охлажденных баллонах гораздо ниже, чем в газообразном состоянии. По трубопроводу же увеличивается дальность передачи и ее объемы, кроме того, данный способ экономически выгоден.
Метан в составе природного газа
Газ метан является основным сырьевым компонентом в составе природной смеси. Его содержание колеблется в пределах 70-98%. Сам по себе это третий по распространенности на планете газ, который входит в состав нефти, межзвездного пространства, атмосферы других планет.
С точки зрения химии, газ метан - предельный углеводород, относящийся к ряду насыщенных алифатических соединений. Самый первый представитель алканов или парафинов. Химическая активность его невелика, он достаточно спокоен. Способен вступать в реакции:
- замещения;
- полного окисления;
- конверсии.

Горит бесцветным некоптящим пламенем, запаха не имеет.
Виды природного газа
Существует три основных вида рассматриваемого вещества.
- Сухой природный газ - это такой, в котором метана более 97%. То есть содержание примесей, в том числе других углеводородов, крайне низкое.
- Тощий газ. Так называют смесь, содержащую незначительное количество тяжелых углеводородов.
- Жирный природный газ - тот, что богат на тяжелые углеводороды и неорганические компоненты (азот, водород, гелий, аргон, углекислый газ, сероводород).

Такое понятие, как коэффициент сухости газа, позволяет оценить качество сырья, из которого в дальнейшем будет изготовляться продукция. Ведь сам природный газ - это лишь база. Для разных отраслей промышленности нужен свой продукт, поэтому он проходит тщательную обработку и очистку в соответствии с конкретными требованиями.
Качество продукции
Качество природного газа напрямую зависит от состава. Если метан преобладает, то такой продукт будет самым лучшим как источник топлива. Если же больше всего в составе жирных углеводородов, то для химической промышленности такое сырье - наиболее подходящее.
Чтобы поставлять природный газ надлежащего качества, существуют специальные химические заводы, на которых он проходит тщательную очистку и обработку до дальнейшей отправки в конечный пункт. Методы работы будут зависеть от того, для каких целей предназначается продукт.

Так, например, если он будет использоваться для бытовых целей, то в него добавляют специальные вещества-одоранты, в частности меркаптаны. Это делается для того, чтобы газ стал иметь запах, ведь тогда в случае утечки его несложно будет обнаружить. Все меркаптаны имеют резкий неприятный запах.
Использование природного газа
Потребление природного газа осуществляется многими отраслями промышленности и объектами. Например:
- ТЭЦ.
- Котельные.
- Газовые двигатели.
- Химическое производство (изготовление пластмасс и прочих материалов).
- Топливо для машин.
- Обогрев жилых помещений.
- Приготовление пищи.
Поэтому мировая добыча данного сырья так велика, и импорт и экспорт оцениваются в миллиарды долларов.
Экологический аспект
С точки зрения чистоты для природы нет лучшего источника топлива, чем природный газ. Экологические организации полностью одобряют его использование. Однако в последние годы сгорание природного газа приводит к накоплению одного из продуктов реакции - диоксида углерода.

А так как он относится к парниковым газам, то для планеты его скопления очень опасны. Поэтому ведутся множественные работы, разрабатываются проекты по защите экологического состояния планеты от надвигающегося парникового эффекта.
Читайте также:

